T.C.
EGE ÜNİVERSİTESİ TIP FAKÜLTESİ
ACİL TIP ANABİLİM DALI
DENEYSEL SEPSİS MODELLERİNDE MORUS NİGRA (KARA DUT)’NIN SEPSİS TEDAVİSİ VE MORTALİTESİNDEKİ ETKİSİ
UZMANLIK TEZİ Dr. Murat Ali ŞEN
TEZ DANIŞMANI Prof. Dr. Murat ERSEL
İZMİR 2019
T.C.
EGE ÜNİVERSİTESİ TIP FAKÜLTESİ
ACİL TIP ANABİLİM DALI
DENEYSEL SEPSİS MODELLERİNDE MORUS NİGRA (KARA DUT)’NIN SEPSİS TEDAVİSİ VE MORTALİTESİNDEKİ ETKİSİ
UZMANLIK TEZİ Dr. Murat Ali ŞEN
TEZ DANIŞMANI Prof. Dr. Murat ERSEL
İZMİR 2019
iii
TEŞEKKÜR
15.01.2015 tarihinde baĢlamıĢ olduğum acil tıp asistanlık eğitimi süresince her türlü bilgisinden faydalandığım, en çok, sadece tıp alanında değil tüm yaĢama dair etik ahlak konusunda bana öğrettikleri ile övündüğüm, tez danıĢmanım, hastanemizin baĢhekim yardımcısı, Anabilim Dalı baĢkanımız Prof. Dr. Murat ERSEL’e, olayları ele alıĢ, yöneticilik ve liderlik konusundaki deneyimlerinden ilham aldığım Prof. Dr. Selahattin KIYAN’a, hiçbir Ģekilde desteğini benden eksiltmeyen, her yanlıĢımda arkamı toplayıp, öğrenmem gerekenleri açıkça söyleyen Doç. Dr. Funda KARBEK AKARCA’ya, her daim pozitif enerjisi ve sakinliği ile yıllarca görüĢmesek bile evinin kapılarının her daim bana açık olacağını bildiğim sevgili hocam ve abim Dr. Öğrt. Üyesi Yusuf Ali ALTUNCI’ya;
Tez çalıĢması süresince belki de en az ben kadar efor sarfeden Uzm. Dr. Meltem SONGÜR KODĠK’e, bana öğrettikleri ile yanlarında çalıĢmaktan onur duyduğum uzmanlarımız Uzm.Dr. Ġlhan UZ, Uzm.Dr. Enver ÖZÇETE, Uzm. Dr. Sercan YALÇINLI ve Uzm. Dr. Özge CAN’a;
Tıp fakültesine girdiğim andan itibaren yanımda her daim yardımcı olmak için bulunan ve hakkını hiçbir zaman ödeyemeyeceğim Prof. Dr. Yiğit UYANIKGĠL’e, tez çalıĢmamız için zor zamanlarında bile gece gündüz demeden yardım eden Doç. Dr. Öykü Emel Çetin UYANIKGĠL’e, Uzman Biyolog Fatih KARABEY, Uzm. Dr. Türker ÇAVUġOĞLU, Dr. Canberk TOMRUK, Doktora Öğrencisi Cansın ġĠRĠN’e;
5 senelik asistanlık hayatım boyunca bu yükü omuzlamamda yardımcı olan eĢkıdemlerim Dr. Ali Fuat ODUNCU, Dr. Mehmet EFE, Dr. Mehmet Birkan KORGAN’a;
Tez süresince tezime olan ekstra katkıları sebebiyle özellikle Dr. Ahmet Enes ÇELĠK, Dr. Cemile ÜSTÜN, Dr. Gülten KARA olmak üzere tüm acil servis asistanlarına;
Bir doktordan öte, beni bu karakterde yetiĢtirip, maddi ve manevi hiçbir desteklerini esirgemeyen aileme;
Bu süreçte her daim yanımda olan, benimle bir hayatı paylaĢan, özverisiyle, neĢesiyle, her daim beni motive etmesiyle, anlayıĢıyla, ben yorulduğumda tekrar ayağa kalkmamı sağlayan Dr. Eylül Destina FIRAT’a;
Sonsuz teĢekkürler ve Ģükranlarımla
iv İÇİNDEKİLER TEŞEKKÜR ... iii İÇİNDEKİLER ... iv ÖZET ... vii ABSTRACT ... ix TABLOLAR LİSTESİ ... xi
ŞEKİLLER LİSTESİ ... xii
GRAFİKLER LİSTESİ ... xiii
RESİMLER LİSTESİ ... xiv
KISALTMALAR LİSTESİ ... xv 1. GİRİŞ ... 1 2. GENEL BİLGİLER ... 3 2.1 Sepsis ... 3 2.1.1 Tanımlar ve Tarihçe ... 3 2.1.2 Skorlama Sistemleri ... 8 2.1.3 Epidemiyoloji ve Ġnsidans ... 9 2.1.4 Risk Faktörleri ... 10 2.1.5 Etiyoloji ... 10 2.1.6 Sepsis Fizyopatolojisi ... 12 2.1.7 Sepsisin Tedavisi ... 13 2.2 Böbrek ... 15
2.2.1 Böbreğin Genel Bilgi ve Yapısı ... 15
2.2.2 Böbreğin Fonksiyonları ... 16 2.2.3 Sepsis ve Böbrek ... 17 2.3 Karaciğer ... 19 2.3.1 Karaciğerin Anatomisi ... 19 2.3.2 Karaciğerin Fonksiyonları ... 21 2.3.3 Karaciğer ve Sepsis ... 22 2.4 Morus Nigra ... 22
2.4.1 Morus Nigra (Kara Dut)’nın Genel Yapısı ... 22
v
2.5 Deneysel Sepsis Modelleri ... 24
2.5.1 Çekum Bağlama ve Delme Modeli [Cecal Ligation and Puncture (CLP)] .... 24
2.5.2 Eksojen Olarak Lipopolissakkarid Verimi ile GerçekleĢtirilen Deneysel Sepsis Modelleri ... 25
2.5.3 Ġntravenöz ya da Ġntraperitoneal Olarak Canlı Bakteri Uygulanması ... 26
3. DENEYSEL GEREÇ VE YÖNTEM ... 28
3.1 Deneysel Gereç ve Kullanılan Ġlaçlar ... 28
3.1.1 Deneysel Gereçler ... 28
3.2 Kullanılan Ġlaçlar ... 29
3.2.1 Ketamin HCL (Pfizer Ketalar®) ... 29
3.2.2 Ksilazin (Bioveta-Xylazin Bio %2 ®) ... 29
3.2.3 Parasetamol (Bristol-Myers Squibb- Perfalgan ®) ... 29
3.3 Deneklerin Gruplandırılması ... 30
3.3.1 Deneklerin Gruplandırılması ... 30
3.3.1.1 Kontrol Grubu ... 30
3.3.1.2 Çekum Ligasyon ve Perforasyonu Grubu (CLP Grubu) ... 30
3.3.1.3 Serum Fizyolojik Grubu (CLP+SF Grubu) ... 30
3.3.1.4 Morus Nigra Grubu (Karadut Grubu) ... 30
3.3.2 Deneysel Sepsis Modelinin OluĢturulması ve BitiĢi ... 31
3.4 Morus Nigra Ekstraksiyonunun hazırlanması ... 34
3.5 IĢık Mikroskobik Yöntem ... 34
3.5.1 Takip ve Gömme ... 34
3.5.2 Kesit Alma ... 35
3.5.3 IĢık Mikroskobik Boyama ... 35
3.5.3.1 Histokimyasal Boyama ... 35
3.5.3 Mallory Azan Boyama ... 36
3.5.4 Ġmmünohistokimyasal Yöntem ... 37
3.5.5 Ġstatiksel Yöntem ... 37
4. BULGULAR ... 39
4.1 Karaciğer Bulguları ... 39
4.1.1 H.E ve Mallory Azan Boyama ... 39
4.1.2 Ġmmunohistokimyasal Bulgular ... 44
vi
4.2.1 H.E ve Mallory Azan Boyama ... 54
4.2.2 Ġmmunohistokimyasal Bulgular ... 58
5. TARTIŞMA ... 68
6. SONUÇ ... 78
vii
ÖZET
Deneysel Sepsis Modellerinde Morus Nigra(Kara Dut)’nın Sepsis Tedavisinde ve Mortalitesinde Etkisi
Dr. Murat Ali ŞEN
Ege Üniversitesi Tıp Fakültesi Acil Tıp AD. Bornova/İZMİR
AMAÇ: Sepsis yüzyıllardır süregelen bir morbidite ve mortalite sorunudur. Sepsis
tedavisinde mevcut patojene yönelik çeĢitli tedavi yöntemleri kullanılsa da, tedavide kesin ve etkili denebilecek bir yöntem mevcut değildir. Morus nigra, içerdiği fluvanoidler ve
antioksidan kapasitesi ile hem tıbbi, halk arasında Ģifalı olduğuna inanıldığı için hem de toplumsal olarak alternatif bir tedavi yöntemi olabileceğini düĢündürttüren özelliklere sahiptir.
Yapılan literatür taramalarında, direkt olarak Morus nigra’nın sepsis üzerindeki etkilere ya da antibakterisidal özelliklere değinilen bir çalıĢmaya rastlanılmamıĢtır. Bu nedenle içerdiği özellikler sebebiyle sepsis tedavisinde ve mortalitesinde Morus nigra’nın etkilerini gösteren bir çalıĢma yapmayı amaçladık.
YÖNTEM: Ege Üniversitesi Labaratuar Hayvanları Uygulama ve AraĢtırma Merkezi’nden
(EGEHAYMER) temin edilen, seksüel olgunluğa eriĢmiĢ, ağırlıkları 220 ile 300 gram
arasında değiĢen Wistar Albino tipi her iki eĢeyden 28 adet sıçan, 22C oda ısısında, % 45-75 nemde, karanlık ve aydınlık gün geçirme saatleri 12 saatlik eĢit döngülerde olacak Ģekilde, serbest su ve gıda desteği sağlanarak araĢtırmaya alındılar. 7 günlük planlanan çalıĢmada gruplar belirlendi. Grup I (Kontrol grubu) herhangi bir tedavi almadı. Diğer gruplara ait sıçanlara 0.günde CLP iĢlemi uygulandı. Grup II (CLP grubu) sadece CLP iĢlemi geçirip 7.güne kadar takibi sağlandı. Grup III (CLP+SF) grubu, CLP iĢlemi sonrası 24 saatte 1 olacak Ģekilde, 7 gün boyunca, Morus nigra’nın çözücüsü 3mL intraperitoneal SF enjeksiyonu aldı. Grup IV (Kara dut grubu) ise CLP sonrası 7 gün boyunca 24 saatte 1 3mL kara dut çözeltisi aldı. 7.günün sonunda denekler, böbrek ve karaciğer biyopsilerinin alınması için sakrifiye edildi. Alınan örnekler H&E, Mallory azan, Anti-enos, Anti-inos, Anti-gfap boyamalara tabii tutuldu. Preparatlar ıĢık mikroskopu altında x4, x20 ve x40 büyütmelerinde incelendi.
viii
BULGULAR: IĢık mikroskopu altında incelenen preparatlarda, ITO hücre miktarına, gruplar
arası cast formasyonu mevcudiyetine, eritrosit ekstravazasyonuna, fırçamsı kenar kaybına, hepatik sinuzoidlerde dilatasyona ve konjesyona, portal alanda inflamasyona, tubuler dilatasyona ve vena centraliste konjesyona bakıldı. Yapılan değerlendirme ve istatiksel analiz sonucu, Kara dut ekstresi alan deneklerde CLP ve CLP+SF gruplarındaki deneklere oranla, ITO hücre miktarında p<0.0001, cast formasyonunda p<0.0001, eritrosit ekstravazasyonunda p<0.0001 olacak Ģekilde istatiksel anlamlı üstünlük saptandı. Kara dut grubunda fırçamsı kenar kaybı ise CLP grubuna p<0.0001, CLP+SF grubuna p<0.001 olacak Ģekilde istatistiksel bir anlam ifade etti. Kara dut grubunda bakılan hepatic dilatasyon ve konjesyon, portal alanda inflamasyon, tubuler dilatasyon CLP ve CLP+SF gruplarına oranla p<0.0001 olarak istatistiksel olarak anlamlı belirlendi. Deneklerden alınan örneklerde incelenen vena centralis konjesyonununda Kara dut grubu ile CLP ve CLP+SF gruplarına karĢı yapılan değerlendirme sonucu p<0.001 olarak belirlendi. Kontrol grubu ile Kara dut grubu arasında yapılan karĢılaĢtırılmada ise, gruplar arası cast formasyonunda, fırçamsı kenar kaybında, hepatik venlerde dilatasyon ve konjesyonda, portal alanda inflamasyonda ve tubuler dilatasyon değerlendirilmelerinde Kontrol grubunun Kara dut grubuna p<0.01 olacak Ģekilde anlamlı istatiksel üstünlük saptadığı belirlendi. Kontrol ve Kara dut grubu arasında yapılan incelemeler sonucu, vena centraliste konjesyon, eritrosit ekstravazasonu, ITO hücre miktarı parametrelerinde Kontrol grubunun Kara dut grubuna anlamlı istatistiksel üstünlük sağladı görüldü. (p<0.001)
SONUÇ: Yapılan bu tez çalıĢmasında, CLP yöntemi ile oluĢturulmuĢ deneysel sepsis
modellerinde, intraperitoneal yoldan uygulanana Morus nigra tedavisinin, böbrek ve karaciğer dokularından alınan örneklerde, inflamatuar ve nekrotik etkileri azalttığı görüldü. Ancak dokulardaki akut evre etkileri istatistiksel ve histopatolojik olarak azalttığı, dokuların tamamen normale dönmesini sağlamakta ise baĢarısız olduğu görüldü.
ANAHTAR KELİMELER: Morus nigra ; sepsis ; Kara dut ; tedavi ; çekum ligasyon ve
ix
ABSTRACT
Effect of Morus nigra (Black Mulberry) on sepsis treatment and mortality in experimental sepsis models
Dr. Murat Ali ŞEN
Ege University Faculty of Medicine Department of Emergency Medicine, Bornova/İZMİR
PURPOSE: Sepsis is a problem of morbidity and mortality that has been going on for
centuries. Although various treatment methods for the pathogen are used in the treatment of sepsis, there is no definite and effective method in the treatment of sepsis. Morus nigra, with its fluvanoids and antioxidant capacity, has features that make it possible to think that it can be an alternative treatment method both in the medical literature and because it is believed to be healing among the society.
In the literature review, no direct study was performed on the effects of Morus nigra on sepsis or antibactericidal properties. Therefore, we aimed to investigate the effects of Morus nigra in the treatment and mortality of sepsis due to its features.
METHOD: 28 healthy Wistar-albino rats, which were obtained from Ege Universtiy
Experimental Animals Application and Reserch Center, wew of sexual maturity, of weight 220-300 grams, of both sex, were subjected to study. Rats were seperated 4 groups. After anesthesia, we do nothing on Group I, and performed CLP procedure Group II,III,IV at day zero. Then, we just observed Group II and named CLP group, to see the effects of CLP procedure on liver and kidneys. We did daily injections of 3 ml salin intraperitonally on Group III and we did daily injections of 3 ml intraperitonally black mulberry solution on Group IV. At the day 7, all animals sacrifed for harvesting kidney and liver’s histological examples. All examples evaluated under light microscope. The data from this evalution, entered to the GraphPad Prism 6.0 database and statistical analyze performed also with this program.
FINDINGS: In the preparations examined under light microscope, ITO cell amount,
presence of intergroup cast formation, erythrocyte extravasation, brushy side loss, dilatation and congestion of hepatic sinusoids, portal area inflammation, tubular dilatation and
congestion in the vena centralis were examined. As a result of the evaluation and statistical analysis, statistically significant superiority was found in Group 4 subjects, p <0.0001 in ITO
x cell amount, p <0.0001 in cast formation, p <0.0001 in erythrocyte extravasation compared to group II and group III subjects. Also, the loss of brushy sides in the Group 4 was statistically significant as p <0.0001 over the Group 2 and p <0.001 over the Group 3. Hepatic dilatation and congestion, inflammation in portal area, tubular dilatation in the Group 4 were
statistically significant at p <0.0001 compared to Group 2 and Group 3. In the evaluation of congestion of vena centralis in the samples taken from the subjects, the result of the
evaluation of Group 4 against Group 3 and Group 2 was determined as p <0.001 which is statistically meaningful. In the comparison between the Group I and the Group 4, it was determined that the Group 1 had significant statistical superiority to the Group 4 in the cast formation, brushy side loss, dilatation and congestion in hepatic veins, inflammation in the portal area and tubular dilatation which it was resulted as p<0.01. As a result of the
examinations between Group 1 and Group 4, at the parameters like, congestion on vena centralis, erythrocyte extravasation, ITO cell quantity, Group 1 showed significant statistical superiority to the Group 4. (P <0.001)
RESULT: In this study, it was seen that intraperitoneal administration of Morus nigra
treatment in experimental sepsis models created by CLP method decreased inflammatory and necrotic effects in samples taken from kidney and liver tissues. However, black mulberry has been shown to reduce the acute stage effects in tissues, but failed to returning tissues to normal.
KEYWORDS: Morus nigra ; sepsis ; Black mullberry ; treatment ; ceacum ligation and
xi
TABLOLAR LİSTESİ
Tablo 1. Sepsiste kabul edilen tanısal kriterler ... 6
Tablo 2. Toplantılara göre tanımlar ve değiĢiklikler ... 8
Tablo 3. Ġntraabdominal kaynaklı sepsislerde sıklıkla karĢılaĢılan etkenler... 11
Tablo 4. Sepsis Tedavisinde 1. Saat Önerileri Tablosu ... 14
Tablo 5. Karaciğere ait vena centraliste gerçekleĢen konjesyonun grup ve preparat bazlı skorlaması ... 48
Tablo 6. Karaciğere ait hepatik sinuzoidlerde dilatasyon ve konjesyonun, grup ve preparat bazlı skorlaması ... 50
Tablo 7. Karaciğere ait portal alanda inflamasyonun, grup ve preparat bazlı skorlaması ... 51
Tablo 8. Böbreğe ait fırçamsı kenar kaybının, grup ve preparat bazlı skorlaması ... 61
Tablo 9. Böbreğe ait tübüler dilatasyonun, grup ve preparat bazlı skorlaması ... 62
Tablo 10. Böbreğe ait eritrosit ekstravazasyonunun, grup ve preparat bazlı skorlaması ... 64
Tablo 11. Böbreğe ait cast formasyonunun, grup ve preparat bazlı skorlaması ... 66
Tablo 12: CPL ile gerçekleĢtirilen deneysel sepsis modelinin insan vücudunda gerçekleĢen sepsis ile karĢılaĢtırılması ... 68
xii
ŞEKİLLER LİSTESİ
Şekil 1. Sedatize ve tespit edilmiĢ sıçanın karın ön duvarının traĢlanması ... 31
Şekil 2. Yapılan kesi sonrası karın kavitesine ulaĢım ... 32
Şekil 3. Çekumun belirlenmesi ... 33
Şekil 4. Çekumun bağlanması ... 33
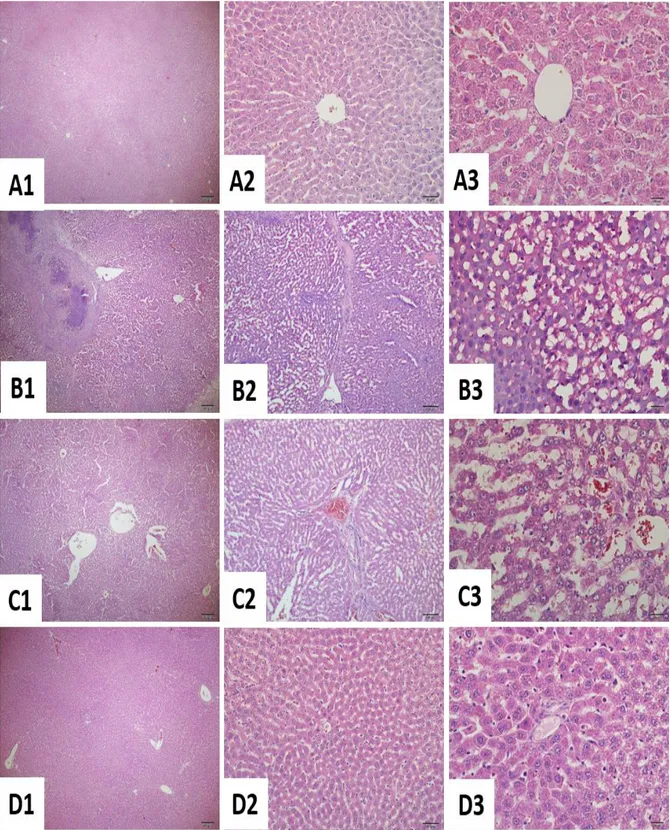
Şekil 5. CLP grubuna ait bir ratın 7. gün sonunda sakrifiye edildikten sonra histolojik inceleme örneklerinin alımı esnasında makroskopik olarak görülebilen fibroz ve enfekte odaklar ... 40
Şekil 6. CLP+SF grubuna ait bir ratın 7. gün sonunda sakrifiye edildikten sonra histolojik inceleme örneklerinin alımı esnasında makroskopik olarak görülebilen fibroz doku .. 41
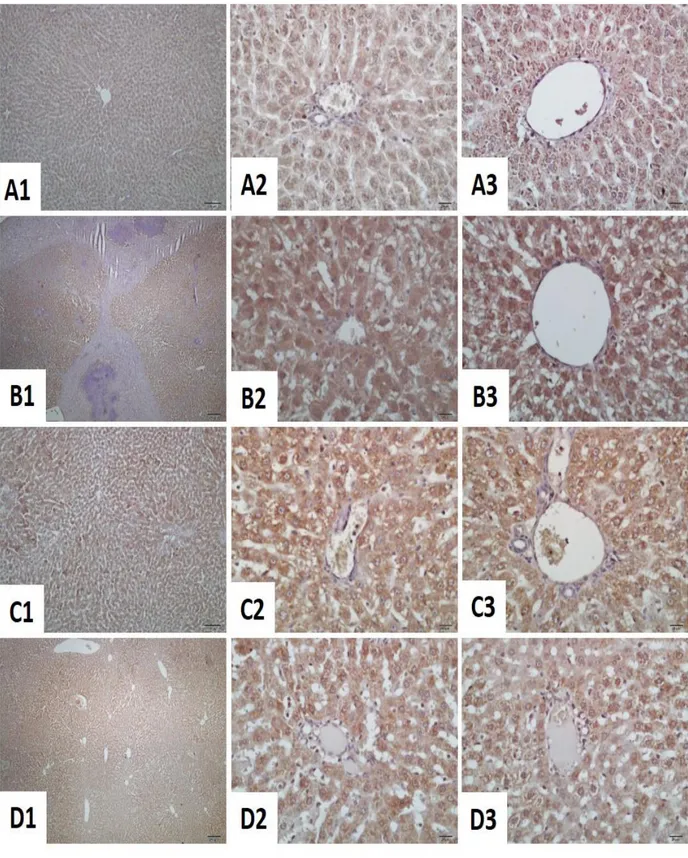
Şekil 7. Kontrol ve sepsis modeli uygulanan grupların karaciğer histopatolojik görünümü. H&E boyama. ... 42
Şekil 8. Kontrol ve sepsis modeli uygulanan grupların karaciğer histopatolojik görünümü. Mallory azan boyama. ... 43
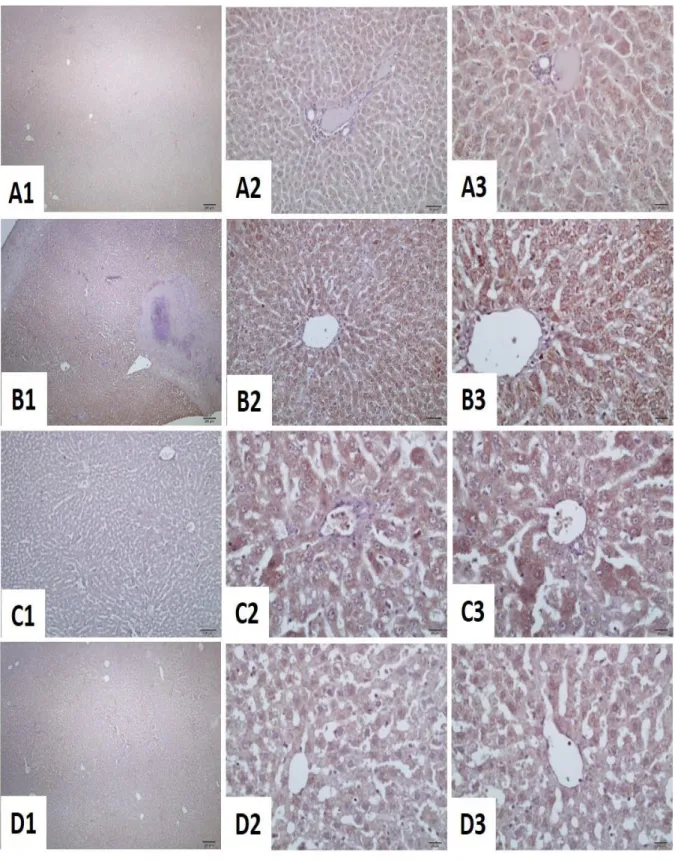
Şekil 9. Kontrol ve sepsis modeli uygulanan grupların karaciğer histopatolojik görünümü. Anti-inos boyama. ... 45
Şekil 10. Kontrol ve sepsis modeli uygulanan grupların karaciğer histopatolojik görünümü. Anti-enos boyama. ... 46
Şekil 11. Kontrol ve sepsis modeli uygulanan grupların karaciğer histopatolojik görünümü. Anti-GFAP boyama. ... 47
Şekil 12. Karadut grubuna ait bir ratın 7.gün sonunda sakrifiye edildikten sonra histolojik inceleme örneklerinin alımı esnasında makroskopik olarak batın ön duvarının görünümü ... 55
Şekil 13. Kontrol ve sepsis modeli uygulanan grupların böbrek histopatolojik görünümü. H.E boyama. ... 56
Şekil 14. Kontrol ve sepsis modeli uygulanan grupların böbrek histopatolojik görünümü. Mallory azan boyama. ... 57
Şekil 15. Kontrol ve sepsis modeli uygulanan grupların böbrek histopatolojik görünümü. Anti-inos boyama. ... 59
Şekil 16. Kontrol ve sepsis modeli uygulanan grupların böbrek histopatolojik görünümü. Anti-enos boyama. ... 60
xiii
GRAFİKLER LİSTESİ
Grafik 1. Vena Centraliste Konjesyon Skorlama Grafiği ... 48
Grafik 2. Hepatik Sinuzoidlerde Dilatasyon ve Konjesyon Skorlama Grafiği ... 50
Grafik 3. Portal Alanda Ġnflamasyon Skorlama Grafiği ... 52
Grafik 4. ĠTO Hücre Sayım Miktarı ... 53
Grafik 5. Fırçamsı Kenar Kaybı Skorlama Grafiği ... 61
Grafik 6. Tübüler Dilatasyon Skorlama Grafiği ... 63
Grafik 7. Eritrosit Ektravasazyonu Skorlama Grafiği ... 65
xiv
RESİMLER LİSTESİ
Resim 1. Böbreklerin vücuttaki yerleĢim yeri ... 16
Resim 2. Renal Histoloji ... 18
Resim 3. Karaciğer Anatomisi ... 20
Resim 4. Karaciğer histolojisi ... 21
Resim 5. Morus nigra meyveleri ... 23
Resim 6. Normal karaciğer ve Fibroz sonucu oluĢan karaciğerin Ģematik karĢılaĢtırımı…….75
xv
KISALTMALAR LİSTESİ
CLP : Çekum ligasyon ve perforasyon SF : Serum fizyolojik mL : Mililitre x4 : 4 kat büyütme x20 : 20 kat büyütme x40 : 40 kat büyütme MÖ : Milattan önce
SCCM : Society of Critical Care Medicine ACCP : American Collage of Chest Physicians SIRS : Sistemik inflamatuar yanıt sendromu CRP : C- reaktif protein
SIS : Surgical Infection Society ATS : American Thoracic Society INR : International normalized ratio dL : Desilitre
mmol : Milimol L : Litre
µL : Mikrolitre
MODS : Multiple Organ Disfonksiyon Sendromu SOFA : Sepsis-Related Organ Failure Assessment MAP : Ortalama arteryel basınç
KOAH : Kronik obstrüktif akciğer hastalığı HIV : Human immun yetmezlik virusu NO : Nitrik oksit
TNF : Tümor nekroz faktör
PAF : Trombosit aktive edici faktör
DIC : Dissemine intravasküler koagülasyon OAB : Ortalama arteryel basınç
LPS : Lipopolisakkarit
EGEHAYMER : Ege Üniversitesi Labaratuar Hayvanları Uygulama ve AraĢtırma Merkezi NMDA : N-Metil D-Aspartik asit
mg : Miligram kg : Kilogram
xvi
NaCl : Sodyum Klorür H&E : Hematoksilen eozin
LSEC : Karaciğer sinüzoidal endotel hücreleri GFAP : Glial fibriler asidik protein
MNHI : Mononükleer hücre infiltrasyonu PNL : Polimorfo nüveli lökosit
IL-6 : Ġnterlökin-6
AST : Aspartat aminotransferaz ALT : Alanin aminotransferaz COX-2 : Siklooksijenaz-2
1
1. GİRİŞ
Sepsisin, tıp literatürüne giriĢi ilk defa MÖ 400 yıllarında yaĢamıĢ olan Hippocrates’in sepsis, vücudun çöküĢü ile tanımlasıyla olmuĢtur [1,2]. Tarihin ilk zamanlarından, günümüze kadar olan süreçte enfektif ajanlar varlığını korumuĢ, değiĢmiĢ ve sepsis kavramı geçerliliğini sürdürür hale getirmiĢtir. 2016 senesinde, 3. Uluslararası Sepsis ve Septik ġok Tanımlama Konsensunun yayınlamıĢ olduğu kılavuz ile sepsis kavramı, konağa yerleĢen patojenik ajanın oluĢturduğu enfeksiyona karĢı, konak organizmanın bu ajana verdiği düzensiz yanıt ve buna bağlı olarak gerçekleĢen organ iĢlev bozukluğu olarak tanımlanmıĢtır [1,3-7]. Sepsis için daha önceki senelerde (1991 ve 2001) gerçekleĢtirilen kavram tanımlamaları daha çok SIRS (sistemik inflamatuar yanıt sendromu) merkezlidir. Eski tanımlamalarda mevcut olan laktik asidoz, mental statü değiĢiklikleri, öligüri ve sıvı replasmanına yanıt veren hipotansiyon mevcudiyeti Ağır sepsis olarak kılavuzlarda karĢılık bulmuĢtur. Mevcut tablolarda sıvı tedavisine cevabın olmadığı hipotansiyon durumuna ise Septik ġok denilmiĢtir. 2016 senesinde yayınlanan bildirim ile kavram ve uygulama konusunda çeliĢkilere düĢen Ağır Sepsis kavramı tamamiyle kaldırılmıĢtır. Bu kılavuza göre bir hastanın sepsis tanısı alması için, Ģüpheli ya da ispatlanmıĢ bir enfeksiyon varlığına mütakip SOFA skorunun 2’den büyük olması gerektiği bildirildi. Septik Ģok kavramı ise sepsis tanısı almıĢ olan kiĢilerde, hipovoleminin olmaması durumunda, ortalama arteryel basıncın 65 mmhg üstüne çıkabilmesi için vazopressör ajan ihtiyacının olması ve laktat seviyelerinde normal üstü artıĢın gerekli olduğu belirtildi [3-7].
Sepsis, özellikle yoğun bakım üniteleri ve acil servisler baĢta olmak üzere, mevcut tüm hastane birimlerinde yüksek morbidite ve mortaliteyle seyreden bir tablodur. Bu nedenle tedavisi de durumun ciddiyeti kadar acil ve agresif olmalıdır.Sepsisin son 10 yılda, ülkemizde ve tüm dünyada görülme insidansı yaklaĢık olarak iki katına çıkmıĢ, hem iĢ gücü kaybı, hem ülke ekonomisinde mali kayıplar hem de mortalite ve morbitide olarak kayıplara yol açmıĢtır [8].
Günümüz bilgileri ıĢığında sepsis halen mortalite ve morbiditenin en önemli sebeplerinden biridir ve tedavisi için yeni ve çeĢitli ajanlara ihtiyaç vardır.
Dut, ılıman bölgelerde yetiĢmekte olan bir meyve türüdür. Tropik ve subtropik bölgelerde de yetiĢimi sağlanabilmektedir. Dut, Urticales takımının Moraceae familyasından Morus cinsine girmektedir. Bu cinse ait üyelerden en bilineneleri Morus alba ( Ak dut ), Morus nigra ( Kara Dut ) , Morus rubra ( Al dut ) ve Morus latifolia’dır. Yaptığımız literatür çalıĢmalarında Morus nigra’ antioksidan ve aniinflamatuar özelliklerine değinilmiĢtir. Ancak
2 bakterisidal ya da enfektif durumlarda etkinliğini içeren çalıĢma mevcut değildir. Sahip olduğu potansiyel özellikler düĢünülünce Morus nigra’nın terapötik bir ajan olabileceği düĢünülmüĢ ve sıçanlar üzerinde gerçekleĢtirdiğimiz bir deneysel sepsis modelinde, intraperitoneal yoldan verilen Morus nigra ekstresinin tedavi ve mortaliteye olan etkilerinin görülmesi amaçlanmıĢtır.
3
2. GENEL BİLGİLER
2.1 Sepsis
2.1.1 Tanımlar ve Tarihçe
Mevcudiyetinin kanıtları eski çağlara kadar uzanan sepsis, tarihteki ilk yazılı tıbbi tutanaklarda da olmak üzere, insan ölüm sebeplerinin en baĢında gelmektedir. Sepsis, Antik Yunancada “çürüme, kokuĢma” anlamına gelen “sepo” kelimesinden gelir ve eski çağlardan beri bakteri varlığında organik materyal, bitki ve hayvanların çürümesi anlamında kullanılmıĢtır [1].
Ġlk bulgulara göre sepsis kavramı ilk defa günümüzden 2700 yıl önce, Homeric’in yazdığı Ģiirlerde görülmektedir. MÖ. 400 yıllarında yaĢamıĢ olan filozof ve tıbbın öncüllerinden olan hekim Hippocrates, Corpus Hippocraticum adlı kitabunda sepsis kavramından bahsetmiĢ ve sepsisi vücudun biyolojik olarak çöküĢü olarak tanımlamıĢtır [1,2]. Ġzmir, Bergama doğumlu hekim ve filozof Galen ömrünün bir kısmında sepsis hakkında çalıĢmıĢtır. (MS 129-199). Anthony van Leeuwenhoek (1632-1273) ve Hieronymus ise birçok hastalığın etkeni olarak mikroorganizmalardan ĢüphelenmiĢ ve germ teorisinin oluĢmasına imkan vermiĢtir. Ignaz Semmelweiss puerperal sepsis oranını, sadece el yıkama ile %3’ün altına indirmiĢtir [3,4,5]. Sepsis ve enfejsiyon hastalıklarında, antibakteriyel ya da antiseptik ajanların kullanımı da yine Hippocrates’e kadar dayanmaktadır. Hippocrates kendi zamanlarında sepsis tedavisi için inorganik tuz, Ģarap ve mür kullanmıĢtır. 2500 yıl öncesinde antik Çin’de, çıban ve karbonkül tedavisinde soya fasülyesi sütü kullanılmıĢtır. 1827-1912 yılları arasında yaĢamıĢ olan Joseph Lister açık yarası mevcut olan hastalarda, derideki çatlaklardan giren mikrobiyal etkenler sonrası sepsis geliĢtiğini düĢümüĢtür. BU dönemlerde Lister, eldeki mevcut bulguları ile açık yaraların karbolik asit ile sarılmasını denemiĢtir. Yaptığı uygulama ile sepsis geliĢiminde azalma ve ölüm oranlarında düĢüĢ sağlamıĢtır [6].
Mevcut olan bu bilgi ve görüĢlerden asırlar sonra günümüzde sepsis zararlı mikroorganizmaların bulaĢı sonrası, vücüdun bağıĢıklık, inflamasyon ve koagülasyon sistemlerinde oluĢan inflamatuar yanıttan, çoklu organ yetmezliğine kadar ilerleyebilecek, ciddi ve ölümcül bir klinik tablo olarak karĢımıza çıkabilmektedir [7].
Sepsis, özellikle yoğun bakım üniteleri ve acil servisler baĢta olmak üzere, mevcut tüm hastane birimlerinde yüksek morbidite ve mortaliteyle seyreden bir tablodur. Bu nedenle tedavisi de durumun ciddiyeti kadar acil ve agresif olmalıdır.Sepsisin son 10 yılda, ülkemizde ve tüm dünyada görülme insidansı yaklaĢık olarak iki katına çıkmıĢ, hem iĢ gücü kaybı, hem
4 ülke ekonomisinde mali kayıplar hem de mortalite ve morbitide olarak kayıplara yol açmıĢtır [8].
Sepsis ve sepsis tedavisinde yaĢanan zorluklardan bir baĢkası da konuyla ilgili mevcut kavram ve terminolojide karıĢıklıklardır. 1990’lı yıllarda günümüze kadar olan süreçte, tekrarlayan konsensüs ve toplantılar sonucu sepsis kavramı ile ilgili tanımlar, terminoloji ve bulgular sınıflandırılamaya ve netleĢtirilmeye çalıĢılmıĢtır. Sepsis ile ilgili 1991, 2001, 2012 ve son olarak da 2016 da yapılan uluslararası konferanslarda belli tanım, kriter ve kılavuzlar oluĢturulmuĢtur. Tüm klinisyenlerin aynı terminolojiyi konuĢabilmeleri için zemin aranmıĢ ve hazırlanmıĢtır [9].
Sepsis ile ilgili ilk konsensüs, Society of Critical Care Medicine (SCCM) ve American Collage of Chest Physicians (ACCP)’ın, sepsis terminolojisi ve kategorizasyonu için 1991 yılında bir araya gelinmesi ile yapılmıĢtır. Yapılan toplantı 1992 yılında tekrar edilmiĢ, septisemi sepsis ve refrakter Ģok gibi tanımlar sonlandırılmıĢtır. Bu tanımların yerine ise, infeksiyon, bakteriyemi, sepsis, sistemik inflamutar yanıt sendromu, septik Ģok ve buna sekonder geliĢen çoklu organ yetmezliği sendromu kavramları geliĢtirilmiĢtir. Sistemik inflamatuar yanıt sendromu (SIRS) ilk defa tip literatüne 1992 senesinde yapılan bu toplantı ile girmiĢtir [10,11].
2001 yılında ise ACCP, SCCM, American Thoracic Society (ATS), European Society of Intensive Care Medicine (ESICM) ve Surgical Infection Society (SIS) derneklerinin yaptığı toplantı ile Sepsis-2 konsensus paneli gerçekleĢtirilmiĢtir. Bu konsensusta sepsis, ağır sepsis ve ek olarak septik Ģok 1992’de belirtilenle aynı kalmak suretiyle, sepsis belirti ve bulguları daha kapsayıcı olmak üzere geniĢletilmiĢtir. Yine bu toplantıda sepsisin tanımı için gerekli olan kriterler arasına bilirubin, kreatinin, prokalsitonin, laktik asit, C-reaktif protein (CRP) gibi biyokimyasal ölçütlerdeki artıĢın da eklenmesi önerilmiĢtir. 2012’de yapılan toplantıda ise 2001 yılında yapılan konferansta kabul edilen kriteler arasında ufak değiĢiklikler yapılmıĢtır. Bu toplantılar sonucunda belirlenen tanım ve kriterler Ģöyledir [12,13];
İnfeksiyon: Normalde steril olan vücut doku ve yapılarına patojen ya da potansiyel
patojen mikroorganizmların yerleĢmesi sonucu oluĢan patolojik olaylardır.
Bakteriyemi: Canlı bakterilerin kan dolaĢımına katılmasına verilen addır.
Mikroorganizmanın varlığı alınacak kültür ile saptanabilir
Sistemik inflamatuar yanıt sendromu (SIRS): Ġnfeksiyon iliĢkili ya da iliĢkisiz
5 tetiklenmesidir. SIRS’ın infeksiyon dıĢında birçok sebebi olabilir. Cerrahi iĢlemler, tiroid krizi, adrenal yetmezlik, pankreatit, maligniteler, otoimmun bozukluklar ve sendromlar, yanık, travmalar, bu sebeplerden bazılarıdır. SIRS tanısı koyulabilmesi için ise hastanın mevcut tablosunda aĢağıda yazmakta olan bulgulardan 2 tanesinin bulunması yeterlidir [13,14].
Kalp atım hızının > 90/dk olması
Vücut ısısının > 38C veya < 36C olması
Solunum sayısının > 20/dk veya PaCO2 < 32 mmHg olması
Lökosit sayısının > 12000 / μL veya < 4000 /μL ya da %10’dan fazla immatür nötrof l granülos tler n dolaĢımda var olması
Sepsis: SIRS tablosuna ait olan bulgulardan iki ya da daha fazlasının bulunması ile
birlikte, kanıtlanmıĢ ya da muhtemel infeksiyon varlığı olarak tanımlanmaktadır. Eğer sistemik inflamasyon bulguları direkt olarak infeksiyona bağlı ise artık terim olarak sepsis kullanılmalıdır. 2012’de yayınlanmıĢ olan sepsis tanımlamasında bir takım tanı kriterleri belirlenmiĢ olsa da bu tanı kriterlerinin hiçbiri sepsis tanısı için spesifik değildir [10]. Etkeni kanıtlanmıĢ ya da Ģüpheli infeksiyon varlığı durumunda sepsis için aĢağıdaki tanısal kriterlere bakılmalıdır (Tablo 1)
Ağır Sepsis: Sepsis mevcudiyeti ile birlikte bir ya da daha fazla orga veya sistemin
fonksiyonunun bozulmasıdır. Ġnfeksiyon varlığı ile birlikte aĢağıdaki bulguların olması ağır sepsis düĢündürür.
Sepsis sonucu geliĢen hipotansiyon
Laktatın normal değerin üstüne çıkması
Ġdrar çıkıĢının 2 saatten daha uzun bir sürede 0.5 ml/kg/saat’in altında seyretmesi
Kreatinin > 2.0 mg/dL olması
Üre > 50 mg/dL olması
Ġnfeksiyon kaynağının pnömoni olmadığı durumlarda PaO2/FiO2 < 200 olması
Total bilirubin > 2 mg/dl olması
Trombosit sayısının < 100.000 μl olması
6
Tablo 1. Sepsiste kabul edilen tanısal kriterler Genel değişkenler
AteĢ > 38.3 C veya Hipotermi < 36C
Kalp atım hızı normal değere göre> 90/dk ya da yaĢa göre normal değerin 2 Standart Sapma (SS) yukarısı
Takipne > 30/dk
Mental durumda bozukluk
Belirgin ödem ya da pozitif sıvı dengesi (24 saat boyunca > 20 mL/kg)
Hiperglisemi (diyabet yokluğunda plazma glukozu > 140 mg/dL ya da 7.7 mmol/L)
İnflamatuar değişkenler
Lökositoz ( Lökosit sayısı > 12.000 / μL Lökopeni (Lökosit sayısı <4000 /μL)
Normal lökosit sayısı ve immatur formların %10’dan fazla
Plazma C-reakt f prote n değer nde artıĢ (normal değer n 2 SS üzer nde) Plazma prokals ton n n normal değer n 2 standart sapma üzer nde olması
Hemod nam k değ şkenler
Arter yal h potans yon (er Ģk nde s stol k kan basıncı <90 mmHg, ortalama arter yal basınç <70 mmHg, veya sistolik kan basıncında >40 mmHg azalma veya normal yaĢ değer ne göre k SS daha düĢük olması)
Organ d sfonks yon değ şkenler
Arteriyel hipoksemi (Parsiyel arteriyel oksijen basıncı (PO2)/ inspire edilen oksijen bölümü (FiO2 ); PaO2/FiO2 <300)
Kreat n n artıĢı (> 0.5 mg/dl ya da 44.2 μmol/l)
Koagülasyon anormallikleri (INR (uluslararası normal oran) >1.5 ya da aPTT (aktive parsiyel tromboplastin zamanı) >60 saniye)
Ġleus (bağırsak hareketler n n azalması veya durması)
Trombositopeni (trombosit sayısı <100.000 /μl) Hiperbilirubinemi (total bilirubin >4 mg/dL ya da 70 μmol/l)
Doku perfü yon değ şkenler
7
Septik şok: Sepsisten Ģüphelenilen durumlarda yeterli sıvı replasmanına rağmen,
hipotansiyon ile birlikte oligüri, akut mental değiĢiklik, laktik asidoz gibi, kiĢinin perfüzyonunda bozukluk olduğunu gösteren belirtilerin ve organ disfonksiyonuna ait bulguların devam etmesi ile karakteriz durumdur. Bir diğer deyiĢle sıvı replasmanı yapılmasına rağmen ağır sepsis sürecindeki devam durumudur.
Multiple Organ Disfonksiyon Sendromu (MODS): Sepsis ve septik Ģok bulguları
mevcut olan hastalarda geliĢen, organ iĢlevlerinin bozulduğu ve gerekli homeostazisin sürdürülemediği durumdur.
2016 yılında ESICM ve SCCM tarafından yapılmıĢ olan Sepsis-3 isimli toplantıda belirtilen tanımlamalar yeniden değerlendirilmiĢtir. Bu konsensus sonucu olarak sepsis tanımı “infeksiyona karĢı gerçekleĢen disregüle konak yanıtına bağlı organ disfonksiyonu” Ģeklinde değiĢtirilmiĢtir [9].
Sepsis düĢünülen olgularda tanı için, yeni belirlenmiĢ kriterlerde “kanıtlanmıĢ infeksiyonun yanında yaĢamı tehdit etmekte olan organ yetmezliği” kriter olarak belirtilmiĢtir. Bu organ iĢlev yetmezlik ve bozukluğu “Sepsis-Related Organ Failure Assessment” (SOFA) skorunda 2 puan ve üstü, puan alımı ile karakterizedir.
ġiddetli sepsis tanımı ve SIRS kriterlerinin kullanımı ise günümüzde terk edilmeye baĢlanmıĢtır. Septik Ģok tanımında ise önceden sepsis ile birlikte sıvı replasmanına direnç gösteren hipotansiyon kriteri mevcut iken, yeni kriterlerde “yeterli sıvı resüstasyonu verilmesine rağmen ortalama arteryel basınç (MAP) değerinin 65 mmHg ve üzerinde tutulması için vazopressör gerekliliği ve serum laktat düzeyinin 2 mmol/l üzerinde olması” olarak isim bulmuĢtur [9]. Yapılan değiĢiklikler Tablo 2’de özet haline getirilmiĢtir.
8
Tablo 2. Toplantılara göre tanımlar ve değ Ģ kl kler
TANIM YORUM
SEPSİS 1991
SEPSĠS Enfeksiyon ile birlikte SIRS SIRS noninfeksiyoz nedenli de olabilir. Ciddi enfeksiyonu olan hastalarda organ iĢlev bozukluğu olmamasına rağmen SIRS olmasıdır.
CĠDDĠ SEPSĠS Akut organ yetmezliği ile birlikte sepsis görülmesi
Sepsisin, sepsis-Ģiddetli sepsis-septik Ģok evrelerinin hepsinde enfeksiyon görülmesi gibi yanlıĢ bir izlenim vardır. SIRS ile birlikte organ yetmezliği görülmesidir.
SEPTĠK ġOK Sıvı resüstasyonundan sonra kalıcı hipotansiyon ile sepsis
Metabolik komponente bakılmaksızın (laktat) kan basıncının düĢük olmasıdır. SEPSİS-2 2001 DeğiĢiklik yok Sepsis ile ilgili bulgu ve belirtilerin
listesi geniĢletildi SEPSİS 3, 2016
SEPSĠS Konağın infektif ajana uygunsuz yanıtıyla iliĢkili olarak hayatı tehdit edici organ yetmezliği olmasıdır
Enfeksiyonun organ yetmezliğine neden olması durumudur. Uygunsuz konak yanıtının tetiklenmesi Ģart değildir.
SEPTĠK ġOK Yeterli sıvı resüstasyonuna rağmen ortalama arteryel basıncın 65 mmHg üstünde tutulması için vazopresör gerekliliğinin olması ve serum laktat düzeyi > 2 mmol/L’dir
Hem dolaĢım, hem de metabolik anomaliler göze alınarak “ağır sepsis” terimi yenilendi. Yeni sepsis-3 kriterlerinin klinik sonuçları geliĢtirdiği doğrulanmalıdır.
2.1.2 Skorlama Sistemleri
Skorlama sistemleri geç 1960’lar ve erken 1970’lerden bu yana üzerinde çalıĢmanın gerçekleĢtiği, amaç olarak hastalığın ciddiyetini belirlemek, organ iĢlev bozukluğunun derecesini bulmak, hastalıktan iyileĢmeyi saptamak, uygulanan tedaviyi hesaplamak, hastları belirli standartlara göre değerlendirmek ve acil servisler ile yoğun bakım üniteleri baĢta olmak üzere hastane servislerinin performansını karĢılaĢtırmak için yaygın ve sık olarak kullanılan sistemlerdir. Bu sistemlerin çoğunda günlük ölçümlerden sağlanan bilgiler kullanılmaktadır [15].
YatıĢ sırasında ya da öncesi çoğu hastanın tanısı belirlenememiĢ olabileceğinden, tanıya dayanan skorlama sistemlerinin bu hastalara uygulanabilmesi fazla mümkün değildir. Bu sebeple yatıĢ öncesi kullanılan bazı skorlama sistemleri fizyolojik ölçümlerde daha baĢaırılıdır. Bu fizyolojik ölçümlerin ve verilerin kullanıldığı skorlama sistemleri, hastlağın klinik gidiĢatı ve mortalitesi ile uyum gösterir [16,17,18].
9 Fizyolojik değerlendirme ve ölçümlerdeki değiĢikliklere bağlı Ģekilde hastalığın c dd yet n tanımlayan; Akut F zyoloj ve Kron k Sağlık Değerlend rmes (Acute Phys ology and Chron c Health Evaluat on; APACHE), Bas tleĢt r lm Ģ Akut F zyoloj Skoru (S mpl f ed Acute Phys ology Score; SAPS), Çoklu Organ Yetmezl ğ Skoru (Mult ple Organ Dysfunct on Score; MODS), Mortal te Tahm n Model (Mortal ty Pred ct on Model; MPM), Loj st k Organ D sfonks yon Skoru (Log st c Organ Dysfunct on Score; LODS), ArdıĢık Organ Yetmezl ğ Değerlend rme Skoru (Seps s Related Organ Fa lure Assessment Score; SOFA) ve y ne günümüzde d ğer skorlardan daha baĢarılı ve kolay uygulanab l r olduğu bel rt len Hızlı ArdıĢık Organ Yetmezl ğ Değerlend rme Skoru (Qu ck- Sepsis Related Organ Failure Assessment; qSOFA) sepsisin skorlama sistemlerindendir [9,16,19].
2.1.3 Epidemiyoloji ve İnsidans
Sepsis, yüksek ölüm oranları ile seyreden, bunun yanı sıra ise yüksek tedavi maliyetiyle de sorun oluĢturan ciddi bir sağlık problemidir. Mevcut tabloyu oluĢturan bulguların asıl sebebi altta bulunan baĢka hastalıklar da olabileceğinden sepsis epidemiyolojisi ile ilgili veriler sınırlıdır. Keza oluĢan tablonun sorumlusu en az sepsis kadar altta yatan hastalık da olabilir [20].
Sepsis insidansı küresl olarak bölgelere göre değiĢiklikler göstermekle birlikte, geliĢmiĢ diyebileceğimiz ülkelerde insidans yüksek olmasına rağmen, mortalite açısından daha düĢük oranlıdır. Son on yılda yapılan araĢtırmalara göre sepsis insidansı artarak devam etmektedir. GerçekleĢtirilen incelemelerde sepsise bağlı mortalite oranları Amerika BirleĢik Devlet’inde %28.3, batı ve orta Avrupa’da ise %41 olarak belirlenmiĢtir. Yeni Zelanda ve Avusturalya’da yapılan yine çok merkezli bir baĢka çalıĢmada ise mortalite oranları %18-20 arasında bulunmuĢtur [12,19,21].
Uluslararası çok merkezli yapılan retrospektif bir çalıĢma göstermektedir ki, 1995 ve 2015 yılları arasında yapılan incelemede sepsis sıklığı 100.000’de 437 kiĢi/yıl iken, ağır sepsis için 100.000’de 270 kiĢi/yıl olarak bulunmuĢtur. Fakat bu verilerin kısıtlılığı sadece geliĢmiĢ ülkelerde mevcut olan verileri yansıtmasıdır [22]
Yapılan araĢtırmaların bir baĢka sonucu da, sepsis epidemiyolojisinde ırk ve cinsiyet farklılıklarının da önemli bir rol oynamasıdır. Örnek verilecek olursa afroamerikan topluma ait erkek bireylerde sepsis sıklığı daha yüksektir. Bununla birlikte erkek ve kadın cinsiyet (%58.8) kıyaslamasında da erkek cinsiyetin (%59.6) sepsis açısından daha riskli olduğu görülmüĢtür [23]. Bunun nedeni olarak da sigara kullanımına bağlı KOAH (Kronik Obstrüktif Akciğer Hastalığı), HIV (Human Indeficiency Virus), kronik alkolizm gibi hastalık ve
10 durumların erkek cinsiyette daha sık görülmesi ile iliĢkilidir. Yine kıĢ aylarında artan respiratuar sendromlar nedeniyle kıĢ aylarında görülen sepsis insidansı yaz aylarına göre daha yüksektir. Yoğun bakım ünitelerinde ise nozokomiyal infeksiyonların daha sık görüldüğü hastanelerde sepsis insidansının daha fazla olması göze çarpmaktadır [22,24].
Türkiye’de ise sepsis insidansını ve epidemiyolojisini gösteren çalıĢmalar sınırlıdır. En büyük ve kapsamlı çalıĢmalardan biri olarak 1983-1989 yılları arasındaki olguların değerlendirildiği Hacettepe Üniversitesi tarafından yapılan çalıĢma öne çıkmaktadır. Bu çalıĢmada yedi senelik dönemdeki sepsis ve bakteriyemi etkenleri değerlendirilmiĢ, sonuç olarak ise insidans 4.2/1000 ve mortalite %45 olarak bulunmuĢtur [18].
GeliĢmiĢ toplumlardaki oranlar ülkemiz nüfusuna uyarlarınırsa, beklenen septik hasta sayısının 100.000 civarında olması öngörülmektedir [25].
2.1.4 Risk Faktörleri
Sepsis için kimlerin riskli durumda olduğunu bilmek, sepsisin önlenmesi açısından yüksek derecede önem taĢır. Hastaya ve tedaviye ait bazı risk faktörleri Ģunlardır:
Altta yatan malignite varlığı
YaĢ (Yenidoğanlar ve 65 yaĢ üstü hastlar riskli gruptadır)
Mevcut ek hastalık (KOAH, Diabetus Mellitus, Kronik Böbrek Yetmezliği, Konjestif Kalp Yetmezliği, Karaciğer Sirozu)
Konak immun sistemini zayıflatan ilaç ve hastalıklar (Hematolojik maligniteler, nötropeni, disproteinemiler, kortikosteroid ve immunosupressif ilaç kullanımı vb.)
GeniĢ vücut yüzdeli yanık ve travma olguları
Lokalize mevcut infeksiyonlar
Lohusalık ve septik abortus
Yakın geçmiĢte kullanılmıĢ, etkene ve sebebe uygun olmayan antibiyotik tedavisi
Yakın zamanlı yoğun bakım ünitesinde yatıĢ öyküsünün olması
GeçirilmiĢ invaziv cerrahi giriĢimler
Kan, kan ürünü ya da parenteral mayinin fazla miktarda verilmesi
2.1.5 Etiyoloji
Teorik olarak eğer konak ve mikroorganizma için Ģartlar elveriĢli ise, mevcut olan tüm mikroorganizmalar sistemik infeksiyon yanıtını baĢlatarak, konağı sepsis ve bununla iliĢkili sendromlar oluĢturabilir. Etiyolojide sepsisten sorumlu en sık organizmalar bakterilerdir. Bakterileri, mantarlar,viruslar ve parazitler izler. Etken olarak 1960-1980 yılları
11 arasından ağırlıklı bir Ģekilde gram negatif bakteriler izlenirken, 1980’lerin ortalarında gram pozitif bakteriler sonucu geliĢen sepsis sıklığında artıĢ izlenir hale gelmiĢ ve gram negatif bakteriler ile iliĢkili sepsis ile aynı oranlara sahip olmaya baĢlamıĢtır. Sepsis etkeni olarak tespit edilen mikroorganizmalar, kurumdan kuruma değiĢiklik gösterse de , sepsis nedeni olarak hastalarda en sık gözüken mikroorganizmalar; Staphylococcus aureus, Escherichia coli, Klebsiella pneumoniae, Koagülaz boyaması negatif olan stafilokoklar (KNS), enterokoklar, Pseudomonas aeruginosa, Candida türleri ve diğer Enterobacteriaceae üyeleri olarak bildirilmiĢtir [26,27].
Sepsis kaynağı olarak en sık üriner sistem enfeksiyonları görülmektedir. Solunum sistemi enfeksiyonları, damar içi kataterler, solunum sistemi enfeksiyonları ise önemli sepsis kaynaklarıdır. Ġntraabdominal enfeksiyonlar ise gastrointestinal sitemin herhangi bir noktasından oluĢan perforasyon ya da gastorintestinal sistemin cerrahi operasyonları ile geliĢir ve polimikrobiyal bir yapıdadır. Gastrointestinal sistemden kaynaklanan sepsis yoğun bakım ünitelerinde sıklıkla ağır sepsise sebep olabilen enfeksiyonlardır [28]. Ġntraabdomianl infeksiyonlarda hem anaerobik hem de aeorobik bakteriler suçlanmaktadır. Aerob bakteriler ortamdaki oksidasyon-redüksiyon potansiyellerini azaltarak, ortamı anaerob bakteriler için daha uygun hale getirirken, anaerob bakteriler ise kısa zincirli yağ asitleri üreterek nötrofillerin etkenlere karĢı olan fonksiyonunu bozar. Ġntraabdominal sepsis etkenleri olarak, birçok fizyolojik olaydan gram negatif bakteriler sorumlu iken, anaerob bakteriler ise genel olarak abse oluĢumundan sorumludur [26,28]. Mortalite oranları yüksek seyreden intraabdomianl sepsis olgularaında en sık karĢılaĢılan etkenler Tablo 3’te belirtilmiĢtir.
Tablo 3. Ġntraabdominal kaynaklı sepsislerde sıklıkla karĢılaĢılan etkenler
Fakültatif Gram (-) Basil Zorunlu Anaeroblar Fakültatif Gram (+) Koklar
Escherichia coli Bacteroides fragilis Enterococcus sp.
Klebsiella sp. Fusobacterium sp. Staphylococcys sp.
Proteus sp. Clostridium sp. Streptococcus sp.
Enterobakter sp. Peptococcus sp.
Morganella morganii Lactobacillus sp. Diğer Enterik Gram (-)
Basiller
Peptostreptococcus sp.
Aerobik Gram (-) Basiller Pseudomonas aeruginosa
12
2.1.6 Sepsis Fizyopatolojisi
Sepsisin ortaya çıkmasındaki en önemli etkenler, konağın immun sistem durumu ve bakteriyel etkenin virulans faktörüdür. Sepsis etkeni bakteriler genellikle damar dıĢı bir infeksiyon odağından kaynaklanır ve dolaĢıma girer. Sepsisin oluĢum sırasında immun sistem ile bakteriyel etkenin virulans faktörü arasındaki denge önemlidir. Deri, mukoza, kompleman sistemi, immunoglobinler, fagositik hücreler, sitokinler ve lenfositler immun sistemi oluĢturur. Sepsise bağlı geliĢen tabloların oluĢmasında bakterilerin yapıları, invazyon yetenekleri ve toksinleri de etkilidir [29].
Sepsis geliĢimi için ilk basamak bir mikroorganizma tarafından bir kiĢinin enfekte olmasıdır. Sepsisin tetiklenmesi için ise mikroorganizmanın dolaĢıma girmesi tek baĢına yeterli olmaz. Etken giriĢi ile birlikte, endojen mediyatörler de salınıp aktive olmalıdır. Ġmmun sistemin ilk yanıtı, fagositik hücreler aracılığıyla olur. (Makrofajlar, monistler, granülositler) Fagositik hücrelerin arkasından immunglobülinler ve immünkompetan hücreler de yanıt oluĢturmak için aktive olur. Bu yanıtın oluĢmasındaki en önemli etkenler bakteri hücre duvarına ait olan bileĢenlerdir. Gram (-) bakterilerde bu bileĢen endotoksinler iken, Gram (+) bakterilerde teikoik asit olarak öne çıkmaktadır [30].
Septik Ģok tablosu sepsis beraberinde görülen patofizyolojik olayların en önemlilerinden biridir. Septik Ģok tablosu geliĢen hastalarda izole edilen bakterilerde en sık Gram (-) bakteri grupları görülmektedir. GeliĢen septik Ģok tablosuyla iliĢkili olarak, trombaksan A2, Prostoglandin I2, histamin, nitrik oksit (NO) ve serotonin gibi vazodilatasyona sebep olan mediyatörlerin ortaya çıkımı söz konusu olur. Bu bahsi geçen vazoaktif mediyatörler, dolaĢım sistemindeki vasküler direnci azaltarak, kan akımının da azalamasına sebep olur. Sepsiste dolaĢıma salınan bu vazoaktif mediyatörlerin etkisi sonucunda hipotansiyon ve buna da bağlı olarak Ģok tablosu geliĢir [31,32,33].
Bakteriyel antijenlerden etkisi en iyi bilineni endotoksindir. Endotoksin; endotele ait hücreleri, mononükleer fagositleri ve diğer hücreleri aktifleyerek kompleman sistemi ve koagülasyona ait kaskadın aktivasyonuna neden olur. Sepsis tablosu geliĢen hastalardaki hedef organ damar entodelidir. Salınan mediyatörlerin tamamı damarlar üzerine etki gösterir. Bu mediyatörler (Tümör nekroz faktör-α (TNF-α), Platelet-Trombosit aktive edici faktör (PAF) Tromboksan A2, Endotoksin, Ġnterlökin-1 (IL-1), Nitrik oksit) endoteldeki geçirgenliği arttırır. Kompleman sistemindeki aktifleĢme, damar geçirgenliğinde artma sebebiyle sonuç olarak endotel hasarı meydana gelir. Ayrıca nötrofillerden salınan toksik oksijen radikalleri ve bazı lizozomal enzimler de endoteldeki geçirgenliği arttırır ve bu artıĢ, endotel dıĢına sıvı kaçıĢını, mikrotrombüs oluĢumunu ve endoteldeki hasarı arttırır. Eğer endotel hasarı
13 Ģiddetlenir ve hasarın bulunduğu organda perfüzyon bozukluğuna sebep olursa organ yetmezliği geliĢimine yol açar. Endotel hasarı birden çok organda gerçekleĢir ise çoklu bir organ hasarı söz konusu olur ve bu multipl organ yetmezliği olarak adlandırılır. Bu hasar kontrol edilemez boyuta gelmeye baĢladığında metabolik düzensizlikler geliĢir. Akciğer, böbrek, karaciğer ve kalp sepsiste organ yetmezliği ile en sık karĢılaĢılan organlardır [31,34].
Sepsiste olaya sebep olan yapı mikroorganizmalar ya da onlara ait toksinler olsa da, sepsis geliĢiminde konak kiĢinin organizmaya karĢı aĢırı yanıtı, yaygın inflamasyon, çoklu organ iĢlevsizliği ve yetersizliği ile sonuç bulur. Sepsis, damar içi volümdeki kayıp sonrası hemostatik balans bozukluğu, endotelin permiabilitesindeki bozulma sonucu endotel disfonksiyonu, bunlarla birlikte geliĢen kardiyovasküler bozukluklar ve hücre içi hemostazda bozulma ile birlikte görülür. Sepsiste görülen bahsi geçen çoklu bozulma ve organ yetersizliklerinden ve hatta ölümden sorumlu olan durum ise hücre hipoksisi ve apoptozdur [35].
ĠlerlemiĢ sepsiste birden fazla organda mikroorganizmaya maruz kalma, mevcut mikroorganizmaya ait toksinler, buna bağlı konak tarafından salınmıĢ mediyatörlerin vermiĢ olduğu etki, perfüzyon bozuklukları ve Dissemine Intravasküler Koagülopati (DIC) sonucu geliĢen patolojik değiĢiklikler oluĢabilir. Mevcut tabloda gerçekleĢen hasar histopatolojik olarak, fibrin polimerleri, hemoraji, nekroz, konjesyon ve ödem ile karakterizedir. Özellikle akciğerde solunum yetmezliği sonrası hemorajik değiĢiklikler sık görülür. Akciğerlerden sonra lezyonlar sıklıkla karaciğerde zonal nekrozlar ve barsaklarda akut iskemik enterokolit olarak görülür [36].
2.1.7 Sepsisin Tedavisi
Ġlk yayınlanması 2004 yılında olan Sepsiste Sağkalım Kampanyası (Surviving Sepsis Campaign) sepsis tedavisinde önerilmekte olan en yeni ve en güncel tedavi kılavuzu olarak kabul görmüĢtür [37]. Son olarak 2916 yılında güncellenen önerilerin esasında Sepsis Paketi mevcut olup (Sepsis Bundle) yapılması gerekenler bir paket halinde önerildiği için bu isim verilmiĢtir [38]. Bu kılavuza 2018 yılında ise bir takım güncellemeler getirilmiĢtir. 2005 yılında beri bu paketler, sepsis tedavisinin köĢetaĢı olmuĢtur. Yayınlanan son güncellemeler ile birlikte önceden 3.saat ve 6.saat olarak ayrılan paketler, artık 1.saat paketi olarak bir baĢlık altında toplanmıĢtır [39]. 1.saat paketinde yapılan değiĢiklik, öneri ve öneri düzeyleri Tablo 4 olarak aĢağıda verilmiĢtir.
14
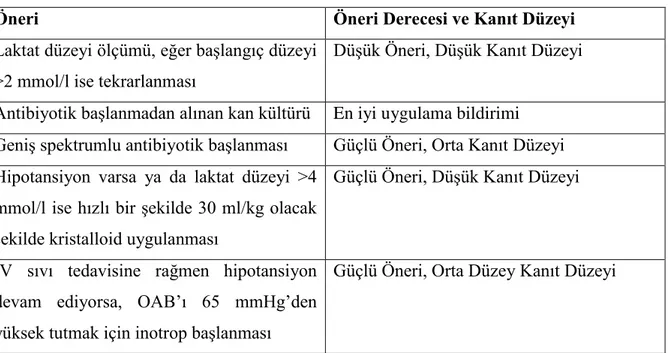
Tablo 4. Sepsis Tedavisinde 1. Saat Önerileri Tablosu
Öneri Öneri Derecesi ve Kanıt Dü eyi
Laktat düzeyi ölçümü, eğer baĢlangıç düzeyi >2 mmol/l ise tekrarlanması
DüĢük Öneri, DüĢük Kanıt Düzeyi Antibiyotik baĢlanmadan alınan kan kültürü En iyi uygulama bildirimi
GeniĢ spektrumlu antibiyotik baĢlanması Güçlü Öneri, Orta Kanıt Düzeyi Hipotansiyon varsa ya da laktat düzeyi >4
mmol/l ise hızlı bir Ģekilde 30 ml/kg olacak Ģekilde kristalloid uygulanması
Güçlü Öneri, DüĢük Kanıt Düzeyi
IV sıvı tedavisine rağmen hipotansiyon devam ediyorsa, OAB’ı 65 mmHg’den yüksek tutmak için inotrop baĢlanması
Güçlü Öneri, Orta Düzey Kanıt Düzeyi
Serumda bulunan laktat düzeyi, doku perfüzyonunun tam olarak bir direkt belirteci olmasa da, artan adrenerjik deĢarja bağlı, aerobik glikoliz ve bununla ilgili kötü sonuçlara bağlı olarak artmıĢ olması, dokuda gerçekleĢen bir hipoksinin göstergesi olabilir [40,41]. Laktat düzeyine göre yapılan resüsitasyon sonrası mortalitenin azaldığını gösteren randomize kontrollü çalıĢmalar mevcuttur [42,43].
Sepsis tanısı ve tedavisinde alınacak olan steril kan kültürü, baĢlanılan antibiyotiğin ilk dakikaları içerinde ya da öncesinde alınmalıdır [44]. Bu tedavi baĢlayan kiĢiye, hastalığı yaratan etkenleri erken tanıması ve doğru ya da uygun tedavi baĢlanımı için fayda sağlar [45]. Kan kültürü aerobik ve anaerobik olmak üzere en az 2 set olarak alınmalıdır.
Sepsis ya da septik Ģok Ģüphesi altında takip edilen hastalarda muhtemel tüm etkenlere etki edecek Ģekilde bir veya daha fazla antibiyotik hızlı bir Ģekilde baĢlanmalı [6]. Eğer hastada etken izolasyonu olmaz ya da etken belirlenmesi sağlanır ise, mevcut olan tedavi daraltılabilir.
Sepsis Ģüphesi ile baĢlanan erken ve etkili sıvı tedavisi, sepsis ya da septik Ģok iliĢkili olan hipotansiyon veya laktat yüksekliği olan durumlarda büyük bir önem arzeder. Yayınlanan kılavuzlar, 30 mL/kg’dan olmak üzere kristalloid sıvı tedavisi önermektedir. Sepsis tanısı alan hastaların tedavisinde, kristalloid sıvıların kolloid sıvılara karĢı belirgin bir üstünlüğü olmamamasına rağmen, albümin tedavisinin maliyetinin fazla etkin bulunmaması sebebiyle, sepsiste önerilen öncelikli sıvı resüsitasyonu kristalloidler olmuĢtur. Hatta bazı
15 yayınlar yoğun bakım ünitesine kabulü olan hastalarda pozitif sıvı dengesi varlığının zararlı olduğunu da göstermektedir [47,48].
Hayati organlara yeterli kan akıĢının sağlanması ve bu organları perfüze edebilmek, sepsis tedavisindeki en önemli basamaklardan biridir. Perfüzyonun sağlanmasında yaĢanacak bir gecikme olmaksızın, verilen sıvı resüsitasyonuna yanıt vermeyen hipotansiyon durumunda vazopressör tedavisi ile OAB’yi 65 mmHg’nin üstüne çıkarmak için ilk bir saat içinde tedavi baĢlanmalıdır. GerçekleĢtirilen meta analizlere bağlı olarak bu hasta gruplarında dopaminden kaçınılmalı ve ilk tercih için nöradrenalin düĢünülmelidir. Bununla birlikte nöradrenalin dozunu azaltmak için düĢük doz vazopressin ve dirençli hipotansiyonu önlemek için epinefrin kullanımı da önerilmektedir.
2.2 Böbrek
2.2.1 Böbreğin Genel Bilgi ve Yapısı
Ġnsan vücunda böbrekler, vücudun her iki yanında, retroperitoneal alanda yer alan uzunlamasına 9-13 cm boyularında ve 2-3 cm kalınlığındaki organlardır. Karın alt duvarında retroperitoneal alanda bulunurlar. Karaciğerin etkisi sebebiyle sağ böbrek soldaki böbreğe göre biraz daha alt tarafta yerleĢim gösterir. Böbrekler mobil organlardır. Bunun etkisiyle solunum esnasında ve pozisyonel olarak 3 cm’ye kadar yer değiĢtirebilirler. Böbrek morfolojik olarak 2 kısıma ayrılır. Bu kısımlar parankim ve sinüs(hilus)’tur. Böbrek parankimi korteks ve medullayı ihtiva eder. Medulladan sinüse doğru uzanım gösteren piramit Ģeklinde ek kısımları mevcuttur ve bunlar “piramis” olarak isimlendirilir. Piramislerin en uç kesimi ise “papilla” olarak isimlendirilir. Mevcut olan her bir piramis ve buna uyan alanı ihtiva eden alandaki korteks bir renal lobu oluĢturur. Böbrekteki papillalar, minör kaliks adı verilen ve sayısı 7-14 arasında değiĢen boĢluklara açılır. Minör kaliksler ise birleĢip majör kaliksleri, majör kaliksler ise birleĢip renal pelvisi oluĢturur. Renal pelvisin devam eden kısmı üreter olarak adlandırılır. Renal hilus, böbreğin sinir,arter,ven ve renal pelvisin böbrek içine giriĢ çıkıĢ yaptığı alanın adıdır. Renal hilus, buradaki yapılara destek olan yağ dokusu ihtiva eder [49].
Böbreği dıĢtan içe doğru sayacak olursak, fasia renalis, kapsula adiposa ve kapsula fibroza olmak üzere 3 kılıf sarar. Fasia renalis, karın duvarından kaynaklanan fasia subserosanın kapsula adiposayı sarması ile oluĢur. Sağ böbrek 12. kosta ile komĢuluk yaparken, sol böbreğin daha yukarıda olması sebebiyle bu seviye 11. ve 12. kot civarındadır. Sol böbrek ayrıca glandula suprarenalis, duodenum, pankreas kuyruğu ve kolon ile de komĢuluk eder [50].
16
Resim 1. Böbreklerin vücuttaki yerleĢim yeri [51]
Korpus pararenalis böbreklerin karın arka duvarına yapıĢmasını sağlayan yağ dokusunun adıdır. Gerota fasiyası, böbrekten köken alan patolojik durumları sınırlamaya yarıyan patolojik bir engeldir. Böbrek kapsula fibrosa ile çevrilmiĢtir. Bu yapı çok sayıda fibroz lifler, daha az olacak Ģekilde sarı elasitk lifler ve minimal sayıda da düz kas lifi ihtiva eder. Böbreğin iç kısmında, böbreğe giren ve çıkan yapılarla birlikte renal pelvisi de içeren bölgeye hilus denir [52].
2.2.2 Böbreğin Fonksiyonları
Vücut metabolizmasının ve iç ortamın normal seviyede devamının korunması çok ehemmiyetlidir. Ġç ortamın kimyasal yapısının herhangi bir anormallik olmadan dengede tutulması, büyük ölçüde 2 organ tarafından gerçekleĢtirilir. Bu organlardan birincisi oksijen-karbondioksit dönüĢümünü sağlayan akciğerlerdir. Böbrek ise yabancı sayılabilecek madde ve itrah edilmesi gereken diğer önemli bileĢiklerin miktarını düzenler. Kanın pH’sının ayarlanmasında yine bu iki organ büyük miktarda görev alır. Böbrekler, iç ortamın normal düzeyde ilerlemesini gerçekleĢtirdiği 3 eylem ile sağlar. Bunlar filtrasyon, rezorbsiyon ve sekresyondur.
17 Filtrasyon: Kan plazmasının bir kısmının, içinde eriyik halde bulunan öğeler ile birlikte, süzülme yoluyla itrah edilmesidir. Kandan ayrılan süzüntünün muhteviyatı, proteinler ve proteine bağlı öğeler hariç, kan plazmasının aynısıdır.
Rezorbsiyon: Filtrasyon ile süzme iĢleminden geçen ve kandan uzaklaĢtırılan, ancak homeostasis için elzem olan öğelerin emilerek kana geri katılmasıdır.
Sekresyon: Beden için yararsız ya da zararlı olan kalıntı ve yabancı öğelerin kandan alınıp tübülüs sıvısına aktarılmasıdır [53].
Bunların dıĢında böbreklerin endokrin sistem üzerine etkileri de mevcuttur. Prostoglandin, renin, kalsitriol, eritropoetin gibi hormonların yapım yeri yine böbreklerdir. Ayrıca böbrekler, glukagon, insülin, aldosteron ve parathormon gibi bazı hormonların da yıkıma uğradığı alandır [54].
2.2.3 Sepsis ve Böbrek
Yoğun bakım ünitelerinde yatmakta olan tüm hastların yaklaĢık olarak %15-20’sinde sepsis kaynaklı akut böbrek yetmezliğinde, renal hasarın derecesine göre %20,9 ile %56,8 arasında mortalite mevcuttur. Bu sebeple, sepsis kaynaklı erken dönem böbrek yetmezliğinin önceden tanınması, riskli durumların ve patogenezinin iyi anlamlandırılması önem arz eder. Son yıllarda gerçekleĢtirilen çalıĢmalarla, sepsise bağlı akut böbrek yetmezliğinde patolojik mekanızmanın sepsis iliĢkisiz akut böbrek hasarından farklılıklar gösterdiği ortaya konmuĢtur [55]. Sepsis ile iliĢkili gerçekleĢen erken dönem böbrek yetmezliğinin patofizyolojisi ile alakalı görüĢler, renal vazokonstriksiyon, akut tübüler nekroz ve iskemiden, heterojen vazodilatason, hiperemi ve akut tübüler apoptaza doğru yön değiĢtirmektedir.
18
Resim 2. Renal Histoloji [56]
Özellikle apoptoz renal hasar oluĢumunda gittikçe ön plana çıkmaktadır. Yakın zamanlı yapılmıĢ ve yayınlanmıĢ çalıĢmalarda, sepsis Ģüphsi mevcut olan hastalardan gerçekleĢtirilen renal biyopsiler sonucunda tübüler apoptozun daha çok görülmesine yoğunlaĢılmıĢtır. Apoptozis, iskemi, eksojen toksinler ya da endojen mediyatörler tarafından aktiflenebilir. Yoğun bakım gerektiren hastalarda ve bazı hayvan deneylerinde de sık olarak görülen hipergliseminin de apoptoz oluĢumunda renal tübül hücrelerine zarar vererek sebep olduğu gösterilmiĢtir [57].
Bu yeni bilgiler öncülüğünde sepsis tedavisi için yeni seçenekler ortaya atılmıĢtır. Hiperglisemi tedavisi, antiinflamatuar etkiyle birlikte nefroprotektif rolüyle de birlikte ayrı bir ehemmiyete sahiptir. Toksik mediyatörleri vücut dolaĢımından uzaklaĢtıran hemofiltrasyon metodları öncelikli olarak iĢleme konulmalıdır. Proinflamutar sitokinleri inhibe eden ghrelin ve apoptatik yolak blokajı yapan kaspaz inhibitörleri ile nitrik oksit sentaz inhibitörleri ise henüz deneysel yöntemler olarak mevcudiyetini sürdürmektedir. Mevcut patogeneze yönelik, yeni tedavi metotları ile mortalite ve morbiditede azalma sağlanması amaçlanmaktadır. Yeni bulunan ilaçlar, antibiyotikler ve immunmodülasyona göre verilen tedavi süreçlerine rağmen, septik Ģok, halen %30-90 mortalite oranı ile seyreden, önemli bir sağlık sorunudur [55].
Bu durum septik Ģok ile alakalı olarak yapılan deneysel çalıĢmalarda önemli bir hızla artıĢa neden olurken, mevcut tabloların çok çeĢitli olması, tedavi imkanlarındaki çeĢitlilikler,
19 değiĢik etiyolojik nedenler sonucu istenilen düzeyde baĢarı sağlanamamaktadır [58]. Aynı Ģekilde, klinik deneysel araĢtırmalar ıĢık tutacak olan deneysel hayvan modellerinde ise farklı septis modelleri, değiĢen hayvan türlerinde yapılan uygulamalar gibi nedenlerle sonuçlarda farklılık ve çeliĢkiler mevcuttur. Deneysel sepsis modellerinin yeterliliği de yeri geldiğinde tartıĢılır hale gelmiĢtir. Bu modellerde sıkça kullanılmakta olan fare, rat gibi hayvanların ise insanlara göre, septik Ģok esnasında endotoksikne daha az duyar göstermesi tartıĢmalara sebep olurken, Gram (+) bakterilerle çalıĢmaların az olması gibi bazı faktörler de bu yapıların eleĢtirel hale gelmesini sağlamaktadır [59].
Deneysel hayvan çalıĢmalarındaki yukarıda bahsi geçen bütün olumsuzluklara rağmen, en önemli nokta Ģudur ki, insanlar üzerinde uygulanacak ilaçların klinik çalıĢmalar öncesinde mutlaka ve mutlaka hayvan deneylerinde incelenip değerlendirilmesi gerekliliğidir.
2.3 Karaciğer
2.3.1 Karaciğerin Anatomisi
Karaciğer, en dıĢta bulunan yüzü Capsula fibroza ile çevrelenmiĢ, elastiki yapıda mevcut olan, vücuttaki en büyük metabolizma organıdır. Karaciğerin rengi, canlının türüne, içermiĢ olduğu kan ürünleri miktarına, beslenme ve kronik hastalıkları bağlı olarak değiĢiklik göstermesine rağmen genel olarak doğal hali kırmızıya çalan bir kahverengi Ģeklindedir. Henüz yeni doğan canlılarda ve gebelerde sarıya yakın bir kahverengi olabilirken, kronik hastalık taĢıyan kiĢilerde koyulaĢmıĢ bir kahverengi olabilir. Karaciğer, karın ön üst duvarına yakın kısımda facies diaphragmatica ve arka alt duvarına yakın kısmında ise facies visceralis olmak üzere 2 yüze sahiptir. Ön yüz diyaframın kavisine uygun olacak Ģekilde dıĢ bükey bir halde iken, arka yüz böbrek,özefagus, mide, duodenum, transvers kolon ve fleksura coli ile komĢuluk içerirken iç bükey bir kavise sahiptir. Karaciğer genel olarak 4 lobdan oluĢur. Bunlar, lobus hepatis dexter ve sinister (sağ ve sol lob) ile lobus caudatus ve quadratus (kuyruklu ve dört köĢeli) olarak adlandırılmıĢtır [60].
Safra salgısı, karaciğerin önem arz eden bir fonksiyonu olup, karaciğer içinden ductuli biliferi denilen safra kanallarıyla taĢınmaktadır. Bu kanallar karaciğer içinde birleĢip, karaciğerin dıĢına taĢınır ve ductus hepaticus communisi oluĢtururlar. Ductus hepaticus communisin birleĢmesi sonrasında da ductus cysticus denilen safra kesesi kanalını meydana getirirler. Safra kesesi karaciğerin viseral adı verilen yüzünde, lobus quadratus ve lobus hepatis dexter arasında, fossa vesica fella isimli boĢlukta bulunmaktadır. At, deve ve ratlarda safra kesesi bulunmamaktadır [60].
20
Resim 3. Karaciğer Anatomisi [61]
Karaciğer sahip olduğu büyük damarlarla da önemlidir. Karaciğere giren vena portae ve arteria hepatica, çıkan damar ise vena cava caudalis’tir. Vena portae, bağırsaklardan emilmiĢ besinle yüklü venöz kan ile birlikte, mide, pankreas ve dalaktan gelen venöz kanı karaciğere doğru taĢımaktadır. Karaciğere içinde dallara ayrılan vena portae en son karaciğerin en küçük histolojik yapısı olan lobulusların çevresinde sinusoidlere açılmaktadır. Burada aldığı isim vena interlobularis portalis olmaktadır. Aynı Ģekilde a.hepatica’nın son dalları da sinusoidlere açılır. BirleĢen sinusoidler, lobulusların merkezinde kendisine yer bulan vena centralis’lere açılır. Lobuluslardan ayrılan vena centralis’ler birleĢerek vena interlobularis hepaticusu, bu yapılarda vena hepatica ve sonunda da vena cava caudalis’leri oluĢturmaktadır [60].
21
Resim 4. Karaciğer histolojisi [62]
2.3.2 Karaciğerin Fonksiyonları
Karaciğer, vücut homeostazının devamlılığının sağlanmasında çok önemli bir fonksiyona sahiptir. Fonkiyon olarak metabolik iĢlevlerin düzenlenmesinde merkezdedir. Karaciğerde, sindirim sonucu alınana aminoasit, lipit, karbonhidrat ve vitaminin iĢlenmesi, serum için lazım olaan proteinlerin sentezi, demir düzey ve metabolizmasının düzenlenmesi, safranın yapım ve salınımı, vücutta oluĢan atık ürünlerin ve dıĢardan alınmıĢ ancak zararı olabilecek maddelerin atılımı ya da detoksifiye edilmesi ve safraya verilmesi gibi temel görevleri gerçekleĢtirmektedir [60].
Karaciğer çeĢitli olumsuz etkilere maruz kalabilen bir organdır. Metabolik ve toksik ajanlar, dolaĢım bozuklukları, mikrobiyal etkenler bunların baĢlıcalarıdır. Çok yüksek bir fonksiyon yelpazesine sahip olan bu organ, bu olumsuzluklara rağmen yüksek düzeyde bir yenilenme kabiliyetine sahiptir. Herhangi bir operasyon sonucu yaklaĢık %60’ına kadar alınmıĢ sağlık bir karaciğerde bile karaciğer yetmezliği ya da fonksiyon bozukluğu ancak minimal ya da geçici oranda görülür. 30-45 gün içinde rejenerasyon sonucu yeni doku geliĢimi gözlenir. Safra akıĢının bozulmadığı durumlarda, yoğun nekroz geliĢmiĢ karaciğer
22 dokusuna sahip hastalarda, karaciğer yetmezliğinin akut evre etkilerinin sonuçları atlatılabilirse, sebepler ortadan kalktığında tam bir doku yenilenmesi gerçekleĢebilir [60].
Karaciğer yetmezliği, viral hepatit, sepsis, kronik alkolizm, metabolik ve kalıtsal hastalıklar sonucu geliĢebilir. Ancak karaciğerin sahip olduğu yüksek yenilenme kapasitesi sonucu, karaciğer yetmezliği, hepatositlerin yaygın nekrozu ve fonksiyonların %90 civarında kaybedilmesinden sonra gerçekleĢir [60].
2.3.3 Karaciğer ve Sepsis
Ġnsan vücuduna ait en büyük salgı bezi olan karaciğer, immünolojik ve metabolik homeostazisin sağlanmasındaki en önemli rollerden birine sahiptir. Toksik maddeleri detoksifiye etmek, enerji üretiminde bulunmak, alınan besinlerin dönüĢtürülmesi ve metabolitlerine ayrılmasını sağlamak, hormonal dengeye katkıda bulunmak, pıhtılaĢma ile ilgili faktörleri üretmek gibi bir çok fonksiyona sahiptir. Bu önemli fizyolojik iĢlevleri, sepsisin sağ kalımında karaciğere önemli görevler verir [63]. Sepsis öncesinde hastada kronik bir karaciğer rahatsızlığı bulunması sepsis prognuzunu olumsuz etkiler. Sepsisin fizyopatogenezinde karaciğer önemli, etkin ve bunlarla birlikte kompleks bir rol üstlenir. Sepsis ile ilgili histopatolojik çalıĢmalarda, dokularda oluĢan kolestaz varlığı baĢta olmak üzere, karaciğer dokusunda oluĢan hasar bulguları incelenmiĢtir [64,65].
Sepsis sonucunda karaciğer, patojenler, toksinler, meditaörler ve hipoperfüzyon tarafından hasar görür. Bu hasar sonucu oluĢan karaciğer disfonksiyonunun, sağ kalım üzerine olumsuz etkileri çeĢitli çalıĢmalarda gösterilmiĢtir [64,66].
2.4 Morus Nigra
2.4.1 Morus Nigra (Kara Dut)’nın Genel Yapısı
Dut, ılıman bölgelerde yetiĢmekte olan bir meyve türüdür. Tropik ve subtropik bölgelerde de yetiĢimi sağlanabilmektedir. Dut, Urticales takımının Moraceae familyasından Morus cinsine girmektedir. Bu cinse ait üyelerden en bilineneleri Morus alba ( Ak dut ), Morus nigra ( Kara Dut ) , Morus rubra ( Al dut ) ve Morus latifolia’dır [67].
Kara dut 2-3 cm uzunluğunda ve kendine özgü sulu ve ekĢi bir tada sahip olup, rengi ile ön plana gelmektedir [64]. Kara dut meyvesi baz olarak Ģeker (%48 fruktoz ve %52 glukoz), %92 oranında sitrik asit ve %8 oranında malik asit gibi organik asitler ve antisiyaninden oluĢmaktadır [68].
23
Resim 5. Morus nigra meyveleri [69]
Yapılan analiz ve gerçekleĢtirilen çalıĢmalar ele alındığında kara dut bileĢimi Ģu Ģekilde özetlenebilir[70,71]:
Kuru madde miktarı (%): 12,5-29,5
Kül miktarı (%): 0,12-1,04
Protein miktarı (%): 0,9-2,64
Ham yağ miktarı (%): 2,5-6,79
pH değeri: 3,30-5,65
Suda çözünürlük (TSS)(%): 14,30-30,80
Mineral bileĢimi: Potasyum en baskın mineraldir Kalsiyum: 0,21-6,6 mg/g Fosfat: 0,40-5,8 mg/g Potasyum: 1,27-15 mg/g Çinko: 0,02-12 mg/g Sodyum: 0,92-3,29 mg/g Magnezyum: 0,37-2,40 mg/g