T.C.
EGE ÜNİVERSİTESİ TIP FAKÜLTESİ ÇOCUK SAĞLIĞI VE HASTALIKLARI
ANABİLİM DALI Prof.Dr.Savaş KANSOY
ÇOCUKLUK ÇAĞI PRİMER HİPERTANSİYON PATOGENEZİNDE RENİN, ALDESTERON, ANJİOTENSİN VE LİPİD METABOLİZMA GENLERİNİN
ARAŞTIRILMASI VE GENOTİP-FENOTİP İLİŞKİSİ
UZMANLIK TEZİ
Dr. Özgür ÖZDEMİR ŞİMŞEK
Tez Danışmanı
ÖNSÖZ
Uzmanlık eğitimim süresince bilgi ve deneyimlerinden faydalandığım tez danışmanım, hocam, sayın Doç.Dr. Ahmet Keskinoğlu ve anabilim dalı başkanı sayın Prof. Dr. Savaş Kansoy başta olmak üzere tüm hocalarım ve uzmanlarıma,
Laboratuvar çalışmalarını yapan hocam Prof.Dr.Afig Berdeli ve ekibi olmak üzere emeği geçen tüm laboratuvar çalışanlarına,
Her aşamada desteğini benden esirgemeyen Prof.Dr.Pembe Keskinoğlu’na,
Tezimin başlangıcından sonuna kadar her aşamasında yanımda olan ablam; Uzm.Dr.Yasemin Özdemir Şahan’a,
Birlikte çalışmaktan zevk aldığım ve mutluluk duyduğum tüm asistan ve hemşire arkadaşlarıma,
En sıkıntılı günlerimde bile benden desteğini ve şefkatini hiç esirgemeyen annem, babam, anneannem ve hep yanımda olan eşim Dr.Tarık Şimşek’e,
SONSUZ TEŞEKKÜRLERİMİ SUNARIM…
Dr.Özgür ÖZDEMİR ŞİMŞEK
İÇİNDEKİLER
GİRİŞ VE AMAÇ...1 GENEL BİLGİLER...3 1. TANIMLAMA...3 2. HİPERTANSİYON ETİYOLOJİSİ...5 2. 1. Primer Hipertansiyon...5 2. 2. Sekonder Hipertansiyon...7 3. HİPERTANSİYON EPİDEMİYOLOJİSİ...84. HİPERTANSİYON HASTASININ DEĞERLENDİRİLMESİ...8
4.1. Kan Basıncı Ölçüm Yöntemleri...8
4.1.a. Palpasyon yöntemi...9
4.1.b. Oskültasyon yöntemi...9
4.1.c. Osilometrik yöntem...10
4.1.d. Doppler yöntemi... 10
4.1.e. Ambulatuvar Kan Basıncı Monitarizasyonu(ABPM)...10
4.2. Klinik...13
4.3. Hedef Organ Hasarının Belirlenmesi...14
5. HİPERTANSİYON PATOGENEZİ...15
5. 1. Genetik Yatkınlık...15
5. 1. 1. Poligenetik Değişimlerin Hipertansiyona Yatkınlık Üzerine Etkisi...15
5.1.1.a.Ace-Renin-Anjiotensin Polimorfizmi...17
5.1.1.b. Aldosteron Polimorfizmi...18
5.1.2. Monogenetik Değişimlerde Hipertansiyon Gelişimi...19
5.2. Sempatik Sinir Sistemi Aktivasyonu...22
5.3. Ekstraselüler Sıvı, Sodyum ve Potasyum Metabolizması...23
5.4. Renin-Anjiyotensin-Aldosteron Sistemi...25
5.4.1. Aldosteron...26
5.5. Obezite, İnsülin Direnci ve Hiperinsülinemi ...29
5.5.1. Yağ Dokusu ve Renin Angiotensin Sistemi...30
6. MİNERALOKORTİKOİD RESEPTÖRLER...31
6.1. Genin Yapısı...32
6.2. Hücresel Mekanizmalar...34
6.3. Moleküler İlişkiler...35
6.4. MR ekspresyonu ve düzenlenmesi...37
6.5. Promoter Bağlanması ve Transkripsiyonel Aktivasyon, Posttranslasyonel Modifikasyonlar...42
7. HİPERTANSİYON TEDAVİSİ...42
7.1. Nonfarmakolojik Tedavi (Yaşam şekli değişimi)...43
7.2. İlaç Tedavisi...45
8. YÖNTEM...48
8.1. Araştırma Tasarımı...48
8.2. Araştırma Gruplarının Örneklemi...48
8.3. Araştırmanın Değişkenleri...48
8.3.1. Bağımlı Değişkenler...48
8.3.2. Bağımsız Değişkenler...49
8.4. Ölçümler ve Veri Toplama Yöntemleri...49
8.4.2. Obezite Değerlendirmesi...49
8.4.3. Biyokimyasal Değerlendirilmesi...49
8.4.4. Hedef Organ Hasarı Değerlendirilmesi...50
8.4.5. Ölçüm Teknikleri...50
8.5. Moleküler analizler...50
8.5.1.DNA İzolasyon...50
8.5.2. DNA'nın Kontrolü...51
8.6. Veri Analizi ve İstatistik Değerlendirme...56
8.7. Araştırma ile İlgili Etik Durumlar...56
9. BULGULAR...57 10.TARTIŞMA...68 11.SONUÇ VE ÖNERİLER...76 12.ÖZET...77 13.ABSTRACT...79 14. KAYNAKLAR...81
TABLOLAR
Tablo 1. Çocukluk Dönemi Hipertansiyon Sınıflaması
Tablo 2. Üç Yaşın Altında Kan Basıncının Ölçülmesi Gereken Durumlar Tablo 3. Çocukluk Dönemi Yaş gruplarına Göre Hipertansiyon Nedenleri Tablo 4. Çocukluk Dönemi Uygun Manşon boyutları
Tablo 5. ABPM’nin Yararlanıldığı Durumlar Tablo 6. Non-dipper Hipertansiyon Nedenleri
Tablo 7. Ambulatuvar Kan Basıncı Sonuçlarına Göre Hipertansiyon Sınıflaması Tablo 8. Monogenik Mineralokortikoid Hipertansiyon Sendromları
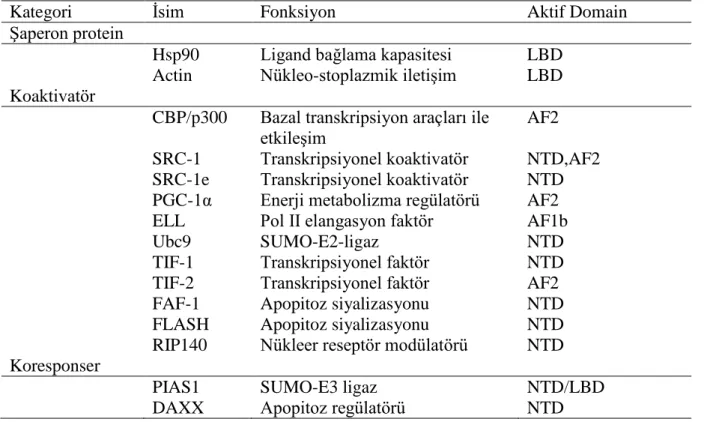
Tablo 9. Hiperinsülineminin Hipertansiyona Yol Açabileceği Mekanizmalar Tablo 10. Mineralokortikoid Reseptörlerinin Etkileştiği Proteinler
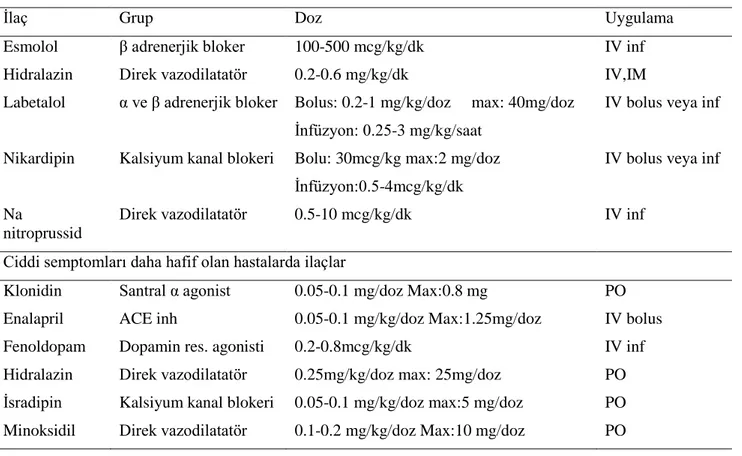
Tablo 11. Mineralokortikoid Reseptörlerinin Epitelyal Dokulardaki Biyolojik Etkileri Tablo 12. Mineralokortikoid Reseptörlerin Non-epitelyal Dokulardaki Biyolojik Etkileri Tablo 13. 1-17 Yaş Arası Ciddi HT’u Olan Hastalarda Antihipertansif İlaçlar
Tablo 14. 1-17 Yaş Arası HT’u Olan Hastalarda Ayaktan Kullanılan Antihipertansif İlaçlar Tablo 15. Hasta ve Kontrol Grubunun Demografik ve Antropometrik Özellikleri
Tablo 16. Hasta ve Kontrol Grubunun Soygeçmişinde HT Varlığının Gösterilmesi Tablo 17. Hasta ve Kontrol Grubunun Biyokimyasal Analizleri
Tablo 18. Hasta ve Kontrol Grubunun Klinik Değerlendirilmesi
Tablo 19. Tedavi Alan Hastaların Tedavi Öncesi ve Sonrası Sistolik ve Diastolik Kan Basıncı Değerleri ve Evrelemesi
Tablo 20. Antihipertansif Tedavide Kullanılan İlaçların Dağılımı
Tablo 21.Tedavide Kullanılan İlaçların Hipertansiyon Evrelerine Göre Dağılımı Tablo 22. Hastalarda Hedef Organ Tutulumunun Dağılımı
Tablo 23. Hasta ve Kontrol Grubunda ACE Gen Polimorfizm Sıklıkları Tablo 24. Hasta ve Kontrol Grubunda Renin Gen Polimorfizm Sıklıkları Tablo 25. Hasta ve Kontrol Grubunda Anjiotensin Gen Polimorfizm Sıklıkları Tablo 26. Hasta ve Kontrol Grubunda Aldosteron Gen Polimorfizm Sıklıkları Tablo 27. Hasta ve Kontrol Grubunda FABP2 Gen Polimorfizm Sıklıkları Tablo 28. Hasta ve Kontrol Grubunda ApoB100 Gen Polimorfizm Sıklıkları
Tablo 29. Hasta Grubunda Kan Basıncı 99 Persantiline Göre Gen Polimorfizm Dağılımları Tablo 30. Hasta Grubunda Kan Basıncı 95 Persantiline Göre Gen Polimorfizm Dağılımları Tablo 31. Hasta ve Kontrol Grubunun Genotipinin Hardy Weinberg Eşitliğine Uyumu Tablo 32. Hasta Kontrol Ayırımında Altı Gen İçin VKİ’nin Kontrol Edildiği LR Modelleri Tablo 33. Hasta Grubu Kan Basıncı Persantili 99 Üzeri ve Altı Grup Ayrımında Altı Gen İçin VKİ’nin Kontrol Edildiği LR Modelleri
ŞEKİLLER
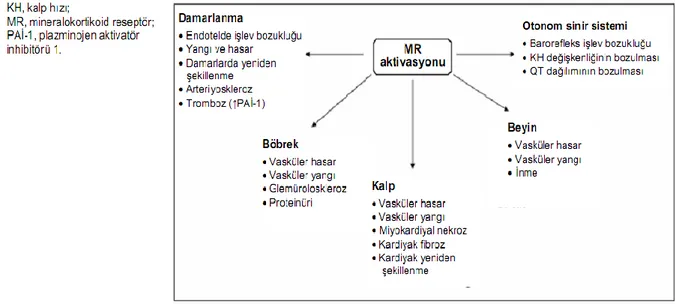
Şekil 1. Polarize Epitelyal Hücrelerde Aldosteronun Etki Mekanizmasının Şematizasyonu Şekil 2. Mineralokortikoid Reseptör Aktivasyonunun Kardiyovasküler Sistem Üzerindeki İstenmeyen Etkileri
Şekil 3. Mineralokortikoid Geninin Yapısının Şematik Gösterilmesi
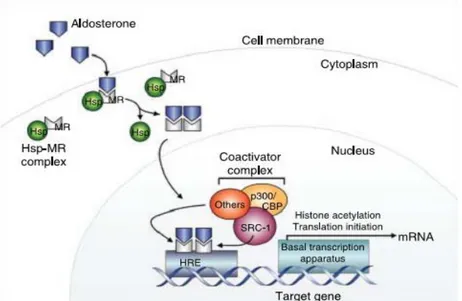
Şekil 4. Mineralokortikoid Reseptörün Sinyal İletimi ve Ligand Bağlanması Şekil 5. Polarize Renal Epitelyal Hücrelerde MR Aktivasyon Modeli
KISALTMALAR
ABPM: Ambulatuar Kan Basıncı Monitörizasyonu ACE : Anjiotensin Konverting Enzim
ACEİ : ACE İnhibitörleri
ACTH : Adrenokortikotropik Hormon ADH : Antidiüretik Hormon
AGT : Anjiotensin
ANP : Atriyal Natriüretik Peptid ARB : Anjiotensin Reseptör Blokeri BOS : Beyin Omurilik Sıvısı
CIMT : Karotis İntima Media Kalınlığı CHIF : Kanal Artırıcı Faktör
DBD : DNA-Binding Domain DM : Diabetes Mellitus
EGF : Endoteliyal Büyüme Faktörü ELL : Elongasyon Faktör
EnaC : Epitelyal Sodyum Kanalı GR : Glukokortikoid Reseptör
GRA : Glukokortikoid Aracılı Aldosteronizm HRE : Hormon Sorumlu Element
HSP : Isı Şok Proteinleri HT : Hipertansiyon
KAH : Konjenital Adrenal Hiperplazi KB : Kan Basıncı
KKY : Konjestif Kalp Yetmezliği KVH : Kardiyovasküler Hastalık
LVH : Sol Ventrikül Hipertrofisi
MONSTER: Medications, Obesity, Neonatal History, Symptoms-sign, Trend the family, Endocrin or Renal
MR : Mineralokortikoid Reseptör MSS : Merkezi Sinir Sistemi NCX1 : Na-Ca Exchanger Tip 1
NHBPEP :National High Blood Pressure Education Program NLS : Nükleer Lokalizasyon Sinyali
NO : Nitrik Oksit
NTD : N-Terminal Domain RAS : Renin – Anjiotensin sistem
SGK : Serum Glukokortikoid-Regulated Kinaz SNP : Tek Nükleotid Polimorfizmi
SRC : Steroid Reseptör Koaktivatör SSS : Sempatik Sinir Sistemi STIFNESS: Arteriyel Katılık TXA2 : Tromboksan
GİRİŞ ve AMAÇ
Pediatrik hipertansiyon (HT) özellikle son yıllarda önem kazanmış ve ciddi bir sağlık sorunu haline gelmiştir. Çocukluk çağı HT’sinin önem kazanmasının en önemli nedeni erişkin döneminde saptanan hipertansiyonun çocuklukta başlaması ve erişkin dönemindeki kardiyovasküler sistem, kronik böbrek yetmezliği ve serebrovasküler hastalıklar için önemli bir risk faktörü olarak morbitide ve morbititeyi arttırmasıdır.
Hipertansiyon, kan basıncını belirleyen ve birbiriyle etkileşen birçok faktör olması nedeniyle tek bir etiyoloji veya patofizyolojik mekanizmanın sorumlu olmadığı multifaktöryel bir hastalıktır. Genetik, renin-anjiyotensin sistemi (RAS), sempatik sinir sistemi, renal sodyum retansiyonu, kalp debisini arttıran durumlar, vasküler hipertrofi, endotel kökenli faktörler, vazokonstriktör maddelerin aşırı üretimi, vazodilatör maddelerin yetersiz üretimi, obezite ve insülin direnci, diyetin sodyumdan zengin potasyumdan fakir olması, kişinin yaşam tarzı bu çoklu faktörler arasındadır.
Çocuk ve ergenlerde yapılan çalışmalarda son yıllarda prevalanstaki artış obezitede artma, beslenme alışkanlıklarındaki olumsuz değişiklikler sonucu yüksek kalori, yağ ve tuz içeren besinlerin tüketilmesi, fiziksel aktivitede azalma, uyku bozuklukları ve artan stres faktörüne bağlanmaktadır. Primer HT, sıklıkla ailede HT öyküsü ile ilişkilidir. Ailede HT öyküsü olan çocuklar erişkin dönemde de normalin üstünde kan basıncına sahiptir.
Çocukluk dönemi HT’sinin %50’si kalıtımsaldır. Genetik temeli poligeniktir ve pek çok patofizyolojik mekanizma ile ilişkilidir. Aynı zamanda tek gen defektleri ile HT ilişkisi çocukluk döneminde de tanımlanmıştır.
Kan basıncı ile ilişkili olduğu düşünülen, doğrudan veya dolaylı olarak renal tübüler transportu düzenleyen hormon veya hormon üretiminde yer alan enzim, reseptör, sinyal moleküllerini kodlayan birçok değişken saptanmıştır.
Renin böbrekte jukstaglomerüler hücrelerden salınır ve karaciğerden plazmaya verilen anjiyotensinojenin anjiyotensin-I’e çevirilmesini katalize eder. Renin salınımı kan basıncının düzenlenmesinde önemlidir. Mineralokortikoidler, Angiotensin-II (AGT-II), tuz alımı, beta blokerler, Antidiüretik hormon (ADH), tromboksan A2 (TxA2) ve endotelyal büyüme faktörü (EGF) renin salınımını baskılar.
Angiotensin -II’nin AT1 ve AT2 olmak üzere 2 tip reseptörü vardır. Etkilerinin çoğu AT1 üzerindendir. Ang-II’nin AT1 reseptörüne bağlanmasıyla periferik damarlarda vazokonstriksiyon, intimal hiperplazi ve angiogenezis, myokardda kontraktilite, kollojen sentezi, hipertrofi ve fibrozis, adrenal bezden aldosteron sentezi, böbrekten sodyum geri alımı, beyin ve hipofizde merkezi sinir sistemi (MSS) aktivitesi ve vasopressin salınımı yapar.
Aldesteronun kardiyovasküler ve MSS üzerine önemli etkileri vardır. Aldesteron adipozit diferansiyasyonunu ve termogenezisi düzenler.
Obeziteye bağlı HT gelişiminde rol oynayan vazoaktif maddeler yağ dokusundan salınır. Obezitede, yağ dokusu kökenli RAS’ın, HT gelişiminde rol aldığı gösterilmiştir.
Obezite ve HT arasındaki ilişkiyi gösteren çalışmalarda vücut kitle indeksi (VKİ) değeri 27 kg/m2 ’nin üzerinde olan aşırı kilolu bireylerin HT risklerinin, üç kat daha yüksek olduğu gösterilmiştir. Obezitede lipid ve glukoz metabolizma bozukluklarında, yüksek dansiteli lipoprotein (HDL) ve kolesterol azalır, trigliseridden zengin küçük yoğun LDL partiküller ve apopiloprotein (apo) B ve E artar. Apolipoprotein B-100’ün artması, lipoproteinlerin glikozile olup reseptörlerince tanınmasını sağlar. Bu döngü artmış dislipidemi yatkınlığı nedeni ile HT’ye yol açabilir. Yağ dokusu ve makrofajlarda sentez edilen; yağ asidi bağlayan protein-2 ( FABP-2 ) metabolik sendrom gelişme sürecine katkıda bulunur.
Bu çalışmada; multifaktöriyel kalıtım gösteren primer HT etiyolojisinde renin, aldesteron sentetaz, angiyotensin genleri, lipid metabolizma gen polimorfizmlerininin etkisini saptamak amaçlandı. Bu çalışma sonuçları ile HT etiyolojisinde varolan olası polimorfizmler olgu-kontrol gruplarında araştırılarak karşılaştırıldı. Alt amaç olarak, bu çalışmada araştırılan genetik değişimler, obezite kontrol edilerek incelendi. Çocuklarda primer HT’nin tanı anındaki kan basıncı (KB) persantillerine göre polimorfizm sıklıkları (genotip dağılımları) değerlendirildi.
GENEL BİLGİLER
1. TANIMLAMA
Arteriyal kan basıncı= kalp atım hacmi x periferik damar direncinden oluşur. Bu bileşenlerin büyüme-gelişme ile farklılaşması, kan basıncı değerlerinin doğumdan ergenliğin sonuna kadar artışına yol açar. Çocuklarda, erişkinlerden farklı olarak tek bir normal veya patolojik kan basıncı değeri yoktur. Çocuklarda KB değerlerinin standardize edilmesi amacıyla 1977, 1987,1996 yıllarında çalışma grupları oluşturulmuş ve en son 2004 yılında NHBPEP (National High Blood Pressure Education Program: The Fourth report on the diagnosis) çocuk ve ergenlerde yüksek KB çalışma grubunun verileri dikkate alınarak çocukluk dönemi KB değerleri ve HT tanımlaması yapılmıştır (1).
Tablo 1. Çocukluk Dönemi Hipertansiyon Sınıflaması
Sistolik veya Diyastolik KB Persantili
Normal <90p
Pre HT 90-95p veya >120/80 mmHg
Evre 1 HT 95-99 p + 5 mmHg
Evre 2 HT >99p + 5mmHg
Çocuk ve ergenlerde KB’nin tanımlamalarında ülkeler çoğunlukla Amerika Birleşik Devletlerinde ulusal sağlık araştırmalarından elde edilen kan basıncı ölçümlerinin kullanıldığı ve 4. kez revize edilmiş olan ‘National High Blood Pressure Education Program: The Fourth report on the diagnosis’ raporundaki her cinsiyet için yaş ve boya göre standardize edilmiş kan basıncı eğrilerini kullanmaktadır. Yapılan farklı çalışmalarda kan basıncı üzerine etnisisite, ırk, büyüme gelişme paternlerinin etkisi satanması ile bazı ülkeler kendi KB eğrilerini oluşturmuştur. Son yıllarda Avrupada ulusal düzeylerde yapılan çalışmalarda KB eğrileri oluşturulurken, ağırlığın etkisi de kontrol edilmiştir. Ağırlık, KB eğrilerini saptamada önemli bir değişken olarak saptandığında, VKİ 90 persantil, diğer çalışmada ise 85 persantil üzerindeki çocuklar örnek grubundan çıkarılarak KB eğri tahminlemeleri gerçekleştirilmiştir(2,3).
Ülkemizde Tümer ve arkadaşlarının yapmış olduğu KB eğrilerini belirleme çalışması 1998 yılında gerçekleştirilmiş, bu çalışmanın örneği yalnızca Ankara bölgesindeki belirli okullardan alınmıştır. Bu çalışmada cinsiyete göre yaş ve boy değişkenleri ile KB eğrileri belirlenmiştir. Sıklıkla kullanılan 4.raporun ve ülkemizde gerçekleştirilmiş çalışmadan tahminlenen kan basıncı eğrileri ve tabloları aşağıdaki adresten ulaşılabilir:
- https://www.nhlbi.nih.gov/files/docs/resources/heart/hbp_ped.pdf
Bu kan basıncı değerleri göz önüne alınarak HT hastasının tanısını koymada aşağıdaki snıflamadan yararlanılır:
Normal KB: Sistolik ve diyastolik KB’nin 90 p’nin altında olmasıdır.
Prehipertansiyon: Sistolik veya diyastolik KB’nin yada her ikisinin 90 p’nin üstünde ama 95 p’den küçük olması olarak tanımlanmıştır. KB en az iki kez aynı muayenede değerlendirilmeli ve bulunan sonuç en az 3 kere doğrulanmalıdır.
Evre I Hipertansiyon: KB ölçümü 95-99 p arasındaki değerden 5 mmHg daha fazla olmasıdır.
Evre II Hipertansiyon: KB 99 p’den 5 mmHg daha fazla olması olarak tanımlanmıştır. Bu evreleme sistemi, klinisyenin HT hastasını hızlı bir şekilde değerlendirmesine ve tedavi yaklaşımına olanak sağlamıştır (4,5)
Hipertansif Acil: Hedef organ hasarı gelişmemiş HT’yi tanımlamaktadır(5). Acil Hipertansif: Hedef organ hasarı gelişmiş ciddi HT’yi tanımlamaktadır(5).
Beyaz Önlük Hipertansiyonu: Hastane dışında KB normal iken sağlık personeli tarafından yapılan ölçümlerde hastanın yaşadığı geçici stres ve anksiyete nedeniye KB >95p saptanmasıdır(6).
Beyaz önlük HT’sini saptamak ve bu tanıyı desteklemek için medikal ortam dışında KB ölçümü için ambulatuvar kan basıncı monitorizasyonu (ABPM)’ndan yararlanılır(7).
Görülme sıklığının %35-45 oranında bildirilmektedir. Benign gözükmekle birlikte prehipertansif bir durum olduğu ve zamanla persistan HT’ye dönüşebildiği
Maskeli Hipertansiyon: Klinik ölçümlerde normotansif iken ABPM ölçümlerinde ve hastane dışı ölçümlerde KB’nin yüksek saptanmasıdır. Maskeli HT, çocukluk çağında %7-11 oranındadır. Bu hastaların %50’sinde izlemde kalıcı HT geliştiği ve sol ventrikül kitle indeksinde artış olduğu bildirilmektedir (6).
Maskeli HT’nin sol ventrikül hipertrofisi ve kötü kardiyak prognoz ile ilişkili olduğu belirtilmektedir. Maskeli HT’de ailede HT öyküsü sıklıkla pozitiftir, obez hastalarda 2.5 kat daha fazla görülür ve ABPM ölçümlerinde kardiyak nabzın daha yüksek olduğu saptanmıştır. Bu özelliklerin birinin veya hepsinin birlikte varolması, HT ve kardiyovasküler hastalık (KVH) riskini arttırır(8).
Sağlıklı çocuk izleminde ve çocuk taramalarında, 3 yaşından sonra her çocuğun KB değerlendirmesi yapılmalıdır. Tablo 2’de belirtilen durumlarda ise 3 yaş altında fizik muayenenin bir parçası olarak KB ölçümünün yapılması önerilmektedir(4,9).
Tablo 2. Üç Yaşın Altında Kan Basıncının Ölçülmesi Gereken Durumlar
Prematüre, düşük doğum ağırlığı diğer yoğun bakım gerektiren yenidoğan komplikasyonları Konjenital kalp hastalıkları
İdrar yolu enfeksiyonu, proteinüri
Bilinen böbrek hastalığı veya ürolojik malformasyon Ailede konjenital böbrek hastalığı
Solid organ transplantasyonu
Kan basıncını yükselttiği bilinen ilaç kullanımı İntrakraniyal basınç artışı
Sistemik hastalık varlığı
2. HİPERTANSİYON ETİYOLOJİSİ
2.1. Primer Hipertansiyon
Nedeni saptanamayan HT anlamındadır. Son zamanlarda esansiyel veya idiyopatik HT deyimleri yerine, böbrek işlevleri için gereken KB düzeyini tanımladığı için primer HT teriminin kullanılması önerilmektedir (10,11).
Erişkin yaş grubunda en sık görülen HT tipi primer HT iken, çocukluk yaş grubunda ise 6-10 yaşından itibaren primer HT tanımı başlamakta, ergen grubunda ise erişkinde olduğu gibi primer HT ilk sırayı almaktadır(12,13,14). Bu oran süt çocukluğu döneminde <%1 iken, okul çağı döneminde %15-30, ergenlerde %85-95 oranındadır. Sekonder HT ise süt çocukluğu döneminde %99 iken, okul çağında %70-85, ergenlerde ise %5-15 oranında bildirilmektedir(14,15,16,17).
Primer HT sıklıkla ailede HT öyküsü ile ilişkilidir. Bu olgular çocukluk döneminde daha yüksek KB persantillerine, erişkin dönemde ise normalin üstünde KB’ye sahip olurlar(7).
Çocukluk dönemi HT’sinin %50’si kalıtımsaldır. Primer HT’li erişkin hastaların %49’unda çocukluğunda da primer HT’li olduğu bildirilmiştir. Sekonder HT’li hastaların %46’sının çocukluk çağında da sekonder HT’li oldukları bildirilmiştir. Başka bir çalışmada primer HT’li ergenlerin %86’sında aile öyküsü olduğu belirtilmektedir(4,9). Primer HT genetik temeli poligeniktir ve pek çok patofizyolojik mekanizma ile ilişkilidir. Ayrıca tek gen defektleri ile ilişkili primer HT, çocukluk döneminde de görülmektedir(4).
Irk ve düşük sosyokültürel düzey ile primer HT arasında ilişki vardır. Afrika kökenli Amerikalı ergenler ve erişkinlerde HT sıklığı beyaz ırka göre iki kat fazladır (4). Bu farklılığın beslenme ve yaşam biçimi değişiminden mi, yoksa etnisite ve düşük sosyoekonomik durum nedeni ile mi geliştiği halen araştırma konusudur.
Obezite primer HT’ye eşlik eden bir faktördür ve ergen HT hastalarının yaklaşık yarısı obezdir. Çok iyi anlaşılamamış olmasına rağmen obezite, yüksek sodyum alımı ve insülin direnci yoluyla KB artışına katkıda bulunmaktadır. Diyet alışkanlıkları ve yaşam tarzı arasında ilişki vardır. Sedanter yaşam, artmış vücut kitle indeksi (VKİ) ve karbonhidrat alımı, ile yüksek sistolik kan basıncı(KB) arasında ilişki bulunmuştur. Gençlerde obezitenin yaygınlaşması ile primer HT sıklığında artış ortaya çıkmıştır(4,15,16).
Metabolik sendrom olarak da bilinen HT, şişmanlık, hiperlipidemi ve diyabetes mellitus birlikteliği uzun dönemde kardiyovasküler hastalık görülme sıklığını belirgin olarak artırmaktadır(7).
Çocukluk çağında primer HT’nin patogenezi tam olarak açık değildir. Ancak genetik ve çevresel faktörler arasındaki etkileşimin sonucu geliştiği düşünülmektedir(6,10,17).
2.2. Sekonder Hipertansiyon
Sekonder HT altta yatan başka bir hastalığa bağlı olarak gelişir. Bu nedenle bir çocukta HT tespit edilmiş ise aksi kanıtlanana kadar sekonder HT olarak kabul edilip araştırılmalıdır(4,10).
Çocukluk döneminde erişkinden farklı olarak yaş küçüldükçe ve KB derecesi arttıkça sekonder nedenler daha sık görülür. Çocuk ve ergenlerde değerlendirmede esas amaç sekonder nedenlerin tanımlanmasıdır. Ek olarak eşlik eden risk faktörleri ve hedef organ hasarı araştırılmalıdır.
Spesifik etiyolojilerin sıklığı yaş gruplarına göre değişiklik gösterir(Tablo 3). Renal parankim hastalıkları (polikistik böbrek, multikistik displastik böbrek hastalığı, hidronefroz, kronik piyelonefrit, kronik böbrek yetmezliği) sekonder HT’nin %75’ini oluşturur. Bunu renovasküler anormallikler (renal arter stenozu veya trombozu ve renal ven trombozu) izler (4,18). Tedavi amaçlı steroid, dekonjestanlar gibi ilaçlar ve kafein gibi maddeler kendileri HT’ye yol açtığı gibi sekonder nedeni artırabilir. Diğer faktörler daha az sıklıktadır. Wilms tümörü, nöroblastom ve nadiren feokromasitoma HT ile ilişkili bulunmuştur. Williams sendromu renal arter stenozu ile ilişkili iken, Turner sendromunda ise aort koarktasyonu nedeni ile HT’ye yol açmaktadır. Endokrinopatilerden hipertiroidizm, Cushing sendromu, hiperaldosteronizm ve diyabet sekonder HT ile ilişkili bulunmuştur(4).
Tablo 3. Çocukluk Dönemi Yaş gruplarına Göre Hipertansiyon Nedenleri
YENİDOĞAN 0-1 YIL 1-6 YAŞ 7-12 YAŞ 13-18 YAŞ
Renal arter trombozu Renal arter stenozu Renal ven trombozu Konj. renal anomali Aort koarktasyonu Bronkopulmoner displazi
Patent duktus arteriozus Kafa içi kanama
Aort koarktasyonu Renovasküler hastalık Renal parankimal hastalık Renal parankimal hastalık Renovasküler hastalık Aort koarktasyonu Endokrin nedenler Primer(birincil) Renal parankimal hastalık Renovasküler hastalık Primer(birincil) Aort koarktasyonu Endokrin nedenler İatrojenik Primer(birincil) İatrojenik Renal parankimal hastalık Renovasküler hastalık Aort koarktasyonu Endokrin nedenler
3. HİPERTANSİYON EPİDEMİYOLOJİSİ
Pediatrik HT, özellikle son yıllarda önem kazanmış ve ciddi bir sağlık sorunu haline gelmiştir. Çocukluk çağı HT’sinin önem kazanmasının en önemli nedeni erişkin döneminde saptanan HT’nin, çocukluk çağında başlaması ve erişkin dönemindeki kardiyovasküler sistem, kronik böbrek yetmezliği ve serebrovasküler hastalıklar için önemli bir risk faktörü olarak, morbitide ve morbititeyi arttırmasıdır(19,20,21,22).
Tüm dünyada 1 milyardan fazla insanın hipertansif olduğu, yılda 7 milyondan fazla ölümün hipertansiyona bağlı geliştiği tahmin edilmektedir. Hipertansif hastaların %30’u hastalıklarından habersiz, %40’ı tedavisizdir(23).
Çocukluk dönemi HT prevalansı önceki çalışmalarda %1-3 sıklıkta, sonraları bu sıklık % 4,5’a yükselmiştir. Yakın zamanlarda yapılan çalışmalarda çocuklarda %11, ergenlerde ise % 23’lere kadar arttığı bulunmuştur. Obez çocuklarda ise prevalansın %11-30’lara kadar çıktığı saptanmıştır(8,17,24,25)
Çocukluk çağı ve ergenlerde yapılan çalışmalarda son yıllardaki artış obezitede artma, beslenme alışkanlıklarındaki olumsuz değişiklikler sonucu yüksek kalori, yağ ve tuz içeren besinlerin tüketilmesi, fiziksel aktivitede azalma, uyku bozuklukları ve artan stres faktörü ile ilişkilendirilmektedir(6,10,17).
4. HİPERTANSİYON HASTASININ DEĞERLENDİRİLMESİ
4.1. Kan Basıncı Ölçüm Yöntemleri
Sağlıklı bir ölçüm için 5-10 dakikalık dinlenme sonrası ölçüm yapılmalıdır. Süt çocuğu yatar pozisyonda, çocuk ve ergenlerde ise oturur veya yatar pozisyon kullanılmalıdır. Aort koarktasyonu varlığında KB daha düşük ölçüleceğinden sağ kol tercih edilmelidir. Ölçüm sırasında kol, kalp seviyesinde tutulmalıdır (4,6,9,17).
Ölçüm için çocuğun koluna uygun manşon seçilmeli, manşon genişliği kol çevresinin %40, uzunluğu ise üst kolun %80-100’ünü kaplamalıdır(5,26). Bu boyutlardan daha küçük manşonlar normalden yüksek, daha büyük maşonlar ise düşük sonuçlar alınmasına yol açar. Çocukluk döneminde kullanılacak manşon boyutları Tablo 4’te gösterilmiştir.
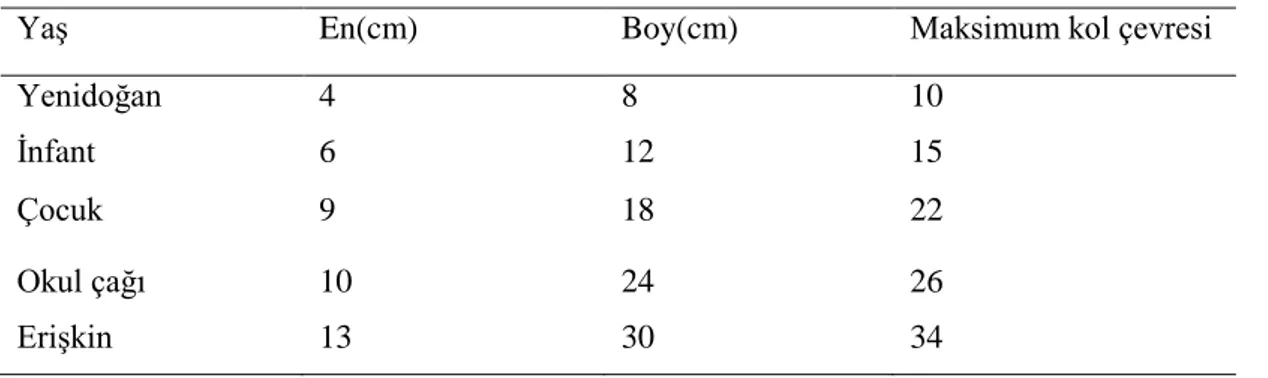
Tablo 4. Çocukluk Dönemi Uygun Manşon boyutları
Yaş En(cm) Boy(cm) Maksimum kol çevresi
Yenidoğan 4 8 10
İnfant 6 12 15
Çocuk 9 18 22
Okul çağı 10 24 26
Erişkin 13 30 34
KB ölçümünde en güvenilir yöntem intraarteriyel kan basıncı ölçümüdür. Ancak invaziv bir girişim gerektirdiğinden yoğun bakım koşullarında kullanılabilmektedir. Bu nedenle indirekt ölçüm yöntemleri geliştirilmiştir. Bunlar palpasyon, oskültasyon, doppler ve ossilometrik yöntemlerdir (4,6,17).
4.1.1. Palpasyon Yöntemi: Eski bir yöntemdir. Ölçüm için el yukarıya kaldırılıp avuç içi beyazlaşana kadar kol manşet ile sıkılır. Daha sonra saniyede 2-3 mmHg azaltılırken, avuç içinin ilk pembeleştiği basınç sistolik KB olarak değerlendirilir. Bu yöntem ile sadece sistolik KB ölçülebilir(12).
4.1.2. Oskültasyon Yöntemi: En az 5-10 dakika dinlendikten sonra sandalyede oturur pozisyonda, sağ koldan antekubital fossa kalp seviyesinde tutularak ölçülmelidir. Manşon şişirilirken radial nabız palpe edilmektedir. Radial nabız kaybolduktan sonra 20 mmHg daha şişirilerek 2-3 mm/sn hızla basınç azaltılırken steteskop ile brakial nabız dinlenerek ölçülür(5,12). Bu yöntemde Korotkoff denilen KB ölçümü sırasında kanın damar çeperine yaptığı basıncın sesi duyulur. Bu seslerin fazlara göre ayrımı şu şekilde yapılmıştır:
-Faz 1: Ölçüm yapıldığında manşonun basıncı azaltılmaya başladıktan sonra sesin ilk duyulduğu anda okunan değer, sistolik basınçtır. Radyal arterden palpe edilebilen nabız ile eş zamanlı olarak başlayan seslerdir.
-Faz 2: Yumuşak ve uzun seslerdir. -Faz 3: Daha çıtırtılı ve yüksek seslerdir.
-Faz 4: Boğuk ve yumuşak seslerdir. Diyastolik basınç çok düşük ise seslerin hafiflemeye başladığı düzey olup diyastolik basınç olarak kaydedilir.
-Faz 5: Seslerin tamamen kaybolduğu fazdır. Sesin işitilmez olduğu anda okunan değer ise (Korotkoff faz 5) diyastolik kan basıncı olarak kabul edilir.
Diastolik KB değeri için süt çocuğu ve küçük çocuklarda 4.sesin büyük çocuklarda ve adolesanlarda 5. sesin kullanımı önerilmektedir(5).
4.1.3. Osilometrik Yöntem: Bu teknik özellikle ölçüm sırasında uyum sorunu yaşanan küçük çocuklarda ve yenidoğanlarda kullanılmaktadır. Ossilometrik ölçüm tekniklerinde sistolik KB ve ortalama arter basıncı, manşon şişirildikten sonra arterial pulsasyonların yansıması ile belirlenir. Bu cihazlarla ortalama arterial basınç saptanır(12). Osilometrik yöntemle 90p üstünde KB değeri saptanırsa oskülatuar yöntemle yeniden değerlendirme yapılmalıdır(4).
4.1.d.Doppler Yöntemi: Bu teknik ile ölçülen KB’deki sistolik KB, diyastolik KB’ye oranla çok daha doğru olarak saptanır. Gerek ossilometrik gerekse doppler tekniği ile elde edilen değerlerin karşılaştırılacağı yaşa, cinsiyet ve antropometrik boyutlara göre düzenlenmiş standart tablolar henüz tam olarak geliştirilememiştir. Bu durum söz konusu aletlerin kullanım ve güvenilirliğini sınırlamaktadır(12).
4.1.e. Ambulatuvar Kan Basıncı Monitarizasyonu(ABPM): Kan basıncı, gece gündüz sirkadiyen bir ritm şeklindedir. Sabah erken saatlerde KB en düşük, akşam geç saatlerde en yüksektir. Bunda endojen olaylar, genetik yapılar, uyku ve uyanıklılıktan etkilenir. Kan basıncında gün içindede sık değişim olduğu için tek bir ölçüm yerine gün içindeki değişimi görmek daha yararlıdır. Kişinin KB’sinin gün içindeki aktivite, stres ve istirahat gibi durumlardaki değişikliklerin bilinmesi hastaya verilecek ilaç tedavisinin seçimi ve etkinliğini görmek açısından da avantaj sağlar(9). Tablo 5’te ABPM’nin yararlanıldığı durumlar gösterilmiştir.
Tablo 5. ABPM’nin Yararlanıldığı Durumlar Beyaz gömlek HT
İlaç direnci
Hipertansif tedavi sırasında hipotansiyon bulguları olanlar Otonomik disfonksiyon
Gün içinde farklı değerler gösteren KB ölçümleri Sınırda hipertansiyon olan olguların tanımlanması Hedef organ hasarının değerlendirilmesi
Hipertansif tedavi etkinliğinin izlemi
Sekonder hipertansiyonda mevcut non-dipper özelliğin ortaya çıkarılması
Uyku sırasında fiziksel aktivite, emosyonel faktörler, sempatik sinir sistemi aktivitesi, hormonal değişiklikler nedeniyle uykuda kan basıncında %10-20 düzeyinde düşme (dipper) görülür. Bu düşmenin görülmediği (nondipper) hastalar hedef organ hasarı açısından risklidir. Primer HT’de “dipper” özelliği, sekonder HT’de ise “non-dipper” özelliği belirgindir. Bu durum, primer HT’ye sekonderden ayırt etme konusunda yararlıdır. Buna karşın çocukların %30’unda KB’nin fizyolojik olarak “non-dipper” özelliğinde olduğu da bildirilmiştir. Gece uyurken normal fizyolojik koşullarda beklenen KB düşüşünün olmadığı başlıca patolojiler Tablo 6’da özetlenmiştir(4,9). ABPM’de ossilometrik yöntem ile ölçüm yapılmaktadır. Hastaya uygun manşon boyutu ile dominant olmayan kola uygulanmaktadır. Uyanıkken 20-30, uyurken de 30-60 dakikada bir ölçüm yapılmalı, cihaz çocuğun günlük aktivitesini kısıtlamamalıdır(9).
Tablo 6. Non-dipper Hipertansiyon Nedenleri Otonomik nöropati
Diabetik nefropati
Diyaliz, Kronik böbrek hastalığı Renal transplantasyon
Konjestif kalp yetmezliği Uyku-apne sendromu Cushing sendromu Feokromasitoma Mineralokortikoid artışı Malign hipertansiyon Ortostatik hipotansiyon Gebelik hipertansiyonu Siyah ırk
ABPM’de elde edilen değerlerin yorumlanması için KB yükünden yararlanılmaktadır. KB yükü: Yaş, cins ve boy persantiline göre (konvansiyonel ölçüm için tanımlanan) 90 persantile uyan kan basıncından yüksek olan ölçüm sayısının, toplam ölçüm sayısına oranı (%) olarak tanımlanmıştır. Kan basıncı yükü %25 ve/veya üzerinde olursa HT, %40 ve/veya üzerinde ise de hedef organ zedelenmesinin meydana geldiğinden söz edilebilir(25). ABPM verilerin değerlendirilmesinde çocukluk dönemine uygun düzenlenmiş tabloların uygun olmadığı da kabul edilmektedir. Bu tablolar iki yaşından itibaren kullanılabilir(4,9,17). Özellikle Tablo 7’de ABPM’ye göre HT klasifikasyonu gösterilmektedir(4).
Tablo 7. Ambulatuvar Kan Basıncı Sonuçlarına Göre Hipertansiyon Sınıflaması
Sınıflama Klinik Kan Basıncı Ortalama Sistolik KB Sistolik KB Yükü
Normal <95p <95P <25 Beyaz önlük HT >95P <95p <25 Maskeli HT <95p >95P >25 Prehipertansiyon >95P <95p 25-50 Hipertansiyon >95P >95P 25-50 Ciddi Hipertansiyon >95P >95P >50
4.2. Klinik
Çocuklarda HT sıklıkla bir yakınma veya bulguya neden olmaz. Çoğu olgu klinik olarak sessizdir. Bu nedenle 3 yaşından büyük çocuklarda her fizik muayenede KB’nin ölçülmesi gereklidir(18). HT’li hastanın değerlendirilmesi anamnez ve fizik muayene ile başlar. Değerlendirmenin kapsamı çocuğun yaşı, HT’nin ciddiyeti, hedef organ hasarının boyutu ve uzun dönem risk etmenlerinin varlığı ile ilişkilidir(4,7,26). Sekonder nedenler ile ilişkili semptomlar, KVH risk faktörleri ve genetik geçişler hakkında ayrıntılı aile öyküsü alınmalıdır. Geçmişte ve şu anda kullandığı ilaçlar, ek diyet destekleri sorgulanmalıdır. Yenidoğan döneminde klinik bulgular non spesifiktir. İrritabilite, letarji, düşük kilo alımı, solunum sıkıntısı, konjestif kalp yetmezliği (KKY) ve nöbet görülebilir. Ergenlerde halsizlik, baş ağrısı ve görme bozukluğu saptanabilir. Yaşam şekli ve beslenme alışkanlıkları (Na, K ve Ca alımı), sigara içiciliği, pasif içicilik ve uyku bozuklukları sorgulanmalıdır(26).
Hipertansif çocukların değerlendirilmesinde ilaçlar (amfetamin, kafein, NSAİ, siklosporin), obezite, neonatal öykü (neonatal asfiksi, umblikal arter kateterizasyonu, bronkopulmoner displazi), semptom ve bulgular (kilo kaybı, ateş, solukluk, baş ağrısı, hirsutizm, üfürüm, nabız farklılığı), aile öyküsü (primer HT, hiperlipidemi, kardiyovasküler hastalık, DM) ve renal veya endokrin (abdominal üfürüm, polikistik böbrek hastalığı, glomerülonefrit, anbigus genitale, ay dede yüz) nedenlerin ingilizce baş harflerinden oluşan MONSTER(Medications, Obesity, Neonatal History, Symptoms-sign, Trend the family, Endocrin or Renal) sınıflaması bu konuda temel yaklaşıma yardımcı olmaktadır(26).
Hipertansif acil, yaşamı tehdit edici komplikasyonlara (ensefalopati: konvülzyon, inme ve fokal defisitler; kalp yetersizliği, miyokard enfarktüsü, akciğer ödemi, dissekan aort anevrizması, akut böbrek yetersizliği) yol açan ciddi HT olarak tanımlanır(7).
Çok spesifik testler, evre I veya evre II HT’de, tedaviye rağmen ısrarlı HT’si olan çocuklarda, yenidoğan ve süt çocukluğu döneminde önerilir. Obezite varlığında çok fazla spesifik test yapmaya gerek olmadığı belirtilmektedir. Bulgusuz evre I hipertansif çocukların 1 ay, evre II hastaların ise 1 hafta içinde değerlendirmelerinin tamamlanması ve tedavilerinin düzenlenmesi gereklidir(4,7).
4.3. Hedef Organ Hasarının Belirlenmesi
Tedavi almayan ağır hipertansif olguların %75’inde, en az bir hedef organ hasarı saptanmaktadır. Hipertansiyonun tedavi kararında ve hastalığın prognozunda önemli bir faktör olan hedef organ hasarının non-invaziv ve sensitif göstergesi gereklidir. Özellikle kardiyovasküler sistemde gelişen hasar, hastalığın mortalitesini arttırmaktadır. Bu nedenle özellikle kardiyovasküler sistem taraması hastalar için önem taşır(7,27,28)
Arteriyel katılık (stiffnes): Damar duvarındaki elastik doku kaybına bağlı olarak gelişen kan akımındaki sürekliliğin azalmasıdır. Arter duvarında oluşan hasar (ateroskleroz ve veya arterioskleroz), arteriyel duvardaki elastin kollajen oranını azalmasına ve arteriyal katılığın artmasına neden olur. Arteriyel katılık, hipertansif hastalarda kardiyovasküler komplikasyonların ve HT’ye bağlı hedef organ hasarının güçlü bir belirtecidir(29). Artmış ateroskleroz primer sol ventrikül hipertrofisinin (LVH) de bir göstergesidir (5,29).
Karotis intima-media kalınlığı (cIMT): HT, arteriyal duvarda patolojik yeniden yapılanma (remodeling) oluşturarak hem intima hem de media tabakasında orantısız kalınlaşmaya yol açar. Erken aterosklerosisin ilk bulgusudur. Karotis intima-media kalınlığı arteriyal ve kardiyovasküler hastalık değerlendirmesi için erken göstergedir. Hipertansif çocuklarda ise cIMT sağlıklı kontrollerden yüksek bulunmuştur. Sağlıklı çocuklarda normal cIMT değeri yaş gruplarına göre değişkenlik göstermekte olup ortalama 0.39 ±0.04 olarak belirlenmiştir(30).
Sol Ventrikül Hipertrofisi: Damar direncinde ortaya çıkan artış sol ventrikül iş yükünü önemli ölçüde arttırarak, kardiyak hipertrofiye yol açar. Artan sol ventrikül kitlesi sonucu, LV kavitesinde azalma gerçekleşir. Israrlı HT’li çocuk hastaların büyük bir çoğunluğunda LVH olduğu bildirilmiştir(4). Ağır hipertansiflerde LVH’nin riskinde artış yanı sıra maskelenmiş HT’de de artış bildirilmiştir(5). Yapılan çalışmalarda beyaz önlük HT’si olan çocuklarda normotansif kontrollere göre LV kitle indeksinde artış saptanmıştır. Ek olarak LVH, artmış cIMT ile korelasyon göstermektedir. NHBPEH çalışmasında HT’li hastalara tedavi kararı verilmeden önce LVH değerlendirlmesi önerilmektedir. Böylece LVH varlığı hem tedavi hemde izlemi gerektiren hasar göstergesidir(3,4,30,31).
Göz dibi incelemesi: Altı-sekiz yaşındaki çocuklarda sistolik kan basıncının 10 mmHg artması ile her yıl retinal arteriollerin 1.43-2.08 μm daraldığı bildirilmiştir. Hipertansif
Mikroalbüminüri, diyabetli hastaların yanı sıra primer HT’li hastalarda da erken kardiyak ve böbrek hasarının belirlenmesinde oldukça duyarlı bulunmuştur(3,7).
5. HİPERTANSİYON PATOGENEZİ
Kan basıncı kalp debisi ve periferik vasküler direnç ile doğru orantılıdır. Hipertansiyon oluşumunda kalp debisi ve periferik vasküler direnci etkileyen pek çok faktör rol almaktadır. Kan basıncını belirleyen ve birbiriyle etkileşen birçok faktör olması nedeniyle HT, sorumlu tek bir etiyoloji veya patofizyolojik mekanizmanın olmadığı multifaktöryel bir hastalıktır. Bu çoklu faktörler arasında, genetik faktörler, renal sodyum retansiyonu, renin-anjiyotensin sistemi, sempatik sinir sistemi, kalp debisini arttıran faktörler, vasküler hipertrofi, endotel kökenli faktörler, vazokonstriktör maddelerin aşırı üretimi, vazodilatör maddelerin yetersiz üretimi, obezite ve insülin direnci, diyetin sodyumdan zengin potasyumdan fakir olması, kişinin yaşam tarzı gibi nedenler sayılabilir(32).
5.1. Genetik Yatkınlık
Hipertansif hastalarda genetik etmenler temelde iki grup olarak incelenmektedir. Bunlar monogenik ya da poligenik formlardır. Monogenik formlar daha seyrek görülür. Poligenik değişimler daha sık görülür ve epigenetik değişimlerin etkisinin de bulunduğu bilinmektedir.
5.1.1. Poligenetik Değişimlerin Hipertansiyona Yatkınlık Üzerine Etkisi
Primer HT; gen-gen ve gen-çevre etkileşimli poligenik bir hastalıktır. Daha sık görülen poligenik formda ise oldukça heterojen birçok sorun aynı hastada bulunabilir(33). Genellikle primer HT’nin etiyolojisindeki etkileri araştırılan RAS sistemindeki genetik yapı ile ilgili değişikler sözkonusudur. Gen-çevre etkileşimde epigenetik değişimler gerçekleşmektedir.
Epigenetik düzenleme, DNA dizisinde değişiklik olmaksızın gen ekspresyonunda oluşan değişikliklerdir. Epigenetik değişikliklerin kalıtım yoluyla aktarılabildiği gösterilmiştir.
Epigenetik düzenlemede DNA metilasyonu ve histon modifikasyonu önemlidir(34). Tek yumurta ikizlerinde DNA metilasyonu ve histon asetilasyonunun incelendiği bir çalışmada yaşamın erken dönemlerinde ikizler arasında hemen hemen hiç epigenetik farklılık yokken, 28 yaşın üzerindeki ikizler arasında belirgin farklılıklar olduğu belirlenmiştir(35). Hastaların %30-50’sinde genetik yatkınlık olduğu gösterilmiştir. Anne veya babadan biri hipertansif ise çocuklarında HT gelişme riskinin 2 kat arttığı saptamıştır(35). Ailesel hipertansiflerde yüksek KB olan bireylerin çocuklarının hipertansif olma eğiliminde, düşük KB olan ebeveynlerin çocuklarının ise aynı oranda hipotansif olma eğiliminde oldukları saptanmıştır. Bu etkileşim, kişinin KB fenotipine etki eden poligenik bir genetik bir altyapı üzerinde gerçekleştiğini düşündürmektedir (32,33,34,35). Monozigotik ikizlerde KB yüksekliği her ikisinde de gösterilmiştir. Anne ile adapte edilen çocuk arasında KB’nin korele olmaması bu KB yüksekliğinin genetik bir yatkınlıkla ortaya çıktığını desteklemektedir (10,36,37).
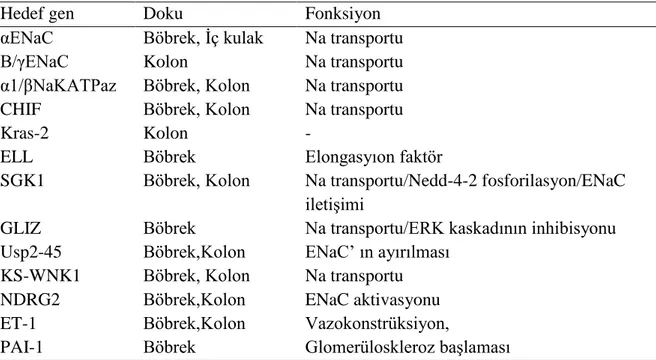
Kan basıncı ile ilişkili olduğu düşünülen, doğrudan veya dolaylı olarak renal tübüler transportu düzenleyen renin, anjiotensin, anjiotensinojen, prostosiklin sentaz, büyüme hormonu, insülin benzeri büyüme faktörü, tiroksin hidroksilaz, antiyal natriüretik faktör, insülin reseptörü, dopamin reseptörü, anjiotensin reseptörü, adrenerjik reseptör, leptin reseptörü, G-proteini, addusin gibi hormon yada hormon üretiminde yer alan enzim, reseptör, sinyal moleküllerini kodlayan birçok değişken saptanmıştır(38). Ayrıca Nöropeptid Y, transforming growth faktör, IL-6, NO sentetaz, lipoprotein lipaz, adipsin, kalmodüline bağlı protein kinaz 2, pankreatik fosfolipaz A gibi yüksek kan basıncı ile ilişkili gen ve gen ürünlerinin tübüler transportu ile ilişkisi olabileceği belirtilmektedir. Genellikle bu polimorfizmlerin KB üzerine etkisinin hafif olduğu bildirilmekte olup, HT’nin gelişmesi için farklı polimorfizmlerin kombinasyonununda olabileceği belirtilmektedir(36,38).
Hipertansiyon etiyolojisinde polimorfizmler, mutasyonlardan daha sıktır. Toplumda %1’den daha yüksek sıklıkta bulunan genetik çeşitlilik tipi ya da gen seçenekleri polimorfizm olarak isimlendirilir. İnsan genomunda en çok bulunan genetik çeşitlilik tipi, tek nükleotit polimorfizmleridir (SNP). Genomda binlerce aday polimorfik genin bulunması, genomda bu farklılıkları taşıyan kişilerin hastalıklara olan duyarlılıklarını da değiştirmektedir.
5.1.1.1.Ace-Renin-Anjiotensinojen Polimorfizmleri:
ACE (anjiotensin konverting enzim) geni 17q23 bölgesinde yer alır ve 21 kb uzunluğundadır. ACE geni 287 baz çiftlik Alu repeat sekansta 16 numaralı intronun varlığı (insersiyon formatında) ya da yokluğu (delesyon) zemininde İnsersiyon/Delesyon polimorfizmi ile karakterizedir. Bu durum 3 farklı genotipi ortaya çıkarmaktadır (DD, ID, II). Söz konusu polimorfizmin plazma ACE ve ortalama ACE düzeyi ile güçlü bir ilişkisi bulunmaktadır.
ACE gen polimorfizmi allel sıklığı coğrafya ve etnik unsurlara bağlı olarak değişiklik göstermektedir. Söz konusu polimorfizmin bu değişkenliği belli bölgelerde ve toplumlarda yoğunlaşan hastalıklarla olası bağlantısı üzerine özel bir ilgi oluşturmaktadır. Dünya üzerinde ACE gen polimorfizmi ile değişik hastalıklar arasındaki bağlantıyı araştıran çok sayıda çalışma yapılmıştır ve ACE geni I/D polimorfizmi bir çok hastalığın başlangıcı ya da seyri ile ilişkilendirilmektedir(39).
Türk toplumunda yapılan bir araştırmada pozitif aile hikayesi olan ciddi HT’li hastalarda DD genotipinin predispozan bir faktör olduğu ve ADE I/D polimorfizminin HT üzerine bağımsız faktörlerden biri olarak etki edebileceği sonucuna varılmıştır(40).
Kan basıncı üzerinde etkisi olan ve plazma anjiyotensinojen (AGT) düzeyini etkileyen AGT gen bölgesi bu sistemin en önemli üyelerindendir. AGT geni, 13 kilobaz (kb) uzunluğunda 5 ekson ve 4 introndan oluşan ve 1q42-43 arasında yerleşen gendir (41, 42). HT ile ilişkisi olası genler üzerinde yapılan çalışmalarda AGT geninin 2. Eksonunda metioninin treoninle yer değiştirmesini sağlayan 235. kodonda (M235T) ve treoninin metioninle yer değiştirmesini sağlayan 174. kodonda (T174M) tek nükleotid polimorfizmleri saptanmış ve bu iki bölgeye büyük ilgi duyulmuştur (42).
2005 yılında Çin’de yapılan bir çalışmada M235T genotipi taşıyanlarda HT riski çok arttığı gösterilmiştir. Yine 2005 yılında Rozita Rosli ve arkadaşları tarafından Malezyalılar üzerinde yapılan bir başka çalışmada M235T polimorfizmi incelendiğinde HT’li hastalardaki TT sıklığı kontrole göre çok yükseldiği gözlenmiştir.
5.1.1.2. Aldosteron Polimorfizmleri:
Aldosteron, bir mitokondriyal Sitokrom P450 enzimi olan aldosteron sentaz (CYP11B2) enzimi tarafından adrenal bezlerin zona glomeruloza hücrelerinde bir dizi biyokimyasal reaksiyonla (11 P hidroksilasyon, 18-hidroksilasyon ve 18-oksidasyon) sentezlenir (43,44). Aldosteron sentaz enzimi, kromozom 8q23.4 bölgesinde bulunan CYP11B2 geni tarafından kodlanır. Bu genin değişik bölgelerinde meydana gelen mutasyonlar, enzim aktivitesinde çeşitli değişimlere yol açmaktadır (45,46). Şimdiye kadar CYP11B2 geninde pek çok polimorfizm tanımlanmıştır. Bunlardan en önemlisi 344T/C polimorfizmidir ve bu bölge 1 transkripsiyon faktörünün bağlanma bölgesidir (46). SF-1.in çalışılmış tüm steroid hidroksilaz genlerinin promotor bölgelerine bağlandığı ve ilgili genlerin transkripsiyonunu sağladığı belirlenmiştir. Bu bölgede şekillenen polimorfizm, SF-1 transkripsiyon faktörünün bağlanma yeteneğini etkilediğinden HT ile ilişkilendirilmiştir (47,48).
5.1.1.3. Fabp2 VE ApoB100 Polimorfizmleri:
Metabolik sendrom kriterlerinde yer alan HT, dislipidemi ve obezite birbirinden ayrılamaz kısır bir döngü içerisindedir.
FABP2, lipid metabolizmasında bulunan FABP’nin ekspresyonunda yer alır. FABP2 uzun zincirli yağ asitlerinin intestinal sistemden emiliminden, hücre içine transportuna kadar bir çok basamakta rol almaktadır(49). Bu gende II.ekzonda 54.kodonda olan guanin bazının adenozine yer değişimi ile eskprese olması beklenen alanin yerine treonin aminoasidi sentezlenir ve tek nükleotid polimorfizmi oluşur(50,51). Bir çok yapılan çalışmada, mevcut polimorfizm ile olgularda artmış insülin direnci, artmış VKİ, HDL düzeylerinde düşüklük ve hipertrigliseridemi saptanmıştır.
ApoB100 ise; hem VLDL hem de LDL nin öncü partikülü olup, LDL için de reseptör görevi görmektedir. Karaciğerde trigliseritler lipoprotein lipaz ile sentez ve sekrete edilir. Hepatik lipaz geninin kromozomal yerleşimi 15q21 olup, 9 ekzon içerir(52). Değişikliğe uğramamış bir apolipoprotein molekülü; 30 G/G ve 21 A alleli içermektedir. Bu bölgede oluşan nokta mutasyonlar sonucunda G250A polimorfizmi oluşur; enzim aktivitesinde değişikliğe yol açar. Mutasyona uğramış apolipoprotein molekülleri yapılan çalışmalarda postprandiyal artmış lipemik cevaptan sorumlu tutulmaktadır(53,54).
5.1.2. Monogenetik Değişimlerde Hipertansiyon Gelişimi
Monogenik HT ise; distal ve toplayıcı tüplerde yer alan epitelyal sodyum kanalı (ENaC) genindeki mutasyon nedeniyle ortaya çıkan aşırı Na reabsorbsiyonu sonucu oluşur. Bu durum azalmış plazma renin aktivitesi, Na retansiyonu, hipokalemi ve alkalozis ile karekterizedir. Bu grup HT’de aşırı aldosteron üretimi veya baskılanmış aldosteron üretimi eşlik edebilir. Monogenik formlar daha nadir görülmekle birlikte monogenik HT; çocukluk çağı ve adelosanlarda HT ayırıcı tanısı içinde yer almalıdır(33,34,55).
HT’ye yatkın kişilerde bu mutasyonların saptanması, hastaların erken tanı alması ve hedef organ tutulumunun önlenmesi açısından önem taşımaktadır(33).
Monogenik HT sendromlarının başlıcaları Tablo 8’de gösterilmiştir.
Tablo 8. Monogenik Mineralokortikoid Hipertansiyon Sendromları Familyal hiperaldosteronizm Tip 1 ve Tip 2
Konjenital adrenal hiperplazinin hipertansif formu 11βhidroksisteroid dehidrogenaz eksikliği
Liddle sendromu
Mineralokortikoid reseptör mutasyon aktivasyonu Glukokortikoid direnci
Familyal Hiperaldosteronizm Tip I(FH I):
Glukokortikoid aracılı aldosteronizm (GRA): Otozomal dominant geçişlidir. Hipertansiyon, değişken hiperaldosteronizm, düşük PRA, normal veya düşük K, anormal adrenal steroid üretimi (18 okzokortizol, 18 hidroksikortizol) ile karekterizedir. Bu hastalık polipeptid 1 geni (CYP11B1) ile polipeptid 2 geninin (CYP11B2) nin füzyonu sonucu gelişir(şimerik gen). Bu hibrid mutasyon, zona fasikülata da ACTH ile regüle edilen aldosteronun ektopik ekspresyonuna yol açar(33,55) .
Familyal Hiperaldosteronizm Tip II(FH II):
Primer aldosteronizmin herediter formudur. Buradaki net mutasyon belli olmayıp, farklı çalışmalar 7p22 kromozomu üstünde durur.
11β Hidroksilaz Eksikliği:
11β hidroksilaz eksikliği en sık hipertansif konjenital adrenal hiperplazi (KAH) formudur. Tüm KAH olgularının %5-8’inde vardır. Otozomal resesif geçişlidir. Burada 11 deoksikortizolün kortizole dönüşümünü sağlayan 11β hidroksilaz enzimini kodlayan CYP11B1 genindeki mutasyon sonucu ortaya çıkar(33).
17 α Hidroksilaz eksikliği:
Diğer hipertansif KAH’ler p450c17 sitokrom defektine bağlı 17 α hidroksilaz eksikliği sonucu ortaya çıkar. Orta dereceli arteryel HT, renin-anjiotensin-aldosteron(RAAS) sistem supresyonu yapar(33,55).
11β Hidroksisteroid Dehidrogenaz (11βHSD2) Eksikliği:
Otozomal resesif kalıtımlı heterozigottur ve hastalar normal fenotipe sahiptir. 11βHSD2 enzim aktivitesinin bozulmuştur.
Bu enzim aktif olan kortizolü inaktif olan kortizona çevirir. Konjenital olarak bu enzimin yokluğunda bu koruyucu mekanizma bozulur, inaktif metabolite dönüşemeyen kortizol düzeyi artar. Mineralokortikoid reseptörlerin (MR) kortizole olan afinitesi aldosterona afinitesine eşittir. Ancak kortizol salınımı aldosterondan 100 kat fazla olduğu için, kortizol MR’sini doyurur(56). Bu nedenle kortizol hipofiz ve kalp gibi pek çok dokuda eses mineralokortikoid reseptörleri işgal eder. Bununla birlikte normal dolaşan düzeylerde tipik hedef dokularda (böbrek, kolon ve tükürük bezleri) lokal olarak kortizona dönüştürüldüğü için mineralokortikoid etkiye katkıda bulunmamaktadır. Kortizol bu enzimlerin yetersizliği ya da inhibisyonu durumunda dönüşümün azalmasına bağlı olarak mineralokortikoid HT’ye yol açabilir. Mineralokortikoid reseptörleri üzerinden Na tutulmasına yol açıp, KB’nin yükselmesine neden olmaktadır (33,37,56,57).
Bu hastalarda hipokalemi, metabolik alkaloz ve hiperkalsiüri birlikteliği enzim aktivitesinin tamaman olmadığını gösterirken, nefrokalsinozis ve metabolik alkaloz olmayışı bir miktar rezidüel enzim aktivitesinin olduğunu gösterir(55,58).
5.1.3. Glukokortikoid Reseptör Mutasyonu: (Primer Glukokortikoid Direnci) Nadiren görülen jeneralize veya parsiyel hedef organ glukokortikoid bozulmuş sensitivitesi vardır. Dolaşımdaki ACTH’nın kompansatuvar yükselişi kortizol, mineralokortikoid ve androjenler gibi adrenal steroidleri arttırır ancak hiperkortikolizm bulgusu klinik olarak yoktur. Klinik değişken olup asemptomatikten ağır hiperaldosteronizme kadar değişebilen mineralokortikoid yetersizliği ve/veya fazlalığı ortaya çıkabilir. Ayırıcı tanı Cushing ile yapılmalıdır.
Moleküler temelde, insan glukokortikoid reseptör geninde mutasyon vardır, böylece glukokortikoid sinyal transdüksiyonu bozulmuş olup dokuların glukokortikoid hassasiyeti bozulmuştur(33).
5.1.4. Mineralokortikoid Reseptör Mutasyon Aktivitesi
4q31.1 lokusunda MR gen mutasyonu sonucu olur, 810. kodonda (S810L) lösin’in yerine serin yer alır. Bu hastalarda MR anormal bir yapıdadır.
Erken başlangıçlı HT ve hamilelikte progesteronun etkisiyle kötüleşen HT görülür ancak MR(L810) taşıyıcılarında (erkek ve hamile olmayanlar) HT’den sorumlu steroidler henüz tanımlanmamıştır(33,34).
5.1.5. Liddle’s Sendromu
Otozomal dominant geçişli bir hastalıktır. Distal tübüllerdeki epitelyal Na kanallarının (ENaC) mutasyonu sonucu ortaya çıkar. Bu bu kanallar α,β,γ dan oluşan 3 subünite sahiptir. Liddle’s sendromunda β ve γ subünitindeki mutasyon nedeniyle epitelyal Na kanalları sürekli aktivedir böylece artmış Na emilimi, K kaybı ve volüm artışı vardır.
Klinik olarak HT, poliüri, düşük renin ve aldosteron ile hipokalemik metabolik alkaloz görülmektedir. Düşük reninli tuza hassas ve spiranolaktona cevapsız HT’li olgularda ENaC’ın genetik analizi önerilir. Bu bozukluk triamteren gibi epitelyal Na transport inhibitörlerine cevap vermektedir. Tedavide tuz kısıtlaması ve potasyum replasmanı uygulanır, spiranolaktona yanıtsızdır. Epitelyal sodyum kanallarını direkt olarak inhibe eden triamteren idrar Na’sını arttırır, HT’yi düzeltir. Bu olgular renal transplantasyona cevap verir, KB’leri normale döner, elektrolitleri düzelir(33,37).
5.2. Sempatik Sinir Sistemi Aktivasyonu
Sempatik sinir sistemi(SSS) uyarılmasının sonunda kalp hızında artış, periferik vazokonstriksiyon, adrenallerden norepinefrin salınımı ve sıvı retansiyonuna neden olarak KB’de yükselmelere yol açar.
SSS aktivasyonuyla renal efferent sempatik lifler de uyarılır, böylece renal kan akımında düşme ve renal vasküler dirençte artmayla sonuçlanan vazokonstriksiyona neden olur. Renal sempatik uyarılma doğrudan sodyum reabsorbsiyonu ve jukstaglomerüler aparattan renin salınımını uyarır. Artmış SSS aktivitesinin damar duvarında oluşturduğu yapısal değişikliklerin (damar düz kas hücresi hipertrofisi ve buna bağlı kompliyans azalması) zamanla SSS’deki aktivitede azalma olmasına rağmen KB düzeyinin yüksek devam etmesine neden olduğu düşünülmektedir. Stresin SSS aktivitesini uyardığı ve KB’yi yükselttiği bilinmektedir.
Sık olarak görüldüğü gibi HT ve obezite birlikte olduğu zaman SSS aktivitesindeki artışın HT patogenezindeki rolü daha fazla olabilir. SSS aktivitesinin HT patogenezindeki spesifik rolünden ayrı olarak artmış kardiyovasküler morbidite ve mortaliteyle de ilişkisi vardır. Sabahın erken saatlerinde alfa sempatik aktivitede ani bir artma meydana gelerek KB’de belirgin yükselmeler görülür(32).
Açıklanmamış primer HT’li genç bireylerde KB yüksekliğinin primer mekanizmasında sempatik sinir sistemi aktivasyonunun (overaktivasyonu) rol aldığı ileri sürülmüş. Primer HT’li çocuklarda normotansif çocuklara göre dinlenme anında taşikardi saptanmıştır ve dinlenme anındaki kalp hızı ve KB’nin korele olduğu büyük epidemiyolojik çalışmalarda gösterilmiştir. Falknerr tarafından yapılan çalışmalarda hipertansif adolesanların mental stres durumlarında normotansif çocuklara göre artmış kalp hızı, sistolik KB ve diastolik KB’ye sahip olduğu gösterilmiştir(10,59).
Ayrıca sempatik sinir sistemi beyaz önlük HT’si patogenezinde de rol alır. Beyaz önlük HT’si olan kişiler tipik olarak sinirli ve dinlenme zamanında taşikardiktirler(10,32,60). Parasempatik ve sempatik yanıt arasındaki dengesizlik primer HT’de ortaya çıktığı gibi beyaz önlük HT’de de görülür(59,60).
5.3. Ekstraselüler Sıvı, Sodyum ve Potasyum Metabolizması
Na, ana ekstrasellüler katyondur ve KB üzerine en etkili çevresel faktördür. Tersine K ana intrasellüler katyon olup HT patogenezinde rolü azdır.
Günlük tuz alımı (NaCl <50 mmol/gün) 50 mmolden az olanlarda primer HT ve yaşlanmaya bağlı KB yüksekliği oldukça azdır. Günlük tuz tüketimi 100 mmolden fazla olanlarda ise HT sıklığı yüksektir. Bazı toplumlarda HT prevalansı <%1 iken endüstrileşmiş toplumlarda ise erişkinlerin 1/3’ünün hipertansif olmasında diyet önemli rol oynar. HT görülme oranı düşük olan toplumların beslenmesi değiştirilirse (yeni düzenlenen diyette K/Na oranı azalırsa) HT görülme oranı artar. Normotansiflerde Na sensivitesi HT prekürsörüdür. Diyetsel K miktarı Na sensitivitesi üzerine güçlü ve doza bağımlı inhibitör etki yapar. Doğal gıdalara göre, hazır gıdalarda yüksek Na ve düşük K içerir. Örneğin; 2 dilim hamburgerde(57 gram), 32 mmol Na ve 4 mmol K içerir. 1 fincan tavuk çorbasında 48 mmol Na ve 1.4 mmol K içerir. Meyve sebze içeren diyetlerde ise düşük Na yüksek K içerir. Portakalda 131(gram), Na içermezken 6 mmol K içerir. Doğal beslenen toplumlarda günlük K alımı 150 mmol/G’ün üzerinde iken Na alımı ise 20-40 mmol/G’dir. Diyetteki K/Na oranı >3 olup çoğunlukla bu oran 10’a yakındır. Endüstrileşmiş toplumlarda 30-70 mmol/G K ve 100-400 mmol/G Na alırlar ve diyet K/Na oranı <0.4’tür (55,56,57). Doğal gıdalarda tuz oranı %12 iken işlenmiş (pişerken eklenen gıdalarda) %80’dir(61).
Arter Duvarı Üzerindeki Etkiler: Na retansiyonu ve K eksikliği vasküler düz kas arteriyal ve arteriolar Na pompasını inhibe eder, dolayısıyla intrasellüler sıvıda K azalır ve Na artar, artmış intasellüler Na düzeyi; Na-Ca exchanger Tip 1 (NCX1)’i uyarır, Ca hücre içine alınır. Hipokalemi hücre zarındaki K kanalları inhibe eder, membran depolarize olur. Na pompasınında elektrojenik özelliği olduğundan Na pompasının inhibisyonu kendi membran potansiyelini düşürür, vasküler düz kasta membran depolarizasyonu olur. İntrasellüler Ca daha da artar. Artan sitozolik Ca vasküler düs kas kasılmasını tetikler(61).
Na-K homeostazı primer HT’de defektif olan endotel aracılı vazodilatasyonda önemli rol oynar. Na retansiyonu nitrik oksit(NO) sentezini azaltır ve nitrik oksit üretiminin endojen inhibitörü olan asimetrik dimetil L-arginin plazma seviyesini arttırarak endotelyal vazodilatasyonu olumsuz etkisi vardır. Na kısıtlamasının her ikisi üzerine de ters etkisi vardır(61).
Yüksek K’li diyet K kanallarını açar, Na pompasını uyarır, endotel hücresini hiperpolarize eder, endotel bağımlı vazodilatasyon olur. Endotel hücresi hiperpolarize olunca vasküler düz kas hücrelerine iletilir, sitozolik Ca azalır, vazodilatasyon ortaya çıkar. Deneysel K kısıtlaması ile endotel bağımlı vazodilatasyonun inhibe olduğu gösterilmiş. Deneysel çalışmalara göre vasküler tonus etkilerine ek olarak, K’den zengin diyet; arteryel trombozisi, atherosklerozu ve arter duvarındaki medial hipertrofiyi inhibe ederek KVS riski azaltır(61).
İntraventriküler hipertonik salin verilerek, beyin omurilik sıvı(BOS) Na’sı arttırılırsa KB artar, ancak KCL verilirse BOS K’sı artarsa KB düşer(61).
Metabolizma üzerine etkileri ise; hipokalemi insülin salınımını inhibe eder, glukoz intoleransı ortaya çıkarır. Hiperkalemi veya K verilmesi pankreas β hücrelerindeki membran potansiyelini değiştirerek insülin salınım hızını arttırır. İnsülin NO salınımı ile iskelet kasında endotel bağımlı vazodilatasyonu tetikler, ancak bu yol primer HT’de bozulmuştur. Tiazid ile tetiklenen hipokalemi Tip 2 DM’de glukoz toleransını kötüleştirir. Hipokaleminin düzeltilmesi glukoz intoleransını da düzeltir. Diüretiklerle birlikte ACEİ ve ARB’ler K retansiyonu sağlar ve Tip 2 diabet başlama riskini azaltır. Tiazide bağlı hipokaleminin K verilerek düzeltilmesi diüretiğin antihipertansif etkisini de arttırır (61,62).
Primer HT’de Na tutulumunu açıklayan başlıca mekanizmalarda vardır:
-Konjenital olarak nefron sayısının azlığı(intrauterin büyüme geriliğine bağlı düşük doğum ağırlığı, konjenital oligonefropati), renal medüller kan akımının bozulması, iskemi veya interstisyel inflamasyona bağlı gelişen renal filtrasyon yüzeyinin azalmasına bağlı Na eksresyonunun azalması nedeniyle intraglomerüler basıncın artması sonucu HT gelişmesidir.
-Sodyum retansiyonuna neden olan ikinci mekanizma da basınç natriürez ilişkisinin bozulmasıdır. Normal kişilerde KB yükseldiğinde, böbreklerden sodyum ve su atılımı artarak intravasküler hacim küçültülür ve böylece KB normale döner. Bu fenomene basınç natriürezi denir. Hipertansiflerde ise KB ile sodyum atılımı arasındaki bu ilişki bozulur, KB’nin bu yolla regülasyonu gerçekleşmez(32,61).
5.4. Renin-Anjiyotensin-Aldosteron Sistemi
Renin böbrekte jukstaglomerüler hücrelerden salınır ve karaciğerden plazmaya verilen anjiyotensinojenin anjiyotensin-I’e çevirilmesi reaksiyonunu katalize eder. Reninin proksimal tübüler ve mezangial hücreler ile beyin, testis, karaciğer damar duvarında da renin mRNA saptanmasıda reninin böbrek dışında da sentezlendiğini düşündürmüştür. Renin salınımını afferent arterioler basınç azalması, renal perfüzyonun azalması, kan volümünün azalması, alfa ve beta adrenerjik uyarı, makula densada NaCl yoğunluğunun azalması, aldosteron azalması, PGE2 ve PGI2 artması, ANP, TNF, IL-1 renin salınımını uyarır. Mineralokortikoidler, AGT-II, tuz alımı, beta blokerler, ADH, tromboksan A2 ve endotelyal büyüme faktörü ise renin salınımını baskılar(32,63).
Oluşan anjiotensin I, anjiyotensin dönüştürücü enzim (ACE) tarafından anjiyotensin-II’ye yıkılır. Özellikle patolojik olaylarda lokal AGT-II üretimi ACE aktivitesinden bağımsız olarak alternatif yollarla oluşabilmektedir. Kalpte ve kan damarlarında AGT-II oluşumundan serin proteaz kimaz aktivitesi sorumlu tutulmaktadır.
Renin anjiotensin sisteminin fizyolojik ve patolojik etkileri anjiyotensin-II (AGT-II) üzerinden gerçekleşir. AII’nin AT1 ve AT2 olmak üzere 2 tip reseptörü vardır ve etkilerinin çoğu AT1 üzerinden olur. AII’nin AT1 reseptörüne bağlanmasıyla periferik damarlarda vazokonstriksiyon, intimal hiperplazi ve angiogenezis, myokardda kontraktilite, kollojen sentezi, hipertrofi ve fibrozis, adrenal bezden aldosteron sentezi, böbrekten sodyum geri alımı, beyin ve hipofizde SSS aktivitesi ve vasopressin salınımı yapar.
Kan basıncında yükselme olduğunda negatif feedback yoluyla jukstaglomerüler hücrelerden renin salgısı azalır. Bu nedenle primer HT’si olanlarda bu inhibisyona bağlı olarak plazma renin düzeyinin düşük olması beklenir. Ancak hipertansiflerde plazma renin düzeyleri homojen olmayıp KB düzeyi ile orantılı değildir. Sadece %30’unda renin düzeyi düşük olup %50’sinde normal, %20’sinde ise yüksektir. Hipertansif hastalarda plazma renin düzeylerinin uygunsuz bir şekilde normal veya yüksek olması nefron heterojenitesinin sorumlu olduğu öne sürülmektedir(32,63,64).
5.4.1. Aldosteron
Diyetle alınan Na kısıtlaması RAS’ı aktivite ederek adrenal zona glomerülozadan, anjiyotensin II ile uyarılan aldosteron salınımını arttırır. Aldosteron böbrekteki distal kıvrımlı tübüllerde ve toplayıcı tübüllerde sunulan mineralokortikoid reseptöre bağlanır ve klasik etkileri olan Na ve su tutulumunu ve potasyum salgılanmasını uyarır(65).
Aldosteron MR aracılığıyla etki göstererek hedef genlerin transkripsiyonunu düzenler. Ayrıca aldosteronun hızlı non genomik etkileri ile; protein kinaz C’nin, hücre dışı sinyallerle düzenlenen kinazlar 1/2’nin, c-Jun NH2-terminal kinazları ½’nin ve siklik adenozin 3´,5´monofosfat aktivitesinin uyarılması ve hücre içi iyon akışlarının uyarılması sayılabilir.
Protein kinaz C’nin baskılanması MR bağımlı transkripsiyonel aktiviteyi belirgin biçimde düşündürmektedir(65).
Aldosteron başlıca AGTII ve K etkisiyle adrenal korteks zona glomerülozada sentezlenen steroid yapıda bir hormondur ve primer olarak renin anjiyotensin sisteminin kontrolü altındadır. Doku ACE aktivitesi ile oluşan AGTII damar endoteli ve düz kas hücrelerinde lokal aldosteron sentezine neden olur. Aldosteron sentez inhibitörleri ise atriyal natriüretik peptid(ANP), dopamin ve somatostatindir(10,63).
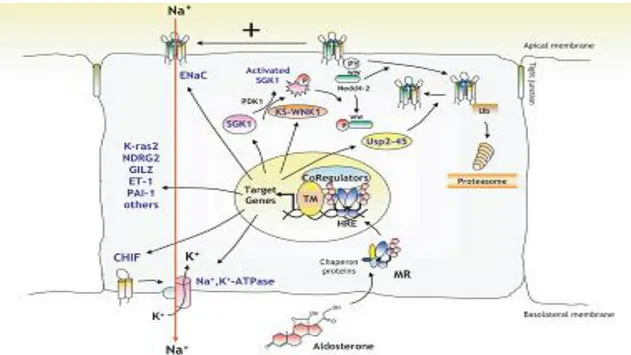
Aldesteron sodyum dengesi, su homeostazisi ve kan basıncı regülasyonun da önemli rol oynar. Aldesteron etkisinde temel aktörler MR ve epitelyal sodyum kanalı(ENaC)’tır. Aldesteronun ana etksi epitalyal hedef hücrelerin apikal membranda yer alan ENaC ve bazolateral membranda yer alan aktif transport NaK ATPaz pompası ile sodyum reabsorbsiyonu ve K ve hidrojen sekresyonudur(66) (Şekil 1).
Böbrekte kortikal toplayıcı tüplerde aldesteron, transepitelyal Na transportunu yapan kanalları (EnaC ve NaK ATPaz) aktivasyonunu stimule eder. Aldesteron serum ve glukokortikoid tarafından düzenlenen kinaz (SGK)’nın mRNA düzeyini arttırır; bu da ENaC’ı direkt stimule eder. Başka aldosteron regulatuvar genlerde identifiye edilmiştir. Bunlar: kanal arttıran faktör(CHIF), K-Ras2, cmyc, cJun, cFos, Fra-2 dır. Son zamanlarda N-myc down regüle eden gen 2 (NDRG2) böbrek distal toplayı tüplerde erken faz aldesteron yanıtını düzenler(66,67,68).
Aldesteron kardiyovasküler ve SSS üzerine önemli etkileri vardır. Aldosteron adipozit diferansiyasyonunu ve termogenezisi düzenler; mineralokortikoidlerin enerji dengesini düzenleyici rolü vardır(66).
Klinik bir çalışmada kardiyak aldosteron üretimi normal hastalarda saptanmazken diyastolik ya da sistolik kalp yetmezliğinde olan hastalarda transkardiyak konsatrasyon gradienti tespit edilmiştir. Ek olarak teorik ve deneysel çalışmalarda kalpte aldosteronun lokal üretimi parakrin/endokrin yollarla olduğu saptanmıştır.(69).
Aldosteron lökosit endotelyal hücre adezyon molekülü(ICAM-1) gibi proinflamatuvar sitokinlerin üretimini, vasküler makrofaj infiltrasyonunu ve aterosklerozu arttırdığı gösterilmiştir(56,66).
Aldesteron Na taşınmasında önemli olduğu gibi renal hasar mediatörüdür. Direkt etki ile aldesterona hassas olmayan distal nefronlarda ROS oluşturur, profibrotik aktiviteyi arttırır, hücre siklus düzenleyicilerinin dengesini değiştirir(70).
Benzer şekilde aldosteron uygulaması ile proteinürinin arttığı, podosit hasarı oluştuğu ve nefrin ve podosit ve nefrin sayısında azalma olduğu gösterilmiştir. Hasarlı podosit işaretleyicici olan densin miktarının aldosteron enjeksiyonu sonrası miktarının arttığı gösterilmiştir(70,71).
Glomerüler mezangial hücrelerin p450scc, 3βOHsteroid dehidrogenaz, 21 hidroksilaz ve CYP11B2 gibi steroidojenik enzimler aracılığıyla aldosteron ürettikleri gösterilmiştir.Bu nedenle lokal olarak üretilen aldosteronun mezangiyal hücrelerde MR’yi aktive ederek mineralokortikoid genlerin transkripsiyonunu uyardığı düşünülmektedir(71).