T.C.
SELÇUK ÜNİVERSİTESİ FEN BİLİMLERİ ENSTİTÜSÜ
AÇİL GRUPLU POLİSTİRENLERİN SENTEZİ VE ÜRÜNLERİN ALDEHİTLERLE REAKSİYONLARININ İNCELENMESİ
İsmet CEYLAN YÜKSEK LİSANS TEZİ
Kimya Anabilim Dalını
Mart - 2011 KONYA Her Hakkı Saklıdır
vi
ÖZET
YÜKSEK LİSANS TEZİ
AÇİL GRUPLU POLİSTİRENLERİN SENTEZİ VE ÜRÜNLERİN ALDEHİTLERLE REAKSİYONLARININ İNCELENMESİ
İsmet CEYLAN
Selçuk Üniversitesi Fen Bilimleri Enstitüsü Kimya Anabilim Dalı
Danışman: Yrd. Doç. Dr. Ahmet OKUDAN 2011, 77 Sayfa
Jüri
Yrd. Doç. Dr. Ahmet OKUDAN Prof. Dr. İbrahim KARATAŞ
Doç. Dr. Mahmut KUŞ
Bu çalışmada öncelikle polistirenin bazı anhidritlerle Lewis asidi
[
BF3.O(C2H5)2]
katalizörü ortamında Friedel-Crafts reaksiyonuna göre kimyasalmodifikasyonu gerçekleştirilmiştir. Bu reaksiyon için önceden belirlenen optimum şart kullanılmıştır.
Elde edilen karboksil gruplu modifiye polistirenler çeşitli aldehitlerle etkileştirilerek kondensasyon reaksiyonları gerçekleştirilmiştir.
Elde edilen bütün ürünlerin yapıları spektroskopik yöntemler kullanılarak aydınlatılmış olup, polistirenin aromatik halkasına bağlanan karboksil grubu miktarı volumetrik olarak tayin edilmiştir.
vii ABSTRACT
MS THESIS
SYNTESIS OF POLYSTYRENE HAVING ACYL GROUP AND INVESTIGATION OF REACTIONS OF PRODUCES WITH ALDEHYDES
İsmet CEYLAN
THE GRADUATE SCHOOL OF NATURAL AND APPLIED SCIENCE OF SELÇUK UNIVERSITY
THE DEGREE OF MASTER OF SCIENCE IN CHEMISTRY
Advisor: Asst. Prof. Dr. Ahmet OKUDAN 2011, 77 Pages
Jury
Asst. Prof. Dr. Ahmet OKUDAN Prof. Dr. İbrahim KARATAŞ Assoc. Prof. Dr. Mahmut KUŞ
In this study, the chemical modification of polystyrene has been primarily carried out with some anhydrides with Lewis acid catalysts like [BF3.O(C2H5)2]
according to Friedel-Crafts reaction. The pre-determined optimum conditions were used for this reaction.
The condensation reactions was carried out by the treatment of modified polystyrene containing carboxyl group which was obtained previously with various aldehydes.
The structures of received all products were characterized by the using of spectroscopic methots and carboxyl group values connected to aromatic rings of polystyrene were analyzed as volumetric.
viii ÖNSÖZ
Bu çalışma, Selçuk Üniversitesi Fen Fakültesi Kimya Bölümü Öğretim Üyelerinden Yrd. Doç. Dr. Ahmet OKUDAN’ın yönetiminde hazırlanarak, Selçuk Üniversitesi Fen Bilimleri Enstitüsüne Yüksek Lisans tezi olarak sunulmuştur.
Tezimin her aşamasında maddi ve manevi desteğini esirgemeyen ve önerileriyle yol gösteren danışmanım Yrd. Doç. Dr. Ahmet OKUDAN’a saygı ve şükranlarımı sunuyorum.
Çalışmalarımın çeşitli aşamalarında bana yardımcı olan Mehmet BÜYÜKSARI, İ.Levent ÖNDER, H. Hüseyin GÜNEŞ ve Ayşe KARASAKAL’a teşekkür ederim.
Ayrıca S.Ü. Fen Edebiyat Fakültesi Kimya Bölümü öğretim üyelerine, Araştırma Görevlisi hocalarıma Kimya Bölümü Depo görevlilerine ve Kimya Bölümünün diğer bütün üyelerine teşekkür ederim.
İsmet CEYLAN KONYA-2011
ix İÇİNDEKİLER ÖZET ... vi ABSTRACT ... vii ÖNSÖZ ... viii İÇİNDEKİLER ... ix 1. GİRİŞ ...1
1.1. Polimerler ve Polimer Biliminin Gelişimi ...1
1.2. Polimerlerin Kimyasal Özellikleri ...5
1.3. Polimerlerin Fiziksel Özellikleri ...6
1.4. Polimerleşme Reaksiyonları ...8 1.4.1. Kondensasyon polimerizasyonu ...9 1.4.2. Katılma polimerizasyonu ... 10 1.5. Polistiren ... 11 1.5.1. Polistirenin özellikleri ... 12 1.5.2. Polistirenin modifikasyonu ... 12
1.6. Çalışmanın Amacı ve Kapsamı ... 16
2. KAYNAK ARAŞTIRMASI ... 18
3. MATERYAL VE METOT ... 27
3.1. Kullanılan Kimyasal Maddeler ... 27
3.2. Deneyde Kullanılan Cihaz ve Aletler ... 27
3.3. Polistirenin Anhidritle Kimyasal Modifikasyonu ... 28
3.4. Polistirene Bağlanan Karboksil Grubu Miktarının Tayini ... 29
3.5. Açil Gruplu Modifiye Polistirenin Aldehitlerle Kondensasyon Reaksiyonu ... 31
4. ARAŞTIRMA BULGULARI VE TARTIŞMA ... 33
5. SONUÇ VE ÖNERİLER ... 44
6. KAYNAKLAR ... 46
EKLER ... 50
1. GİRİŞ
Modern teknolojinin her geçen yıl ilerlemesiyle polimer malzemelere olan ihtiyaç da katlanarak artmaktadır. Yaşantımızın hemen hemen her alanında, geniş ölçüde polimerlere dayalı malzemeler kullanmaktayız. Elektrik elektronik, inşaat sanayisi, giyim gibi polimere dayalı sektörleri çoğaltmak mümkündür.
Polimeri meydana getiren birimlere monomer, oluşan yüksek moleküllü maddeye ise makromolekül adı verilir. Aynı yapıdaki organik moleküllerin kovalent bağlar ile birbirine bağlanmasından oluşurlar. Polimerlerin molekül kütleleri on ve yüzbinlere hatta bazı hallerde milyonlarla ifade edilebilir. Polistirende binlerce karbon ve hidrojen atomu mevcuttur. Polimerler genellikle 5.000 – 250.000 ve daha fazla molekül ağırlığı bölgesinde bulunur.
Polistiren; yüksek dielektrik özellikli, kimyasallara ve suya dayanıklı materyaldir. Fakat ısı ve mekanik darbeye dayanıklılığı, adhezyon özelliği düşüktür. Yapılan tez çalışmasında, blok polistirenlerin [BF3.O(C2H5)2] katalizörlüğünde
anhidritlerle modifikasyon reaksiyonları, daha sonra sentezlenen açil (-COR) gruplu polistirenlerin; asetaldehit, krotonaldehit ve propiyonaldehit gibi doymuş ve doymamış alifatik aldehitlerle kondensasyon reaksiyonlarının gerçekleştirilmesi ve reaksiyon ürünlerinin yapılarının aydınlatılması amaçlanmıştır.
1.1. Polimerler ve Polimer Biliminin Gelişimi
Polimerler en basit tanımıyla çok sayıda aynı veya farklı grupların kimyasal bağlarla bağlanan, uzun zincirli yapıda olan yüksek molekül ağırlıklı bileşiklerdir. Polimerler çok sayıda monomerden oluşmaktadır. Polimer yapı birimleri (mer) monomerlerine eşit ya da hemen hemen eşittir (Baysal, 1994). Monomer birimlerinden başlayarak polimer moleküllerinin elde edilmesine yol açan reaksiyonlara polimerizasyon reaksiyonları denir.
Polimerik maddeler; katı, sıvı ve çözelti halinde kullanılırlar. Bütün bu hallerde değişik polimer yapılarının bulunabilme ihtimali son derece yüksektir. Yapı ile termal, mekanik ve diğer fiziksel özellikler yakından ilgilidir. Polimer yapılarının bölümlendirilmesinde ve polimer yapısı ile fiziksel ve mekanik özellikler arasındaki ilişkinin incelenmesinde molekül yapısının iki farklı yönünü incelemekte yarar vardır. Bunlar kimyasal bileşim ve moleküler mimaridir.
Kimyasal bileşim terimi; polimerde yinelenen birimleri, bir başka deyişle yerel yapıyı tanımlar. Polimerin kimyasal formülü ve adı kimyasal bileşimle belirtilir. Moleküler mimari terimi ise makromolekülün yapısının tümünü kapsar. Polimerin dorusal, dallanmış ya da üç boyutlu bir ağ örgüsü oluşuna göre yapısal düzen değişmektedir.
Polimerlerin molekül kütlesi farklı büyüklükteki moleküllerin molekül kütlelerinden oluşan ortalama bir değerdir. Bu nedenle polimer için molekül kütlesi değil ortalama molekül kütlesi kavramı kabul edilmiştir (Basan, 2001).
Yüksek molekül ağırlığına sahip oluşlarından ileri gelen yüksek viskozite, sünebilme ve şekil verebilme, kalıplanabilme özellikleri polimerlerin aynı zamanda malzeme olarak kullanılabilmelerine de imkân sağlar. Burada çok sayıda molekülün kovalent bağlarla birbirine yapışması polimer maddenin malzeme olarak kullanılmasının ilk sebebidir. Yüksek viskozite, elastik ve plastik özellikler moleküllerin birbirine kovalent bağlarla bağlanması sonucu olarak ortaya çıkar.
Polimerler monomerlerin kimyasal reaksiyonu sonucunda meydana gelen makromoleküllerdir. Monomerler, polimerleri oluşturmak üzere zincirler şeklinde bir araya gelip, kimyasal olarak bağlanabilirler. Bu yolla lineer, dallanmış, ağ yapılı polimerler oluşabilir. Polimerler, büyük moleküller olarak bir arada genellikle kovalent bağlarla tutulurlar. Bir polimeri oluşturmak üzere birleşen birimler birbirinin tıpatıp aynısı moleküller olabileceği gibi iki veya daha çok çeşitli moleküller de olabilir. Bir polimer molekülünde bulunan ortalama monomer ünitesi sayısına polimerizasyon derecesi denir. Tek tür tekrar ünitesiyle oluşan polimerler homopolimer olarak adlandırılırlar. Homopolimerler lineer, dallanmış çapraz bağ veya ağ yapıda olabilirler.
Bunlar Şekil 1.1’ de görülmektedir. İki farklı tekrar ünitesine sahip polimerler kopolimer, üç ayrı tür tekrar ünitesi içerenler ise terpolimer olarak adlandırılır.
Kopolimerler dört grupta toplanabilir:
1. Rastgele kopolimer: İki ayrı tekrar ünitesinin molekülleri rastgele dizilmiştir.
2. Ardışık kopolimer: İki ayrı tekrar ünitesinin molekülleri dönüşümlü olarak birbiri ardına sıralanmıştır.
3. Blok kopolimer: Bir tekrar ünitesinin molekülleri blok halinde birbirine bağlı olup, bir zincire öteki monomerin zinciri bağlanmıştır.
4. Aşı kopolimer: Bir polimerin uzun zincirine öteki monomerin zincirinin bağlanmış haline denir.
Kopolimer türleri şematik olarak Şekil 1.2’ de görülmektedir,
Şekil 1.2. Kopolimer türleri
Polimerlerin basit maddelerden farkları ise şu şekilde sıralanabilir;
- Küçük moleküllü maddeler (monomerler) genellikle gaz veya sıvı haldedirler, polimerler ise büyük moleküllü oldukları için katı ve genellikle serttirler.
- Küçük moleküllü bileşikler genellikle çözücülerde kolay çözünürler. Polimerler ise hem zor çözünürler hem de çözünme şekilleri küçük moleküllü bileşiklerden tamamen farklıdır. Çözücü molekülleri polimer moleküllerinden çok küçük olduğu için, önce polimerin içine diffüziye olurlar. Bu sebeple polimer şişer, polimerin hacmi 1.000 kat kadar artar. Bunun neticesinde mokromoleküller arasında olan bağ kuvvetleri zayıflar ve makromoleküller birbirinden ayrılarak çözeltiye geçerler. - Küçük moleküllü bileşiklerin çözeltileri şeffaf olduğu halde, polimerlerin çözeltilerinde ışığın dağılması gözlenir.
- Küçük moleküllü bileşiklerin kristalleşmesi genellikle kolay ve belli bir sıcaklıkta olduğu halde polimerlerin kristalleşme işlemi çok zor ve geniş bir sıcaklık aralığında olmaktadır. Polimerlerin kristalleşme işleminde sıcaklığın azalması ve sistemin viskozitesinin artması sebebiyle makromoleküller kendi hallerini zor
değiştirirler. Bunun için polimerler eriyik halinden katı haline dönüştüklerinde amorf maddelerde olduğu gibi camlaşma hali görülür, bunlardan farklı olarak polimerlerin camsılaşma hali geniş sıcaklık aralığında olur. Bu camlaşma sıcaklığı polimerik maddelerde önem taşır ve bunun üzerinde polimere şekil verilebilir.
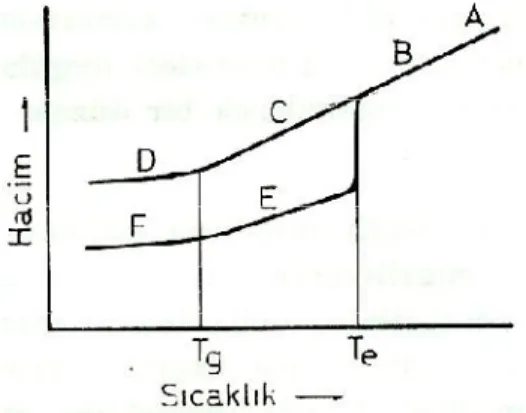
Şekil 1.3. Kristallenebilir polimerlerde hacim-sıcaklık eğrileri. (A) sıvı bölgesi, (B) bir miktar
esneklik gösteren sıvı, (C) kauçuksu bölge, (D) camsı bölge, (E) kauçuk, (F) camsı bir matris içindeki kristaller.
Küçük moleküllü bileşiklerin kristalleşme sürecinde sıcaklık azaldıkça moleküller birbirine yakınlaşır ve sistemin hacmi azalır. Hacmin böyle düz bir şekilde değişmesi maddenin ani olarak sıçrayışıyla sıvı halden kristal haline dönüşümüne kadar devam eder. Bazı hallerde maddenin sıvı halinden kristal haline dönüşümü bozulur ve camsılaşma süreci başlar. Bu tür değişiklikler amorf maddelere aittir.
- Polimerler yüksek elastik kabiliyetine sahiptirler. Polimerik maddelerde elastomer özellik polimerin yapısıyla ilgilidir. Polimer zinciri düzenli bir yapıda olursa kristal oranı fazla olacağından elastomer özellik beklenemez. Bir polimerin elastomer özellik gösterebilmesi için polimerdeki amorf polimer oranının fazla olması gerekmektedir.
- Polimer çözeltilerinden veya eriyik hallerinden ince tabakalar meydana getirilebilir.
Polimerler bu özelliklerinden dolayı teknikte büyük önem taşırlar. Polimerler sertliğine, yüksek sıcaklığa ve darbeye dayanıklılığına, yüksek dielektrikliğine, korozyona karşı dayanıklılığına göre geniş kullanım alanına sahiptirler (Mehmedov, 1981).
Polimer konusundaki ilk çalışmalar, 1839 yılında Goodyear’in kauçuğu kükürtle volkanize ederek Eboniti elde etmesiyle başlamıştır. Böylece su geçirmez botlar, yağmurluklar, dayanıklı taşıma aracı, lastiklerin ve benzeri ürünlerin üretimi
başlamıştır.1879 yılında izopren, 1880’de metakrilik asit polimerleştirildi. 1846 yılında Schönbein nitroselülozu, 1862 yılında Cross rayonu, 1865 yılında Schutzenberger selüloz asetatı bulmuşlardır. Böyle maddelere bugün için yarı sentetik maddeler denmektedir. 1907 yılında Bakeland fenol-formaldehitten %100 sentetik olan Bakalit’i elde etmiştir. 1920 yılında Staudinger, polistiren ve polioksietilen için ilk kez uzun zincirli molekül formülleri öne sürdü. 1929 yılında Almanya’da polistiren elde edilmiştir. Amerika’da Crothers ve arkadaşları poliadisyon ve polikondensasyon reaksiyonlarını başararak çeşitli polimerleri elde etmişlerdir. Böylece Staudinger ve Carothers bugünkü polimer kimyasının temelini atmış oldular.
Doğal polimerler insanların giyim, barınma ve yiyecek ihtiyaçlarına çok eskiden beri cevap vermektedir. Yüksek molekül ağırlığına sahip oluşlarından ileri gelen, yüksek viskozite, elastik ve plastik (şekil verebilme, kalıplanabilme) özellikleri, yüksek sıcaklığa ve darbeye dayanıklılığı, ayrıca korozyona karşı dayanıklılığı ve yüksek dielektrikliliğine sahip olması polimerlerin başlı başına bir bilim dalı olarak incelenmesini gerekli kılmıştır.
1.2. Polimerlerin Kimyasal Özellikleri
Polimerlerin kimyasal özellikleri hiç şüphesiz yapılarına bağlı olacaktır. Bir polimer yapısında bulunan fonksiyonel grupların reaksiyon kabiliyetinin polimerlerin molekül ağırlığına bağlı olmadığı kabul edilir. Bu fonksiyonel gruplar molekülün neresinde bulunursa bulunsun, kendilerine özgü reaksiyon vermelidirler.
Genel bir kural olarak bir polimerin herhangi bir madde ile reaksiyona girme yatkınlığı, küçük molekül ağırlığında olan ve polimer yapısındaki mer’e benzeyen bir maddenin o maddeye karşı reaksiyon yatkınlığı aynıdır.
Bunu daha açık hale getirmek için örnekleyelim; n-hekzan oda sıcaklığında kuvvetli asit ve bazlardan etkilenmez. Polietilen yapı bakımından n-hekzana benzediğinden oda aynı sıcaklıkta kuvvetli asit ve bazlardan etkilenmez.
Polimerlerin kimyasal reaksiyonu küçük moleküllü bileşiklerin reaksiyonları ile aynıdır ancak polimer moleküllerinin çok büyük olmaları ve fonksiyonel grupların çok olmaları nedeniyle onların girebildiği reaksiyonlarda bazı özel durumlar gerektirir. Polimer moleküllerinin reaksiyonları küçük moleküllü bileşiklerin reaksiyonlarına göre daha yavaştır ve polimer molekülündeki fonksiyonların tamamı reaksiyona girmez (Kurbanova, 1996).
1.3. Polimerlerin Fiziksel Özellikleri
Polimerler oda sıcaklığında katıdırlar. Lineer ve dallanmış polimerler, sıcaklığın yükselmesi ile viskozitesi çok büyük sıvı haline dönüşür. Çapraz bağlı ve üç boyutlu ağ yapıda olan polimerler çok zor erir veya hiç erimezler. Sıcaklığın etkisi ile molekül ağırlığı daha küçük olan maddelere parçalanırlar. Bu olaya degrasyon denir.
Polimerlerin molekül ağırlığı belli değere ulaştıktan sonra (Örneğin:10.000) yoğunluk ve erime noktası gibi fiziksel faktörlerde artık bir değişme gözlenmez. Oysa daha küçük molekül ağırlığındaki polimerlerde bu özellikler; polimerin molekül ağırlığı ile belirgin bir şekilde değişir. Yani polimerin molekül ağırlığı arttıkça, yoğunluk artar ve erime noktası yükselir.
Lineer ve dallanmış polimerlerin hemen hemen hepsi uygun çözücülerde oldukça derişik çözelti yaparak çözünürler.
“Birbirlerine benzer maddeler birbirlerini çözerler.” ilkesine uygun olarak her polimer kendi mer yapısına benzeyen çözücüde çözünürler. Örneğin polistiren etil benzende her oranda çözünür.
(a) (b)
Şekil 1.4. Polistiren (a) ve etilbenzenin (b) kimyasal formülleri
Bir polimerin çözünmesi iki aşamada gerçekleşebilen yavaş bir olaydır.
- Çözücü molekülleri önce polimer içine yavaş yavaş girerek şişkin bir jel oluştururlar.
- Polimer molekülleri ile çözücü arasındaki karşılıklı etkileşmeler kuvvetli ise, ikinci aşamada polimer çözücü içerinde gerçek bir çözelti vermek üzere çözünebilir.
Polimer jelinin çözelti halinde dağılması karıştırma ile hızlandırılır. Yüksek molekül ağırlıklı bir polimerin çözünmesi bazen günler alabilir. Polimer molekülleri arasındaki çapraz bağlar, kristalik ya da kuvvetli hidrojen bağının bulunması, başlangıçta bulunan jelin dağılmasını bir başka deyişle polimerin çözünmesini önleyebilir.
Polar olmayan doğrusal, amorf bir polimer, birim hacimdeki buharlaşma enerjisi kendisininkine çok yakın olan bir çözücü ile her oranda karışabilir. Mesela; polistiren; benzen, toluen CCl4 ve metil etil keton ile her oranda karıştığı halde, hekzan ya da
asetonda sınırlı oranda şişer. Hekzanın birim hacimdeki buharlaşma enerjisi düşük, asetonunki ise yüksektir. Oysa toluen, hem hekzan hem de asetonda her oranda karışabilir. Bu durum bir polimerin çözünmesi için, kullanılan çözücünün birim hacimdeki buharlaşma enerjisinin ne denli önemli olduğunu göstermektedir.
Polar olmayan polimerlerin çözünürlük davranışları çoğu kez birim hacimdeki buharlaşma enerjisi ile açıklanabildiği halde, polar polimerlerin polar çözücü molekülleri ile özgül çekim kuvvetlerinin de hesaba katılması gerekir. Örneğin; Lewis asit grupları ihtiva eden polimer molekülleri, Lewis bazları niteliğindeki çözücülerde çok kolay çözünürler. Bir sistem için uygun çözücünün seçiminde polarite, farklı aktif taneciklere göre solvasyon gücü, çözücü ve başlatıcı arasındaki özel etkileşimler ayrıca monomer, başlatıcı ve polimer sisteminin erime noktası, saflaştırma kolaylığı ve homojenliği gibi etkenler önemlidir (Beşergil, 2002).
Kristal yapılı polimerlerin çözünürlüğü amorf polimerlere göre çok düşüktür. Polar olmayan kristal yapılı bir polimer, erime noktasının oldukça altındaki sıcaklıklarda, hiçbir çözücüde çözünmez. Polimer ile çözücünün birim hacimdeki buharlaşma enerjisi tıpatıp uysa bile, çözünme olayı yeterince endotermik olduğunu için, polimerlerin çözünmediği görülür. Amorf bölgelere girebilen çözücü molekülleri polimeri kısmen şişirir, ama kristal yapısını eriterek polimeri çözemez. Polimerin çözünmesi için, polimer çözücü sistemini kristallerin erime noktasına yakın ısıtmak gerekir.
Polar kristal polimerler de birçok çözücülerde çözülemez. Ancak polar polimerlerin uygun polar çözücülerle karışması ekzotermik bir olay olduğundan, polar bir polimer erime noktasının oldukça altındaki sıcaklıklarda bile çözebilen çözücüler olabilir.
Polimerler bazı sıvılarda şişme basamağında kalır hiçbir zaman çözeltiye geçemez. Böyle durumlarda ortamda iki faz vardır;
- Çözücü fazı
1.4. Polimerleşme Reaksiyonları
Polimerler, küçük moleküllü bileşiklerin yani monomerlerin polimerleşme reaksiyonu, ya da polimerlerin kimyasal metotlarla (aşı) diğer polimerlere dönüşüm reaksiyonları ile sentezlenebilir (Kurbanova, 1996).
Çok sayıda aynı veya muhtelif düşük moleküllü maddelerin (monomerlerin) birleşerek ve aralarından hiçbir madde ayrılmadan yüksek moleküllü birleşme meydana getirme reaksiyonuna “Kondensasyon Reaksiyonu” denir. Bu süreç aynı maddenin molekülleri kullanılırsa “Homopolimerleşme” (Polietilen, Polistiren gibi) iki veya daha fazla muhtelif monomerler kullanılırsa “Kopolimerleşme” (Stiren ile Metilakrilat gibi) adı verilir.
Polimerleşme süreci üç basamakta gerçekleşir:
1. Monomerin aktifleşmesi ve polimerleşmenin başlaması
M1 M1· (1.1)
2. Polimer zincirinin büyümesi
M1 – M2 – M3 – M4 – M5 --- (1.2)
3. Polimer zincirinin sonlanması
M1 – M2 – M3 – M4 – M5 --- (-M )n (1.3)
Polimerleşmenin üç çeşidi vardır:
A. Kondensasyon (Basamaklı) Polimerleşme B. Zincir Polimerleşmesi:
a) Radikalik Polimerleşme b) İyonik Polimerleşme I. Katyonik Polimerleşme II. Anyonik Polimerleşme
C. Monomer halkasının açılması ile oluşan polimerleşme (Adisyon)
Örneğin; İzobütilen monomerinden poliizobütilen sentezi katyonik polimerleşmeye örnek olarak verilebilir.
-Friedel-Crafts katalizörünün kokatalizör ile kompleks oluşturması:
(1.4)
Oluşan kompleksin monomerle birleşip aktif merkez olan karbokatyonu oluşturması;
(1.5)
I. Basamak: Polimer zincirinin büyümesi
(1.6)
II. Basamak: Polimer zincirinden bir proton kopmasıyla polimer zincirinin tamamlanması:
(1.7) 1.4.1. Kondensasyon polimerizasyonu
Polikondensasyon reaksiyonları yüksek moleküllü bileşiklerin sentezi için çok yaygın kullanılan metotlardan biridir. En az iki fonksiyonlu grup (COOH, NH2, OH)
içeren monomerlerin küçük moleküllü bileşikler (H2O, NH3, HCl) ayrışmasıyla
oluşturdukları polimerleşme reaksiyonudur. Poliesterler, poliamidler bu tür polimerlerdir. Polikondensasyon reaksiyonları kademeli olur ve her kademede oluşan madde karışımdan kolay ayrılır. Bifonksiyonel monomerlerin polikondensasyonundan
düz zincirli (polietilentereftalat), ikiden fazla fonksiyonel grubu olan monomerlerden dallanmış veya çapraz bağlı polimerler (resol, poligliserinftalat) oluşur (Kurbanlı ve ark., 2005).
Aynı monomer moleküllerinin polikondensasyonuna homopolikondensasyon denir. Örneğin 7-aminoheptanoik asidin polikondensasyonundan poliheptanamidin sentezi:
H2N – (CH2)6 – COOH + H2N – (CH2) 6 – COOH → H-[HN – (CH2)6 – CO]n- OH (1.8)
Farklı monomerler arasında olan polikondensasyon reaksiyonuna heteropolikondensasyon reaksiyonu denir. Örneğin, adipik asit ile hekzametilendiamin arasındaki polikondensasyon reaksiyonu:
n. HOOC– (CH2)4– COOH + n. H2N– (CH2)6– NH2 →
→ HO–[OC– (CH2)4 – CONH–(CH2)6–NH]n-H + (2n-1)H2O (1.9)
1.4.2. Katılma polimerizasyonu
Katılma Polimerleri zincir reaksiyonları ile monomerlerin doğrudan doğruya polimer moleküllerine girmeleri ile oluşur. Zincir taşıyıcı bir iyon (anyon veya katyon) olabildiği gibi çiftleşmemiş bir elektronu bulunan ve serbest radikal denilen etkin bir madde de olabilir. Serbest radikaller, genel olarak, katalizör ya da başlatıcı denilen ve bazı koşullarda kararsız maddelerin parçalanması ile oluşur. Bu serbest radikal, bir vinil monomerinin çift bağı ile reaksiyona girerek monomere katılır ve yeniden çiftleşmemiş elektronu bulunan bir radikal verir. Çok kısa bir süre içinde (birkaç saniye) çok sayıda monomer molekülü büyümekte olan zincire katılır. En sonunda iki serbest radikal birbiri ile reaksiyona girer ve polimer molekülleri oluşur. Vinil monomerlerinin benzoil peroksit ile başlatılan radikal zincir reaksiyonu katılma polimerizasyonlarına örnek olarak verilebilir.
(1.10) (1.11) (1.12) (1.13) (1.14) 1.5. Polistiren
Polistiren kolay işlenen ve özellikleri iyi olan bir termoplastiktir. Kolay işlenmesi ve ucuzluğu sayesinde kâğıt, tahta ve metallerin yerini almıştır. Polistirenin monomeri olan stiren, petrol rafinelerinde bazı ürünlerin krakinginden ayrılan franksiyonlardan veya sanayide etil benzenin katalizör ortamında dehidrojenasyonu ile sentezlenir. Stiren monomerinin polimerizasyonu ile polistiren elde edilmektedir:
(1.15)
Polistiren ilk olarak II. Dünya Savaşı öncesi üretilmiş ve özellikle Almanya ve Amerika tarafından kullanılmıştır. 1970'de polistiren ve stirenin kopolimerlerinden elde edilen plastikler dünyada üretimi yapılan plastiklerin %13'ü kadardır.
1.5.1. Polistirenin özellikleri
Polistiren renksiz, şeffaf, suya dayanıklı, yüksek dielektrik özelliğine sahip, inert, lineer bir polimerdir. Ticari polistiren, ataktik ve amorftur. Polistirenin yoğunluğu 1,05-1,08 g/cm3 aralığındadır. Polistiren, birçok polimer gibi bilhassa sıcaklığa karşı dayanıklı değildir. Polistiren açık alevde tutuşur, fakat çok yavaş yanar. Kimyasal olarak, bazlar ve zayıf asitler polistirenlere tesir etmezler. Kuvvetli asitler bunlara tesir ederler. Polistiren açık havada kullanılmaya elverişli değildir.
Polistiren, optik bakımdan tabii olarak berraktır. Buna berrak saydamlıktan donuk siyahlığa kadar çeşitli renkler verilebilir. Isıya ve darbeye karşı az dayanıklı olması kullanım alanını daraltmaktadır. Polistirenin bu özelliklerinin geliştirilmesi için stirenin aşı ve blok kopolimerleri sentezlenmektedir.
Polistirene kolayca şekil verilebilir ve 80-150°C' da elastik olmaktadır, 200-250°C' da ise parçalanır. Optik özellikleri mükemmeldir. Plastik optik parçalar yapımında kullanılır. İyi bir elektrik yalıtkanıdır. Isı ve elektrik yalıtkanı olarak, ambalaj malzemesi olarak, şişe mantarı, kondensatörler için kaplamalar, kabloların izolesi için kablo sanayisinde, bardak, makine aksamı, mutfak malzemeleri yapımında kullanılır (Mindlin, 1973).
Ayrıca soğutmalı kamyonların soğutma kabinleri yapımında, sinema ve fotoğraf filmi yapımında, mikroskoplarda kullanılır. Duvarların ısı yalıtımı için duvar aralarına polistiren yapraklar konulmaktadır.
Polistirenin aşağıdaki özellikleri çeşitli yerlerde kullanılmasını sağlamaktadır. 1. Hafiftir,
2. Kalıplanması kolaydır,
3. Kokusuz, tatsız ve zehirsizdir, 4. Suya karşı dayanıklıdır.
1.5.2. Polistirenin modifikasyonu
Polimerlerin özelliklerini iyileştirebilmek için kimyasal reaksiyonlar ile polimer molekülerinde bazı değişiklikler yapılmaktadır. Bu tür değişikliklere modifikasyon adı verilir. Fiziksel ve kimyasal olmak üzere iki çeşit modifikasyon metodundan yararlanılır.
Fiziksel modifikasyon metodunda polimerler mekanik olarak karıştırılır. Bu şekilde elimizdeki polimerin elastikliği, sıcaklığa dayanıklılığı, sertliği değiştirilerek istenilen duruma getirilir. Ancak bazı sorunlarda ortaya çıkabilir. Örneğin karışıma katılan bir polimer havadan etkilenebilir veya polimerler ayrı fazlar oluştururlar ki bu, makromoleküller arası etkileşimin çok az olması anlamına gelir, dolayısıyla zaman ilerledikçe darbeye karşı dayanıklılık azalır.
Polimerin yüksek fiziko-mekanik özelliklere sahip olabilmeleri için bu fazlar arasında kimyasal bağlar olmalıdır. Muhtelif polifonksiyonel modifikatörlerle kimyasal modifikasyonu gerçekleştirmek mümkündür. Böylece ısıya ve darbeye dayanıklılığı artırılabilir. Kimyasal modifikasyon geniş bir alanı kapsadığından dolayı bilimsel açıdan da önem taşır. Polimerler;
– Büyük molekül ağırlıklı bileşikler, düşük molekül ağırlıklı bileşikler gibi muhtelif kimyasal reaksiyonlara girer.
– Polimerlerin kimyasal modifikasyonu ile yeni polimerler sentezlenir ki bu polimerleri, uygun monomerler ile polimerleştirerek sentezlemek mümkün değildir.
– Polimerlerin kimyasal modifikasyonu, pratik olarak kullanılmasına göre uygun monomerlerin sentezi ve onların polimerleşmesinden hem ucuz hem de daha kolaydır.
Büyük molekül ağırlıklı bileşiklerle, monomerlerin kimyasal reaksiyonları arasında bazı farklar vardır. Bu farklar;
1. Polimerlerin kimyasal modifikasyon reaksiyonlarında, polimerin esas reaksiyonu ile beraber yan reaksiyonları da olur ki, bunları birbirinden ayırmak mümkün değildir. Ancak monomerlerin kimyasal reaksiyonlarındaki yan reaksiyon ürünlerini fiziksel ve kimyasal metotlarla ayırmak mümkündür. Bu sebeple polimerlerin, kimyasal modifikasyon metotları yarı reaksiyonlar meydana gelmemesi için çok dikkatli seçilmelidir.
2. Polimerlerde sterik ve statik sebeplerden dolayı bazı hallerde reaksiyon tamamıyla sonuna kadar gitmez ve reaksiyona girmeyen başlangıç maddelerini polimerden ayırmak zor olur. Ancak monomerlerin kimyasal reaksiyonlarında ise reaksiyona girmeyen başlangıç maddelerini ayırmak mümkündür.
Polimerlerin kimyasal modifikasyonuna polistirenin modifikasyonu örnek olarak gösterilebilir. Polistirenin kimyasal modifikasyonu halojenleşme, nitrolaşma, metalleşme, sülfolaşma, açilleşme, alkilleşme vs. reaksiyonları ile yapılır. Bu konu oldukça fazla incelenmiştir (Mets ve ark., 1971; Mogno, 1977; Gibson, 1980; Swiger, 1974; Kussing, 1983; Betfor, 1979).
Yapılan birçok çalışmada, kimyasal modifikasyonla elde edilmiş modifiye polistirenin, polistirenden farklı olarak yüksek fizikomekanik özelliklere, darbeye karşı dayanıklılığa, nispi uzamaya, ayrıca termal özelliklere sahip olduğu tespit edilmiştir (Venwo ve ark., 1977; Swiger, 1975).
Elde edilen ürünlerin kullanım sahaların araştırılması sonucunda polistirenin açilleşme ve alkilleşme reaksiyonlarından elde edilen maddeler hem teorik hem de pratik olarak önem taşımaktadır. Kurbanova ve arkadaşları polistirenin kimyasal modifikasyonu için araştırmalar yapmış ve katyonik katalizörlü ortamda molekül ağırlığı 500.000 olan emülsiyon olan polistirenlerin, alkilleşme, açilleşme, alkanilleşme reaksiyonlarını incelemiştir. Kurbanova ve arkadaşları emülsiyon polimerizasyonla elde ettikleri polistireni çeşitli monomerlerle etkileştirmişler ve değişik fonksiyonel gruplu polistirenler sentezlemişlerdir. Oluşan üründeki fonksiyonel grupların polistirene, muhtelif substratlara karşı adhezyon kabiliyeti, darbeye karşı dayanıklılık, ışığa hassaslık gibi yeni özellikler kazandırdıkları tespit etmişlerdir.
Polistirenin aromatik halkasında olan kimyasal modifikasyon reaksiyonlarının daha fazla araştırılması ile yeni fonksiyonel gruplar bağlanmış polistirenler elde edilebilir. Polistirenin önemli eksikliklerinden biri muhtelif substratlara karşı adhezyon kabiliyetinin olmamasıdır. Bu ise polistirenin polimerik kaplama maddesi olarak kullanılmasını engellemektedir. Polimerlerin organik anhidritlerle radikalik ve katyonik katalizörler ortamında kimyasal modifikasyonu ile adhezyon kabiliyeti kazandıkları görülmektedir. Polimerlerin kimyasal modifikasyonları ile elde edilen alkilleşme ve açilleşme ürünleri ışığa hassaslık özelliği kazanmışlardır. Ayrıca fonksiyonel grupların bağlanması ile polimerlerin sıcaklığa ve korozyona karşı dayanıklıklarının artması da kullanım alanlarını genişletmektedir. Yapılan birçok çalışmada kimyasal modifikasyonla elde edilmiş modifiye polistirenlerin, polistirenden farklı olarak yüksek fiziko-mekanik özelliklere, darbeye karşı dayanıklılığa, nisbi uzamaya ve termal özelliklere sahip olduğu tespit edilmiştir (Venwo ve ark., 1977; Swiger, 1975 ve 1976).
Polistirenin aromatik halkasında yapılan kimyasal modifikasyon reaksiyonlarından nitrolaşma, sülfolaşma, halojenleşme gibi reaksiyonları aşağıda görülmektedir.
(1.16)
Polimerler reaksiyona girmeden önce uygun bir çözücüde iyi bir şekilde çözünmesi ve bu çözünme gerekirse uzuncu bir müddet beklenerek manyetik karıştırıcılarda kullanılarak yapılmalıdır. Bu şekilde makromoleküllerin reaksiyona girmesi kolaylaşacaktır. Polimer reaksiyonlarında kullanılan katalizör polimerin yapısını bozmayacak şekilde kuvvetli katalizör olmalıdır. Polimerlerin statik ve sterik etkilerinden dolayı bağlanacak olan fonksiyonel grup polimer zinciri boyunca aralıklarla bağlanır. İstenilen modifikasyonun sağlanması ve verimi artırmak için monomere göre daha etkin reaksiyon şartlarında çalışmaktadır. Reaksiyon süresindeki artışın verim üzerine olumlu etkileri gözlenmiştir.
1.6. Çalışmanın Amacı ve Kapsamı
Polimerler, yüksek fiziko-mekanik özelliklere sahip malzeme olarak sanayide çokça kullanılmaktadır. Adhezyon kabiliyeti yüksek, darbeye, sıcaklığa, korozyona karşı dayanıklı, ışığa hassas özelliklere sahip polimer materyallerin sentezi ve kullanım alanlarının genişletilmesi, polimer kimyasının önemli konularından biridir. Modifikasyon metoduyla elde edilen fonksiyonel gruplu polistirenlerin, sanayide birçok alanda kullanım sahası bulunmaktadır. Mesela, imidazol halkalı polistiren, elektriği iletmeyen malzeme ve aynı zamanda sentetik liflerin boyanmasında katkı maddesi olarak, sikloalkil grupları bağlanan polistiren sıcaklığa dayanıklı materyal olarak, alkilleşmiş polistiren ışığa hassas polimerler olarak kullanılmaktadır (Kenyon, 1958; Hulsbergen, 1977).
Polistiren, mekanik dayanıklığı az olan, adhezyon kabiliyeti olmayan ışığa hassaslık özelliği göstermeyen, sıcaklığa, atmosfere ve darbeye karşı dayanıklılığı az olan bir polimerdir. Polistirenin bu özelliklerini (adhezyon, ışığa hassaslık) iyileştirmek için kimyasal modifikasyona tabi tutulduğu bilinmektedir. Bu bilgiden hareketle Kurbanova ve arkadaşları (1998), kimyasal modifikasyon metoduyla karboksil gruplu polistiren sentezlemişlerdir. Yaptıkları bu çalışmada polistirene bağlanan karboksil grubu miktarının, modifiye ürünü termogravimetrik ve fiziko-mekanik özelliklerini doğrudan etkilediğini gözlemişlerdir. Karboksil grubu miktarının artışıyla modifiye ürünün adhezyon kabiliyeti, ışığa karşı hassaslığı, yüksek sıcaklığa, gerilmeye, atmosfere ve darbeye karşı dayanıklılığının arttığı gözlenmiştir.
Bu çalışmada çeşitli anhidritlerle modifiye edilmiş polistirenin asetaldehit, propiyonaldehit ve krotonaldehit ile olan kondensasyon reaksiyonları ve bu yolla yeni
bir tür modifiye polimerler sentezlenmesi amaçlanmaktadır. Elde edilecek bu polimerle, polistirenin kullanım alanının daha da genişletilmesi amaçlanmaktadır.
Polistiren Lewis Asitleri katalizörlüğünde farklı anhidritlerle modifiye edilecektir. Sentezlenecek karboksil gruplu polistirenin çeşitli aldehitlerle kondensasyon reaksiyonu gerçekleştirilecektir. Modifiye karboksil gruplu polistiren daha önceden tespit edilen optimum şart da yapılacaktır (Önder, 2009; Kul, 2007). Elde edilen ürünlerin yapıları spektroskopik yöntemler kullanılarak aydınlatılacaktır.
2. KAYNAK ARAŞTIRMASI
Polistiren, stirenin polimerleşmesiyle elde edilen lineer bir polimerdir. Polistirenin monomeri olan stiren, etil benzenin katalizör ortamında dehidrojenasyonu ile elde edilebilmektedir. Bunun için önce etil benzen, AlCl3 katalizörü ortamında
benzenin etilenle (2:1, 3:1 oranında benzen:etilen) 90-950C’ da alkilleşmesinden elde edilir.
(2.1)
Etil benzen daha sonra ZnO veya Fe2O3 katalizörleri ile 600-6300C’ da stirene
dönüştürülür.
(2.2)
Stiren, sentezinde yan ürün olarak oluşan divinil benzenden vakum kolonlarında fraksiyonla ayrılır. Stiren elde edildikten sonra depolama esnasında kendi kendine polimerleşebilir. Onun için stiren paketlenirken içerisine inhibitör ilave edilir.
Polistiren, radikalik veya iyonik olmak üzere stirenin polimerleşmesinden elde edilir. Polimerleşme süreci; kütle, çözelti, emülsiyon veya süspansiyon polimerleşme metodlarıyla yapılabilir.
(2.3)
Sentezlenen polistirenin ortalama molekül ağırlığı elde ediliş metoduna göre farklılık gösterir. Emülsiyon polimerleşme metodunda en yüksek molekül ağırlıklı polistiren elde edilirken, diğer metodlarla elde edilen polistirenlerin molekül ağırlıkları daha düşük olur.
Polistiren, düşük molekül ağırlıklı bileşiklere göre çok daha az aktif bir bileşiktir ve reaksiyon kabiliyeti daha zayıftır. Ancak muayyen reaksiyon şartlarında polistiren, hem düz zincirlerinden yani alifatik karbon zincirinden hem de aromatik halkasından yer değiştirme reaksiyonları verir (Tonimoto,1968). Fonksiyonel grup, katyonik katalizörler kullanıldığında polistirenin, aromatik halkasına, radikalik katalizörler kullanıldığında ise polistirenin alifatik zincirine bağlanır.
Polistirenin aromatik halkasındaki reaksiyonlar, gün geçtikçe alifatik düz zincirdeki reaksiyonlara göre daha da artış göstermektedir. Polistirenin aromatik halkasında alifatik zincirine göre, daha fazla reaksiyon yapılmasının sebebi polistirenin aromatik halkasındaki aktif fenil grubundan ileri gelmektedir. Polistirenin aromatik halkası birçok kimyasal reaksiyonlara, mesela sülfolaşma, sülfoklorlaşma, klorlaşma, nitrolaşma ve sonra aminleşme, açilleşme, alkilleşme klormetilleşme, metalleşme vs girebilir. Organik kimyada küçük molekül ağırlıklı bileşikler, yani monomerler için karakteristik reaksiyonlardan olan organik anhidritlerle açilleşme reaksiyonları Friedel-Crafts reaksiyonuyla yapılmaktadır. Pummer (1936) yaptığı çalışmada benzenin maleik anhidritle açilleşmesini Lewis asitleri varlığında gerçekleştirmiştir. Polistirenin kimyasal modifikasyonu için aromatik halka üzerinden birçok çalışma yapılmıştır. Wolf ve arkadaşları (1969) polistirenin, katyonik katalizörlü ortamda malomnik adipik, teraftalik asit, dikloritler ve fosgenle reaksiyonundan keton grubu polistireni sentezlemişlerdir. Harrison ve arkadaşları (1975) polistirenin benzoil klorürle olan reaksiyonunu incelemişler ve karboksil grubu polistireni iki basamakla sentezlemişlerdir. Ayres ve Mann (1965) ise polistirenin önce klormetilleşmesini, sonra da onun iki defa oksilasyonu ile karboksil gruplu polistiren elde edilmesini, katyonik katalizörlük ortamda üç basamakta gerçekleştirmişlerdir.
Polimerler, yüksek fiziko-mekanik özelliklere sahip malzeme olarak kullanılmakla beraber, son yıllarda termik, adhezyon, ışığa hassas özellikli polimer materyallerinin sentezi ve kullanım alanlarının araştırılması oldukça önem kazanmıştır.
Polistirenin kimyasal modifikasyon reaksiyonları, yani halojenleme, nitrolama, metalleşme, sülfolama, açilleme, alkilleme reaksiyonları vs. oldukça fazla incelenmiştir. Elde edilen ürünlerin kullanılma sahalarının araştırılması sonucunda polistirenin açilleşme ve alkilleşme reaksiyonlarından elde edilen maddeler hem teorik hem de pratik olarak önem taşımaktadır. Kurbanova ve arkadaşları (1974 ve 1990) polistirenin kimyasal modifikasyonu için araştırmalar yapmış ve katyonik katalizörlü ortamda molekül ağırlığı 500.000 olan emülsiyon polistirenlerin, alkilleme, açilleme,
alkenilleme reaksiyonlarını incelemiştir. Kurbanova ve arkadaşları emülsiyon polimerizasyonla elde ettikleri polistireni çeşitli monomerlerle etkileştirmişler ve değişik fonksiyonel gruplu polistirenler sentezlemişlerdir. Elde edilen ürünlerdeki fonksiyonel grupların polistirene, muhtelif substratlara karşı adhezyona kabiliyeti, darbeye karşı dayanıklılık, ışığa hassaslık gibi yeni özellikler kazandırdıklarını tespit etmişlerdir. Aynı zamanda bu reaksiyonlarıyla karşılaştırmış ve her iki reaksiyonun, yani hem polistirenin hem de model bileşiklerin Flory prensibine uygunluklarını belirlemişlerdir.
(2.4)
Polistirenin modifikasyon reaksiyonlarında Friedel-Crafts alkilasyonu ve açilasyonundan yararlanılmıştır. Friedel-Crafts açilasyonu ile polistirenin termal özellikleri geliştirilmiştir (Brauman, 1979; Biswas, 1983).
Polistirenin aromatik halkasında olan kimyasal modifikasyon reaksiyonlarının daha da araştırılması ile yeni fonksiyonel gruplar bağlanmış polistirenler elde
edilebilecektir. Polistirenin önemli eksikliklerinden biri muhtelif substratlara karşı adhezyon kabiliyetinin olmamasıdır. Bu ise polistirenin organik anhidritlerle radikalik ve katyonik katalizörler ortamında kimyasal modifikasyonu ile adhezyon kabiliyeti kazandıkları görülmektedir. Polimerlerin kimyasal modifikasyonu ile elde edilen alkillenme ve açillenme ürünleri ışığa hassaslık özelliği kazanmışlardır. Ayrıca fonksiyonel grupların bağlanması ile polimerlerin sıcaklığa ve korozyona karşı dayanıklıklarının artması da kullanım alanlarını genişletmektedir. Yapılan birçok çalışmada, kimyasal modifikasyonla elde edilmiş modifiye polistirenin, polistirenden farklı olarak yüksek fiziko-mekanik özelliklere; darbeye karşı dayanıklığa, nisbi uzamaya, ayrıca termik özelliklere sahip olduğu tespit edilmiştir (Venwo ve ark., 1977; Swiger, 1975 ve 1976). Polistirenin aromatik halkasında yapılan kimyasal modifikasyon reaksiyonlarından nitrolanma, sülfolanma, halojenlenme gibi reaksiyonları aşağıda görülmektedir.
Polistirenden iyot ve iyodat asidi ile H2SO4 katalizörlüğünde poli-iyotstiren
sentezlenir ve ondan da poli-lityumstiren sentezlenmektedir. Polistirenin birçok türevleri poli-lityumstirenden sentezlenmektedir. Zira poli-lityumstiren büyük molekül ağırlıklı organometalik bir bileşiktir ve reaksiyon kabiliyetine göre düşük molekül ağırlıklı organometalik bileşiklere benzer özellikler göstermektedir (Braun, 1959).
Polistirenin sayfa 15’deki polistirenin kimyasal modifikasyon reaksiyonlarından görüldüğü gibi, poli-p-lityumstirenin hidrolizinden polistiren, dimetilformamidle reaksiyonundan poli-p-formilstiren, nitrillerle reaksiyonundan ise polimer ketonlar elde edilir ki, bunları aynı zamanda Friedel-Crafts reaksiyonu ile polistirenden sentezlemek mümkündür. Elementel kükürtle, lityumstirenin etkileşmesinden poli-p-merkaptostiren elde edilir ki, bu polimer, elektron değiştirici reçine olarak kullanılabilir. Karbonil ihtiva eden bileşiklerle (aldehitlerle, ketonlarla) etkileştirildiğinde sekonder ve tersiyer alkolleri meydana getirir. Poli-p-lityumstirenin bazı reaksiyonları yukarıda gösterilmiştir.
Klormetillenmiş polistiren kolaylıkla birçok kimyasal reaksiyonlara girebilmektedir (Gibson, W.Q. 1976; Parker, D.B., 1967; Jmamura, S., 1979). Bu durum C-Cl bağının kırılma enerjisinin az olması ve klormetilleşmiş polistirendeki klor atomunun çok hareketli olmasındandır. Roever (1975) yaptığı çalışmada, klormetilleşmiş polistirenin aminlerle reaksiyonundan amin gruplu polistirenler sentezlenmiş ve elde edilen amin gruplu polistirenlerin anyon değiştirici olarak kullanılabileceğini, amonyakla, primer ve sekonder aminlerle zayıf bazik karakterli, tersiyer aminlerle ise kuvvetli bazik karakterli anyon değiştirici reçineler elde edildiğini tespit etmiştir. Ayrıca yapılan birçok çalışmada modifiye polistirenlerin iyon değiştirici reçine olarak kullanılabileceğini göstermektedir. Helfferich (1959) bu kaide ile polistirene, imindiasetikasit grubu bağlamıştır.
(2.6)
Polistirenin alkilleşmesi ile ilgili yapılan araştırmalardan biri de; polistirenin, aromatik doymamış asidin kloranhidriti ile reaksiyonundan ışığa hassas polimer elde edilmiştir (Garney, F. A., 1967).
(2.7)
Kenyon (1955, 1958) Friedel-Crafts reaksiyonu ile açil polistireni elde etmiş ve bu elde edilen açil polistirenin aldehitlerle reaksiyonundan da ışığa hassas polistireni sentezlemiştir.
(2.8)
Blanchette (1958) polivinilasetofenonun hidroksilamin klorhidratla reaksiyonundan oksim elde etmiştir.
(2.9)
Polistiren kendiliğinden oksitleşip, peroksit meydana getiremez. Polistirenin izopropil klorürle Friedel-Crafts reaksiyonu ile alkilleşmesiyle elde edilen izopropil polistiren benzoil peroksitle çok kolay oksitleşip hidroperoksit gruplar meydana getirir.
Elde edilen bu hidroperaoksit gruplar stirenin veya metilmetakrilatın polimerleşmesi için başlangıç basamağında aktif merkez gibi davranabilmektedir.
Okudan (1998) polistirenden kimyasal modifikasyon metoduyla maleik anhidrit ve değişik katyonik katalizörler ortamında, tespit ettiği optimum şartta karboksil gruplu polistirenler sentezlemiştir.
Zheng ve ark. (2007) yaptıkları çalışmada; Güçlü polar gurup içeren, karboksilik asit gibi, etilen ve alil benzen kopolimerlerinin içine bozulma ya da çapraz bağ olmaksızın Friedel-Crafts açilasyon reaksiyonları sayesinde glutarik anhidrit, süksinik anhidrit, ftalik anhidrit ile sentezlenebildiğini göstermişlerdir.
(2.11)
Juan ve Li (2004) yaptıkları çalışmada; Syndiotactic polistiren(sPS) için kimyasal modifikasyonu süksinik anhidrit ile Friedel-Crafts açilasyon reaksiyonu ile gerçekleştirmişlerdir.
(2.13)
Chen ve ark. (2008) yaptıkları çalışmada; Maleik anhidriti Friedel-Crafts açilasyon reaksiyonu ile sindiyo taktik polistiren üzerine modifiye etmişlerdir.
(2.14)
(2.15)
Kumari ve ark. (1995) %2 divinilbenzenle çapraz bağlı polistireni önce kimyasal modifikasyonla aldehit veya keton reçineye, daha sonra oksim reçinesine dönüştürmüşler. Oksim reçinesinin sodyum hidroksitin sulu çözelti ortamında karbon disülfürle reaksiyonundan ise ditiyokarbonat reçinesi elde edilmiştir.
Literatürde aldehit reaksiyonlarının ve Aldol kondensasyonunun da birçok araştırmacı tarafından incelendiği de görülmektedir.
Dimitrov ve ark. (1992) ise organik çözücüler ortamında katalizör olarak okzalik asit kullanarak krezol-benzaldehit oligomerlerini sentezlemişler. Araştırmacılar tarafından monomerlerin mol oranını ve reaksiyon ortamının polikondensasyon reaksiyonunun verimine, yumuşama noktasına ve oligomerlerin molekül ağırlığına etkisi de incelenmiştir. Reaksiyon ürünlerinin yapısı IR ve NMR spektroskopi yöntemiyle aydınlatılmıştır. Elde edilen sonuçlara göre reaksiyon mekanizması ileri sürülmüştür.
Abello ve ark. (2007) tarafından kamfolenik aldehidin metiletilketonla Aldol kondensasyonu incelenmiş, reaksiyon sıcaklığının girdilerin mol oranının ve katalizörün reaksiyona etkisi belirlenmiştir. Reaksiyon ürünlerinin termal, FTIR analizleri yapılmıştır.
(2,16)
(2.17)
Kuriakose ve Rajasekharan Pillai (1994) polimerik benzaldehitle benzoinin kondensasyonunu yapmışlar. Polimerik benzaldehit, divinilbenzen ve tetraetilenglikol diakrilatla çapraz bağlı polistiren elde edilmiştir. Bu polimerik aldehitlerin siyanür iyonu katalizörlüğündeki kondensasyon ürünleri IR ve 13C-CP-MAS NMR spektroskopisi ile karakterize edilmiş, molekül kütlesinin ve çapraz bağlanma yoğunluğunun kondensasyona etkisi incelenmiştir.
Scheidt (1964) asetaldehit, krotonaldehit ve propiyonaldehitin lityum fosfat katalizörlüğünde aldol kondensasyonunu %95 verimle gerçekleştirmiştir. Aynı reaksiyon şartlarında, fakat kalsiyum hidroksit katalizörlüğünde ise uygun olarak %40, %42 ve %18 verimler elde edilmiştir.
3. MATERYAL VE METOT
3.1. Kullanılan Kimyasal Maddeler
Deneylerde ortalama molekül ağırlığı 230.000 olan Aldrich markalı polistiren kullanılmıştır.
Süksinik anhidrit, dikloretanda kristallendirilerek saflaştırıldı ve vakumda 120
o
C ‘ de kurutulduktan sonra kullanıldı.
Glutarik anhidrit, benzende kristallendirilerek saflaştırıldı ve vakumda (50-55)
o
C ‘ de kurutulduktan sonra kullanıldı.
Propiyonik anhidrit, 155-156oC’ de franksiyonlu distilasyondan geçirilerek kullanıldı.
Strakonik anhidrit, vakumda 7 oC ‘ de kurutulduktan sonra kullanıldı. Lewis asidi olarak [BF3.O(C2H5)2] kullanıldı.
Çözücü olarak kullanılan; kloroform, toluen, benzen, çöktürücü olarak kullanılan metanol ve diğer kimyasal maddeler Merck ve Fluka firmalarından temin edilmiş olup kaynama noktalarında destillenerek kullanıldı.
Modifiye polistirenlerin kondensasyon reaksiyonu için çözücü olarak toluen, katalizör olarak %10’luk KOH (metanoldeki çözeltisi), propiyonaldehit (d = 0,801 g/mL), krotonaldehit ( d = 0,85 g/mL ), asetaldehit (d = 0,78 g/mL ), nötürleştirme için %10’ luk CH3COOH (sulu çözeltisi) kullanıldı.
3.2. Deneyde Kullanılan Cihaz ve Aletler
IR Spektrofotometresi : Perkin-Elmer spektrum 100 spektrometresi (Selçuk Üniversitesi Fen Fakültesi Kimya Bölümü-KONYA)
H-NMR Spektrofotometresi : Varian 400 MR (Selçuk Üniversitesi Fen Fakültesi Kimya Bölümü-KONYA)
Analitik terazi, ısıtıcılı sıcaklık kontrollü manyetik karıştırıcı, etüv, vakumlu etüv, cam malzeme olarak üç boyunlu balon, geri soğutucu, büret, balon jojeler, erlenler, beherler, huniler, saat camları, petri kapları, pipetler, mezürler, bagetler, termometre ve manyetik karıştırıcı kullanıldı.
3.3. Polistirenin Anhidritle Kimyasal Modifikasyonu
Polistiren optimum şartta (Okudan 1998) modifiye edildi. Buna göre; polistirenden 5.2 gram (0,05 mol) alındı ve üç boyutlu balonda 70 ml kloroformda 20
0
C de çözüldü. Üzerine 0,01 mol (polistirene göre % 20) anhidrit (glutarik anhidrit, propiyonik anhidrit, süksinik anhidrit, strakonik anhidrit) ilave edildi ve sonra çözünme tamamlanana kadar karıştırıldı. Çözülmüş polistiren ve anhidrit karışımına sıcaklık değiştirilmeden 1,26 ml (0,01 mol) damla damla [BF3.O(C2H5)2] katalizörü ilave edildi
ve 2 saat süreyle karıştırıldı. Elde edilen modifiye polistirenler metanolde çöktürüldü, vakumda 60 0C de 5 saat süreyle kurutuldu.
Polistirenin kimyasal modifikasyonunda kullanılan anhidritlere göre reaksiyonlar aşağıda gösterilmiştir.
− Polistirenin glutarik anhidrit ile modifikasyon reaksiyonu;
(3.1)
− Polistirenin strakonik anhidrit ile modifikasyon reaksiyonu;
− Polistirenin süksinik anhidrit ile modifikasyon reaksiyonu;
(3.3)
− Polistirenin propiyonik anhidrit ile modifikasyon reaksiyonu;
(3.4)
3.4. Polistirene Bağlanan Karboksil Grubu Miktarının Tayini
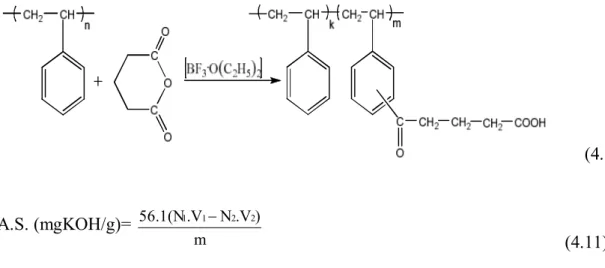
Modifiye polistirenden 1 g alınarak, yuvarlak dipli bir balonda 20 ml toluende çözüldü. Üzerine, yaklaşık 15 ml 0,1 N KOH ilave edildi. Sonra balon geri soğutucu altında kaynayan su banyosunda bir saat bekletildi. Reaksiyon fazlası KOH, sıcak olarak 0,1 N HCl ile (ff indikatörü yanında) titre edildi. Reaksiyona giren KOH miktarından, polistirene bağlanan karboksil grubu miktarı aşağıdaki gibi hesaplandı (Okudan, 1998).
A.S. (mgKOH/g) = 56,1 V1 N1- V2 N2
m
(3.5)
N1= KOH çözeltinin normalitesi.
V1= İlave edilen KOH hacmi (ml).
V2= HCl çözeltisinin normalitesi.
N2= Titrasyonda sarf olunan HCl hacmi (ml).
m = Numune miktarı (g). f = Faktör.
A.S.= Asit sayısı
%COOH Miktarı ise şu şekilde hesaplanır:
%COOH = V1 - V2 .f. 0,0045.100
m (3.6)
Propiyonik anhidrit halkalı yapıya sahip olmadığı için karboksil grubu tayini modifikasyon sırasında yapılmaktadır. Sıcaklık 20°C’ da sabit olacak şekilde katalizörün ilavesi ile başlayan reaksiyondan 0. dakikada 2 mL numune alınır ve reaksiyonu durdurmak amacıyla alınan numune 10 mL saf su bulunan erlene konulur. Reaksiyon başlangıcında polistirene bağlanan açil grubu, reaksiyon ortamında oluşan asetik asit miktarına bağlı olarak, asidin fenolftalein indikatörlüğünde 0,1N KOH ile titre edilmesiyle tayin edilir.
Katalizörün ilavesiyle numune alındıktan sonra, reaksiyonun tamamen sonlanması için 3 saat daha karıştırılır. Reaksiyon sonunda tekrar 2 mL numune alınır ve yukarıdaki yöntemle titre işlemi tekrarlanır.
Titrasyonda harcanan 0,1N KOH miktarından açillemeye giren propiyonik anhidritin mol miktarı hesaplanır:
[AA
mol] =
ΔV(ml).TKOH.(g/ml).10002.MaKOH(g/ml) (3.7)
ΔV: İki numunedeki polistirenin ihtiva ettiği asetil grubunun tayini için ortamda oluşan asetik asitlerin titrasyonuna sarf olunan 0,1N KOH miktarı (mL).
TKOH: 1 mL 0,1N KOH çözeltisinde olan KOH miktarı (g/mL).
Ma KOH : 56 g/mol
Propiyonik anhidritin başlangıç mol miktarından açillemeye giren propiyonik anhidritin % miktarı hesaplanır:
[
AA]=
nbaş.Vçöz. (3.8)
n baş : Reaksiyona giren maddelerin toplam mol miktarı
% [AAmol] =
[AAmol] x 100
[AA]o
(3.9)
[AA]o : Başlangıçtaki propiyonik anhidritin mol miktarı
[AAmol]: Açillemeye giren propiyonik anhidritin mol miktarı
Reaksiyon tamamlandığında karışım bir behere dökülür, modifiye edilmiş polimer metanolle çöktürülerek vakumlu etüvde 60°C' da 5 saat sürede kurutulur (Kaya A., 2005).
3.5. Açil Gruplu Modifiye Polistirenin Aldehitlerle Kondensasyon Reaksiyonu
Karıştırıcı, geri soğutucu, termometre ile donatılmış üç boyunlu balonda 0,1 mol modifiye açil polistiren üzerine 50 mL toluen ilave edilir ve karıştırılarak tamamen çözünmesi sağlanır. Çözeltiye 0,01 mol %10’luk KOH (metanoldeki çözeltisi) ilave edilerek karıştırılır. Daha sonra kullanılan aldehite uygun değişen sıcaklıklarda 0,033 mol aldehit (asetaldehit, krotonaldehit, propiyonaldehit) damla damla ilave edilir ve 3 saat boyunca sabit sıcaklıkta karıştırılır. Sonra 5 mL %10’luk CH3COOH (sulu
çözeltisi) ile nötrleştirildi ve polimer metanolle çöktürülerek karışımdan ayrıştırıldı (Aliyev A, İsmayilova (Kurbanlı) R., 1970, 1971; M. Kul, 2007).
Deneylerde kullanılan aldehitler; − Asetaldehit; CH3 C H O (3.10) − Propiyonaldehit (3.11) − Krotonaldehit (3.12)
Glutarik anhidrit ile modifiye edilmiş polistirenin aldehitlerle kondensasyon reaksiyonu;
(3.13)
Süksinik anhidrit ile modifiye edilmiş polistirenin aldehitlerle kondensasyon reaksiyonu;
(3.14)
Propiyonik anhidrit ile modifiye edilmiş polistirenin aldehitlerle kondensasyon reaksiyonu;
(3.15)
R; Deneyde kullanılan aldehite göre değişen, asetaldehit için -CH3, propiyonaldehit için
4. ARAŞTIRMA BULGULARI VE TARTIŞMA
Polistirenin, farklı anhidritlerle açilleşme reaksiyonu, katyonik katalizör ortamında anhidrit grubunun kırılması ile başlamaktadır. Birinci basamakta kullanılan anhidrit, Lewis asidi ile etkileşip bir kompleks oluşturmaktadır. İkinci basamakta bu kompleks polistirenle etkileşmekte, üçüncü basamakta ise BF3 ve polistirenin aromatik
halkasından bir hidrojenin ayrılmasıyla açilasyon grubu aromatik halkanın orto ve para köşesine bağlanarak açilleşmeyi gerçekleştirmektedir.
Halkalı yapıya sahip anhidritler için reaksiyon mekanizması;
(4.1)
(4.2)
(4.3)
Propiyonik anhidritle gerçekleşen reaksiyon için reaksiyon mekanizması ise;
(4,5)
(4,6)
(4,7)
Polistiren farklı anhidritlerle [BF3.O(C2H5)2] katalizörlü ortamda modifiye
edilmiştir. Modifikasyon için aşağıdaki optimum şartta çalışılmıştır (Okudan 1998). PS : MA : 1: 0,20 mol veya MA - % 20 (Polistirene göre)
[BF3.O(C2H5)2 : % 100 MA’e göre
Sıcaklık : 25 C Reaksiyon süresi : 2 saat
Polistirenin reaksiyonlarda kullanılan anhidritlerle optimum şartta modifiye edilmesi sonucu elde edilen modifiye polistirenlere bağlanan -COOH grubu miktarı titrasyon metoduyla hesaplandı. Örneğin glutarik anhidritle yapılan deneyde elde edilen 0,4939 gram modifiye polistirendeki karboksil grubu miktarının mg KOH, mg ekv KOH ve % olarak değerinin bulunması aşağıdaki gibi yapılmıştır.
A.S.(mgKOH/g) = 56,1 V1 N1- V2 N2
m (4.8)
N1 : KOH çözeltisinin normalitesi : 0,08432 N V1 : İlave edilen KOH hacmi : 15 mL N2 : HCl çözeltisinin normalitesi : 0,1016 N V2 : Titrasyonda sarf olunan HCl hacmi : 8,3 mL m : Numune miktarı : 0.4939 g
A.S. : Asit Sayısı
A.S = 56,1x(15x0,084328,3x0,1016)/0,4939 =47,8876 mg KOH/1 g polimer = 47,8876/56
= 0,855 mg ekv KOH/1 g polimer
Çizelge 4.1. Farklı anhidritler kullanılarak elde edilen modifiye polistirenlerdeki mg ekv KOH
miktarları Glutarik anhidrit Strakonik anhidrit Propiyonik anhidrit Süksinik anhidrit 0,855 0,832 0,794 0,764
% COOH gurubu miktarının bulunuşu şöyledir; %COOH= V1 - V2 .f. 0,0045.100 m (4.9) % COOH = [(15-8,3)x0,83x 0,0045 x100]/0,4939 = % 5,06
Aynı şekilde farklı anhidritleri kullanarak elde edilen modifiye polistirenlerde % COOH gurubu miktarı yukarıdaki eşitliğe göre hesaplanmıştır.
Çizelge 4.2. Farklı anhidritler kullanılarak elde edilen modifiye polistirenlerdeki % COOH
gurubu miktarları Glutarik anhidrit Strakonik anhidrit Propiyonik anhidrit Süksinik anhidrit 5,06 4,88 4,57 4,41
Yukarıda Tablo da görüldüğü gibi % COOH grubu miktarları % 5,06 ile % 4,41 arasında değişmektedir. Glutarik anhidritle yapılan modifikasyonda en yüksek verim elde edilmiştir.
Modifiye polistirene bağlanan karboksil grubunun tekrarlanan birimi (m)’in bulunuşu da şöyledir. Örneğin modifikasyonda glutarik anhidrit kullanıldığında;
(4.10) A.S. (mgKOH/g)= m ) .V N .V 56.1(N1 1 2 2 (4.11)
0.4939 g polimerde 47,8876 mg KOH varsa, 56000 mg KOH, 577,5691 g polimerde olacaktır. 577,5691 g polimerin 202 gramı fonksiyonlaşmış polistiren olduğuna göre;
577,5691-202 = 375,5691g fonksiyonlaşmamış polistiren geriye kalacaktır. Bir tek polistiren biriminin ağırlığı 104 g olduğuna göre;
375,5691/104 3,61 tekrarlanan birim değeri (m) bulunmuş olur.
Buna göre polistirendeki aromatik halkalardan yaklaşık 4 tanesinin sadece birine karboksil grubu bağlanmaktadır.
Bu da polistirene yaklaşık % 28 mol oranında karboksil grubu bağlandığını göstermektedir.
Yapılan deneylerde bulunan m değerleri ve % bağlanma miktarları aşağıdaki tablolarda gösterilmiştir.
Çizelge 4.3. Farklı anhidritler kullanılarak elde edilen modifiye polistirenlerdeki tekrarlanan
birim değerleri (m) Glutarik anhidrit Strakonik anhidrit Propiyonik anhidrit Süksinik anhidrit 3,61 3.83 4.16 4.49
Tablo görüldüğü gibi polistirene bağlanan tekrarlanan birim değeri yaklaşık 4 halkada bir olmak üzere değişmektedir. En iyi değer Glutarik Anhidritle modifiye olan polistirende olmaktadır ki bu her 4 halkadan birinde bağlanma olduğu anlamına gelmektedir. Değerler birbirine yakın olmakla birlikte en düşük bağlanma değeri süksinik anhidritte görülmektedir.
Çizelge 4.4. Farklı anhidritler kullanılarak elde edilen modifiye polistirenlerdeki % bağlanma
miktarları Glutarik anhidrit Strakonik anhidrit Propiyonik anhidrit Süksinik anhidrit 27,70 26.10 24,03 22.27
Yukarıda gösterilen tabloda polistirene bağlanan tekrarlanan birim değerine bağlı olarak polistirene bağlanan en iyi olan değer glutarik anhidritle modifiye olan polistirende % 27,70 olmaktadır. Değerler birbirine yakın olmakla birlikte bu değerin
strakonik anhidritte % 26.10, propiyonik anhidritte % 24,03, ve süksinik anhidritte % 22,27 olduğu görülmektedir.
Modifikasyon sonucu elde edilen açil polistirenler; doymuş ve doymamış alifatik aldehitlerden asetaldehit, krotonaldehit ve propiyonaldehit ile ayrı ayrı kondensasyon reaksiyonları sonucu doymamış keton gruplu polistirenler sentezlenmiştir. Kondensasyon ürünlerinin yapıları IR ve 1H-NMR spektroskopisi ile aydınlatılmıştır.
Viskozimetrik metodla yapılan ölçümlerden sonra kondensasyon ürünü olan doymamış keton gruplu polistirenlerin ortalama molekül kütleleri, Mark-Hauwink denklemine göre hesaplandı.
Molekül kütlesi 230000 g/mol olan polistirenden glutarik anhidritler ile modifiye edilen ve elde edilen açil gruplu polistirenin asetaldehitle olan kondensasyonundan elde edilen doymamış keton gruplu polistirenin ortalama molekül kütlesini hesaplayalım.
nisbi = t / to (4.12)
to = 7,47s
nisbi = 13,44 /7,47 = 1,80
Polistirenin toluendeki 25°C' daki K ve sabiti değerleri, K=1,70x10-4 ve = 0.69'dur.
[ ] = 0,6390 – 0.6390-0,6357
5
[ ] = 0,6384
*Ek-3’deki tablodan (0) ve (5) değerleri; 0,6390 ve 0,6357 olmaktadır.
Log[ ] = LogK + LogM (4.13)
LogM = (Log0,6384 + 4 - Log1.7)/0,69 M = 151605 g/mol
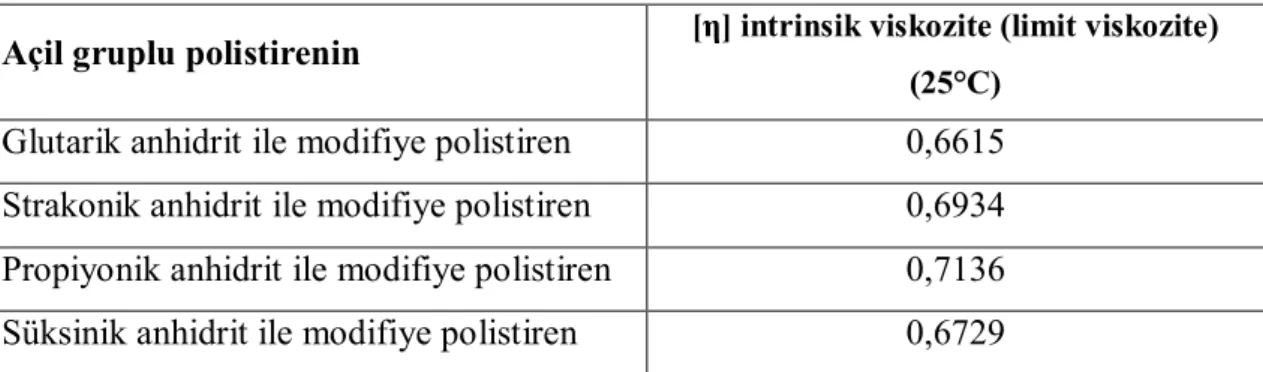
Çizelge 4.5. Açil gruplu polistirenin (polistiren molekül kütlesi 230000 g/mol) ortalama molekül
kütleleri
Açil gruplu polistirenin [η] intrinsik viskozite (limit viskozite) (25°C)
Glutarik anhidrit ile modifiye polistiren 0,6615
Strakonik anhidrit ile modifiye polistiren 0,6934
Propiyonik anhidrit ile modifiye polistiren 0,7136
Süksinik anhidrit ile modifiye polistiren 0,6729
Çizelge 4.6. Glutarik anhidrit ile modifiye edilmiş açil gruplu polistirenin (polistiren molekül
kütlesi 230000 g/mol) alifatik aldehitlerle kondensasyonundan elde edilen doymamış keton gruplu polistirenlerin ortalama molekül kütleleri
Doymamış Keton Gruplu Polistirenler [η] intrinsik viskozite (limit viskozite) (25°C)
Asetaldehitle kondensasyon ürünü 0,7384
Krotonaldehitle kondensasyon ürünü 0,6673
Propiyonaldehitle kondensasyon ürünü 0,7762
Çizelge 4.7. Propiyonik anhidrit ile modifiye edilmiş açil gruplu polistirenin (polistiren molekül
kütlesi 230000 g/mol) alifatik aldehitlerle kondensasyonundan elde edilen doymamış keton gruplu polistirenlerin ortalama molekül kütleleri
Doymamış Keton Gruplu Polistirenler [η] intrinsik viskozite (limit viskozite) (25°C)
Asetaldehitle kondensasyon ürünü 0,7931
Krotonaldehitle kondensasyon ürünü 0,7166
Propiyonaldehitle kondensasyon ürünü 0,8244
Çizelge 4.8. Süksinik anhidrit ile modifiye edilmiş açil gruplu polistirenin (polistiren molekül
kütlesi 230000 g/mol) alifatik aldehitlerle kondensasyonundan elde edilen doymamış keton gruplu polistirenlerin ortalama molekül kütleleri
Doymamış Keton Gruplu Polistirenler [η] intrinsik viskozite (limit viskozite) (25°C)
Asetaldehitle Kondensasyon Ürünü 0,8259
Krotonaldehitle Kondensasyon Ürünü 0,7568
Yukarıdaki tablolardan görüldüğü gibi kondensasyon ürünü doymamış keton gruplu polistirenlerin ortalama molekül kütlelerinde; polistirene göre azalma olmuştur.
230.000 g/mol molekül kütleli polistirenin kimyasal modifikasyon sonucu oluşan açil gruplu polistirenlerin molekül kütlelerinde önemli derecede azalma olduğu belirlenmiştir. Açil gruplu polistirenlerin molekül kütlelerindeki azalma katalizör olarak kullanılan [BF3.O(C2H5)2] lewis asidinin etkisinden kaynaklandığı düşünülmektedir.
Doymamış keton gruplu polistirenlerin ortalama molekül kütlelerinde; açil polistirenlerin ortalama molekül kütlelerine göre bir miktar artış olmuştur. Krotonaldehitin yapısındaki doymamışlıkdan dolayı krotonaldehitle elde edilen doymamış keton gruplu polistirenlerin molekül kütleleri, diğer doymamış keton gruplu polistirenlerin molekül kütlelerine göre daha düşüktür.
Kimyasal modifikasyon neticesinde elde edilen ürünlerin yapısı, hem karboksil grubunun titrasyon metotla tayini, hem IR-spektrumu hemde 1H-NMR-spektrumu ile tespit edilmiştir.
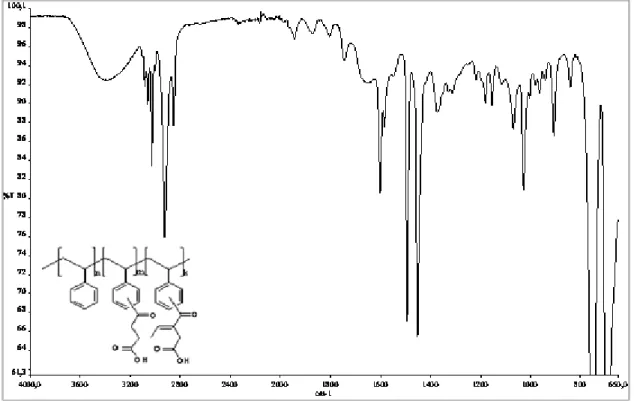
Polistirenin IR-spektrumu verilerine bakıldığında 2900-3050 cm-1 arasında polistirenin aromatik zincirindeki C–H gerilmeleri, 1601 cm-1, 1583 cm-1, 1492 cm-1 ve 1451 cm-1 gözlenen absorpsiyon bantlan aromatik halka C-C ve C=C gerilme titreşimleri, 500-900 cm-1 de ise C-H düzlem dışı eğilme titreşimleri görülmektedir.
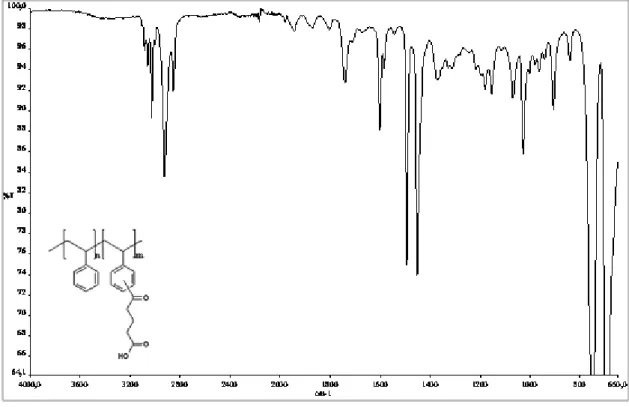
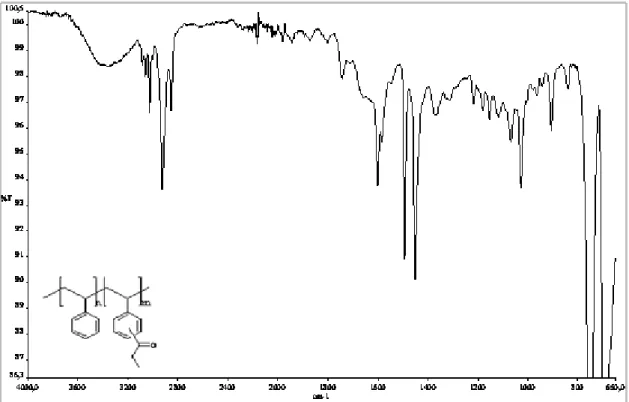
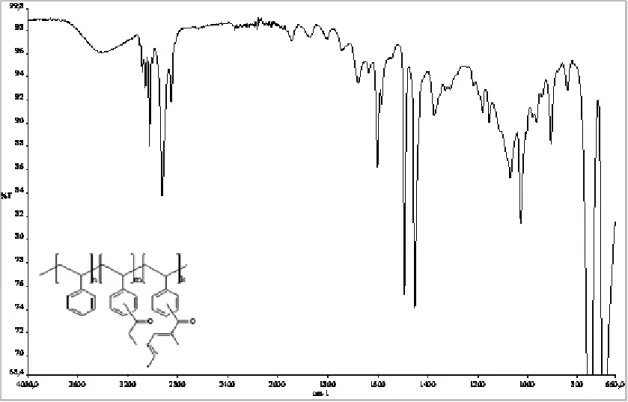
Polistirenin çeşitli anhidritle (glutarik anhidrit, strakonik anhidrit, süksinik anhidrit ve propiyonik anhidrit) modifikasyonu sonucu elde edilen modifiye polistirenin IR-spektrumu verilerine bakıldığında; Polistirenin IR-spektrumu verilerinden farklı olarak 3500 cm-1 de görülen geniş karboksil asit O-H piki, 1740 cm-1 de görülen C=O piki, 1450 cm-1 de görülen aromatik C=C piki ile örtüşen alifatik C-H düzlem içi eğilmesine ait pikler olduğu düşünülmektedir.
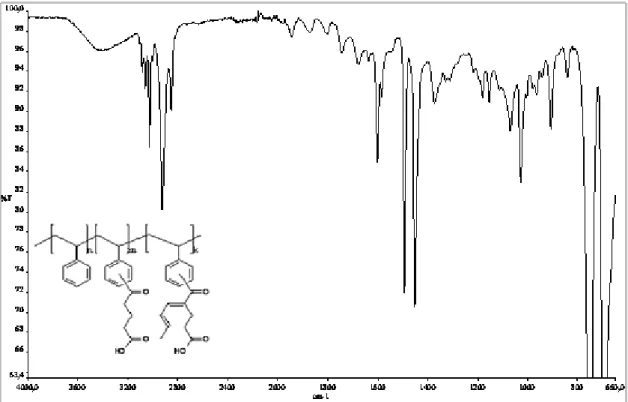
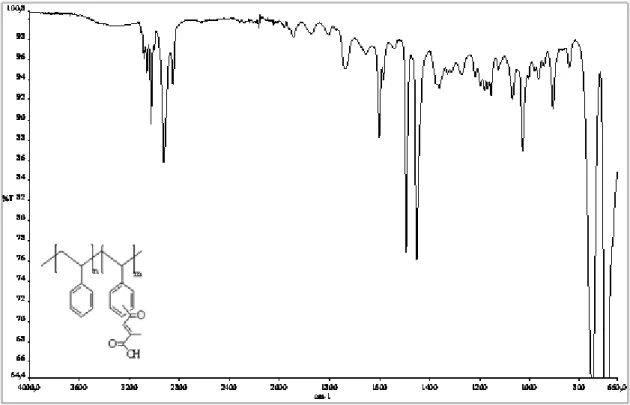
Bazı Anhidritle (glutarik anhidrit, süksinik anhidrit ve propiyonik anhidrit) modifiye edilmiş karboksil gruplu polistirenlerin IR-spektrumu verilerinden farklı olarak çeşitli aldehitlerle ile kondensasyonu sonucu elde edilen ürünlerin IR-spektrumu verilerine bakıldığında; 1637 cm-1 de görülen pikin konjuge durumundaki C=C bağından, 1218 cm-1 de görülen pikin ise alifatik C-H düzlem dışı eğilmesi kaynaklandığı düşünülmektedir.
IR-spektrumu verilerine göre hem karboksil gruplu modifiye polistirenin hemde onların kondensasyon ürünlerinin oluştuğu görülmektedir.