İÇ HASTALIKLARI ANA BİLİM DALI PROF. DR. FEHMİ AKÇİÇEK
İÇ HASTALIKLARI YOĞUN BAKIM ÜNİTESİNDE
İNTRAVENÖZ İMMÜNGLOBULİN DENEYİMİMİZ
Dr. Murat KARATEKE
İÇ HASTALIKLARI ANA BİLİM DALI TIPTA UZMANLIK TEZİ
TEZ DANIŞMANI Doç. Dr. Devrim BOZKURT
ÖNSÖZ
Uzmanlık eğitimimin başlangıcından itibaren güler yüz ve hoşgörüsüyle hep yanımda olduğunu hissettiren, daha iyi bir çalışma ortamı sunan ve deneyimleri ile eğitim hayatıma birçok katkısı olan İç Hastalıkları Ana Bilim Dalı Başkanımız Sayın Prof. Dr. Fehmi Akçiçek’e Asistanlık dönemimde ve tezimin hazırlanmasında desteklerini hiçbir zaman esirgemeyen, bilgi ve tecrübeleriyle daha üstün bir klinik bakış açısı kazanmamı sağlayan, kendisinden çok şey öğrendiğim değerli hocam ve tez danışmanım Doç. Dr. Devrim Bozkurt’a
Bilgi ve deneyimi ile tez yazım sürecimde desteklerini esirgemeyen Bilişim Teknolijileri Uzmanı Dr. Mustafa Coşkun’a
Asistanlığım boyunca birlikte çalışma olanağı bulduğum tüm uzman doktorlara ve asistan arkadaşlarıma
Bıkmadan usanmadan yardımıma koşan, her zaman sabırla yanımda olan eşim Dr. Bahar Karateke’ye ve bugünlere onlarsız gelmem mümkün olmayan aileme teşekkür ederim.
İÇİNDEKİLER
ÖNSÖZ ... 1
İÇİNDEKİLER ... 2
KISALTMALAR DİZİNİ ... 3
TABLOLAR VE ŞEKİL LİSTESİ ... 4
1.GİRİŞ VE AMAÇ ... 5
2.GENEL BİLGİLER ... 6
2.1. İntravenöz İmmünglobulin Tanımı ve Tarihçesi ... 6
2.2. İntravenöz İmmünglobulin Etki Mekanizması ... 8
2.3. İntravenöz İmmünglobulin Preparatları ve Özellikleri ... 12
2.4. İntravenöz İmmünglobulin Uygulanması ... 13
2.5. İntravenöz İmmünglobulin Tedavisinin Yan Etkileri ... 15
2.6. İntravenöz İmmünglobulin Endikasyonları ... 19
3. MATERYAL METOD ... 30 4.BULGULAR ... 32 5.TARTIŞMA ... 39 6.SONUÇ ... 46 7.ÖZET ... 48 8.KAYNAKLAR ... 49
KISALTMALAR DİZİNİ AA : Aplastik Anemi
Anti-GBM : Anti-Glomeruler Bazal Membran ANCA : Anti-Nötrofilik Sitoplazmik Antikor BDH : Bağ Doku Hastalığı
FSGS : Fokal Segmental Glomerüloskleroz GBS : Gullian Barre Sendromu
HBsAg : Hepatit B Yüzey Antijeni HBV : Hepatit B Virüsü
HCV : Hepatit C Virüsü
HLH : Hemofagositik Lenfohistiositoz HÜS : Hemolitik Üremik Sendrom IBM : International Business Machines İHA : İmmun Hemolitik Anemi
İV : İntravenöz
İVİG : İntravenöz İmmünglobülin İTP : İmmun Trombositopenik Purpura MG : Myastenia Graves
MM : Multiple Miyelom NLO : Nötrofil/Lenfosit Oranı OİHA : Otoimmün Hemolitik Anemi OTH : Ortalama Trombosit Hacmi RPGN : Rapid Progresif Glomerulonefrit SESA : Saf Eritroid Seri Aplazisi SLE : Sistemik Lupus Eritematoz
SPSS : Statistical Package For Social Sciences SUT : Sağlık Uygulama Tebliği
TGF : Transforme Growth Faktör TPD : Terapötik Plazma Değişimi vWF : von Willebrand Faktör
TABLOLAR DİZİNİ
Tablo 2.1. İVİG çalışma grubu tarafından yayınlanan kılavuz özeti………....21
Tablo 4.1. Çalışma hastalarının demografik özellikleri... 32
Tablo 4.2. İVİG uygulama endikasyonları, hasta ve mortalite sayısı ... ………33
Tablo 4.3. Çalışma hastalarının tanımlayıcı istatistik verileri………..34
Tablo 4.4. İVİG verilen tüm hastalarda mortalite prediktörlerinin tekli değişkenli analizi….35 Tablo 4.5. İVİG verilen romatolojik acil hastalarında mortalite prediktörlerinin tekli değişkenli analizi………...36
Tablo 4.6. İVİG verilen romatolojik acil hastalarında mortalite prediktörlerinin çoklu değişkenli analizi ... .37
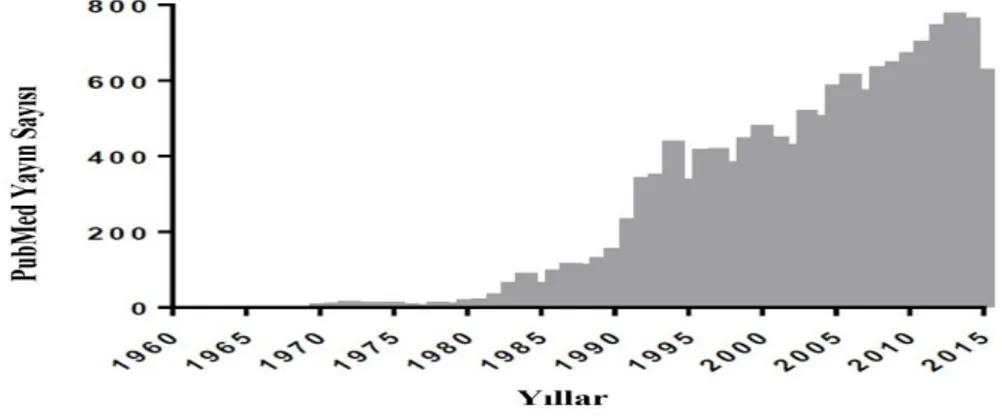
ŞEKİLLER Şekil 1: Yıllara göre İVİG üzerine PubMed üzerinden yayınlanan makale sayısı ... 9
Şekil 2: F(ab′)2 ve Fc Bağımlı Yolaklar Aracılığı ile İVİG Etki Mekanizması ... 10
Şekil 3: Doğal ve Kazanılmış Bağışıklık Üzerine İVİG Etkileri ... 11
Şekil 4: İVİG Aracılığı ile Patolojik IgG Klirensi ... 12
1. GİRİŞ VE AMAÇ
İntravenöz immünglobulin seçilmiş donör popülasyonunun plazma havuzundan elde edilmiş immünglobulin deriveleri solüsyonudur ve bu solüsyonların ilk kullanımı antikor üretim yetersizliğiyle karakterize primer ya da seçilmiş sekonder immun yetmezlik tanılı hastalarda yerine koyma amaçlı olmuştur.
İntravenöz immünglobulin preperatları günümüzde otoimmün ve inflamatuvar hastalıklarda çok geniş kullanım alanı bulmuştur. İmmün yetmezlikler dışında immün aktive klinik durumlarda da, immünmodülasyon amacıyla başarıyla kullanılmaktadır.
Yoğun bakım hastalarında immun aktive durumlar, sepsis, makrofaj aktivasyon sendromu, dirençli immün trombositopeni, immün hemolitik anemi, bağ doku hastalığı aktivasyonu ve vaskülit gibi hayatı tehdit eden patolojilerde intravenöz immünglobulin tamamlayıcı tedavi seçeneğidir. Bu hastalarda spesifik olmayan klinik belirti ve laboratuvar bulguların varlığı bir çok hastada geç tanı konulmasına ve hastanın kaybedilmesine neden olmaktadır. İmmun aktivasyon durumlarında intravenöz immünglobulin tedavisi hem aktif inflamasyonu azaltan, hem de tanıya gidişe ve spesifik tedavi verebilmeye olanak sağlayan önemli bir tedavi yöntemidir.
Bu çalışmada, İç Hastalıkları Yoğun Bakım Ünitesi’nde, 2010-2017 yılları arasında immun aktivasyon durumları nedeniyle yatırılarak, intravenöz immünglobulin uygulanan (SUT endikasyonları dahilinde) hastaların demografik verilerini, başlangıç ve sonlanım laboratuvar verilerini incelemeyi ve yoğun bakım ünitesi yatışı süresince hasta sağ kalımını etkileyen faktörleri saptamayı amaçladık.
2. GENEL BİLGİLER
2.1. İntravenöz İmmünglobulin Tanımı ve Tarihçesi
İntravenöz immünglobulin seçilmiş donör populasyonunun plazma havuzundan elde edilmiş immünglobulin deriveleri solüsyonudur. İntravenöz immünglobulin binlerce sağlıklı vericiden sağlanan plazmaların havuzlanması ile elde edilen normal insan poliklonal immün globülin G nin tedavi edici preparatıdır. Ig G yanında Ig A, Ig M, Ig G F(ab)2 parçaları, solübl CD4, CD8 ve TGFβ içerir. Çok sayıda donörden hazırlanması nedeniyle donörlerin doğal infeksiyon ve immunizasyon ile oluşmuş çok çeşitli tipteki antikorlarını içerirler[1, 2].
Kullanımda olan intravenöz immünglobulin preparatları, IgA ve IgG subgrupları yönünden aralarında minör farklılıklar içerirler. Ticari bir intravenöz immünglobulin preparatı % 95 ve üzeri IgG, % 2.5’dan az IgA ve IgM içerir. IgG subgrupları ise donör havuzunun içeriğine göre; IgG1 % 55-70, IgG2 % 30-38, IgG3 % 0-6, IgG4 % 0.7 - 2.6 şeklinde değişen oranlarda bulunur. İntravenöz immuünglobulin içerisinde bulunan IgA ve IgM’ in yarılanma ömrü kısa olduğu için tedavi edici değildir.
Klinik geçmişi, 17.yüzyılda Lower ve King’in pis kanın, sağlıklı bir vücuttan alınan iyi kan ile temizlenmesi’ düşüncesinden ilham alarak transfüzyon denemelerine dayanmaktadır. 1889 von Behring ve Kitasato, tetanoz hastalığına karşı bağışıklanan tavşandan alınan kanın, bağışıklanmayan tavşana verilerek tavşanı hastalıktan koruduğunu göstermişlerdir[3]. İkinci Dünya Savaşı esnasında Cohn ve arkadaşları antikordan zenginleştirilmiş, kızamık ve hepatit A’dan koruyan ve kas içine uygulanabilen immünoglobulin preperatı geliştirmişlerdir. Bruton, 1952 yılında ilk kez agammaglobulinemisi olan hastaları belirledikden sonra, bu hastalara Cohn ve arkadaşlarının geliştirdiği immünoglobulini kas içine uyguladığında yararlı sonuçlar elde etmiş ancak damar içine verilince anaflaksi yaptığını gözlemlemiştir[3]. İlk başta primer ve sekonder immün yetmezliklerde yerine koyma tedavisi olarak kullanım alanı bulmuşken günümüzde birçok otoimmün ve sistemik inflamatuar hastalığın tedavisinde de yaygın olarak kullanılmaktadır. Kalıtsal immün yetmezliği ve trombositopenisi olan bir hastada intravenöz immünglobulin kullanımı sırasında trombosit sayısının artışının Imbach ve ark. tarafından gözlenmesinden sonra yüksek doz intravenöz immünglobulin tedavisi otoimmün hastalıklarda kullanım alanına girmiştir[4]. İmmünglobulinin kas içine kullanım zorlukları ve yan etkilerinin olması nedeniyle 1981 de damar içine uygulanabilen solüsyonun kullanıma girmesine neden olmuştur. Ayrıca son 10 yılda Avrupa’da infüzyon pompası aracılığı ile cilt altına uygulanabilen, %16’lık preparatlar geliştirilmiş ve uygulanmaktadır [5].
İntravenöz immünglobulin üretim aşamasında plazma iki yoldan elde edilir[6]; • %20 oranında kan vericileri
• %80 plazma vericilerinden plazmaferez ile
İntravenöz immünglobulin preperatları hazırlanma sürecinde sırası ile şu işlemlere tabi tutulur; • Agregatlar, ultasantrifüj veya jel filtrasyon yöntemi ile fiziksel olarak uzaklaştırılır. • Proteolitik enzimler ile işleme tabii tutulur.
• Kimyasal olarak sülfidril bağları azaltılır, daha sonra serbest kalan disulfid bağların alkalizasyonu sağlanır.
• Stabilizan ajan olarak disakkaridler eklenir. • Düşük PH’ da inkübasyon yapılır.
Stabilizatör olarak glukoz, maltoz, glisin, sükroz, mannitol veya albumin kullanılır. Plazma osmolaritesinin 280-296 mOsm/L olmasına karşın intravenöz immünglobulin preperatlarının konsatrasyonları 1000 mOsm/L’yi geçebilmektedir. Bu hiperosmolar olan sıvı aşırı sıvı şiftine yol açarak sonrasında hemodinamik değişikliklere neden olabilmektedir.
İntravenöz immünglobulin solüsyonlarının dayanıklı kalabilmeleri için pH’nın 4-4.5 düzeylerinde olması gerekmektedir. Bu pH düzeyinde agregatlar sınırlanmış halde stabilizatöre ihtiyaç duymamalarına karşın fizyolojik pH’a gelindiğinde aktifleşmektedirler. Stabilizatör olarak kullanılacak maddelerinde ek yan etkileri oluşturmaları mümkündür. Örneğin İVİG solüsyonları içindeki sükroz ve stabilizer maddeler renal fonksiyonların bozulmasına yol açabilmektedir. İntravenöz immünglobulinin ortalama yarı ömrü üç haftadır[7].
Kan yolu ile kontaminasyona yol açan patojenlerin eliminasyonu için bir dizi işlem uygulanması gerekmektedir. Solvent/deterjant veya pastörizasyon ile viral inaktivasyon sağlanarak son ürün HBV, HCV ve HIV’den arındırılmaktadır. Solvent/Deterjan (S/D) ile zarflı virüslerin lipid tabakası parçalanır, pH 4 uygulaması ile zarfsız virüslerden arınma(non-lipid ve bazı lipid membranlı virusler), kromatografik yöntem ile virus inaktivasyonu yapılır. Pastörizasyon işlemi; 10 saat 60°C de ısıtılıp stabilize etmek için aminoasit, sitrat, şeker eklenerek sağlanır. Kuru ürünlerin 68°C ısıtılması ile HIV inaktive edilir. Thiomersol eklenen veya içermeyen steril %16,5 lik (165 mg/ml) solüsyon tüm bu işlemler sonucunda kullanıma hazır hale gelir[8].
DSÖ tarafından belirlenen ideal intravenöz immünglobulin preperatında bulunması gereken nitelikler şöyledir[6, 9];
• Ürün en az 1000 vericiden elde edilmiş olmalıdır • Yarılanma ömrü 20 günden fazla olmalıdır
• Monomerik IgG düzeyi %90 nın üzerinde olmalıdır
• IgG altgrup dağılımı sağlıklı bireylerde ki oranlara uymalıdır (IgG1:% 60, IgG2:% 29.4, IgG3:% 6.5, IgG4:% 4.1.)
• Fc işlevleri eksiksiz olmalıdır (Kompleman bağlama, opsonizasyon gibi)
• Pirojen, aggregat, vazoaktif madde, prekallikrein aktivatörü, kinin, plazmin içermemelidir
• Yan etkisi az olmalıdır
• Minimal IgA ve IgM içermelidir
• Steril olmalıdır; HIV 1/2 antikorları, HBsAg, HCV antikorları taranmış olmalıdır • Ucuz olmalıdır
2.2. İntravenöz İmmünglobulinin Etki Mekanizması
Yüksek maliyet ve arz sıkıntısı göz önüne alındığında, olası bir intravenöz immünglobulin yerine geçebilecek molekülün geliştirilmesi sağlık ekonomisi üzerinde ciddi büyük bir etkiye sahip olacaktır. Yaygın kullanımı ve yaygın etkinliğine rağmen, özellikle otoimmün ve inflamatuar hastalık durumlarında etkili olan immünmodülatör mekanizmalar halen iyi anlaşılamamıştır.
Yeni, daha güvenli, daha etkili ve düşük maliyetli İVİG benzeri anti-inflamatuar tedavilerin geliştirilmesi amacıyla İVİG etki mekanizması araştırmacıların ilgi odağı olmuştur. Şekil 1 de pubmed taramalarında yapılan incelemede son 10 yılda İVİG üzerine yayın sayısının iki kat arttığı ve sadece 2015 yılında 613 tane yayın yapıldığı görülmektedir.
Şekil 1: Yıllara göre İVİG üzerine PubMed üzerinden yayınlanan makale sayısı
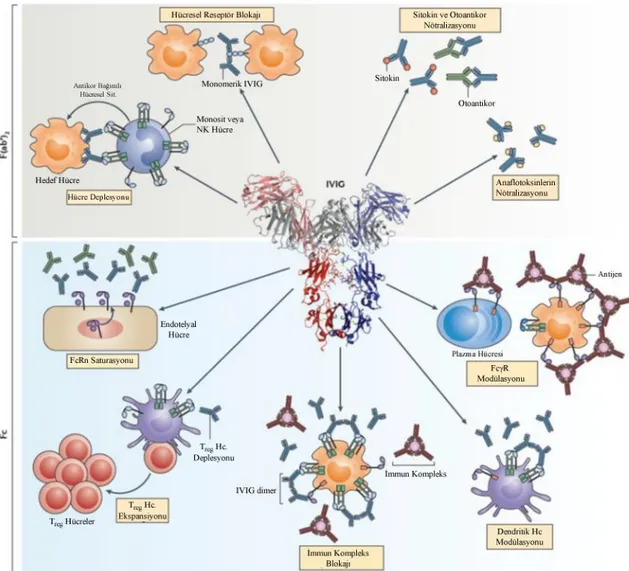
İntravenöz immünglobulinin karmaşık etki mekanızması mevcuttur. İnfeksiyonlara karşı yerine koyma tedavisi ile koruma ve Rh uyuşmazlığında yararlanılan alloimmunizasyon etkisi dışında bu çalışmanın esas konusu anti-inflamatuvar ve immünmodülatör etkileridir. Bu bağlamda immünmodülatör etkisini antikorun hem Fab hem de Fc reseptörleri üzerinden gerçekleştirdiğine dair kanıtlar mevcuttur ve bu etkiler şekil 2 de özetlenmiştir.
Anti-inflamatuar ve immünmodulatör etki
• Dalak ve karaciğerde bulunan fagositer hücrelerin Fc reseptörleri ile etkileşime girer. İmmün trombositopenide bu etki ile otoantikor kaplı trombositler retiküloendotelyal sistemden korunur[4].
• Dendritik hücrelerin farklılaşma ve olgunlaşma sürecini inhibe eder[10].
• Periferik kanda bulunan monositleri (pro inflamatuvar alt kümelerinin-CD 14+/CD16++) baskılar[11].
• Spesifik antikorlar sayesinde periferik dolaşımda bulunan sitokinleri nötralize eder. • Vasküler endotele bağlanan lökosit adhezyon molekülünü bloke eder. Orak hücre
hastalığına ait bir fare modelinde IVIG, lökositlerin vasküler endotele bağlanmasını önleyerek vazo-oklüsif krizi tersine çevirerek kan akışını arttırdığı gösterilmiştir[12]. • Anti-Fas antikorları ile Fas ligand aracılı apoptozu engeller. Toksik epidermal
nekroliziste bu etkisinin ön planda olduğu düşünülmektedir[13].
• Efektör makrofajlar üzerinde bulunan inhibitör etkili Fc Gamma RIIB reseptörlerini indüklerler. Yüksek doz intravenöz immünglobulin ile tedavi edilen kronik inflamatuvar demiyelinizan polinöropati hastalarının monositlerinde Fc-gamma-RIIB reseptörünün upregülasyonu gösterilmiştir[14].
Şekil 2: F(ab′)2 ve Fc Bağımlı Yolaklar Aracılığı ile İVİG Etki Mekanizması
• Anti-idiotipik antikorları ihtiva eder. Bu anti-idiotipik antikorlar dolaşımda bulunan otoantikorlara ve B hücre immünglobulin reseptörlerine bağlanır. Bu bağlanma sonrası otoantikorların klirensi artar aynı zamanda B hücre aracılı antikor üretimi azaltılır. • Mikrobiyal toksinlere karşı nötralizasyon sağlar. Stafilokok toksik şok sendromu ve
şiddetli grup A streptokok enfeksiyonunda nötralize edici antikorlar stafilokok toksini ve streptokok süper antijenlerine bağlanır. Bu da sitokin salınımını baskılar[15, 16]. • Kompleman sistem üzerine etkileri birden fazladır. İmmün kompleks depozitlerinin
solubulizasyonu ve klirensi sağlar, aktifleşmiş kompleman sistem komponentlerinin(c4b, MAC vb.) hedef dokulara bağlanmasını engeller[17]. Kompleman komponentlerinden C3b proteini için alternatif bağlanma alanı oluşturur
ve kompleman sistem aktivasyonunu yavaşlatır. Yine C3a ve C5a gibi anaflatojenik vasıflı kompleman fragmanlarını nötralize edebilir[18].
• T regülatuvar hücrelerin (CD4+CD25+FoxP3+ Tregs) artışını teşvik eder ve
Proinflamatuvar Th17 yolağı inhibe eder[19]. İVİG’in doğal ve kazanılmış bağışıklık üzerine olan tüm etkileri şekil 3’te özetlenmiştir.
Şekil 3: Doğal ve Kazanılmış Bağışıklık Üzerine İVİG Etkileri
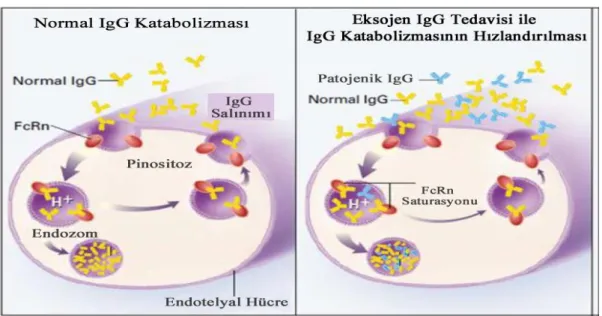
• Vasküler endotelyal sistemde bulunan FcRn reseptörlerinin saturasyonunu sağlar. Bu reseptörler sature olduğunda patolojik Ig G lerin klirensi hızlanır[20].
Şekil 4: İVİG Aracılığı ile Patolojik IgG Klirensi
2.3. İntravenöz İmmünglobulin Preparatları ve Özellikleri
Mevcut kullanımda olan intravenöz immünglobulin preparatlarının genel olarak çeşitli immün yetmezlik ve otoimmün/inflamatuvar hastalıkların tedavisinde eşit derecede etkili olduğuna inanılmaktadır. Bununla birlikte, preparatlar üretim teknikleri, formulasyon, hacim yükü, osmolarite, sodyum içeriği, şeker içeriği, ph değeri, Ig A içeriği, saklama koşulları, raf ömrü gibi konularda birbirlerinden farklılık gösterebilir ve bu farklılıklar bir takım hastalık gruplarında klinik önem arz etmektedir.
• Formülasyon: Ürünler sıvı veya liyofilize formda üretilebilir. Liyofilize ürünlerin derişim % 3-12, sıvı ürünlerin derişimi ise % 5-10 şeklindedir. Liyofilize ürünlerde yan etki görülme sıklığı daha fazladır. Bu durum seyrelticinin tipine (SF, dekstrozlu sıvı, distile su), hazırlanma biçimine, yüksek osmolariteye ve karıştırma esnasında protein denatürasyonuna bağlı olabilir.
• Hacim yükü: Ürünlerin toplam sıvı miktarı özellikle kardiyak ve nefrolojik ek komorbiditleri olan yaşlı hastalarda önemlidir. Bu durumlarda yüksek derişimli, daha az sıvı miktarı içeren ürün kullanılmalıdır[21].
• Sodyum ve albümin miktarı: Yine artmış intravaskuler hacmi tolere edemeyen hastalarda düşük sodyum ve albümin içeriği olan ürünlerin tercih edilmesi önemlidir.
• Şeker içeriği: Stabilizasyon amacı ile kullanılan şeker içeriği bir takım hastalıklarda yan etki sıklığını artırır. Örneğin osmotik renal hasarı artırması nedeni ile zeminde böbrek yetersizliği olan hastalarda sukroz içeren ürünlerin kullanımı önerilmemektedir[22]. Bazı şeker ölçü cihazları maltoz ve glukoz ayrımını yapamadığı için diyabetik hastalarda maltoz içeren ürünlere dikkat edilmelidir. Aynı şekilde hiperglisemi kliniği açısından yakın takip edilmelidir[21].
• Osmolarite: Ürünün şeker ve sodyum içeriği osmolariteyi belirler. Hiperosmolar çözeltilerde özellikle immobil hastalarda, kriyoglobulinemi tanılı hastalarda, monoklonal gamopati saptanan hastalarda, artmış lipoprotein düzeyi saptanan hastalarda tromboembolik olay sıklığı artmıştır. Bununla birlikte son zamanlarda artmış tromboembolik olay sıklığından ürünlerin içerisinde bulunan aktif faktör 11a sorumlu tutulmaktadır[23].
• Ig A içeriği: Selektif Ig A eksikliği ve anti- Ig A varlığında anaflaksi riski nedeni ile ürün içerisinde bulunan Ig A düzeyi önem arz etmektedir[24].
Çoğu hasta preparatların büyük çoğunluğunu tolere etse dahi iyi tolere edilen bir ürün kullanıldığı zaman, zorlayıcı bir sebep olmadıkça ürünlerin değiştirilmemesi önerilmektedir. Alternatif ürünlerin uygulanması sadece klinisyenin onayı ile yapılmalıdır[25].
2.4. İntravenöz İmmünglobulin Uygulanması
Ürünler 2-8℃ arası sıcaklıkta buzdolabında saklanmalıdır. Kesinlikle dondurulmamalıdır. Yan etki sıklığını azaltmak için buzdolabında saklanan ürünlerin hastaya verilmeden önce oda sıcaklığına ulaşması beklenmelidir. Bu aşamayı hızlandırmak için herhangi bir mikrodalga fırın veya başka ısıtıcı kesinlikle kullanılmamalıdır. Yapılması durumunda ürün içerisinde bulunan proteinlerin denatürasyonuna yol açacaktır. Aşırı köpürmeye neden olan şiddetli karıştırmadan kaçınılmalıdır. Ürünün tamamen çözündüğünden ve çözeltinin homojen olduğundan emin olmak için, yeniden doyurulmuş liyofilize ürünler ilaç vermeden önce kontrol edilmelidir. Tüm ürünler uygulamadan önce partikülasyon gelişimi ve kutunun bütünlüğü açısından özenle incelenmelidir. Partiküler yapıda olan ve flakon bütünlüğü bozuk olan ürünler kullanılmamalıdır.
Uygulama öncesi hastaya tedavi ve yan etkileri hakkında ayrıntılı bir şekilde bilgi verilmeli ve kan ürünü replasmanı onam formu imzalatılmalıdır. Hastaya verilecek ürünün
ticari ismi/üretici firma ismi, dozu, parti numarası ve son kullanma tarihi hasta dosyasına kaydedilmelidir.
İnfüzyon tedavisine başlamadan önce hastanın vital bulguları kontrol edilip kaydedilmelidir. Olası yan etkiler açısından gerekli tıbbi malzeme ve ilaçlar hazırda bekletilmelidir.
Tedavi öncesi tam kan sayımı, hepatik transaminazlar, kreatinin, kan şekeri ve tam idrar tetkiki testlerinin yapılması önerilmektedir. Bu basamak uygulama öncesi komplikasyon riskini tahmin etme ve mevcut olan bir enfeksiyonun belirlenmesinde önemlidir.
Birçok hastada premedikasyon gerekli değildir. Premedikasyon kararı daha önceki uygulamalarda reaksiyon öyküsü, ürünün özellikleri ve uygulama yöntemi, hastanın genel durumu(aktif infeksiyon gibi) değerlendirilerek karar verilir[26]. Premedikasyon kararı verilirse infüzyondan 30 dakika önce uygulanmalıdır. Premedikasyon amacı ile parasetamol 650-1000 mg po./ibuprofen 400-800 mg po. ve difenhidramin 25-50 mg iv/im/po uygulanabilir. Daha önce ki infüzyonlarda baş ağrısı gibi yan etkiler yaşayan veya ciddi yan etki nedeni ile ürün değişimi yapılan hastalarda premedikasyon tedavisine glukokortikoidler(metil-prednizolon 40-60 mg po/iv gibi) eklenebilir.
Premedikasyonun yanında belli hasta gruplarında prehidrasyonda önemlidir. Tedavi öncesi yeterli hidrasyon özellikle kronik böbrek yetmezliği, diabetes mellitus, paraproteinemi, nefrotoksik ajanlar ile birlikte kullanılan durumlar, koagülopatinin eşlik ettiği durumlarda tromboz ve nefrotoksisite gelişme riskini azaltmak için önemlidir. Yüksek doz intravenöz immünglobulin verilecek hastalara 10-20 ml/kg normal salin ile prehidrasyon önerilir. Böylelikle hiperviskosite ve sukroz ilişkili osmotik renal hasar için koruma sağlanmış olur[27]. Bakteriyel infeksiyon şüphesi olan hastalara aşırı inflamatuar reaksiyon riskini azaltmak için intravenöz immünglobulin infüzyonundan önce antibiyotik tedavisi başlanmalıdır.
Geçirilmiş tromboembolik hadise öyküsü olan ve tromboemboli geçirme riski yüksek hastalarda prehidrasyon, düşük osmolaliteli ürünlerin kullanımı, proflaktik antiplatelet ajan kullanımı ve immobilizasyonun önlenmesi dikkat edilmesi gereken konulardır.
Akut böbrek yetmezliği olan ve gelişmesi açısından yüksek riskli hastalarda kontrollü hidrasyon yapılması, sükroz içeren ürünlerden kaçınılması, % 5’ten daha yoğun ürünlerin tercih edilmemesi, yüksek doz tedavi planlanan hastalarda(özellikle yaşlı hastalarda) toplam dozun bölünerek farklı günlerde verilmesi özellikle dikkat edilmesi gereken konulardır. Normal
böbrek fonksiyonu olan bireylerde sükroz içeren ürün kullanılıyorsa saatlik sükroz infuzyonu 3 mg/kg’dan fazla olmamalıdır.
Uygulama ile ilişkili bir diğer konu ise infüzyon hızı ve infüzyon esnasında ki yakın klinik takiptir. İnfüzyon ilişkili yan etkiler incelendiğinde bunların önemli bir kısmının uygulama hızı ile ilişkili olduğu görülmüştür. Bu nedenle infüzyonu dakikada % 0.01 ml / kg gibi yavaş bir hızda başlatmak doğru olandır. İnfüzyon hızı klinik ve vital bulguların takibinde bir problem yoksa 20-30 dakikalık aralıklar ile iki katına çıkarılabilir. Maksimum 0,08 ml/kg/dk infüzyon hızı uygundur.
Tedavi doz planı intravenöz immünglobulinin klinikte hangi amaçla kullanıldığı ile ilişkilidir. İmmün yetmezlik durumlarında 400-800 mg/kg/ay şeklinde yerine koyma tedavisi yapılır[28]. Hasta klinik takibine göre doz modifikasyonu yapılabilir. Anti inflamatuvar ve immümmodülasyon amacı ile kullanılan durumlarda genellikle 1 gr/kg gibi yüksek doz intravenöz immünglobulin uygulanmalıdır[29, 30]. Obez ve morbid obez hastalarda ideal doz aralığı hakkında yeterli kanıt bulunmamaktadır.
2.5. İntravenöz İmmünglobulin Tedavisinin Yan Etkileri
Tüm intravenöz immünglobulin reaksiyonlarının % 5-15 i kadarında ilaç yan etkilerin gözlendiği ve bu tablonun intravenöz immünglobulin tedavisi alan bireylerin % 20-50’ sinin etkilediği bildirilmektedir[31]. Düzenli program içinde intravenöz immünglobulin alan hastalarda yan etkiler nadirdir. Bu reaksiyonların çoğu baş ağrısı, titreme veya ciltte kızarıklık gibi hafif, geçici ve geri döndürülebilir reaksiyonlardır[24, 26]. Ciddi reaksiyonlar hastaların % 2-6’ sında ortaya çıkar[32].
Yan etki sıklığı infüzyon hızı, verilen doz miktarı ve kullanılan ürünün formülasyonu ile yakından ilişkilidir. Bilinen yan etkilerin çoğu ilk infüzyon esnasında veya ürün değişimi sonrası yeni ürünün ilk infüzyonunda görülmektedir[33]. Yan etki görülme sıklığını etkiyeleyen bir diğer faktör ise ek klinik durumların varlığıdır[26]. Eşlik eden koroner arter hastalığı, hipertansiyon, sigara, hiperlipidemi, diabetes mellitus, 65 yaş üzeri olmak, sepsis, immobilizasyon, östrojen veya nefrotoksik ajanların eş zamanlı kullanımı, hipervizkosite durumları, eşlik eden organ disfonksiyonları, hiperkoagulobiliteye yol açan nedenler ek risk faktörleri için örnek gösterilebilir[31, 34, 35].
İntravenöz immünglobulin tedavisine karşı gelişen reaksiyonlar şiddetine, organ/sistem tutulumuna, gelişme mekanizmasına ve başladığı zamana göre sınıflandırılabilir.
• Şiddet: İntravenöz immünglobuline karşı gelişen yan etkilerin çoğu hafif ve geçicidir. Anafilaksi, miyokardiyal ve serebral iskemi, akut böbrek yetmezliği, aseptik menenjit, ciddi hemoliz ve tromboembolik hadiseler şiddetli reaksiyonlara örnek gösterilebilir. • Organ/Sistem: Özellikle şiddetli reaksiyonlar sonucunda kardiyovaskuler sistem,
respiratuvar sistem, renal sistem, kütanöz dokular, hematopoietik sistem ve santral sinir sistemi ile ilgili klinik durumlar ortaya çıkabilir.
• Mekanizma: İntravenöz immünglobulin tedavisine karşı gelişen reaksiyonların temelini üründeki immün komponentlere(immün kompleks, koagülasyon faktörleri vb.) karşı gelişen immun yanıt(kompleman aktivasyonu gibi) oluşturmaktadır. Daha nadir olmakla birlikte özgül antikor spesifitesi(kan grubu antijenlerine karşı gelişen antikorlar sonucu hemoliz gibi), ürün içerisinde bulunan faktör 11a gibi Ig G dışı proteinlerin varlığı, sükroz gibi yardımcı maddelerin varlığı ve infuzyon esnasında aşırı sıvı yüklenmesi gibi nedenlerde reaksiyonların gelişmesinde rol almaktadır[31].
• Başlangıç zamanı:
Hızlı başlayan yan etkiler: İnfüzyon esnasında veya tedavi sonrası 6 saat içerisinde gerçekleşen reaksiyonlardır. Tüm reaksiyonların % 60 ını hızlı başlayan reaksiyonlar oluşturur[31]. Uygulama alanında ağrı/şişlik/kızarıklık, ateş, titreme, yüzde kızarıklık, baş ağrısı, bulantı, kusma, anksiyete, yorgunluk, artralji, miyalji, hipo/hipertansiyon gibi belirti ve bulgular sık görülen hızlı reaksiyonlara örnektir. Anafilaksi ve benzeri klinik tablo, transfüzyon ilişkili akciğer hasarı, transfer ilişkili hipervolemi daha nadir gözlenen fakat daha şiddetli seyreden reaksiyonlara örnek gösterilebilir.
Gecikmiş yan etkiler: İnfüzyon sonrası günler içerisinde gelişen reaksiyonlardır. Bu reaksiyonları sistem tutulumuna göre 4 alt başlıkta toplamak mümkündür.
Tromboembolik olaylar: Erken veya geç dönemde görülebilir. Görülme sıklığı serilerde % 0,3-0,8 olarak belirtilmiştir[36]. Tedavi sonrası ortaya çıkan tromboz riskinden kan vizkositesinin artması, eritrosit agregasyonuna neden olması, platelet aktivasyonunu uyarması, faktör 11a nın Ig G ile ko-pürifiye olması sorumlu tutulmaktadır[31]. Trombofili öyküsü, yüksek doz ve hızlı infüzyon uygulanması ve ek komorbiditelerin varlığı tromboz riskini artıran faktörlerdir. Arteriyal veya venöz trombozlar olabilir fakat tüm tromboembolik hadiselerin %80’nini arteriyal trombozlar oluşturmaktadır. Akut koroner sendrom, geçici iskemik atak, ciddi
serebro vasküler olay, derin ven trombozu, pulmoner emboli ve infuzyon alanında tromboz gelişebilir[35, 37-40]. Arteriyal trombozlar sıklıkla tedavi günü ve sonraki gün gerçekleşir. Venöz trombozlar ise sıklıkla sonraki gün ve haftalarda meydana gelir[31].
Santral sinir sistemi yan etkileri: Uzamış baş ağrısı, migren atak gelişimi, aseptik menenjit, serebrovasküler olay gibi nörolojik tablolara yol açabilir[41].
Renovasküler sistem yan etkileri: Akut böbrek yetmezliği ve hiponatremi önemli yan etkileridir. Bu açıdan öncesinde var olan kronik böbrek yetmezliği, diabetes mellitus, dehidratasyon, 65 yaş üzeri olmak, sepsis varlığı, paraproteinemi(hiperviskosite) ve nefrotoksik ajanların birlikte kullanılıyor olması önemli risk faktörleridir. Akut böbrek yetmezliği % 1 den daha az meydana gelir [42]. Klinik tablo asemptomatik kreatinin yüksekliğinden anürik böbrek yetmezliğine kadar değişiklik gösterebilir. Tedavi sonrası sıklıkla 4-10 gün içerisinde spontan iyileşme gözlenir fakat kalıcı böbrek yetmezliği vakalarıda bildirilmiştir[42]. Akut böbrek yetmezliğinden esas olarak sükroz içeren ürünler(osmotik nefrozis aracılı) sorumlu tutulmaktadır[43]. Bilinen kronik böbrek yetmezliği veya tedavi sonrası gelişen böbrek yetmezliği olan hastalarda intravenöz immünglobulin içerisinde bulunan sükroz, maltoz, proteinler ile ilişkili olarak hiperozmolar veya izoozmolar(psödohiponatremi) hiponatremi gelişebilir[44, 45]. Hematolojik sistem yan etkileri: İntravenöz immünglobulin tedavisi sonrası
hemolitik anemi gelişebilir[24, 46, 47]. Ürün içerisinde bulunan ve izoaglutinin olarak adlandırılan antikorların kan grubu antijenlerine bağlanması ile ilişkili olduğu düşünülmektedir. İntravasküler hemoliz ile uyumlu klinik ve laboratuvar bulguları saptanır. Direkt antiglobulin testi pozitifliği saptanabilir. Hemoliz açısından en önemli risk faktörleri hızlı infüzyon yapılması, yüksek doz tedavi uygulanması, kadın cinsiyet olmak ve O kan grubu dışında kan grubuna sahip olmaktır.[48]. Hemoliz riski yüksek hastalarda yavaş infüzyon yapılması, toplam dozun parçalanması, doz azaltılması, ürün değişimi alınacak önlemler arasındadır[49]. Kan ürünü replasmanı gerektirecek kadar hemolizi olan hastalarda O kan grubu ürünlerin kullanımı önerilir[49].Tedavi sonrası nötropeni gelişebilir. Gelişiminde ürün içerisinde bulunan antikor veya kompleman komponentlerinin nötrofil marjinasyonuna yol açması ve sialik asit bağlayıcı Ig benzeri lektin 9 olarak adlandırılan anti nötrofil antikorunun immun klirensi indüklemesi sorumlu tutulmaktadır[50]. Sıklıkla geçicidir ve girişim gerektirmez[51]. İnfeksiyon
varlığında ve beraberinde gelişen transfüzyon ilişkili akut akciğer hasarında dikkatli olunmalıdır.
Geç yan etkiler: Tedavi sonrası haftalar ve aylar sonra ortaya çıkan reaksiyonlar üç alt başlık halinde incelenebilir.
Dermatolojik sistem yan etkileri: Tedavi sonrası izlemde haftalar içerisinde egzematöz dermatit(özellikle palmar ve plantar bölgede) gelişebilir[52]. Tedavi ilişkili geç dönemde gelişen alopesi ve eritema multiforme vakalarıda raporlanmıştır[31].
Aşı etkinliğinin bozulması: İntravenöz immünglobulin tedavisi kızamık, kızamıkçık ve kabakulak gibi canlı aşılara verilen yanıtın bozulmasına neden olabilir, bu yüzden zamanlamasına dikkat edilmelidir.
İnfeksiyon bulaş riski: Günümüz intravenöz immünglobulin preparatlarının üreticileri, beklenmedik potansiyel infeksiyöz ajanların bulaşma riskini azaltmak için çok yönlü bir strateji uygulamaktadır. Bu strateji, uygun dönor seçimi ile başlar ve bulaşıcı hastalık risk faktörlerinin belirlenmesi için sınırlı bir fizik muayene ve bir anketin doldurulmasını, donörlerin HIV 1, HIV 2, hepatit B, hepatit C testlerinden geçirilmesini, virüsler için plazma havuzu testini ve üretimde kararlı viral inaktivasyon/azaltma adımlarının hayata geçirilmesini içerir. 1994 yılında hepatit C bulaşı olan 112 vaka bildirilmiştir[53]. Bu sarsıcı deneyimden sonra ruhsatlandırılmış intravenöz immünglobulin ürünlerine hepatit C gibi zarflı virüslerin taşınmasını/geçişini azaltmak amacıyla solvent/deterjan uygulaması geliştirilmiştir[54]. Pastörizasyon, düşük pH’da inkübasyon, hidrolaz nanofiltrasyon diğer inaktivasyon/redüksiyon metodlarıdır. Alınan tüm önlemlere rağmen intravenöz immünglobulin preperatları daha tanımlanmamış olanlar dahil infeksiyon ajanları içerebilir. Ürünler enfeksiyöz ajanlardan tamamen arındırılamayabilir. Bu yüzden preparatların üzerinde “ Bu ürün insan kanından üretildiği için, virüsler, Creutzfeld Jacob hastalığı ajanı gibi enfeksiyöz ajanların bulaşı açısından risk taşımaktadır.” şeklinde bir ibare bulunmaktadır.
Laboratuvar değişiklikleri: Tedavi sonrası birtakım laboratuvar anormallikleri saptanabilir. Semptomatik olmayan hastalarda bu değişikliklerin hemen hepsi klinik açıdan önemli değildir. Bununla beraber öngörülen bu değişikliklerin iyi bilinmesi kapsamlı bir değerlendirme ve ek girişimlerden kaçınılması açısından önemlidir.
o Vizkosite artışı ile ilişkili olarak eritrosit sedimantasyon hızında artış olabilir[55].
o Plazmanın su dışı komponent oranını (protein yükü ile ilişkili) artırması nedeni ile pseudohiponatremi gelişebilir[56]. Klinik olarak önemi olan gerçek hiponatremi yukarıda ayrıntılı bir şekilde açıklanmıştır.
o Tedavi sonrası pasif olarak iletilen antikorlara bağlı olarak çeşitli antikorların (özellikle antiviral titreler, muhtemelen ANA, ANCA, RF) serolojik testleri yanlışlıkla pozitif hale gelebilir. Ig G nin yarı ömrünün 21-28 gün olduğu göz önüne alınır ise infüzyon sonrası hemen bakılan bu testlerin güvenilirliği azalmaktadır.
o İntravenöz immünglobulin tedavisi alan hastaların % 30 kadarında klinik olarak anlamlı hemolizin eşlik etmediği direkt coombs testi pozitifliği saptanmıştır.
o Sistemik aspergilloz tanısı için kullanılan beta-D-glukan testi yalancı pozitifliğide bir diğer laboratuvar etkisidir.
2.6. İntravenöz İmmünglobulin Endikasyonları
İntravenöz immünglobulin tedavisi anti inflamatuvar ve immünmodülatör etkisinden faydalanmak için birçok hematolojik, romatolojik, nörolojik ve infeksiyöz hastalıkta uzun yıllardır kullanılmaktadır. Mayıs 2008 tarihinde İngiltere Sağlık Bakanlığı tarafından yayınlanan ve Temmuz 2011 tarihinde güncellemesi yapılan İmmünglobulin Klinik Kullanım Kılavuzu en kapsamlı ve en güncel kılavuzdur[57]. Bu yüzden bu bölümde intravenöz immünglobulin kullanım alanları; İngiltere Sağlık Bakanlığının yayınladığı kılavuz ve beraberinde spesifik hastalık kılavuzları, sistemik derlemeler, randomize kontrollü çalışmaların meta-analizi, randomize olmayan kontrollü çalışmalar, deneysel çalışmalar, vaka kontrol çalışmaları, uzman komite raporları ve saygın otorite görüşleri üzerinden değerlendirilecektir.
İngiltere Sağlık Bakanlığı tarafından yayınlanan kılavuza göre immunglobulin tedavisinin endikasyonları 4 kategori altında toplanmıştır[57].
Kategori I(Kırmızı-yüksek öncelikli- endikasyonlar):
İmmünglobulin tedavisinin verilmediği durumlarda hayatı tehdit eden durumların olduğu ve ilk sıra tedavi olarak tercih edilmesi gereken hastalıklardır.
Kategori II(Mavi-orta öncelikli- endikasyonlar):
İmmünglobulin tedavisinin ya tek başına veya diğer tedavi modelleriyle birlikte ikinci sıra tedavi olarak kabul edildiği hastalıklardır.
Kategori III(Gri-düşük öncelikli- endikasyonlar):
İmmünglobulin tedavisinin, optimum rolünün belirlenemediği (mevcut kanıtlar zayıftır) hastalıklardır. Bu kategorideki uygulamalar olguya özgünleştirilmelidir.
Kategori IV(Siyah-etkili olmayan- endikasyonlar):
Yayımlanmış kanıtlara göre immünglobulin tedavisinin etkisiz veya zararlı olduğunun gösterildiği veya öne sürüldüğü hastalıklardır. Bu durumdaki İmmünglobulin tedavisi uygulamaları sadece onaylı araştırma protokolleri altında yapılmalıdır.
Kılavuza göre kanıt seviyesi ve düzeyi belirleme ölçütleri şunlardır;
Kanıt seviyesi 1a: Kanıt randomize kontrollü çalışmaların meta analizlerden elde edilmiştir. Kanıt seviyesi 1b: Kanıt en azından bir tane randomize kontrollü çalışma sonucu ile elde edilmiştir.
Kanıt seviyesi 2a: Kanıt en azından 1 tane non-randomize iyi tasarlanmış kontrollü çalışmadan elde edilmiştir.
Kanıt seviyesi 2b: Kanıt en azından 1 tane non-randomize iyi tasarlanmış yarı deneysel çalışmadan elde edilmiştir.
Kanıt seviyesi 3: Kanıt deneysel olmayan iyi tasarlanmış tanımlayıcı çalışmalar sonucunda elde edilmiştir.(Korelasyon çalışmaları, vaka çalışmaları gibi)
Kanıt seviyesi 4: Kanıt uzman komite raporları, saygın otorite görüşleri ve klinik tecrübelere dayandırılmıştır.
Kanıt düzeyi A: Kanıt seviyesi 1a ve 1b kabul edilen çalışmalardan elde edilen veriler. Kanıt düzeyi B: Kanıt seviyesi 2a ve 2b kabul edilen çalışmalardan elde edilen veriler.
Kanıt düzeyi C: Kanıt seviyesi 3 ve 4 kabul edilen çalışmalardan elde edilen veriler. Kılavuza göre tedavi sürelerinin tanımı:
Kısa dönem tedavi: 3aydan daha az süre verilen tedavi. Uzun dönem tedavi: 3 aydan daha uzun süre verilen tedavi.
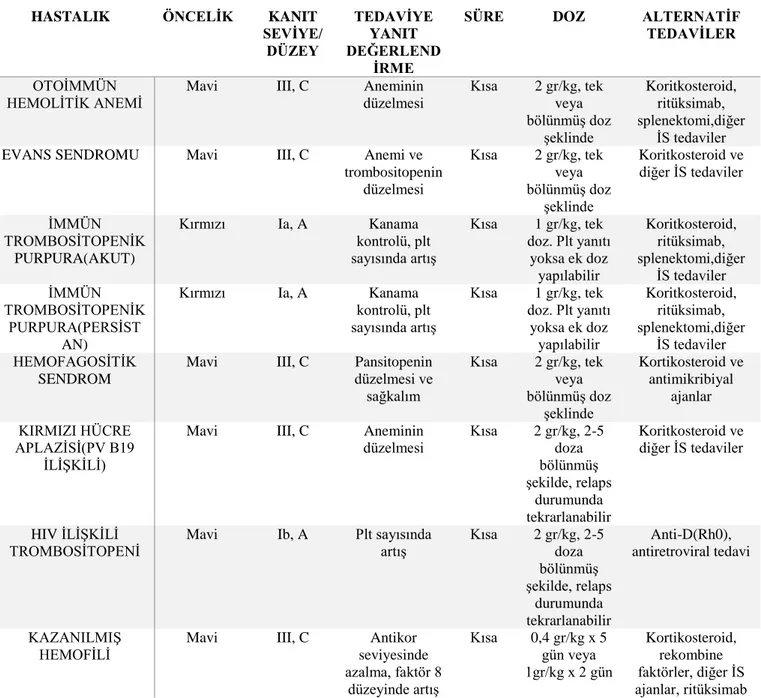
Bu bölümde iç hastalıkları pratiğinde daha sık karşılaşılan hematolojik, romatolojik ve infeksiyöz patolojilerde immünmodülasyon amacı ile İVİG kullanım endikasyonları ayrıntılı değerlendirilecektir. Tablo 2.1.’de İngiltere Sağlık Bakanlığı İVİG çalışma grubunun hazırladığı endikasyonlar ve ek öneriler özetlenmiştir.
Tablo 2.1. İngiltere Sağlık Bakanlığı İVİG çalışma grubu tarafından yayınlanan kılavuz özeti
HASTALIK ÖNCELİK KANIT SEVİYE/ DÜZEY TEDAVİYE YANIT DEĞERLEND İRME
SÜRE DOZ ALTERNATİF TEDAVİLER
OTOİMMÜN HEMOLİTİK ANEMİ
Mavi III, C Aneminin düzelmesi Kısa 2 gr/kg, tek veya bölünmüş doz şeklinde Koritkosteroid, ritüksimab, splenektomi,diğer İS tedaviler EVANS SENDROMU Mavi III, C Anemi ve
trombositopenin düzelmesi Kısa 2 gr/kg, tek veya bölünmüş doz şeklinde Koritkosteroid ve diğer İS tedaviler İMMÜN TROMBOSİTOPENİK PURPURA(AKUT) Kırmızı Ia, A Kanama kontrolü, plt sayısında artış Kısa 1 gr/kg, tek doz. Plt yanıtı yoksa ek doz yapılabilir Koritkosteroid, ritüksimab, splenektomi,diğer İS tedaviler İMMÜN TROMBOSİTOPENİK PURPURA(PERSİST AN) Kırmızı Ia, A Kanama kontrolü, plt sayısında artış Kısa 1 gr/kg, tek doz. Plt yanıtı yoksa ek doz yapılabilir Koritkosteroid, ritüksimab, splenektomi,diğer İS tedaviler HEMOFAGOSİTİK SENDROM
Mavi III, C Pansitopenin düzelmesi ve sağkalım Kısa 2 gr/kg, tek veya bölünmüş doz şeklinde Kortikosteroid ve antimikribiyal ajanlar KIRMIZI HÜCRE APLAZİSİ(PV B19 İLİŞKİLİ)
Mavi III, C Aneminin düzelmesi Kısa 2 gr/kg, 2-5 doza bölünmüş şekilde, relaps durumunda tekrarlanabilir Koritkosteroid ve diğer İS tedaviler HIV İLİŞKİLİ TROMBOSİTOPENİ
Mavi Ib, A Plt sayısında
artış Kısa 2 gr/kg, 2-5 doza bölünmüş şekilde, relaps durumunda tekrarlanabilir Anti-D(Rh0), antiretroviral tedavi KAZANILMIŞ HEMOFİLİ
Mavi III, C Antikor seviyesinde azalma, faktör 8 düzeyinde artış Kısa 0,4 gr/kg x 5 gün veya 1gr/kg x 2 gün Kortikosteroid, rekombine faktörler, diğer İS ajanlar, ritüksimab
OTOİMMÜN VWH Mavi III, C Antikor seviyesinde azalma, vWF düzeyinde artış Kısa 0,4 gr/kg x 5 gün veya 1gr/kg x 2 gün Kortikosteroid, rekombine faktörler, diğer İS ajanlar, ritüksimab POST TRANSFÜZYON PURPURA
Mavi III, C Kanama kontrolü, plt sayısında artış Kısa 2 gr/kg, 2-5 doza bölünmüş şekilde Kortikosteroid, plazma değişimi KLL, MM ,NHL VE HKHN İLE İLİŞKİLİ SEKONDER ANTİKOR YETMEZLİĞİ
Mavi Ib, A İnfeksiyon sıklığında azalma, hospitalizasyon sıklığında azalma, IgG düzeyinde artış
Uzun 0,4 gr/kg/ay Profilaktik ve terapotik antibiyoterapi
PRE-TRANSPLANT ANTİKOR UYUMSUZLUĞU
Mavi III, C Hasta ve greft sağ kalımı, greft
fonksiyonu, rejeksiyon episodları, hospitalizasyon sıklığı Kısa 2 gr/kg, gerektiğinde doz tekrarlanabilir Kortikosteroid ve diğer İS tedaviler POST TRANSPLANT ANTİKOR ARACILI REJEKSİYON POST TRANSPLANT VİRAL PNÖMONİLER
Mavi III, C Hasta sağ kalımı, radyolojik bulgularda gerileme, hastanede yatış süresinde azalma Kısa 0,5 gr/kg x 5 gün Sistemik antiviraller, ybü destek tedavisi KR. İNF. DEMİYELİNİZAN POLİRADİKÜLO NÖROPATİ Kırmızı Ia, A Klinik skorlamalarda düzelme Kısa 2 gr/kg, relapslarda doz tekrarı yapılabilir Kortikosteroid, diğer İS tedaviler, plazmaferez GUİLLAİN BARE SENDROMU Kırmızı Ia, A Klinik bulgularda düzelme Kısa 2 gr/kg, yanıt yok ise 14 gün sonra ek doz Plazmaferez İNFLAMATUVAR MİYOPATİLER (DM, PM, IBM)
Mavi IIb, B Klinik ve kas skorlarında
düzelme
Uzun 6 hafta ara ile 2 doz 2 gr/kg, relapslarda ek doz Kortikosteroid, diğer İS tedaviler, plazmaferez MYASTENİA GRAVİS VE LEMS
Mavi Ib, A Halsizlik ve güçsüzlük skorlarında düzelme Kısa 2 gr/kg Kortikosteroid, diğer İS tedaviler, plazmaferez, pridostigmin MULTİFOKAL MOTOR NÖROPATİ
Mavi Ia, A Klinik skorlamalarda
düzelme
Uzun 6 hafta ara ile 2 doz 2 gr/kg, relapslarda ek
doz
Kanıtlanmış ek alternatif tedavi yok
PARAPROTEİN İLİŞKİLİ DEMİYENİZAN NÖROPATİ Mavi Ia, A Klinik skorlamalarda düzelme
Uzun 6 hafta ara ile 2 doz 2 gr/kg, relapslarda ek doz Kortikosteroid, plazmaferez RASMUSSEN SENDROMU
Mavi IIb, B Nöbet sıklığında azalma ve
kognitif fonksiyonlarda
düzelme
Uzun 6 hafta ara ile 2 doz 2 gr/kg, relapslarda ek
doz
Kombine antiepileptik tedavi
2.6.1. Hematolojik Hastalıklarda İntravenöz İmmünglobulin Kullanımı Kazanılmış kırmızı hücre aplazisi:
Parvovirus B19'a bağlı kazanılmış kırmızı hücre aplazisinde bir kontrolsüz çalışma ve vaka raporları kortikosteroid tedavisi başarısız olduğunda intravenöz immünglobulin tedavisinin yararlı olabileceğini göstermektedir. Kılavuzda kategori 2 olarak önerilmektedir[58, 59] (Kanıt Seviyesi: 3, kanıt düzeyi: C). Parvovirüs B19 dışı nedenler sonrası gelişen kırmızı hücre aplazisinde olgu raporları anlamlı fayda sağlamadığı yönünde görüş bildirmektedir ve kılavuzda kategori 3 olarak önerilmektedir (Kanıt Seviyesi: 3, kanıt düzeyi: C).
Erişkin HIV ilişkili trombositopeni:
Bir randomize kontrollü çalışmada erişkin HIV infeksiyonu ilişkili trombositopenide diğer tedavi seçeneklerinin işe yaramadığı ve hayatı tehdit eden kanamaların olduğu durumlarda intravenöz immünglobulin tedavisinin etkinliği raporlanmıştır[60]. Kılavuzda kategori 1 olarak önerilmektedir. (Kanıt Seviyesi: 1b, kanıt düzeyi: A)
Koagülasyon faktör inhibitör varlığı:
Hayatı tehdit eden kanamanın olduğu ve kortikosteroid, siklofosfamid, ritüksimab ve faktör replasman tedavilerine yanıt vermeyen kazanılmış hemofili vakalarında intravenöz immünglobulin tedavisinin vaka serileri ve raporları ile faydasının olduğunu bildirilmiştir[61, 62]. Kılavuzda kategori 3 olarak önerilmektedir (Kanıt Seviyesi: 3, kanıt düzeyi: C). Uluslararası bir seride kazanılmış von willebrand hastalarında(63 hasta) yüksek doz intravenöz immünglobulin tedavisine yanıtlar yüz güldürücü olmuştur[63]. Bu yüzden kazanılmış von willebrand hastalarında, diğer standart tedavilere yanıt vermeyen hayati tehdit eden kanama varlığında ya da invaziv işlemlerden önce hızlı yanıt için kategori 2 olarak önerilmektedir (Kanıt Seviyesi: 2a, kanıt düzeyi: B)
Otoimmun hemolitik anemi:
Birinci basamak tedavi olarak kortikosteroid tedavisine dirençli vakalarda diğer tedavi protokolleri(ritüksimab veya splenektomi) ile kullanımı kılavuzda kategori 2 olarak önerilmektedir[64]. Klinik açıdan anlamlı direkt coombs testi pozitifliği, hemoglobin 6-7 gr/dl civarı olması ve hepatosplenomegali varlığı tedaviye iyi yanıt ile ilişkilendirilmektedir[65]. (Kanıt Seviyesi: 3, kanıt düzeyi: C)
Evans sendromu:
Olgu serileri ve olgu sunumları intravenöz immünglobulin tedavisinin kortikosteroidler ve siklofosfamid gibi sitotoksik ilaçlarla birlikte immünsüpresif tedavinin bir parçası olarak evans sendromunda yararlı olduğunu göstermektedir[66, 67]. Kılavuzda kategori 2 olarak önerilmektedir. (Kanıt Seviyesi: 3, kanıt düzeyi: C)
Hemofagositik lenfohistiositoz/hemofagositik sendrom:
Hemofagositik lenfohistiositoz (HLH) sitotoksik T-lenfositler ve NK hücrelerin fonksiyonlarında bozulma, makrofaj ve T-lenfositlerin aktivasyonu, proinflamatuvar sitokinlerin artmış üretimi ve hemofagositoz sonucu ateş, hepatosplenomegali ve sitopeninin ön planda olduğu klinik durum ile karakterize bir hastalıktır. Genetik veya edinsel nedenler sonucu ortaya çıkan bu hastalık nadir de olsa klasik klinik bulgulardan farklı şekillerde kendini gösterebilir. Olgu serileri ve sunumlarında virüs ilişkili hemofagositik sendrom vakalarında diğer tedavi seçenekleri ile birlikte (antiviraller, yüksek doz kortikosteroid ve diğer immünmodülatör ajanlar) başarıyla kullanılmıştır[68, 69]. Kılavuzda kategori 2 olarak önerilmektedir. (Kanıt Seviyesi: 3, kanıt düzeyi: C)
İdiyopatik trombositopenik purpura:
İntravenöz immünglobulin tedavisi şiddetli ITP ve düşük trombosit sayısına sahip erişkinlerde önemli ve yararlı bir tedavi şeklidir, kılavuzda kategori 1 olarak önerilmektedir. Yüksek doz İVİG, randomize çok merkezli çalışmalarda sistemik kortikosteroidlerle karşılaştırıldığında, klinik açıdan önemli bir avantaj sağladığı gösterilmiştir[29, 70]. Akut veya inatçı ITP hastalarında hayatı tehdit edici kanaması olan hastalarda kortikosteroidlerin kontraendike olduğu veya hızlı yanıt istenen durumlarda periferik yaymada diğer trombositopeni nedenleri ekarte edildikten sonra ilk tercih olarak verilebilir. Cerrahi girişim öncesi kortikosteroide yanıtsız hastalarda intravenöz immünglobulin tedavisi uygundur. (Kanıt Seviyesi: 4, kanıt düzeyi: C). Gebelikte kortikosteroidlerin ve intravenöz immünglobulin tedavisinin karşılaştırmalı olarak yayınlanmış hiçbir çalışması yoktur ve gebe kadınların yönetimini gebe olmayan hastalardan ayırt etmek için çok az veri vardır[29, 71]. Kortikosteroidler hamile kadınlarda standart tedavidir, ancak tedavi uzun süre devam ediyorsa, kortikosteroidlere yanıt yoksa veya bunların kullanımı uygun değilse intravenöz immünglobulin tedavisi düşünülmelidir[72, 73]. (Kanıt Seviyesi: 2b, kanıt düzeyi: B)
Bir kaç olgu sunumu, kortikosteroidler ve intravenöz immünglobulin tedavisinin birlikte kullanıldığı durumlarda post-transfüzyon purpurasında fayda sağladığını göstermiştir fakat kontrollü herhangi bir çalışma yapılmamıştır[74, 75]. Bununla birlikte hastalığın potansiyel hayatı tehdit edici niteliği, nadir olması ve diğer etkili tedavilerin kanıtlarının yokluğu göz önüne alındığında intravenöz immünglobulin transfüzyondan sonraki 2-14 gün içerisinde platelet sayısında azalma ve kanama saptanan hastalarda kategori 2 olarak önerilmektedir. (Kanıt Seviyesi: 3, kanıt düzeyi: C)
Hematopoetik kök hücre nakli sonrası serum Ig G azlığı:
Nakil sonrası serumda düşük IgG düzeylerine sahip hastalarda intravenöz immünglobulin tedavisi kategori 1 olarak önerilmektedir. (Kanıt Seviyesi: 2b, kanıt düzeyi: B) Kronik lenfositik lösemi:
KLL hastalarında (özellikle Ig G düzeyi <5 gr/lt olan hastalar ) intravenöz immünglobulin tedavisi ile bakteriyel infeksiyonların sıklığının azaldığı raporlanmıştır[76, 77]. Bu yüzden düşük serum Ig G saptanan KLL hastalarında profilaktik antibiyoterapinin yanında intravenöz immünglobulin tedavisi infeksiyonların sıklığını azaltmak için kategori 2 olarak önerilmektedir. (Kanıt Seviyesi: 1b, kanıt düzeyi: A)
Multiple myelom:
Yapılan bir randomize kontrollü çalışmada intravenöz immünglobulin tedavisinin, sık tekrarlayan bakteriyel infeksiyonların eşlik ettiği MM hastalarında (özellikle plato faz esnasında, azalmış serum Ig G seviyeleri ile birlikte) infeksiyon sıklığını azalttığı gösterilmiştir[78]. Bu yüzden kategori 2 olarak önerilmektedir. (Kanıt Seviyesi: 1b, kanıt düzeyi: A)
Aplastik anemi:
İntravenöz immünglobulin tedavisinin faydasına yönelik olgu raporlarında fikir ayrılığı vardır[79, 80]. Kılavuzda kategori 3 olarak önerilmektedir(Kanıt Seviyesi: 3, kanıt düzeyi: C). Otoimmün nötropeni:
Birkaç küçük olgu serisinde otoimmun nötropenide intravenöz immünglobulin tedavisinin faydalı olduğu rapor edilmiştir[81, 82]. Fakat kortikosteroid ve diğer tedavi seçeneklerine üstünlük sağladığına dair yeterli çalışma yoktur. Kategori 3 olarak önerilmektedir (Kanıt Seviyesi: 3, kanıt düzeyi: C).
Hemolitik üremik sendrom:
Olgu raporlarında hemolitik üremik sendroma yönelik intravenöz immünglobulin tedavisinin etkinliği ile ilgili çelişkili sonuçlar vardır[83, 84]. Kılavuzda kategori 3 olarak önerilmektedir (Kanıt Seviyesi: 3, kanıt düzeyi: C).
Post transfüzyon hiperhemolizis(Özellikle orak hücre anemili hastalarda):
Kan ürünü replasmanı sonucu donör ve alıcı eritrositlerinin yıkımı ile seyreden ciddi ve atipik gecikmiş hemolitik reaksiyondur. Kortikosteroid ile birlikte intravenöz immünglobulin tedavisinin etkili olduğuna yönelik çalışmalar mevcuttur[85, 86]. Kılavuzda kategori 2 olarak önerilmektedir (Kanıt Seviyesi: 4, kanıt düzeyi: C).
2.6.2. Romatolojik Hastalıklarda İntravenöz İmmünglobulin Kullanımı İnflamatuvar miyopatiler:
Kontrollü çalışmalar intravenöz immünglobulin tedavisinin dermatomiyozit hastalarında etkili olduğunu göstermiştir[87, 88]. Bir randomize kontrollü çalışmada erişkin başlangıçlı dermatomiyozit hastalarında 3 aydan daha uzun süren anlamlı iyileşme sağlandığı raporlanmıştır[89]. Ayrıca bir vaka serisinde refrakter juvenil dermatomiyozit hastalarında alternatif tedaviye ek olarak uygulandığında faydalı olduğu raporlanmıştır[90]. Agresif hastalık veya alternatif tedavilere dirençli durumlarda kategori 2 olarak önerilmektedir (Kanıt Seviyesi: 2a, kanıt düzeyi: B).
Katastrofik antifosfolipid sendromu:
KAFS’u çok hızlı ilerleyen, arteriyel ve venöz trombozlar ile karakterize, mortalite oranı yüksek bir hastalıktır. İmmunsupresif tedaviler(özellikle siklofosfamid) mortalite oranını artırabilir. Geniş bir kayıt tabanlı çalışma KAFS tanılı hastalarda terapotik plazmaferez ile birlikte intravenöz immünglobulin tedavisinin destek tedavisi ve antikoagulan tedavi ile birlikte uygulandığında faydalı olabileceğini rapor etmiştir[91]. Kılavuzda kategori 3 olarak önerilmektedir (Kanıt Seviyesi: 3, kanıt düzeyi: C).
Kawasaki hastalığı:
Özellikle çocukluk döneminde ortaya çıkan, etiyolojisi tam olarak bilinmeyen sistemik vaskülittir. Meta analizlerde ve çok merkezli prospektif çalışmalarda intravenöz
immünglobulin tedavisinin faydalı olduğuna yönelik ikna edici sonuçlar raporlanmıştır[92, 93]. Tanı ile birlikte yüksek doz aspirin ile tek doz 2 g/kg intravenöz immünglobulin tedavisi kategori 1 öneridir(Kanıt Seviyesi: 1a, kanıt düzeyi: A). İlk doz sonrası anlamlı yanıt yoksa veya 48 saat içinde nüks varsa ikinci doz uygulanabilir, ikinci doz İVİG ile de yanıt yoksa pulse kortikosteroid tedavisi uygulanabilir[57] (Kanıt Seviyesi: 3, kanıt düzeyi: C).
Sistemik lupus eritamatozis:
Küçük çaplı bir retrospektif çalışmada(n:59) SLE’li hastaların %65’inde intravenöz immünglobulin tedavisi sonrası geçici klinik ve laboratuvar regresyon raporlanmıştır[94]. Çeşitli olgu sunumları SLE ilişkili renal, kardiyak, SSS ve kemik iliği gibi organ spesifik tutulum bulguları olan hastalarda yüksek doz intravenöz immünglobulin tedavisinin hastalık regresyonu açısından anlamlı olduğunu rapor etmiştir[95-99]. Bununla birlikte tromboemboli ve azotemi yan etkileri göz önünde bulundurulmalıdır. Kılavuzda kategori 3 olarak önerilmektedir(Kanıt Seviyesi: 3, kanıt düzeyi: C).
Sistemik vaskülitler ve ANCA ilişkili patolojiler:
16 sistemik vaskülit hastası ile yapılan çalışmada intravenöz immünglobulin tedavisi ile 15 hastada remisyon sağlanmıştır, izlemde 7 hastada relaps izlenmiştir[100]. Randomize, plasebo kontrollü bir başka çalışmada; ANCA ilişkili sistemik vaskülit tanısı ile izlenen ve daha önce verilen tedavilere rağmen inatçı hastalık aktivasyonu olan 34 hasta ele alındı. 17 hastaya İVİG, diğer 17 hastaya ise plasebo uygulandı. İVİG verilen grupta hastalık aktivitesinin regrese olduğu fakat bu etkinin 3 aydan daha uzun sürmediği gözlendi[101]. Kılavuzda kategori 3 olarak önerilmektedir(Kanıt Seviyesi: 3, kanıt düzeyi: C).
2.6.3. İnfeksiyon Hastalıklarında İntravenöz İmmünglobulin Kullanımı Şiddetli invaziv grup A streptokok hastalıkları:
Çok sayıda olgu sunumu, bir retrospektif vaka kontrol çalışması ve bir randomize kontrollü çalışma, intravenöz immünglobulin tedavisinin şiddetli invaziv grup A streptokoksik hastalıklarda fayda sağladığı gösterilmiştir[102, 103]. Deneysel çalışmalar, intravenöz immünglobulinin süperantijen toksinlerini ve opsonize bakterileri nötralize edebilme yeteneği sayesinde ilk sıra tedavilerin(antibiyoterapi, cerrahi debridman vb.) başarısız olması durumunda kullanımını desteklemektedir[104, 105]. Alternatif tedavilerin faydalı olmadığı
durumlarda intravenöz immünglobulin tedavisi verilebilir. Kılavuzda kategori 2 olarak önerilmektedir (Kanıt Seviyesi: 3, kanıt düzeyi: C).
Stafilokoksik toksik şok sendromu:
S. Aureusun bazı suşları tarafından üretilen süperantijen toksinleri; özellikle patojenle daha önce karşılaşmamış genç hastalar için ciddi tehdit oluşturmaktadır. Bir uzman raporu birinci basamak tedavilerin etkili olmadığı durumlarda intravenöz immünglobulin tedavisini önermektedir[57]. Kılavuzda intravenöz immünglobulin tedavisi agresif tedaviye yanıtın olmadığı, drenaj yapılamayan odak varlığı veya inatçı pulmoner ödem ile birlikte oligüri varlığında kategori 2 olarak önerilmektedir (Kanıt Seviyesi: 3, kanıt düzeyi: C).
PVL ilişkili nekrotizan stafilokokal sepsis:
Panton valentin lökosidin, şiddetli nekrotizan pulmoner infeksiyonlar ile ilişkili stafilokokal virulan faktördür, serilerde mortalite oranı % 75 dir. Olgu sunumları intravenöz immünglobulin tedavisinin PVL ilişkili nekrotizan stafilokokal infeksiyonlarda fayda sağladığını ortaya koymuştur[106, 107]. Yoğun bakım ünitesinde destek tedavisi ve sistemik antibiyoterapiye yanıt vermeyen hastalarda kategori 2 olarak önerilmektedir (Kanıt Seviyesi: 3, kanıt düzeyi: C).
Şiddetli veya tekrarlayan clostridium difficile koliti:
Nazokomiyal diyarelerin en sık nedeni C. Difficile kolitidir. Küçük bir vaka serisi rekürren C. Difficile koliti vakalarında intravenöz immünglobulin tedavisinin etkili olduğunu raporlamıştır[108]. Sınırlı klinik çalışmalar fulminant C. Difficile koliti hastalarında standart antimikrobiyal tedaviyle birlikte uygulandığında intravenöz immünglobulin tedavisinin etkili olduğunu belirtmiştir[109, 110]. Kılavuzda şiddetli veya tekrarlayan vakalarda birinci basamak tedaviler etkili olmadığında kategori 2 olarak önerilmektedir (Kanıt Seviyesi: 3, kanıt düzeyi: C).
2.6.4. Transplantasyon Alanında İntravenöz İmmünglobulin Kullanımı Antikor uyumsuz transplantasyon:
Yüksek HLA sensitizasyonu saptanan ve renal transplantasyon uygulanan 101 tane son dönem böbrek yetmezliği hastası üzerinde yapılan çift kör, plasebo kontrollü, randomize çalışmada; İVİG’in Anti-HLA antikor titrelerini azaltmada ve transplantasyon oranlarını artırmada ki üstünlüğü raporlanmıştır[111]. Bir başka çalışmada 76 tane yüksek HLA sensitizasyonu saptanan son dönem böbrek yetmezliği hastasına desensitizasyon amacı ile İVİG(2 gr/kg, 1. Ve 30. Gün) ve ritüksimab(1 gr, 15. Gün) tedavisi uygulanmıştır. Çalışma sonucunda post-transplant dönemde antikor aracılı rejeksiyon oranlarının azalması ve artmış sağ kalım ile ilişkili Anti-HLA titrelerinde anlamlı azalma raporlanmıştır[112]. Anti-HLA antikorlar ile ilişkili böbrek, kalp ve akciğer nakli ertelenen hastalarda kılavuzda kategori 2 olarak önerilmektedir (Kanıt Seviyesi: 3, kanıt düzeyi: C).
Antikor aracılı rejeksiyonlar:
Solid organ nakillerinin antikor aracılı rejeksiyonlarında şimdiye kadar spontan iyileşme gösterilememiştir. Bir randomize kontrollü çalışmada kortikosteroid dirençli-antikor aracılı rejeksiyon gelişen renal transplant hastalarında terapotik plazma değişimi sonrası uygulanan İVİG tedavisi ile ilgili ümit verici sonuçlar raporlanmıştır[113]. Bir başka çalışmada; antikor aracılı rejeksiyon gelişen 24 renal transplant hastasında tek başına yüksek doz İVİG ve kombine tedavinin (İVİG + plazmaferez + ritüksimab) etkinliği kıyaslanmıştır. Sonuç olarak 3 yıllık allogreft sağ kalımı monoterapide %50, kombine tedavide ise %91,7 saptanmıştır[114]. Steroid dirençli rejeksiyon gelişmesi durumunda veya diğer tedavilerin kontraendike olması durumunda kılavuzda kategori 2 olarak önerilmektedir (Kanıt Seviyesi: 3, kanıt düzeyi: C).
3. MATERYAL METOD
3.1. Çalışma tasarımı ve hastalar:
Bu çalışmada; Ege Üniversitesi Tıp Fakültesi Hastanesi İç Hastalıkları Anabilim Dalı Yoğun Bakım Ünitesinde 2010-2017 yılları arasında, 3 gün ve daha uzun süre yatış öyküsü olan 3883 hastanın dosyaları retrospektif incelendi, içlerinden İVİG tedavisi verilen hastalar saptandı. Sağlık Uygulama Tebliği(SUT) kuralları dahilinde hipogamaglobulinemi, sepsis/ septik şok, immün trombositopeni, immün hemolitik anemi endikasyonları ile İVİG uygulanan 252 hasta çalışmaya dahil edildi. Çalışmamızda, ağır klinik tablo ile geç dönemde kabul edilmeleri ve müdahale için yeterli zamanın olmamasına bağlı olarak kaybedilmeleri göz önüne alındığında, mortalite oranlarının etkilenme riski sebebiyle, 3 günden az yatan hastalar incelemeye alınmadı.
Hastaların adı, soyadı, yaşları, protokol numaraları, cinsiyeti, yatış süreleri, komorbid durumları (DM, KVS hastalıkları, KBY, hemodiyaliz), insülin kullanımı, laboratuvar kayıtları (Tam kan sayımları, kan biyokimyasında serum albümin, üre, kreatinin, ürik asit, plazma sodyum, laktat dehidrogenaz(LDH), idrar sodyum atılımı, C-Reaktif Protein(CRP) değerleri ve endikasyonu olan hastalardaki, PAAC grafilerindeki kardiyo-torasik indeksleri (KTİ), kardiyak troponin T, NTproBNP ve prokalsitonin değerleri her bir hasta için hazırlanan, olgu rapor formuna kaydedildi. Hastaların yatış sebepleri, IVIg uygulnma endikasyonları, doz ve gün sayıları ve mortalite nedenleri epikrizlerinden incelenerek kaydedildi.
Tüm hastalar Ege Üniversitesi Tıp Fakültesi İç Hastalıkları YBÜ’de yatan hastalardan seçildi. Hastaların laboratuvar verileri, Ege Üniversitesi Tıp Fakültesi Hastanesi bünyesindeki Tıbbi Biyokimya laboratuvarında, hastaların radyolojik incelemeleri aynı Radyodiagnostik Ana Bilim Dalı’nda ve diğer tüm işlemler Ege Üniversitesi Tıp Fakültesi Hastanesi bünyesindeki Ana Bilim Dallarınca gerçekleştirilmiştir. Tüm hastalar Yoğun Bakım Ünitesinde aynı öğretim görevlisi tarafından, 2 aylık Yoğun Bakım rotasyonları şeklinde eğitimlerini tamamlayan İç Hastalıkları Anabilim Dalı kıdemli asistanlarınca, aynı salonda ve aynı hemşirelerce izlenmiştir. İzlenilen ünitede her yatakta monitorizasyon, oksijen desteği vardır. Yoğun Bakım Ünitesinde toplamda 4 adet mekanik ventilatör bulunmaktadır. Yoğun Bakım Ünitemiz toplamda 12 yatak ve 2 adet tam donanımlı agoni odasından oluşmaktadır.
3.2. Veri toplama ve hesaplamalar
Yoğun Bakıma giriş laboratuvar değerleri bazal, yoğun bakımdan çıkış (taburculuk veya exitus) laboratuvar verileri ise sonlanım değeri olarak kaydedildi. Tam kan sayımı tetkikinde bulunan, nötrofil sayısı ve lenfosit sayısı oranlaması (NLO) ve zamansal değişimi (∆NLO= sonlanım değeri-bazal değer farkı) ve ortalama trombosit hacmi (MPV), zamansal MPV değişimi (∆MPV= sonlanım değeri-bazal değer farkı) hesaplamaları yapıldı. Çalışmaya dahil edilen hastaların verilerine yoğun bakım kayıt defteri, hastane epikriz sistemi, laboratuar – sonuç kayıt sistemi incelenmesi ile ulaşılmıştır.
3.3. İstatiksel analiz yöntemleri
İstatistiksel analizi için SPSS 23.0 (SPSS Inc, Chichago, IL, USA) programı kullanıldı. Nitelik değişkenler bakımından gruplar arasında farklılık olup olmadığı ki kare testi ile araştırıldı. İki grup arasında sayısal değişkenler bakımından farklılık olup olmadığı parametrik test varsayımlarının karşılanması durumunda bağımsız gruplarda t testi ile karşılanmaması durumunda ise Mann Whitney U testi ile değerlendirildi. Kategorik değişkenler sayım-sayı, yüzde (%) olarak özetlenirken devamlı değişkenler de ortalama, ortanca, standart sapma, çeyrekler arası aralık, minimum, maksimum olarak özetlenmiştir. Bağımsız parametrelerin mortalite üzerindeki etkilerini değerlendirmek için Cox orantılı-hazard regresyon modeli ve çok değişkenli logistik regresyon analizi kullanılmıştır.
4. BULGULAR
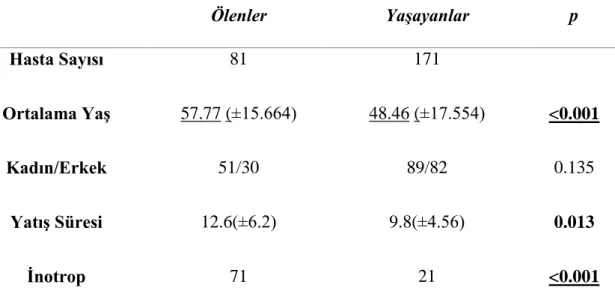
Bu çalışmada; Ege Üniversitesi Tıp Fakültesi Hastanesi İç Hastalıkları Anabilim Dalı Yoğun Bakım Ünitesinde 2010-2017 yılları arasında, 3 gün ve daha uzun süre yatış öyküsü olan 3883 hastanın dosyaları retrospektif incelendi, içlerinden İVİG tedavisi verilen hastalar saptandı. Sağlık Uygulama Tebliği(SUT) kuralları dahilinde hipogamaglobulinemi, sepsis/ septik şok, immün trombositopeni, immün hemolitik anemi endikasyonları ile İVİG uygulanan 252 hasta çalışmaya dahil edildi. Romatolojik patolojiler zemininde artmış immun yanıt (sistemik inflamatuvar yanıt sendromu kriterlerini sağlayan fakat infeksiyon/hastalık aktivasyonu ayrımı klinik ve laboratuvar bulgular ile net olarak yapılamayan ve ön planda sepsis kabul edilerek tedavi planlanan hasta grubu) ile İVİG verilen hastalar için alt grup analizi yapıldı. Çalışmamızda, ağır klinik tablo ile geç dönemde kabul edilmeleri ve müdahale için yeterli zamanın olmamasına bağlı olarak kaybedilmeleri göz önüne alındığında, mortalite oranlarının etkilenme riski sebebiyle, 3 günden az yatan hastalar incelemeye alınmadı. Tablo 4.1’de çalışma hastalarının demografik verileri özetlenmiştir. 252 hastanın verileri incelendi. Tüm popülasyonda mortalite sayısı 81 idi. Ölen grup daha yaşlıydı. Fakat cinsiyet açısından anlamlı fark yoktu.
Tablo 4.1. Çalışma hastalarının demografik özellikleri
Çalışmaya alınan hastaların İVİG endikasyonları, mortalite oranları Tablo 4.2’de özetlenmiştir. Vaskülit, bağ doku hastalığı ve hemofagositik lenfohistiositik sendrom tanıları olan hastalar başvuru esnasında sistemik inflamatuvar yanıt sendromu kriterlerini sağlıyorlardı.
Ölenler Yaşayanlar p Hasta Sayısı 81 171 Ortalama Yaş 57.77 (±15.664) 48.46 (±17.554) <0.001 Kadın/Erkek 51/30 89/82 0.135 Yatış Süresi 12.6(±6.2) 9.8(±4.56) 0.013 İnotrop 71 21 <0.001
İnfeksiyon ve hastalık aktivasyonu ayrımının klinik/laboratuvar bulguları ile net olarak ayrımının güç olduğu bu hasta grubunda sepsis ön tanısı ile İVİG tedavisi uygulandı fakat analizlerde bu hasta popülasyonu için ayrı alt gruplar tanımlandı.
Çoklu organ yetmezliği sendromuna yol açan sepsis ve septik şok tanılı 122 hastaya, steroide dirençli immun trombositopeni tanısı ile 38 hastaya, steroid yanıtsız immun hemolitik anemi tanısı ile 14 hastaya, 23 tanesi romatoloji ilişkili patolojiler zemininde gelişen 25 hemofagositik lenfohistiositoz sendromu hastasına, hayati organ tutuluşuna neden olan bağ doku hastalığı ve ANCA ilişkili vaskülit tanılı toplam 53 hastaya; geniş spektrumlu antibiyotik ve/veya çoklu sistemik immunsupresif tedavilerin yanında İVİG tedavisi verildiği saptandı.
Tablo 4.2. İVİG uygulama endikasyonları, hasta ve mortalite sayısı
En yüksek mortalite oranı sepsis kolunda idi. İmmun trombositopeni ve immun hemolitik anemi hastalarında mortalite oranları çok düşüktü ve dramatik yanıt alındığı saptanan tedavi kolu da bu gruptu. Hemofagositik lenfohistiositoz sendromu kolunda hematolojik malignite hastaları çıkarıldığında mortalite oranımız %24,6 saptandı ve literatürle uyumlu mortalite oranı vardı.
122 38 14 25 24 29 54 3 1 10 6 7 0 20 40 60 80 100 120 140 SEPSİS ITP İHA HLH BDH Vaskülit HASTA SAYISI
İzlemde mortalite IVIG verilenler
(%44,3 )
(%7,9 )
(%7,1 )
(%40 )
(%25)
(%24,1 )
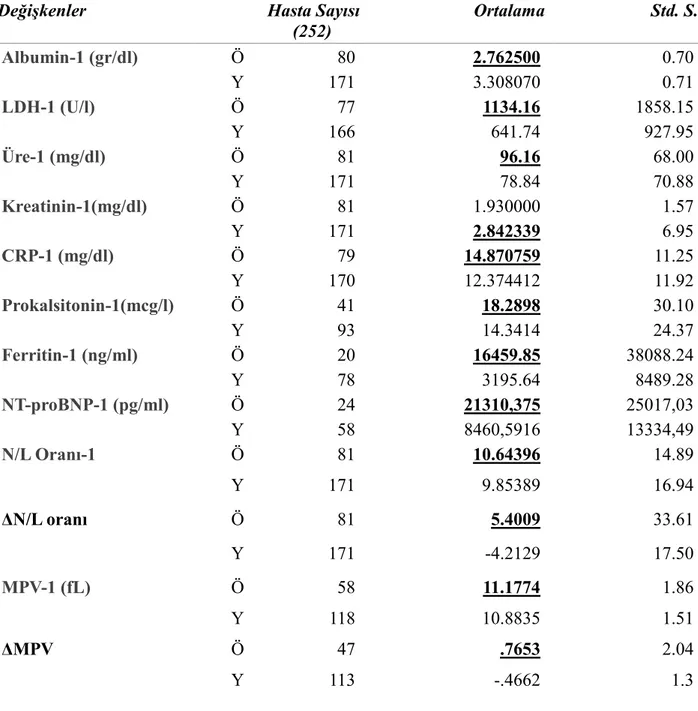
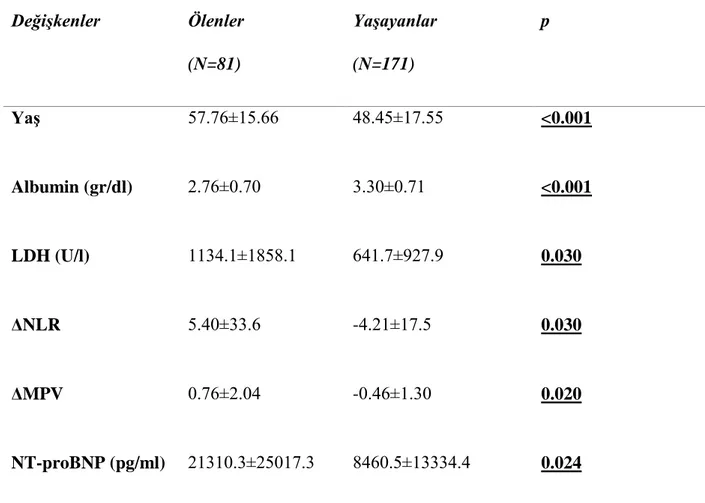
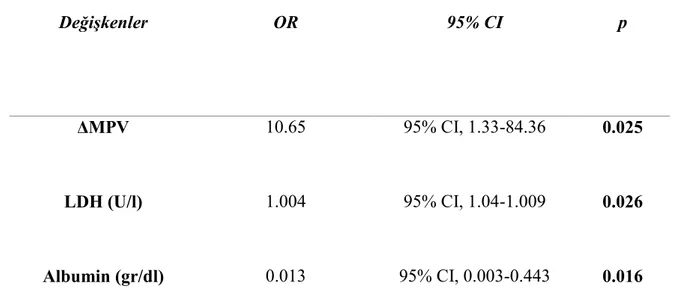
Hastaların tanımlayıcı istatistik verileri Tablo 4.3’te verilmiştir. Yoğun bakım kabulünde bakılan laboratuvar verilerinde ölen grupta albümin giriş değerleri daha düşük saptandı. LDH, üre, crp, prokalsitonin, ferritin ve NT proBNP değerleri daha yüksekti. Ayrıca ölen grupta, kabulde bakılan bazal NLO ve OTH değerleri daha yüksekti. Bunlara ek olarak ölen grupta OTH’nin ve NLO’nun izlemde artış gösterdiği saptandı ve bu delta olarak ifade edildi.
Tablo 4.3. Çalışma hastalarının tanımlayıcı istatistik verileri
Değişkenler Hasta Sayısı
(252) Ortalama Std. S. Albumin-1 (gr/dl) Ö 80 2.762500 0.70 Y 171 3.308070 0.71 LDH-1 (U/l) Ö 77 1134.16 1858.15 Y 166 641.74 927.95 Üre-1 (mg/dl) Ö 81 96.16 68.00 Y 171 78.84 70.88 Kreatinin-1(mg/dl) Ö 81 1.930000 1.57 Y 171 2.842339 6.95 CRP-1 (mg/dl) Ö 79 14.870759 11.25 Y 170 12.374412 11.92 Prokalsitonin-1(mcg/l) Ö 41 18.2898 30.10 Y 93 14.3414 24.37 Ferritin-1 (ng/ml) Ö 20 16459.85 38088.24 Y 78 3195.64 8489.28 NT-proBNP-1 (pg/ml) Ö 24 21310,375 25017,03 Y 58 8460,5916 13334,49 N/L Oranı-1 Ö 81 10.64396 14.89 Y 171 9.85389 16.94 ΔN/L oranı Ö 81 5.4009 33.61 Y 171 -4.2129 17.50 MPV-1 (fL) Ö 58 11.1774 1.86 Y 118 10.8835 1.51 ΔMPV Ö 47 .7653 2.04 Y 113 -.4662 1.3
*1 Bazal değer, LDH; Laktat Dehidrogenaz, L; Lenfosit, NLR; Nötrofil/Lenfosit oranı, Delta-NLR; sonlanım NLR - bazal