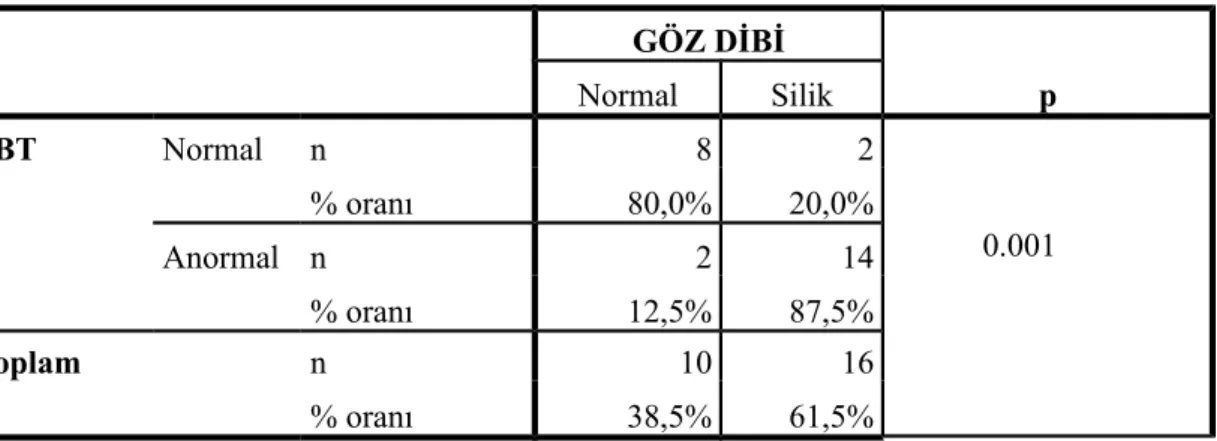
Beyin ödemi olan hastalarda serum NT-proBNP'nin rolü ve klinik gidiş ile ilişkisinin değerlendirilmesi
Tam metin
Şekil
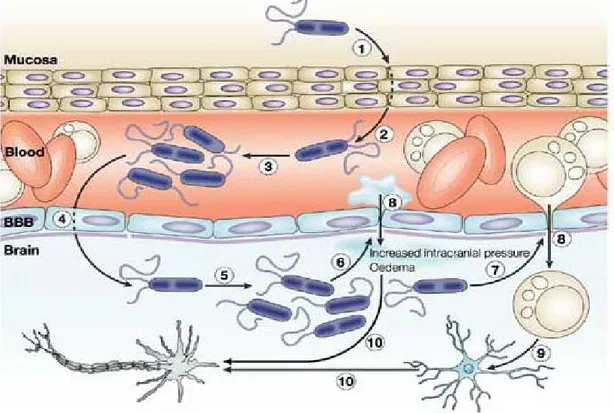
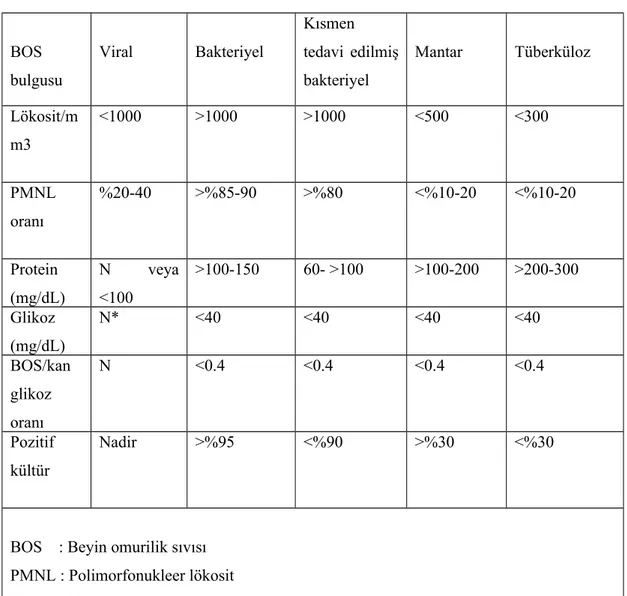
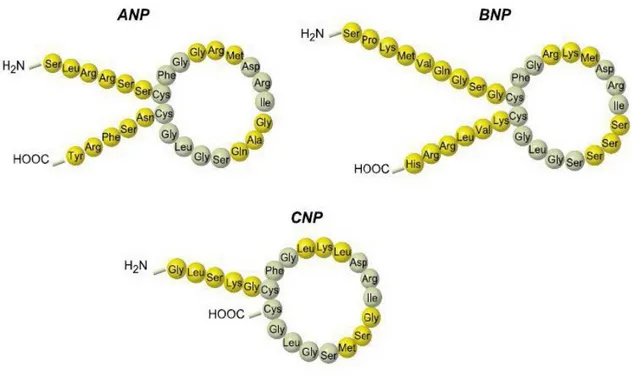

Outline
Benzer Belgeler
Fikir Üretilmesi (konu ile ilgili akla gelen tüm fikirleri, ne kadar garip veya komik olursa olsun söylenmesi ve kaydedilmesi).. Fikir ve Görüşlerin Sınıflandırılması
Effects of subthalamic nucleus deep brain stimulation on quality of life and motor and depressive symptoms in Parkinson’s disease. Chou KL, Taylor JL,
Doğal olarak aynı sonuçları elde ede- ceklerini umuyorlardı, ancak tam tersi oldu ve sağ yarımküre ayrıntılarla uğ- raşırken etkin hale geçti, sol yarımkü- re de
Diyelim yeni aç›lan bir üniversitemizde bölüm baflkan› oldunuz; sizin ilk antrenmanda -pardon, toplant›da, verece¤iniz konuflmay› duyar gibi oluyorum: “Bak›n
YÜZYIL SONUNDA BEYOĞLU'NUN SOSYAL TOPOĞRAFYA8I Türkçe SAİD N.. • DOĞAL GÜZELLİKLER Türkçe T.T.O.K. Edition) English Dr. Auflage) Deutsch Dr. édition) Français
Ekimizde sıkı sıkıya uymaya özen gösterdiğimiz en önemli ilke, elbette, yazılı ve görsel malzemeye her türlü emeği geçen kişilerin kat kılarını açık
Saniyen Maliye Polisine vermiş olduğum ifadede söz konusu edilen 31.034.80 liralık kasa fazlasını Aykut ve Salih Beylere tesli mime karşılık onlardan almış
The age and sex of the patient, indication for keratoplasty and type of the operation (penet- rating keratoplasty (PK), deep anterior lamellar keratoplasty (DALK),