Antikolinesteraz ilaçların sıçan mide fundus ve ileum düz kasında elektriksel alan stimülasyonu aracılı kasılma yanıtları üzerine antimuskarinik etkileri
Tam metin
Şekil

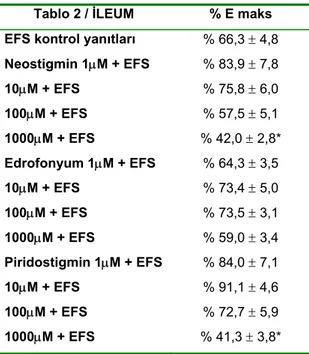
Benzer Belgeler
Ar›tma tesisisi genel ç›k›fl ve flebeke sular›nda EPEC, Salmonel- la, Shigella, Yersinia, Campylobacter, Vibrio ve Plesiomonas bulunmam›flt›r.. Sonuç olarak ‹stanbul'un
After taking a look at the work of different researches related to the analysis, by using different techniques and data sets from different sources we used COVID-19 datasets
a) Knowledge of the current job market trends (JMT) is the first input that forms the basis for the rest of the inputs. The latest trends in the job markets with respect to
i Salâhaddin PINAR İsmail ŞENÇALAR Kadri ŞENÇALAR Celâl TOKSES Tahsin KARAKUŞ Memleketimizin en kıymetli SES ve SAZ sanatkârları bir arada Hakkı DERMAN Şerif
Sonuç: Deneysel diyabetin sıçan mide dokusunda ghrelin pozitif hücre sayısını azalttığı, tedavi olarak verilen enalaprilin bu hücrelerin sayısını
SAR g¨or¨unt¨u olus¸turulması is¸leminin sıkıs¸tırılmıs¸ algılama tekni˘gi kullanılarak yapılması ic¸in denklem (3).’de hedef alanın
İşletmelerde Yıldırma ve Tükenmişlik İlişkisi: Duygusal Zekanın Düzenleyici Rolü, Yüksek Lisans Tezi, Balıkesir Üniversitesi, Sosyal Bilimler Enstitüsü,
We prove that; the class of quasi σ-rigid rings is closed under taking finite direct products (see Corollary 2.4).. We denote RG the group ring of a group G over a ring R and, for