T.C.
DİCLE ÜNİVERSİTESİ
TIP FAKÜLTESİ
İÇ HASTALIKLARI ANABİLİM DALI
EVRE 3-4 KRONİK BÖBREK HASTALARINDA PROOKSİDAN VE
ANTİOKSİDAN PARAMETRELERİN ATEROSKLEROZ
BELİRTEÇLERİ VE EKOKARDİYOGRAFİK BULGULARLA
İLİŞKİSİNİN DEĞERLENDİRİLMESİ
UZMANLIK TEZİ
Dr. Hatice AYAĞ
TEZ DANIŞMANI
Prof. Dr. Mehmet Emin YILMAZ
TEŞEKKÜR
Bilimsel düşünme ve çalışmayı bizlere öğreten, engin bilgi ve birikimlerini bizimle paylaşan, bugünlere gelmemizde büyük emeği olan, hekimliği bizlere öğreten değerli hocamız Prof. Dr. Ekrem MÜFTÜOĞLU’ na başta olmak üzere, İç Hastalıkları A.B.D. Başkanımız Prof. Dr. M. Emin YILMAZ’a yetişmemde büyük emekleri olan bütün değerli öğretim üyeleri; Prof. Dr. Vedat GÖRAL, Prof. Dr. Orhan AYYILDIZ, Prof. Dr. Abdurrahman IŞIKDOĞAN, Prof. Dr. Kendal YALÇIN, Doç. Dr. Alpaslan TUZCU, Doç.Dr. Muhsin KAYA, , Yrd. Doç. Dr. Hasan KAYABAŞI, Yrd. Doç. Dr. M.Ali KAPLAN, Yrd.Doç.Dr. Ali İnal, Uz.Dr. Yaşar YILDIRIM, Uz Dr. Remzi Beştaş, Uz.Dr. Coşkun Beyaz, Uz.Dr. Feyzullah Uçmak, Uz.Dr. Mehmet Küçüköner’e teşekkürlerimi sunuyorum.
Tezimin her aşamasında büyük emeği olan, yardımlarını esirgemeyen sayın Doç. Dr. Ali Kemal KADİROĞLU, Prof. Dr. Naime Canoruç, Prof. Dr. Nuriye Mete, Yrd. Doç. Dr. Osman Evliyaoğlu, laborant Hayriye Bayram, Dr.Salih Hattapoğlu, Dr.Tuğba Cezlan ve Rotasyon eğitimim sırasında bilgilerini benden esirgemeyen Kardiyoloji A.B.D. , Enfeksiyon Hastalıkları ve Mikrobiyoloji A.B.D. , Göğüs Hastalıkları ve Tüberküloz A.B.D., Radyoloji A.B.D.başkanlarına ve değerli öğretim üyelerine,
Birlikte çalışmaktan her zaman büyük mutluluk ve onur duyduğum tüm asistan arkadaşlarıma ve İç Hastalıkları A.B.D. çalışanlarına teşekkürlerimi sunuyorum.
Hayatımın her aşamasında bana destek olan sevgili annem, babam ve kardeşlerim’e ve sevgili dostum Dr. İkram Durç Öztürk’e sonsuz teşekkürü borç bilirim.
İÇİNDEKİLER Bölüm Sayfa No TEŞEKKÜR 1 İÇİNDEKİLER 2 SİMGELER KISALTMALAR 3 ŞEKİLLER VE TABLOLAR 5 1. GİRİŞ VE AMAÇ 7 2. GENEL BİLGİLER 8
2.1. Kronik Böbrek Hastalığı 8
2.1.1. Tanım ve Evreleme 8
2.1.2. Epidemiyoloji 9
2.1.3. Etiyoloji 10
2.1.4. Patogenez ve Patogenezde Oksidatif Stresin Rolü 11
2.1.5. Klinik Semptom ve Belirtiler 12
2.1.6. Komplikasyonlar 13
2.2. Kronik Böbrek Hastalığı ve Kardiyovasküler Hastalıklar 20
2.3. Oksidatif Stres ve Kronik Böbrek Hastalığı 26
2.4. SDBY-Oksidatif Stres ve Antioksidan Savunma Sistemleri 45
2.5.Oksidatif Stres ve Kardiyovasküler hastalıklar 46
2.6. Oksidatif Stres ve İnflamasyon İlişkisi 46
2.7.Oksidatif Stres ve Ateroskleroz 48
3. MATERYAL VE METOD 51 4. BULGULAR 55 5. TARTIŞMA 63 6. ÖZET 70 7. SUMMARY 72 8. KAYNAKLAR 74
SİMGELER VE KISALTMALAR KBH: Kronik Böbrek Hastalığı
KBY: Kronik Böbrek Yetmezliği
NKF/DOQI: National Kidney Foundation Kidney Disease Outcomes Quality
initiative
SDBY: Son Dönem Böbrek Yetmezliği
MDRD: Modification of Diet in Renal Disease CrCl: Kreatinin klirensi
GFR: Glomerular Filtration Rate TND: Türk Nefroloji Derneği RRT: Renal Raplasman Tedavisi
RAAS: Renin Anjiotensin Aldosteron Sistemi TGF-β: Transforming Büyüme Faktörü Beta JNC7: Joint National Committe-7
ESH/ESC: European Society of Hypertension/ European Society of Cardiology K/DOQİ: Kidney Disease Outcomes Quality İnitative
EPO: Eritropoetin
USRDS: United States Renal Data System KVH: Kardiyovasküler Hastalık LVH: Left Ventrikul Hypertrophy KAH: Koroner Arter Hastalığı
IVSd: İnter Ventrikuler Septum Diameter LVDd: Left Ventrikuler Diameter Diastol LVDs: Left Ventrikuler Diameter Sistol LAD: Left Atrial Diameter
EF: Ejeksiyon Fraksiyonu
NHANES: National Health and Nutrition Examination Survey ROT: Reaktif Oksijen Türleri
RNS: Reaktif Nitrojen Türleri ADMA: Asimetrik Dimetilarginin
MDA: Maolndialdehid KTX: Katalaz
GSH-px: Glutatyon Peroksidaz SOD: Süperoksit dismutaz
EBCT: Electron Beam Computerize Tomography NO: Nitrik Oksit
AGEs: İleri Glikolizason Son Ürünleri iPTH: İmmünreaktif Paratiroid Hormon O2ˉ : Süperoksit Radikali
H2O2: Hidrojen Peroksit
ROOˉ: Peroksil
OHˉ: Hidrojen Radikali OH2ˉ: Perhidroksi
HOCl: Hipoklorik asit RO: Alkoksil N02 : Nitrojen dioksit
GST: Glutatyon S Transferazlar ONOOH: Peroksinitrit
XOD: Ksantin Oksidaz XDH: Ksantin Dehidrojenaz HNO3: Nitrik asit
ETS: Mitokondriyal Elektron Teansport Sistemi -sH: Tiyol Radikalleri
NOS: Nitrik Oksit Sentaz GC: Guanilat Siklaz Fe: Demir
ŞEKİLLER
Sayfa
Şekil 1: Diyaliz hastalarında ölüm nedenleri ( Data from USRDS,2005 ) 20
Şekil.2:Kronik böbrek hastalığında risk faktörleri(ComprehensiveClinical Nephrology 2007) 21
Şekil 3. Oksidatif stres belirteçleri havuzunu etkileyen faktörler 27 Şekil 4 . Serbest Radikal Reaksiyonları 29 Şekil 5. Reaktif oksijen türlerinin oluşumu 30
Şekil 6. Reaktif oksijen ve nitrojen türlerinin vücuttaki etkiler 38
Şekil 7. 8 hidroksi guanin oluşum mekanizması 38
Şekil 8. Ateroskleroz başlangıcında endotel disfonksiyonunun rolü 49
Şekil 9. İntima kalınlaşması, Aterom plağı 53
Şekil 10. Sağ karotis intima media kalınlığı usg. görüntüsü 54
TABLOLAR Tablo 1: Kronik böbrek hastalığı evrelemesi 9
Tablo 2: Kronik Böbrek Hastalığının Başlangıç ve Progresyonu’nu Etkileyen Faktörler 10
Tablo 3: Son Dönem Böbrek Yetmezliği Nedenleri 11
Tablo 4. Kronik Böbrek Yetmezliği'nin progresyonunda rol oynayan faktörler 12
Tablo 5. Kronik böbrek hastalığında hedef kan basıncı düzeyleri 14
Tablo 6. Kronik böbrek hastalığında anemi sebepleri 15
Tablo 7. Kardiyovasküler risk faktörleri 22
Tablo 8. Oksijen Türevi Bileşikler 29
Tablo 9. Fagositlerin ürettiği reaktif oksidan ürünler 34
Tablo 10. Oksidatif stres ve antioksidan belirteçler 39
Tablo 11. Reaktif oksijen partiküllerinin patogenezinde rol oynadığı düşünülen böbrek hastalıkları 44
Tablo 12: Çalışmaya dahil edilme ve hariç tutma kriterleri 51
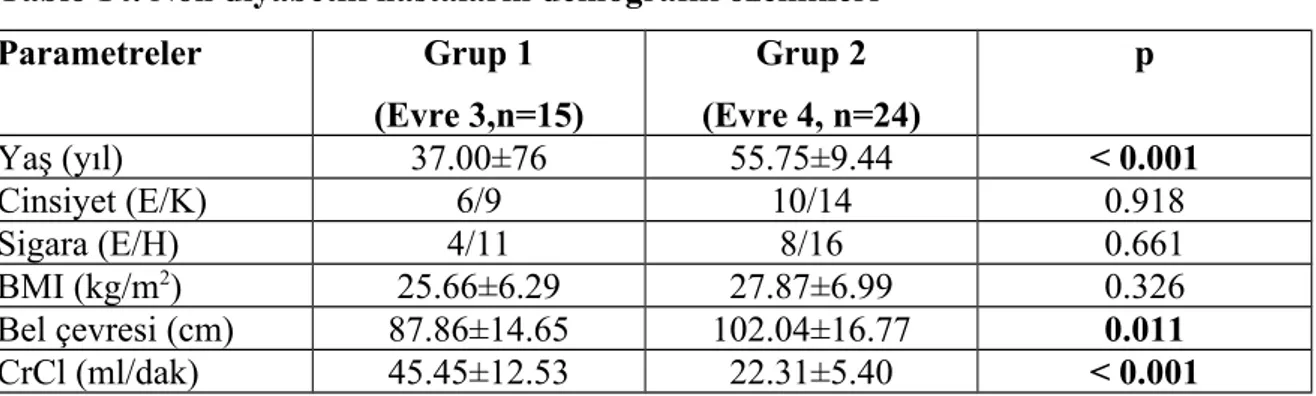
Tablo 14. Non diyabetik hastaların demografik özellikleri 55
Tablo 15. Diyabetik hastaların Tam kan, Biyokimya, Tam İdrar, Esbach bulguları 57
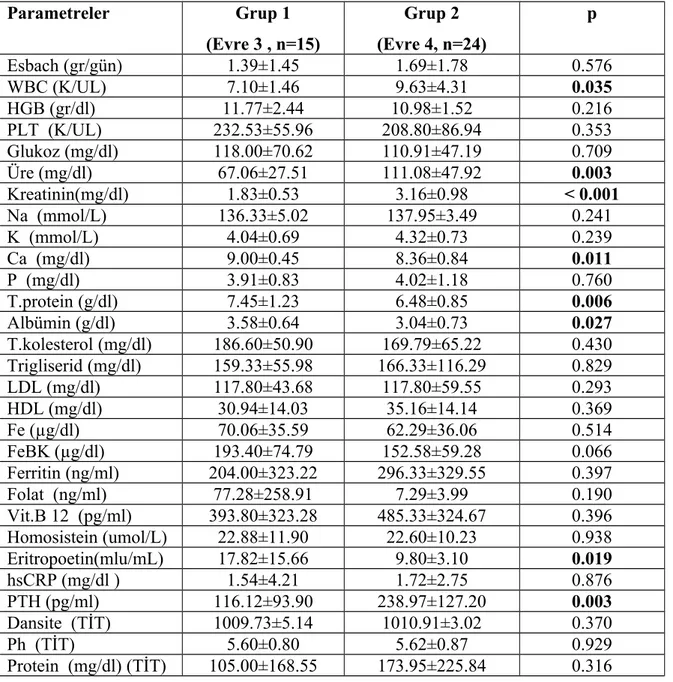
Tablo 16. Non-diyabetik hastaların Tam kan, Biyokimya, Tam İdrar, Esbach bulguları 58
Tablo 17. Diyabetik hastaların prooksidan, anti oksidan sistem parametreleri 59
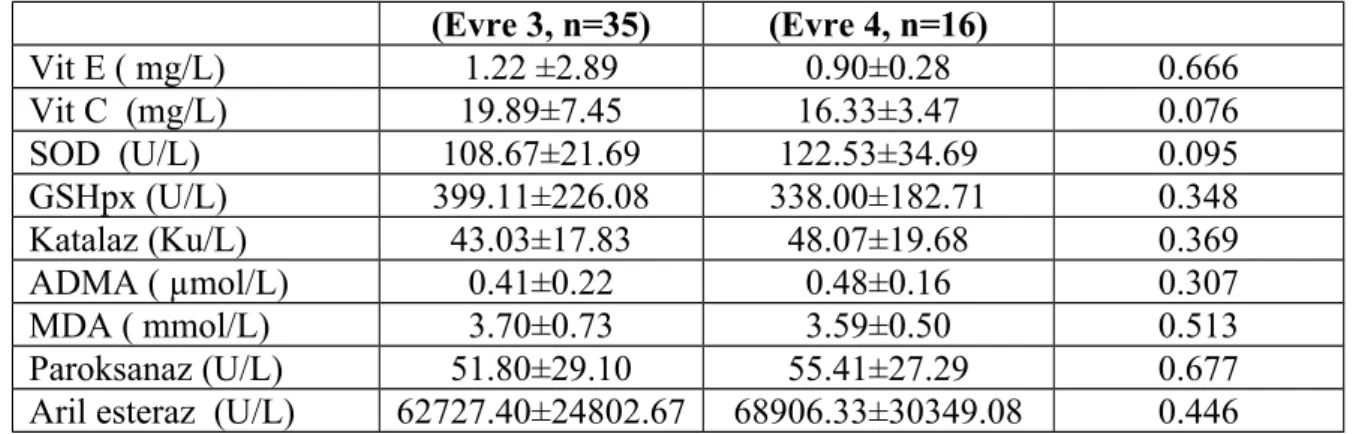
Tablo 18. Non diyabetik hastaların prooksidan, antioksidan sistem parametreleri 60
Tablo 19. Diyabetik hastaların ekokardiyografik ve ateroskleroz parametreleri 60
Tablo20. Non diyabetik hastaların ekokardiyografik ve ateroskleroz parametreleri 61
Tablo 21. Diyabetik hastalarda Korelasyon tablosu 62
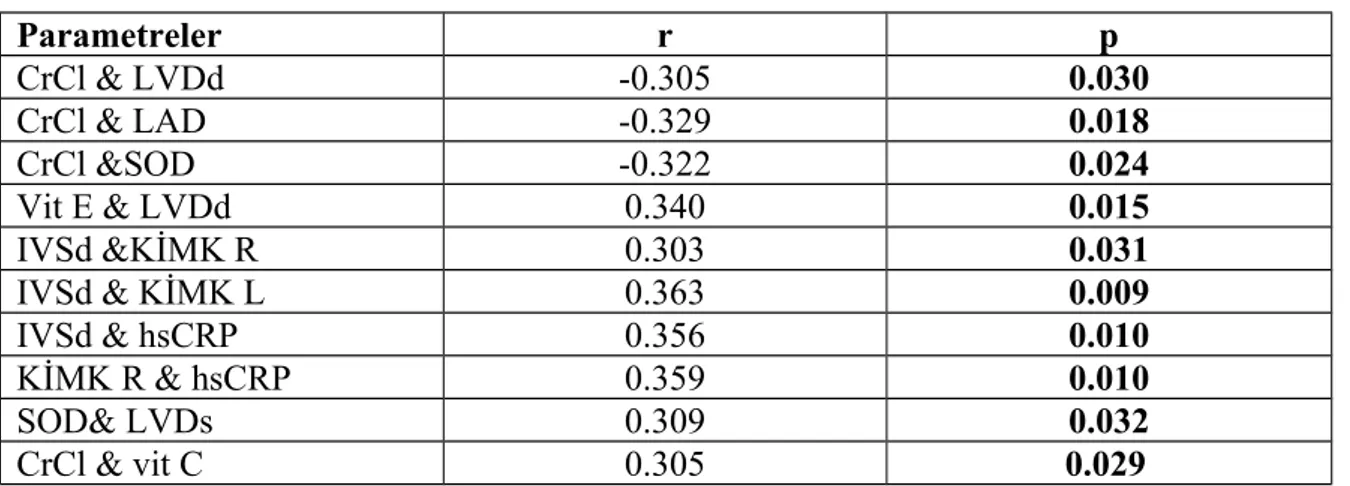
Tablo 22. Non diyabetik hastaların korelasyon tablosu 62
1.GİRİŞ VE AMAÇ
Kronik böbrek yetmezliğinin en sık sebebi diğer toplumlarda olduğu gibi ülkemizde de
diyabetes mellitustur. Gerek diyabete bağlı KBH’nda gerekse diğer nedenlere bağlı KBH’nda KVH’ların insidansı artmaktadır ve bu hasta kohortunda en sık morbidite ve mortalite nedenidir. Aslında birçok KBH hastaları son dönem böbrek yetmezliği gelişmeden kardiyovasküler hastalık nedeniyle ölmektedir ki bu hastalarda aynı yaştaki sağlıklı kontrol grubu ile yapılan çalışmada kardiyovasküler mortalite riski %15-30 daha fazla bulunmuştur. Bundan dolayı kronik böbrek hastaları KVH’lar için yüksek riskli hasta grubu olarak değerlendirilir. KVH’ların erken tanınması ve tedavi edilmesi KBH’larında morbiditeyi ve mortaliteyi azaltabilir
KBH hastalarında prooksidan ve antioksidan parametreler arasındaki denge artmış oksidatif strese kaymıştır. Bu durum RRT başlamadan çok önce saptanabilir ve kronik renal hastalık progresyonu ile artış gösterir. Kronik böbrek hastalığı süreci başladığı andan itibaren, hastalarda OS’in giderek artmasının nedenleri arasında ileri yaş, diyabet, üremi, kronik inflamasyon, hipervolemi, hipertansiyon ve RRT ile ilşkili faktörler gibi böbrek hastalığına sahip hasta populasyonunun özelliklerini içerir.
Çok geniş sayıda yayın diyabetin artmış oksidatif stres durumu olduğunu göstermektedir ve oksidanların diyabetin vasküler komplikasyonlarının gelişimine sebep olan mekanizmalarla ilşkili olduğu ileri sürülmektedir.
Evre 3-5 kronik böbrek hastaları ateroskleroz gelişimi ve bununla ilişkili morbidite ve mortalitede artış için büyük risk taşırlar. İlginç olarak oksidatif stres belirteçleri aterosklerotik proçesin yansıması olan karotis intima media kalınlığı ile ilişkili bulunmuştur. Renal katabolizma ve fonksiyonlarda azalmayla beraber, üremik oksidan mediatörler birikir, vasküler hücre disfonksiyonuna ve ateroskleroz gelişimine neden olur.
Yapılan çalışmalarda artmış oksidatif stresin kronik böbrek hastalığının erken ve geç safhalarında kardiyovasküler hasarla ilişkili olabileceği hem erişkin hem de pediatrik yaş gruplarında ortaya konulmuştur. Bazı araştırmalar kalp yetmezliği gelişiminin oksidatif stresle ilişkili olduğu hipotezini desteklemektedir.
Bu çalışmada evre 3-4 diyabetik ve non diyabetik hasta gruplarında oksidatif stresi, oksidatif stresin bu hasta gruplarında ateroskleroz ve ekokardiyografik bulgular ile ilşkisini değerlendirmeyi amaçladık.
2.GENEL BİLGİLER
2.1.KRONİK BÖBREK HASTALIĞI 2.1.1.Tanım ve Evre
Kronik böbrek hastalığı (KBH), böbrek parankiminde; çeşitli etiyolojik faktörlere
bağlı olarak kronik inflamatuar ve dejeneratif değişikliklerin ortaya çıktığı bir hastalık gurubudur. National Kidney Foundation Kidney Disease Outcomes Quality İnitiative (NKF/DOQI) tarafından yapılan tanımlamaya göre KBY; 3 ay veya daha fazla devam eden böbrek hasarı bulgusunun olması (Böbrek hasarı; böbreğin yapısal veya fonksiyonel anormalliklerinin glomeruler filtrasyon hızında (GFH) azalma olsun ya da olmasın, klinikte patolojik anormalikler olması), böbrek hasarı olsun ya da olmasın, 3 ay veya daha uzun süreli GFH’nın 60 ml/dak/1.73m2 altında olması (1) şeklinde belirtilmiştir.Böbrek fonksiyonlarında
bozulmanın devam etmesi sonucu kronik böbrek hastalığı son dönem böbrek yetmezliğine ilerler. Son dönem böbrek yetmezliği, böbrek fonksiyonlarının geriye dönüşümsüz kaybı ile karakterize ve hayatı tehdit eden üremiden korunmak için hastaya devamlı olarak diyaliz ve transplantasyon gibi renal replasman tedavilerinin (RRT) uygulandığı klinik bir tablodur. Üremi ise akut veya kronik böbrek yetmezliğinin sonucu oluşan ve tüm organlardaki fonksiyon bozukluğunu yansıtan klinik ve laboratuvar bir sendromu tanımlar. Akut hasarlanmayı takiben böbrek, fonksiyonlarını tekrar kazanabilir. Öte yandan, böbreğin kronik hastalıklarının %90 ından fazlası SDBY ile sonuçlanır (2)
Tek başına serum kreatinin düzeyi, azalmış böbrek fonksiyonunun belirlenmesinde yetersiz olup yetmezliği gruplamak üzere saptanan eşik değerler klinik gözlemlerden yola çıkarak ampirik olarak belirlendiğinden yakın zamana kadar KBH’nın gerçek sıklığı anlaşılamamıştır (3). Cockroft ve Gault tarafından geliştirilmiş olan bir formül ile hesaplanan GFR, renal fonksiyon bozukluğunun düzeyini, sadece serum kreatinine göre göstermektedir(4). NKF (National Kidney Foundation) tarafından önerilen ve MDRD (Modification of Diet in Renal Disease) çalışma grubunun geliştirdiği formül Cockroft-Gault’inkine göre renal fonksiyonu daha doğru olarak göstermektedir (5).
Cockcroft-Gault formülü
CCr (ml/dk) = (140-Yaş) x Ağırlık / 72 x Cr (Kadınlarda x 0.85)
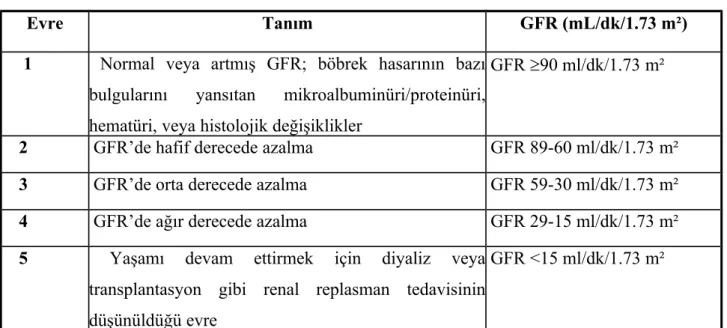
Tablo 1: Kronik böbrek hastalığı evrelemesi.
Evre Tanım GFR (mL/dk/1.73 m²)
1 Normal veya artmış GFR; böbrek hasarının bazı bulgularını yansıtan mikroalbuminüri/proteinüri, hematüri, veya histolojik değişiklikler
GFR ³90 ml/dk/1.73 m²
2 GFR’de hafif derecede azalma GFR 89-60 ml/dk/1.73 m²
3 GFR’de orta derecede azalma GFR 59-30 ml/dk/1.73 m²
4 GFR’de ağır derecede azalma GFR 29-15 ml/dk/1.73 m²
5 Yaşamı devam ettirmek için diyaliz veya transplantasyon gibi renal replasman tedavisinin düşünüldüğü evre
GFR <15 ml/dk/1.73 m²
2.1.2. Epidemiyoloji
Kronik böbrek hastalığının gerçek prevelans ve insidansı erken evre hastalarda
asemptomatik seyretmesi nedeniyle tam olarak bilinmemektedir. Türk Nefroloji Derneği (TND) verilerine göre 2007 yılı sonu itibariyle ükemizde hemodiyaliz tedavisi gören hasta sayısı 39267, kronik periton diyalizi tedavisi gören hasta sayısı ise 5307’dir (6). Toplam 621 merkezden alınan bilgilere göre, 2006 yılında Türkiye’de SDBY prevalansı milyonda 578, insidansı milyonda 189 bulunmuştur (3).
İngiltere’de RRT (Renal Raplasman Tedavisi) ile tedavi edilen SDBY insidansı yılda, her 1 milyon populasyonda yaklaşık 100 yeni hastadır (7). Bunun yılda % 5- 8 yükseldiği tahmin edilmektedir fakat halen Avrupa ortalamasının (yılda yaklaşık 129/her 1 milyon populasyonda) ve Amerika ortalamasının (yılda yaklaşık 333/her 1 milyon populasyonda) altındadır (8) (Tablo 2). Kronik böbrek hastalığı, tedavi maliyeti nedeniyle de önemli bir halk sağlığı sorunu olmaktadır. Tedavi maliyeti 2002’de yıllık 17 milyar dolara ulaştığı belirtilmektedir(9). 2010 yılına kadar dünya çapında 2 milyondan fazla kişi 1 trilyon $ maliyetle RRT ile tedavi edilecektir (10).
Dünya çapında nüfusun yaşlanması ve diabetes melitus prevelansındaki artışa paralel olarak SDBY ‘li hasta sayısı artmaktadır.
Tablo 2: Kronik Böbrek Hastalığının Başlangıç ve Progresyonu’nu Etkileyen Faktörler.
Başlangıç markerları ve faktörleri Progresyon Marker ve Faktörleri
Modifiye edilemeyen faktörler Modifiye edilebilir faktörler
Obezite Yaş HT
Dislipidemi Cinsiyet Proteinüri
Sigara Irk Lipidler
HT Genetik Glisemi
Renal kitle kaybı Obezite
Hiperürisemi
Sigara, Alkol, Kafein, Analjezik ve NSAII
2.1.3. Etyoloji
Son yıllarda SDBY insidansında tüm dünyada artış görülmektedir. Ülkeler arası
farklılıklar olmakla birlikte SDBY’nin en sık sebepleri diyabetes melitus, hipertansiyon, kronik glomerülonefritler, kronik interstisyel nefrit, herediter/konjenital hastalıklar ve malignitelerdir (11). ABD de istatistiklere göre 2010 yılında SDBY insidansının yıllık %6-7 olacağı öne sürülmüştür (12). Diyabetes Mellitus, hipertansiyon ve kronik glomerülonefrit SDBY’nin etyolojisinde ilk üç sırada yer almakta ve hastalığın etyolojisinin yaklaşık %80 inde sorumlu tutulmaktadırlar. Türk Nefroloji Derneği (TND) kayıtlarına göre ülkemizdeki veriler de buna paraleldir (Tablo 3). TND verilerine göre 2007 yılı sonu itibariyle hemodiyaliz tedavisi gören hastalarda diabetes mellitus, hipertansiyon ve kronik glomerülonefrit son dönem böbrek yetersizliği nedenleri arasında ilk üç sırayı almaktadır (6). Bunun dışında kistik böbrek hastalıkları, vezikoüreteral reflü, ürolojik problemler, herediter böbrek hastalıkları , multipl myeloma böbreği, amiloidoz, vs… SDBY neden olabilen diğer hastalıklardır. Olguların yaklaşık %10-20 sinde ise etiyolojik neden saptanamamaktatır.
Tablo 3: Son Dönem Böbrek Yetmezliği Nedenleri
HASTALIK ABD * İNDİLTERE** TÜRKİYE***
Diabetes Mellitus 46.8 18.1 23.7
Hipertansiyon 28.6 10.4 22.9
Glomerulonefrit 8.1 12.2 8.7
Kronik Tubulointerstisyel Nefrit - 8.1
-Kistik Böbrek Hastalığı 2.5 5.9 5.8
Veziko Ureteral Reflü - -
-Ürolojik Nedenler 2.1 - 6.2
Diğer Nedenler 12.2 18.2 14.9
Etyolojisi Bilinmeyenler 4.6 25.2 17.8
* : USRDS Annual Report 2007 ** : EDTA Regıstry 2005
*** : TND Regıstry 2007
2.1.4. Patogenez ve Patogenezde Oksidatif stresin rolü
KBY, metabolik, kardiovasküler ve hematolojik komplikasyonları kapsayan kompleks
patolojilerle karakterize bir sendromdur. Histopatolojik olarak incelendiğinde tüm nedenlere bağlı SDBY periglomerüler ve interstisyel fibroz, glomeruloskleroz, interstisyel kronik inflamatuar hücre infiltrasyonu ve tubuler atrofi gibi benzer bulgular saptanır. Bu veriler patogenezde ortak mekanizmaların rol oynadığını düşündürtmektedir. Bu progresyonda mekanik (hiperperfüzyon, hiperfiltrasyon, intraglomeruler hipertansiyon) ve biyolojik (lipidler, sitokinler, büyüme faktörleri ve oksidatif stres gibi) faktörler rol alırlar.
KBH etyopatogenezini açıklamak üzere, birbirinden farklı birçok mekanizma öne sürülmüş ve glomerüler hücreler, nötrofil, monosit/makrofajlar, trombositler, kompleman ve koagülasyon sistemi, proinflamatuar sitokinler ve büyüme faktörleri, anjioyensin II, endotelin, nitrik oksit (NO) ve serbest oksijen radikalleri gibi birçok mediyatörün, renal hasar oluşumunda rol oynayabileceği düşünülmektedir (12). Oksijen radikallerinin üretiminin artışı ve/veya antioksidan sistemlerin yetersizliği de KBY'nin patogenezine katkıda bulunur (13). Renal hücrelerin enerji üretimini ve transport fonksiyonlarını bozabilen oksidatif stres yükü;
morfolojik lezyonların oluşumundan ve proteinlere karşı glomerüler geçirgenliğin artmasından da sorumlu tutulmaktadır (12,13,14). KBY'de varolan renal parankimal hasar ve azalmış glomerül filtrasyon hızıyla ilgili olarak antioksidan kapasitenin azaldığı, lipid peroksidasyonunun ise arttığı bildirilmiştir (13,14). Renal kitlenin % 75 kaybının serbest radikal üretimini arttırdığı, serum kreatinini 5 mg/dl'den fazla olan hastaların eritrosit membran lipid peroksidasyonunun yükselmiş olduğunu bildirilmiştir (14).
Aşağıda oksidatif stresin organizmada oluşum mekanizmaları, fizyolojik ve patolojik süreçlerde etkileri tartışıldıktan sonra KBH oluşumunda ve komplikasyonlarn meydana gelmesinideki rolü ve KBH tedavileri üzerindeki etkileri incelenmiştir.
Tablo 4. Kronik Böbrek Yetmezliği'nin progresyonunda rol oynayan faktörler
• Proteinüri (>1.5 g/gün veya İdrar protein/kreatinin oranı >1 g/gün) • Hipertansiyon
• Altta yatan hastalığın tipi; Diabet gibi • Erkek cinsiyet
• Obezite
• Diabetes Mellitus • Hiperlipidemi • Sigara içimi
• Yüksek proteinli diyet • Fosfat retansiyonu • Metabolik asidozis
2.1.5.Klinik Semptom ve Belirtiler
Böbreğin fonksiyonel adaptasyon yeteneği nedeniyle böbrek dokusunun % 75 oranında
kaybı, glomerül filtrasyonunda, ancak yarıyarıya bir azalmaya neden olur. Böbrek rezervinde ileri derecede azalma olmasıyla, böbrek fonksiyonunda ölçülebilir bir düşme söz konusu olur.
Kronik böbrek hastalığının erken teşhisi, sadece böbrek yetmezliğinin ilerlemesini
geciktirmez aynı zamanda komplikasyonlardan da korur (özellikle artmış kardiyovasküler riskten). Evre 1-3 (GFR >30 ml/dk) kronik böbrek hastaları genellikle asemptomatiktirler ve sıvı-elektrolit bozuklukları veya endokrin bozukluklar görülmez. Genellikle bu bozukluklar evre 4-5 (GFR <30 ml/dk) hastalarda gelişir. Evre 5 kronik böbrek hastalığında görülen üremik belirtiler başlıca toksinlerin birikimi sonucu gelişir. Altta yatan böbrek hastalığına
bağlı olarak proteinüri veya hematüri gelişebilir. İdrarın konsantrasyon bozukluğuna bağlı olarak sıklıkla noktüri görülür. Halsizlik, bitkinlik, yorgunluk, iştahsızlık, mental kapasitede azalma üreminin erken belirtilerindendir. Şiddetli böbrek yetmezliğinde (GFR <10 ml/dk diyabetik olmayan hastalar; GFR<15 ml/dk olan diyabetik hastalar) nöromüsküler semptomlar (hiperrefleksi, kas seğirmeleri, periferik sensoryal ve motor nöropatiler, kas krampları, inme, (genellikle hipertansif ve metabolik ensefalopatinin sonucu olarak)) görülebilir. İştahsızlık, bulantı, kusma, kilo kaybı, stomatit, ağızda kötü tat görülebilir. Cilt sarı, kahverengi görünüm alabilir. Kaşıntı rahatsız edici boyutlarda görülebilir. İleri böbrek hastalığında, perikardit ve GİS ülserasyonu ve kanama yaygındır. Kardiyomiyopati (hipertansif, iskemik) ve renal sodyum ve su retansiyonu ödem ve kalp yetmezliğine yol açabilmektedir.
Böbrek fonksiyonları için çeşitli görüntüleme ve laboratuar yöntemleri kullanılabilirse de böbreğin ekskresyon fonksiyonunu en iyi gösteren parametre glomerüler filtrasyon hızıdır (GFH). Renal sintigrafi gibi yöntemlerle daha doğru saptanabilirse de, klinik pratikte GFH; kreatinin klirensi, Cockcroft-Gault formülü ve MDRD (The Modification of Diet in Renal Disease) formülü gibi basit ve güvenilir yöntemlerle ölçülerek böbrek rezervleri değerlendirilir ve evrelere ayrılır. Endojen kreatinin klirensi normalde 90-125 ml/dk’dır. GFH normalin %20-35’nin altına düştüğünde azotemi gelişmeye başlar ve normalin % 5-10’u seviyesine indiğinde, üremik sendrom (Evre5; Son Dönem Böbrek Yetmezliği) tablosu meydana gelir (15).
2.1.6. KOMPLİKASYONLAR Hipertansiyon
Hipertansiyon renal fonksiyonlar bozuldukça KBH’larının %80-85’inde önemli bir problem olarak ortaya çıkmaktadır (16). Hipertansiyon tedavisi kardiyovasküler hastalıklardan ölüm riskini ve proteinüriyi azaltarak böbrek fonksiyonlarındaki bozulmayı azaltmaktadır. Başarılı kan basıncı kontrolü renal fonksiyonlarda azalmanın hızını yavaşlatır. Kalp ve arterlerin her ikisinde hasarı azaltabilir ve kardiyovasküler komplikasyonların riskini azaltır. Genellikle çoklu ilaç rejimleri gerekmesine rağmen KBH’lığı olan hastalarda antihipertansif ajanların tüm sınıfları kullanılabilir ve böbrek hastalığının altta yatan nedeni ilaç seçimini etkileyebilir (2). Yaşam tarzı değişiklikleri, kilo kaybı ve diyette günlük <2.4 gr (100 mmol) sodyum kısıtlaması teşvik edilmelidir.
Kronik böbrek hastalarında hedef kan basıncı K/DOQİ kılavuzu ve Joint National Committe-7 (JNC7), EuropeanSociety of Hypertension/ European Society of Cardiology
(ESH/ESC) ‘ye göre 130/80 mm/Hg, eğer 1 g/gün’den fazla proteinüri varsa 125/75 mm/Hg olarak hedeflenmelidir.(17,18) Hastalıklara göre hedef tansiyonları tablo 5’de özetlenmiştir.
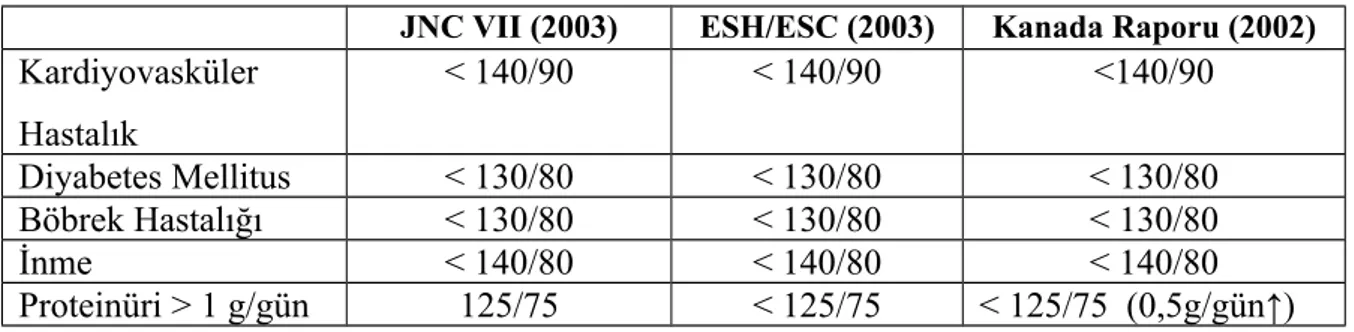
Tablo 5: Kronik böbrek hastalığında hedef kan basıncı düzeyleri
JNC VII (2003) ESH/ESC (2003) Kanada Raporu (2002)
Kardiyovasküler Hastalık < 140/90 < 140/90 <140/90 Diyabetes Mellitus < 130/80 < 130/80 < 130/80 Böbrek Hastalığı < 130/80 < 130/80 < 130/80 İnme < 140/80 < 140/80 < 140/80 Proteinüri > 1 g/gün 125/75 < 125/75 < 125/75 (0,5g/gün↑) Anemi
Böbrek hastalarında GFH 60 ml/dakika altına düşünce normokrom normositer tipte anemi oldukça sık karşılaşılan sorundur (19). K/DOQI kılavuzu 2006 önerilerine göre hemoglobin değerinin erkeklerde <13,5 g/dL, bayanlarda <12 g/dL anemi olarak kabul edilmeli ve prediyaliz hastalarında 11-12 g/dL hedef tedavi düzeyi olmalıdır. Hastalar anemi açısından takip edilirken KBH dışı nedenlerin de anemi sebebi olabileceği akılda tutulmalıdır (20).
Renal anemi, tipik olarak izole normokrom, normositer anemidir ve lökopeni ve trombositopeni yoktur. Eritrositlerin üremik toksinlere bağlı yaşam süresinin kısalması ve böbreklerden eritropoetin (EPO) üretiminin azalması ile beraber eritropoetine kemik iliğinde azalmış cevap en başta gelen sebeplerdir (21).
Anemi tedavi edilmezse, dokulara oksijen taşınmasında bozukluğa (22), kardiyak debide artmaya, sol ventrikül hipertrofisine, kalp yetersizliğine (23), kognitif ve entellektüel fonksiyonlarda azalmaya (24) ve immün sistemde bozukluklara (25) neden olur. Eğer uygun şekilde tedavi edilmezse anemi hastanın yaşam kalitesini ve yaşam süresini azaltır (26)
KBH’ da anemi nedenleri Tablo 6’ da gösterilmiştir
Tablo 6: Kronik böbrek hastalığında anemi sebepleri
Yetersiz diyaliz Hemoliz
Demir eksikliği Beslenme bozuklukları
VitB12/Folik Asit eksikliği Kan kaybı
Hiperparatiroidizm Aluminyum birikimi
Azalmış kemik iliği fonksiyonu Hemoglobinopatiler Azalmış eritrosit ömrü (70 gün)
Dislipidemi
Anormal lipid metabolizması KBH’da sık karşılaşılan bir problemdir (27). Trigliserid
yüksek olmakla beraber total kolesterol düzeyleri genellikle normal, HDL kolesterol düzeyi düşük olarak gözlenir. Lipoprotein lipaz tarafından çok düşük dansiteli lipoproteinin (VLDL) yıkılmasındaki bozukluğun hipertrigliseridemiye neden olan majör mekanizma oldugu gözükmektedir (28).
Hipertrigliseridemi tek başına kardiyovasküler hastalıklar açısından önemli bir risk artışı yapmamaktadır, muhtemelen öteki risk faktörleri ile birlikte hızlanmış ateroskleroza yatkınlığa sebep olmaktadır. Kronik böbrek hastalığı koroner arter hastalığı eşdeğeri olduğu ve LDL düzeylerinin yüksekliği de kardiyovasküler hastalıklar açısından yüksek risk içerdiği için agresif tedavi önerilmektedir. KBH’ da hedef LDL’nin 100 mg/dL’nin altına düşürülmesi şeklindedir (27).
Kemik ve Mineral Metabolizması
Bu bozukluğun spektrumu; serum kalsiyum, fosfor, magnezyum anormallikleri ve paratiroid hormon ve D vitamin metabolizma bozukluğunu içerir. Bu anormallikler ile birlikte üremik durum ile ilişkili diğer faktörler iskelet sistemini etkiler ve renal osteodistrofi olarak bilinen kemiğin kompleks bozuklukları ile sonuçlanır. Renal osteodistrofide görülen iskelet anomalilerinin spektrumu;
Osteitis fibroza; osteoblast, osteoklast aktivitesi ve peritrabeküler fibrozisle karakterize
hiperparatiroidizmin bir belirtisi
Osteomalazi; sıklıkla alüminyum birikmesinin neden olduğu yeni osteoid mineralizasyon
defektinin bir belirtisi.
Adinamik kemik hastalığı; düşük kemik turnoveri ile karakterize bir durum Osteopeni veya Osteoporoz
Hemodiyaliz hastalarında, osteitis fibroza ve adinamik kemik hastalığı hemen hemen eşit sıklıkta görülür. Osteomalazi hastaların küçük bir kısmında görülür. Ca metabolizması; PTH ve vitamin D hormonal sistemin yakın etkileşimi içindedir. KBH seyrinde bu her iki sistemde bozukluk meydana gelir ve iskelet sisteminde ters etki ile birliktedir. KBH'de total serum Ca konsantrasyonu düşmeye eğilimlidir, fakat serbest Ca seviyesi birçok hastada kompansatuar hiperparatiroidizm nedeniyle normal sınırlar içindedir (29). Fosfor retansiyonu ve böbrekten azalmış aktif D3 vit (Calcitriol) üretimini içeren birtakım faktörler hipokalsemiye yol açar. Bunlar bağırsaktan kalsiyum absorbsiyonunu azaltırlar ve iskelet sisteminde PTH'nin kalsemik etkisine direnç geliştirilen Kalsiyum PTH sekresyonunun major düzenleyicisi olduğu için, persistan hipokalsemi hiperparatiroidizm gelişmesinin güçlü bir stimulanıdır.
Progresif KBH'da fosfor böbrekler tarafından tutulur. Ancak GFR normalin <%30'una düşmeyene kadar hiperfosfatemi gelişmez. İleri evre KBH'ye kadar, kompansatuar hiperparatiroidizm, fosfatüri ile sonuçlanır ve serum fosfat seviyesini normal aralıkta tutar. Fosfat retansiyonu, böbreklerden Calcitriol üretimini azaltır ve böylece intestinal kalsiyum absorbsiyonunun azalmasına yol açarlar bundan dolayı PTH sekresyonu stimule olur. Buna ilaveten hiperfosfatemi, paratiroid bezinde calcitriol etkisine direnç ile ilişkilidir ve hiperparatirodizm gelişmesine katkıda bulunur. Aynı zamanda hiperfosfatemi iskelet sisteminde dirence, hipokalsemiye yol açar ve PTH sekresyonunu stimule eder. Fosfat'ın, serum kalsiyum ve calcitriol değişikliklerinden bağımsız olarak kendiliğinden PTH sekresyonuna etkisi olduğu görülmektedir (30,31). Fosfat serum kalsiyum seviyesinden bağımsız olarak paratiroid büyümesi üzerine de etkili olabilir (32,33).
25 hidroksivitamin D, böbreklerde 1-alfa hidroksilaz enzimi tarafından aktif metaboliti olan 1,25 hidroksivitamin D'ye dönüştürülür. Böbrekler calcitriol üretiminin major yeridir ve böbrek kitlesinde azalma olduğunda calcitriol üretimi azalır. Plazma calcitriol seviyesi, hafif ve orta böbrek hastalığında normal olabilir.
Metabolik Asidoz
Böbrekler asit-baz dengesinin sağlanmasında çok önemli rol oynar. Kronik böbrek
hastalığında GFR %50 oranında azalıncaya kadar, arteriyel pH, serum bikarbonat (HCO3) düzeyi ve pCO2 normaldir. Böbrek fonksiyonlarının daha fazla kötüleşmesiyle metabolik asidoz yerleşir; söz konusu asidoz, çoğu kez vücut sıvılarındaki PO4, SO4 ve diğer organik asitlerin birikimine bağlı artmış anyon açığı olan asidozdur. Başlangıçta bu asidoz asemptomatiktir; serum HCO3 düzeyi çoğu kez 12-15 mEq/L dolayındadır ve kan pH’sı
7.25’in altına genellikle düşmez. Ancak, asit yükünde ani bir artış (katabolizma artışı, ateşli hastalıklar, diyabetik ketoasidoz, laktik asidoz gibi) veya yetersizliğin çok ilerlemesi durumunda hayatı tehdit eden ağır asidoz tablosu ortaya çıkar. Kussmaul solunumu ve bilinç kaybı olur; hızla diyaliz yapılmazsa hasta kaybedilir.
Asidozun gelişimi hiperkalemiyi agreve eder, protein anabolizmasını inhibe eder ve hidrojen iyonlarının tamponlandığı kemiklerden kalsiyum kaybını hızlandırır (34). Evre 5 KBH’ li hastalarda şiddetli asidozun mevcudiyeti (örn, serum HCO3 <20 mmol/l) diyalize başlamanın bir endikasyonudur.
Malnutrisyon
Malnütrisyon diyaliz hastalarında yaygındır fakat evre 4-5 hastalarda da görülebilir ve
ölüm için artmış risk ile ilişkilidir (35). Son dönem böbrek yetmezlikli hastalarda PEM’nin olması mortalitede 2-10 kat artışa neden olmaktadır. Protein alımındaki ve vücut ağırlığındaki düşüklük hemodiyaliz hastalarında mortalitenin bir göstergesidir. Yapılan çalışmalarda serum albumin düzeyindeki 1 gr/dl’lik azalmanın kardiyovasküler mortalitede %39-66’lık bir artışa neden olduğu tespit edilmiştir. Malnütrisyon diyaliz öncesi hastalarda %30-51 oranında görülürken, HD hastalarında %23-76, PD hastalarında ise %18-50 oranında görülmektedir. Üremik toksinlerin vücutta birikimi, inflamasyon ve inflamatuar sitokinler artması sonucunda, hastalar spontan olarak protein ve enerji alımını azaltmaktadır (36). İlerleyici metabolik asidoz, ubiquitin aracılı protein yıkımını artırıp dallı zincirli amino(DZAA) asit metabolizmasını olumsuz yönde etkilemektedir. Bütün bunlara ek olarak yapılan kontrolsüz protein kısıtlaması malnütrisyona yatkınlığı daha da arttırmaktadır (37). Bu nedenle protein kısıtlaması yapılırken albumin, prealbumin, ağırlık takibi, transferrin, triceps kas kalınlığı gibi beslenme parametreleri sıkı kontrol edilmelidir.
Sodyum ve Su Retansiyonu
KBH'nin komplikasyonlarından birisi de su ve elektrolit metabolizmasının bozulmasıdır. Böbrek yetmezliğinin ileri evrelerine kadar serbest su klirensi korunmuş olmasına rağmen, KBH'li hastaların idrarı dilüe etme ve konsantre etme yetenekleri bozulmuştur. Plazma sodyum konsantrasyonu genellikle normal sınırlarda olmasına rağmen, KBH'de böbrekler tarafından sodyum tutulumu ve kullanımı değişir. GFR düştükçe, başlangıçta sodyum ve su hemostazı devam ettirilir, çünkü glomerüller tarafından filtre edilen sodyum ve suyun büyük miktarı atılır.
KBH'nin erken etkilerinden biri de büyük miktarda sodyum ve su alımını böbreğin kompanse etmesindeki kısıtlanmadır. Normal kişilerde hidrasyon durumuna bağlı olarak idrar atılımı 20-1500 ml/saat olarak değişebilir, kronik böbrek hastalarında bu aralık sınırlanmıştır. Bu kişilerde, aşırı su alımı dilüsyonel hiponatremi yapabilir. Böbrek fonksiyonları düştükçe, birçok hastada sodyum retansiyonu gelişir ve ekstraselüler volüm genişler. Bu hastalar ayaklarda şişlik veya pulmoner ödeme bağlı nefes darlığı, kısa nefes almadan şikayetçi olabilirler. Sodyum alımının günlük 2.4 gr (100 mmol) sınırlandırılması böyle şikayetleri azalmasına yardımcı olabilir ve kan basıncındaki artışı kontrol etmemize yardımcı olur.
Hiperkalemi
Böbrek hastalıklarında potasyum (K) düzeyi yükseldikçe aldosteron sekresyonu uyarılır,
bu mekanizma ile distal tübüllerden K atılımı arttırılarak serum düzeyinin yükselmesi önlenmektedir (38). Hiperpotasemi idrar miktarının 400 mL/gün’den daha az olması, GFH’nın 5-10 mL/dak altına düşmesi, yüksek K’lu diyet, renin anjiotensin sistemi (RAS) blokajı yapan ilaçlar ve diyabetes mellitus gibi hipoaldosteronizm yapan durumlar, primer olarak böbrek medüllasını tutan hastalıklar zemininde gelişebilmektedir. İlerlemiş hastalarda asidoza bağlı olarak hücre içine K alım mekanizmasının bozulması da buna katkı sağlamaktadır (39).
Hiperpotasemi diyetten K alımının azaltılması, serum K düzeyini artıran nonsteroid antiinflamatuarlar, β blokörler ve RAS blokajı yapan ilaçların alımına dikkat edilerek önlenebilir (40,41).
Endokrin Anormallikleri
Sekonder hiperparatiroidizm, üremik hastalarda en sık görülen endokrin problemdir.
Artmış PTH, bu hastalardaki kaşıntı, kardiyomiyopati, anemi, empotans ve nöropati gibi pek çok belirtinin patogenezinde rol alır; ayrıca renal osteodistrofiye yol açar.
KBH’da İnsülinin klirensi azalır, fakat artmış periferik direnç ile bu durum dengelenir. Bunun sonucu olarak, genellikle herhangi bir klinik durum meydana gelmez ve hastalar hipoglisemiye eğilimli değildirler. Ancak, diyabetik hastalarda, böbrek fonksiyonları azaldıkça insülini azaltmak gerekebilir ve diyaliz başladığında tersine eğilim olabilir (42).
sT3 ve sT4 düzeyleri düşük veya normal olabilir. Hastalar ötiroid görünümlerine
rağmen hipofiz yanıtı azalmıştır (43). Toplam plazma tiroksin (T4) seviyeleri normal olabilir ve T4 -T3 konversiyonu bozulduğu için reverse T3 artabilir. Tiroid bağlayıcı ajanın kaybına bağlı olarak dolaşan toplam T4 konsantrasyonunu daha fazla azaltabilir (44). Hastalar klinik olarak hipotiroidik olmazlar.
Büyüme hormonunun bazal düzeyi böbrek hastalığının derecesi ile orantılı olarak
yüksektir ve önemli bir aracısı olan insülin like growth-1 (IGF-I)’e karşı direnç vardır (43). Çocuklarda, büyüme geriliği gelişebilir ve bu durum fizyolojik dozun üstünde eksojen rekombinant büyüme hormonu verilmesi ile düzeltilebilir.
Erkeklerde prolaktin seviyeleri evre 5 KBH’da artar ve jinekomasti ve seksüel disfonksiyona katkıda bulunabilir. Testosteron seviyeleri sıklıkla düşük veya normaldir. Gonadotropinler artabilir ve testiküler disfonksiyonu işaret eder (45). Erkeklerdeki en önemli seksüel problem erektil disfonksiyondur. Bu endokrin bozukluklardan çok nörolojik, psikolojik ve vasküler anormalliklerden kaynaklanır ve sildanefil sitrat gibi fosfodiesteraz tip 5 inhibitörlerine yanıt verebilir.
Evre 4-5 KBH olan kadınlarda hipofizer-ovaryan aks bozulabilir (46). LH seviyeleri artmasına rağmen, normal pulsatil salınım ve preovulatuar pik yoktur. Bundan dolayı sikluslar sıklıkla anovulatuardır ve düzensiz olabilir veya amenore olabilir. Yükselmiş prolaktin seviyeleri de infertiliteye katkıda bulunabilir.
Nörolojik Komplikasyonlar
Üremide santral veya periferik sinir sisteminin tutulmasına bağlı olarak; Periferik nöropati, Otonom nöropati, Üremik ensefalopati, Uyku bozuklukları ve Huzursuz bacak gibi komplikasyonlar görülür.
GİS Komplikasyonları
KBH’ da aşağıda ki GİS hastalıklarının görülme sıklığı artmıştır. Gastroparezi GÖR Peptik Ülser Gastrit ve duodenit GİS Kanama Akut Pankreatit
Spontan Kolonik Perforasyon
Nonokluzif Mezenterik İskemi/Nekroz
Kronik böbrek hastalarının yaşam süresi azalmıştır. Diyaliz hastalarının erken ölüm sebeplerinin % 50’sine yakınını inme ve AMI, konjestif kalp yetmezliği gibi kalp hastalıkları oluşturur (47). Renal replasman tedavisindeki hastaların kardiyovasküler hastalıklardan dolayı erken ölüm riskinin beklenmedik bir şekilde arttığı görülmektedir. Günümüzde renal replasman tedavisinde olumlu gelişmelere rağmen son dönem böbrek yetmezlikli hastalarda, kardiyovasküler hastalık riski genel popülasyonla karşılaştırıldığında yaklaşık 10 ila 20 kat dahafazladır(48).
Şekil 1. Diyaliz hastalarında ölüm nedenleri ( Data from USRDS,2005 )
Kardiyovasküler mortalitenin en önemli nedeni ateroskleroz olmasına rağmen, KVH paterni bu hipervolemi ve sol ventikül hipertrofisinde atipiktir. Bunlara ilaveten, ani kardiyak ölüm, aritmiler, hipertansiyon, koroner arter hastalığı (KAH), periferik arter hastalığı, perikardit insidansı anlamlı derecede artmıştır ve kardiak arrest ve aritmi bu hasta populasyonunda kardiyovasküler ölümün major nedenidir. GFR’nin düşmesi ile HT’nun prevalansı progresif artar ve diyaliz hastalarının %75-%85’inde mevcuttur. Hipertansiyonun
sonucu olarak (ve diğer faktörler, örneğin; anemi, volum fazlalığı) KBH’ da LVH prevalansı artar. Bundan dolayı kronik böbrek hastaları KVH için yüksek riskli hasta grubu olarak değerlendirilmelidir. NKF bünyesindeki çalışma grubu, 1999 yılında KBH’nda artan kardiyovasküler riski vurgulayan bir rapor yayınlamıştır. Bu raporda KBH’nın KVH açısından en en yüksek risk sınıfında değerlendirilmesi, tedavi önerilerinin bu konu göz önünde bulundurularak yapılması gerektiği vurgulanmıştır (50).
Kardiyovasküler ölüm için artrmış risk genç kronik böbrek hastalarında en fazladır. Bilinen başlıca risk faktörleri (sigara, HT, yaş vb.) yanı sıra KBH ile ortaya çıkan hastalığa özgü risk faktörleri de KVH sıklığının artmasına sebep olur. Bu risk faktörleri: sıvı fazlalığı, anemi, proteinüri, hiperparatiroidizm, kalsiyum-fosfor metabolizmasındaki bozukluklar, malnütrisyon, inflamasyon, oksidatif stres, lipid metabolizma bozuklukları, hiperhomosisteinemi, üremik toksinler ve damar kalsifikasyonu olarak sıralanabilir (51,52). Fakat tüm bunlar bu hasta popülasyonundaki artmış kardiyovasküler riskin ancak yarısını açıklamaktadır.
Etyoloji ve Risk Faktörleri
Şekil.2. Kronik böbrek hastalığında risk faktörleri(ComprehensiveClinical Nephrology 2007)
Tablo 7: Kardiyovasküler risk faktörleri
Geleneksel Risk Faktörleri Yeni Risk Faktörleri Üremi Spesifik Risk Faktörleri
Erkek Cinsiyet İnflamasyon Volum Yüklenmesi
Sigara Endotel Disfonksiyonu Hiperhomosisteinemi
Diyabetes Mellitus Oksidatif Stres Üremik Toksinler
Hipertansiyon Sempatik Aktivasyon Vasküler Klasifikasyon
Sol Ventrikül Hipertrofisi Proteinlerin Karbamilasyonu Hiperparatiroidizm
İnsülin Rezistansı Anemi
Dislipidemi Fosfat retansiyonu
Geleneksel Risk Faktörleri Yaş, Cinsiyet ve Sigara
RRT alan birçok hastada yaşla birlikte KVH sıklığı artar. ABD’de diyalize başlayan hastaların yaş ortalaması 60 yaştan büyüktür ve ölüm riski yaşla yıllık %3 artar. Kronik böbrek hastalarının tüm yaş gruplarında MI insidansı erkeklerde, kadınlara göre yaklaşık 2,5 kat daha fazladır. Sigara, kronik böbrek hastalarında KVH’larla ilişkilidir. Yapılan
çalışmalarda KBH’nın çoğunda diyaliz öncesi sigara içimi mevcuttur. Sigaranın bırakılmasını önermek gerekmektedir.
Diabetes Mellitus
DM, SDBY’ nin en önemli nedenidir ve kardiyovasküler komplikasyonların prognozu bu hastalarda daha kötüdür. RRT başlayan diyabetik hastalar dislipidemi, hipertansiyon, artmış oksidatif stres, inflamasyon belirtilerini içeren birçok KVH risk profili gösterirler. Diyaliz başlanan diyabetik hastalar diyabetik olmayan SDBY’li hastalar ile karşılaştırıldığında DM’nin tüm ölümler ve kardiyovasküler hastalıklarla ilişkili ölümler için bağımsız bir risk faktörü olduğu şaşırtıcı değildir. Diyabetik hastalarda risk KAH için %65, erken ölüm için %36, MI sonrası ölüm için %34’ tür.
Hipertansiyon
İlerleyici kronik böbrek hastalığı olan hastaların % 60-90’ında diyaliz tedavisine
başlamadan önce sistemik hipertansiyon gelişir (53). Hem ekstrasellüler sıvı hacminin genişlemesi (54,55) hem de sempatik aşırı aktivite ve renin-anjiyotensin eksenine bağlı vazokontsrüksiyon (56) son dönem hastaları dahil böbrek hastalarındaki hipertansiyonun patogenezinde rol oynar.
HT, KVH için önemli bir risk faktörüdür. Düşük kan basıncı KBY hastalarının
mortalitesi ile koreledir. Artmış nabız basıncı ile birlikte izole sistolik hipertansiyon KBY hastalarında en sık görülen basınç anomalisidir. Damar sertliği artmış nabız dalga hızına neden olur ve erken yansıyan nabız dalgası tarafından artmış sistolik pik basıncı ile sonuçlanır. Sonuç olarak sol ventrikül disfonksiyonu ve sonunda KKY gelişir. HT, LVH’ne neden olarak KBH’daki kardiak hasarda önemli bir rol oynar (57). Foley ve arkadaşları ortalama kan basıncındaki artışın yaş, diyabet, iskemik kalp hastalığı, hemoglobin ve serum albumininde düzelme sağlandığında bile, SVH’da ilerleyici bir artışa, kalp yetmezliğine ve iskemik kalp hastalığına neden olduğunu göstermişlerdir (58).
Dislipidemi
KBH populasyonunda hiperkolesterolemi, KVH ve mortalite arasındaki ilişki zayıftır; çünkü kardiyomyopati ve ateroskleroz gibi kardiyovasküler anormalikler bu hastalarda dislipidemiye göre diğer faktörlerle daha fazla ilişkilidir. Paradoksal olarak yüksek serum kolesterolünden ziyade düşük serum kolesterolü diyaliz hastalarında düşük survey ile ilişkilidir (59). Bu ters epidemiyoloji malnütrisyon veya inflamasyon ile ilişkilidir. Birçok
SDBY hastasında trigiliserid seviyeleri artar, oysa total serum kolesterolu beslenme durumu ve inflamasyonun varlığına bağlı olarak artmış, düşük veya normal olabilir. HDL kolesterol tipik olarak azalmıştır ve LDL, VLDL, Lipoprotein (a) seviyeleri artmaya eğilimlidir. Artmış Lipoprotein (a) seviyeleri KVH için artmış mortalite ile ilişkilidir.
İnsülin Rezistansı
National Health and Nutrition Examination Survey (NHANES) verileri, farklı böbrek fonksiyon düzeyleri olan hastalarda metabolik sendromun, inflamasyon ile ilişkili olduğunu öne sürmüşlerdir (60).
Geleneksel Olmayan ve Üremi Spesifik Risk Faktörleri Oksidatif Stres
Böbrek ve böbrek dışı yapılan Kohort çalışmaları, artmış oksidatif stresin (serbest radikallerin fazlalığı) aterogenez ve aterosklerotik kardiyovasküler olaylar ve diğer SDBY komplikasyonları ile ilişkili olabildiğini göstermiştir. Vasküler duvarda reaktif oksijen türlerinin bulunması aterosklerozun karakteristik özelliğidir. Oksidatif stres, reaktif oksijen ürünleri ve antioksidan koruyucu sistemler arasındaki dengesizlikten kaynaklanır. Sadece reaktif oksijen ürünlerinin artması, oksidatif stres anlamına gelmez. Beraberinde antioksidan mekanizmaların da etkilenmesi, yani her ikisi arasındaki dengenin bozulması gerekir (61).
İnflamasyon
Diyaliz hastalarının çoğunda kronik inflamasyon mevcuttur (62). İnflamatuar yanıtın akut fazı, vücudun herhangi bir uyarıya karşı ( infeksiyon, travma vb.) ani bir şekilde başlattığı fizyolojik değişikliklerdir. Birçok çalışma CRP, IL-6, fibrinojen ve beyaz küre sayısı gibi çeşitli inflamasyon markerlarının, kronik böbrek hastalarının mortalitesi için güçlü ve bağımsız prediktörler olduklarını göstermiştir (62). KBH’da diğer bir güçlü sonuç belirleyici hipoalbuminemidir ve inflamatuar biyomarkerları ile güçlü biçimde ilişkilidir. İnflamatuar belirteç olan CRP ile proinflamatuar sitokinlerin artışı KBY hastalarında morbidite artışına yol açmaktadır. İnflamasyonda artan CRP, IL-1 ve IL-6 gibi proinflamatuar sitokinlerin ateş, halsizlik, iştahsızlık, bulantı-kusma, malnütrisyon ve ateroskleroz gibi çeşitli sistemik etkileri vardır. CRP ile birlikte IL-6, TNF-alfa vasküler kalsifikasyon, oksidatif stres ve endotel disfonksiyonu gibi aterojenik özelliklere sahip olabilirler.
Endotel disfonksiyonu KBH’nın önemli bir özelliğidir. KBH’da endotel disfonksiyonun nedenleri; inflamasyon, asimetrik dimetilarginin (ADMA) retansiyonu, oksidatif stres, hiperhomosisteinemi, dislipidemi, hiperglisemi ve hipertansiyondur.(63) NO sentazın endojen bir inhibitörü olan ADMA, böbrek yetmezliğinde birikir ve NO düzeyinde azalmaya sebep olur. NO düzeyindeki azalma, KBY ile ilişkili endotelyal disfonksiyonda, en önemli rolü oynamaktadır (64).
KBH’da endotelyal disfonksiyon hem büyük hem de küçük çaplı arterlerde izlenir (65). Mikroalbuminuri endotelyal disfonksiyon ile ilişkilidir ve onun bir göstergesi olabilir (66).
Anemi
Anemi iskemik kalp yetmezliğine sebep olmakla birlikte bundan bağımsız olarak da novo kalp yetmezliği ve mortalite artışı ile ilişkili bulunmuştur (67). Anemi SDBY’de LVH ve LV dilatasyonu için temel nedenlerdendir. Hemoglobin değerlerindeki her 1 gr/dl’lik düşme LV kitle indeksinde 10 gr/m² lik artışla sonuçlanmaktadır (67). Bazı çalışmalarda eritropoetin tedavisi ile LV dilatasyonunun ve LVH’ nin kısmen gerilediği gösterilmiştir (68,69).
Sekonder Hiperparatiroidizm ve Mineral Metabolizması
Kalsiyum ve fosfat metabolizması bozuklukları evre 3 KBH gibi erken evrelerde başlar. Ateroskleroz ve arteriel kalsifikasyon için potansiyel nedendirler. Çeşitli epidemiyolojik çalışmalar, hiperfosfatemi ve yüksek (kalsiyum x fosfor) çarpımının mortalitenin bağımsız, güçlü bir risk belirleyicisi olduğunu göstermiştir. Oysa hiperkalsemi orta risk taşır ve artmış immünreaktif paratiroid hormon (iPTH) zayıf risk taşır, fakat halen anlamlı riske sahiptir (70). Artmış serum fosfat düzeyleri de valvuler kalsifikasyon ve kardiak ölümler (özellikle KAH ve ani ölümden ileri gelen ölümler) ile ilişkilidir.
Kardiyovasküler Kalsifikasyon
Kardiyovasküler kalsifikasyon arterial media, arterosklerotik plaklar, miyokardium ve kalp kapaklarını tutabilir. Medial kalsifikasyon arteryel sertliğe neden olur ve sonuç olarak nabız basıncı artar. Sol ventrikül hipertrofisine ve artmış kardiyovasküler mortalite riskine yol açarlar. Vasküler kalsifikasyonu ölçmede ve tespit etmede değişik metodlar geliştirilmiştir. Bu metodlardan en önemli olan ikisi; EBCT (electron beam tomografi) ve multiplice spiral CT’dir. Diğer kullanılan metodlar ise; Ekokardiografi, Ultrason, CT, MR ve Angiografidir (71).
AGEs, proteinlerin nonenzimatik glikozilasyonu ve oksidatif reaksiyonlar sonucunda oluşmaktadır (72). In vivo olarak birkaç AGEs yapısal olarak biliniyor. Bunlardan N-carboxymethyl-lysine (CML), Pentozidin, İmiddazolon ve Pirralin dolaşımda proteine bağlı ve serbest olarak bulunur (72).
KBH’da N-carboxymethyl-lysine (CML), Pentozidin ve diğer ileri glikolizasyon son ürünleri birikir. Arteroskleroz ve diyaliz ilişkili amiloidoza katkıda bulunabilirler. Ancak ne yükselmiş Pentozidin ne de CML seviyeleri KBH’da mortaliteyi tahmin ettirmez ve diğer ileri glikozilasyon son ürünlerinin böbrek hastalarındaki rolü tam belli değildir.
Hiperhomosisteinemi
Hiperhomosisteinemi prevalansı evre 5 KBH’da % 90’dan fazladır. Böbrek fonksiyonları plazma homosistein konsantrasyonunun önemli bir belirleyicisidir. GFR yaklaşık 70 ml/dk’nın altına düştüğü zaman, serum homosistein düzeyleri ters orantılı olarak artmaya başlar. Homosistein aracılıklı vasküler hasar direkt endotelial toksisite yanısıra trombosit ve pıhtılaşma faktörlerindeki fonksiyonel bozukluklar nedeniyle de gelişmektedir. Yapılan çalışmalar homosistein düzeylerindeki artışın kardiyovasküler ve tüm nedenlere bağlı mortalite için önemli bir risk faktörü olduğu gösterilmiştir. SDBY hastalarında homosistein düzeyindeki her 10 μmol/l’lik artışın aterotrombotik olaylarda %35 risk artışına, fatal kardiyovasküler komplikasyonlarda %20’lik risk artışına neden olduğu rapor edilmiştir (73,74).
2.3. OKSİDATİF STRES VE KRONİK BÖBREK HASTALIĞI
2.3.1. Oksidatif Stres, Fizyopatolojisi, Kronik Böbrek Hastalığında Önemi 2.3.1.1. Oksidatif Stres
Oksidatif stres (OS), pro oksidan bileşiklerin oluşumuyla birlikte, yetersiz antioksidan savunma mekanizmaları arasındaki dengenin oksidan bileşiklerin lehine artması sonucu ortaya çıkan doku hasarı olarak tanımlanmaktadır (75). Prooksidanlar reaktif ürünler olup, reaktif nitrojen ürünleri (RNS) ve reaktif oksijen türleri (ROT) olarak iki gruba ayrılırlar. ROT; süperoksit radikalleri (O2ˉ), hidrojen peroksit (H2O2), nitrik oksit (NO), peroksit radikalleri (ROO*), hidroksil radikalleri (OH*) ve hypoklorus radikallerini kapsar ve bunlar hücrede normal metabolik bir olayın ürünüdürler (76).
Oksidatif bileşiklerin oluşumu, fizyolojik şartlarda inflamasyon ve doku tamiri sürecinde önemli bir basamaktır. Bu oluşum doku iyileşmesi ve yeniden oluşumuna katkısı yanında malign hücrelere ve vücuda giren mikroorganizmalara karşı savunma mekanizmasının önemli bir kısmını oluşturmaktadır. OS; ateroskleroz, hipertansiyon,
nörodejeneratif değişiklikler, yaşlanma ve malignite gelişmesi ile ilişkili bulunmuştur. Diğer taraftan, uygunsuz veya uyumsuz bir şekilde oksidatif süreç başlamasına, hücre ve doku hasarına neden olan üremi gibi bir takım kronik patolojik durumlar da söz konusu olabilir (77). Oksidatif stresi etkileyen faktörler şekil 3’de gösterilmiştir.
Şekil 3. Oksidatif stres belirteçleri havuzunu etkileyen faktörler
2.3.2.Serbest Radikaller ve Oksidanlar
Serbest radikaller; paylaşılmamış bir veya birden fazla elektrona sahip molekül veya atomlar olup, paylaşılmamış elektronun üzerinde bulunan oksijen molekülleridirler (75,78). Ya ortamda bulunan kimyasal veya fiziksel enerji kaynakların kovalent bağların hemolizi sonucu iki farklı paylaşılmamış olan elektron oluşturması ile ya da redoks reaksiyonu ile serbest radikal oluşumuna neden olur. Bu reaksiyonlarda bir elektron ya kaybedilir veya kazanılır.
A —> e- + A+ (Oksidasyon)
B+ e- —> B¯ (Redüksiyon-indüksiyon)
Her oksidasyon reaksiyonu bir redüksiyon reaksiyonu ile birliktedir ve oksidatif stres her iki reaksiyonda da meydana gelir. Serbest oksijen radikallerin aktiviteleri farklılık gösterir. Hidroksil (HOˉ) gibi bazı radikaller yüksek aktiviteye sahipken, E vitamininin oksidasyon ürünü olan tokoferoksil gibi bazı bileşiklerin aktiviteleri çok düşük olup ihmal edilebilir öneme sahiptirler (79). Serbest radikal, aynı maddeyi oksidant veya redüktant olarak
kullanabilir. Reaksiyonun oluşma hızı; ortamın ısısına, pH'sına ve ortamdaki katalizörlere bağlıdır (80).
2.3.2.1. Serbest Radikal Reaksiyonları
Oksijen radikalleri içinde, süperoksit anyonu (O2ˉ) , oksijenin bir elektron almasıyla oluşan ilk ürün olup, en kolay ve en fazla oluşan serbest radikaldir. Canlılarda diğer radikallerin oluşumu sıklıkla O2¯ nin birikimine bağlıdır. O2¯ radikalinin ana kaynağı ise
moleküler oksijenin metabolize edildiği, mitokondriyal elektron transport zinciridir (78,81) ve normal şartlarda oluşan O2ˉ ler organizmadan dismutasyon reaksiyonu ile uzaklaştırılır. Bu
reaksiyonlarla hidrojen peroksit (H2O2) ve perhidroksi (OH2¯) radikallerinin meydana gelir.
Dismutasyon reaksiyonları kendiliğinden ya da süperoksid dismutaz (SOD) ile katalizlenerek meydana gelebilir.
O
2¯ + H + —> HO2¯HO
2¯+ HO
2ˉ→ H
2O
2HO
2¯ +HO
2¯ →H
2O
2 +O
2O2¯ + O2¯→2 H
+→H2O¯ + O2
Oluşan H2
O
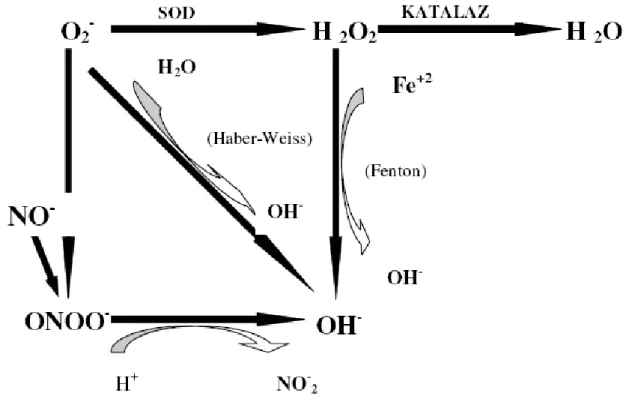
2, Süperoksit Dismutaz (SOD) gibi antioksidan enzim sistemlerinden olan katalaz (KAT) ve glutatyon peroksidaz (GSH-px) ile suya dönüştürülür (şekil 4). Serbest oksijen radikalleri içinde en fazla reaktif olan hidroksil (OH¯) radikalidir ve hemen her molekül ile reaksiyona girebilir. Süperoksit anyonu (O2¯ ) ve hidrojenperoksit (H2O2) etkileşir ve sonuçta OH− radikali meydana gelir.İskemi oluştuğunda ve de özellikle reperfüzyon ile dokuların oksijenasyonu ile oluşan bu reaksiyonu demir gibi metaloproteinler, askorbik asit ve NADPH katalize edebilir
Fe
+3+ 02ˉ --- Fe
+2+ O2
Fe
+2+H2O2 --- Fe
+3+OHˉ+ OH ˉ
Organizmada OHˉ radikaline karşı Süperoksid dismutaz (SOD), katalaz (KAT), glutatyon peroksidaz (GSH-px) gibi eritrosit kökenli bir antioksidan savunma mekanizmaları yoktur (82).
Şekil 4. Serbest Radikal Reaksiyonları 2.3.3 Reaktif Oksijen Türleri
Oksijen 8 atom numaralı kararsız bir elementtir. Enerji düzeylerindeki elektronlarının yapısıyla ilişkili olarak doğada dioksijen (O2) halinde bulunur (83). Oksijen molekülündeki
aynı yöne dönen iki elektrona sahip 2P son orbitali önemlidir ve bu orbitallerden herhangi birindeki elektron hareketleri "singlet oksijen" ve "oksijen radikali" meydana getirir. Reaktif oksijen türleri, biyoaktif lipitler (araşidonik asitler), lipit oksidasyonunun alt ürünleri, aldehitler, hücre içi enzim ve metalleri etkileyerek doku hasarı meydana getirirler (84). Tablo 8. Oksijen türevi bileşikleri
Oluşan radikal eşleşmemiş tek elektrona sahip olması nedeniyle dengesiz olup tek elektronlarını bir başka moleküle verebilir (redüksiyon) ya da başka molekülden elektron transfer ederek elektron çifti oluşturabilirler (oksidasyon). Sonuçta radikal olmayan yapıyı radikal şekle dönüştürebilirler (83).
2.3.3.1. Süperoksit Radikalleri (O2)
Süperoksit radikalleri (O2), hücrelerde redükte elektron taşıyıcılarının otooksidasyonu
ile oluşmaktadırlar. Zayıf bir oksidan olan O2 kendi başına önemli hücre hasarına yol
açmaz, ancak oksidatif strese yol açabilen bir dizi reaksiyonu tetikleyebilir (85). Bu reaksiyonların en önemlilerinden biri Haber-Weiss reaksiyonu olup, O2 ve H2O2 demir
varlığında etkileşerek oldukça reaktif olan ve DNA hasarı yapabilen HO radikalini oluştururlar (86).
O2+eˉ→ O2ˉ
H2O2+O2 → HOˉ +O2
O2 radikalleri, intasellüler demir depolarından demiri serbestleştirir ve serbest demir
iyonu Haber-Weiss gibi reaksiyonlarda veya diğer serbest radikal aracılıklı hücre hasarında rol alabilir. Superoksit radikalleri çok kısa bir yarı ömre sahip olup dismutasyon ile H2O2 ve
oksijen oluştururlar.
Şekil 5. Reaktif oksijen türlerinin oluşumu.
2.3.3.2. Hidroksil Radikalleri (HO)
Hidroksil radikali (HO), biyolojik sistemlerdeki en potent serbest radikaldir. Dokular radyasyona maruz kaldıklarında, enerjinin çoğu hücre içindeki su tarafından absorblanır ve radyasyon oksijen-hidrojen arasında kovalent bağa neden olur. Sonuçta biri hidrojen (H), diğeri hidroksil radikali (OH) olan iki radikal meydana gelir (85).
H — O — H —> H + OH
Hidrojen peroksitin (H2O2) Fe+2 veya Cu+2 ile reaksiyona girmesiyle de OH radikali
Fe
+2+ H2O2 → Fe
+3+ OH + OH
Cu
++ H2O2 → Cu
+2+ OH + OH
OH radikalleri başta lipid, protein ve nükleik asitler (DNA ve RNA) olmak üzere hemen tüm hücresel moleküllerle reaksiyona girebilirler. Nükleik asitlerle etkileşim, özellikle DNA içeriğinde bulunan bir karbonhidrat olan deoksiriboz ile reaksiyona girmesi çeşitli mutasyonlara ve mutant moleküllere neden olabilir. Ayrıca OH radikalleri, aromatik halkaya katılma özellikleri nedeniyle DNA ve RNA'daki pürin ve pirimidinlere katılarak serbest radikal oluşumuna yol açarlar. DNA'nın baz ve şekerlerinde ciddi hasarlar oluşturarak DNA'da iplik kırılmaları meydana getirir, büyük hasarlar hücresel koruyucu sistemler tarafından onarılamazlarsa çeşitli mutasyonlar ve hücre ölümleri görülür (85,87).
OH'ın sebep olduğu ve en iyi bilinen biyolojik hasarı, lipid peroksidasyonudur. Lipid peroksidasyonu hem intrasellüler hem de ekstraselüler antioksidan potansiyele sahiptir. OH, özellikle araşidonik asit gibi doymamış yağ asit yan zincirlerinden -C atomunun birinden H atomunun çıkartılması ve su oluşumu ile sonuçlandığı reaksiyonlarda olduğu gibi membran fosfolipitlerinin doymamış yağ asit yan zincirlerine hücum eder. Peroksil radikalleri, doymamış yağ asitlerinin yan zincirlerine saldırır; yağ asidinin yan zincirlerini lipit hidroperoksitlere dönüştürüp membranda lipit hidroperoksitlerinin birikimi de membran fonksiyonunun bozulmasına ve bazı enzimlerin aktive olmalarına neden olur (83,88,89).
2.3.3.3. Hidrojen Peroksit (H2O2)
Hidrojen peroksit (H2O2) aslında eşleşmemiş elektronu bulunmadığından bir radikal
değildir. Süperoksit anyonunun (O2ˉ ) hidrojenle yaptığı reaksiyona dismutasyon reaksiyonu
denir.
2O
2 + 2H + —> H2O2+ O2Reaksiyon hızı asidik pH'da fazladır (83,90). NADPH oksidaz ve Glukoz oksidaz gibi enzimler elektron eklenmesini katalizleyerek O2 veya H2O2 oluştururlar.
NADPH + 2O2 —> 2NADP + 2O2
R — CH2OH + O2 —> R — CHO — H2O2
2.3.3.4. Hipoklorik Asit (HOCl)
Hipoklorik asit (HOCl), radikal olmamasına rağmen reaktif oksijen türleri (ROT) içinde sınıflandırılır. Hipoklorik asit, bakterilerin fagositik hücreler tarafından öldürülmesinde
rol oynar. Aktive olan nötrofiller, monositler, makrofajlar (doku makrofajları da dahil) ve eozinofiller tarafından süperoksit radikalleri (O2) üretilir ve özellikle nötrofillerde
miyeloperoksidaz enzimi aracılığıyla önce O2 oluşturulur, daha sonra bu ürünün
dismutasyonuyla oluşan H2O2 klorür iyonuyla birleştirilerek potent bir antibakteriyel olan
HOCl meydana getirilir (83).
2.3.3.5. Singlet O2 (O2)
Yapısında eşleşmemiş elektron içermediğinden serbest radikal olmamasına rağmen serbest radikal reaksiyonlarını başlattığı için serbest radikal olarak kabul edilmiştir. O2,
oksijen elektronlarından birinin dışarıdan enerji alması sonucu kendi dönüş yönünün tersi yönünde bir yörüngeye yer değiştirmesi ile oluşabileceği gibi O2'nin dismutasyonu ve
H2O2'nin hipoklorit ile reaksiyonu sonucunda da meydana gelebilir. Deri ve retina gibi gün
ışığına maruz kalan bölgelerde sıkça oluştuğu saptanmıştır. Serbest oksijen radikallerinin etkisiyle peroksil (ROO), alkoksil (RO), tiol radikalleri (RS) veya karbon merkezli radikaller (R) meydana gelebilir (91).
2.3.3.6. Ozon (O3)
Ozon, güneş ışınlarına karşı önemli bir stratosferik koruyucu olmasına karşın yeryüzünde toksik/oksidan bir ajandır. Bazı bilimsel cihazlarla ve kirli şehir havasında bulunur. Akciğerlere zararlıdır, DNA, lipid ve proteinleri kolayca okside eder (92).
2.3.3.7. Reaktif Nitrojen Türleri (NO, NO2, NO+ , NO- )
Nitrik Oksit (NO), lipofilik özellikte oksijensiz ortamda kararlı, ortamda düşük konsantrasyonlarda oksijen varlığında dahi kararlılığını koruyabilen , biyolojik olarak aktif olan memeli hücrelerinin bilinen en küçük molekül ağırlıklı ürünüdür (93,94,95). Düşük dozlarda toksik değildir, hatta fizyolojik olarak kabul edilebilecek çok önemli fonksiyonları yapabilir (93). Vasküler endotel hücrelerinde, Nitrik Oksid Sentaz (NOS) enzimi aracılığıyla L-arjininden sentezlenir. NO'in yarı ömrü 10-20 saniye gibi çok kısa bir zamandır. Kolayca (özellikle) düz kas hücresine girerek Guanilat Siklaz (GC) enzimine bağlanır ve siklik guanozin monofosfat (cGMP) sentezini uyararak vazodilatasyon meydana getirir. NO, moleküler oksijen ile bağlanıp nitrojendioksit (NO2) oluşturarak metabolize olur (96). NO'in
molekül de biyolojik olarak oksidan özellik kazanabilmekte ve önemli patolojik süreçlerde rol oynayabilmektedir (95).
NO + o2ˉ —► ONOO
-ONOO
-+H
+—► ONOOH
ONOOH —► NO2 + OH
Sonuçta NO, endotel hücre disfonksiyonu ve bununla ilişkili olan DM, hipertansiyon, ateroskleroz gibi bazı önemli hastalıklarda etkili olabilmektedir.
2.3.4. Başlıca Serbest Radikal Üretim Kaynakları
Serbest radikaller, organizmada normal hücre metabolizması sırasında oksidasyon ve redüksiyon reaksiyonları sırasında oluşabildiği gibi çeşitli dış kaynaklı nedenlerle (stres, radyasyon, ksenobiyotikler, vs) de oluşabilir. Mitokondrial elektron transport sistemi (ETS), sitokrom P-450, ksantin oksidaz, triptofan dioksijenaz, lipooksijenaz, prostoglandin sentetaz, hemoglobin, flavoproteinler, lipid peroksidasyonu, iskemi, travma ve entoksikasyon gibi durumlar, katekolamin ve antibiyotikler gibi moleküller serbest radikalleri oluşturabilirler (91,97). Serbest radikal oluşturan kaynaklar endojen ve ekzojen olmak üzere iki gruba ayrılabilir.
2.3.4.1. Endojen Serbest Radikal Üretim Kaynakları
Fizyolojik koşullarda metabolizmada, bazı metabolik olayların idamesi için meydana gelen birçok biyokimyasal reaksiyonun çeşitli basamaklarında, serbest radikaller oluşmaktadır. Bunlar;
2.3.4.1.1a. Mitokondriyal Elektron Transport Sistemi (ETS)
Mitokondrideki enerji metabolizması sırasında O2 kullanılır ve bunun % 1-5 kadarı
süperoksit ile sonlanr. ETS'de, NADH dehidrogenaz ve koenzim Q gibi elektron taşıyıcılardan oksijene olan elektron transferiyle radikal oluşur. Fizyolojik koşullarda reaktif oksijen türlerinin temel kaynağı normal oksijen metabolizması olduğu için ETS serbest radikal üretiminin en önemli kaynağıdır (98).
2.3.4.1.1b. Endoplazmik Retikulum (ER)
ER'da bulunan sitokrum P-450 sistemi birçok substratı oksitleyebilir. Oksijen molekülünün bir atomu substrata bağlanırken, diğer atomu su oluşturur. Kimyasal ajanların
serbest radikal oluşturmadaki en önemli mekanizmaları, mikrozomal sitokrum P-450 sistemi aktivasyonudur ve bu sistemde moleküller ya indirgenerek ya da oksitlenerek serbest radikal oluşturulur. Oluşan serbest radikaller ve bunların ürünü olan tiyol (-SH) grubu birçok endojen makromolekülde (DNA, RNA, enzimler, vb) bulunduğu için reaktif ara ürünler oluşturup toksik etki gösterebilirler (98).
2.3.4.1.1c. Redoks Döngüsü
Ksenobiyotiklerden serbest radikaller mikrozomal reaksiyonlarla oluşturulduğu gibi redoks siklusu (menadion, nitrofurantoin, gibi ek elektron kazanma eğilimindeki bileşikler) yoluyla da meydana gelebilir. Oluşan radikaller, tekrar ana bileşiğe dönüşmek için oksijenle oksitlenir ve süperoksit radikalini meydana getirirler (99). Oluşan ksenobiyotik ve süperoksit radikalleri ferritinden demiri serbestleştirir, reaktif hidroksil radikali gibi ikincil radikallerin oluşumunu sağlar (85).
2.3.4.1.1d. Araşidonik Asit Metabolizması
Hücre membranlarındaki prostaglandinlerin kaynağı araşidonik asittir. Fagositik hücrelerin uyarılması, fosfolipaz ve protein kinazın aktivasyonu, plazma membranlarında araşidonik asidin salınımına neden olur. Araşidonik asit, peroksitlerle aktive olan iki enzim olan siklooksijenaz ve lipooksijenaz katalizlediği tepkimeler sırasında serbest radikaller meydana gelir (100). Siklooksijenaz aktivitesi daha sonra prostaglandinlerin sentezi içinde gerekli olan endoperoksitlerin oluşumuyla sonuçlanırken, lipooksijenaz lipit peroksitler üzerinden lökotrienlerin oluşumunu katalizler (100). Ayrıca bu sırada bazı ksenobiyotiklerden oluşan reaktif ara ürünler hedef moleküllerle etkileşerek toksisite gösterirler
2.3.4.1.1e. Fagositoz
Aktive fagositler patojen mikroorganizmalarla savaşta önem arzeden intrasellüler radikal oluşumuna neden olurlar (Tablo 9). Ksenobiyotikler, radyasyon ve stres aktive olmuş fagositlerde serbest radikal üretimini arttırırlar.
Tablo 9. Fagositlerin ürettiği reaktif oksidan ürünler.
Trombositler H2O2, O2 , OH. Nötrofiller H2O2, O2 OH, HOCl Eozinofiller H2O2, O2, OH, HOCl Makrofajlar H2O2, O2, OH, HOCl, NO