T.C.
SELÇUK ÜNĠVERSĠTESĠ FEN BĠLĠMLERĠ ENSTĠTÜSÜ
SIVI KRĠSTAL ÖZELLĠĞĠ GÖSTEREN OKSĠM TÜREVLERĠNĠN
SENTEZĠ VE OPTĠK ÖZELLĠKLERĠNĠN ĠNCELENMESĠ
Önder ALICI DOKTORA TEZĠ Kimya Anabilim Dalını
Ekim-2013 KONYA Her Hakkı Saklıdır
TEZ BĠLDĠRĠMĠ
Bu tezdeki bütün bilgilerin etik davranış ve akademik kurallar çerçevesinde elde edildiğini ve tez yazım kurallarına uygun olarak hazırlanan bu çalışmada bana ait olmayan her türlü ifade ve bilginin kaynağına eksiksiz atıf yapıldığını bildiririm.
DECLARATION PAGE
I hereby declare that all information in this document has been obtained and presented in accordance with academic rules and ethical conduct. I also declare that, as required by these rules and conduct, I have fully cited and referenced all material and results that are not original to this work.
İmza Önder ALICI Tarih: 07/10/2013
iv
ÖZET DOKTORA TEZĠ
SIVI KRĠSTAL ÖZELLĠĞĠ GÖSTEREN OKSĠM TÜREVLERĠNĠN SENTEZĠ VE OPTĠK ÖZELLĠKLERĠNĠN ĠNCELENMESĠ
Önder ALICI
Selçuk Üniversitesi Fen Bilimleri Enstitüsü Kimya Anabilim Dalı
DanıĢman: Prof. Dr. Ġbrahim KARATAġ 2013, 174 Sayfa
Jüri
Prof. Dr. Ġbrahim KARATAġ Prof. Dr. Ġbrahim EROL Prof. Dr. Mehmet SEZGĠN
Doç. Dr. Ahmet KOÇAK Doç. Dr. Ahmet COġKUN
Bu tez çalışmasında, önce α-kloro-mono oksim türevleri sentezlenmiştir. Sonra sıvı kristal özellik gösteren çeşitli amin türevleri sentezlenmiştir. Elde edilen bu aminler ile α-kloro-mono oksim bileşiklerinin reaksiyonlarından literatürde bulunmayan yeni oksim türevleri sentezlenmiştir. Ancak bu sübstitüe amino oksim bileşiklerinin sıvı kristal özellikleri göstermediği tespit edilmiştir.
Çalışmanın ikinci bölümünde ise daha farklı bir yol izlenerek sıvı kristal özellik gösteren 4′-(n-bromoalkiloksi)bifenil-4-karbonitril türevleri sentezlenmiştir. Daha sonra bu bileşikler ile
p-hidroksibenzaldehit‟ in kondensasyon reaksiyonu soncu farklı aldehit türevleri elde edilmiştir. Bu
bileşiklerin aldehit grupları hidroksilamin ile oksim bileşiklerine dönüştürülmüştür. Böylece yeni oksim bileşikleri sentezlenmiştir. Daha sonra bu oksim bileşikleri metil iyodür yardımı ile O-alkil eter bileşikleri elde edilmiştir. Bu yeni bileşiklerin sıvı kristal özellikleri DSC ve POM yöntemleri kullanılarak aydınlatılmıştır.
Çalışmanın üçüncü ve son bölümünde ise önceden sentezlenen 4′-(n-bromoalkiloksi)bifenil-4-karbonitril türevleri ile 2,4-dihidroksi benzaldehit‟ in kondensasyonu sonucu dimer aldehit türevleri elde edilmiştir. Elde edilen bu dimer aldehit türevlerinden ise yeni oksim bileşikleri elde edilmiştir. Böylece literatürde bulunmayan yeni dimer sıvı kristal oksim bileşikleri sentezlenmiştir.
Sentezlenen bütün yeni bileşiklerin yapıları FT-IR, 1
H-NMR ve 13C-NMR teknikleri kullanılarak aydınlatıldı.
Anahtar Kelimeler: Alkilasyon, Differential Scanning Calorimetry (DSC), Polarize Optik Mikroskop (POM), Oksimler, Sıvı Kristal
v
ABSTRACT Ph.D THESIS
SYNTHESIS OF OXIME DERIVATIVES SHOWING LIQUID CRYSTAL PROPERTY AND INVESTIGATION OF THEIR OPTICAL PROPERTIES
Önder ALICI
THE GRADUATE SCHOOL OF NATURAL AND APPLIED SCIENCE OF SELÇUK UNIVERSITY
DEPARTMENT OF CHEMISTRY Advisor: Prof. Dr. Ġbrahim KARATAġ
2013, 174 Pages Jury
Prof. Dr. Ġbrahim KARATAġ Prof. Dr. Ġbrahim EROL Prof. Dr. Mehmet SEZGĠN
Doç. Dr. Ahmet KOÇAK Doç. Dr. Ahmet COġKUN
In this study, firstly, the α-chloro-mono-oxime derivatives were synthesized as starting materially. After then, various amine derivatives liquid crystal properties were synthesized. Reaction was realized of α-chloro-mono-oxime derivatives with these amines and new oxime derivatives, not found the literature, were synthesized. These derivatives of new oxime were determined to not having liquid crystal properties.
In the second part of the study, 4′-(n-bromoalkyloxy)biphenyl-4-carbonitrile derivatives showing liquid crystal the property were synthesized. After then, condensation reaction was determined to p-hydroxybenzaldehyde with this compound and new aldehyde derivatives were synthesized. This aldehyde derivatives were converted to new oxime derivatives, not found the literature. After of all, these new oxime derivatives were converted to oxime ether derivatives with iodomethane. Liquid crystal properties of these new compounds were determined by using techniques DSC and POM.
In the last section of the study, 4′-(n-bromoalkyloxy)biphenyl-4-carbonitrile derivatives was recognised to condensation reaction with 2,4-dihydroxybenzaldehyde, and new aldehyde derivatives were synthesized. So, new dimer liquid crystal oxime derivatives were synthesized.
Structures of the new compounds were determined by using techniques of FT-IR, 1H-NMR and
13C-NMR.
Keywords: Alkylation, Differential Scanning Calorimetry (DSC), Liquid Crystals, Polarized Optical Microscopy (POM), Oximes
vi
ÖNSÖZ
Bu çalışma, Selçuk Üniversitesi Fen Fakültesi Kimya Bölümü Öğretim Üyelerinden Prof. Dr. İbrahim KARATAŞ yönetiminde hazırlanarak, Selçuk Üniversitesi Fen Bilimleri Enstitüsüne Doktora tezi olarak sunulmuştur.
Doktora tezimi yöneten ve çalışmalarımın her safhasında yakın ilgi ve yardımlarını gördüğüm ve bana her zaman destek olan değerli hocam Prof. Dr. İbrahim KARATAŞ‟ a saygı ve şükranlarımı sunmayı bir borç bilirim.
Ayrıca çalışmalarım sırasında yardımlarını esirgemeyen, Arş. Gör. Dr. Begüm TABAKCI, Arş. Gör. Dr. Sait MALKONDU, Uzman Dr. Serkan ERDEMİR ve Uzman İlker AKIN‟ a teşekkürlerimi sunarım.
Tahsil hayatım boyunca bana maddi ve manevi destek olan aileme, ayrıca hayatımın bu zorlu döneminde bana sabırla ve özenle destek olan sevgili eşim Meliha Kutluca ALICI‟ ya ayrıca teşekkürü bir borç bilirim.
Yine tez çalışmama 09101038 proje numarasıyla maddi destek sağlayan Selçuk Üniversitesi Bilimsel Araştırma Projesi Daire Başkanlığına teşekkürü bir borç bilirim.
Önder ALICI KONYA-2013
vii ĠÇĠNDEKĠLER ÖZET ... iv ABSTRACT ... v ÖNSÖZ ... vi ĠÇĠNDEKĠLER ... vii
SĠMGELER VE BAZI KISALTMALAR ... ix
ġEKĠLLER DĠZĠNĠ ... x
1. GĠRĠġ ... 1
1.1. OKSİMLER ... 1
1.1.1. Oksimlerin Spektroskopik Özellikleri ... 3
1.1.2. Oksimlerin Eldesi ... 5
1.1.3. Oksimlerin Reaksiyonları ... 7
1.1.4. Oksimlerin Kullanım Alanları ... 13
1.2. SIVI KRİSTALLER ... 15 1.2.1. Sıvı Kristallerin Tarihi ... 15 1.2.2. Sıvı Kristaller ve Özellikleri ... 16 1.2.3. Sıvı Kristallerin Sınıflandırılması ... 18 1.2.3.1. Liyotropik Sıvı Kristaller ... 19 1.2.3.2. Termotropik Sıvı Kristaller ... 20 1.2.3.2.1. Kalamitik Sıvı Kristaller ... 21 A) Nematik Sıvı Kristaller ... 24 B) Simektik Sıvı Kristaller ... 24
C) Kolesterik (Kiral) Sıvı Kristaller ... 26
1.2.3.2.2. Diskotik Sıvı Kristaller ... 27
1.2.4. Sıvı Kristallerin Kullanım Alanları ... 29
1.2.5. Sıvı Kristallerin Karakterizasyonu ... 30 2. KAYNAK ARAġTIRMASI ... 32 2.1. Sıvı Kristal Oksimler ... 32 3. MATERYAL VE YÖNTEM ... 35 3.1. Kullanılan Maddeler ... 35 3.2. Kullanılan Aletler ... 35 4. DENEYSEL BÖLÜM ... 36 4.1. p-Bromobenzaldoksim (1) ... 36 4.2. α-Kloro-p-bromobenzaldoksim (2) ... 37 4.3. p-Nitrobenzaldoksim (3) ... 37 4.4. α-Kloro-p-nitrobenzaldoksim (4) ... 38 4.5. N-(6-Bromohegzil)ftalimit (5) ... 38 4.6. N-(10-Bromodekan)ftalimit (6) ... 39
viii 4.7. 4'-(3-(1,3-Dioksoisoindolin-2-yl)propoksi)-[1,1'-bifenil]-4-karbonitril (7) ... 40 4.8. 4'-(6-(1,3-Dioksoisoindolin-2-yl)hegziloksi)-[1,1'-bifenil]-4-karbonitril (8) ... 41 4.9. 4'-(10-(1,3-Dioksoisoindolin-2-yl)desiloksi)-[1,1'-bifenil]-4-karbonitril (9) ... 42 4.10. 4'-(3-Aminopropoksi)bifenil-4-karbonitril (10) ... 43 4.11. 4'-(6-Aminohegziloksi)bifenil-4-karbonitril (11) ... 44 4.12. 4'-(10-Aminodesiloksi)bifenil-4-karbonitril (12) ... 44 4.13. α-[4'-(3-Aminopropoksi)bifenil-4-karbonitril]-p-bromobenzaldoksim (13) ... 45 4.14. α-[4'-(6-Aminohegziloksi)bifenil-4-karbonitril]-p-bromobenzaldoksim (14) ... 46 4.15. α-[4'-(10-Aminodesiloksi)bifenil-4-karbonitril]-p-bromobenzaldoksim (15) ... 47 4.16. α-[4'-(3-Aminopropoksi)bifenil-4-karbonitril]-p-nitrobenzaldoksim (16) ... 48 4.17. α-[4'-(6-Aminohegziloksi)bifenil-4-karbonitril]-p-nitrobenzaldoksim (17) ... 49 4.18. α-[4'-(10-Aminodesiloksi)bifenil-4-karbonitril]-p-nitrobenzaldoksim (18) ... 50 4.19. 4′-(6-Bromohegziloksi)bifenil-4-karbonitril (19) ... 51 4.20. 4′-(8-Bromooktiloksi)bifenil-4-karbonitril (20) ... 52 4.21. 4′-(10-Bromodesiloksi)bifenil-4-karbonitril (21) ... 53 4.22. 4-(6-[4'-Siyanobifenil-4-alkiloksi]hegziloksi)benzaldehit (22) ... 53 4.23. 4-(8-[4‟-Siyanobifenil-4-alkiloksi]oktiloksi)benzaldehit (23) ... 55 4.24. 4-(10-[4'-Siyanobifenil-4-alkiloksi]desiloksi)Benzaldehit (24) ... 55 4.25. 4-(6-[4'-Siyanobifenil-4-alkiloksi]hegziloksi)benzaldoksim (25) ... 56 4.26. 4-(8-[4'-Siyanobifenil-4-alkiloksi]oktiloksi)benzaldoksim (26)... 57 4.27. 4-(10-[4'-Siyanobifenil-4-alkiloksi]desiloksi)benzaldoksim (27) ... 58 4.28. 4-(6-[4'-Siyanobifenil-4-alkiloksi]hegziloksi)benzaldoksimmetileter (28) ... 59 4.29. 4-(8-[4'-Siyanobifenil-4-alkiloksi]oktiloksi)benzaldoksimmetileter (29) ... 60 4.30. 4-(10-[4'-Siyanobifenil-4-alkiloksi]desiloksi)benzaldoksimmetileter (30) ... 61 4.31. 2,4-Di-(6-[4'-siyanobifenil-4-alkiloksi]hegziloksi)benzaldehit (31) ... 62 4.32. 2,4-Di-(8-[4'-siyanobifenil-4-alkiloksi]oktiloksi)benzaldehit (32) ... 63 4.33. 2,4-Di-(10-[4'-siyanobifenil-4-alkiloksi]desiloksi)benzaldehit (33) ... 64 4.34. 2,4-Di-(6-[4'-siyanobifenil-4-alkiloksi]hegziloksi)benzaldoksim (34) ... 65 4.35. 2,4-Di-(8-[4'-siyanobifenil-4-alkiloksi]oktiloksi)benzaldoksim (35) ... 66 4.36. 2,4-Di-(10-[4'-siyanobifenil-4-alkiloksi]desiloksi)benzaldoksim (36) ... 68
5. ARAġTIRMA SONUÇLARI VE TARTIġMA ... 69
5.1. Sentezlenen Bileşiklerin Karakterizasyonu ... 69
5.2. Bileşiklerin Sıvı Kristal Davranışları ... 78
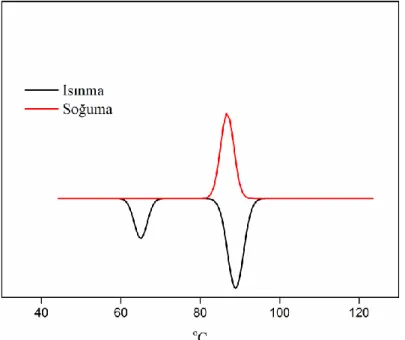
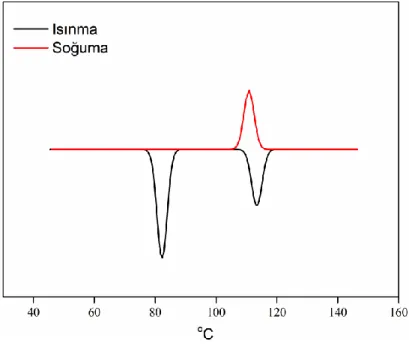
5.2.1. Diferansiyel Taramalı Kalorimetri (DSC) Sonuçları ... 78
5.2.2. Polarize Optik Mikroskop (POM) Sonuçları ... 89
6. SONUÇLAR VE ÖNERĠLER ... 96
KAYNAKLAR ... 98
EKLER ... 105
EK-1 Sentezlenen Maddelerin FT-IR Spektrumları ... 105
EK-2 Sentezlenen Maddelerin 1H-NMR Spektrumları ... 123
EK-3 Sentezlenen Maddelerin 13C-NMR Spektrumları ... 141
ix
SĠMGELER VE BAZI KISALTMALAR
DMF N,N-Dimetilformamit
DMSO Dimetilsülfoksit
CH2Cl2 Diklormetan
CDCl3 Dötoro kloroform
DMSO-d6 Dötoro dimetilsülfoksit
EtOAc Etil Asetat
EtOH Etanol
THF Tetrahidrofuran
NCS N-Klorosüksinimit
POM Polarize Optik Mikroskop
DSC Diferential Scanning Calorimetry
EN Erime Noktası
FT-IR Fourier Transform Infrared Spectroscopy 1
H-NMR Hidrojen Nükleer Manyetik Rezonans Spektroskopisi 13
C-NMR Karbon Nükleer Manyetik Rezonans Spektroskopisi
x
ġEKĠLLER DĠZĠNĠ
ġekil 1.1 Monooksimlerde geometrik izomeri ... 2
ġekil 1.2 Ketoksimlerde geometrik izomeri ... 2
ġekil 1.3 vic-Dioksimlerde geometrik izomeri ... 2
ġekil 1.4. Oksimlerin Hidroksilamin ile Sentezi ... 5
ġekil 1.5. Ketonların Nitrosolanması ile Oksim Eldesi ... 5
ġekil 1.6. Ketoksimlerden Dioksim Eldesi ... 6
ġekil 1.7. Ketoksimler ile Aminlerin Reaksiyonu ... 6
ġekil 1.8. Dioksimlerin Kloralhidrat‟ tan Eldesi ... 6
ġekil 1.9. Aminlerden Oksim Eldesi ... 6
ġekil 1.10. Ketiminlerden Oksim Eldesi ... 7
ġekil 1.11. Oksimlerde İzomerlik Dönüşümleri ... 7
ġekil 1.12. Oksimlerin Bozunma Reaksiyonu ... 7
ġekil 1.13. Oksimlerin İndirgenme Reaksiyonu ... 8
ġekil 1.14. Oksimlerin Yükseltgenmesi ... 8
ġekil 1.15. Oksimlerde Beckmann Çevrimi ... 8
ġekil 1.16. Oksimlerin Klorlanması ... 9
ġekil 1.17. α-Kloro Oksimlere Amin Türevlerinin Katılması ... 9
ġekil 1.18. Kloroglioksimler ile Amin Türevlerinin Reaksiyonu ... 10
ġekil 1.19. Dikloroglioksimler ile Diamin Polimerizasyonu ... 10
ġekil 1.20. Oksimlerden Nitril Oksit Eldesi ... 11
ġekil 1.21. Oksimlerin Alkilasyonu ... 11
ġekil 1.22. Oksimlerin Açilasyonu ... 11
ġekil 1.23. Dioksimlerin genel kompleks yapıları ... 12
ġekil 1.24. vic-Dioksimlerin amphi-formlarının Ni(II) kompleksi ... 13
ġekil 1.2.1. Kolesteril benzoat (Ph-COO-Kolest-5-en (KB)‟ ın yapı formülü ... 15
Faz Geçişleri K 145.5 N* 178.5 Iso ... 15
ġekil 1.2.2. Sıvı Kristal Genel Gösterimi ... 17
ġekil 1.2.3. Sıvı Kristallerde Düzen Parametresi ... 18
ġekil 1.2.4. Sıvı kristallerin Sınıflandırılması ... 19
ġekil 1.2.5. Liyotropik sıvı kristal örneği ... 19
ġekil 1.2.6.Termotropik Sıvı kristallerde Faz Geçişler ... 20
ġekil 1.2.7. Kalamitik Sıvı Kristallerin Genel Yapısı (a>>b) ... 21
ġekil 1.2.8. 4-metoksibenziliden-4‟-n-butilanilin (MBBA) (K 22 o C, N 47 oC Iso) ... 22
ġekil 1.2.9. 4-n-Pentil-4‟-siyanobifenil (5CB) (K 18 o C, N 36 oC Iso) ... 22
ġekil 1.2.10. Nematik Faz Düzenlenmesi (Solda), 1,5-Hegandiol-bis{4-[4-(4-n oktiloksi-benzoiloksi)benzilidinamino]benzoat}bileşiğinin Nematik Faz POM Görüntüsü (Sağda) ... 24
ġekil 1.2.11. Simektik Faz Düzenlenmesi (Solda), Simektik Faz POM Görüntüsü (Sağda) ... 25
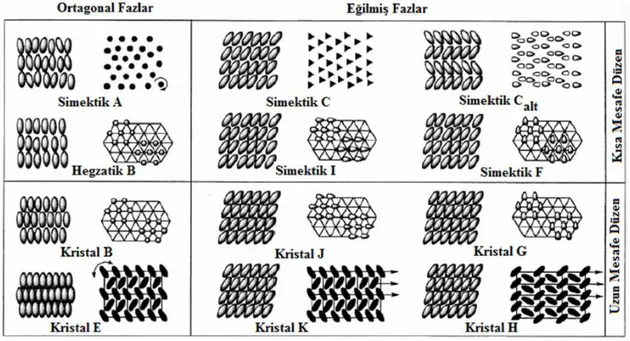
ġekil 1.2.12. Farklı Simektik Faz Düzenlenmeleri ... 25
ġekil 1.2.13. Simektik A tabakaların düzenlenmesi ... 26
ġekil 1.2.14. Simektik C tabakaların düzenlenmesi ... 26
ġekil 1.2.15. Hidroksipropil selüloz (Solda) ve Kolesteril benzoat (Sağda) ... 27
ġekil 1.2.16. Kolesterik sıvı kristallerin içindeki heliksel yapı gösterimi ... 27
ġekil 1.2.17. Diskotik Sıvı Kristallerin Genel Yapısı (Solda) Diskotik Sıvı Kristale Örnek (Sağda) ... 28
ġekil 1.2.18. Kolumnar diskotik faz gösterimi ... 28
ġekil 1.2.19. Nematik diskotik faz gösterimi ... 29
xi
ġekil 2.1.1. Sıvı Kristal Oksim Kompleksi ... 32
ġekil 2.1.2. Sıvı Kristal Oksim Bileşikleri Serisi ... 33
ġekil 2.1.3. Sıvı Kristal Oksim Ester Türevleri ... 33
ġekil 5.1. Oksim Bileşiklerin Sentez Şeması ... 69
ġekil 5.2. Aminlerin Sentez Şeması ... 70
ġekil 5.3. Yeni Oksim Bileşiklerinin Sentez Şeması... 72
ġekil 5.4. 4′-(n-bromoalkiloksi)bifenil-4-karbonitril Türevlerinin Sentez Şeması ... 74
ġekil 5.5. Sıvı Kristal Oksim ve Oksim Eterlerin Sentez Şeması ... 75
ġekil 5.6. Dimer Aldehit ve Oksim Bileşiklerin Sentez Şeması ... 77
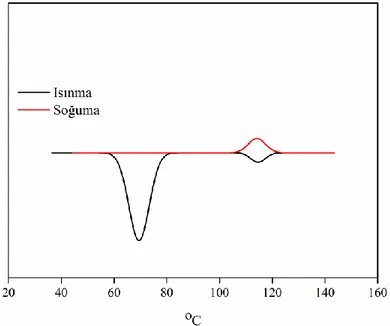
ġekil 5.2.1.1. Bileşik 22‟ nin DSC Grafiği ... 79
ġekil 5.2.1.2. Bileşik 23’ ün DSC Eğrisi ... 80
ġekil 5.2.1.3. Bileşik 24‟ ün DSC Eğrisi ... 80
ġekil 5.2.1.4. Bileşik 25‟ in DSC Eğrisi ... 81
ġekil 5.2.1.5. Bileşik 26‟ nın DSC Eğrisi ... 82
ġekil 5.2.1.6. Bileşik 27‟ nin DSC Eğrisi ... 82
ġekil 5.2.1.7. Bileşik 28‟ in DSC Eğrisi ... 83
ġekil 5.2.1.8. Bileşik 29‟ un DSC Eğrisi ... 84
ġekil 5.2.1.9. Bileşik 30‟ un DSC Eğrisi ... 84
ġekil 5.2.1.10. Bileşik 31‟ in DSC Eğrisi ... 85
ġekil 5.2.1.11. Bileşik 32‟ nin DSC Eğrisi ... 86
ġekil 5.2.1.12. Bileşik 33‟ ün DSC Eğrisi ... 86
ġekil 5.2.1.13. Bileşik 34‟ ün DSC Eğrisi ... 87
ġekil 5.2.1.14. Bileşik 35‟ in DSC Eğrisi ... 88
ġekil 5.2.1.15. Bileşik 36‟ nın DSC Eğrisi ... 88
ġekil 5.2.2.1. Bileşik 22‟ nin POM Görüntüsü ... 89
ġekil 5.2.2.2. Bileşik 23‟ ün POM Görüntüsü ... 90
ġekil 5.2.2.3. Bileşik 24‟ ün POM Görüntüsü ... 90
ġekil 5.2.2.4. Bileşik 25‟ in POM Görüntüsü ... 91
ġekil 5.2.2.5. Bileşik 27‟ nin POM Görüntüsü ... 92
ġekil 5.2.2.6. Bileşik 28‟ in POM Görüntüsü ... 92
ġekil 5.2.2.7. Bileşik 29‟ un POM Görüntüsü ... 93
ġekil 5.2.2.8. Bileşik 30‟ un POM Görüntüsü ... 93
ġekil 5.2.2.9. Bileşik 31‟ in POM Görüntüsü ... 94
ġekil 5.2.2.10. Bileşik 33‟ ün POM Görüntüsü ... 94
1. GĠRĠġ
1.1. OKSĠMLER
Oksimler aldehit ve ketonların bazik ortamda hidroksilamin hidroklorür ile verdikleri kondensasyon ürünü olarak bilinmektedirler. Genel formülleri RCH=NOH veya R1R2C=NOH olarak gösterilirler. Oksim kelimesi oksi-imin kelimelerinden gelmektedir. Oksimler türetildikleri aldehit ve ketonların sonlarına oksim kelimesi eklenerek isimlendirilebildiği gibi (benzaldoksim, asetonoksim, benzofenonoksim), ana grup keton ve aldehit olmak şartıyla “hidroksimino” eki ile de isimlendirilmektedir. Örneğin CH3-CH2-C(NOH)-COOH bileşiği, 2-hidroksimino bütanonik asit olarak isimlendirilir. İlk oksim çalışması Meyer tarafından 1882 yılında yapılmıştır. Aşağıda bazı oksimlerin isimlendirilmeleri verilmiştir.
a) Benzaldoksim b) α-Naftaldoksim c) Asetofenon oksim Oksimler genellikle renksiz, orta derecede erime noktasına sahip maddelerdir. Kendi kaynama noktalarında bozulmazlar. Oksimler amfoter özellik göstermektedir. Oksimlerin asitlik özellikleri OH grupları üzerindeki oynak protonlardan kaynaklanır. Buna karşılık, azot atomu üzerindeki ortaklanmamış elektron çifti nedeniyle zayıf bazik özellik gösterirler. Bu yüzden suda az, asit ve bazların seyreltik çözeltilerinde kolayca çözünmektedir. Basit oksimlerin pKa‟ları 10 ile 12 arasındadır. vic-Dioksimler ise monooksimlerden daha kuvvetli asidik özellik gösterir. α-Keto grubu, oksimlerde asitlik gücünü artırmaktadır ve bu tip oksimlerin pKa‟ları 7-10 arasında değişmektedir. Bu yüzden α-dioksimler, monooksimlerden daha kuvvetli asittir (Hüseyinzade ve İrez, 1990).
Oksimler ve türevlerinin geometrik özellikleri ile izomerleri cis (syn) ve anti ön ekleriyle anlatılmaktadır (Smith, 1966).Syn ön eki oksim grubunun çift bağı etrafındaki hidrojen ve hidroksil ile aynı tarafta, anti ön eki ise zıt tarafta olması halinde kullanılır. Şekil 1.1‟ de bu fark gösterilmiştir.
syn- Benzaldoksim anti-Benzaldoksim e.n: 35 ºC e.n: 132 ºC
ġekil 1.1 Monooksimlerde geometrik izomeri
Ketoksimlerde syn- ve anti- ön ekleri referans alınarak sübstientin yerine göre seçilir. Bununla beraber bu izomerlerin gösterimi, Cahn-Ingold-Prelog sistemine dayanır (C.I.P kuralı). Bunun için önce karbon atomundaki iki grup birbirini izleme kuralına göre sıralanır. Sonra izomer çift bağın [C=N] aynı tarafta sıralı olan –OH grubunun aynı tarafta olmasına göre Z izomeri syn, E izomeride anti olarak bilinir (Patai, 1970). Şekil 1.2‟ de, etilmetilketoksim iki şekilde yazılarak, OH ve etil grubunun farklı tarafta olması anti- (E) ekini, aynı tarafta olması syn- (Z) ekini almasına neden olur.
anti- Etil metil ketoksim syn-Etil metil ketoksim E- Etil metil ketoksim Z-Etil metil ketoksim
ġekil 1.2 Ketoksimlerde geometrik izomeri
vic-Dioksimlerin izomerleri ise, OH gruplarının, birbirlerinin pozisyonlarına bağlı olarak kullanılmaktadır. OH gruplarının aynı tarafa yönlendiği yapılar syn (Z-Z), zıt tarafa yönlendiği yapılar anti (E-E) ve birbirine paralel yönlendiği yapılar amphi (Z-E) olarak adlandırılır (Nesmeyanov ve ark., 1974)
syn (Z-Z)-Fenilglioksim amphi (Z-E)-Fenilglioksim anti (E-E)-Fenilglioksim E.N:212-214 0C E.N: 164-166 0C E.N: 243-244 0C
Syn, anti ve amphi formlarında olan oksimler birbirlerinden farklı özellikler taşırlar. Örneğin bazı istisnalar hariç syn ve amphi formlarının erime noktaları anti formlarına göre daha düşüktür (Smith, 1966). Dioksim türü bileşiklerde anti, amphi ve syn izomerlere göre daha düşük enerjili, yani daha kararlıdır (Nesmeyanov, 1974). Aynı zamanda oksimlerin anti formu organik reaksiyonlar için daha uygundur. Birçok katılma ve ayrılma reaksiyonları anti formda oluşur (Burakevich ve ark., 1971).
1.1.1. Oksimlerin Spektroskopik Özellikleri
Oksimlerin UV-VIS spektrumlarında, en önemli ve karakteristik absorpsiyon bandı C=N grubunun n---->Π* elektronik geçişine ait band olup, yaklaşık 250-300 nm aralığında gözlenir. Bu bileşiklerin geçiş metalleri ile oluşturduğu komplekslerde n---->Π* geçişine ait bantlar bir miktar uzun dalga boylarına kaymaktadır. Ancak özellikle aromatik halka içeren bileşiklerde bu geçişlere ait absorpsiyon bantları, aromatik halkaya ait B bantları ile girişim yapabilmektedir.
1,2-Fenilen-bis(aminoglioksim) için etil alkolde 280, 255, 245 nm‟ lerde absorpsiyon bantları gözlenmesine karşılık, dimetilformamid (DMF) içinde Cu(II) kompleksi 360, 288 ve 269 nm‟ lerde ve Ni(II) kompleksi ise DMF‟ de 448, 343, 280 ve 268 nm‟ lerde absorpsiyon pikleri vermektedir (Koçak, 1984).
Aldoksim ve ketoksimler için karakteristik IR bantları 3300-3130 cm-1 deki (OH), 1660-1600 cm-1 (C=N) ve 1000-930 cm-1 deki (NO) titreşimleridir (Avram ve ark., 1972; Ungnade ve ark. 1963; Burger ve ark. 1965; Silverstein ve ark. 1974). Seyreltik çözelti veya gaz halinde spektrum alındığında oksimin (O-H) grubuna ait gerilme titreşimi 3600-3500 cm-1 gözlenir; bunun sebebi O-H grubunun serbest olmasıdır. Vic-dioksimlerde (O-H) gruplarının birbirine göre üç farklı pozisyonda bulunmaları mümkündür. Anti formundaki oksimlerde bulunan (O-H) gerilme titreşiminin amphi formundakilere nazaran daha yüksek frekansta bulunduğu literatürlerde belirtilmektedir (Avram ve Mateescu, 1972; Serin ve Bekaroğlu, 1983).
Doymuş, konjuge olmayan oksimlerde (C=N) bandı 1685-1650 cm-1 yakınlarına kadar kayabilir. Anti-glioksimlerde (C=N) titreşiminin 1621 cm-1 civarında zayıf bir band olarak görülmesi, merkez simetrili bir yapıda olmalarından ileri gelir; anti-kloroglioksimde s-cis yapısını doğrulayacak şekilde orta şiddette bir dublet (1626, 1592 cm-1) halindedir.
Oksimlerde bir çift bağa komşu (N-O) titreşimine tekabül eden (N-O) bandı, 970-925 cm-1 arasında şiddetli bir absorpsiyon gösterir (Brown, 1955). (N-O) frekansı konfigürasyona bağlı olarak önemli bir değişiklik göstermez, ancak oksim grubuna bağlı sübstitüentlerin niteliğine göre değişir. Örneğin; Dimetilglioksim‟ de 952 cm-1
, anti-kloroglioksim‟ de 978 cm-1, anti-dikloroglioksim‟ de 1000 cm-1 (Avram ve Mateescu, 1972; Ungnade ve ark., 1963).
Dioksimler amphi yapısında bulunduğunda, oksim gruplarına ait protonlardan biri, komşu oksimin azotu ile hidrojen köprüsü oluşturur ve yapıdaki O-H gruplarının çevreleri farklılanmış olur. Siklohegzandiondioksim ve oluşturduğu kompleksin IR spektrumları karşılaştırıldığında ligand için 3380 cm-1
de gözlenen O-H titreşim bandı kompleks için 1775 cm-1
de, ligand için 1640 cm-1 de gözlenen C=N titreşim bandı kompleks için 1575 cm-1
de ve yine ligand için 960 cm-1 de gözlenen N-O bandı, kompleks için 1066 cm-1
de gözlenmektedir. Komplekslerde 1775 cm-1 de gözlenen absorpsiyon, kompleks oluşumu ile meydana gelen hidrojen köprülerini göstermektedir (Meyer ve ark., 1969).
Dioksim komplekslerinde, metale bağlanmanın oksim oksijenleri üzerinde olması durumunda, titreşim frekans değerlerinde az da olsa kaymalar olur. Karbon ve azot üzerinde değişik fonksiyonel grup olması halinde, konjugasyona bağlı olarak C=N gerilme bantları, çok az bir kayma ile 1670-1610 cm-1
aralığında gözlenmektedir (Chakravorty, 1974; Keeney ve ark.,1984,; Kotali, ve Papageorgio, 1991).
Ar-CH=N-OH yapısındaki mono oksimlerin 1H-NMR spektrumlarında fenil halkası protonları 7-7.5 ppm, OH protonları 10-12 ppm ve C-H protonları 8-8.5 ppm civarlarında görülmektedir (Kleinspehn ve ark., 1967; Silverstein ve ark. 1974).
Aldoksimlerde syn ve anti olarak adlandırılan iki farklı yapının bulunduğu 1 H-NMR spektrumu yardımı ile belirlenebilmektedir. Çeşitli aldoksimlerin spektrumlarında aldehit protonuna (C-H) ait kimyasal kayma değerleri, birbirinden 0,6 ppm uzaklıkta olan bir dublet şeklinde çıkmaktadır (Patai, 1970). İki farklı absorbsiyonun aynı anda görülmesi syn ve anti izomerlerinin varlığıyla açıklanabilir.
Dioksimlerde ise, O-H protonlarının çevrelerine bağlı olarak anti, syn ve amphi geometrik izomer durumlarına göre 1H-NMR piklerinde farklılık gözlenir. Anti izomerler için 10 ppm‟ in üzerinde tek pik gözlenmesine karşılık, amphi izomerlerde O-H gruplarından biri, bileşikteki diğer oksim azotu ile hidrojen bağı oluşturduğundan ve syn izomerlerde ise, komşu oksijenle etkileştiğinden, birbirine yakın iki pik gözlenir. Bu
protonlar D2O ilavesi durumunda döteryum ile yer değiştirirler ve 1H-NMR pikleri kaybolur (Deveci ve ark., 1991; Sevindir ve Mirzaoğlu, 1992).
Simetrik olarak sübstitüe olmamış vic-dioksimlerde (O-H) protonları iki ayrı singlet halinde görülür (Guetteve ark., 1967). Metilglioksim, fenilglioksim, N-fenilaminoglioksim gibi mono sübstitüe glioksimlerde aldehit protonuna komşu (O-H) ptotonu, sübstitüe oksimdeki (O-H) protonundan daha kuvvetli alanda ortaya çıkmaktadır (İrez ve Bekaroğlu, 1983 Guette ve ark., 1967). Bu iki singlet arasındaki fark 0,6 ppm‟e kadar ulaşmaktadır.
1.1.2. Oksimlerin Eldesi
a) Aldehit ve ketonların hidroksilamin ile reaksiyonundan: Oksimler eskiden
beri aldehit ve ketonların hidroksilamin ile olan reaksiyonundan elde edilmektedir. Reaksiyon sulu alkollü ortamda, kaynama sıcaklığında ve optimum pH' larda gerçekleştirilir (Bierlein ve Lingafelter, 1951; Constantinos ve ark., 2005).
ġekil 1.4. Oksimlerin Hidroksilamin ile Sentezi
b) Nitrosolama metodu: Özellikle keto oksimlerin hazırlanmasında oldukça
kullanışlı bir yoldur ve aktif metilen gruplu bileşiklerden yararlanılır (Burakevich ve ark., 1971; Uçan ve Mirzaoğlu, 1990).
ġekil 1.5. Ketonların Nitrosolanması ile Oksim Eldesi
Keto oksimlerin (izonitroso oksimler) karbonil grubunun önceki metod da olduğu gibi, hidroksilamin ile reaksiyonundan 1,2-(vic) dioksimler elde edilir (Uçan ve Mirzaoğlu 1990).
ġekil 1.6. Ketoksimlerden Dioksim Eldesi
İzonitroso oksimlerin hidroksilamin ile olduğu gibi hidrazin, amin vb. bileşikler ile olan kondensasyon reaksiyonundan çeşitli oksim türevlerini verirler (Chakravorty 1974; Deveci, 1994).
ġekil 1.7. Ketoksimler ile Aminlerin Reaksiyonu
c) Kloralhidrat ile hidroksilamin reaksiyonundan: vic-Dioksimlerin önemli
bir üyesi olan kloroglioksim, kloralhidrat ile hidroksilaminin bazik ortamdaki reaksiyonundan elde edilir (Hesse ve Krehbiel, 1955; Gök, 1981; Deveci 1994).
ġekil 1.8. Dioksimlerin Kloralhidrat‟ tan Eldesi
d) Primer aminlerin yükseltgenmesiyle: Primer aminler sodyum tungstat
katalizörlüğünde hidrojen peroksit ile yükseltgendiğinde oksimleri verirler (Smith 1966).
ġekil 1.9. Aminlerden Oksim Eldesi
e) Ketiminlerin hidroksilaminle reaksiyonundan: Ketiminler hidroksil-aminle
reaksiyona girerek kolayca oksimleri verirler (Hauser ve Hoffenberg, 1955). Ketonlar ise bu reaksiyonu daha kolay verirler.
ġekil 1.10. Ketiminlerden Oksim Eldesi 1.1.3. Oksimlerin Reaksiyonları
a) Asitlerin etkisi: Oksimler kuvvetli mineral asitlerle, tuzlarına dönüşürler.
Ayrıca oksimlerin syn ve amphi izomerleri derişik HCl ile anti izomerlerine dönüşürler (Gök 1981; Gök ve Serin, 1988).
ġekil 1.11. Oksimlerde İzomerlik Dönüşümleri
b) Isı ve ıĢık etkisi: Oksimler oldukça kararlı maddeler olmalarına rağmen,
uzun süre ışık ve hava oksijenine maruz kaldıklarında bazı bozunmalar olur. Bozunmalar sonucunda genellikle ana karbonil bileşiği ile bazı azotlu maddeler meydana gelir (Smith 1966; Macit, 1996).
c) Oksimlerin indirgenmesi: Oksimler, çeşitli reaktiflerle imin basamağından
geçerek, primer aminlere kadar indirgenebilirler (March, 1977) vic-Dioksimlerde aynı şekilde kolayca diaminlere indirgenebilirler (Chakravorty 1974).
ġekil 1.13. Oksimlerin İndirgenme Reaksiyonu
d) Oksimlerin yükseltgenmesi: Aldoksimler -78 0C de oksitlendiğinde nitril oksitleri, vic-dioksimler ise furoksanları verir. Aldoksimlerde, C-H bağının oksitlenme kararsızlığından dolayı değişik ürünler oluşur (Chakravorty 1974).
ġekil 1.14. Oksimlerin Yükseltgenmesi
e) Beckmann çevrilmesi: Oksimler; özellikle keto oksimler, sülfürik asit,
hidroklorik asit, polifosforik asit gibi kuvvetli asitlerle veya fosfor pentaklorür, fosfor pentaoksit varlığında bir çevrilmeye uğrarlar. Alkil veya aril grubu azot atomu üzerine göç ederek, N-sübstitüe amitler meydana gelir. Yani Beckmann çevrimi, oksimlerin katalizlenmiş izomerizasyonundan amitlere dönüşümüdür. Örneğin asetofenonoksim derişik sülfürik asit beraberinde Beckmann çevrilmesine uğrayarak N-fenil asetamit oluşur (Tüzün, 1999).
f) Oksimlerin klorlanması: Oksimler uygun çözücü içerisinde klorlama vasıtaları ile
klorlandığı zaman yapıdaki imin (-CH=N-O-) hidrojeni yerine klor geçerek, hidroksamoil klorürleri (oksim klorürleri) verirler. Örneğin asetaldoksimin klorlanmasıyla asethidroksamoil klorür elde edilir (Weiland, 1907).
ġekil 1.16. Oksimlerin Klorlanması
Hidroksamoil klorürler (oksim klorürleri), oksimlerine göre daha aktiftirler ve çeşitli nükleofillerle reaksiyona girerek kendi bünyelerinde bulunan klorür yerine başka gruplar geçebilir. Örneğin, amonyak ile amidoksimleri, aminler ile N-sübstitue amidoksimleri, hidroksilamin ile de hidroksilamidoksimleri verirler.
ġekil 1.17. α-Kloro Oksimlere Amin Türevlerinin Katılması
Son yıllarda, vic-dioksim klorürleri ile mono ve diaminler arasındaki reaksiyonlardan çeşitli dioksim ve tetraoksim türevleri sentezlenmiştir (Grundmann ve Grunanger, 1971; Chakravorty, 1974; İrez ve Bekaroğlu, 1983; Deveci ve ark., 1991; Karataş, ve ark., 1991).
ġekil 1.18. Kloroglioksimler ile Amin Türevlerinin Reaksiyonu
Yine diklor glioksim ve tereftalohidroksamoil klorür gibi oksimler ile diaminlerin reaksiyonundan organik polimerler elde edilmiştir (Karataş ve İrez, 1993; Grundmann ve ark., 1965).
ġekil 1.19. Dikloroglioksimler ile Diamin Polimerizasyonu
Mono ve dioksim klorürleri, soğukta ve bazik ortamda basit nitril oksitler ve disiyandioksitler oluştururlar. Bunlar çözelti ortamında ve soğukta kararlıdırlar, ancak oldukça aktif maddelerdir. Bu nitriloksitlerin çözeltilerine mono ve diaminlerin katılmasıyla mono ve diamidoksimler elde edilir (Gök, 1981; Grundmann ve ark., 1965).
ġekil 1.20. Oksimlerden Nitril Oksit Eldesi
g) Alkilleme reaktifleri ile reaksiyonları: Oksimler polar çözücü ve bazik ortamlarda
alkil halojenürler, alkil dülfatlar veya alkil tosilatlar ile reaksiyona girerek oksim eterleri oluştururlar (March, 1977; Baji ve ark.,1995).
ġekil 1.21. Oksimlerin Alkilasyonu
h) Açilleme reaktifleri ile reaksiyonları: Açilleme reaktifleri, oksimler ile reaksiyona
girerek o-açil türevlerini oluşturur. Oluşan bu açil türevleri çok kararsız bileşikler olduklarından bazik ortamda hidrolize uğrayarak oksimleri oluştururlar (Freeman, 1979).
i) Oksimlerin Kompleksleri: Oksimler geçiş elementleri ve alkali katyonlar ile
kompleks verirler; bunların kararlılığı oksim yapısına ve katyona bağlıdır. Bazı basit oksimler ile demir klorür‟ ün renk reaksiyonu verdiği bilinmektedir. Suda çözünmeyen, organik çözücülerde çözünen, en önemli kompleksler α-dioksimler, α-keto oksimler ve o-hidroksi benzaldoksimler ile yapılır. Bunlar analitik kimyada çöktürme ve renk testinde önemli uygulama alanları bulmuşlardır. Bu konuda çalışmalar ilk defa 1905‟ te Tschugaeff tarafından nikel dimetilglioksim kompleksinin izole edilmesinden sonra başlamış ve günümüze kadar artarak sürmüştür. Analitik kimyadaki iç komplekslerinin kullanışını uygulayan Tschugaeff, nikel ile dimetilglioksimin reaksiyona girerek kırmızı renkte çözünmeyen bir bileşik verdiğini keşfeden kişidir.
vic-dioksimlerin nikel ile verdikleri kompleksler, bu yüzyılın başlarından beri ilgi uyandırmıştır. Özellikle dimetilglioksimin nikelin kantitatif tayininde kullanılması, bu ilginin esas sebebi olmuştur (Godycki ve Rundle, 1953).
Günümüzde birçok vic-dioksimin geçiş metalleri ile yaptığı komplekslerinin yapısı X-ray metodu ile aydınlatılmıştır. Genel olarak bu komplekslerde, metal iyonu ile dioksim molekülündeki dört azot atomu ile aynı düzlemdedir (Şekil 1.24).
ġekil 1.23. Dioksimlerin genel kompleks yapıları
vic-Dioksim komplekslerinde oluşan moleküller arası H-köprüleri, kompleksin kararlılığını arttırır ve suda çözünmelerini engeller. Köprü oluşturan hidrojen atomunun iki oksijen atomuna olan uzaklığı birbirine eşittir. anti-Dioksim kompleksilerinde H-köprüsü oluşumu nedeniyle 1
H-NMR spektrumunda oksimin –OH protonu yaklaşık 16-17 ppm gibi çok zayıf alana kayar (Gul ve Bekaroğlu, 1983). İki oksijen atomu arasındaki uzaklık ise X-ray analizi ile 2,44 A0 olarak ölçülmüştür. Yine bu komplekslerdeki C=N ve N-O bağ uzunlukları sırasıyla 1,3 ve 1,34 A0 civarında bulunmuştur. Bu değerler serbest oksimler ile karşılaştırıldığında N-O bağ uzunluğunun kompleks oluşumu sonunda kısaldığı, C=N bağının ise değişmediği gözlenmiştir.
vic-Dioksimlerin stereokimyası, oksim komplekslerinin yapısını belirleyici bir faktördür. Bunların anti kompleksleri, amphi ve syn komplekslerine göre daha kararlıdır. Bu yüzden vic-dioksimlerin izomerleri nikel ile farklı renk ve özellikte kompleksler verirler. Özellikle, vic-dioksimlerin anti izomerleri nikel ile kiremit kırmızısı (Burakevich ve ark., 1971; Ertaş ve ark., 1987), amphi izomerleri yeşilimsi-sarı kompleksler oluştururlar (Burakevich ve ark., 1971) (Şekil 1.24). ancak, bu iki kompleks formun, birbirine dönüşüm enerjilerinin düşük olması sebebiyle, birbirine dönüşebilirler. Düşük enerjili olan anti- formuna dönüşüm genellikle hakim ise de bunun istisnaları vardır (Serin ve Bekaroğlu, 1983).
ġekil 1.24. vic-Dioksimlerin amphi-formlarının Ni(II) kompleksi 1.1.4. Oksimlerin Kullanım Alanları
Oksimler analitik, organik, anorganik, endüstriyel ve biyokimyanın birçok alanında değişik amaçlarla kullanılmaktadır. Bazı oksim ve onların çeşitli alkil, oksialkil ve amino türevleri fizyolojik ve biyolojik aktif özelliklere sahip oldukları, ayrıca motor yağlarının, boyaların, epoksit reçinelerinin, lastiklerin v.b. bazı özelliklerinin iyileştirilmesi için katkı maddesi olarak kullanıldıkları bilinmektedir (Carlos ve David, 1972; Lecterc ve ark., 1980; Lecterc ve ark., 1977).
Sanayide kullanılan birçok polimer madde yüksek sıcaklığa, ışığa, darbeye, gerilmeye ve benzeri etkilere dayanıksızdır. Polimerik materyallerin bu eksik özelliklerini iyileştirmek için çeşitli aktif katkı maddeleri kullanılmaktadır, bu amaçla oksimlerin bazıları da aktif katkı maddesi olarak kullanılır. Yine doymamış oksimlerin, polimerlerin ışığa karşı özelliklerini iyileştirdiği ve epoksi reçinelerinin yapışma özelliğini artırdığı bilinmektedir (Carlos ve David 1972). Bir oksim türü olan amidoksimler; teknolojide oldukça geniş uygulama alanına sahiptirler. Örneğin, birkaç aromatik amidoksim yağ devir sistemlerinde korozyonu önleyici olarak kullanılmaktadır (Kara, 1995). Benzamidoksimin ve süksinik diamidoksimin gümüş tuzları fototermografik özelliklere sahiptir. Bazı diamidoksimler termoplastik maddeler
için uygun yayıcılar olarak yine bir amidoksim grubu içeren katyonik nişasta kağıt kuvvetlendirici olarak önerilmiştir. Kısmen amidoksimlenmiş poliakrilonitril liflerinin boya tutma kapasitesi artar (Kara 1995). Poliakrilamidoksim türevlerinin deniz suyundan uranyum elde edilmesinde en iyi absorban olduğu belirlenmiştir.
Yine; - karbonunda arilsülfonil, sülfamid veya bir sülfon grubu içeren amidoksimler antibakteriyel maddeler olarak düşünülürler. Örneğin; 4-sülfamil– benzamid dioksim, raşitizm hastalığına karşı aktiflik gösterir. Triazolil halkalı amidoksimler ise analjesikler olarak kullanılırlar ve tümüyle sübstitüe alifatik olanlar antihistaminik aktifliği artırırlar. Yine; 2-metoksi-aminoakridin-6-amidoksim ve 9-anilakridin-3-amidoksim tedavi edici olup farmakolojik özelliklere sahiptir. Bir amidoksim grubuna sahip bazı halojenlenmiş fenoller Mycobacterium tuberculosis‟e karşı etkindirler (Kara 1995).
Koordinasyon bileşiklerinin biyolojik yapılardaki önemi, sanayideki kullanım oranının ve alanının günden güne artması, son zamanlarda kanser araştırmalarında antitümör etkilerinin bulunması, kompleksler „„özellikle vic-dioksim kompleksleri‟‟ üzerindeki araştırmaların yoğunlaşmasına sebep olmuştur. vic-Dioksim komplekslerinin vitamin B12 ve bitkilerin klorofil renk maddesine benzerliğinden dolayı biyolojik yapıların aydınlatılmasında kullanılması, önemini arttırmıştır (Tan ve Bekaroğlu, 1983).
Oldukça geniş kullanım sahası olan oksimlerin bir kısmı ilaçların imalatında hammadde olarak kullanılır iken bir kısmı da ilaçların yapımında etkinliği artırıcı katkı maddesi olarak kullanılmaktadır. Oksimler daha çok antidepresan ve antibiyotik gibi ilaçların imalatında kullanılmaktadır. Örneğin, 3-hidroksi-5-hidroksimetil-2-metilisonikotinaldoksim (piridoksal oksim) epilepsi tedavisinde (Pham ve ark., 1970), eritomisinn oksimler antibiyotik olarak ve O-(w-aminoalkil) oksimler lokal anastezik ve analjezik olarak kullanıldığı bilinmektedir (Kurihara ve ark., 1980).
Oksimler ve bazı türevleri parfüm sanayinde de kullanılmaktadır. Örneğin, propan trimer ve tetramer Oksimlerin çiçek kokulu parfüm yapımında kullanıldığı (Hercules, 1981), izobütaldoksim, izovaleraldoksim ve 2-metilbütiraldoksim, Hedychium Coronarium bitkisinin kokusuna benzer bir koku verdiği bilinmektedir (Toyoda ve ark., 1993).
Ayrıca son zamanlarda oksim bileşikleri ve bunların kompleksleri, alkil ve O-açil oksimler ayrıca oksim polimer bileşikleri sıvı kristal teknolojisinde de kullanılmaya başlanmıştır (Fujita ve ark., 2011).
1.2. SIVI KRĠSTALLER 1.2.1. Sıvı Kristallerin Tarihi
Sıvı kristaller ilk olarak Avusturyalı botanikçi Friedrich Reinitzer, 1888‟de, Graz Üniversitesi‟nde yaptığı çalışmalar sonucunda keşfedilmiştir. Rezinitzer‟ in bitki ve hayvanlarda bulunan ve doğal maddeler olan kolesterol esterleri üzerinde çalışmasının amacı, maddelerin basit formülleri ve erime noktaları gibi fiziksel özelliklerini tam olarak saptamaya çalışmaktır. Çünkü basit formülün, maddelerin kimyasal tanımlaması anlamına geldiğini düşünmüştür. Bu maddelerin ısıtma ya da soğutma sırasında tersinir ve tekrar edebilen "çift erime" geçişi sergilediğini gözlemlemiştir. Kolesteril benzoat adlı madde ısıtıldığında, kristal katı 145,5 oC‟ de çıplak gözle anlaşılması güç bulanık bir sıvıya, ardından da 178,5 oC‟ de berrak bir sıvıya dönüşmüştür. Friedrich Reinitzer bu bulanık sıvının maddenin yeni bir fazı olduğunu öneren ilk kişi olmuştur (Reinitzer, 1888). Kolesteril benzoat‟ ın yapı formülü aşağıda verilmiştir.
ġekil 1.2.1. Kolesteril benzoat (Ph-COO-Kolest-5-en (KB)‟ ın yapı formülü Faz Geçişleri K 145.5 N* 178.5 Iso
Bu durum olağan dışı olduğundan dolayı Reinitzer madde örneklerini, kristal yapılarının aydınlatılması amacıyla, ışık ile kristal yapıların birbirlerine olan etkileri üzerinde çalışan yani kristal optiği konusunda uzmanlaşmış olan Alman Fizikçi Otto Lehmann‟ a göndermiştir (Lehmann, 1889). Lehmann, elindeki bu bilgilerden yola çıkarak sıvıların optiksel özelliklerinin, birbirine paralel yönlenmiş moleküllere bağlı olduğu sonucuna varmıştır ve hem sıvı hem de katının özelliklerini gösteren bu yeni durumu "sıvı kristal (LC)" olarak tanımlamıştır. Bu sıralarda kolesterol yapısı henüz bilinmemektedir.
Kimyasal bileşiklerin molekül yapıları arasındaki ilişkiyi ve sıvı kristal davranışını bulmak amacıyla 1900‟lü yıllardan hemen sonra Halle Üniversitesi‟nde
(Almanya) kimyager Daniel Vorländer tarafından sistematik bir çalışma başlatılmıştır (Sluckin ve ark., 2004).
20. yüzyılın başında George Friedel sıvı kristaller üzerinde birçok deney yapmış ve elektrik alanların yönlendirici etkisi ile sıvı kristallerdeki kusurların görünüşünü açıklayan ilk kişi olmuştur. 1922‟de her maddenin farklı moleküler düzenlemesi olduğuna dayanarak sıvı kristallerin sınıflandırılmasında bir öneride bulunmuştur. 1922 ve İkinci Dünya Savaşı arasındaki dönemde Oseen ve Zöcher sıvı kristallerin incelenmesinde matematiksel bir temel kuram önermişlerdir (Gray, 1962). Aslında bir kısım bilim adamı sıvı kristal maddelerle çalışmış olmalarına rağmen bu fenomenin farkına varamamışlardır. Savaş başladıktan sonra birçok bilim adamı sıvı kristallerin önemli özelliklerinin yeni keşfedildiğine, bu keşfin 1950‟ lere kadar yapılamadığına inanmışlardır. Brown Amerika‟da, Chistiakoff Sovyetler Birligi‟nde, Gray ve Frank İngiltere‟de sıvı kristallere olan ilginin yeniden canlanmasına neden olmuşlardır (Gray, 1962). Maier ve Saupe sıvı kristallerin mikroskobik bir teorisini formülleştirmiş (Maier ve Saupe, 1960). 1968 yılında RCA bilim adamları ilk sıvı kristal gösterisini sunmuşlardır (Castellano, 2005).
1890‟ a kadar araştırılmış tüm sıvı kristal maddeler doğadan izole edilmiş maddelerdir. İlk sentetik sıvı kristal olan p-azoksianisol Gatterman ve Ritschke tarafından üretilmiştir (Gattermann ve Ritschke, 1890). Çok çeşitli kullanım alanlarına sahip olan sıvı kristaller, olağanüstü özellik ve davranışları sayesinde ve özellikle sıvı kristal göstergelerdeki (LC-Displays) ticari ilgi ve önemleri nedeniyle üzerinde yoğun çalışmaların yapıldığı ve ilginin arttığı bir alan olmuştur (Goodby ve ark., 2001).
1.2.2. Sıvı Kristaller ve Özellikleri
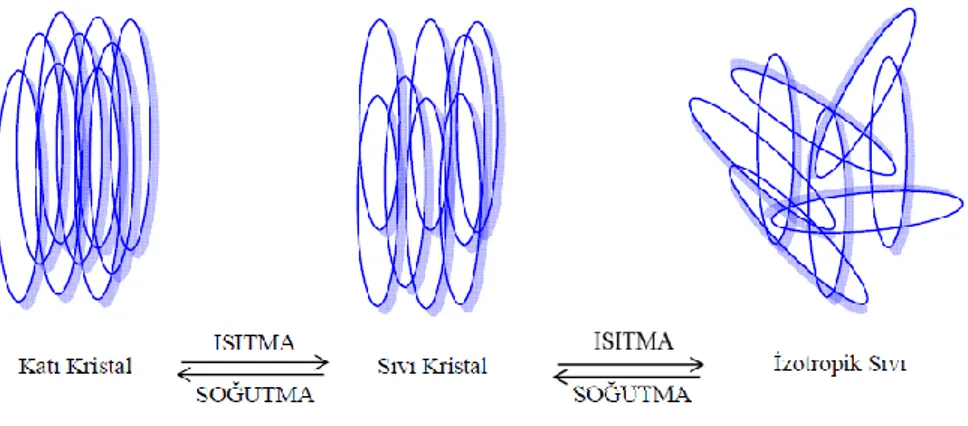
Saf organik maddelerin çoğu ısıtıldığında sadece katı-sıvı geçişi yapmaz, bunun yerine bir veya daha fazla ara faz gösterir. Katı ve sıvı fazların her ikisinin özelliğini taşıyan; katı faz düzenine ve kısmi yönelimsel düzenlerinden dolayı sıvı akışkanlığına sahip olan bu ara fazlar sıvı kristal faz veya yunanca ara faz anlamına gelen mesofaz denilmektedir (Donino ve ark., 2003; O'Ohare ve Bruce, 1992).
ġekil 1.2.2. Sıvı Kristal Genel Gösterimi
Sıvı kristal bileşikler, kristal katı ve isotropik sıvı arasında bir ara özellik gösterirler. Kristal yapıdaki moleküller, boşlukta düzenli bir yerleşimdedir. Moleküllerin üç boyutlu düzende yönü ve pozisyonu belirlidir. Sıvılar bu düzene sahip değildir. Şekil 1.2.2‟ de bir sıvı kristal fazın genel gösterimi verilmiştir.
Sıvı kristal faz geçişleri, iki şekilde gözlenebilir. İlki isotropik sıvının soğutulması ile oluşan, termodinamik olarak kararsız mesofazlara monotropik faz denir. İkincisi ise, hem katının sıcaklığının artması hem de sıvının sıcaklığının düşmesi ile oluşan, termodinamik olarak kararlı mesofazlara ise enansiyotropik faz denir. Sıvı kristal hal, sıvı halden daha düzenli katı halden ise daha düzensizdir (Coşkun, 2006).
Sıvı kristal durumunun, katı ve sıvı fazlardan ayırt edici özelliği, moleküllerin (mesogen) direktör ‘n’ denilen ortak bir eksen boyunca yönelme eğilimleridir. Bu özellik ile sıvı kristal moleküller, kendine özgü düzeni olmayan sıvı fazdaki molekülerinden ve katı fazdaki düzenli yapılardan farklılık gösterirler. Sıvı kristal moleküllerde yönelimsel düzen özelliği katı ve sıvı faz arasındadır ve bu sıvı kristal durumu ile eşanlamlı kullanılan mesogenik durumun ilk koşuludur (Elmalı 2006).
Moleküllerin yapı içinde ne kadar düzenli olduğunun ölçüsü düzen parametresi (S) ile tanımlanır. Bu düzen parametresi genellikle aşağıda gösterildiği gibi verilir (Gennes, 1993).
S= (1/2)[3cos2 θ-1]
ġekil 1.2.3. Sıvı Kristallerde Düzen Parametresi
Şekil 1.2.3‟ de görüldüğü gibi sıvı kristal moleküllerinin eğilimlerinin direktör boyunca yönelmesi anisotropi olarak bilinir (Dunmur, 2001).
Sıvı kristal moleküllerin yapısını açıklamak için üç faklı parametreden yararlanılır:
1) Konumsal düzen, 2) Yönelimsel düzen, 3) Bağ yönelimsel düzeni
Bu parametrelerden her biri sıvı kristal örneğinin hangi mertebede düzenleneceğini tanımlar. Konumsal düzen, moleküllerin ve molekül gruplarının birbirlerine göre konumu belirler ve ortalama molekül veya molekül gruplarının hangi mertebede geçiş simetrisini (katı maddelerin gösterdiği gibi) göstereceği ile ilgilidir.
Yönelimsel düzen, moleküllerin direktör doğrultusunda oluşan düzenini ifade eder;
moleküllerin temel uzun zincir üzerinde gösterdikleri yönelim derecesi ile ilgilidir. Bağ
yönelimsel düzen ise zincir üzerinde yer alan düzen olmaksızın en yakın komşu
moleküldeki merkezlerin zincire katılmasını tanımlar. Bu durum merkez uzunluklarına bağlı olarak uzun diziler için pek olası değildir, fakat kısa zincirler, zincir düzenine aittirler (Dunmur, 2001).
1.2.3. Sıvı Kristallerin Sınıflandırılması
Sıvı kristaller oluşum nedenlerine bağlı olarak iki ana gruba ayrılırlar. Bunlar termotropik sıvı kristaller ve liyotropik sıvı kristallerdir. Termotropik sıvı kristaller ince-uzun (çubuksu) yapıda veya disk biçimindeki moleküllerden oluşan ve farklı alt
gruplar içeren sistemlerdir. Liyotropik sıvı kristaller ise bir kısım amfibilik nitelikteki uzun zincirli moleküller olup, insan vücudu gibi canlı sistemlerdeki rolü oldukça önemlidir. Bu tür maddelerin canlı organizmasındaki fiziksel ve biyolojik rollerinin farkına yeni yeni varılmaktadır.
ġekil 1.2.4. Sıvı kristallerin Sınıflandırılması
1.2.3.1. Liyotropik Sıvı Kristaller
Sıvı kristallerin bu sınıfındaki maddeler sadece çözücü ile karıştırıldığında sıvı kristal özellik gösterirler. Bu çeşit maddeler için sıvı kristalin kararlılığını, sıcaklıktan ziyade çözeltinin konsantrasyonu belirler. Bu çeşit sıvı kristalleri termotropik sıvı kristallerden ayırmak amacıyla liyotropik sıvı kristaller denmiştir (Colling ve Hird, 2001).
Liyotropik sıvı kristaller genellikle birden fazla organik bileşiğin çeşitli konsantrasyonlarda karışmasıyla elde edilir. Sıcaklık değişimi sıvı kristallerin bu sınıfı için önemli bir parametre değildir. Bu tip sıvı kristallere en güzel örnek bildiğimiz sabundur. Aşağıdaki şekilde de görüldüğü gibi molekül polar bir baş kısmına bir hidrokarbon grubunun bağlanmasıyla oluşmuştur (Akbaş, 2011).
1.2.3.2. Termotropik Sıvı Kristaller
Termotropik sıvı kristaller sıcaklığın değişimi ile gözlenen sıvı kristal fazlardır (Dierking, 2003). Bu tip sıvı kristal bileşikler çubuksu veya disk biçimindeki moleküllerden oluşmaktadır.
Termotropik sıvı kristaller lineer olduğu kadar non-lineer optik özelliklerinden dolayı çok fazla incelenen ve en geniş kullanım alanına sahip olan sıvı kristallerdir (Khoo, 1995).
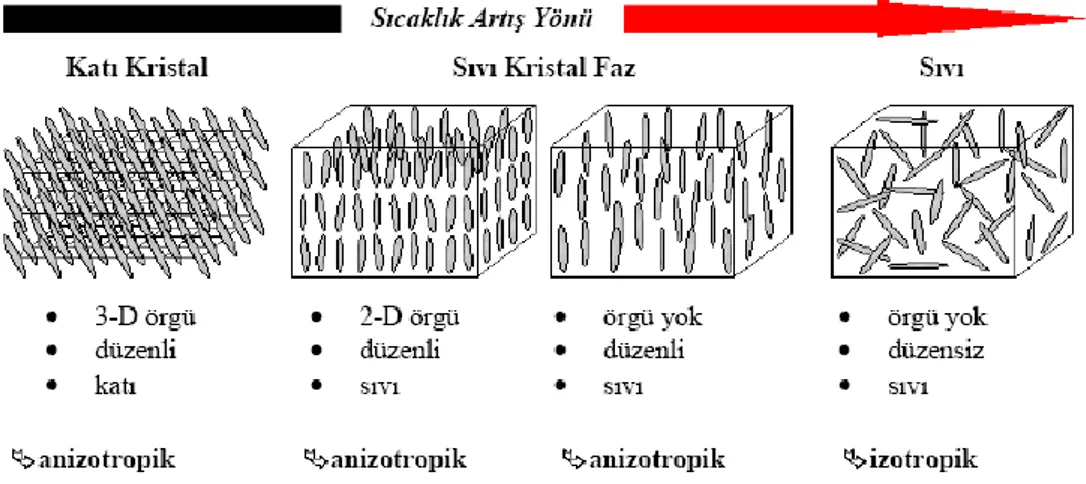
Kristal yapı ısıtıldığında izotropik sıvıya doğru olan geçişte tek basamaklı bir geçiş yerine birkaç ara faz meydana gelerek bir geçiş oluyor ise bu tip sıvı kristallere termotropik sıvı kristaller denir. Termotropik sıvı kristallerde meydana gelen ara fazların oluşumunun sebebi sıcaklıktır. Bu tip sıvı kristallerin molekül yapıları incelendiğinde moleküllerin genellikle ince çubuksu veya disk şeklinde olduğu görülmüştür (Priestley ve ark., 1975).
ġekil 1.2.6.Termotropik Sıvı kristallerde Faz Geçişler
Maddenin katı fazdan mezofaza geçiş sıcaklığı „erime noktası‟, mezofazdan isotropik sıvıya dönüştüğü sıcaklık „berraklaşma (clear) noktası‟ olarak adlandırılmaktadır. Termotropik sıvı kristaller termal kararlılıklarına göre ikiye ayrılırlar. Sadece isotropik sıvının soğutulması ile oluşan termodinamik olarak kararsız mesofazlara monotropik faz denir. Hem katı kristalin sıcaklığının artması ile hem de isotropik sıvının sıcaklığının düşmesi ile oluşan termodinamik olarak kararlı mesofazlara ise enansiyotropik faz denir. Enansiyotropik faz kristalin erime noktası ile berraklaşma noktası arasında yer alır (Donino ve ark., 2003; Espinet ve ark., 1992).
1.2.3.2.1. Kalamitik Sıvı Kristaller
Kalamitik sıvı kristaller çubuksu molekül geometrisine sahip mesogenlerdir. Kalamitik ya da çubuk şeklindeki moleküller sert bir çekirdekten ve bu çekirdeğe bağlı alifatik zincirlerden meydana gelmektedir.
ġekil 1.2.7. Kalamitik Sıvı Kristallerin Genel Yapısı (a>>b)
Aşağıda kalamitik sıvı kristal yapılarını oluşturan bileşenlerin genel bir tablosu verilmiştir.
Tablo 1.2.1. Kalamitik Sıvı Kristallerin Genel Bileşenleri
-L- (Bağlantı Grubu) R/R′ C=N CN N=N NO2 COO Alkil COS Alkiloksi C≡C F/Cl/Br/I Florlu Alkil Florlu Alkoksi Bu tip mesogenler ilk keşfedilen ve ticari özelliklerinden dolayı en çok araştırılan gruptur. 1969 yılında oda sıcaklığında sıvı kristal özellik gösteren ilk bileşik 4-metoksibenziliden-4‟-butilanilin (MBBA) sentezlenmiştir. Daha sonra optikçe ve
kimyasal olarak kararlı olan siyanobifenil bileşikleri keşfedilmiş ve bunların ilki olan 4-pentil-4‟-siyanobifenil (5CB) 1973 yılında sentezlenmiştir. Bu bileşiklerin yapıları ve faz geçiş sıcaklıkları aşağıdaki şekilde gösterilmiştir (Collings ve Hird, 2001).
ġekil 1.2.8. 4-metoksibenziliden-4‟-n-butilanilin (MBBA) (K 22 oC, N 47 oC Iso)
ġekil 1.2.9. 4-n-Pentil-4‟-siyanobifenil (5CB) (K 18 o
C, N 36 oC Iso)
Esnek Yan Zincirler
R: Yan zincirler genellikle alkil grupları (CnH2n+1), alkiloksi grupları (CnH2n+1O), alkenil
grupları (CnH2n-1) veya alkeniloksi (CnH2n-1O) gruplarından biri olabilir. Sıvı kristallerin mesofaz oluşumlarında ve faz geçişlerine yan grupların esneklik ve uzunluğunun etkisi vardır. Genellikle homolog bileşiklerde "n" sayısı küçük ise mesogenik faz gözlenemez, "n" sayısı yükseldikçe monotropik sıvı kristal faz gözlenir. "n" Sayısının yeteri kadar artması ile enansiyotropik nematik faz ve ardından simektik mesofaz gözlenir. Bileşikte yan zincirdeki "n" sayısının artması yani zincire eklenen karbon sayısının artması ile daha yüksek geçiş sıcaklıkları gözlenir (Whang ve Zhou, 2004).
R’: Genellikle bu gruplar alkil, alkiloksi, siyano, nitro, isosiyanat, sülfid ve
halojenürlerden (F, Cl, CF3 ve OCF3) biri olabilir. Bu gruplar öncelikli olarak dielektrik anisotropi ve refraktif indeks oluşumuna neden olmaktadırlar (Whang ve Zhou, 2004).
Eğer yan gruplardan biri kiral bir merkez ile yer değiştirmiş ise, kiral nematik ve simektik mesofazların oluşumuna neden olur. Bu durum sıvı kristal bileşiklerin pek çok fiziksel özelliğini değiştirir (Whang ve Zhou, 2004).
Aromatik Çekirdekler
Pek çok kalamitik sıvı kristal bileşik iki veya daha çok aromatik halkadan oluşur. Bu aromatik çekirdekler çoğunlukla fenil, siklohekzan, doymamış bifeniller,
terfenil veya bunların çeşitli bileşimleridir. Daha uzun çekirdek yapısı daha yüksek erime sıcaklığına neden olur (Whang ve Zhou, 2004).
Bağlantı Grupları
Bağlantı grupları faz geçişlerine ve fiziksel özelliklere olan etkileri nedeniyle çok önemlidirler. Genellikle çalışılan bağlantı grupları;
a) Doymamış gruplar; Etilen (C2H4) gibi,
b) Esterler,
c) İkili veya üçlü bağ içeren doymamış gruplar; sitilben, azo, Schiff bazları, asetilen
veya diasetilen gibi…
Aromatik çekirdek üzerinde 2-, 3- veya 4- pozisyondaki hidrojen yerine siyano, floro veya kloro gibi polar gruplarından birinin substitusyonu, sıvı kristal bileşiğin fiziksel özelliklerinin değişmesine ve yeniden düzenlenmesine neden olur. Çoğunlukla subtitue olmuş aromatik çekirdek içeren bileşiklerin sıvı kristal özellikleri, substitue olmamış analoglarına oranla belirgin bir şekilde değişiklik gösterir (Whang ve Zhou, 2004).
Sıvı kristal bileşiklerin kendi kendine organize olabilmesi için gerekli olan temel öge, düzen ve hareketliliğin bileşimidir. Sıvı kristal sistemlerin hareketliliği, esnek yan zincirler olarak adlandırılan molekül ya da molekül parçalarının genlik hareketiyle sağlanır. Moleküler düzen ise, yönelimsel ve pozisyonel olmak üzere iki ögeden meydana gelir. Pozisyonel düzen başlıca amfifilik ve özel çekici kuvvetler etkisi ile oluşur. Bu kuvvetler moleküllerin kendi kendini düzenlemesine yardımcı olurlar (Tschierske, 2001).
Sıvı kristal tipleri içerisinde en yaygın olanı kalamitik sıvı kristallerdir. Bunlar nematik, simektik ve kolesterik olmak üzere üçe ayrılırlar.
A) Nematik Sıvı Kristaller
Kalamitik sıvı kristallerin nematik fazı en basit sıvı kristal fazdır. Bu fazda moleküllerin yönelimsel düzenleri vardır fakat yerel düzenleri yoktur. “Nematik” adı, bu tür yapıların polarize mikroskop altında gösterdikleri ipliksi görünümden dolayı ilk kez Friedel tarafından iplik anlamına gelen yunanca bir sözcükten türetilmiştir (Gündüz, 1992). Bu fazdaki moleküller yalnızca tercihli yönelimsel düzene sahiptir. Bu fazda pozisyonel düzen yoktur (Gennes, 1974). Belirli bir düzenlenme olmuş olsa da sürekli akıcılık ve hareketlilik vardır. En akışkan mezofazdır ve bu özelliği ile isotropik faza en çok benzeyen mezofazdır (Collings ve Hird, 2001).
ġekil 1.2.10. Nematik Faz Düzenlenmesi (Solda), 1,5-Hegandiol-bis{4-[4-(4-n oktiloksi-benzoiloksi)benzilidinamino]benzoat}bileşiğinin Nematik Faz POM Görüntüsü (Sağda)
B) Simektik Sıvı Kristaller
Nematik mezofazdan daha düzenli bir mezofaz yapısıdır. Yunanca smetos (sabun) kelimesinden türetilmiştir. Simektik mezofaz, kalamitik sıvı kristal materyallerinin belirgin bir mezofazıdır. Simektik fazı oluşturan moleküller, yönelimsel düzenlerin yanı sıra ek olarak tabakalar halinde düzenlenmiştir Bunlar farklı tabaka fazları oluşturduklarından dolayı nematik faza göre daha fazla bir düzen meydana getirir (Yılmaz, 2003). Mezofazlar arasında katılara en çok benzeyen simektik fazdır ve yüksek vizkoziteli veya mumsu katı benzeri maddeler halinde oluşur.
ġekil 1.2.11. Simektik Faz Düzenlenmesi (Solda), Simektik Faz POM Görüntüsü (Sağda)
Simektik mezofazlar, bileşiği oluşturan moleküllerin tabaka normaline göre eğimli olup olmamalarına göre sınıflandırılabilir. Aşağıdaki şekilde farklı simektik mezofazlardaki farklı düzenlenmeler gösterilmektedir. Alfabetik olarak 12 tane faz tanımlanmıştır. Fakat en belirgin mezofazlar A ve C dir (Collings ve Hird, 2001; Demus ve ark., 1998).
ġekil 1.2.12. Farklı Simektik Faz Düzenlenmeleri Simektik A Fazı
Simektik fazlar içerisinde en düşük moleküler düzen içeren faz, simektik A olarak tanımlanmıştır. Bu faz türünde moleküller iki boyutta rahatça hareket ederler ve diğer simektik fazlara göre daha düzensiz katmanlar oluşturur. Üçüncü boyuttaki hareket katmalar arasında olabilir ancak bu hareket belirli bir enerji düzeyi ile sınırlıdır.
SA fazında moleküllerin büyük aksiyel komponentlerinin yönelimsel düzenleri katmanların düzlemine dik olarak yer almaktadır (Koçyiğit, 2009).
ġekil 1.2.13. Simektik A tabakaların düzenlenmesi
Simektik C Fazı
Simektik C mezofazında ise moleküller simektik A mezofazındaki gibi yerleşmişlerdir fakat moleküller tabakalar arasında eğimli yönlenirler. Bu faz, simektik A mesofazının eğimli analoğudur (Collings ve Hird, 2001).
ġekil 1.2.14. Simektik C tabakaların düzenlenmesi
C) Kolesterik (Kiral) Sıvı Kristaller
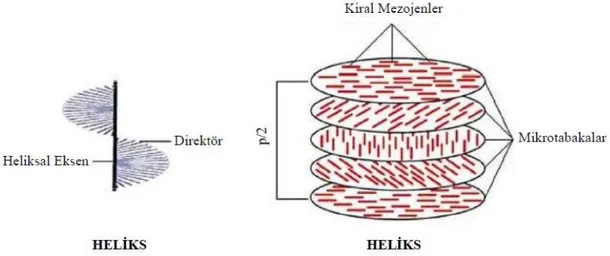
Sarmal yapılı, dolayısıyla kiral olan bir sıvı kristal tipidir. Kolesterik sıvı kristaller kiral nematik sıvı kristaller olarak da bilinir. Tabakalar halinde dizilirler, her bir tabaka içinde konumsal bir düzen yoktur, ama molekülün uzun ekseni (direktörü) tabakadan tabakaya farklıdır. Direktör eksendeki varyasyon periyodik olma eğilimlidir. Bu varyasyonun periyodu (360°'lik bir tam dönüşün tamamlandığı mesafe) hatve (İngilizce pitch; p) olarak adlandırılır. Hatve sıcaklıkla değişir ve eğer kiral nematik sıvı kristal iki substrat arasında sıkıştırılmışsa, sınır koşullarına duyarlılık gösterir.
Kolesterik faz gösteren bileşiklere örnek olarak hidroksipropil selüloz ve kolesteril benzoat sayılabilir (Abdullah ve ark., 2010).
ġekil 1.2.15. Hidroksipropil selüloz (Solda) ve Kolesteril benzoat (Sağda)
ġekil 1.2.16. Kolesterik sıvı kristallerin içindeki heliksel yapı gösterimi
1.2.3.2.2. Diskotik Sıvı Kristaller
Sadece çubuksu yapıdaki moleküler değil aynı zamanda disk şeklindeki moleküllerin de sıvı kristal özellik gösterebileceğini, „Sıvı Kristal Fiziği‟ adlı kitapta bahsedilmiştir (Gennes, 1974). Diskotik sıvı kristallerin keşfi, Chandrasekhar‟ın 1977 yılında (Chandrasekhar ve ark., 1977) yayınlamış olduğu benzen hegzaesterleri üzerine yaptığı çalışmayla başlamıştır. Diskotik sıvı kristaller genellikle aromatik yapıda, düzlemsel sert bir çekirdek ve çevresinde genellikle uzun yan zincirlerin bulunduğu yassı disk şeklindeki moleküller olarak tanımlanırlar. Disk şeklindeki bu yapıların merkezinde benzen, trifenil ve ftalosiyanin gibi poliaromatik yapılar yer alır.
Kalamitik mezogenlerde olduğu gibi, yan zincir ve çekirdeklerdeki farklılaşma molekülün fiziksel özelliklerine büyük ölçüde etki eder. Diskotik sıvı kristal molekülleri uzunluk, diskin yüksekliği ve genişliği, çapları bakımından büyük farklılıklar gösterebilirler. Bu durum diskotik moleküllerde anisotropiye neden olur (Elmalı 2006).
ġekil 1.2.17. Diskotik Sıvı Kristallerin Genel Yapısı (Solda) Diskotik Sıvı Kristale Örnek (Sağda)
Diskotik mesofazların yaygın olarak bilinen iki temel tipi; kolumnar ve nematik fazlardır (Collings ve Hird, 2001).
Çubuk şeklindeki moleküllerin nematik fazı ile karıştırılmasın diye diskotik nematik fazlar ND ile gösterilir (Collings ve Patel, 1997). Diskotik nematik fazlarda uzun aralıklı konumsal düzenlilik yoktur, moleküller kısa eksenler boyunca yönlenirler. Hem çubuk hem de disk şeklindeki moleküllerdeki nematik fazların simetrileri aynı iken, çubuk şeklindeki moleküllerin nematik fazı diamanyetiktir ve optik olarak pozitif, disk şeklindeki ise negatiftir.
Kolumnar Faz
Disk şeklindeki moleküllerin, birbiri üzerine dizilip kolon şeklini aldığı mezofazdır. Bu kolonların farklı şekilde düzenlenmesi, farklı geometrilerin meydana gelmesine neden olur. Kolumnar mezofaz, düzenlenme yapılarına ve istiflenme biçimlerine göre gruplandırılır. Nematik kolumnar sıvı kristallerde, uzun dizi şeklinde sıralanma yoktur ve diğer kolumnar fazlardan daha az düzenlidirler. Uzun sıra şeklinde dizilmiş diğer kolumnar mezofazlar ise, iki boyutlu kafes yapılarına göre sınıflandırılırlar, bunlar; altıgen, dörtgen, kare ve eğik yapılardır.
Nematik Diskotik Faz
Yönelme düzeni bakımından diskotik sıvı kristallerin nematik fazları, kalamitik mezogenlerle benzerlik gösterir. Aşağıdaki şekilde görüldüğü gibi, moleküller aynı yöne doğru yönelmişlerdir fakat konumsal düzen yoktur. Nematik diskotik faz en az düzenli mezofazdır. Nematik diskotik faza, kolumnar fazdan daha az rastlanır.
ġekil 1.2.19. Nematik diskotik faz gösterimi 1.2.4. Sıvı Kristallerin Kullanım Alanları
Sıvı kristal yapılar uzun yıllardır bilinmesine rağmen, son yıllarda oldukça ilgi görmüştür. Bu ilginin artmasının bazı sebepleri olmuştur. Bunların ilki, sıvı kristallerin gösterge endüstrisinde yeni bir devir açmış olması bilim çevrelerince aşırı bir ilgiye sebep olmuştur. Diğer önemli sebep ise, insan vücudu gibi canlı sistemlerinde bulunmaları ve hücre yapısı içerisindeki biyolojik olayların kontrol işlevleri neden ile biyofizik alanındaki araştırmalara yeni bir kapı açmalarıdır. Son olarak ise sıvı kristal bileşiklerin fiziksel özelliklerinin son derece ilginç olmasıdır (Gündüz ve Karapınar 1992).
Sıvı kristal teknolojisinin bilinen en yaygın kullanım alanı kısaca LCD olarak bilinen sıvı kristal ekranlardır. Bir sıvı kristal ekran elde etmek için birkaç yöntem vardır. En çok bilineni “bükümlü nematik sıvı kristal” yöntemidir. Bu yöntemle nematik sıvı kristal madde iki cam levha arasına konularak bir nematik sıvı kristal hücre elde edilir.
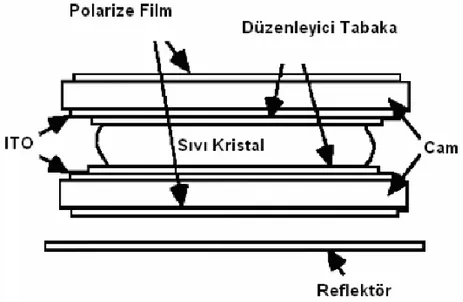
ġekil 1.2.20. Sıvı Kristal Gösterge Hücresi
Camın iç kısmında kalan bölüm önce indiyum kalay oksit (ITO) ile daha sonra da bir yüzey aktif madde ile kaplanır (Collings ve Michael, 1997). Cam levhalardan biri diğerine göre 90o
açı ile çevrilir. Bu durumda üst levha yakınındaki moleküller levhalara paralel, alt levha yakınındaki moleküler ise dik olarak düzenlenmiş olur. Sıvı kristal hücrenin kalınlığı (20-100µm) optik dalga boylarından aşırı büyük olduğu için moleküllerin hücre içindeki yönelimsel hareketi sonucu sıvı kristal hücre üzerine düşen polarize ışığın polarizasyon düzleminin 90o
dönmesine neden olur.
Sıvı kristaller, sıcaklık sensörü olarak da yaygın bir kullanım alanına sahiptir. Tıpta, hastalıklı dokuların teşhisinde sıvı kristal sensörler kullanılır. Deri sıcaklığındaki değişimlerini gözleyerek, sinir ve damar yollarının açık olup olmadığı doktor tarafından belirlenebilir. Deri enfeksiyonları ve tümörlerinin sıcaklığı bunları çevreleyen derinin sıcaklığından iki üç derece daha büyüktür. Bu sıcaklık farkı sıvı kristal sensörle tespit edilebilmektedir (Collings, 2002).
1.2.5. Sıvı Kristallerin Karakterizasyonu
Sıvı kristal fazların bazıları tek bir teknik kullanımıyla oldukça basit bir şekilde belirlenebilir. Fakat sıvı kristal faz tipinin daha kesin olarak belirlenmesinde birkaç farklı teknik kullanılır. Sıvı kristal fazların belirlenmesinde kullanılan en yaygın teknik, polarize optik mikroskoptur (POM). Bu her sıvı kristal fazın farklı optik yapıya sahip olduğunu gösterir.
Diferansiyel Tarama Kalorimetrisi (DSC), optik polarize mikroskobun tamamlayıcısı olarak kullanılır ve faz geçişinde görülen entalpi değişimiyle sıvı kristal fazların varlığını gösterir. Bu teknik sıvı kristal faz tipini belirleyemez, fakat entalpi değişim düzeyi moleküler düzenlenme derecesi hakkında bazı bilgiler verir.
Mezofazların (arafaz) belirlenmesi ve sınıflandırılmasındaki esas teknik X-ışını analizidir. Bir kristalin X-ışını analizi ile mezofaz içindeki moleküllerin pozisyonlarını ayrıntılı olarak belirlemek mümkündür. Yapı belirlemede kullanılan diğer teknikler, Nötron skattering ve NMR (liyotropik sıvı kristal fazların analizinde kullanılır) çalışmalarını kapsar.
2. KAYNAK ARAġTIRMASI
2.1. Sıvı Kristal Oksimler
Gülay Gümüş‟ ün 1999 yılında hazırlamış olduğu yüksek lisans tezi sıvı kristal oksim bileşiklerinin üzerine olmuştur. Bu çalışmada ilk olarak sıvı kristal özellik gösteren temel bileşikler çeşitli sentetik metodlar kullanılarak sentezlenmiştir. Daha sonra bu temel bileşikler ile dikloroglioksim bileşiğinin reaksiyonu gerçekleştirilmiştir ve böylece sıvı kristal oksim bileşiği elde edilmiştir. Daha sonra bu oksim bileşiklerinin nikel ve paladyum kompleksleri elde edilmiş ve bu komplekslerin sıvı kristal özellikleri DSC, POM ve X-ray analiz yöntemleri kullanılarak aydınlatılmıştır. Aşağıda bu bileşiklerin molekül yapıları ve sıvı kristal geçiş sıcaklıkları verilmiştir (Gümüş 1999).
ġekil 2.1.1. Sıvı Kristal Oksim Kompleksi
Mahajan ve Nandedkar, 1998 yılında hazırlamış oldukları çalışmada, iki seri oksim bileşikleri sentezlemişlerdir. Sentezlenen bu seri bileşiklerin sıvı kristal özellikleri incelemişler ve olumlu sonuçlara ulaşmışlardır. Bu seri bileşiklerin molekül yapıları ve sıvı kristal geçiş sıcaklıkları aşağıda verilmiştir.
ġekil 2.1.2. Sıvı Kristal Oksim Bileşikleri Serisi
Tavares A. ve ark. 2012 yılında yaptıkları çalışmalarda çeşitli aldoksim ester bileşiklerinin serilerini sentezlemişlerdir. Sentezledikleri bu ester türevlerinin sıvı kristal özelliklerini incelemişler ve değişik sıvı kristal fazlarda olduklarını tespit etmişlerdir. Sentezledikleri bileşiklerin sıvı kristal özeliklerini tespit etmek için ATR/FT-IR spektroskopisini, DSC (Differential Scanning Calorimetry) ve X-Ray analiz yöntemlerini kullanmışlardır. Sentezlenen bileşik serileri ve sıvı kristal geçiş sıcaklıları şekil 2.1.3 de mevcuttur.

![ġekil 1.2.10. Nematik Faz Düzenlenmesi (Solda), 1,5-Hegandiol-bis{4-[4-(4-n oktiloksi- oktiloksi-benzoiloksi)benzilidinamino]benzoat}bileşiğinin Nematik Faz POM Görüntüsü (Sağda)](https://thumb-eu.123doks.com/thumbv2/9libnet/4604100.85248/35.892.165.776.452.662/düzenlenmesi-hegandiol-oktiloksi-oktiloksi-benzoiloksi-benzilidinamino-bileşiğinin-görüntüsü.webp)