T.C.
İNÖNÜ ÜNİVERSİTESİ
TIP FAKÜLTESİ
ENDOMETRİOMALARIN HİSTOKİMYASAL (PAS,
VAN GİESON) VE İMMÜNHİSTOKİMYASAL (VİMENTİN,
NSE, SYN, PGP9.5, P53, C-KİT) BOYANMA
ÖZELLİKLERİNİN NORMAL OVER DOKUSU VE
NONENDOMETRİOTİK OVARİAN KİSTLERLE
KARŞILAŞTIRILMASI
UZMANLIK TEZİ
DR. FATMA TANILIR ÇAĞIRAN
KADIN HASTALIKLARI VE DOĞUM ANABİLİM DALI
TEZ DANIŞMANI
PROF. DR. ÖNDER ÇELİK
T.C.
İNÖNÜ ÜNİVERSİTESİ
TIP FAKÜLTESİ
ENDOMETRİOMALARIN HİSTOKİMYASAL (PAS,
VAN GİESON) VE İMMÜNHİSTOKİMYASAL (VİMENTİN,
NSE, SYN, PGP9.5, P53, C-KİT) BOYANMA
ÖZELLİKLERİNİN NORMAL OVER DOKUSU VE
NONENDOMETRİOTİK OVARİAN KİSTLERLE
KARŞILAŞTIRILMASI
UZMANLIK TEZİ
DR. FATMA TANILIR ÇAĞIRAN
KADIN HASTALIKLARI VE DOĞUM ANABİLİM DALI
TEZ DANIŞMANI
PROF. DR. ÖNDER ÇELİK
MALATYA-2012
Bu tez, İnönü Üniversitesi Bilimsel Araştırma Projeleri tarafından 2011\166 proje numarası ile desteklenmiştir.
TEŞEKKÜRLER
Uzmanlık tezimin hazırlanması aşamasında her türlü destek ve yardımlarından dolayı değerli hocam Prof. Dr. Önder Çelik, Prof. Dr. Nasuhi Engin Aydın, Yrd. Doç. Dr. Abdullah Karaer, Doç. Dr. Mehmet Gül ve Kadın Hastalıkları ve Doğum Ana Bilim Dalındaki tüm hocalarıma minnet ve şükranlarımı arz ederim. Tezimin hazırlanması sırasındaki yardımlarından dolayı değerli Patoloji Anabilim Dalı çalışanlarına teşekkür ederim.
Anneme, babama, tüm aileme, tüm asistan arkadaşlarıma, Kadın Hastalıkları ve Doğum Anabilim Dalı bünyesinde çalışan tüm hemşire ve personel arkadaşlarıma teşekkür ederim.
İhtisas eğitimim süresince ve tezimin hazırlanması esnasında bana gösterdiği sabır ve destekten dolayı sevgili eşim Ferhat'a, canım oğlum Baran'a teşekkür ederim.
İÇİNDEKİLER Sayfa no TEŞEKKÜR... I İÇİNDEKİLER... II TABLO LİSTESİ... IV ŞEKİL LİSTESİ... V RESİM LİSTESİ... VI KISALTMA LİSTESİ... VII
1. GİRİŞ... 1
2. GENEL BİLGİLER... 3
2.1 ENDOMETRİOZİS... 3
2.1.1. Tanım... 3
2.1.2. Etyoloji... 3
2.1.1.1. Retrograd Menstrusyan Teorisi... 4
2.1.1.2. İmplantasyon Teorisi... 4
2.1.1.3. Doğrudan Transplantasyon Teorisi... 4
2.1.1.4. Çölomik Metaplazi Teorisi... 4
2.1.1.5. İndüksiyon Teorisi... 5 2.1.1.6. Kök Hücre Teorisi... 5 2.1.1.7. Lenfatik/Hematojen Yayılım... 5 2.1.1.8. Mülleriosis... 5 2.1.1.9. Genetik Faktörler... 5 2.1.1.10. İmmünolojik Faktörler... 6
2.1.1.11. Diğer immünolojik Faktörler... 7
2.1.2. Epidemiyoloji... 17 2.1.3. Patoloji... 17 2.1.3.1. Makroskopik Görünüş... 18 2.1.3.2. Mikroskopik Görünüş... 20 2.1.4. Semptom... 20 2.1.5. Teşhis... 22 2.1.6. Sınıflandırma... 23 2.1.7. Tedavi... 25 2.1.7.1. Medikal Tedavi... 26 2.1.7.2. Cerrahi Tedavi... 26
2.1.7.2.1. Ablatif Cerrahi Tedavi... 26
2.1.7.2.2. Cerrahi Olarak Endometriozisis Lezyonunun Çıkarılması………. 26 2.2. Kontrol Grupları... 27 2.2.1. Over... 27 2.2.1.1.Overin Embriyolojisi... 27 2.2.1.2. Overin Anatomisi... 27 2.2.1.3.Overin Histolojisi... 28
2.2.1.4. Overin Sinir Ağı... 29
2.2.2. Benign Seröz Tümörler... 29
2.2.3. Benign Müsinöz Tümörler... 30
2.3. Histokimyasal ve İmmunhistokimyasal Boyalar... 30
2.3.1. Histokimyasal Boyalar... 30
2.3.1.1.Periodic Asid Schiff Reaksiyonu... 30
2.3.1.2. van Gieson boyama yöntemi... 30
2.3.2.1.Vimentin... 31 2.3.2.2. NSE... 31 2.3.2.3. SYN... 32 2.3.2.4. PGP9.5... 32 2.3.2.5. p53... 33 2.3.2.6. c-Kit... 33 3. GEREÇ ve YÖNTEM... 34 3.1. Hasta Seçimi... 34 3.2. Gereç... 35 3.2.1. Numuneler... 35
3.2.2. Kullanılan Kimyasal Malzemeler... 35
3.3. Yöntem... 35
3.3.1. Numunelerin Alınması ve Hazırlanması... 35
3.3.2. İmmunhistokimyasal Boyama Protokolü... 36
3.3.3. Histokimyasal Boyama Protokolü... 36
3.3.3.1. PAS Boyama Protokolü... 36
3.3.3.2.van Gieson Boyama Protokolü... 36
3.3.4. Patolojik İnceleme Sonuçları... 37
3.3.5. İstatistiksel Değerlendirme... 38
4. BULGULAR... 39
4.1. PAS Boyasının ve Makrofaj Pozitifliğinin Karşılaştırılması.... 40
4.2. van Gieson Boyasının Karşılaştırılması... 42
4.3. Vimentin Antikorunun Karşılaştırılması... 44
4.4. NSE Antikorunun Karşılaştırılması... 46
4.5. Synaptofizin Antikorunun Karşılaştırılması... 48
4.6. PGP9.5 Antikorunun Karşılaştırılması... 49
4.7. p53 Antikorunun Karşılaştırılması... 50
4.8. c-Kit(CD117) Antikorunun Karşılaştırılması... 52
4.9. Endometriomaların Seröz Kistadenomla karşılaştırılması... 53
4.10. Endometriomaların Müsinöz Kistadenomla karşılaştırılması.55 4.11. Endometriomaların Normal Over Dokusu ile karşılaştırılması57 5. TARTIŞMA... 60
6. SONUÇ VE ÖNERİ... 64
7. ÖZET... 66
8. SUMMARY... 68
TABLO LİSTESİ
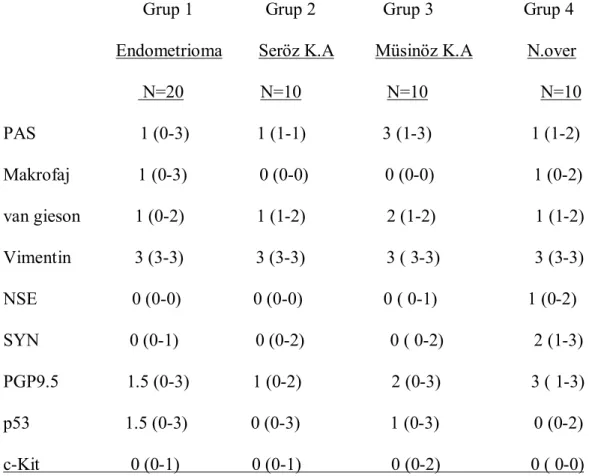
Tablo No Sayfa No Tablo 1: Grupların İmmunhistokimyasal boyanma sonuçlarının istatiksel
değerlendirilmesi...39 Tablo 2: Endometrioma ile Seröz Kistadenomun H-Score yöntemi ile
Student's t testine göre mean değerlerinin karşılaştırılması ve P değerleri...54 Tablo 3: Endometrioma ile Seröz Kistadenomun Mann Whitney U testine göre
ortanca değerlerinin karşılaştırılması ve P değerleri...55 Tablo 4: Endometrioma ile Müsinöz Kistadenomun H-Score yöntemi ile
Student's t testine göre mean değerlerinin karşılaştırılması ve P değerleri...56 Tablo 5: Endometrioma ile Müsinöz Kistadenomun Mann Whitney U
yöntemi ile median değerlerinin karşılaştırılması ve P değerleri...57 Tablo 6: Endometrioma ile Normal Over Dokusunun H-Score yöntemi ile
Student's t testine göre mean değerlerinin karşılaştırılması ve P değerleri...58 Tablo 7: Endometrioma ile Normal Over Dokusunun Mann Whitney U yöntemi ile
ŞEKİL LİSTESİ
Şekil No: Sayfa No
Şekil 1: NF-KB yolağı... 9
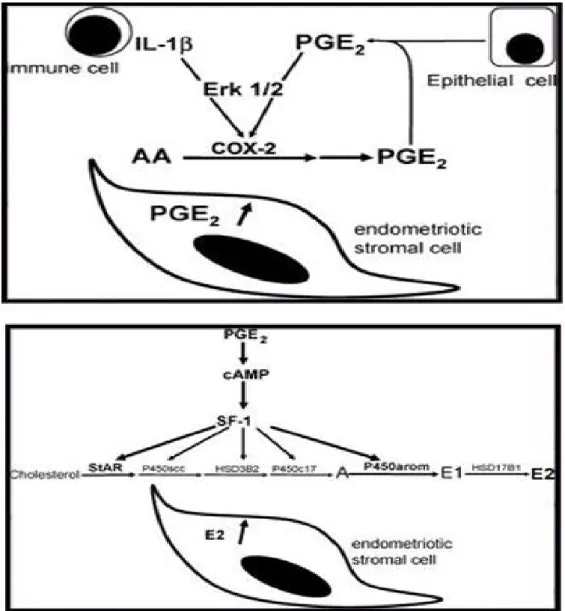
Şekil 2: PGE2-SF-1 üzerinden estradiol üretimi... 14
Şekil 3: Aromataz Enziminin Etkileşimi... 15
Şekil 4: Demir birikimine bağlı olarak NF-kB üzerinden periton hasarı... 16
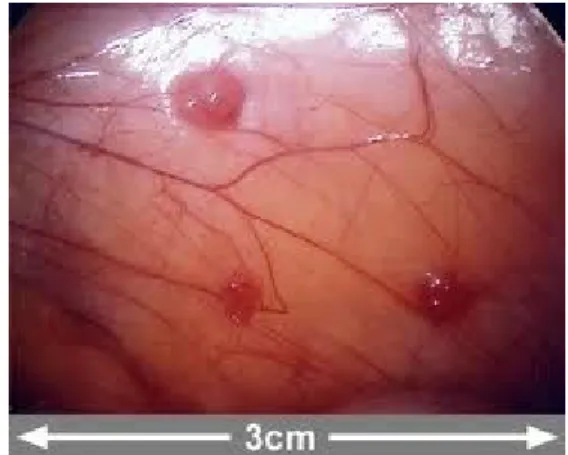
Şekil 5: Peritondaki Endometriotik İmplantlar... 18
Şekil 6: Overdeki Endometriotik İmplantlar... 18
Şekil 7: Endometriozisin radyolojik ve histomorfolojik görünümü... 20
Şekil 8: ASRM tarafından yenilenmiş endometriozis sınıflaması... 24
Şekil 9: ASRM tarafından yenilenmiş endometriozis sınıflaması... 25
Şekil 10: PAS boyasının gruplar arasındaki istatiksel dağılımı... 40
Şekil 11: Makrofaj yoğunluğunun gruplar arasındaki istatiksel dağılımı... 42
Şekil 12: van Gieson boyasının gruplar arasındaki istatiksel dağılımı... 43
Şekil 13: Vimentin boyasının gruplar arasındaki istatiksel dağılımı... 45
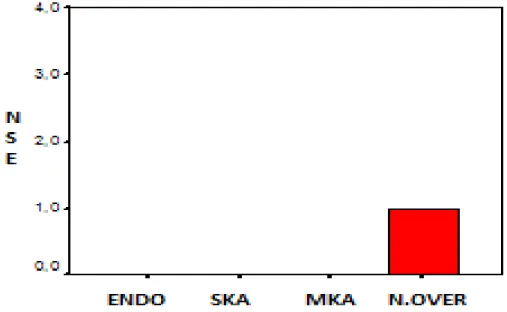
Şekil 14: NSE antikorunun gruplar arasındaki istatiksel dağılımı... 47
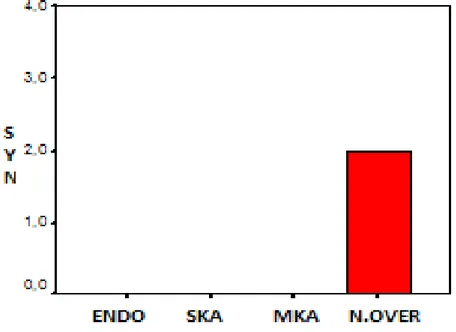
Şekil 15: SYN antikorunun gruplar arasındaki istatiksel dağılımı... 48
Şekil 16: PGP9.5 antikorunun gruplar arasındaki istatiksel dağılımı... 49
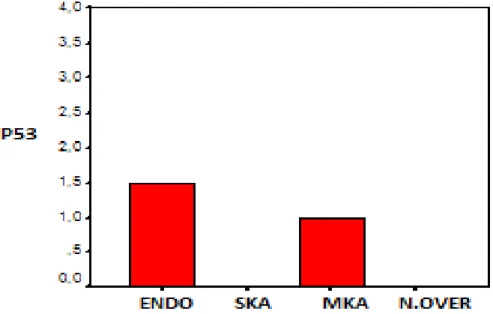
Şekil 17: p53 antikorunun gruplar arasındaki istatiksel dağılımı... 51
RESİM LİSTESİ
Resim No: Sayfa No
Resim 1: PAS yöntemi ile boyanan endometrioma dokusu... 40
Resim 2: PAS yöntemi ile boyanan endometrioma dokusu... 41
Resim 3: PAS yöntemi ile boyanan endometrioma dokusu... 41
Resim 4: van Gieson yöntemi ile boyanan endometrioma dokusu... 43
Resim 5: van Gieson yöntemi ile boyanan endometrioma dokusu... 44
Resim 6: van Gieson yöntemi ile boyanan endometrioma dokusu... 44
Resim 7: Vimentin yöntemi ile boyanan endometrioma dokusu... 45
Resim 8: Vimentin yöntemi ile boyanan endometrioma dokusu... 46
Resim 9: NSE yöntemi ile boyanan endometrioma dokusu... 47
Resim 10: NSE antikoru ile boyanan endometrioma dokusu... 47
Resim 11: SYN antikoru ile boyanan normal over dokusu dokusu... 48
Resim 12: SYN antikoru ile boyanan normal over dokusu... 49
Resim 13: PGP9.5 antikoru ile boyanan endometrioma dokusu... 50
Resim 14: PGP9.5 antikoru ile boyanan endometrioma dokusu... 50
Resim 15: p53 antikoru ile boyanan endometrioma dokusu ... 51
Resim 16: p53 antikoru ile boyanan endometrioma dokusu... 51
Resim 17: c-Kit antikoru ile boyanan müsinöz kistadenom dokusu... 52
KISALTMA LİSTESİ NSE : Nöron spesifik enolaz
SYN : Synaptofizin
PGP9.5 : Protein gen ürünü
C-KİT : Gastrointestinal stromal germ hücre markırı PAS : Periodic asit shiff
NK : Natural Killer
TNF : Tümör nekroz faktör EGF : Epidermal growth faktör CYP 19 : Sitokrom 19
MGDF : Makrofaj deriveted faktör GALT : Galatoz-1 fosfat üridil tansferaz OXEGENE : Oxford endometriozis gene
TRAİL : TNF bağımlı apopitozis indükleyici HGF : Hepatosit growth faktör
IF : İnterferon
IP-10 : IF ile uyarılabilir protein 10 GnRH : Gonadotropin releasing hormon TH 1-2 : T- helper 1-2
IL 17 : Interlökin 17 SCF : Stem cell faktör
MMP : Matrix metalloproteinase 1 uPA : Ürokinaz plazminojen aktivatörü COX : Siklooksigenaz 2
NOS : Nitrik oksit sentetaz NF-KB : Nuclear faktör kappa beta
ICAM -1 : Intercellular adhesion molecule 1 LPS : Lipopolisakkarit
VCAM : Vasküler cell adhesion molecule VEGF : Vasküler endotelyal growth faktör PGE2 : Postoglandin E2
Star : Steroidojenik akut regulatuar protein
COUP-TF : Chicken ovalbumin upstream transcription faktör
DAX-1 : Dys-function is associated with dosage sensitive sex reversal
WT-1 : Wilms tm 1
C/EBPβ-α : CCAAT/enhancer binding protein beta-alfa 17Βohsd : 17 beta hidroksisteroid dehidrogenaz P300/CBP : Creb bağlayan protein
TLR : Toll like reseptör SY38 : Synaptofizin 38
LLNEC : Büyük hücreli undifferansiye nöroendokrin karsinom Ber-EP4 : Antiepithelial spesific antijen
APUD : Amine precursor uptake and decarboxylation cells Bcl-2 : Burkitt hücreli lenfoma 2
Ca : Karsinom
1.GİRİŞ
Endometriozis üreme çağındaki kadınların %5-15’ini etkileyen östrojen bağımlı benign progresif bir hastalıktır. Endometriozis endometrial dokunun uterin kavitenin dışında yer alması ile karakterizedir. En sık üreme çağındaki kadınlarda görülür. Pelvik ağrı, dismenore ve infertilite gibi semptomlara sebep olabilir. İnfertil hastaların %40'ında, pelvik ağrısı olanların %40-50'sinde endometriozis tespit edilmiştir. En sık implantasyon yerleri, pelvik organlar ve periton olmakla birlikte, farklı doku ve organlarda da gözlenebilir. Etyolojisi tam belli olmamasına rağmen çeşitli hipotezler öne sürülmüş ve genel kabul gören, Sampson’nun retrograd menstruasyon hipotezine göre periton boşluğuna ilerleyen menstrüel kan implante olup, endometriozise ilerleyen canlı endometrial hücreler içermektedir (1). Sağlam fallop tüpü olan kadınların %75-95’inde retrograd menstrüasyon olmaktadır. Reflü olan endometrial hücrelerin pelviste implante olup endometriozise ilerlemesinin neden sadece bazı kadınlarda olduğu hala açıklık kazanmamıştır. Peritoneal sıvıdaki çözünebilen faktörler ve hücre içeriği endometriozisin implatasyon ve ilerlemesinden sorumlu tutulmuştur. Endometriozis ile ilişkili inflamatuar cevap, doku tamiri ve neovaskularizasyon peritoneal sıvıdaki makrofaj ve sitokinlere bağlıdır (2). Sitokinler; hücre çoğalması, aktivasyonu, motilitesi, adezyonu, kemotaksisi ve morfogenezinde rol alan muhtelif proteinlerdir. İnterlökinleri (IL-1, IL-2, IL-6, IL-8) ve TNF-α’yı içeren birçok sitokinin endometriozisin patogenezi ile ilişkisi daha önce çalışılmıştır (3-7). IL-8 ve TNF-α’nın endometrial hücrelerin adezyon ve çoğalmasını başlattıkları bilinmektedir (8-9). Endometriozisle ilişkili immünolojik değişiklikler lokal ve sistemik olabilir.
Endometriozisin tanısında altın standart yöntem laparoskopidir. Endometriozisli dismenore semptomu olan hastalarda yapılan bir çalışmada L/S ile alınan endometriotik odaklarda myelinsiz sinir liflerinin yoğun olduğu gösterilmiştir (10). Biz de bu çalışmada Nerve Fiber boyaları ile endometriomalarda sinir liflerinin yoğunluğuna baktık ve pelvik ağrı, dismenore, adezyonların oluşumunda bu sinir liflerinin rolünün olup olmadığını araştırdık.
Endometriomalarda bu çalışmada histolojik sapmada endometriozis zemininde neoplasm gelişiminin olup olmadığını anlamak için p53 ve c-Kit antikorları ile boyama paternlerinin özelliklerini araştırdık. Son zamanlarda moleküler ve patolojik çalışmalar, endometriozisin neoplazi eğilimli bir hastalık olduğunu göstermektedir. Endometriozis, ovarian berrak hücreli kanser ve endometrioid kanser tiplerinde prekürsör olarak rol oynamaktadır. Endometriozisteki moleküler olaylar benign görünür sonradan oksidatif stres, inflamasyon ve genetik defektler (P53 mutasyonu, P53 ekspresyonu, c-Kit aktivasyonu) ovarian kanserin endometriotik odaklarda oluşmasına neden olur (10). Yapılan bir çalışmada endometriozise sahip kadınlarda p53’ün kodon 72 parçasında meydana gelen varyasyonlar sonucunda özellikle arginin ve prolin aminoasitlerindeki
değişimler sonucu apopitozis mekanizmasının tetiklendiği gösterilmiştir. Bu mekanizmanın uyarılması ile endometriozisli kadınlarda neoplazm geliştiği düşünülmektedir. Bu çalışmada p53 ve c-Kit antijenleri kullanılarak endometriozis zemininde malignite gelişip gelişmediğini amaçladık.
Bu çalışmada endometrioma zemininde düz kas, myelinli-myelinsiz sinir lifleri, bağ dokusu farklılıkları, glikojen ve kollajen yoğunluğu, makrofaj ve immun sistem elemanlarında artış olup olmadığını anlamak için histokimyasal ve immunhistokimyasal boyama yöntemlerini kullanarak normal over dokusu ve overin non-endometriotik benign lezyonlarıyla arasındaki farklılıkları araştırdık.
2.GENEL BİLGİLER 2.1.Endometriozis
2.1.1.Endometriozis'in Tanımı
Endometriozis, endometrial bez ve stromanın uterus kavitesi ve kas tabakası dışında bulunmasıdır. Endometriozisin görüldüğü en sık bölge pelvis olmakla beraber vücutta herhangi bir yerde endometrial adacıklar görülebilir.
Endometriozisin kesin nedenleri bilinmese de, histogenezisini tanımlamak için birkaç teori ortaya atılmıştır.
2.1.1.1. Retrograd Menstruasyon Teorisi:
İlk ve en çok kabul gören teori 1920 yılında Dr. John Sampson tarafından ileri sürülmüştür. Menstruasyon döneminde endometrial dokunun fallop tüplerinden ilerleyerek pelvik organlara ekimini ve büyümesini izah eder. Tubadan batın boşluğuna geçen endometrial doku parçaları mezotelyumda hasar olsun yada olmasın yapışıp invaze ettikten sonra canlılıklarını sürdürür ve büyümelerini sağlayan kan damarlarını geliştirirler. Ancak bazı klinik ve deneysel veriler bu teorinin karşısındadır. İlk olarak retrograd menstruasyon kadınların çoğunda olmasına rağmen %15'den daha az kadında endometriozis gelişmektedir. Ayrıca peritoneal sıvıda endometrial hücreler bulunmamaktadır. Bu hastalığın, erken pubertede hatta nadiren de olsa yenidoğanlarda, Mayer Rokitansky Kuster Hauser sendromu olanlarda da görülebilmesi bu teori ile tamamen çelişmektedir. Buna rağmen endometriotik doku ototransplantın karakteristiklerinden yoksundur. Ayrıca bu teori endometriozisin akciğerler, deri, lenf nodları ve memede olmasını açıklamakta yetersizdir (1).
Bu teoriyi destekleyen çalışmalar:
1-Retrograd menstrüasyon kadınların %70-90'nda görülür, endometriozisli kadınlarda hastalığı olmayanlara göre daha sık izlenir. Menstrüasyon gören kadınların %59-79'unda peritoneal sıvıda endometrial hücrelerin varlığı rapor edilmiştir.
2-Menstrüasyon gören kadınlara yapılan laparoskopi sırasında tüplerin fimbrial uçlarında kan akımı izlenmiştir.
3-Endometriozis en sık pelvisle bağlantılı olan bölümlerde görülür. En sık overler, anterior ve posteior cul de sac, uterosakral ligamentler, posterior uterus, posterior broad ligamentlerde görülür.
4-Menstrüel akımdaki endometrial fragmanlar, doku kültürlerinde gelişebilirler ve kadınlarda menstrüasyondan sonra peritoneal sıvıdan elde edilebilirler.
5-Maymun serviksleri transpoze edilerek, menstrüasyon peritoneal kavitede oluşturulunca, endometriozis geliştiği gösterilmiştir.
6-Menstrüel akım obstrüksiyonu olan kadınlarda endometriozis insidansının daha yüksek olduğu saptanmıştır. Genital organda menstrüel kanın dışarı atımını sağlayan yolda herhangi bir tıkanıklık olması bu genç kadınlarda endometriozis oluşum insidansını arttırır.
7-Endometriozis riski, siklusu kısa ve daha uzun süreli menstrüasyon gören kadınlarda daha yüksektir.
8-Endometriozisli kadınların uteruslarında artmış ve düzensiz peristaltizm saptanmıştır ve bu da sonuçta artmış endometrial reflüye neden olmaktadır.
9-Ovarian endometriozis, uterustan overe lenfatik akım yolu ile veya retrograd menstrüasyon ile açıklanabilir.
2.1.1.2. İmplantasyon Teorisi:
Endometrial dokunun menstrüasyon sırasında fallop tüpünden geçerek batına dökülmesi ve yerleşmesi esasına dayanır. Bu nedenle endometriozisin gelişimi periton boşluğuna ulaşan doku miktarına, endometrial hücrelerin peritona yapışmasını sağlayan faktörlere veya kadının immün sisteminin menstrüel kanı yok edebilmesine bağlıdır.
2.1.1.3. Doğrudan Transplantasyon Teorisi:
Epizyotomi yerinde, sezaryen ve diğer cerrahi skarlarda endometriozis oluşumunu izah etmektedir. Pelvis dışındaki dokularda endometriozis gelişimi endometrial hücre veya dokuların, lenfatik veya kan yoluyla yayılımı ile olabilir.
2.1.1.4. Çölomik Metaplazi Teorisi:
Çölomik kavite farklılaşmamış hücreler ve endometrial dokuya dönüşme potansiyeli olan hücreler içermektedir. Bu teori endometriumu da içeren pelvik organların tamamının çölomik kaviteyi döşeyen hücrelerden köken aldığını embriyolojik çalışmaların sonucuna dayanarak savunmaktadır.
Çölomik metaplazi teorisinin savunulduğu parametreler şunlardır: 1-Endometriozis müllerian anomali yokluğunda da adolesan kızlarda olabilir. 2-Endometriozis prepubertal kızlarda rapor edilmiştir.
4- Baş parmak, uyluk, dizde endometriozis gelişimi ise mezenkimal ekstremite tomurcuklarından erken embriyogenez sırasında çölomik epitele yakın kısımlardan gelişmiş olabileceğini destekler.
2.1.1.5. İndüksiyon Teorisi:
Çölomik metaplazi teorisinin daha genişletilmiş formudur ve peritona yayılan endometrial debrinin farklılaşmamış periton hücrelerini aktive ederek metaplaziye gitmesini sağlayan faktör salgıladığını ileri sürer.Periton hücrelerinin kendiliğinden ya da bir etken yardımı ile metaplazi geliştirdiğini gösteren bir delil yoktur.
Endometriozisli kadınların periton sıvılarında lökosit miktarının ve bu hücrelerden salınan sitokin miktarının artması, endometriozisin başlaması ve ekilmiş ektopik dokuların büyümesine sebep olabilir. İmmün sistem kesinleşmemiş olmakla beraber önemli bir ölçüde endometriozis patogenezinde rol almaktadır.
2.1.1.6. Kök Hücre Teorisi:
Kemik iliğinden kaynaklanan kök hücreler farklı anatomik bölgelerde endometriotik dokulara farklılaşabilir (10).
2.1.1.7. Lenfatik/Hematojen Yayılım:
Endometrial kavitede menstrüel doku ven ve lenfatikler aracılığıyla diğer bölgelere göç etme kabiliyetine sahiptir.
2.1.1.8. Mülleriosis (Müllerianosis) :
17. yy sonları ve 18. yy endometriozisin embriyogenezisteki küçük defektlerden kaynaklandığı öne sürülmüştü. Bu teori tekrar popularite kazanmış olup Mülleriosis ya da Müllerianosis olarak adlandırılmıştır. Önceleri endometriozis olarak tanımlanmış ancak daha sonra farklı bir hastalık olduğu anlaşılmıştır (10).
1-Ektopik endometrium mevcudiyeti insan fetuslarında otopsilerde %11 oranında gösterilmiştir.
2-Ektopik endometrium organogenezisin son aşamasında gözden kaybolabilir. 3-Müllerian sistem teorisi uyarınca; in utero aynı moleküller, çevre müllerian kanal fetal gelişimi boyunca peritoneal implantların ekstrauterin dislokasyonunu kolaylaştırabilir.
2.1.1.9. Genetik Faktörler:
Bazı kadınlarda peritoneal kaviteye menstrual debrislerin taşınmasına rağmen endometriozis gelişmemesi, genetik ve immünolojik faktörleri düşündürmektedir. Simpson, endometriozisli hastaların birinci derece akrabalarında, riskin 6-9 kat fazla olduğunu göstermiştir (10-16). Ciddi endometrioziste kız kardeşler için bu risk 15 katına çıkabilir.
Dmowski ve arkadaşları, endometriozisli maymunlarda, endometrium dokusuna karşı hücresel immünitenin oluştuğunu göstermiştir (14). Belirgin Mendelyen kalıtım paterni belirlenememiş, multifaktöryel kalıtım kabul edilmiştir (16). Endometriozis ve diğer otoimmun hastalıklar arasında, endometriozis ve bireysel insan lökosit antijenleri arasında olduğu gibi bir ilişki gösterilmiştir (17, 18). Somatik kromozomlardaki genetik değişikliklere (19) ve tümör supressör genlerini inaktive eden DNA delesyonlarının, endometriozisin başlangıcı, devamı veya ilerlemesinde katkıda bulunan olaylar olduğu öne sürülmektedir (20, 21).
OXEGENE (Oxford Endometriozis Gene), Gene Behind Endometriozis, International Endogene Study çalışmaları etkilenmiş kızkardeşler üzerinde kantitatif genetik analize dayanarak (etkilenmiş kızkardeşlerin nedensel allel açısından benzer kopyaları taşıma şansı beklenenden fazladır) oluşturulmuştur (10).
Endometriozisin nokta mutasyon ya da polimorfizmi sonucu meydana geldiğini düşündüren gen analizleri;
1-GALT gen (galaktoz-1-fosfat üridil transferaz gen)
2-Faz II detoksifikasyon geni (Glutatyon-S transferaz ailesi, bu gen ailesi üyelerinin 2, 3, 7, 8- tetraklordiabenzo- P- dioksin detoksifikasyonundan sorumlu)
3-Faz I detoksifikasyon genleri (Ah reseptör, CYPA1, NAT2), Östrojen reseptör, Aromataz gen (CYP19) üzerinde çalışılmış ama farklı çalışmalarda tutarlı sonuçlar elde edilememiştir.
Endometriotik dokuda genetik değişikliklerden biri tümör supressör gen (PTEN, K-ras, P53) ve onkogenlerin, endometriozis etyopatogenezisinde rolü olabilir. DNA microarray yöntemi ile yapılan çalışmada endometriozisli hastaların ötopik endometriumlarında 4133 geni farklı eksprese ettiklerini bildirmişler. Bu genlerin adezyon molekülleri, endometrial epitelden sekrete edilen proteinler, sitokinler ve immun sistemle ilişkili genler olduğu microarray ile saptanmıştır.
2.1.1.10. İmmünolojik Faktörler :
Menstrüasyon sırasında endometrial fragmanların peritoneal kaviteye reflüsü çok yaygın bir olay olmakla birlikte her kadında endometriozis gelişmez. Endometriozisli kadınlarda immun sistemde değişiklikler olabilir ve hastalık, pelvik kaviteden kaynaklanan canlı endometrial hücrelerin azalmış immunolojik klirensi sonucu gelişebilir (22, 23). Normal durumlarda reflü olan endometrial hücreler ekstrasellüler matrikse yapışmaz ve bu hücreler kendi adhezyon reseptörlerinden farklı uyarıları alarak apopitozise uğrarlar. Endometriozisli kadınlarda bu hücreler, peritonun mezotelial hücrelerine yapışma, prolifere olma ve neoangiogenezis oluşturma kapasitesine sahiptir ve bu da aktif endometriozis gelişmesi ile sonuçlanmaktadır (24).
Otolog endometrial hücrelere karşı azalmış hücre kaynaklı sitotoksisitenin, endometriozisle beraber olduğu rapor edilmiştir (25, 26, 27). Otolog endometrial hücrelerin, bir kadının immun sistemine doğal bir hedef oluşturabilmesi için genetik ve immunolojik bir takım faktörlerin olması gerekmektedir (26). Diğer otolog dokuların, otolog transplantasyonunun genelde başarılı olduğu görülmektedir.
Endometriozisli hastaların düşük Naturel Killer (NK) hücre aktivitesine sahip olduğunu bildiren çalışmalar (28, 29, 30, 31, 32) ve aksine bu hastalarda artmış NK aktivitesini gösteren çalışmalar da mevcuttur (28, 29, 33). Ancak NK hücre aktivitesinde, normal bireylerde dahi geniş varyasyonlar görülür. NK aktivitesi sigara, ilaç, egzersiz gibi değişkenlerden etkilenmektedir.
Endometriozisli kadınlarda peritoneal makrofajların yüksek bazal aktivasyonu, sperm motilitesini azaltıp, sperm fagositozunu arttırarak veya fertilizasyonu önleyerek fertiliteyi bozmaktadır (34, 35). Bunları olasılıkla, TNFα gibi sitokinlerin artmış sekresyonu ile yaparlar (36). TNFα aynı zamanda, ektopik endometriumun pelvik implantasyonunu arttırabilir. İnvitro olarak, insan endometrial stromal hücrelerin mezotelyal hücrelere yapışmasının, TNFα’nin fizyolojik dozunun mezotelyal hücrelerle etkileşimi ile arttığı gösterilmiştir.
Makrofaj ve diğer hücreler endometrial hücrelerin büyümesini, Epidermal Growth Faktör (EGF), Makrofaj Deriveted Faktör (MGDF), fibronektin gibi büyüme ve anjiogenetik faktörlerin ve integrinler gibi adhezyon moleküllerinin sekresyonu ile hızlandırır (36, 37, 38, 39, 40).
Aktif pelvik makrofajların ve lenfositlerin artmış konsantrasyonunun yanı sıra, büyüme faktörleri ve spesifik sitokinlerin yükselmiş düzeyleri, endometriozis ile immun yanıtın yakın ilişkisi hipotezini desteklemektedir.
Öne sürülen etyolojik teoriler, hastadan hastaya olan farklılıkları açıklamaya yardımcıdır. Endometrial hücreler mekanik olarak yayılabilir, metaplaziden gelişebilir ve hastalığın progresyonu bireylerin immun yanıtlarından etkilenebilir.
2.1.1.11. Diğer İmmunolojik Faktörler
2.1.1.11.1. TNF Bağımlı Apopitoz İndükleyici Ligand (TRAIL) Aktivitesi: Çeşitli çalışmalarda regürjite endometrial hücrelerin temizlenmesinde apopitozun önemli bir mekanizma olduğu gösterilmiştir. Endometriotik hücrelerde apopitoz mekanizmaları bozulmuş olabilir. TRAIL, TNF süperailesi üyesidir ve DR-4, DR-5 reseptörlerine bağlanarak apopitozu indükler. DR-5 endometrial stromal hücrelerde bulunmaktadır. Harada ve ark endometriozisli kadınlarda peritoneal sıvıda osteoprotegerin düzeylerinin aşırı artmış olduğunu göstermişlerdir (10). Osteoprotegerin, TRAIL reseptörlerinin inhibitörüdür ve ileri evre hastalarda TRAIL/Osteoprotegerin oranının azaldığı fark edilmiştir. Ayrıca DR-5 reseptörlerinin, endometriozisli kadınlarda stromal ekspresyonu sağlıklı kadınlara göre anlamlı olarak azaldığı gösterilmiştir. Sonuçta endometriotik stromal hücrelerin apopitozdan kaçmaya eğilimli oldukları anlaşılmaktadır. Ayrıca tunikamisin maddesi ile endometriotik hücrelerde DR-5 ekspresyonu ve TRAIL aracılı apopitozun arttırılabileceği bildirilmiştir (10).
2.1.1.11.2. Aberan Peritoneal Çevre:
Endometriozisli hücrelerin proliferasyon ve migrasyonundan ve anjiogenetik aktiviteden sorumlu olan mediatörlerden biri hepatosit büyüme faktörüdür (HGF). Endometriozisli kadınlarda özellikle ileri evre hastalıkta peritoneal sıvıda HGF düzeylerinin arttığı saptanmıştır. Öte yandan bir anti-anjiogenik belirteç olan IFγ ile uyarılabilir protein 10 (IP-10) düzeylerinin endometriozislilerde azaldığı bulunmuştur (10).
2.1.1.11.3. Ovulasyon Etkisi:
Preovulatuar folikül ovulasyonla birlikte içindeki folikül sıvısını peritona bırakır. Bu sıvı çeşitli büyüme faktörleri ve midkin proteini içerir. Midkin heparin bağlayıcı büyüme faktörü ailesinden bir proteindir. Folikül sıvısında bol miktarda bulunur ve folikülogeneziste rol oynadığı düşünülmektedir. Ayrıca endometriotik odakların gelişimine katkıda bulunabilir. Kültüre edilmiş endometrial stromal hücrelerde midkinin proliferasyonu arttırdığı Hirota ve ark. tarafından gösterilmiştir (10). Endometriozisli kadınlarda peritoneal sıvı midkin düzeyleri anlamlı olarak yüksek bulunmuştur (10). Bu da regürjite olan endometrial debrislerin implantasyonuna katkıda bulunan bir faktör olabilir. Bu artış GnRH analogları tedavisi ile baskılanabilmektedir.
2.1.1.11.4. Th 2 Hücreler
Endometriotik lezyonlarda lenfosit, makrofaj, NK hücreler, mast hücreleri ve dendritik hücreler bulunmaktadır. Bu hücreler çeşitli mediatörler aracılığı ile endometriotik hücrelerle iletişim halindedir. Bu immün hücrelerin endometriozis patofizyolojisinde kritik rol oynayabileceği ve bir tedavi hedefi olabileceği düşünülmektedir.
Endometriozisli kadınlarda Th2 hücrelerden üretilen bir sitokin olan IL-4, periton sıvısında artmıştır. Ayrıca stromada Th2 lenfositlerin bulunduğu ve bunlarda IL-4 mRNA düzeylerinin yükseldiği gösterilmiştir. IL-4, Th2 hücreleri için potent bir kemoatraktan olan ve aynı zamanda anjiogenik bir sitokin olan ötaksin salınımını arttırmaktadır. Sonuçta endometriozis Th2 bağımlı bir inflamatuar hastalık olarak da kabul edilebilir.
2.1.1.11.5. Th17 Hücreler
Çıplak Th hücreler; Th1, Th2, Th17 ve regülatuar hücrelere farklılaşmaktadır. İnflamasyonda esas görevli olan ise Th17 hücreler ve bunların major sitokini olan IL-17’dir. Endometriozislilerde Hirata ve ark, immünhistokimyasal olarak epitel yüzeyinde ve hemosiderinli stromal dokularda IL-17 pozitif hücrelerin sağlıklı kadınlara göre çok daha yüksek düzeyde bulunduğunu göstermişlerdir (10). IL-17’nin IL-8 salgısını ve stromal hücrelerin proliferasyonunu arttırdığı bilinmektedir.
2.1.1.11.6. Mast Hücre Aracılı Mekanizmalar
Endometriotik dokularda mast hücrelerinin bulunduğu bilinmektedir. Bu hücrelerin adezyonunda stem cell factor (SCF) ve bunun reseptörü olan c-Kit rol oynamaktadır. Hirata ve ark. özellikle erken evre endometriozislilerde peritoneal SCF konsantrasyonunu arttığını bildirmektedirler (10). Mast hücrelerden salınan bir enzim olan triptaz, endometriotik hücre membranda protez aktive reseptör-2 (PAR-2)
ekspresyonunu arttırmaktadır. Bu da bir yandan endometriotik hücrelerde proliferasyonu uyarmakta, diğer yandan IL-6 ve IL-8 salınımını arttırmakta ve bu da nötrofil, makrofajların endometriotik dokulara kemotaksisine neden olmaktadır.
2.1.1.11.7. Adiponektin
Adiponektin bir adipositokindir, glukoz metabolizması ve yağ asidi katabolizmasında görev almaktadır. İn vivo çalışmalarda adiponektinin endometrial hücrelerden IL-6 ve IL-8 salınımını azalttığı yani anti-inflamatuar özellik gösterdiği bulunmuştur. Endometriozislilerde ise serum ve periton sıvısında adiponektin konsantrasyonunun azaldığı bildirilmiştir. Sonuçta bugünkü bilgilerimize göre endometriozisin başlangıç noktası menstrüel regürjitasyondan daha önce, ötopik endometriumdaki farklılıklar olarak göze çarpmaktadır. Ayrıca hastalarda var olan peritoneal çevre farklılıkları, regürjite olan endometriotik hücrelerin bu dokuda tutunması, yaşaması ve çoğalmasına katkıda bulunmaktadır.
2.1.1.11.8. Endometriozis ve NF-kB Yolağı
Şekil 1. NF-KB yolağı (10).
Regürjite olan endometrial hücreler peritoneal kavitede sırayla'yaşar’'adere olur’'invazyon gösterir’ ve 'prolifere olur’. Etyolojide anatomik, genetik, çevresel, hormonal, immün, oksidatif stres faktörleri ve inflamatuar sitokinler birlikte etkindir. NF-kB hücre proliferasyonu, apopitoz, adezyon, invazyon ve anjiogeneziste kritik rol oynayan bir promoter faktördür. Endometriozisin erken gelişim evrelerinde rol oynadığı gösterilmiştir. NF-kB, IL-1, IL-6, IL-8, inducible NOS, COX-2 aktivasyonunda, IFγ, TNFα, ICAM-1 gibi mediatörlerin salınımında, apopitozun kontrolünde, hücre proliferasyonunda (EGF), doku invazyonunda (MMP-1, uPA) ve anjiogenezde genetik düzeyde kontrol sağlayan transkripsiyon faktörüdür.
Üç farklı NF-kB yolağı tanımlanmıştır:
2- Aktive IKK alfa: Non-kanonik yolağı aktive eder.
3- Çok çeşitli uyarılar atipik yolak adı verilen yolağı uyarır. 2.1.1.11.8.1. Ötopik Endometriumda NF-kB
NF-kB yolağı, B hücreleri, bazı monositler ve malign hücrelerde aktifleşirken, diğer vücut hücrelerinden birçoğunda inaktiftir. NF-kB aktivasyonu ötopik endometriumda da gerçekleşir. Endometriozis odaklarında NF-kB aracılı COX-2, IL-8 gibi proinflamatuar sitokin sentezi gösterilmiştir. Ötopik endometriumda implantasyon ve menstrüasyon sırasında NF-kB aktivasyonu bulunmuştur. Progesteronun NF-kB’yi inaktive eden IKK alfa aktivitesini arttırdığı gösterilmiştir.
2.1.1.11.8.2. Endometrioziste NF-kB
İn vivo ve in vitro çalışmalarda, endometrioziste bazal ve TNFα ile uyarılmış kanonik NF-kB yolağının (p50/p65) aktifleştiği gösterilmiştir. Peritondaki kırmızı endometriotik lezyonlar en baskın inflamasyonu içerenlerdir. Daha sonra kanama ve skatrizasyonla siyah renge bürünür. Kırmızı lezyonlarda p65 dimerlerinin siyah lezyonlara göre anlamlı olarak yüksek olduğu bulunmuştur. Tıpkı pre-B ya da matür B hücrelerinde olduğu gibi, kırmızı ve siyah lezyonlarda ıKB alfa aktivitesi de benzer bulunmuştur. Böylece aktif NF-kB ile IkB kompleksi bir denge içinde sürdürülmektedir. Sonuç olarak endometriotik lezyonlarda kanonik yol aktiftir.
2.1.1.11.8.3. NF-kB ve Endometriozisteki İnflamatuar Yanıt
Endometriotik hücrelerde NF-kB aktivasyonu ve sonucunda IL-6, IL-8, TNFα, ICAM-1 sentezi olduğu in vivo ve in vitro çalışmalarda gösterilmiştir. Ayrıca sığır endometrial hücrelerinde COX-2’nin de NF-kB bağımlı aktive olduğu gösterilmiştir. NF-kB aktivasyonu, VCAM, ICAM ve E-selektin ekspresyonunu arttırır ki bunlar endotel kökenli sitokinlerdir, endometriotik odaklarda endotel varlığının göstergesi olabilir. Özellikle kırmızı endometriotik lezyonlarda NF-kB aktivasyonu ve IL-1 Reseptör 1 ekspresyonu belirgindir (10).
2.1.1.11.8.4. NF-kB ve Endometrial Hücrenin Yaşaması
NF-kB’nin proliferatif ve antiapopitotik olduğu birçok çalışmada gösterilmiştir. İn vivo çalışmalarda NF-kB inhibisyonu erken evre endometriotik lezyonlarda hücre çoğalmasının yavaşlaması ile sonuçlanır. İn vitro çalışmalarda ise NF-kB blokajı ile hücre çoğalmasının engellendiği ve apopitozisin uyarıldığı gösterilmiştir. Ayrıca endometrioziste daha önce hiç çalışılmamış olmasına rağmen diğer bazı hücrelerde NF-kB’nin HGF ve Survivin sentezinde de rol oynadığı gösterilmiştir, bu da endometriotik hücrelerde NF-kB inhibisyonunun anti-proliferatif etkisine katkıda bulunan faktörlerden biri olabilir.
2.1.1.11.8.5. Makrofajlarda NF-kB, Demir ve Oksidatif Stres
Endometriozisteki inflamasyona makrofajların katkısı bilinmektedir. Makrofajlar normalde fagositoz, demir metabolizması, antimikrobiyal aktivite ve TNF aracılı sitotoksisite gösterirler. Peritoneal kavitedeki makrofajlar buraya adere olan
endometriotik hücreleri, eritrositleri ve doku parçalarını temizleme özelliğine sahiptir. Zaten bu mekanizmanın retrograd akımı karşılayamaması ile endometriozisin oluştuğu düşünülebilir.
Makrofajlardan üretilen IL1, IL-6, IL-8, TNFα, iNOS ve VEGF endometriotik lezyonların büyümesine katkıda bulunabilir. Makrofajlardaki bu inflamatuar yanıt, oksidatif stres ve demir ile tetiklenebilir, burada da aracı yine NF-kB’dir. Fizyolojik dozlardaki demir makrofaj fonksiyonunu arttırır, aşırı demir birikimi ise makrofaj fagositozunu bozarken NF-kB’nin de bilinen bir stimülatörüdür. Endometriozisli hastalarda endometrial hücrelerde, peritonda ve makrofajlarda aşırı demir birikimi olduğu gösterilmiştir. Endometriotik lezyonlardaki biriken demirin oksidatif stresten ve inflamasyondan sorumlu olabileceği çeşitli çalışmalarla gösterilmiştir. Demek ki endometrioziste odaklarda demir birikimi bir yandan makrofaj fonksiyonlarını bozarken, diğer yandan NF-kB bağımlı inflamasyonu da arttırmaktadır.
2.1.1.11.8.6. NF-kB ve Hücre Adezyonu
Adezyon ve invazyon endometriozisin başlangıç adımlarıdır. Endometriotik hücreler ile diğer hücreler ve ekstraselüler matriks arasında rol oynayan integrin ve kaderin benzeri moleküller bulunmaktadır. Endometriotik hücre peritona tutununca MMP ve plazmin ailesi gibi ekstraselüler matriksi degrade eden enzimler üretir ve submezotelyal alana tutunur. NF-kB’nin MMP, ürokinaz tip plazminojen aktivatörü (uPA) ve doku plazminojen aktivatörü sentezini arttırdığı gösterilmiştir. uPA promotör bölgesine NF-kB direk bağlanıp aktive edebilir. NF-kB’nin endometriotik hücre dışındaki diğer bir çok hücrede MMP1, MMP2, MMP3, MMP9 ve MMP13 sentezini arttırdığı gösterilmiştir. NF-kB inhibisyonunun ise endometriotik hücrelerde invazyonu engellediği saptanmıştır.
2.1.1.11.8.7. NF-kB ve Anjiogenezis
Rat endometriozis modelinde NF-kB inhibisyonunun VEGF ekspresyonunu azalttığı gösterilmiştir. Ayrıca endometriotik hücrelerde NF-kB aktivasyonu ile MIF ve IL-8 sentezinin arttığı bilinmektedir ki ikisi de anjiogenik mediatörlerdir.
2.1.1.11.8.8. NF-kB İnhibitörleri ve Endometriozis
NF-kB inhibisyonunun in vivo ve in vitro çalışmalarda endometriozis lezyonlarını gerilettiği gösterilmiştir. Curcumin, sulindac, talidomid, SN-50, IKK inhibitör, GnRH analogları, üriner hCG, progesteron, MG 132 vs. gibi NF-kB inhibitörlerinin kullanımı proinflamatuar sitokin salınımını, COX-2 aktivasyonunu, adezyon moleküllerini azaltmaktadır. Ratlarda prolidin ditiokarbomat, bortezomib ve kafeik asit fenetil ester kullanımı NF-kB yolağı üzerinden hücre proliferasyonunu, anjiogenezisi, sitokin ekspresyonunu ve endometriotik odakları geriletmektedir.
Bu konuda kliniğimizden de literatüre katkıda bulunulmuştur. 2008 yılındaki çalışmada deneysel endometriozis modelinde bortezomib’in NF-kB inhibisyonu yaparak odakları gerilettiği gösterilmiştir (10).
Yine kliniğimizin yaptığı ve yeni tamamlanan bir başka çalışmada bir NF-kB inhibitörü olan ve hastaların çok daha rahat kullanabileceği bir ajan olan disülfiramın deneysel endometriozis modelinde terapötik potansiyeli olduğu gösterilmiştir.
Sonuçta NF-kB yolağının endometriozis etyolojisinde kilit bir kademe olduğu ve tedavinin yeni hedefi olabileceği aşikardır.
2.1.1.11.9. Hormonal Faktörler ve Steroidogenez : Östrojen endometriozis için esansiyeldir.
Biyolojik aktif östrojen olan östradiol kolesterolden altı basamaklı seri bir enzimatik konversiyonla oluşturulur (overde iki hücrenin parakrin etkileşimi).
İki Hız Sınırlayıcı Enzim ;
1. Kolesterolün mitokondri girişini kolaylaştıran StAR (steroidojenik akut regulatuar protein)
2. Androstenedionun östrona dönüşümünü sağlayan Aromataz
Star, aromataz ve diğer steroidogenik enzimler endometrioziste eksprese edilir. ve endometrik kolesterolden östradiole de novo sentez etme yeteneğine sahiptir.
Normal endometrium dokusu östradiol biyosentez edemezken, endometriozisli hastaların ötopik endometrium dokuları aromataz aktivitesi gösterebilir.
Yakın zamanda yapılan çalışmalar endometriotik odakların adrenal ve ovarian sekresyondaki substratlara gereksinim olmaksızın de novo kolesterolden östrojen üretebildiklerini göstermiştir.
Endometriozisli hastaların ötopik endometriumları aromataz mRNA eksprese ederler ve bu aromataz ekspresyonu ve enzimatik aktivitesi ektopik implantlarda 400 katına çıkar.
Siklooksigenaz 2 (COX-2) ekspresyonu PGE2 sentezi için önemlidir, ötopik endometrium ve endometriotik dokularda ekspresyonu artmıştır.
PGE2 endometriotik dokulardaki östrojen biyosentez yolağında anahtar rol oynar, çünkü anahtar steroidogenik genlerin (en çok stAR ve aromataz) potent stimülatörüdür.
Siklooksijenaz enzimi araşidonik asidi PGG2 dönüştürür, PGG2’de PGE2 sentetaz ile PGE2 dönüşür.
COX-1 ve COX-2 olarak adlandırılan iki farklı gen siklooksijenaz enzimi kodlar ki bunlardan COX-2 endometriozisli hastaların stromal hücrelerinde ve ötopik endometriumlarında up-regüle olur.
IL-1β ve PGE2 endometriotik ve endometrial stromal hücrelerde COX-2 indüklerken, VEGF ve E2 uterin endotelyal hücrelerinde COX-2 indükleyerek dokularda PGE2 oluşumunu artırır.
Endometriozis dokusunda PGE2 sentezinin regulasyonu tam bilinmemektedir. Östrojen, büyüme faktörleri, metalloproteinazlar endometriotik dokunun büyüme ve invazyonunu artırırken, prostaglandin ve sitokinler ağrı, inflamasyon ve infertilite aracılık ederler (10).
Endometrioziste PGE2/cAMP–bağımlı aromataz ekspresyonunda moleküler anormallikler ;
1- Transkripsiyonel artırıcı olan Steroidojenik faktör 1 (SF 1)
2- İnhibitörler olan COUP-TF (chicken ovalbumin upstream transcription factor, COUP-TF)
3- Coup-TF hem endometrial hem de endometriotik hücrelerde;
4- SF-1 endometriotik dokulardan eksprese olurken, normal ötopik endometrial hücrelerde eksprese olmaz.
Coup-TF ötopik endometrial stromal hücrelerde aromatazı inhibe ederken, buna karşın endometriotik stromal hücrelerde aşırı artmış SF-1 ekspresyonu bu inhibisyonun üstesinden gelerek aromataz aktivitesini artırır.
Normal endometrium dokusunda aromataz aktivitesini inhibe edip endometrioziste aktive eden pek çok mekanizma mevcuttur.
C/EBPα aşırı ekspresyonu P450 aromataz enzimini stimule ederken, C/EBPβ inhibe eder.
C/EBPβ in vivo endometriosis dokusunda down reguledir. Ötopik endometriumda ise değişmez.
SF-1 Regulasyonunu Sağlayan
1- DAX-1 (SF-1 bağımlı aromataz ekspresyonunu hem endometriotik hem de endometrial hücrelerde inhibe eder.
2- WT-1 endometriotik/endometrial hücrelerde aromataz promotor II aktivitesini inhibe eder.
Özellikle WT-1endometriotik dokularda invivo down regule olurken, DAX-1'de bu gözlenmez. WT-1 ötopik endometrium steroidogenezin inhibisyonunun fizyolojik önemli bir korepresörüdür.
3- P300/CBP (CREB-bağlayan protein) SF-1 koaktivatörüdür, endometriotik ve endometrial stromal hücrelerde SF-1 koaktivatörüdür.
Endometriotik dokularda aromataz, 17βOHSD tip-2 ve Progesteron reseptörü B/ Progesteron reseptörü A oranlarında çeşitli anormallikler saptanmıştır. Odakların normal endometriumda bulunmayan aromataz aktivitesine sahip olduğu ve östradiolü inaktif östrojen formu olan estriole çeviren 17βOHSD-2 enzim aktivitesinin azaldığı gösterilmiştir. Östrojen, büyüme faktörleri ve metalloproteinazlarla birlikte endometriotik dokunun büyüme ve invazyonunu artırırken, prostaglandin ve sitokinler ağrı, inflamasyon ve infertiliteye aracılık ederler.
Şekil 2. PGE2-SF-1 üzerinden östradiol üretimi (10).
Bir aromataz aktivatörü olan SF-1 endometriotik dokulardan eksprese olurken, normal ötopik endometrial hücrelerde eksprese olmamaktadır. Coup-TF (chicken ovalbumin upstream transcription factor) ötopik endometrial stromal hücrelerde aromatazı inhibe ederken, endometriotik stromal hücrelerde aşırı artmış SF-1 ekspresyonu bu inhibisyonun üstesinden gelerek aromataz aktivitesini artırır.
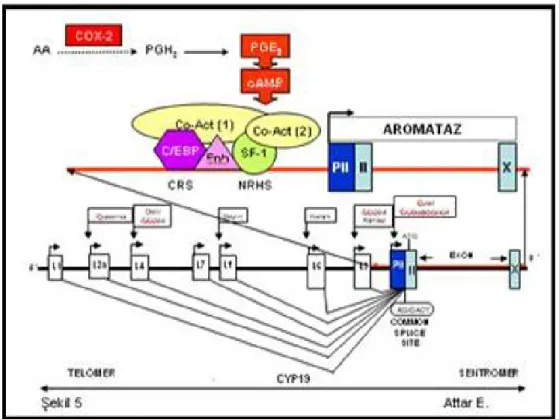
Şekil 3. Aromataz enziminin etkileşimi (10).
Aromataz ekspresyonu, endometriozisli hastaların peritoneal implantlarında ötopik endometrium örneklerine oranla katlarca yüksek bulunmuştur.
Aromataz mRNA ekspresyonu kırmızı implantlarda siyah implantlara göre ve endometriotik kist kapsüllerine göre daha fazla bulunmuştur. Endometriomalı hastaların %60'ında endometriotik dokulardan aromataz ekspresyonu gösterilmiştir (10). Endometriomalı hastalarda biyopsinin, aromataz ekspresyonu çevre ovarian dokulardan kontaminasyon olmadığından emin olunan alandan, deneyimli jinekolog tarafından alınması gerekir. Endometrioziste aromataz aktivitesi ciddi ve aktif hastalığı gösterirken hastalığın evresi ve cerrahi sonrası rekürrensle arasında bir ilişki gösterilmemiştir.
2.1.1.11.10. Demir ve Endometriozis
Demir, endometriotik gen ekspresyonunda önemli bir etkiye sahiptir. Endometriozis gelişen bölgelerdeki kan birikimi hastalığın oluşumu ve ilerlemesi için önemli bir faktördür. Odaklarda eritrositlerin hemolizi sonucu hemoglobinden yüksek konsantrasyonda açığa çıkan hem molekülü bulunmaktadır. Hem, merkezinde taşıdığı demir ile oksijene yüksek afinite ile bağlanabilen bir moleküldür. Serbest demir ve hem, inflamatuar reaksiyonları tetiklemektedir. Aslında inflamasyon hasarı önlemeye yönelik bir defans mekanizmasıdır. Bu moleküller intrasellüler reaktif oksijen radikalleri oluşturup daha sonra NF-kB, AP-1 ve SP-1 gibi transkripsiyon faktörlerini aktive ederler. Demirin patolojik derecede birikimi ROS oluşumuna ve oksidatif strese bağlı toksik etkilere neden olmaktadır. Bundan dolayı, demir bağımlı proteinlerin inhibisyonu ve radikallere bağlı DNA hasarının önlenmesi birer tedavi hedefidir (10).
Şekil 4. Demir birikimine bağlı NF-kB üzeründen periton hasarı (10).
Birçok deneysel modelde demir şelatörlerinin anti-kanserojen etki gösterdiği saptanmıştır. Deksrazoksan, deferoksamin, deferipron ve triapin gibi şelatörlerle ilgili çalışmalar klinik kullanım düzeyine kadar yükselmiştir. Deferipron kanser önleme ve tedavisinde etkili görünmektedir. Deferasiroks günde bir kez oral alınan yeni jenerasyon bir şelatördür ve transfüzyona bağlı aşırı demir birikimi tedavisinde ilk seçenek olmuştur. Sonuçta demir şelasyonu endometrioziste de yeni bir tedavi kapısı olarak umut vaat etmektedir. Demir endometriomalardaki kanamadan ve pelvik kaviteye retrograd mens ile ulaşan eritrositlerden kaynaklanabilir. Dolayısı ile bu iki basamak endometriozisin başlangıcı sayılabilir. Endometriozisin başlangıcı ve progresyonu odaklarda TLR (toll like receptor) aracılı inflamasyona sekonder oluşan hemolitik demir birikiminin bir sonucu olarak tartışılabilir.
2.1.1.11.11. Toll Like Receptor (TLR)
Sağlıklı endometriumda ve endometrioziste TLR-3 ve TLR-4 ekspresyonu olduğu bilinmektedir. TLR-4 ayrıca endometriotik dendritik hücrelerde, monosit ve makrofajlarda bulunmaktadır. TLR’nin Bakteriyel patojenlerin yok edilmesinde görev aldığı düşünülmektedir. Khan ve ark. Endometriozisli kadınlarda periton sıvısında LPS düzeylerinin kontrol olgulara göre anlamlı oranda daha yüksek olduğunu saptamışlardır.
2.1.1.11.12. Fibronektin
Endometrial implantların periton yüzeyine ataşmanı adezyon, invazyon, büyüme ve ekstraselüler matriks çevrim süreçlerini içerir. Fibronektin ve onun reseptörü olan integrinler hücre ataşmanında önemli elemanlardır. Endometriotik stromal hücrelerin tabanında gösterilen fonksiyonel fibronektin odakların implantasyonu sürecinde hücre ataşman ve adezyonunun potansiyel bir bölge olduğunu düşündürmektedir.
2.1.1.11.13. Okside LDL
Endometriozisli kadınlar kontrol olgulara göre artmış LDL düzeyleri gösterirler. Peritoneal sıvı özellikle LDL olmak üzere lipoproteinlerden zengindir. Bu LDL, makrofajdan zengin inflamatuar reaksiyonların okside lipid komponentini oluşturmaktadır. Okside LDL, periton mezotel hücrelerinden ve endometrial hücrelerden monosit kemotaktik protein salınımını uyarır. Endometriozisteki aktif makrofajlar lesitin benzeri okside LDL reseptörü (LOX-1) gibi temizleyici görev yapan reseptörleri içerirler. Okside LDL TLR-4 ve TLR-5 ve temizleyici reseptör heterodimerleri üzerinden inflamatuar sinyali tetikler.
2.1.2. Epidemiyoloji
Endometriozisin genel populasyondaki kesin oranı bilinmemektedir. Endometriozis jinekolojik sebeple opere edilen hastaların %1'inde, sterilizasyon uygulanan hastaların %6-43'ünde, pelvik ağrı nedeniyle laparoskopi yapılan hastaların %12-32'sinde, infertilite nedeniyle laparoskopi yapılan hastaların %21- 48'inde görülür. Endometriozis kronik pelvik ağrı ve dismenore nedeniyle laparoskopi olan genç kızların %50'sinde tespit edilmektedir.
Yaş, ırk ve sosyoekonomik durumun endometriozis prevalansına olan etkisi hala tartışmalıdır. Teşhiste ortalama yaş 25-35 arasındadır. Endometriozis nadiren postmenopozal kadınlarda tespit edilir. Sosyoekonomik seviyesi yüksek olan kadınlarda endometriozisin daha sık görülmesi bu kadınlarda gebeliği ertelediklerinden dolayı olduğu düşünülmektedir. Sosyoekonomik düzeyi aynı olan siyah ve beyaz kadınlarda endometriozis riski aynıdır.
Endometriozise ailesel yatkınlık olabileceği ihtimali tartışılmaktadır. Bir kadında endometriozis varsa birinci derece kadın akrabasında endometriozis olma ihtimali %7'dir (11).
2.1.3. Patoloji
Endometriozis en sık over, posterior cul de sac, uterus, fallop tüpü, sigmoid kolon, appendiks ve round ligamanda izlenir. Daha az sıklıkla tutulum olabilen diğer bölgeler; vajina, serviks ve rektovajinal septumdur. Bunlar posterior cul de sac'a ekilen lezyonların invazyonu sonucu oluşur. İnguinal kanal, abdominal veya perineal skarlarda, ureter, mesane, böbrek, akciğer, karaciğer, diafram, vertebra ve ekstremitelerde de ender olarak görülebilir.
2.1.3.1. Makroskopik Görünüş
Endometriotik implantların değişik görünümleri vardır. Over ve periton yüzeyindeki lezyonlar genellikle kırmızı makül veya nodül şeklinde, normal endometrium dokusuna benzer şekilde görülebilir. Bu implanların büyüklüğü birkaç milimetre ile bir kaç santimetre arasında değişebilmektedir. Hemosiderin birikimi sarı, kahverengi, siyah renk değişikliğine sebep olabilir.
Şekil 5. Peritondaki Endometriotik İmplantlar (41)
Şekil 6. Overdeki Endometriotik İmplantlar (42)
Pigmentsiz lezyonlar; periton üzerinde beyaz opasiteler, şeffaf bül veya pembe polipoid implant şeklinde görülebilir. Etraf peritonda, dokuların retraksiyonu sonucu skar ve periton cepleri oluşabilir.
Endometriozis derin infiltratif hastalık şeklinde de görülebilir. Posterior cul de sac, pelvik yan duvarlar, posterior broad ligaman ve overde tümöre benzeyen kitlesel lezyonlar, invazyon ve yaygın fibrozis sonucu oluşabilir. Retroperitoneal alana derin bir şekilde ilerleyebilir hatta üreteri de içine alabilir. Cul de sac'taki lezyonlar rektovajinal septuma ilerleyebilir. Rektosigmoid kolon ve ince barsak bu alanlara yapışabilir. Over yüzeyindeki endometriotik odak fibröz bir kapsül kaplı kan ve sıvı içeren kist halini alabilir. Bu endometriotik kistler (endometrioma) birkaç milimetre ile 10 santimetreye kadar büyüyebilir. Menstrüasyon ile olan kanama kistin koyu kırmızı veya mavimsi hemorajik renk değişikliğine sebep olur. Kan pigmentinin zamanla azalması sonucu kalın, katran kıvamında içerik oluşur ve bu nedenle çikolata kisti denir.
Bazen içerik sarı saman rengi veya şeffaf sıvıya dönüşebilir. Bu kistler ile pelvik yan duvar veya fallop tüpü arasında ince veya yoğun fibroid adezyonlar sıklıkla oluşur ve kistin görülmesini engelleyebilir.
2.1.3.1.1. Endometrioma
Endometriumun glandüler doku ve stromasının uterus dışında yer alması olarak tanımlanan endometriozis genel kadın populasyonunun %5-15, infertilite nedeni ile araştırılan kadınların %40’nı oluşturan çok yaygın bir hastalıktır (43). Pelvik organlar içinde endometriozisten en fazla etkilenen organ overdir. Ovarian endometriomalar endometriozisli hastaların %14-44'ünde kan ve hemosiderinle dolu ovarian kitlelere denir.
Tipik endometriomaların oluşumu;
1-Ovarian yüzey epiteli veya implantların over korteksi boyunca inversiyonu ve invajinasyonu
2-Ovarian endometriotik implantların fonksiyonel over kistlerini içerecek şekilde ilerlemesi
3-Ovarian çölomik epitelin metaplazisi 4-Folikülogenesis'e bağlı oluşabilir (10).
Endometriomaların %90'ının oluşumundaki ilk ivmelenme, menstrüel dokunun over yüzeyine implante olması ve daha sonra peritona tutunma hipotezidir (10).
Büyük endometriomaların luteal veya foliküler over kistlerine benzer histolojik karakteristikler göstermesi folikülogenezisin rolünü destekler (10).
Endometriomalar ovarian stimulusa yetersiz yanıt, azalmış fertilite ve implantasyon oranları infertilite ile ilişkilendirilmiştir. Klinik görünüm ve histolojik inceleme için kistler 2 ana tipte sınıflandırılır (43).
1.Çikolata renginde sıvı ile dolu küçük yüzeyel kistler (primer endometrioma, tip 1)
2.Foliküler veya luteal ovarian kistler içeren endometriomalar (sekonder endometrioma, tip 2)
Sekonder endometriomalar (tip 2) başka bir sınıflandırmada 3 subtipe bölünmüş (43).
-Tip 2a kistler ; kapsülünden kolayca ayrılabilen büyük endometriomalar -Tip 2b kistler ; yoğun fonksiyonel kist özellikleri içeren endometriomalar -Tip 2c kistler ; tip 2b kistlere ilaveten yaygın yüzeyel endometrial implantın eşlik ettiği endometriomalar
Endometriomalar yerleştiği overin fonksiyonunu ve oosit kalitesini azaltabilir. Endometriozisli hastalarda saptanan endometriomaların çapına, semptomlarına, fertilite isteği olup-olmamasına göre cerrahi tedavi planlanır. 4 cm ve üzerindeki endometriomalara laparoskopik kistektomi yapılırken, 3 cm ve altındaki endometriomalara laparoskopik kist aspirasyonu ve lazer koagulasyon uygulanır. Laparoskopik kistektomi sonrası iyileşme oranları daha fazla ve nüks etme olasılığı daha azalmıştır. Tip 2b ve tip 2c endometriotik kistler laparoskopik olarak çıkarılmaya
çalışılırken over rezervine zarar verilebilir. Biz bu çalışmada 20 endometriomalı hastanın 16 tanesine laparoskopi ile kistektomi, 4 tanesine laparotomi ile kistektomi yaptık.
2.1.3.2. Mikroskopik Görünüş
Endometriozis histomorfolojik olarak normal endometriuma benzer. Endometriotik implantların dört ana komponenti endometrial bez, endometrial stroma, fibrozis ve hemorajidir (Şekil 7).
Şekil 7. Endometriozisin histomorfolojik ve radyolojik görünümü (İnönü Üniversitesi Kadın Hastalıkları ve Doğum ABD)
Her bir içeriğin bulunma oranı değişkendir ve lezyonun yaşına ve bulunduğu yere
bağlıdır. Örnek alınan lezyonlarda endometriotik dokunun bulunabilmesi yeterli doku örneğinin alınmasına ve örnekten sık kesit alınmasını gerektirir.
Ektopik implantlarda bulunan endometriotik bezlerin düzgün şekil ve büyüklüğü yoktur. Bezler mitotik figürler içeren normal siklik değişiklikler gösterebildiği gibi estrojen ile yalancı çok katlı epitel oluşumu veya progesteron etkisi ile vakuol ve intraluminal sekresyon yapabilir. Bezler endojen ve ekzojen östrojene farklı tepkiler verebilir. Bu, steroid hormon reseptörünün fonksiyon ve içeriğindeki farklılığını veya normal bez-stroma ilişkisinin bozulmasına bağlı olabilir. Bezler tepkisel olduğunda, epitel incelir ve menstrüasyon zamanında kanama olur.
Ötopik ve ektopik endometrial stroma dokusu benzerdir. İmplantlarda, normal endometriumda spiral arteriollere benzeyen küçük arterioller bulunur. İnterstisiyel hemoraji ile birlikte kan ürünleri ve hemosiderin yüklü makrofajları sık görülür.
Eskimiş endometriotik implantlarda fibrozis oluşabilir. Bu histolojik bulgu sadece fibroblast çoğalması ve hemosiderin pigment depolanması olan endometrioma iç çeperinde sıklıkla izlenir.
2.1.4. Semptom
Endometriozis hastalığının semptomu ve şiddeti hastalığın yaygınlığına, bulunduğu organa ve menstrüasyon gününe göre değişir. Endometriozisli kadınların en sık şikayeti pelvik ağrıdır, bu menstrüasyondan hemen önce artar ve adetin sonunda azalır. Diğer semptomlar ise adet sancısı, disparoni, anormal uterin kanama ve infertilitedir.
Endometriozis, kronik pelvik ağrısı olan hastaların üçte birinde görülür. Ağrı kramp tarzında, künt veya keskin olarak tarif edilir ve menstrüasyon döneminde artar. Ağrı tek yada iki taraflı olabilir ve birçok hasta rektal basınç hissi veya bel ağrısından yakınır. Endometriomanın rüptürü sonucu oluşan kanamadan dolayı akut karın ağrısı oluşabilir.
Dismenore, disparoniye oranla daha sıktır. Hastalığın yaygınlığı ile ağrı arasında ilişki vardır. Endometriotik implantın morfolojik görünüşü ile ağrı birbirinden bağımsızdır. Cul de sac, uterosakral ligaman, rektovajinal septum ve vajende invazif endometriotik nodülleri olan hastalarda disparoni sıktır.
Oligomenore, polimenore, adet periodunun ortasında yada menstrüasyondan hemen önce kanama gibi anormal uterin kanamalar endometriozisli kadınların üçte birinde görülür. Anormal kanamalar endometriozis ile ilişkili diğer durumlardan örneğin; oligoanovulasyon, luteinize unrüptüre folikül, luteal faz defekti veya fibroid gibi patolojilerden kaynaklabilir.
Gastrointestinal sistem veya üriner sistemde ve pelvis dışında bulunan endometriozis, bulunduğu yere göre semptom verir. Mesane tutulumunda sık idrara çıkma ve ani idrara yetişme hissi olur. Mukoza invazyonu varsa hematüri görülür. Üreteral veya nadir görülen böbrek endometriozisi yan ağrısı veya görünür hematüriye neden olur. Gastrointestinal sistem ile alakalı semptomlar ise; ishal, rektal kanama, konstipasyon ve diskezidir. Tüm semptomlar adet döneminde artabilir. Ekstrapelvik endometriozis vaka raporları çok sayıda mevcuttur. Pulmoner endometriozis adet döneminde oluşan hemoptizi ve dispne ile seyreder. Kutanöz endometroziste ise adet döneminde oluşan hassasiyet, şişlik ve kanama vardır.
İnfertil kadınların %40’ında endometriozis vardır ve endometriozisi olan kadınların %30-35’i infertildir. Endometriozis ve infertilite arasındaki ilişki iyi bilinse de patogenezi henüz tam açıklığa kavuşmamıştır.
Endometriozis ve endometrioma adezyon oluşturarak pelvik anatomiyi ve oositin tuba tarafından tutulumunu bozar. Daha hafif formlarda oluşan infertiliteyi açıklayacak birkaç teori ileri sürülmüştür .
Suçlanan mediatörler ve infertilitenin oluşum mekanizması 1- Anatomik bozukluk ve tubanın tıkanıklığı
2- Anovulasyon, luteal faz bozukluğu ve hormonal bozukluklar 3- Galaktore veya hiperprolaktinemi
4- Periton sıvısındaki sitokinler 5- Otoimmünite
7- Periton sıvısındaki prostoglandinler
8- Embriyonun implantasyon defekti ve spontan abortus 2.1.5. Teşhis
Hastalık prepubertal kızlarda ve hormon tedavisi almayan postmenapozal kadınlarda nadiren tanı alır. Teşhis genellikle 3. veya 4. dekatta konur. Endometriozisin klasik semptomlarından olan pelvik ağrı, dismenore, disparoni, anormal menstrüel kanama ve infertilite şikayeti olan hastalarda düşünülmelidir. Adneksiyel kitle ve infertilitesi olan hastalarda da endometriozis düşünülmelidir. Ayrıca endometriozis olan birçok hasta asemptomatik de olabilir. Hastaların fizik muayene bulguları hastalığın lokalizasyon ve evresine bağlı olarak değişebilir .
2.1.5.1. Klinik bulgular
1- Cul de sac veya uterosakral ligamanda lokalize hassasiyet
2- Cul de sac veya uterosakral ligamanda veya rektovajinal septumda palpe edilen hassas nodüller
3- Uterusun hareketi ile ağrı oluşması 4- Hassas, büyümüş adneksiyel kitle 5- Uterus veya adneksin fiksasyonu
Pelvik muayenede net bir bulgu gözlenemeyebilir. En sık görülen bulgu ise posterior fornikste palpasyon ile hassasiyettir. Uterosakral nodüller en iyi rektovajinal muayene ile tespit edilir. Muayenede endometriozise bağlı nodüller, endometriomaya bağlı büyümüş overler veya uterusun cul de sac'a yapışıklığı tespit edilebilir.
Endometriozisin tanısında altın standart laparoskopi ile lezyonun gözle görülmesidir. Genellikle laparoskopi hem en önemli tanı, hem de en önemli tedavi yöntemidir. Opere edilen bir hastada endometriozisin tüm morfolojik şekilleri gözlenebilir. Laparaskopide implantları içeren tüm yapılar tespit edilmelidir. Cul de sac'ı net değerlendirmek için periton sıvısı aspirasyonu gerekebilir. Over ve fossa overikanın değerlendirilmesi için mevcut adezyonlar açılmalıdır. Overin pelvik yan duvara yapışık olması halinde burda endometriozis varlığı düşünülmelidir. Cerrahın lezyonu görerek koyduğu teşhis periton biyopsiden daha değerlidir. Fakat lezyon hakkında şüphe varsa biyopsi alınmalı ve patolojik incelemesi yapılmalıdır.
Ultrason ile ovaryen endometrioma teşhis edilebilir, fakat peritondaki implantların teşhisinde ultrasonun faydası yoktur. Endometriozis, morfolojik olarak genellikle iki boyutlu olduğu için MRG, BT veya ultrason genellikle negatif sonuç verir. Fakat obez veya muayenesi zor olan, veya uterusa bağlı ağrısı olduğu düşünülen hastalarda teşhis amaçlı bu tetkikler kullanılabilir.
İntestinal endometriozis nadir olarak seromüsküler tabakaya ilerleyip mukozayı infiltre ettiğinden baryumlu barsak filmleri, kolonoskopi çok ileri evre vakalar dışında
teşhiste faydalı değildir. Rektum ön duvarının cul de sac'ı kapattığı ileri evre hastalarda MR veya rektal ultrason istenebilir.
Barsaktakine benzer olarak mesane serozasından başlayan lezyon nadiren mukozaya ilerler, bu nedenle sistoskopinin fazla yardımı olmaz. Bir veya iki üreterin konstrüksiyonundan şüphelenilen vakalarda görüntüleme yöntemi faydalı olabilir. İleri evre vakalarda böbrek fonksiyon bozukluğu görülebilir.
2.1.6. Sınıflandırma
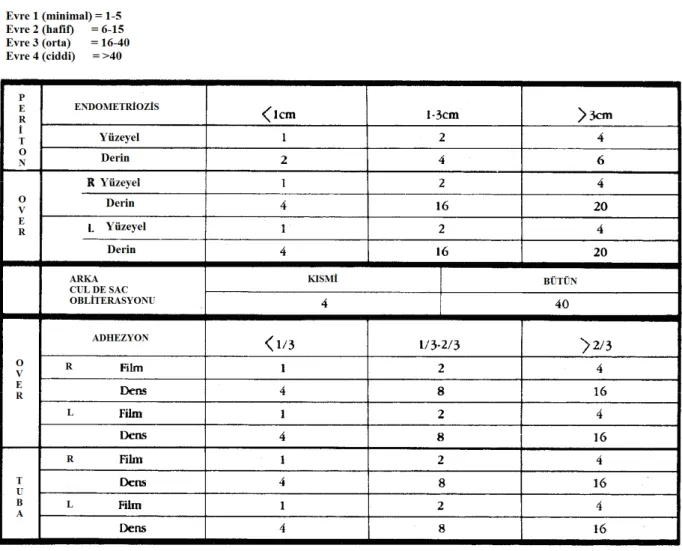
Endometriozis hastalığında birçok sınıflandırma geliştirilmiştir. En sık kullanılan sistem 1979 yılında Amerikan Üreme Sağlığı Birliğinin (ASRM) yayınladığıdır. Bu sistem 1985 ve 1997’de tekrar düzenlenmiştir. Bu sistemde endometriotik implantın büyüklüğü, yeri ve adezyonla ilişkisine göre puan verilir. Yeni ASRM sınıflandırılması infertilite için yapılmıştır ve implantın morfolojik görünüşünü de içerir.
Endometriozis minimal, hafif, orta ve ciddi olarak sınıflandırılır:
Minimal form (Evre I) ; hafif hastalık peritonun 5cm² sinden küçük alanda ve over üzerinde minimal implant olmasıdır. Adezyon çok az veya hiç yoktur.
Hafif formda (Evre II) ; yüzeyel veya derin invazyon gösteren birçok implant vardır.
Orta formda (Evre III) ; birçok yüzeyel ve derin implant vardır ve over endometriomalarını içerir. İnce veya yoğun adezyonlar genellikle mevcuttur.
Ciddi formda (Evre IV) ; derin peritoneal implant,douglas oblitere ve bilateral endometriomalar, yoğun adezyonlar içerir.
Fakat ağrı veya infertilite semptomları ile korele herhangi bir evreleme sistemi henüz yoktur (13).
Şekil 8. ASRM (American Society for Reproductive Medicine ) tarafından yenilenmiş endometriozis sınıflaması (44)
Şekil 9. ASRM (American Society for Reproductive Medicine) tarafından yenilenmiş endometriozis sınıflaması (44).
2.1.7. Tedavi
Endometriozis tedavisinde hedef semptoma yönelik ağrının giderilmesi, fertilitenin sağlanması, korunması ve endometriotik odaklardaki tekrarlama ya da ilerlemenin geciktirilmesi veya önlenmesidir. Genel olarak endometriozisin medikal, konservatif cerrahi tedavilerine rağmen hastalığın yıllık rekürrensi %5-10 olup olguların yaklaşık %50’sinde sorun tekrar karşımıza çıkabilmektedir. Tedavinin hastalığın gerçek aktivitesini ne ölçüde etkilediği tartışmalıdır. Diğer yandan endometriozis implantları ile normal endometrium arasında mikroskopi, reseptörler, endokrin cevap açısından ancak %50-60 benzerliğin olduğu ve tedavi ile implantlardaki gelişim suprese olsa bile her zaman atrofinin sağlanamayacağı bilinmektedir. Endometriotik odağın davranış şeklindeki farklılıklar da olguların tedaviye yanıtlarını değerlendirmede yanlışlıklara neden olabilmektedir.
2.1.7.1. Medikal Tedavi
Medikal tedaviyi tek başına infertiliteyi düzeltmek için kullanmak uygun değildir. Medikal tedavinin tek geçerli endikasyonu geçici olarak ağrının giderilmesidir. Geleneksel medikal tedaviler yalancı gebelik veya yalancı menapoz durumu sağlayarak geçici amenore oluşturur.
Daha önceki çalışmalarda nulliparöz kadınlarda endometriozisin sıklığının fazla olmasından dolayı gebeliğin hastalığın oluşmasını engellediği düşünülmüştür. İlk geliştirildiği yıllara göre oral kontraseptiflerin hormon dozu azaltıldığı halde bazı hastalarda semptomları belirgin olarak azaltır. Bütün kadınları tüm zamanlarda etkileyerek semptomlarını azaltacak bir doz şeması vermek zordur, fakat genel hormon kullanım şeması izlenmelidir. Monofazik düşük doz (<50µg östrojen) hormon seviyesi sabit olan haplar, değişik hormon seviyesi içerenler gibi kırılma kanaması yapmadan semptomları baskılarlar. 20µg dan az hormon içeren haplar kırılma kanamasına sebep olabilirler. 3-6 aylık sürekli tedavi kesilme kanaması yapmadığı için aylık kullanıma tercih edilmelidir. Bu şekilde oluşturulan amenore ile dismenore de azaltılır. Yeni geliştirilen deriye yapıştırılan kontraseptif hormonlar da bu amaç için kullanılabilir.
Medroksiprogesteron asetat 30mg, 90 gün kullanımı gebelikteki yüksek progesteron seviyesini taklit ederek ağrıyı azaltır ve nodülarite ve hassasiyeti azaltır. 6 ay, 30mg noretinodrel kullanımı da ağrının azalmasını sağlar.
Semptomatik postmenopozal endometriozis premenopozal endometriozise göre çok az görülmektedir. Östrojen azalması semptomların azalmasına sebep olmaktadır. Bu nedenle overden östrojen üretimini azaltan tedaviler geliştirilmiştir. Danazol, GnRH agonisti bu amaçla kullanılmaktadır (11).
2.1.7.2. Cerrahi Tedavi
2.1.7.2.1. Ablatif Cerrahi Tedavi
Bazı cerrahi tedavi yöntemleri geniş doku disseksiyonu gerektirmeden hızlı şekilde uygulanabilir. Bunlar lazer vaporizasyonu ile termal ablasyon, monopolar veya bipolar elektrokoagülasyon, argon ışın koagülasyonu, endokoagülasyon, ve harmonik skalpel koagülasyon yöntemleridir. Bu enerji sistemlerinin doku derinliğine etkileri sınırlı olduğu için eksik veya yetersiz tedaviye sebep olabilmesi bu yöntemlerin kullanımı konusunda soru işareti oluşturur. Termal ablasyon tekniklerinin herbirinde cerrahideki nihai kararı cerrah vermektedir. Ne kadar doku yakıldığı, patolojinin invazyon derinliği tama yakın harabiyet verilip verilmediği cerrahın kararıdır (11).
2.1.7.2.2. Cerrahi Olarak Endometriozis Lezyonun Çıkarılması:
Yüzeyel veya derin endometriozisin çıkarılması ile hastalığın tam tedavi edildiği düşünülür. Eksizyon bıçak, elektrocerrahi, CO2 veya fiber lazer veya harmonik skalpel bu amaçla kullanılabilir. Endometrioma kistleri en iyi kistektomi ile tedavi edilir, kistin drenajı ve kist duvarının yakılması tekrar endometrioma gelişmesine sebep olabilir (11).