Obstruktif uyku apne sendromu olan hastalarda protein oksidasyon ürünlerinin araştırılması
Tam metin
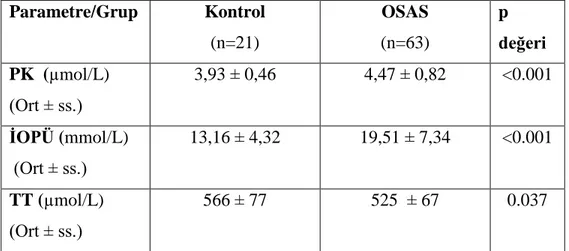
Şekil


Outline
Benzer Belgeler
In the present study, the observed prevalence rate of HAIs detected by WPS was similar to the prevalence rate calculated by the Rhame and Sudderth formula using the data of PIS..
İstanbul'daki Ingiliz Büyükelçisi Slr H.Layard, Sultan Abdülhamid'i köşeye sıkıştırarak BabIâli'nin Osmanlı, Ermenileri leyhinde reformlar yapmasını istedi, aksi
In some forms of respiratory failure, noninva- sive ventilation has proved to be as effective as en- dotracheal intubation to deliver tidal volume and improve gas exchange. Despite
Diğer çalışmalardan farklı olarak çalışmamızda Polisomnografi (PSG) ile tanısı konulan hafif, orta, ağır OUAS’lı hastalarda ve hasta yakınlarında, tedavi
Yap›lan Mann-Whitney U testi sonuçlar›na göre, tüm ölçek için E¤itim Fakültesinde (SO=92.17) görev yapmakta olan ö¤retim eleman- lar›n›n s›ra
Yine istatistiksel olarak anlamlı bulunmamakla birlikte doktorasını tamamlamıú akademisyenlerin doktorasını tamamlamamıú akademisyenlere göre yayınlarını yurt içi ve
Bu çalışmada süt olum dönemindeki Karabuğday bitkisinin (Fagopyrum esculentum Moench.) bazı agronomik özellikleri belirlenmiş, kimyasal ve biyolojik silaj
Araştırmanın her iki yılında da bitki boyu, tabla çapı, bin tohum ağırlığı, kabuk oranı, tohum verimi, ham yağ oranı ve ham yağ verimi bakımından kullanılan