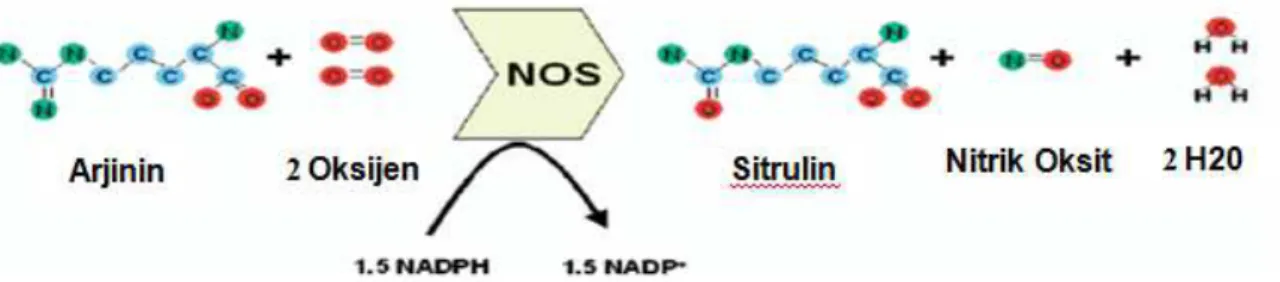
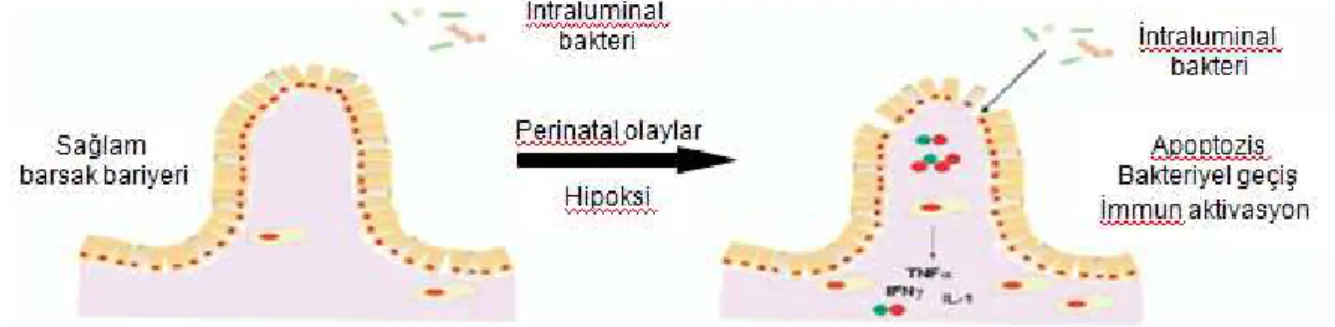
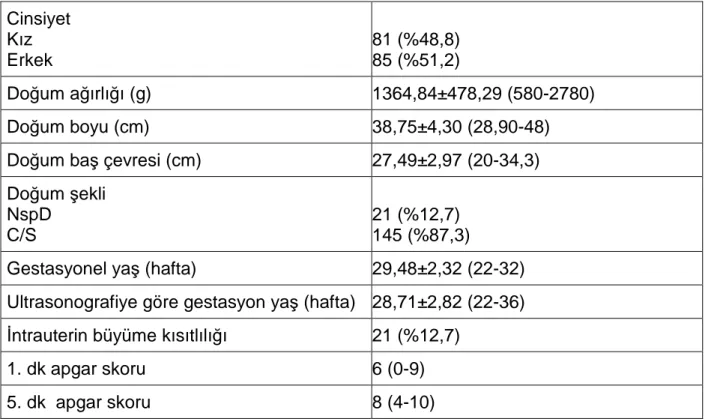
Nekrotizan enterokolit patogenezinde değişik mediyatörlerin gen polimorfizminin rolü
Tam metin
Şekil



Benzer Belgeler
Secondly, Structural Equation Modelling was applied for the purpose of evaluating the Managerial Perception on Competency Mapping (MPCM), Competency Mapping in Career
Design Thinking is an approach where the designers use ideation process to solve complex problems pertained to designing and design engineering.Design Thinking refers to both
,兩組實驗組皆以盲腸結紮及穿刺手術誘發敗血症後,一組由尾靜脈 注射每公斤體重 0.75 克的 GLN (SG 組 ) ,另一組注射等量生理食鹽 水作對照 (SS 組 ) ,於誘發敗血症後
雙和醫院單孔達文西機器手臂,可一洞完成「子宮肌瘤、卵巢腫瘤、內膜癌」 等手術治療
雙和醫院器捐牆揭幕,謝謝您的大愛 雙和醫院為了推動器官捐贈的理念,並配合 6 週年院慶,於 6 月 14
雙和醫院圖書室榮獲「101 年度 NDDS 醫院圖書館類別服務件數」第 2 名 中華圖書資訊館際合作協會 2013 年 5 月 23 日假國立中山大學舉 辦第
38 度以上之高燒會持續 3-4 天 偶會發高燒 嚴重的全身性肌肉酸痛、關節疼痛 輕微的全身性肌肉酸痛、關節疼痛 大多數的人會有發燒惡寒
The current study adopts a quantitative methodology that aims to explore the English language self- efficacy and global anxiety levels, their relationship and the role of