ORTAÖĞRETİM KİMYA VE FİZİK ÖĞRETMENLERİNİN KOROZYON HAKKINDAKİ BİLGİ DÜZEYLERİNİN ARAŞTIRILMASI
Evren DERİN
YÜKSEK LİSANS TEZ ÖNERİSİ
ORTAÖĞRETİM FEN VE MATEMATİK ALANLAR EĞİTİMİ ANA BİLİM DALI
GAZİ ÜNİVERSİTESİ
EĞİTİM BİLİMLERİ ENSTİTÜSÜ
i
TELİF HAKKI ve TEZ FOTOKOPİSİ İZİN FORMU
Bu tezin tüm hakları saklıdır. Kaynak göstermek koşuluyla tezin teslim tarihinden sonra tezden fotokopi çekilebilir.
YAZARIN
Adı : Evren Soyadı : DERİN
Bölümü : Ortaöğretim Fen ve Matematik Alanlar Eğitimi ABD İmza :
Teslim Tarihi :
TEZİN
Türkçe Adı : Ortaöğretim Kimya ve Fizik Öğretmenlerinin Korozyon Hakkındaki Bilgi Düzeylerinin
Araştırılması
İngilizce Adı : The Determination of The Knowledge Level of The Secondary Education Chemistry and Physics Teachers About Corrosion Phenomenon
ii
ETİK İLKELERE UYGUNLUK BEYANI
Tez yazma sürecinde bilimsel ve etik ilkelere uyduğumu, yararlandığım tüm kaynak gösterme ilkelerine uygun olarak kaynakçada belirttiğim ve bu bölümler dışındaki tüm ifadelerin şahsıma ait olduğunu beyan ederim.
Yazar Adı Soyadı : Evren DERİN İmza :
iii
JÜRİ ONAY SAYFASI
Evren DERİN tarafından hazırlanan "ORTAÖĞRETİM KİMYA VE FİZİK ÖĞRETMENLERİNİN KOROZYON HAKKINDAKİ BİLGİ DÜZEYLERİNİN ARAŞTIRILMASI " adlı tez çalışması aşağıdaki jüri tarafından oy birliği ile Gazi Üniversitesi Ortaöğretim Fen ve Matematik Alanlar Eğitimi Ana Bilim Dalı’nda Yüksek Lisans tezi olarak kabul edilmiştir.
Danışman : Prof. Dr. Mehmet Levent AKSU ……… Ortaöğretim Fen ve Matematik Alanlar Eğitimi ABD, Gazi Üniversitesi
Başkan : Prof.Dr.Orhan ATAKOL ………
Kimya Anabilim Dalı, Ankara Üniversitesi
Üye : Prof.Dr. Alev Çetin DOĞAN ………
Ortaöğretim Fen ve Matematik Alanlar Eğitimi ABD, Gazi Üniversitesi
Tez Savunma Tarihi : 01/03/2016
Bu tezin Ortaöğretim Fen ve Matematik Alanlar Eğitimi Ana Bilim Dalı’nda Yüksek Lisans tezi olması için şartları yerine getirdiğini onaylıyorum.
Prof. Dr. Tahir ATICI
iv
ORTAÖĞRETİM KİMYA VE FİZİK ÖĞRETMENLERİNİN
KOROZYON HAKKINDAKİ BİLGİ DÜZEYLERİNİN
ARAŞTIRILMASI
(Yüksek Lisans Tezi)
Evren DERİN
GAZİ ÜNİVERSİTESİ
EĞİTİM BİLİMLERİ ENSİTÜSÜ
Mart 2016
ÖZ
Bu çalışmanın amacı, ortaöğretim kimya ve fizik öğretmenlerinin korozyon eğitimi hakkındaki bilgi düzeylerinin ölçülmesi, korozyon olayının neden olduğu olaylar ve sonuçlarına ilişkin farkındalığını değerlendirmek, yanlış kavramaları tespit etmek,çözüm yolları önermek ve elde edilen bilgiler ışığında ortaöğretim müfredatına korozyon eğitimin konulmasını önermektir. Yapılan araştırma ile korozyon konusunda kimya ve fizik öğretmenlerin korozyon olayın neden olduğu olaylar ve sonuçlarına ilişkin farkındalığını ölçebilmek için öncelikle 20 sorudan oluşan bir test uygulanmıştır. Daha sonra öğretmenlerin korozyon konusu hakkındaki bilgi düzeylerinin arttırabilinmesi için 40 sayfalık slayt bir sunum yapılmıştır. Sunum sonunda 20 soruluk bir test daha ve öğretmenlerin korozyon eğitimi hakkındaki düşüncelerini değerlendiren 4 sorudan oluşan bir anket geliştirilmiştir. Araştırma 2014-2015 öğretim yılında Eskişehir ili Tepebaşı ilçesindeki 2 okulda farklı sınıf seviyelerinde görev yapan, 4’ü Kimya öğretmeni ve 4’ü Fizik öğretmeni olmak üzere toplam 8 öğretmen üzerinde uygulanmıştır. Bulgular genel
v
olarak öğretmenlerin korozyon konusunda yeterli bilgiye sahip olmadıkları yönündedir. Korozyon sebep olduğu maddi ve manevi zararlar göz önüne alındığında öğretmenlerin korozyon hakkında daha da bilinçlendirilip eğitilmesi gerekmektedir. Şu anki müfredatta 9.sınıf ve 11.sınıfta yüzeysel olarak değinilirken korozyon konusu daha kapsamlı ele alınarak bilgi düzeylerinin arttırılması gerektiği görülmektedir.
Anahtar Kelimeler : Korozyon, Ortaöğretim. Sayfa Adedi : 67
vi
THE DETERMINATION OF THE KNOWLEDGE LEVEL OF THE
SECONDARY EDUCATION CHEMISTRY AND PHYSICS
TEACHERS ABOUT CORROSION PHENOMENON
(Master thesis )
Evren DERİN
GAZİ UNIVERSITY
Educational Science Institute
March 2016
ABSTRACT
The purpose of this thesis was to determine the knowledge levels and the elementary education physics and chemistry teachers about the corrosion phenomenon, evaluate their awareness of its consequences , find out their misconceptions and make proposal of the inclusion of this topic in elementary education curriculum in the light of all these findings .The teachers were first subjected to a 20- question test in order to evaluate their awareness of the corrosion phenomenon. Then they were shown a 40- slide presentation in order to increase their knowledge level. At the end of this presentation they were subjected to the same 20 question survey and they were asked to answer 4 additıonal questions about their opinions on the inclusion of corrosion phenomena. The study was carried out upon four chemistry and four physics teachers working in two different schools located at Tepebaşı town of Eskişehir province. The findings revealed that the teachers did not sufficient knowledge about the corrosion phenomena . The teachers are to be educated about this very destructive phenomena .In the current curriculum the topic is superficially mentioned
at the 9th and 11th classes. A much more detailed approach is needed in order to increase
vii
Key words : Corrosion, Secondary Education .
Number of pages : 67
viii
İÇİNDEKİLER
ÖZ………...iv
ABSTRACT………vi
İÇİNDEKİLER………..…..viii
TABLOLAR LİSTESİ………..xii
ŞEKİLLER LİSTESİ………...xiii
SİMGELER ve KISALTMALAR………..xiv
BÖLÜM I……….1
GİRİŞ...1
1.1. Problem Durumu...1
1.2. Araştırmanın Amacı...3
1.3. Araştırmanın Önemi...4
1.4. Araştırmanın Sayıltılar...4
1.5. Araştırmanın Sınırlılıklar...4
1.6. Tanımlar...5
BÖLÜM II ...6
KAVRAMSAL ÇERÇEVE………6
2.1. Korozyon……...6
2.1.1. Korozyon ve Önemi...6
2.1.2. Paslanma...8
2.2. Elektrokimyasal Korozyon ……... ..…..9
ix
2.2.2. Katodik veya İndirgenme Tepkimesi...11
2.2.3. Elektrik Akımı İletimi ...11
2.3. Galvanik Seri...………...12
2.4. Korozotif Ortamlar...14
2.4.1. Atmosferik Korozyon……….………...15
2.4.2. Yer altı ve Sualtı Korozyonu………….…………...15
2.4.3. Deniz Suyu İçindeki Korozyon...16
2.5. Korozyon Çeşitleri...17
2.5.1. Homojen Dağılımlı Korozyon...17
2.5.2. Galvanik Korozyon...17
2.5.3. Çukurcuk Korozyonu...18
2.5.4. Aralık Korozyonu...19
2.5.5. Seçici Korozyon………...19
2.5.6. Tane Sınırları Korozyonu...20
2.5.7. Gerilim Korozyon...20
2.5.8. Erozyonlu Korozyon...21
2.6. Korozyon Etki Eden Faktörler...21
2.6.1. Coğrafi Yerleşim...21
2.6.2. Sıcaklık...22
2.6.3. Oksijen ve Yükseltgenler...23
2.6.4. Malzeme Seçimi………...24
2.6.5. Parça Boyutu...24
2.6.6. Sistem Dizaynı...24
2.7. Korozyondan Korunma Yöntemleri……...25
2.7.1. Katodik Koruma...26
2.7.2. Anodik Koruma...27
2.7.3.İnhibitör İle Koruma…………...28
2.7.4. Boya İle Koruma…………...29
2.7.5. Metalik Kaplama İle Koruma...30
2.8. Fen Okur Yazarlığı...30
x
2.10. Türkiye'de Korozyon Eğitimi ve Öğretimi………...32
2.10.1. Korozyonla İlgili Kurum ve Kuruluşlar……..…32
2.10.2. Türkiye Korozyon Derneği...33
2.10.3. Üniversitelerimizde Korozyon Eğitim Öğretimi.35
2.11. Yurtdışında Korozyon Eğitimi ve Öğretimi...36
BÖLÜM III………....38
YÖNTEM... ...38
3.1. Araştırmanın Modeli... ... ....38
3.2. Evren ve Örneklem………... .. ....38
3.3. Veri Toplama Yöntemi... ...38
3.4. Verilerin Analizi... ..39
BÖLÜM IV………...…...40
BULGULAR ve YORUM……...40
4.1. Bulgular………...40
4.2. Test ve Ölçeğin Güvenirliliğine Yönelik Bulgular...40
4.3. Korozyon Konusunda Fizik ve Kimya Branşlarına Göre
Başarıya İlişkin Bulgular ve Yorumlar………...40
4.4. Korozyon Konusu Anlatımı Sonrası Fizik ve Kimya
Branşlarına Göre Başarıya İlişkin Bulgular ve Yorum.42
4.5. Fizik ve Kimya Öğretmenlerinin Korozyon Eğitimi
Konusundaki Düşünce Bulguları ve Yorumları………44
BÖLÜM V...46
SONUÇLAR ve ÖNERİLER...46
5.1. Sonuç………...46
5.2. Öneriler...47
KAYNAKLAR... .48
EKLER………...51
Ek 1. Test 1………...52
Ek 2. Test 2...57
xi
Ek 3. Korozyon Konusu Bilgi Düzeylerinin Ölçülmesi ve
Müfredatına Önerilmesi İle İlgili Anket Soruları ....62
Ek 4. Ders Slaytları………...63
xii
TABLOLAR LİSTESİ
Tablo 1. Nerst Skalası………...13 Tablo 2. Ortaöğretim Fizik ve Kimya Öğretmenlerin Test-1
Sorularına Doğru Cevap Verme Oranları………...41
Tablo 3. Ortaöğretim Fizik ve Kimya Öğrenmenlerin test-2
Sorularına Doğru Cevap Verme Oranları……….……...43
Tablo 4. Ortaöğretim Fizik ve Kimya Öğretmenlerin Korozyon
xiii
ŞEKİLLER
Şekil 1. Metalin Çevre İle Etkileşimi………..……7
Şekil 2. Demirde Gerçekleşen Atmosfer Korozyonu……….……8
Şekil 3. Fe Metalinde Gerçekleşen Anot ve Katot Reaksiyonları……….9
Şekil 4. Daniel Pili………10
Şekil 5. Bir Korozyon Hücresinde Akım ve Elektronların Yönü………10
Şekil 6. Çelik Çubuk Üzerinde Korozyon Oluşumu……….………...11
Şekil 7. Metal ve Metal Alaşımların Galvanik Serisi………….………..14
Şekil 8. Toprak Korozyonu oluşum Mekanizması……….………...15
Şekil 9. Su altı Korozyonu……….………..….16
Şekil 10. Galvanik Korozyon Oluşum Ortamı………..………..….18
Şekil 11. Çukurcuk Korozyon Oluşum Mekanizması………..………...19
Şekil 12. Korozyon Hızı Üzerine Sıcaklığın Etkisi……….….22
Şekil 13. Havalandırma ve Oksitleyicilerin Korozyon Hızı Üzerine Etkisi……….23
Şekil 14. Korozyon Korumasında Tasarımın Önemi………..25
Şekil 15. Katodik Koruma………....26
xiv
SİMGELER VE KISALTMALAR
CCEC Kanada Korozyon Eğitim Konseyi
KOSGEB Küçük ve Orta Ölçekli İşletmelerin Geliştirme Başkanlığı GSMH Gayri Safi Milli Hasıla
1
BÖLÜM I
GİRİŞ
Bu bölümde araştırmaya ait problem durumu, problem cümlesi, alt problemler, araştırmanın amacı, önemi, varsayımları ve tanımlar yer almaktadır.
1.1.Problem Durumu
Metal ve alaşımlar endüstrinin vazgeçilmez temel maddeleridir. Korozyon, başta metal ve alaşımlar olmak üzere her cins malzemenin çeşitli etkilerle bozunmasıdır. Korozyon istenmeyen bir olaydır, ekonomik bakımdan her ülkenin büyük kayıplara uğramasına neden olur. Korozyon nedeniyle meydana gelen malzeme, enerji ve emek kaybı pek çok ülkenin gayri milli gelirinin yaklaşık %3-%5’i düzeyindedir. Ülkemiz için bu değerin %4.5 dolayında olduğu belirlenmiştir (Bennet, 1978; Çakır, 1993) . Bu değer önemli bir ekonomik kayıptır. Korozyona karşı bilinçli ve programlı yöntemler uygulanarak bu kayıpların ortalama %15-%20 oranında geri kazanabilineceği ilgili araştırmacılar tarafından belirtilmektedir (Uhlig, 1948;Üneri,1998) . Korozyon maddi kayıpların yanı sıra insan hayatı ve sağlığına zarar veren ve çevre kirliliğine neden olan bir olaydır.
Endüstri kuruluşlarının en önemli sorunlarından birisi olan korozyonla mücadelede her ülke kendine özgü olan ve önemliliğinde ön sıralarda bulunan endüstri alalardaki sorunlarla ilgilenen, araştırma geliştirme(ARGE) merkezleri gibi kuruluşlarda çalışmalarını yoğunlaştırmaktadırlar. Korozyon ve neden olduğu sonuçlar konusunda bilgi ve eğitim yetersizliğinin önlenmesi üniversiteler, araştırma merkezleri, endüstri ve yatırımcı kuruluşların yer aldığı organize bir çalışma ile gerçekleşebilir.
Korozyon bilimi çok karmaşık bir bilim dalıdır ve diğer birçok bilim dallarıyla ilişkilidir. Sorunların belirlenmesi ve bunların çözümü için elektrokimya, termodinamik, elektrokimyasal kinetik, elektrokimyasal, termodinamik, yüzey fiziği ve kimyası,
2
mekanik, metalurji ve malzeme bilgisi gibi çeşitli bilim dallarındaki bilgilerin bir arada kullanılması gerekir. Bu nedenle korozyon eğitimi veren öğretmenlerin bilgi ve düzeylerini yeterli düzeyde olması ve bu konunun orta öğretime katılması önem arz etmektedir.
Bilgi teknolojileri çağını yaşadığımız günümüzde ülkeler periyodik olarak eğitim sistemlerini gözden geçirmekte ve tartışmaya açmaktadırlar. Bu nedenle eğitimde değişik metodolojilerin kullanılmasına yönelik yapılan çalışmalar büyük önem taşımaktadır (Kayalı, H., Ürek, Çavaş & Tarman, 2000). Yapılan bir çok araştırmada halen yürürlükte olan ortaöğretim müfredat programının eksiklerine değinilmiş ve öneriler getirilmiştir (Wright vd., 1998; Kayalı vd., 2000; Özmen, H., Dumanoğlu & Ayas, (2000); Ünal, 1998). Ülkemizde bugüne kadar yapılan çalışmalarda ortaöğretim programında korozyon konusunun anlatılmasına yönelik oldukça bir çalışmaya rastlanmamıştır. Yabancı kaynaklı ders kitapları incelendiğinde ortaöğretim programında korozyon ve korozyondan korunma konusunun anlatıldığı saptanmıştır. (Christen, 1970; Botsch, W. Höfling, & Mauch, J. 1977; Anmedick & Kander, 1998; Büttner, 2001; Tremel, 1995)
Korozyon: genel olarak malzemelerin, özel olarak metallerin ve alaşımların çevrenin çeşitli etkileriyle kimyasal ve elektrokimyasal değişme ya da fiziksel çözünme sonucu aşınmaları ile ilgili olmasına rağmen endüstride kullanılan kauçuk, plastik, emaye ve bileşik malzemelerde çevrenin etkileri ile aşınmaktadır (Üneri, 1998). Korozyonun neden olduğu doğrudan ve dolaylı kayıplar ülkemizde de ileri boyutlardadır. Bu nedenle korozyon ve korozyondan korunmanın ilke ve uygulamaları hakkında bilgi vermek önem arz etmektedir. Korozyon konusunda bilgi edinmenin iki önemli nedeni vardır. Birincisi ekonomiktir. Buna bağlı olarak, bugüne kadar yapılan araştırmalar incelendiğinde korozyonun neden olduğu doğrudan ve dolaylı kayıpların giderilmesi için, korozyona karşı verilen savaş başarı ile sürdürülmüştür. İkinci neden ise günümüzde hızla artan çevre bilinci ve buna bağlı olarak ta çevreyi korumada etkili hale gelen yaklaşımlardır. Çevremizi kirleten gaz emisyonları ve atıkların miktarını azaltarak çevreyi korumak ve korozyona karşı verilen savaşın önemini kavramaktır. Kimya eğitiminde korozyon konusunun yeri ve önemi hakkında birçok çalışma yapılmıştır. Şahin ve Bilgiç (1999) tarafından yapılan çalışmada, son teknolojik gelişmeler de korozyona daha az uğrayan metaller geliştirilmesine rağmen ekonomik maliyeti sebebi ile metallerin her yerde kullanılmadığını ve korozyona karşı korunması gerektiğini ortaya çıkarmıştır. Yapılan diğer bir araştırmada daha çok korozyona normal metallerin uğradığı ve sonuçta bu metalleri korozyondan korumak için önlemler alındığı vurgulanmıştır. Örneğin,
3
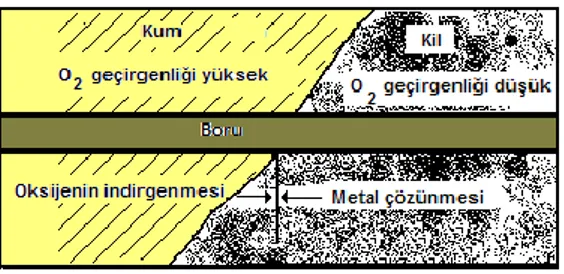
kilometrelerce uzunluğundaki bir petrol boru hattında ya da rafineri tanklarında paslanmaz çeliklerin kullanılması yerine düşük karbon çelikleri kullanıldığı, bunları korozyona karşı korumanında daha ekonomik olduğu ifade edilmiştir (Erbil, 1996). Doruk (1996), tarafından yapılan çalışmada çok fazla teknik bilgi gerektiren konu olarak ortaya çıkan korozyon olayı ve korozyondan korunma yöntemlerinin aslında basit bir elektrokimyasal sisteme dayandığı açıklanmıştır. Slabaugh (1974), tarafından yapılan çalışmada korozyonun kimya derslerinde örnekler ile açıklanması gerektiği vurgulanmış ve çalışmada metallerin elektro kimyasal dizinin korozyon olayı ve katodik koruma basit bir şekilde şematize edilmiştir. Diğer bir araştırmada korozyon olayının kinetik incelemesi eğitime taşınmıştır. Çalışmada korozif olan asidik ortamlarda ortama ilave edilen bazı iyonların
mekanizmaya etkileri araştırılmış ve özellikle O2 indirgenmesi ile kinetik çalışma
gerçekleştirilmiştir. Kinetik incelemeyi bakır gibi iyonların oto katalitik korozyonunda mekanizması ile incelenmiş ve üniversite eğitimindeki yeri ve önemi belirtilmiştir. (Habashi, 1965). Powell, D., Cortez, J., ve Mellon, E.K. (1987), tarafından yapılan çalışmada da kimya eğitimine yeni başlayan çocuklara korozyon konusunu çok iyi açıklayan Pourbaix diyagramları öneminden bahsedilmiştir. Çalışmada Pourbaix diyagramlarının kobalt metali için çizilebileceği bir öğrenci deneyi önerilmiştir ve bu diyagramın öğrenci için önemi vurgulanıp, nasıl kullanılacağı anlatılmıştır.(Free, 2005), tarafından yapılan çalışmada internetteki çeşitli materyalleri kullanarak korozyon öğretiminin artırımını ve öğrencinin kaliteli bir korozyon eğitimi sağlanabileceğini belirtmiştir. Uygulanan online derslerin öğrenciler üzerinde geleneksel yöntemlere göre daha başaralı olduğu saptanmıştır.
Sanayileşmenin getirdiği yeniliklerle birlikte önemi daha da artan bu konunun güncel sonuçlarını, çevresinde gelişen olayların sebeplerini ve sonuçlarını bilebilecek seviyeye öğrencileri ulaştırmak eğitimcilerin büyük bir sorumluluğudur. Bunun içinde eğitimciler korozyon hakkındaki yeterliliklerini artırmalıdır.
1.2.Araştırmanın Amacı
Bu çalışmanın amacı; ortaöğretim kimya ve fizik öğretmenlerinin korozyon hakkındaki bilgi ve düzeylerinin belirlenip araştırılmasıdır. Elde edilen verilere göre ortaöğretim müfredat programında korozyon konusu araştırılıp yeterliliği tartışılacaktır. Araştırmanın amacı doğrultusunda şu sorulara cevap aranmıştır.
4
1. Ortaöğretim kimya ve fizik öğretmenlerinin bilgi ve düzeyleri öğrencilerin konuyu anlamaları açısından yeterli midir?
2. Ortaöğretim müfredatında korozyon eğitimi yeterli düzeyde öğretilmekte midir? 3. Ortaöğretim kimya, fizik öğretmenleri günlük yaşantıda meydana gelen korozyon
olaylarını açıklayabilirler mi?
4. Korozyon eğitimi yeterlilik düzeyi branşa göre değişmekte midir?
1.3.Araştırmanın Önemi
Korozyonun neden olduğu doğrudan ve dolaylı kayıplar ülkemizde de ileri boyutlardadır. Bu nedenle korozyon ve korozyondan korunmanın ilke ve uygulamaları hakkında bilgi vermek önem arz etmektedir. Korozyon konusu hakkında bilgi edinmenin iki önemli nedeni vardır. Birincisi ekonomiktir. Buna bağlı olarak, bugüne kadar yapılan araştırmalar incelendiğinde korozyonun neden olduğu doğrudan ve dolaylı kayıpların giderilmesi için, korozyona karşı verilen savaş başarı ile sürdürülmüştür. İkinci neden ise günümüzde hızla artan çevre bilinci ve buna bağlı olarak ta çevreyi korumada etkili hala gelen yaklaşımlardır. Çevremizi kirleten gaz emisyonları ve atıkların miktarını azaltarak çevreyi korumak ve korozyona karşı verilen savaşın önemini kavramaktır.
Sanayileşme ile birlikte önemi daha da artan ve ülke ekonomisine oldukça büyük yük getiren korozyon olayının ortaöğretim kimya ve fizik öğretmenlerince öneminin anlaşılması, korozyondan korunma ve bu konuda güncel örneklerin verilebilmesi önem arz etmektedir.
1.4.Araştırmanın Sayıltıları
Araştırmaya katılan öğretmenlerin uygulanan ölçme araçlarını içtenlikle ve doğru olarak yanıtlayacağı varsayılmaktadır.
Araştırmada kullanılan ölçme araçları araştırmanın amacına uygun niteliktedir.
1.5.Araştırmanın Sınırlılıkları
Araştırma Eskişehir ili Özel Gülbahar Anadolu Lisesi ve Özel Ertuğrulgazi Anadolu Lisesi ortaöğretim kimya ve fizik öğretmenleri ile sınırlıdır.
5 Araştırma 10 ay ile sınırlıdır.
1.6.Tanımlar
Kimya: Maddenin yapısını, özelliklerini, bileşimini, etkileşimlerini ve tepkimelerini araştıran bilim dalıdır. Kimya bilimi daha kapsamlı bir ifadeyle, maddelerin özellikleriyle, maddelerin sınıflandırılmasıyla, atomlarla, atom teorisiyle, kimyasal bileşiklerle, kimyasal tepkimelerle, maddenin halleriyle, moleküller arası ve moleküler kuvvetlerle, kimyasal bağlarla, tepkime kinetiğiyle ve kimyasal dengenin prensipleriyle ve benzeri konularla ilgilenir.
Fizik: Maddenin kimyasal yapısındaki değişiklikler dışında genel ya da geçici yasalara
bağlı, deneysel olarak araştırılabilen, ölçülebilen, matematiksel olarak
tanımlanabilen madde ve enerji olgularıyla uğraşan bilim dalı; insanın doğal yapısı, dış görünüşü
Korozyon: Metal veya metal alaşımlarının oksitlenme veya diğer kimyasal etkilerle aşınma durumu. Demirin paslanması, alüminyumun oksitlenmesi korozyona örnek olarak verilebilir. Türkçeye yabancı dillerden giren korozyon sözcüğü; yenme, kemirilme gibi anlamlarla alakalıdır. Aşınma, çürüme, paslanma, bozulma ve yenim gibi sözcüklerle karşılanabilir.
Müfredat: Eğitimin bir programa bağlanmasıdır. Öğretim veya eğitim planı için kullanılır. Öğretim programı; ne konuların öğretileceğini, bunun hangi sırayla verileceğini, bir konunun üstünde ne kadar durulacağını açıklar.
6
BÖLÜM II
KAVRAMSAL ÇERÇEVE
2.1. Korozyon
Genel olarak maddelerin, özel olarak metal ve alaşımların çevrenin çeşitli etkileriyle kimyasal ve elektrokimyasal değişme ya da fiziksel çözünme sonucu aşınmasına korozyon denir (Üneri, 2003).
Metallerin çoğu tabiatta bileşik halinde bulunurlar. Bu bileşikler metallerin en kararlı halleridir. Metaller bu bileşikler halinde iken serbest enerjileri en düşük durumdadır. Bu bileşiklerin değişikliğe uğratılması ile metal veya alaşımlar elde edilir. Mineralleri metal haline dönüştürmek için enerji harcanması gerekir.
Metallerin bulundukları ortamın elemanları ile tepkime a girerek önce iyonik hale sonra ortamdaki başka elementlerle birleşerek tabiattaki ilk bileşik hallerine dönmeye çalışmaları neticesi, fiziksel, kimyasal, mekanik veya elektriksel özellikleri istenmeyen değişikliklere uğrarlar. Bu bozulma tepkimesine korozyon denir. Korozyon, metalik malzemelerin içinde bulunduğu ortamla tepkime a girmeleri sonucu, dışarıdan enerji vermeye gerek olmadan doğal olarak meydana gelen bir olaydır. Korozyon nedeni ile malzeme, enerji emek, bilgi ve ürün kaybı hesabı tahmin edilemeyecek kadar büyüktür. Korozyon sebep olduğu maddi kayıplar yanında, çevreyi kirleten ve insan hayatını tehlikeye sokan bir değişimdir ( Doruk, 1982).
2.1.1. Korozyon ve Önemi
Korozyon, bir metalin bulunduğu ortam içinde kimyasal veya elektrokimyasal tepkime lar sonucu bozulması şeklinde tanımlanabilir. Fiziksel nedenlere dayanan bozulmaya ise erozyon denir. Kimyasal korozyon deyimi, metal ve alaşımların gaz ortamlar içindeki oksitlenmesini ifade eder, buna “kuru korozyon” da denilmektedir. Metal ve alaşımların
7
sulu ortamlardaki korozyonu ise “elektrokimyasal korozyon” olarak adlandırılır. Buna “ıslak korozyon”da denilebilir. Gerçekte ise her iki korozyon türü de temelde aynı ve elektrokimyasal esaslıdır. Ancak bu tür deyimler yerleşmiş bulunmaktadır (Doruk, 1982). Korozyon aslında metallerin tabii hallerine dönüş gayretinden başka bir şey değildir. Bilindiği gibi teknolojik öneme sahip metallerin, hemen hemen tamamı tabiatta bileşik halinde bulunur. Bu yüzden, bu bileşiklerden üretilen metal ve alaşımların tekrar kararlı halleri olan bileşik haline dönme eğilimleri vardır. Bu eğilimin sonucunda, metaller içinde bulundukları ortamın elementleri ile tepkime a girerek önce iyon sonra da bileşik haline geçerler ( Doruk, 1982).
Çevre Bileşik Haldeki Metal + Enerji
(Fe, Al, vb) (H2S, O2, N2, H2O vb) (Sülfit, Oksit, vb) (Serbest Enerji)
Şekil 1. Metalin Çevre İle Etkileşimi
Bir metalin çevresi ile etkileşerek fazla enerjisini vermesi ve kararlı bileşiği haline dönüşmesi doğal bir olaydır. Bir metalin en kararlı yapısı kimyasal potansiyelin en düşük olduğu haldir. Ancak bu hal genelde metalin pek fazla istenmeyen oksitlenmiş halidir ve metal genellikle yüksek ısıl işlemlere tabi tutularak oksijenden ayrılır. Ancak saf haldeki metal çok daha yüksek bir kimyasal potansiyele sahip olduğunda elde ettiği ilk fırsatta çok daha düşük kimyasal potansiyel ve yüksek kararlı hal olan oksit yapısına geri döner. İşte bu atmosferik korozyonun temelidir. Bu tip korozyona uğramayan maddeler soy metaller denilen Au, Pd, Ru ve Rh dır. İşte enerji ve emek sarf edilerek güçlükle elde edilen metallerin bu şekilde doğal hallerine dönüşleri, ekonomik açıdan oldukça büyük kayıplara neden olmaktadır. En basit deyimle korozyon sonucu kaybedilen metal, elde edilmesi sırasında harcanan emeğin, enerjinin ve paranın boşa gitmesi demektir. Her ülkenin, özellikle de sanayileşmiş ülkelerin korozyon giderleri oldukça büyük miktarlar tutmaktadır.
Türkiye‟de ise korozyon kayıplarının, Gayri Safi Milli Hâsılanın (GSMH) %4.36‟sına eşit olduğu araştırmalar sonucu elde edilmiştir. 1997 yılında eğitime ayrılan payın, GSMH‟ nın % 1.76‟sı, 1998 yılında % 2.53‟ü olduğu dikkate alınırsa, konunun önemi açıkça görülmektedir (Doğan, 2006).
8
Yadsınamayacak kadar önemli olan bu rakamlar, korozyonla mücadelenin ne kadar önemli olduğunu ortaya koymaktadır. Korozyon, ekonomik açıdan olduğu kadar, insan sağlığı bakımından da oldukça önemlidir. Korozyon ürünlerinin gıda maddelerine karışması tehlikeli sonuçlar doğurabilmekte, korozyon sonucu dayanımını yitirmiş yapıların beklenmedik bir zamanda çökmesi can kaybına neden olabilmektedir. Görevini yapamayacak duruma gelmiş metal malzemenin değiştirilmesi sırasında, tesisin üretim faaliyetlerinin durdurulması da doğrudan ürün kaybına yol açmaktadır. Bunların yanı sıra metalin korozyon yoluyla bileşiklerine dönüşmesi hammadde rezervlerinin daha kısa sürede tüketilmesine neden olmaktadır (Doğan, 2006).
Korozyonun neden olduğu çevresel ve ekonomik zararların boyutu, korozyon çalışmalarının önemini gündeme getirmektedir. Korozyon zararlarını gidermek için çok büyük emek, maliyet ve zaman gerekmektedir. Bu nedenle korozyon hızının ölçülmesi ve korozyon kaynaklı kayıpların önlenebilmesi amacıyla gelişmiş ülkelerde sürekli olarak araştırmalar yapılmaktadır. Ülkemizde de korozyon olayının anlaşılması ve korunma yöntemlerinin geliştirilmesi için artan bir dikkate ihtiyaç vardır (Doğan, 2006).
2.1.2.Paslanma
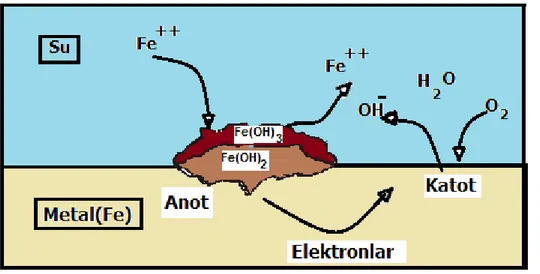
Pas, su ve hava varlığında oluşan demir ve oksijen bileşiklerine (genellikle kırmızı oksitler) verilen genel addır. Pasın değişik formları görsel olarak ve ya spektroskopi ile saptanabilir ve değişik koşullar altında oluşabilirler. Pas, hidratlı demir(III) oksit
(Fe2O3.H2O) ve demir(III) oksit-hidroksit (FeO(OH), Fe(OH)3) içermektedir. Şekil 2 de
demirin atmosfer korozyonu mekanizması verilmiştir.
9
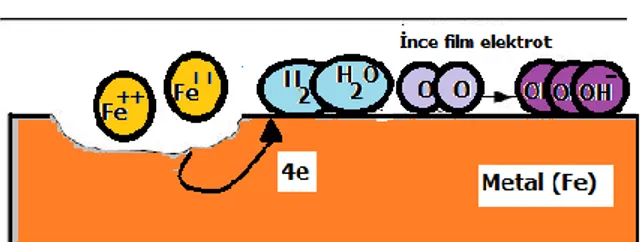
Paslanma demir ve onun çelik gibi alaşımlarının korozyonu için kullanılan ortak bir terimdir. Diğer metallerin uğradıkları korozyonda oksitlenme olsa da pas olarak isimlendirilmemektedir. Şekil 3 de demir metalinde gerçekleşen anot ve katot tepkimeleri verilmiştir.
Şekil 3. Fe Metalinde Gerçekleşen Anot ve Katot Tepkimeleri
Anot Tepkimleri (Yükseltgenme) Katot tepkileri (İndirgenme) FeFe2+ + 2e Fe2+ Fe3+ +e
Notr veya alkali ortam 1/2O2 +H2O+2e2OH
-
Asidik ortam 2H++2eH2
2.2. Elektrokimyasal Korozyon
Korozyon olayı, biri anotta yükseltgenme, diğeri katotta indirgenme şeklinde aynı anda yürüyen iki elektrokimyasal tepkime dan oluşur (Şekil 2.4 ve 2.5). Korozyon metaller ile
ilgili bir terim olup M → Mz+
+ ze şeklindeki bir elektrokimyasal yarı tepkime sonucunda oluşur.Korozyon elektrokimyasal bir terim olduğundan tepkime a giren türler arasında olan potansiyel farkına çok bağlıdır . Korozyona uğrayan metal bir enerji üretecinin kısa devre
yapılmış halidir .
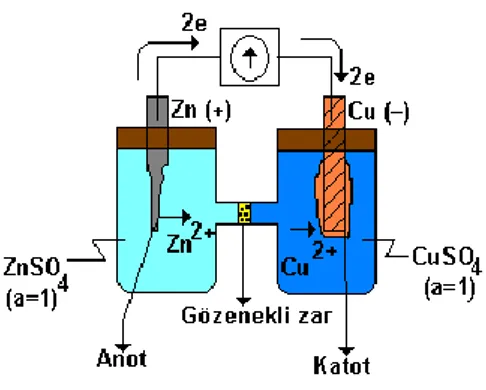
10 Şekil 4. Daniel Pili
Eğer araya bir direnç koymadan Zn ve Cu elektronları birbirine bağlarsak
Şekil 5. Bir Korozyon Hücresinde Akım ve Elektronların Yönü
Daha soy olan Cu katot olarak davranıp bakır iyonları birikirken çinko anot olarak davranıp yükseltgenerek çözünür. Bu durum bu iki metalin uç uca eklenmesiyle eşdeğerdir Bu açıdan bakıldığında korozyon olayı kendiliğinden akım üreten bir galvanik pil olarak düşünülebilir. Korozyonun yürümesi için mutlaka iki ayrı metalin bulunması şart değildir. Korozyon, bir metal yalnız başına elektrolit içinde bulunurken de meydana gelebilir. Metalin kristal yapısı farklı olduğundan yüzeydeki bazı bölgeler daha çok oksijene maruz kalarak mikro katotlar oluştururlar bu durumda daha az maruz kalan kısımlarda mikro anot olarak davranırlar. Bunun sonucunda başlayan mikro korozyon zaman içinde büyüyerek makro çatlaklara sebep olur veya elektrolitte bulunan bazı farklılıklar nedeniyle bir potansiyel farkı oluşabilir. Bunun sonucu olarak metal yüzeyinin bazı bölgeleri katot, bazı bölgeleri de anot olur. Böylece mikro veya makro ölçüde korozyon hücreleri oluşur. Anot ile katot arasındaki elektron akımı metal üzerinden gerçekleşir. Korozyon olayı metalin
11
yükseltgenmesiyle ile anotta meydana gelir ve anotta metal elektron vererek iyon halinde çözeltiye geçer (Yalçın ve Gürü, 2002). Katot da ise katyonlar indirgenerek birikir.
Korozyon olayında katotta metalin indirgenmesi yerine, içinde bulunduğu ortam koşullarına bağlı olarak farklı indirgenme tepkimeleri meydana gelir. Katot tepkimesi elektrolit ortamının pH derecesine ve elektrolit içinde çözünmüş oksijen derişimine bağlıdır. Doğal elektrolitler içinde yürüyen korozyon olaylarında başlıca aşağıdaki üç tepkime söz konusudur (Yalçın ve Gürü, 2002).
Şekil 6. Çelik Çubuk Üzerinde Korozyon Oluşumu
2.2.1. Anodik veya Yükseltgenme Tepkimesi
Bu tepkime metal atomlarının elektron vererek pozitif yüklü iyonlara dönüşmeleridir. Başlangıçta yüksek enerjiye sahip metal iyonları belirli sayıda çözücü molekülü ile bağ kurarak alçak enerji durumuna geçerler ve kararlılık kazanırlar ( Bilgin, 2008).
2.2.2. Katodik veya İndirgenme Tepkimesi
Katodik tepkimelerdeki anodik tepkime sırasında ortaya çıkan elektronlar metal katyonlar tarafından alınarak bunlar yüksüz metaller şeklinde çöktürtülmesidir. Katodik bir tepkime varsa mutlaka anodik bir tepkime de vardır. Kısacası elektron vererek yükseltgenen maddeler iyonlaşarak yok olmakta elektron alan iyonlar ise birikerek geri kazanılmaktadır. Bu iki tepkime elektrokimyasal bir tepkimenin yarı tepkimeleri olarak bilinir.
Katodik olayın hızı bir yandan elektrolit içindeki indirgenebilen iyon ve moleküllerin derişimine diğer yandan da bunların olay yerine, yani katot yüzeyine ulaşım hızına bağlıdır (Yalçın ve Gürü, 2002).
12
Metalik veya elektronik akım elektron aktarımı sonucudur. Bu aktarılan elektronlar metalin son yörüngesinde bulunan değerlik elektronları olup metalin iletkenliği ise bu elektronların hareketliliğine bağlıdır. Örneğin son yörüngesinde 1 elektron içeren lityumun iletkenliği son yörüngesinde 2 tane değerlik elektronu olan berilyumun ve 3 elektron içeren bor dan daha .Çözeltilerde ise durum tamamen farklıdır. Bir kere akım hem pozitif (katyonla) hem de negatif(anyonlar) tarafında çift yönde taşınır ve bunların akım taşıma kapasiteleri büyüklüklerine ve solvatize olma miktarlarına bağlıdır. Yüzeyde oluşan bir oksit tabakası bazen bu akımın akmasını büyük oranda önleyebilir ( anodik koruma ).
2.3. Galvanik Seri
Metallerin oksitlenme eğilimi standart elektrot potansiyellerine göre belirlenebilir. Metallerin standart potansiyelleri Nerst formülü tarafından belirlendiğinden bunun bir adı da NERST Skalasıdır. Bu skala tüm metal iyonlarının birim aktiviteye sahip olduğu durum için geçerli olup 1 atmosferde ve 25ºC’de 1 mol / lt iyon sulu çözeltisi hidrojen gazı ile temastaki platin elektrotundan oluşan standart hidrojen elektrotunun potansiyeli 0V olarak kabul edilmek suretiyle çıkarılmıştır. 1960lara kadar yükseltgenme tepkimesine göre verilen bu değerler 1960’da sonra indirgenme ( veya anti korozyon tepkimesine) göre verilmeye başlamıştır. Bilindiği gibi bir tepkimesin kendiliğinden olması için emk kuvveti veya potansiyelinin (+) olması gerekir. Dolayısıyla bu seride en (+) potansiyele sahip olan metal en soy olanıdır. Bir metalin aktifliği, elektronunu verme eğilimi, diğer bir ifade ile tepkimeye girme eğilimidir. Metaller etkinleştikçe daha kolay korozyona maruz kalır. Nerst skalasında verilen elektrot potansiyelleri, standart potansiyellerdir. Pratikte su ve
zemin içerisindeki elektrot potansiyeli için kalomel veya doygun Cu / CuSO4 referans
elektrotu kullanılır. Bu elektrotların standart hidrojen elektrotuna göre ölçülen elektrot potansiyelleri;
Kalomel elektrot = +0,280 V Cu / CuSO4 = +0,316 V
Ancak bu yöntemde her şey standart halde olmalıdır. Bunun pratik alana uygulanması bir çok açıdan hata getirir. O yüzden burada metallerin standart halde yani birim aktiviteye sahip olmalarının gerekmediği galvanik seriyi kullanmamak çok daha akılcı bir davranış olur.
13
Tablo 1. Nerst Skalası(standart elektrot potansiyelleri , E0)
Metal
Tepkime Standart Oksitlenme
İndirgenme Potansiyeli (V) Li Li+ + eLi -3,03 K K+ + e K -2,925 Na Na+ + e Na 2,713 Mg Mg2+ + 2e Mg -2,371 Al Al3+ + 3e Al -1,66 Zn Zn2+ + 2e Zn -0,763 Cr Cr2+ + 2e Cr -0,74 Fe Fe2+ + 2e Fe -0,44 Cd Cd2+ + 2e Cd -0,402 Ni Ni2++ 2eNi -0,23 Sn Sn2++ 2e Sn -0,14 Pb Pb2+ + 2e Pb -0,126 H 2H+ + 2eH2 0 Cu Cu2+ + 2e Cu +0,337 Hg Hg2+ + 2eHg +0,792 Ag Ag+ + e Ag +0,799 Pt Pt2+ + 2e Pt +1,2 Au Au3++ 3e Au +1,45
Nerst skalasında verilen elektrot potansiyelleri, standart potansiyellerdir. Pratikte su ve
zemin içerisindeki elektrot potansiyeli için kalomel veya doygun Cu / CuSO4 referans
elektrotu kullanılır. Bu elektrotların standart hidrojen elektrotuna göre ölçülen elektrot potansiyelleri;
Kalomel elektrot = +0,280 V Cu / CuSO4 = +0,316 V
Ancak bu yöntemde her şey standart halde olmalıdır. Bunun pratik alana uygulanması bir çok açıdan hata getirir. O yüzden burada metallerin standart halde yani birim aktiviteye sahip olmalarının gerekmediği galvanik seriyi kullanmamak çok daha akılcı bir davranış olur. Galvanik seri kabaca aşağıda gösterilmiştir.
14 Şekil 7. Metal ve Metal Alaşımlarının Galvanik serisi
2.4. Korozif Ortamlar
Korozyon çeşitli ortamlar içinde değişik şekilde ortaya çıkar. Esas olan çözünmüş halde iyon içeren bir çözeltinin (elektrolitin) bulunmasıdır. Bu açıdan bakıldığında yalnız sulu çözeltiler değil, hava, zemin, beton gibi rutubet içeren ortamlar da korozyona neden olabilirler. Bütün bu ortamlar içinde elektrolitik tipte korozyon olayı gerçekleşir. Atmosferde bulunan tanklar, depolar, direkler, korkuluklar, zemin içinde bulunan boru
15
hatları, beton içinde bulunan betonarme demirleri ve deniz içindeki gemiler, iskeleler korozyon olayı ile karşı karşıyadır. Bütün bu ortamlarda meydana gelen korozyon olayı aynı karakterde olmakla beraber, değişik ortamlarda metal yüzeyine oksijen difüzyon hızı birbirinden farklı olduğundan korozyon hızları ve etkisi de birbirinden farklıdır. Bu ortamlarda yürüyen korozyon olaylarının ayrı ayrı ele alınması uygundur (Yalçın ve Gürü, 2002).
2.4.1. Atmosferik Korozyon
Atmosfer içinde bırakılan metaller korozyona uğrar. Yapılan araştırmalar tüm metalik yapıların yaklaşık % 80‟inin atmosferik etki altında kaldığını göstermiştir. Köprüler, direkler, çatılar, balkonlar, korkuluklar, depolar, raylar, taşıt araçları vs. birçok metal yapı sürekli olarak atmosfer etkisinde kalmaktadır. Özellikle endüstriyel olarak kirlenmiş atmosferlerin etkisinde kalan çıplak metal yapılar kısa sürede korozyona uğrarlar. Örneğin çeliğin atmosfer içindeki korozyon hızı su altı ve yeraltı korozyon hızına göre çok az olmasına rağmen, atmosferik korozyonun neden olduğu kayıpları, toplam korozyon zararlarının hemen hemen yarısını oluşturur.
2.4.2. Yeraltı ve Sualtı Korozyonu
Çeşitli amaçlarla yeraltına veya sualtına konulmuş olan metal yapılar öncelikle çelik borular, kazıklar, tanklar, suyun ve zeminin korozif etkisi nedeniyle kısa sürede korozyona uğrayarak kullanılmaz hale gelirler. Yer altı ve sualtında korozyon hücrelerinin oluşma nedenleri çok çeşitlidir.
Şekil 8. Toprak Korozyonu Oluşum Mekanizması
16 •Zemin yapısı ve rutubeti
•Zemin boşluklarında bulunan oksijen konsantrasyonu •Zemin redoks potansiyeli
•Zemin pH değeri
•Zemin özgül elektrik direnci
•Zemin içinde bulunan mikroorganizmalar
Şekil 9. Su Altı Korozyonu
Su altı korozyonuna etki eden en önemli faktörler de şunlardır: •Oksijen konsantrasyonu
•pH değeri
•Kalsiyum karbonat çökelmesi (Yalçın ve Gürü, 2002).
2.4.3. Deniz Suyu İçinde Korozyon
İletkenliği oldukça yüksek olan deniz suyu, temas ettiği metalik yapılar için Şiddetli korozif bir ortam oluşturur. Özellikle demir ve yumuşak çelik demir suyu içinde süratle korozyona uğrar. Deniz suyu içinde en büyük bileşen olarak bulunan klorür iyonu ve diğer halojenler, çeliğin pasifleşmesini önleyerek çukur korozyonu oluşmasına neden olurlar. Diğer taraftan deniz suyu direncinin düşük oluşu metal yüzeyinde oluşan korozyon hücrelerinin etkinliğini arttırır.
Deniz suyunun bileşimi ve korozif etkisi çeşitli denizlerde birbirinden biraz farklıdır. Deniz suyu içinde çözünmüş tuz konsantrasyonu 32–36 g/L arasında değişir. Tropikal
17
bölgelerde ve kıyılardan uzaklarda tuzluluk artar. Deniz suyu içinde bulunan çözünmüş tuzun büyük bir kısmı NaCl halindedir (Yalçın ve Gürü, 2002).
2.5. Korozyon Çeşitleri
2.5.1. Homojen Dağılımlı Korozyon
Metal yüzeyinde eşdeğer şiddette oluşan korozyon türüdür. Korozyon sonucu metal kalınlığı her noktada aynı miktarda azalır. Atmosfer ortamında ve herhangi bir dış etkenden etkilenmeyen tamamı aynı cins malzemeden üretilmiş olan metaller homojen korozyona uğrar. En yaygın korozyon türüdür. Örneğin atmosfer ortamında bulunan demir levhanın her yanı aynı derecede korozyona uğrar. Ağırlık taban alındığında, çelik başta olmak üzere metallere en fazla zarar veren korozyon türüdür.
2.5.2. Korozyona Karşı Alınabilecek Tedbirler
Korozyon olayını kontrol etmek için dikkat edilmesi gereken hususlar temel olarak şunlardır ;
Tasarımın değiştirilmesi Çevrenin değiştirilmesi
Koruyucu kaplama uygulamak Uygun malzeme seçimi
Katodik ve anodik koruma (Doğan, 2006).
En yaygın korozyon türü olarak, homojen dağılımlı korozyonun yol açtığı metal kaybı diğer korozyon türlerine oranla çok yüksektir. Buna karşın en az korkulan korozyon türü olduğunu belirtmek gerekir. Çünkü homojen dağılımlı korozyonun hızı basit laboratuar deneyleri ile saptanabilir. Böylece saldırgan ortamlara terk edilen parça ve yapıların ömrüne ilişkin tutarlı tahminlere ulaşmak mümkün olur ( Doruk, 1982).
18
Birbirleriyle temas halinde olan farklı türden metal ve alaşımların aynı ortama terk edilmesi halinde karşılaşılan korozyon olayıdır. Farklı malzeme kullanımından kaynaklanan korozyon; farklı potansiyelde iki metal birbiriyle temas halinde iken(şekil 2.8) aralarında bir galvanik pil oluştururlar ve aktif olan metal anot, soy metal ise katot görevi görerek aktif metalde korozyona sebep olur. Örneğin bakır ile çeliğin temas etmesi durumunda bakırdan dolayı çelik korozyona uğrayacaktır.
Şekil 10. Galvanik Korozyon Oluşum Ortamı
Bu tür galvanik eşlemeler çoğunlukla arzumuz dışında ve ya imalat gereksinimi olarak karşımıza çıkarlar. Örneğin otomobil motorunun soğutma sisteminde ayrı türden malzemeler soğutucu ortamla temas halindedirler. İlke olarak aktif olan metallerin korozyonu hızlanırken daha soy olan metallerin korozyonu yavaşlayacak ve tamamen önlenecektir (Doruk, 1982).
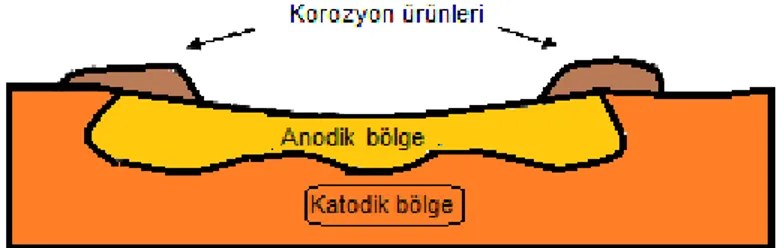
2.5.4. Çukurcuk Korozyonu
Korozyon olayının çok dar bölgelerde yoğunlaşması sonucu ortaya çıkan korozyon türüdür. Metal yüzeyinde oluşan çok sayıda çukurcuklar genellikle bir karıncalanma görünümü verir. Çukurcukların çapı, derinliği ve sıklığı malzeme ve ortama bağlı olarak değişir. Toplam metal kaybı homojen dağılımlı korozyonun aksine çok küçüktür. Ancak parçalar kısa zamanda delinerek kullanılamaz hale gelir. Bozucu etkisi, yaygınlığı ve kontrolündeki güçlükler nedeni ile en korkulan korozyon türüdür
19
Şekil 11. Çukurcuk Korozyonu Oluşum Mekanizması
Çukurcuk korozyonunu birçok metal ve alaşımda görmek mümkündür. Ancak teknolojik ve ekonomik açıdan paslanmaz çelikler ve alüminyum alaşımlarda öncelikle değinmek gerekir. Çukurcuk korozyonu genellikle klor ve brom iyonları içeren nötr ortamlarda oluşur (Doruk, 1982).
2.5.5. Aralık Korozyonu
Korozyon olayının belirli dar bölgeler üzerinde yoğunlaşması sonucu ortaya çıkan bozunma türlerinden biri de aralık korozyonudur. Aralık korozyonu makine parçalarının montajında kesinlikle yok edilemeyen dar bölgeler ve aralıklar içinde başlar.Dar bölge korozyonunun oluşabilmesinin ön koşulu aralıkların, ortamın girmesine izin verecek kadar geniş, ancak gerekli tıkanıklığın sağlanabilmesi için de yeterli darlıkta olmasıdır. Gözlemler bu tür korozyonun milimetrenin onda biri, hatta daha küçük kesirleri ile ifade edebileceğimiz dar alanlarda başlayabildiğini göstermektedir ( Doruk, 1982).
2.5.6. Seçici (Selektif) Korozyon
Alaşımlarda belirli bir metal veya belirli bir faz üzerinde yoğunlaşarak öncelikle çözünmelerini sağlayan korozyon türüdür. İlke olarak elektrokimyasal galvanik seride birbirinden çok uzak metallerden oluşan alaşımlar seçici korozyona uğrarlar. Örneğin altın-gümüş alaşımı seyreltik nitrik asit çözeltisine terk edilince altın-gümüşün çözündüğü ve hatta giderek geriye yalnız saf altının kaldığı görülür.Bakır-çinko alaşımlarında görülen çinko kaybı bu korozyon türüne verebileceğimiz örneklerden biridir ( Doruk, 1982).
Örneğin; %70 Cu + %30 Zn‟den oluşan pirinç içinde bulunan Zn kolayca korozyona uğrayabilir. Korozyon sonucu, alaşım yüzeyinde Zn konsantrasyonu azalır ve normal sarı
20
renk, bakır kırmızısına dönüşür. Çok sık rastlanan bu seçimli korozyon olayına ‟çinko azalması’’ adı verilir.
2.5.7. Tane Sınırları (Taneler Arası) Korozyon
Metal atomları daima geometrik bir düzen içinde kristalleşir. İki veya daha fazla metalden oluşan homojen yapıdaki alaşımlar da belli bir düzen içinde kristalleşir. Bunlara katı çözelti denebilir. Heterojen yapıdaki alaşımlarda ise, iki veya daha fazla katı fazlı karışım söz konusudur. Böyle bir alaşımda kristaller homojen bir yapıda değildir. Taneler arası korozyon, taneler arası sınır çizgilerinde meydana gelir. Bu bölgelerde metallerden biri diğerine göre daha düşük konsantrasyonda bulunur. Bu nedenle sınır çizgileri korozyon için uygun bir ortam oluşturur. Paslanmaz çelikte kaynak yapılan bölgede bu tip taneler arası korozyon olayı meydana gelir.
Tane sınırları korozyonunun en belirgin özelliği çok küçük ağırlık kaybına karşın, korozyon hızının tane sınırları yakınında çok yüksek değerlere ulaşabilmesidir. Bu koşul, parçalarına kısa sürede tüm kesit alanı boyunca korozyona uğrayarak bozunmalarına yol açar. Taneler bütünlük ve şekillerini korurlarken taneler arası bağ bozunmaya uğrar. Bunun sonucunda korozyonun etkin olduğu bölgelerde mekanik dayanç sıfıra indirgenir (Doruk, 1982).
2.5.8. Gerilimli Korozyon
Saldırgan ortamlarda temas halinde olan makine parçaları ve metal yapıların çoğu mekanik gerilimler altındadır. Yüksek basınçlı kaplar, buhar kazanları, içten yanmalı motorların silindir gömlekleri birçok örnekten birkaçıdır. Gerilimli korozyon aynı zamana rastlayan korozif ve mekanik etmenlerin yol açtığı bozunma türü olarak tanımlanabilir.
Gerilimli korozyonun en önemli özelliği kimyasal ve mekanik etkilerin birbirlerini destekler nitelikte gelişmeleridir. Bu nedenle aynı zamana rastlamayan korozif ve mekanik etkilerin toplamı gerilimli korozyon olarak nitelenemez. Gerilimli korozyonun oluşabilmesi için gerekli koşulları şöyle özetleyebiliriz;
1.Duyarlı bir malzeme 2.Etken bir ortam
21 3.Çekme gerilimi
4.Zaman ( Doruk, 1982)
2.5.9. Erozyonlu Korozyon
Malzeme yüzeyi ile ortam arasındaki bağıl hızın yüksek değerlere ulaştığı sistemlerde görülen bozunma türüdür. Metal kaybı metalin iyonlarına dönüşmesi veya yüzeyde oluşan oksit tabakalarının uzaklaştırılarak ortama karışması ile gerçekleşir (Doruk, 1996).
Özellikle boru sistemlerinde ve limanlarda çok rastlanan bu tür korozyonda metal ile korozif ortam arasındaki bağıl hareket nedeniyle metalin aşınma hızı artar. Metal yüzeyinde delikler, oluklar ve hendekler oluşur. Su içinde hareket halindeki birçok yapıda kendini gösterir. Ortamda katı parçacıkların varlığı korozyon hızını daha da artırır ( Bilgin, 2008).
Erozyonlu korozyonun rastlandığı haller hayli yaygındır. Gaz ve sıvıların pompalanması ve uzak mesafelere taşınmasında kullanılan teçhizat ve boru hatları, örneğin kömür ve maden cevherlerinin toz halinde su ile karıştırılarak uzak mesafelere pompalandığı boru hatları, sıcak su ve buhar hazırlama tesisleri verilebilecek
örneklerdir (Doruk, 1982).
2.6. Korozyona Etki Eden Faktörler
2.6.1. Coğrafi Yerleşim
İklim bölgelerindeki şartlara göre meydana gelebilecek korozyonun şiddeti değişebilir. Tropik deniz ve okyanus bölgelerindeki yüksek hava sıcaklığı denizden yükselen tuz yüklü hava ile birleşerek kısa sürede metaller üzerinde şiddetli bir korozyon oluşmasına neden olur. Bu bölgelerde etkin bir koruyucu bakım işlemi uygulanması gerekir (Doğan, 2006). Ilımlı hava iklimine sahip endüstriyel bölgeler ise korozyon riski açısından tropikal bölgelerden hemen sonra gelir. Yüksek sıcaklık ve nemin oluştuğu zamanlarda metal yüzeyleri yaygın olarak korozyon etkisi altında kalır. Fabrikalardan, binalardan ve taşıtlardan çıkan duman, is, toz ve artık gazlar metalleri olumsuz yönde etkiler. Buzul veya çöl iklimine sahip bölgelerde ise korozyon oluşma ihtimali çok azdır. Çünkü söz konusu
22
her iki bölgede de nem oranı düşüktür. Buna karşılık özellikle çöl iklimine sahip bölgelerde iki olumsuz etken olarak çok yüksek sıcaklık ve kum fırtınası tehlikeleri oluşabilir (Doğan, 2006).
2.6.2. Sıcaklık
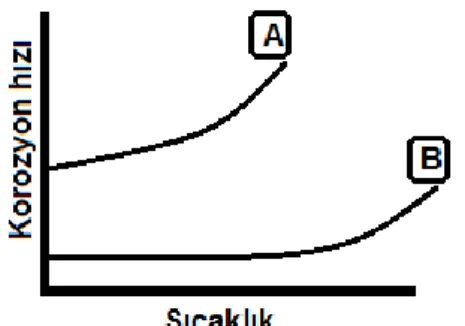
Bilindiği gibi sıcaklık, hemen hemen bütün kimyasal tepkimelerin hızını artırır. Bu yüzden genel olarak sıcaklık arttığı zaman korozyon da artar. Şekil 12’de korozyon hızı üzerine sıcaklığın iki bilinen etkisi görülmektedir.
Şekil 12. Korozyon Hızı Üzerine Sıcaklığın Etkisi
A eğrisi, sıcaklığın artması ile birlikte korozyon hızında çok hızlı ve üstel bir artışın olduğunu gösterir. B eğrisi de çok rastlanan bir durumdur. Şöyle ki sıcaklığın az olması halinde, korozyon ihmal edilebilecek kadar az iken, daha yüksek sıcaklıklarda korozyon hızında çok büyük bir artış görülür. Bunun sebebi, HNO3 içinde 18 Cr–8 Ni paslanmaz çeliğin davranışı ile kolayca açıklanabilir. Bilindiği gibi nitrat asidinin sıcaklığındaki artış, asidin yükseltgeme gücünü büyük ölçüde artırır. Düşük sıcaklıklarda nitrat asidine maruz bırakılan paslanmaz çelik, trans pasif bölgeye geçmesine ve çok hızlı bir şekilde korozyona uğramasına neden olur. Benzer davranışı nikel de gösterir.
Bazı durumlarda sıcaklık yükselmesine rağmen, korozyon hızında düşme görülebilir. Mesela demir, çözülmüş oksijen ihtiva eden su içindeki bu davranışı gösterir. Demirin kaynayan su veya deniz suyu içindeki korozyon hızı düşük sıcaklıklardaki korozyon hızından daha azdır. Bunun nedeni yüksek sıcaklıklarda suyun daha az oksijen içermesinden ileri gelmektedir. Oksijen kaynama sonucu ortamdan uzaklaştırılınca katodik ve buna bağlı olarak da anodik tepkime yavaşlar ve korozyon hızı düşer (Doruk, 1982).
23 2.6.3. Oksijen ve Yükseltgenler
Bu bölümde oksitleyici maddelerin ve oksitlenme gücünün etkisi örnekler üzerinde durularak ele alınacaktır. Korozyon hızı üzerine oksitleyicilerin etkisi şekil 13’de verilen bir grafikle gösterilebilir.
Şekil 13. Havalandırma ve Oksitleyicilerin Korozyon Hızı Üzerine Etkisi
Bu şekilde grafiğin 3 bölümden oluştuğu görülmektedir. 1. bölüm normal bir metalin davranışıdır. Pasifleşen metallerde, pasifleşme olayı, sadece ortama kâfi miktarda yükseltgen ilave edildiği zaman meydana gelir. Şeklin 1. kısmında pasifleşmeyen metaller yer almaktadır. Demir havalandırılmış su içinde pasiflik kazanamaz. Şeklin 2. kısmında görüldüğü gibi, korozyon hızındaki artışı hızlı bir azalma takip eder. 2. bölgedeki davranışı gösteren metallerin korozyon hızları yükseltgenin konsantrasyonundan bağımsızdır. Bu davranış pasifleşebilen 18 Cr-8 Ni, titanyum gibi malzemelerin özelliğidir.
Bir metal oksitleyicinin ilavesinden sonra pasif duruma geçmişse, çok güçlü bir oksitleyicinin etkisine maruz bırakılmadığı takdirde, pasifliğini devam ettirir. Ancak ortama çok güçlü bir oksitleyici ilave edilirse bu defa korozyon hızı şiddetle artış gösterir. Şekil 2.12 de 2 bölgesinden 3 bölgesine geçen metalin davranışı bu durumu yansıtmaktadır. Kromat gibi çok güçlü oksitleme özelliğine sahip maddeler korozif ortama
24
ilave edilirse paslanmaz çelik korozyona uğramaya başlar. Derişik ve sıcak sülfat-nitrat asidi karışımları da çok güçlü yükseltgen özellik taşır. Böyle karışımlarda sülfat-nitrat asidi oranı artırılırsa, pasifleşebilen metallerin pasifliği bozulur.
2.6.4. Malzeme Seçimi
Korozyona sebep olan etkenlerden biri de birbiriyle potansiyel farkı bulunan metallerin bir arada kullanılmasıdır. Bu durum korozyonu başlatıcı ve hızlandırıcı bir etkendir. Mesela çok düşülen bir hata olarak çelik saçtan yapılan panoların üzerine konulan paslanmaz çelik cıvata ve contalar bulundukları bölgede galvanik korozyona sebep olmaktadır. Bu tip durumlarda ana yüzeye civatalar ya da contalar plastik civatalar ile izole edilmelidir .
2.6.5. Parça Boyutu
Kalın kesitli metal parçalara üretim esnasında sıcak işlem uygulanmışsa, bu parçaların korozyona uğrama ihtimali yükselir. Kesit büyüklüğü metal parçanın yapısal özelliğine ve üstleneceği göreve göre tasarlanır. Korozyonun yapacağı etkiyi önlemek amacıyla metalin kesit büyüklüğünün değiştirilmesi genellikle tercih edilmez. Birbirine temas edecek şekilde iki farklı metal birlikte kullanıldığında metallerden aktif olanı ince kesitli ise korozyon hızlı ve hasarlı olarak gerçekleşir. Eğer aktif olan metal kalın kesitli ise korozyon yavaş ve az hasarlı gerçekleşir. Bu durumda iki metal arasında yalıtım gerekebilir. Aksi halde anot durumundaki metal kullanılmaz hale gelecektir (Doğan,2006).
2.6.6. Sistem Dizaynı
Korozif malzemelerin depolandığı sistemlerde korozif ortamın (su vb) birikmesini engellemeye yönelik tasarımlar uygulanmalıdır.
Kazan ve depoların, ayrıca yağmura açık yapı elemanlarının sıvı birikimine olanak vermeyecek şekil ve konumda olmaları gerekir. Örneğin depoların kolay ve tamamen boşaltımını sağlamak için depo tabanı boşaltma deliğine doğru eğimli olmalıdır.
Perçinli ve cıvatalı bağlantılar aralık korozyonu için elverişli dar bölgeler oluştururlar bu nedenle korozyonun beklendiği koşullarda kullanılmamaları, bunun yerine lehim ve kaynak gibi bağlantı türlerine öncelik verilmesi gerekir.
25
Galvanik dizide birbirlerinden uzak olan metal ve alaşımların eşlenmesi olanaklar ölçüsünde önlenmeye çalışılmalıdır. Bu tür eşleşmeler kaçınılmaz bir zorunluluk olarak ortaya çıkarsa aynı cinsten olan metaller yalıtkan conta ve ara parçaları kullanılarak bilir yalıtılmalıdır.Tasarım hususunda dikkat edilmesi gereken bazı hususlar Şekil14‘de gösterilmiştir.
Şekil 14. Korozyon Korumasında Tasarımın Önemi
a) Birbiri üzerine yatay binen iki metal levhanın korunması b) Birbiri ile dikey kesişen iki
metal levhanın korunması c) Borularda koruma d) Tanklarda koruma
2.7. Korozyon Koruma Yöntemleri
26
Belli bir ortam içinde bulunan metalik yapının korozyonunu önlemek veya korozyon hızını azaltmak üzere alınacak önlemleri üç ana grup altında toplanabilir:
•Katodik koruma •Anodik koruma
2. Kimyasal Yöntemler •İnhibitör kullanılması
•Söz konusu ortama dayanıklı bir metal veya alaşımın seçilmesi •Çevrenin kimyasal bileşiminin değiştirilmesi
3. Koruyucu Kaplamalar
•Organik kaplama (boya) uygulanması
•İnorganik kaplama yapılması (Yalçın ve Gürü, 2002).
2.7.1.Katodik Koruma
Katodik korumanın temel ilkeleri elektrokimyasal korozyon teorisine dayanmaktadır. Katodik koruma korozyona uğrayan metallerin katot olarak polarizasyonunu gerektirir. Bu korunacak metali daha aktif bir metal ile (galvanik anot veya kurban anot) eşleyerek sağlanacağı gibi dıştan akım uygulayarak da gerçekleştirilebilir (Şekil 15).
Şekil 15. Katodik Koruma
Galvanik anotlar koruma sırasında belirli hızlarla çözünerek ağırlıklarını kaybederler. Bunları uygun zaman aralıklarıyla yenileyerek koruma işlevine süreklilik kazandırılır.
27
İkinci yöntemde korunan metal ve anot çiftinin akım üretir nitelikte olması gerekmez. Çünkü koruma için gerekli akım uygun bir dış kaynaktan çekilir. Yavaş çözünürlük yanında ekonomik olan malzemeler anot malzemesi olarak kullanılır. Galvanik anotlu, katodik koruma sistemlerinde kullanılan anot malzemeleri genellikle çinko, alüminyum ve magnezyumdur. Dış akım kaynaklı katodik koruma sistemlerinde Fe-Si, Pb-Sb-Ag ve Ti bazlı anotlar kullanılır. Katodik korumanın en fazla uygulandığı alanlar şunlardır;
Gemilerin taban yüzeyleri
Gemilerin balast tankları
Dubalarda ve balast tankları
Yeraltı boru hatları
Mavnalarda ve-iskele ayakları
Petrol depolama tankları
Su depolama tankları
2.7.2. Anodik Koruma
2.7.2.1. Metallerin Polarisazyonu Metallerin polarisasyon eğrileri genel olarak
28
Burada B noktasında metal kolayca korozyona uğrar. C noktasında korozyon hızı maksimum olur. Ancak D noktasından daha anodik potansiyellerde metalin üzeri koruyucu bir filmle kaplanır ( genellikle zor çözünen bir oksit ) ve akım yoğunluğu ve dolayısı ile korozyon hızı hızla düşer . Akım E noktasına kadar değişmez . Ancak E noktasında pasif film çözünmeye ve çukurcuk oluşmaya başlar. Buna “kritik çukurcuk” veya “kırılma” potansiyeli denir. DE bölgesine pasif bölge E’den sonraki bölgeye de “transpassif bölge” adı verilir.
Metal ve alaşımların teknik ve ekonomik açıdan önem taşıyan büyük bir bölümü pasifleşme özelliğine sahiptir. Korozyona uğramakta olan bir metalin pasif tutuma geçmesi sonucu korozyon hızında büyük bir azalma görülür. Anodik koruma bu ilkeye dayalı olarak gerçekleştirilir. Anodik koruma metalleri korozyondan korumak için uygulanan ilginç bir elektrokimyasal yöntemdir. Bu yöntemde metale anodik yönde bir dış akım uygulanarak metalin pasiflik potansiyeline gelmesi sağlanır. Anodik koruma esas olarak bir pasifleştirme işlemi olarak kabul edilebilir. Bu nedenle yöntem ancak pasifleşme özelliği olan metallere uygulanabilir.
Burada yüzeyde sıkı ve koruyucu bir oksit tabakası oluşturulur ve bu tabaka mükemmel bir şekilde malzemeyi sararak onu korozyondan korur.Ancak bu her metale uygulanamaz . Oluşan oksit tabakası gevşek ve kolayca metal üzerinden kolayca sıyrılabilecek bir şekilde ise bu metalin korozyonu artırmaktan başka bir işe yaramaz.
Anodik koruma yapılarak metal sürekli olarak pasif halde tutulur. Pasif hal, korozyon akımının en düşük olduğu haldir. Ancak en düşük korozyon akımı her zaman yeterli derecede düşük olmayabilir ve bu nedenle bazı çözeltiler için bu yöntem uygun çözüm getirmez. Ayrıca; anodik korumada, potansiyel ve akım kontrolünün çok iyi yapılması gerekir. Eğer sistemde bir arıza meydana gelirse, korunan metal kısa sürede korozyona uğrayabilir. Bu nedenle anodik koruma genellikle şiddetli korozyon olayının söz konusu olduğu ortamlarda korozyon hızını azaltmak amacıyla kullanılır (Yalçın ve Gürü, 2002).
2.7.3. İnhibitör İle Koruma
Ortama az miktarda katıldığında korozyon hızını azaltan maddelere korozyon inhibitörü denir. Korozyona karşı dayanıklı fakat pahalı bir malzeme kullanılmak yerine bazı halde ortama inhibitör katılarak daha ucuz malzemelerin kullanılması yoluna gidilir. İnhibitör kullanımı çukur korozyonuna karşı en ekonomik çözüm yoludur (Yalçın ve Gürü, 2002 ).
29
İnhibitörlerin korozyon hızı azaltıcı etkileri çeşitli şekillerde gerçekleşir. Bazı inhibitörler metal yüzeyinde ince bir film oluşturarak, metal ile çevresi arasındaki tepkime hızını yavaşlatır. Bazı halde ortamda bulunan korozyon yapıcı bileşenin, örneğin çözünmüş oksijenin inhibitör tarafından kimyasal olarak bağlanması ile korozyon önlenebilir. İnhibitörler, anodik inhibitör veya katodik inhibitör olarak ikiye ayrılır ( Yalçın ve Gürü, 2002).
2.7.4. Boya ile Koruma
Boyalar, metal yüzeyini çevreden yalıtarak su ve oksijenin metal yüzeyine ulaşmasını önleyen genellikle organik malzemelerdir. Boyaların bileşiminde korozyonu önleyici çeşitli pigmentler kullanılır. Boyalar, uygulama kolaylığı ve düşük maliyetleri nedeniyle korozyondan korumak üzere yaygın olarak kullanılmaktadır. Bu amaçla çok sayıda boya cinsleri geliştirilmiştir. Bunların kimyasal bileşimleri ve fiziksel özellikleri birbirinden farklı olmakla beraber, hepsinde ortak olan, sağlam ve geçirimsiz bir kabuk oluşturarak metalin çevresi ile temasını önlemektir.
Boyalar korozyonu önleme görevini üç şekilde yerine getirir:
•Bütün boyalar, metal yüzeyi ile çevre arasında geçirimsiz bir tabaka oluşturarak metalin çevresi ile tepkime a girmesini önler.
•Bazı boyalar içinde inhibitör etkisi yapan pigmentler bulunur. Bunlar metal yüzeyinin pasifleşmesine neden olurlar.
• Bazı boyalar içinde dolgu maddesi olarak çinko tozu bulunur. Çinko galvanik etki yaparak metali katodik olarak korur (Yalçın ve Gürü, 2002).
Organik kaplamaların en önemli temsilcisi olan boyaların uygulanabilmesinin temel koşulu, korunan metalin bırakılacağı ortamda yeterli bir korozyon dayancına sahip olması gereğidir. Aksi halde malzeme, kaplamanın boşluklu olduğu ve zamanla çatlayarak döküldüğü yerlerde hızla korozyona uğrar. Buna karşıt örnek atmosferik korozyona bırakılan çelik yapılardır. Çelik atmosferin saldırganlık derecesine bağlı olarak belirli sürede paslanır. Ancak paslanmanın hızı çok yavaş olduğundan çelik yapıları boyayarak atmosferik korozyona karşı korumak teknik bakımdan yapılabilir ve aynı zamanda ekonomik bir çözümdür (Doruk,1982).
30 2.7.5. Metalik Kaplama ile Koruma
Metalik bir yüzeyi korumak amacı ile üzerine kaplanan metal, ya bu metale göre ortama daha dayanıklı soy bir metaldir veya bu metali korumak için kendisi tercihli olarak çözünür ve kapladığı metalin çözünmesine engel olur. Yani daha aktiftir. Birinci tip yani soy metal kaplamalarına örnek, bakır üzerine altın veya gümüş, çelik üzerine kalay kurşun veya krom kaplamadır. İkinci tip, yani aktif kaplama metallerine ise, çelik üzerine çinko, kadmiyum, alüminyum kaplama örnek gösterilebilir.
Soy metaller ile yapılan kaplamalarda meydana gelen hatalar, devamsızlıklar (çizikler, gözenekler, kesik – çentik kenarlar) altından açığa çıkan alt metal soy metale göre anot olur. Bu bölgelerde büyük katot – küçük anot etkisi ile Şiddetli korozyon olayı görülür. Bu nedenle bu tip kaplamalarda kaplama hataları çok tehlikeli sonuçlar doğurur. Aktif kaplama metallerindeki küçük devamsızlıklar altından açığa çıkan alt metal ise korozyona uğramaz. Çünkü aktif metal kendisi harcanarak bir çeşit katodik koruma ile alt metali korur. Aktif metalleri ile kaplamada ilginç bir yöntem de, aktif metal yüzeylerinin kromat veya fosfat tabakası ile kaplanmasıdır. Bu durumda aktif metalin çözünmesi büyük ölçüde azalır.
Metalik kaplamaların bileşimleri, yapıları, içerdikleri safsızlıklar korozyon dirençlerine etki eder. Metal kaplamaların seçiminde ortam, metal kaplanmış parçanın kabul edilebilir ömrü, dekoratif etki, metalin türü, parçanın Şekli ve boyutu, daha sonra uygulanacak imalat yöntemleri ve mekanik faktörler rol oynar. Metalik kaplamalarda sağlanmak istenen korozyon direncinin optimum olması için ise, metalik malzemenin kullanılacağı ortam, üzerine kaplama yapılan alt metal cinsi, kaplamanın türü, uygulama şekli, kaplamanın alt veya üstünde başka kaplama bulunup bulunmadığı gibi faktörler önemlidir.(Doğan, 2006)
2.8. Fen Okur-Yazarlığı
Fen okur-yazarlığı, genel bir tanım olarak; bireylerin araştırma-sorgulama,eleştirel
düşünme, problem çözme ve karar verme becerileri geliştirmeleri, yasam boyu öğrenen bireyler olmaları, çevreleri ve dünya hakkındaki merak duygusunu sürdürmeleri için gerekli olan fenle ilgili beceri, tutum, değer, anlayış ve bilgilerin bir bileşimidir.
Ayrıca fen okur-yazarlığı fen bilimlerinin doğasını bilmek, bilginin nasıl elde edildiğini anlamak, fen bilimlerindeki bilgilerin bilinen gerçeklere bağlı olduğunu ve yeni kanıtlar