T.C.
DİCLE ÜNİVERSİTESİ TIP FAKÜLTESİ
ÇOCUK SAĞLIĞI VE HASTALIKLARI ANABİLİM DALI
AİLEVİ AKDENİZ ATEŞLİ ÇOCUKLARDA
DEPRESYON VE HAYAT KALİTESİNİN
DEĞERLENDİRİLMESİ
Dr. Erkan HALİLOĞLU UZMANLIK TEZİ
T.C.
DİCLE ÜNİVERSİTESİ TIP FAKÜLTESİ
ÇOCUK SAĞLIĞI VE HASTALIKLARI ANABİLİM DALI
AİLEVİ AKDENİZ ATEŞLİ ÇOCUKLARDA
DEPRESYON VE HAYAT KALİTESİNİN
DEĞERLENDİRİLMESİ
Dr. Erkan HALİLOĞLU UZMANLIK TEZİ
Tez Danışmanı
Yrd. Doç. Dr. Ünal ULUCA
TEŞEKKÜR
Çocuk Sağlığı ve Hastalıkları uzmanlık eğitimim süresince bilgi ve tecrübelerinden yararlandığım, bana her konuda desteğini sunan Çocuk Sağlığı ve Hastalıkları Anabilim Dalı Başkanımız Prof. Dr. Kenan HASPOLAT’a, tezimin planlanması, yürütülmesi ve hazırlanmasının her aşamasında bana yol gösteren Yrd. Doç. Dr. Ünal ULUCA’ya, anketlerin tamamlanmasında ve değerlendirilmesinde büyük yardımı olan Yrd. Doç. Dr. Şeref ŞİMŞEK’e, uzmanlık eğitimim süresince bilgi ve klinik tecrübelerinden faydalandığım, üzerimde büyük emeği olan değerli hocalarım Prof. Dr. M. Ali TAŞ, Prof. Dr. Aydın ECE, Prof. Dr. Murat SÖKER, Prof. Dr. M. Fuat GÜRKAN, Prof. Dr. Ahmet YARAMIŞ, Prof. Dr. Celal DEVECİOĞLU, Prof. Dr. Gökhan BAYSOY, Doç. Dr. Ayfer GÖZÜ PiRiNÇÇiOĞLU, Doç. Dr. Mustafa TAŞKESEN, Doç. Dr. Meki BİLİCİ, Doç. Dr. Selvi KELEKÇİ, Doç. Dr. Velat ŞEN, Doç. Dr. İlyas YOLBAŞ, Yrd. Doç. Dr. Ali GÜNEŞ, Yrd. Doç. Dr. Fesih AKTAR, Yrd. Doç. Dr. Servet YEL, Yrd. Doç. Dr. İlhan TAN, Yrd. Doç. Dr. Sabahattin ERTUĞRUL ve Yrd. Doç. Dr. Fikri DEMİR’e ayrı ayrı şükranlarımı sunarım.
Dört yıl boyunca mesai ve nöbetlerde pek çok şeyi paylaştığım tüm doktor arkadaşlarıma, bölüm hemşirelerine ve yardımcı sağlık personellerine teşekkür ederim.
Tüm hayatım boyunca benden maddi ve manevi desteğini esirgemeyen anneme, babama, her zaman yanımda olan ve bu süreci beraber paylaştığım eşim Buket’e ve oğlum Yiğit Eymen’e teşekkürlerimle...
Dr. Erkan HALİLOĞLU Diyarbakır-2016
ÖZET
Giriş ve Amaç: Ailevi Akdeniz ateşi (AAA) hastalığı ateş, peritonit, plevrit, artrit ve
erizipel benzeri deri döküntüleri ile seyreden, ataklar halinde gelen genetik geçişli bir hastalıktır. Hastalık uyum problemlerine, yetersizlik duygusunun gelişimine yol açmakta, hastaların yaşamlarında bazı kısıtlılıkların oluşmasına yol açmaktadır.
Bu çalışmanın amacı Diyarbakır ve çevre illerden gelen takipli pediatrik Ailevi Akdeniz ateşi hastalarının depresyon ve hayat kalitesinin değerlendirilmesidir.
Gereç ve Yöntem: Bu çalışma Tel-Hashomer tanı kriterlerine göre tanı konulmuş 51
Ailevi Akdeniz ateşi (AAA) hastası ve 53 sağlıklı çocuğun katılımıyla gerçekleştirildi. Kontrol grubu genel çocuk polikliniğine rutin kontrol amaçlı başvurmuş ve başvuru esnasında herhangi bir hastalığı olmayan çocuklardan oluşturuldu. Depresyon durumu ve hayat kalitesini belirlemede hasta ve sağlıklı grubuna sosyo-demografik veri formu, Çocuk ve Ergenler için Yaşam Kalitesi Ölçeği (SYK), Çocuk Depresyon Ölçeği (ÇDÖ) uygulandı.
Bulgular: Hasta ve kontrol grubu arasında yaş ve cinsiyet dağılımı yönünden fark
yoktu. Sağlıklı grubun ÇDÖ skoru 6,2±4,7 iken hasta grubun ÇDÖ skoru 11,6±5,5 saptandı. Hasta grubun ÇDÖ skoru anlamlı ölçüde yüksek saptandı (p=0,029). Sağlıklı grubun toplam yaşam kalitesi puan ortalaması 103,1±9,5 iken hasta grubun toplam yaşam kalitesi puan ortalaması 85,0±8,4 saptandı. Hasta grubun yaşam kalitesi, sağlıklı gruptan anlamlı ölçüde düşük saptandı (p<0,001). Yaşam kalitesi ölçeği alt boyutları bedensel iyilik, duygusal iyilik, öz saygı, ailesel iyilik, arkadaş durum, okul durum puanları açısından bakıldığında da hasta grupta, sağlıklı gruptan anlamlı düşük olduğu saptandı (p<0,001). Ayrıca hasta grupta AAA Şiddet skoru arttıkça yaşam kalitesinin düştüğü saptandı (p=0,002). Artriti olan hastaların yaşam kalitesi, artriti olmayanlara göre daha düşük saptandı (p<0,001). Kolşisin kullanım dozu normalden düşük, normal ve normalden yüksek olarak sınıflandırılmış şekliyle depresyon varlığı açısından karşılaştırıldığında kolşisini yüksek dozda kullanan hastalarda depresyon oranı daha yüksek tespit edildi (p<0,001). Yaşam kalitesi ölçeği ile karşılaştırıldığında ise doz arttıkça toplam yaşam kalitesi puanının düştüğü tespit
Sonuç: Ailevi Akdeniz ateşi hastalığının depresyon riskini arttırdığı ve yaşam
kalitesini düşürdüğü tespit edildi. Ailevi Akdeniz ateşi hastalığı çocuk ve ergenlerin kaygılarını arttırmakta, depresyona meyilli hale getirmekte, yaşam kalitelerinin düşürüp sosyal, duygusal gelişimlerini ve akademik başarılarını olumsuz yönde etkilemektedir.
Anahtar Kelimeler: Çocuk, Ergen, Ailevi Akdeniz ateşi, Depresyon, Yaşam
SUMMARY
Introduction and Objectives: Familial Mediterranean fever (FMF) is a disease
which is inherited in case of attacks with fever, peritonitis, pleuritis, and erysipelas-like skin rash associated with arthritis. Disease, leads to compatibility problems, feelings of inadequacy and to the formation of some limitations in patient’s lives.
The aim of this study is to evaluate depression and life quality of the pediatric familial Mediterranean fever patients coming from Diyarbakır and nearby cities.
Materials and Methods: This study was performed with 53 healthy children and 51
Familial Mediterranean fever (FMF) patients diagnosed according to Tel-Hashomer criterias. The control group consists of children who applied to the general pediatric outpatient clinic for a routine check and without any illness. Socio-demographic data form, Quality of Life Scale for Children and Adolescents (SYK) and Children's Depression Inventory (CDO) were applied to the both control and patient group in order to find out their depression and life quality level. All participants were informed about the study and signed a consent form for attendance.
Findings: There was no difference between the patient group and the control group
in terms of age and gender. The average CDO score of the patients group was 11.6±5.5, while it was 6.2±4.7 for the control group. CDO score of the patient group were significantly higher than healthy control group (p=0.029). The average Health-Related Quality of Life Questionnaire for Children and Adolescents (SYK) score for the patient group was 85.0±8.4 and SYK score for the healthy control group was 103.1±9.5 the SYK scores of the patient group was significantly higher than the control group (p<0.001). Also have decreased the quality of life in patients with increasing AAA severity score (p=0.002). Quality of life of patients with arthritis was lower than artrit those without (p<0.001). The rate of depression in patients taking high doses of colchicine were higher Colchicine dosage, lower than usual, as it was classified as normal and higher than normal compared for the presence of depression (p <0.001). Compared with the scale of quality of life (SYK) was found to decrease in the dose increases the total quality of life scores (p=0.004).
Conclusion: FMF increases the risk of depression and decreases the quality of life.
The Familial Mediterranean fever, increases the concerns of children and adolescents, it tends to make the depression, reduce the quality of life and seems to negatively affect their social, emotional development and academic achievement.
Keywords: Children, Adolescents, Familial Mediterranean fever, Depression,
İÇİNDEKİLER
TEŞEKKÜR……….I ÖZET...II SUMMARY………...………IV TABLOLAR LİSTESİ...VIIII ŞEKİLLER LİSTESİ...X KISALTMALAR...XII 1 GİRİŞ ve AMAÇ...1 2 GENEL BİLGİLER...12.1 Ailevi Akdeniz Ateşi (AAA) Tanımı...3
2.2 Tarihçe...3 2.3 Epidemiyoloji...4 2.4 Genetik...5 2.5 Patogenez...8 2.6 Klinik Özellikleri...10 2.6.1 Ateş...11 2.6.2 Karın Ağrısı...12 2.6.3 Eklem Bulguları...12 2.6.4 Göğüs Ağrısı...13 2.6.5 Cilt Bulguları...14 2.6.6 Kas Bulguları...15 2.6.7 Vaskülit...15 2.6.8 Skrotal Tutulum...16 2.6.9 İnfertilite...17 2.6.10 Nörolojik Tutulum...17 2.6.11 Splenomegali, Hepatomegali...17
2.7 Laboratuvar Bulguları ve Radyoloji...18
2.8 Tanı...19
2.8.1 Genetik Olarak İlişkili Hastalıklar...22
2.8.2 Ayırıcı Tanı...22 2.9 Amiloidoz...26 2.10 Şiddet Skorlaması...28 2.11 Tedavi...28 2.11.1 Yan Etkileri...32 2.12 Depresyon...32 2.13 Yaşam Kalitesi...36
3 MATERYAL ve METOD...39
3.1 Araştırmanın Türü...39
3.2 Araştırma Modeli...39
3.3 Veri Toplama Araçları...39
3.3.1 Demografik Veri Formu...40
3.3.2 Çocuklar İçin Depresyon Ölçeği (ÇDÖ)...41
3.3.3 Çocuklar İçin Genel Amaçlı Sağlıkla İlgili Yaşam Kalitesi Ölçeği...41
3.3.4 Veri Analizi...42
3.4 Araştırmanın Etik Onayı...43
4 BULGULAR...44
5 TARTIŞMA...68
6 SONUÇLAR...77
7 KAYNAKLAR...80
TABLOLAR LİSTESİ
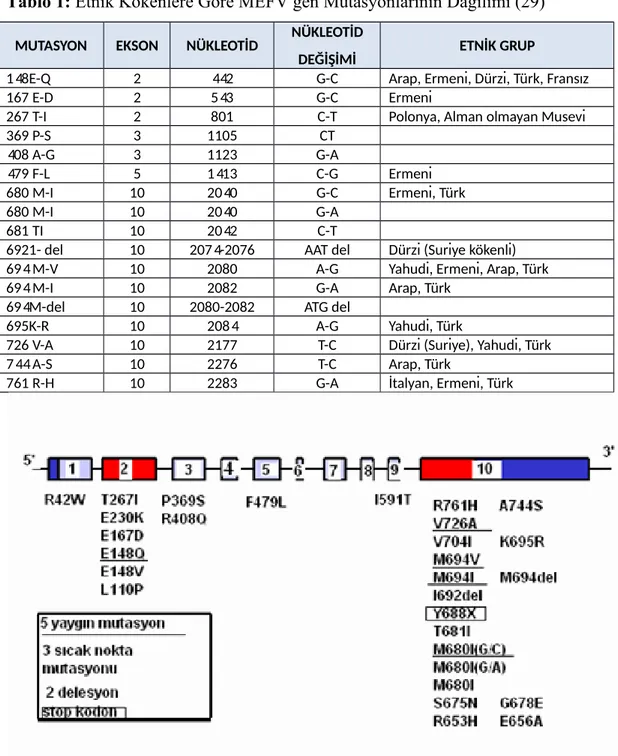
Tablo 1: Etnik Kökenlere Göre MEFV gen Mutasyonlarının Dağılımı (29)………..7
Tablo 2: Ailevi Akdeniz ateşi’nin farklı populasyonlarda klinik prevalansı (35)...11
Tablo 3: Tel-Hashomer tanı kriterleri (61)……….20
Tablo 4: Livneh ve arkadaşlarının önerdiği yeni kriterler (85)………...21
Tablo 5: Ailevi Akdeniz ateşi ataklarında ayırıcı tanı (52)……….23
Tablo 6: Kalıtsal Otoinflamatuar Hastalıklar (99)………..25
Tablo 7: Çocuklar ve ergenlerde depresif durum belirti ve semptomları (148)…….34
Tablo 8: Depresyon değerlendirme ölçütleri (144)……….35
Tablo 9: Çocuklarda sağlıkla ilgili yaşam kalitesi ölçekleri (168)……….37
Tablo 10: Hasta ve Sağlıklı Grubun Yaş ve Cinsiyetlerine Göre Dağılımı…………44
Tablo 11: Hasta Grubunun Semptom Başlama Yaşlarına Göre Dağılımı…………..44
Tablo 12: Hasta Grubunun Tanıda Gecikme Sürelerine Göre Dağılımı………….…44
Tablo 13: Hasta Grubunun Takip Sürelerine Göre Dağılımı………..45
Tablo 14: Hasta Grubunun MEFV Gen Mutasyonlarına Göre Dağılımı………45
Tablo 15: Hasta Grubun Anne ve Baba Akrabalık Durumlarına Göre Dağılımı…...45
Tablo 16:Hasta Grubun Aylık Atak Sayısına Göre Dağılımı………46
Tablo 17: Hasta Grubun AAA’ya Bağlı Klinik Bulgularının Dağılımı………..……46
Tablo 18: Hasta Grubun AAA Şiddet Skoruna Göre Dağılımı………..46
Tablo 19: Hasta Grubun Kolşisin Kullanım Dozuna Göre Dağılımı…………..……47
Tablo 20: Hasta Grubun Depresyon Varlığına Göre Dağılımı………...…47
Tablo 21: Hasta Grubu Cinsiyetlerinin ÇDÖ Puan Ortalamalarına Göre Dağılımı...47
Tablo 22: Sağlıklı Grup Cinsiyetlerinin Çocuk Yaşam Kalitesi Ölçeği Toplam Puan Ortalamalarına Göre Dağılımı………...…48
Tablo 23: Hasta Grup Cinsiyetlerinin Çocuk Yaşam Kalitesi Ölçeği Toplam Puan Ortalamalarına Göre Dağılımı………...……48
Tablo 24: Hasta Grubunun bazı bulgularının Hastalık Yükü Puan Ortalamalarına Göre karşılaştırılması……….……50
Tablo 25: Hasta Grubun bazı bulgularına Göre ÇDÖ Skor Ortalamalarının Dağılımı...51
Tablo 27: Hasta Grubun Takip Sürelerine Göre Çocuk Yaşam Kalitesi Ölçeği Puan Ortalamalarının Dağılımı………..53 Tablo 28: Hasta Grubun Aylık Atak Sayısına Göre Çocuk Yaşam Kalitesi Ölçeği
Puan Ortalamalarının Dağılımı………...…………55 Tablo 29: Hasta Grubun Kolşisin Kullanım Dozlarına Göre Çocuk Yaşam Kalitesi
Puan Ortalamalarının Dağılımı………...57 Tablo 30: Hasta Grubunda Ateş Varlığına göre Çocuk Yaşam Kalitesi Ölçeği
Puan Ortalamalarının Dağılımı………...…59 Tablo 31: Hasta Grubunda Artrit varlığına Göre Çocuk Yaşam Kalitesi Ölçeği
Puan Ortalamasının Dağılımı………..60 Tablo 32: Hasta Grubun AAA Şiddet Skoruna Göre Çocuk Yaşam Kalitesi Ölçeği
Puan Ortalaması Dağılımı………...62 Tablo 33: Hasta Grubunda AAA Şiddet Skoru ile Çocuk Yaşam Kalitesi Ölçeği
Arasında Korelasyon İlişkisi Dağılımı………64 Tablo 34: Hasta Grubunda ÇDÖ Puan Ortalaması ile AAA Şiddet Skoru Arasında
Korelasyon İlişkisi Dağılımı………...64 Tablo 35: Hasta ve Sağlıklı Grubun Yaşam Kalitesi Toplam Puan Ortalamaları ve
Alt Boyutlarının Puan Ortalamalarının Karşılaştırılması………66 Tablo 36: Hasta ve Sağlıklı Grubun ÇDÖ Skoruna Göre Karşılaştırılması……...…66 Tablo 37: Hasta ve Sağlıklı Grubun ÇDÖ’ye Göre Depresyon Varlığının
Karşılaştırılması………..………..…………..67
Şekil 1: Ailevi Akdeniz ateşinin dünyada coğrafik dağılımı (19)...5 Şekil 2: MEFV geni lokalizasyonu (27)...6 Şekil 3: MEFV geni yapısı ve mutasyon dağılımı (26)...8 Şekil 4: Pyrin’in SPRY alanı tarafından, NLRP3-bağımlı Caspase–1 aktivasyonu ve
pro-IL-1ß oluşumunun şematik gösterimi (33)...………9 Şekil 5: Pyrin, mutant pyrin, ASC proteini, pro-IL-1β ve Caspase'ın şematizasyonu
(33)...10
AML : Akut Miyeloid Lösemi Anti-TNF : Anti tümör nekrozis faktörü ASC : Apoptozis benzeri protein AFR : Akut faz reaktanı
BH : Behçet Hastalığı
CRP : C-reaktif protein
C3 : Kompleman 3
C4 : Kompleman 4
ÇDÖ : Çocuklar İçin Depresyon Ölçeği DNA : Deoksiribo Nükleik Asit
ESH : Eritrosit Sedimentasyon Hızı
GİS : Gastrointestinal Sistem
HIDS : Hiper immunglobulin D sendromu
HSP : Henoch Schönlein Purpurası
IFN-α : Interferon alfa IFN-γ : Interferon gama
Ig : İmmünglobin IL : İnterlökin
KINDL : Çocuklar için yaşam kalitesi ölçeği MDS : Miyelodisplastik Sendrom
MEFV : Mediterranean fever
PFAPA : Periyodik Ateş, Aftöz Stomatit, Farenjit ve Adenopati
PAN : Poliarteritis Nodoza SAA : Serum Amiloid A
SİGYK : Sağlıkla İlgili Genel Yaşam Kalitesi
SSRI : Selektif serotonin reuptake inhibitörü TNF – α : Tümör Nekrozis Faktör Alfa
1 GİRİŞ ve AMAÇ
Ailevi Akdeniz ateşi (AAA) Türk, Ermeni, Yahudi ve Arap toplumları gibi Akdeniz toplumlarında daha sık görülen ve ateş, peritonit, plevrit, mono/oligoartrit, erizipel benzeri deri döküntüsüyle seyreden ve ataklar şeklinde gelen otozomal resesif geçişli bir hastalıktır. Atak süresi yaklaşık 24-96 saat sürmekle beraber artrit ve artralji bulguları 1 haftadan daha uzun sürebilmektedir (1-4). Hastalığın nadir formlarında bazen menenjit ve orşit görülebilir. Ataklar arası dönemlerde hastaların klinik olarak herhangi bir şikayeti yoktur (5,6). Fakat subklinik olarak inflamasyon atak dışı dönemlerde de devam edebilmektedir. Çünkü hastaların atak dışı dönemlerinde de akut faz reaktanları ve birçok proinflamatuar sitokininin yüksek olduğu gösterilmiştir (7,8).
Ailevi Akdeniz ateşi pyrin (ateş) proteinini kodlayan MEFV geninin mutasyonunun neden olduğu düşünülen en yaygın kalıtsal otoinflamatuar sendromdur (9,10). Ailevi Akdeniz ateşi hastalığı temelde nötrofiller ile ilişkilidir. Mutasyon sonrası oluşan bozuk pyrin nötrofillerde apoptozis gelişmesini engellemektedir. Böylece nötrofil sayısı artmakta ve nötrofillerin yol açtığı inflamasyon sınırlandırılamamaktadır. Buda hastaların vücudunda süreğen bir inflamasyonun varlığına sebep olmaktadır (1,5,11).
Ailevi Akdeniz ateşinde ki bu süreğen inflamasyon ile yaygın olarak kognitif ve duyusal semptomlar, yorgunluk, aktivitedeki kısıtlanmaya bağlı psikomotor yavaşlama, azalmış motivasyon ve anksiyete sonucu yaşam kalitesi düşer ve depresyona eğilim oluşur. Son yıllarda yapılan çalışmalarda bu hastalık davranışının özellikle enfeksiyonla mücadele ve hayatta kalmayı desteklemek için son derece uyumlu ve planlı bir yanıt olduğunu göstermektedir (1,3,11).
Yapılan birçok araştırmada AAA gibi kronik hastalığa sahip olan çocukların psikososyal problemler açısından risk taşıdığı ortaya konulmuştur. Kronik hastalığı olan çocukların, sağlıklı çocuklara göre düşük kendilik saygılarının olduğunu, daha zayıf vücut imgelerinin olduğunu, psikolojik sağlık, davranış ve sosyal uyumlarında
Ailevi Akdeniz ateşi hastalığı olan çocuklar böylelikle daha fazla uyum sorunları yaşamakta ve yetersizlik duyguları ile sınırlanmalar yaşamaktadırlar. Bu nedenle günlük yaşam aktiviteleri kısıtlanır, okul hayatları zorlaşır ve bu şekilde yaşam kaliteleri olumsuz yönde etkilenir (1,3).
Ailevi Akdeniz ateşi hastalarında zorlu fiziksel aktivite ve egzersizler, kas ve eklem ağrılarına miyaljiye de yol açabildiği için bu hastalarda fiziksel eforda azalma fiziksel, sosyal ve psikolojik anlamda olumsuzluklar oluşturur.
Yapılan bazı çalışmalar sonucu AAA hastası çocuk ve ergenlerin, sağlıklı yaşıtlarına göre daha depresif olduğu gösterilmiştir. Çalışmalarda AAA hastalığındaki atak sayısının arttışı, hastanın pskilojisini olumsuz yönde etkilediği ve depresyon sıklığını arttırdığı ifade edilmiştir. Aynı şekilde duygusal durumlar ve psikolojik streste AAA ataklarını tetikleyebilir (3,5).
Sonuç olarak AAA hastalığı yaşam kalitesinde azalmaya yol açtığı, hastaları depresyona yatkın hale getirdiği gösterilmiştir. Bireyin topluma tam olarak karışmasına engel olduğu ve sosyal faliyetler içinde yeterince yer alamamasına yol açtığı, duygu durumu ile ilgili ciddi değişikliklere yol açabildiği ifade edilmektedir (1,3,5,10).
Ailevi Akdeniz ateşi hastalığında genetik değişiklikler ve hastalığın şiddeti bölgesel farklılıklar göstermektedir. Bu değişikliklerin de yaşam kalitesi ve depresyon üzerine etkili olması olasıdır. Bu çalışmanın amacı; Diyarbakır ve çevre illerden gelen tanılı ve takipli pediatrik Ailevi Akdeniz ateşi hastalarının, yaşam kalitesi ve depresyon açısından değerlendirilmesi ve günümüz şartlarına uygun yaşam kalitesini arttırıcı teknolojik gelişmeler, ilaçlar, alternatif bakım ve tedavilerin geliştirilmesine zemin oluşturmaktır.
2 GENEL BİLGİLER
2.1 Ailevi Akdeniz Ateşi TanımıAilevi Akdeniz ateşi (AAA) tekrarlayan ataklarla seyreden ateş, peritonit, plörit, artrit ve erizipel benzeri eritem ile karakterize otozomal resesif geçişli kalıtsal bir hastalıktır (1). Ailevi Akdeniz ateşi hastalığına yol açtığı bilinen herhangi bir patojen, otoantikor veya antijene özgü T hücresi olmadığı için otoinflamatuar hastalık olarak tanımlanmaktadır (2). Hastalığın en tipik özelliği ataklarla seyretmesi ve atak arası dönemlerde hastaların hiçbir şikâyetinin olmamasıdır. Ataklar, çoğunlukla 24-96 saat arasında sürmekte ve atak sırasında lökositoz, sedimentasyon hızı (ESH), fibrinojen ve C reaktif protein (CRP) gibi akut faz reaktanlarında yükselme görülür. Hastalığın nadir tutulum şekillerinde tekrarlayan orşit ve menenjit bildirilmiştir (2,3).
Ailevi Akdeniz ateşi hastalığı 16. kromozomun kısa kolunda bulunan MEFV genindeki mutasyonlar nedeniyle oluşmaktadır. Bu gen 781 aminoasit içeren bir proteini kodlar (4). Bu protein başlıca nötrofil ve monositlerden eksprese olur. Ateşle ilişkisinden dolayı ‘’pyrin’’ olarakta adlandırılmıştır. Bu proteinin kendisinin veya aktivitesinin eksikliğinde, inflamatuar hadiselerde baskılanma olmaz. Bu durum da atakların oluşmasına yol açar (5).
2.2 Tarihçe
Hastalığın ilk kez 1908 yılında Janeway ve Mosenthal tarafından tekrarlayan ateş, karın ağrısı ve lökositozu olan 16 yaşında Yahudi bir kız hastanın “Unusual Paroxysmal Syndrome” (Olağandışı Paroksismal Sendrom) tanımlamasıyla bildirimi yapılmıştır (6). Gayet tipik ve oldukça gürültülü bir klinik tabloya sebep olmasına rağmen 1945 yılına kadar bağımsız bir antite olarak tanımlanmamışır. Bu tarihte ilk kez ayrıntılı bir tanımlama getirilmiş ve Siegal (7) tarafından ‘‘Benign Paroksismal Peritonit’’ adı ile tanımlanmıştır. Bu tarihten bir yıl sonra 1946’da Türkiyede Abrevaya Marmaralı (8) tarafından ‘‘Garip Bir Karın Sendromu’’ başlığı ile Tıp Cemiyeti Mecmuasında yayınlanmıştır. 1948 yılında Riemann (9) hastalığı, "Peryodik Hastalık" olarak tanımlarken, Catton ve Mammou, 1951’de hastalığın
1958 yılında İsrailli araştırmacı Heller tarafından ilk kez “Familial Mediterranean Fever” (Ailevi Akdeniz ateşi) tanımı kullanılmıştır. 1961 yılında ise hastalığın otosomal resesif kalıtım gösterdiği bildirilmiştir (11,12).
1972 yılında Goldfinger (13), 5 vakalık bir seri üzerindeki tecrübelerinde AAA hastalığında kolşisin kullanımının faydalı olduğunu New England Journal of Medicine’de editöre mektup şeklinde yayınlamıştır. Aynı yıl Türkiye’de de Prof. Dr. Emir Özkan (14) tarafından kolşisinin bu hastalıktaki etkinliği İstanbul Üniversitesi Tıp Mecmuası’nda yayınlanmıştır. Zemer ve ark. (15) yaptıkları çalışmalar sonucunda 1986 yılındada kolşisin tedavisiyle AAA hastalarında amiloidoz gelişiminin önlenebildiğini tespit etmişlerdir.
1992 yılında hastalıktan sorumlu AAA geni 16. kromozomun kısa kolunda haritalanmıştır (16). 1997 yılında ise sorumlu MEFV genini ve bu genin kodladığı 4 pyrin/marenostrin proteinini ve M694V, M694I, M680I ve V726A mutasyonlarını tanımlanmışlardır (17,18).
2.3 Epidemiyoloji
Ailevi Akdeniz ateşi özellikle doğu akdeniz havzasında yaşayan halklar arasında sık görülmektedir. Bu halklar Askenazi Yahudileri, Sefardik Yahudiler, Türkler, Dürziler, Araplar, Ermenilerdir. 20. yüzyılda yoğun kıtalar arası göçlere bağlı olarak bütün dünyada yaygın olarak görülebilen bir hastalık haline gelmiştir (19) (Şekil 1). Japonya, İtalya, Fransa, Almanya, Avustralya, Polonya ve Brezilya gibi bazı toplumlarda da AAA hastaları bildirilmiştir.
Hastalığın sıklığı, etnik kökenlerin alt gruplarına göre de değişkenlik göstermektedir. 15.yüzyılda İspanya’dan Doğu Akdeniz'e göç etmiş olan ve Sefardik adıyla anılan museviler, hastalığın en sık rastlandığı gruptur. Babil kökenli museviler ikinci sırada yer almaktadır. Avrupa, Avustralya, Güney Afrika kökenli musevileri kapsayan Askenazi musevilerinde hastalık daha nadir görülmektedir (20). Arap toplumlarında özellikle Fas, Tunus, Cezayir, Lübnan, Filistin, Libya, Mısır, Suriye ve Irak'ta sık görüldüğü bildirilmektedir (21).
Hastalığın Türklerde görülme sıklığı 1/1073 olarak bildirilirken hastalıktan etkilenenlerin çoğunluğu İç Anadolu (Sivas, Tokat, Kayseri), Batı Karadeniz (Kastamonu, Sinop), Doğu Karadeniz iç kesimleri (Gümüşhane, Bayburt), Doğu Anadolu (Ağrı, Kars, Erzurum) ve Güneydoğu Anadolu’da (Malatya) bulunmaktadır (22,23). Otozomal resesif geçişli bir hastalık olduğu için akraba evliliğinin sık olduğu bölgelerde sıklığı artmaktadır (24). Erkeklerde biraz daha sıktır E/K:1,5-2/1. Hastalığa bağlı gelişen amiloidoza da erkeklerde daha sık rastlanmaktadır (25).
Şekil 1: Ailevi Akdeniz ateşi’nin dünyada coğrafik dağılımı (19)
2.4 Genetik
Ailevi Akdeniz ateşi geni (MEFV), 1997 yılında iki farklı çalışma grubu tarafından (Fransız AAA Konsorsiyumu ile Uluslararası AAA Konsorsiyumu) yapılan çalışmalar sonucu pozisyonel olarak klonlanmıştır. MEFV geni 16. Kromozomun 15 kilobazlık(kb) genomik DNA’sını kapsayan bir bölgesinde yer alır
781 aminoasit uzunluğundadır. Aynı anda bulunan bu genin oluşturduğu bu proteine Fransız grubu ‘’Marenostrin: Akdeniz’’ adını verirken, diğer grup ise “Pyrin: Ateş” adını vermiştir (26). MEFV geni 16. kromozomun kısa kolunun 13,3 pozisyonunda yer alır (27)(Şekil 2). Pyrin proteininin N-terminalinin 92 aminoasitlik bir bölgesinde yer alan bölümüne ‘’pyrin domain’’ ismi verilmiştir. Bu pyrin domain bölgesi sitokin aktivasyonunda ve apoptozisin regülasyonunda rol oynayan proteinlerle etkileşimi kolaylaştırır (28).
Şekil 2: MEFV geni lokalizasyonu (27)
MEFV geninin lokalizasyonunun tam belirlenmesi ve klonlanmasından sonra, farklı etnik kökenlerde 17 mutasyon saptanmıştır. Bu mutasyonlar Tablo 1’de verilmiştir (29). Ailevi Akdeniz ateşinde en fazla görülen 4 mutasyon (missense mutasyon) pyrin proteininin karboksi terminal bölgesinde bulunmuştur (26). Bu 4 missense mutasyon ( M694V, M694I, V726A ve M680I ) ekson 10’da yer almaktadır (29). MEFV geninin 10. Ekzon bölgesi mutasyonlar için hassas bir bölgedir. 10. ekzondaki bu 4 mutasyon, taşıyıcı ya da hasta kromozomlardaki AAA mutasyonlarının %85’ini oluşturur (26)(Şekil 3). Bunlardan da en sık görülen M694V homozigot mutasyonudur. Arap, Yahudi, Ermeni toplumlarında amilodoz gelişme riskini arttırdığı gözlenmiştir. M694V homozigot gen mutasyonu olan
hastalarda erken başlangıç, atak sayı fazlalığı, artrit ve erizipel benzeri eritemin daha fazla olduğu gösterilmiştir (28,30). Bunun tersi bir şekilde V726A mutasyonunda ise bir şekilde amiloidozun daha az geliştiği gözlenmiştir (26).
Tablo 1: Etnik Kökenlere Göre MEFV gen Mutasyonlarının Dağılımı (29) MUTASYON EKSON NÜKLEOTİD NÜKLEOTİD
DEĞİŞİMİ ETNİK GRUP
148E-Q 2 442 G-C Arap, Ermeni, Dürzi, Türk, Fransız
167 E-D 2 543 G-C Ermeni
267 T-I 2 801 C-T Polonya, Alman olmayan Musevi
369 P-S 3 1105 CT 408 A-G 3 1123 G-A 479 F-L 5 1413 C-G Ermeni 680 M-I 10 2040 G-C Ermeni, Türk 680 M-I 10 2040 G-A 681 TI 10 2042 C-T
6921- del 10 2074-2076 AAT del Dürzi (Suriye kökenli)
694 M-V 10 2080 A-G Yahudi, Ermeni, Arap, Türk
694 M-I 10 2082 G-A Arap, Türk
694M-del 10 2080-2082 ATG del
695K-R 10 2084 A-G Yahudi, Türk
726 V-A 10 2177 T-C Dürzi (Suriye), Yahudi, Türk
744 A-S 10 2276 T-C Arap, Türk
Şekil 3: MEFV geni yapısı ve mutasyon dağılımı (26)
2.5 Patogenez
Bağışıklık sisteminin yetersiz aktivasyonu durumunda oluşan hastalıklar immün yetmezlikler olarak adlandırılır ve fenotipik olarak tekrarlayan enfeksiyon ataklarıyla seyreder. Bağışıklık sisteminin abartılı aktivasyonu ise self-reaktif lenfositler ve yüksek titrede antikorların oluşmasına neden olur. Buda otoimmün hastalıklar tablosunu oluşturur (31). Ailevi Akdeniz ateşi hastalığı ile ilgili günümüzde en fazla kabul edilen hipotez, inflamatuar yanıtın düzenlenmesindeki bir bozukluktan kaynaklandığıdır. MEFV genindeki mutasyon sonucu kodladığı Pyrin/Marenostrin proteinin yapısının bozulmasıyla inflamasyonun baskılamasında aksama olmasıdır. Mutasyona uğrayan genin oluşturduğu bozuk pyrin proteini, inflamasyondaki baskılayıcı kontrol görevini yerine getirememektedir. Böylece inflamasyon baskılanıp durdurulamaz ve ateşle birlikte ataklar ile karakterize klinik tablo ortaya çıkmaktadır (32).
Pyrin proteinindeki bozukluk inflamasyonun sınırlandırılamamasına sebep olur. Mutasyona uğramamış normal Pyrin proteini, inlfamazomların (özellikle NLRP3) aktivasyonlarını sınırlandırarak CASPASE-1 ve İnterlökin-1 beta (IL-1β) düzeylerini ve aktivitelerini sınırlandırır. Mutasyona uğramış bozuk pyrin proteini ise inflamazomlar üzerindeki bu baskılamayı gerçekleştiremez ve özellikle NLRP3 inflamazomu ile sitozolde inaktif bulunan pro-CASPASE-1’i otoproteolitik klivaj ile aktif CASPASE-1 haline çevirir. Buda pro-IL-1β’yi matür IL-1β haline çevirir. Sonuç olarak CASPASE-1 ve IL-1β seviyeleri ve aktivasyonları artar. IL-1β konak savunmasını arttıran güçlü bir mediatördür. Aşırı üretimi doku hasarı, kemik erimesi, kollagen birikimi ve neovaskülarizasyona yol açar. Bu nedenle bu iki molekülün AAA hastalığının immün mekanizmalarında önemli rol üstlendiği düşünülmektedir (33) (şekil 4) (şekil 5).
Şekil 4: Pyrin’in SPRY alanı tarafından, NLRP3 bağımlı Caspase-1 aktivasyonu ve
pro-IL-1ß oluşumunun şematik gösterimi (33)
Ailevi Akdeniz ateşi hastalığının temel hücreleri nötrofillerdir. Pyrin mutasyonu sonrası nötrofillerde apoptozis gerçekleşememektedir. Böylece nötrofil sayısı artmakta ve nötrofillerin yol açtığı inflamasyon sınırlanamamaktadır (34).
Şekil 5: Pyrin, mutant pyrin, ASC proteini, pro-İL-1β ve Caspase’ın
şematizasyonu (33)
2.6 Klinik Özellikleri
Ailevi Akdeniz ateşi hastalığı tekrarlayan ve kendini sınırlayan ateş, poliserözite bağlı karın ağrısı atakları (plevrit, peritonit, perikardit), sinovite bağlı artrit ve eklem bulguları, erizipel benzeri döküntüler ve nadir olarakta skrotal tunika vajinalis tutulumu ile karakterize bir inflamatuar hastalıktır. Ailevi Akdeniz ateşi hastalığının etnik kökenlere göre kliniği Tablo 2’de verilmiştir (35).
Hastaların %70’lik kısmında semptomlar hayatın ilk dekadında, %90’lık kısmında da ikinci dekada kadar ortaya çıkmaktadır (36). Erkek kadın oranı: E/K 1,5-2/1’dir (37). Atakların sıklığı ve süresi hem aynı hastada hem de hastalar arasında farklılık gösterebilir. Ortalama olarak ataklar 12-96 saat arası sürer.
Ataklara artrit veya artralji eşlik ediyorsa süre daha da uzayabilir. Ataklar arasında hasta asemptomatiktir. Hastaların yaşı ilerledikçe atak sıklığında azalma ve hastalığın şiddetinde hafifleme gözlenir (38). Ataklar fiziksel aktivite, cerrahi, enfeksiyon ve emosyonel stresle artış gösterir. Kızlarda menstruasyon dönemlerinde daha fazla olabilmektedir (37).
Bir çalışmada cisplatin tedavisi alan hastalarda AAA atak sıklığının arttığı ve hastalığın daha ağır seyrettiği bildirilmiştir. Cisplatin proinflamatuar sitokinlerin (Tümör Nekrozis Faktör-alfa (TNF-α), IL-1, IL-6) yapımını uyardığı için atakları tetiklediği öne sürülmüştür (39). Yapılan bir başka çalışmada ise AAA’lı hastalarda helikobakter pylori varlığında atak sıklığının ve şiddetinin arttığı gösterilmiştir. Bu hasta grubunda helikobakter pylori eradike edildikten sonra bakılan IL-6 seviyelerinde düşme tespit edilmiştir (40).
Tablo 2: Ailevi Akdeniz ateşi’nin farklı populasyonlardaki klinik prevalansı (35) Klinik Bulgular Türkler (%) Yahudiler(% ) Araplar(% ) Ermeniler(% ) Ateş 93 100 100 100 Peritonit 94 95 82 96 Artrit 47 77 37 37 Plevrit 31 40 43 87 Eritem 21 46 3 8 2.6.1 Ateş
Ailevi Akdeniz ateşi’nin en sık görülen ve en tipik bulgularından biridir. Ateş hastaların %90’dan fazlasında bulunur. Genellikle 38-40°C arasında değişir (19). Ateşe bazen titreme de eşlik edebilir. Bir süre yüksek seyreder sonra aniden düşer. Ateşin yanında bazen generalize kas, eklem ve kemik ağrısı, baş ağrısı, migren, lenfadenopati görülebilir (41). Ateş yüksekliği çocuklarda Erişkinlere oranla daha sık saptanır, süt çocuklarında tek bulgu olabilir (42). Kolşisin kullanan hastalarda atak sırasında ateşe rastlanmayabilir (19).
2.6.2 Karın Ağrısı
Karın ağrısı, ateş ile birlikte en sık rastlanılan bulgudur. Hastaların %90’dan fazlasında görülür. Hastaların yarısında karın ağrısı ilk semptom olarak ortaya çıkar. Genellikle ateşin yükselmesiyle başlar ve ateşin düşmesinden 24-48 saat sonrasına kadar devam edebilir (19). Ağrı lokalize kalabileceği gibi tüm batında yaygın da olabilir. Fizik muayenede distansiyon, rebaund, duyarlılık ve hassasiyet olabilir. Direk karın grafilerinde hava-sıvı seviyesi oluşturabilir (35).
Ailevi Akdeniz ateşindeki karın ağrısı peritonit nedeniyle oluştuğu için bazen akut batın tablosu ile karışabilir. Bu nedenle hastaların %30’luk bir kısmında laparoskopi, apendektomi ve kolesistektomi öyküsü vardır (43).
Hastalarda karın ağrısına bulantı, kusma, kabızlık veya ishal eşlik edebilir. Peritonit, barsak hareketlerini azalttığı için hastalarda diyareden çok konstipasyon tablosu gelişir. Peritonun posterior kısmı etkilenirse renal kolik ve pelvik inflamatuar hastalığı taklit edebilir. Diyafram irritasyonu sonucu göğüste batıcı ağrı, birine veya her iki omuza vuran yansıyan ağrılar görülebilir (44). Tedavide kullanılan kolşisin yan etki olarak %10-20 oranında kronik ishal ve karın ağrısına sebep olabilir. Hastalığı ilerleyenlerde gastrointestinal sistem amiloidozuna bağlı malabsorbsiyon nedeniyle düzeltilemeyen ishaller görülebilir (19,45).
2.6.3 Eklem Bulguları
Ailevi Akdeniz ateşi hastalığında eklem tutulumu karşımıza sık çıkan bir tablodur. Vakaların %50-75’inde görülmektedir. Klinik bulgular arasında en uzun süren bulgudur. Genellikle bir hafta içinde iyileşir. En sık tutulan eklemler alt ekstremite eklemlerinin tutulumudur. Travma veya fiziksel yorgunluk artrit atağını tetikleyebilir (46). Genellikle büyük eklemleri tutan kırmızı, ağrılı, ısı artışı olan eklemlerle karakterizedir. Sıklıkla diz veya ayak bileğinde monoartrit olarak gelişir ve çoğu zaman kalıcı hasar bırakmadan iyileşir. Sık tutulum yaptığı eklemlerin yanısıra omuz, temporomandibular ve sternoklavikular eklemleri de tutabilir (35).
Ailevi Akdeniz ateşi artriti ani başlangıçlıdır ve 3 önemli özelliği vardır;
1. İlk 24 saatte artrite yüksek ateş eşlik eder.
2. Genellikle alt ekstremitelerin büyük eklemlerini etkiler (ayak bileği, diz ve kalça
gibi)
3. Semptomlar sıklıkla 24-48 saat içinde zirveye ulaşıp sonra hızla düzelir ve sekel
bırakmadan iyileşir (46).
Artrit sıklığı Türkler’de %47, Yahudiler’de %77, Ermeniler’de %37 Araplar’da %37 bulunmuştur (1,10). Gen mutasyonu M694V homozigot olanlarda artrit riski daha yüksektir (35).
Ailevi Akdeniz ateşi hastalığında eklem tutulumu 3 tipte gözlenir.
1. Asimetrik non-dekstruktif artrit: Hastaların %75’lik kısmında bu tip eklem
tutulumu karsımıza cıkmaktadır. Bir veya iki eklem etkilenir. Kendiliğinden düzelir ve tamamen rezorbe olur. Çoğu zaman diz, ayak bileği, kalça eklemleri tutar. Bu monoartrit atağı kendiliğinden oluşabileceği gibi travma veya egzersizle de oluşabilir. Genellikle bir hafta sürer (35,37,47).
2. Sakroileti içeren kronik dekstruktif artrit: Hastaların %2-5’inde görülür.
Daha çok kalça ve diz eklemlerini etkiler. Persistan effüzyon, kas atrofisi, eklem çevresinde osteoporoz ve litik lezyonlar görülebilir. Kalıcı hasar bırakabilir (35,37,47). Sakroileit tutulumu olan vakalarda HLA-B27 negatiftir (47).
3. Migratuar poliartrit: Akut romatizmal ateş kliniğine benzer kliniğe sahiptir.
Çok nadir görülmektedir (35). Artrit, artralji, myalji ve erizipel benzeri eritem görülen ve erken yaşta başlayan AAA hastalarında daha sık görülmektedir (37,47).
2.6.4 Göğüs Ağrısı
Göğüs ağrısı vakaların yaklaşık %25-40’ında görülür. Daha çok plevrite bağlı oluşur. Nadiren perikardite bağlı oluşur (24). Plevrit çoğu zaman tek taraflıdır. Daha çok kostofrenik sinüste oluşmaktadır. Plevrit tablosu yedi güne kadar sürebilmektedir
derin olmayacak şekilde, plevral zar irritasyonu yaratmayacak şekilde daha yumuşak nefes alıp verirler (48).
Efüzyon tespit edilen hastalardan aspirasyon ile alınan sıvı örnekleri nötrofilden zengin eksuda vasfındadır. Efüzyonun olduğu tarafta akciğer sesleri azalır. Aniden başlaması ve hızlı bir şekilde düzelmesi ile enfeksiyöz plevritten ayırt edilebilir. İyileşme sonrası sekel bırakmaz. Gen mutasyonu M694V homozigot olanlarda plevrit gelişme sıklığı daha fazladır (2,49).
Perikardit ataklarının klinik bulguları plevrit ataklarına benzer. Vakaların %1’den azında perikardit görülür. Bu yüzden perikardit tanısı bazen atlanabilmektedir. Diğer serozal yüzeyler sık tutulurken perikardın nadir tutulmasının nedeni tam olarak bilinmemektedir (50). Ataklar genellikle birkaç gün içinde kendiliğinden sekelsiz düzelir. Elektrokardiyografide (EKG) ST elevasyonu, ekokardiyografide (EKO) perikardiyal efüzyon ve telekardiyografide (TELE) ise kalp gölgesinde genişleme görülebilir (2,50).
Konstriktif perikardit ve perikardial tamponad nadir görülür. Türkiye’de yapılan çok merkezli bir çalışmada 2838 hastadan sadece 64’ünde (%2,4) perikardit tespit edilmiştir. Aynı çalışmada tekrarlayan perikardit bulgusu sadece iki hastada başlangıç bulgusu olarak saptanmış ve AAA’ya ait başka bir klinik bulgu saptanamamıştır (2,50).
2.6.5 Cilt Bulguları
Ailevi Akdeniz ateşinde cilt lezyonlarının görülme sıklığı çeşitli yayınlarda %12-43 arasında bildirilmiştir (51). En sık görülen cilt lezyonu ise erizipel benzeri eritemdir. Lezyonlar düzgün sınırlı, sıcak, şiş ve yama şeklindedir. Genellikle tek taraflı, ekstremitelerin ekstansör yüzünde, diz altında, baldır ön yüzünde ve ayak sırtında izlenen 10-15 cm boyutlarında eritematöz, ağrılı plaklar seklindedir (52). Bu döküntü AAA için karakteristik bir bulgu olarak kabul edilmektedir (53). Selülit veya erizipel ile benzerlik gösterir. Antibiyotik tedavisine gerek olmadan 2-3 gün içinde kendiliğinden düzelir (54).
Histopatolojik olarak lezyonlar incelendiğinde ödem, vaskülit olmaksızın perivasküler alanda polimorfonükleer hücrelerden zengin infiltrasyon görülür. Ayak bileğinde artriti olan hastalarda erizipel benzeri eritemin daha sık gözlendiği bildirilmiştir (2,55).
Ailevi Akdeniz ateşinde görülen diğer cilt lezyonları ise ödem, tekrarlayan oral aftlar, purpura, psöriazis, eritema nodozumdur (56). Ayrıca yüzde, gövdede ve ekstremitelerde çok sayıda eritemler görülebilir. Cilt bulgularının %16’sını anjionörotik ödeme benzeyen ve kendi kendini sınırlayan şişlik oluşturur (52,56).
2.6.6 Kas Bulguları
Kas ağrıları hastaların yaklaşık %20’sinde görülebilmektedir. Özellikle egzersizlerden sonra alt ekstremitelerde ortaya çıkan ağrı, birkaç saat ile birkaç gün devam edebilmektedir (24,53). Spontan, egzersiz ile tetiklenen ve uzamış febril miyalji olarak farklı 3 farklı tipte miyalji gözlenebilir (37). Yapılan bir çalışmada, miyalji tanımlayan hastaların %8’inde spontan gelişen miyalji, %81’inde egzersiz ile tetiklenen miyalji ve %11’lik kısmında ise uzamış febril miyalji tablosu olduğu tespit edilmiştir (57).
Ailevi Akdeniz ateşinde miyaljiye bağlı ağrı sıklıkla alt ekstremitelerde, diz altı bölgelerde, fiziksel egzersiz ve uzun süre ayakta kalma sonrası ortaya çıkar. Egzersiz ile tetiklenen miyaljiye ateş eşlik etmeyebilir. İstirahatle veya nonsteroid antiinflamatuar ilaçlarla düzelir (58). Uzamış febril miyalji tanımı yakın zamanda netleşmiştir. Vaskülitik bir durum olduğu düşünülmektedir. Elektromiyografi (EMG) ve kas biyopsisi normaldir. Uzamış febril miyalji altı haftayı bulabilen, non-steroid antiinflamatuar ilaçlara yanıt vermeyen nadir ama şiddetli bir tablodur. Kolşisinle tedaviye yanıt vermez. 1mg/kg’dan metil prednizolona hızlı yanıt verir. Hipergamaglobulinemi olması, vaskülitik döküntü ve nefrit ile birliktelik göstermesi patogenezde otoimmünitenin sorumlu olabileceği düşündürmektedir (58).
Ayrıca AAA’daki kas ağrı sebepleri arasında fibromiyalji ve kolşisin miyopatisi de sayılabilir (59). MEFV gen analizlerinde sıklıkla M694V homozigot
2.6.7 Vaskülit
Ailevi Akdeniz ateşi hastalarında Poliarteritis Nodoza (PAN), Henoch-Schönlein purpurası (HSP) gibi vaskülitler normal populasyondan daha sık görülmektedir (43). HSP en sık birliktelik gösteren vaskülit olup genel toplumda %0,8 iken AAA hastalarında ortalama %5-7 sıklıkta, PAN ise prevalansı genel toplumda %0,0006 iken AAA’da %1 sıklıkla görülebilmektedir (61).
Ailevi Akdeniz ateşi’nde vaskülitin patogenezi tam bilinmemekle birlikte immün kompleks mekanizması üzerinde durulmaktadır. Vaskülit tespit edilen hastaların %50’sinde dolaşan immün kompleksler olması, artmış kompleman tüketimi ve artmış immun globulin düzeyleri gösterilmiştir (62).
İsrail’de yapılan bir çalışmada çocuklarda HSP gelişmesinin önemli nedenleri arasında AAA’nın varlığı da gösterilmiştir (63). HSP kliniği çoğu zaman AAA kliniğinden daha önce başlar. İzole HSP’ye göre, AAA ile birlikte olan HSP daha erken yaşlarda başlama özelliğine sahiptir. Fakat vaskülitin seyri açısından anlamlı bir farklılık yoktur (64).
Poliarteritis Nodoza’da da ateş ve karın ağrısı kliniği vardır. Ailevi Akdeniz ateşiyle birlikte olan PAN vakaları özellikle genç yaştaki hastalarda sık görülür. Klasik PAN ise orta yaş (50-60 yaş) hastalığıdır (65).
Ailevi Akdeniz ateşi hastalığı ile Behçet Hastalığı (BH) arasındaki ilişki netleştirilememiştir. İkisi de anormal nötrofil aktivasyonunun görüldüğü kronik, tekrarlayıcı inflamatuar hastalıklardır (66). Kolşisin, mikrotubul fonksiyonlarını bozarak nötrofil kemotaksisi ve motilitesini baskılar ve her iki hastalığın da ilk tedavi basamağıdır (66).
2.6.8 Skrotal Tutulum
Ailevi Akdeniz ateşi’nde hastaların çok küçük bir yüzdesinde skrotal tutulum gözlenir. Genç erişkinlerde ve prepubertal dönemde daha sık görülmektedir. Hatta bu dönemde ilk bulgu olabilir. Çoğunlukla tek taraflı olur. Tunika vaginalisin inflamasyonu sonucu oluşur. Tek taraflı ağrı ve kızarıklık ile seyreden akut skrotum
tablosu şeklinde oluşur. Hastalarda giderek artan ağrı, ateş, skrotal şişme ve ödem gelişir (67).
Bu klinik bulgularla testis torsiyonu, bakteriyel epididimit ve orşit tablolarıyla karışabilir (68). Vakalarda sadece tunika vaginalis tutulduğu için testis sintigrafisi yapıldığında hipoperfüzyon gözlenmez ve torsiyondan bu şekilde ayırtedilir. Operasyon gerektirmeden kendiliğinden düzelir. Çok nadir olarak tekrarlayan akut skrotal ataklar sonucu hidrosel, kan damarlarında strangülasyon ile nekroz oluşumu ile orşiektomiye giden olgular bildirilmiştir (69).
2.6.9 İnfertilite
Kadın AAA hastalarında inflamasyona bağlı gelişen pelvik yapışıklıklar ve ataklar sonucunda gelişen düşükler kadın infertilitesini olumsuz etkilemektedir. Yapılan bir çalışmada tedavi verilmeyen 45 kadın AAA hastasından 15’inde ovülasyon disfonksiyonu ile beraber primer infertilite gözlenmiştir (70). Başka bir çalışmada ise uzun süre kolşisin tedavisi almış 36 kadında yapılan incelemede benzer sonuçlar alınmıştır (71).
Erkek AAA hastalarında ise tekrarlayan akut orşit atakları ve skrotal ödemin spermatogenez üzerine olumsuz etki yaptığı gösterilmiştir. Yapılan bir çalışmada testiküler amiloidozu olan hastalarda infertilite tespit edilmiştir. Kolşisin kullanımınında erkeklerde infertilite üzerinde etkili olabileceği öne sürülmüştür. Ancak yapılan çalışmalarda uzun dönem kolşisin alan 150 erkek hastadan sadece ikisinde oligospermi veya azospermi oluştuğu görülmüş ve bu sonuç diğer testiküler patolojilere bağlanmıştır (72).
2.6.10 Nörolojik Tutulum
Hastalar çoğu zaman ataklarla birlikte gelişen baş ağrısından şikayet ederler. Az sayıda olguda meninks irritasyon bulguları ve buna eşlik eden beyin omurilik sıvısında (BOS) protein ve hücre artışı bildirilmiştir (73). Birkaç vakada da Mollaret menenjiti (benign rekürren aseptik menenjit) bildirilmiştir. Nadiren santral sinir sisteminde demyelinizan hastalık ve inme görülebilir. Çok nadir olarak optik nörit,
amiloid oftalmoplejisi ve psödotümör serebri geliştiği de bildirilmiştir (74,75). Ayrıca febril konvülzyon ve EEG anormallikleri saptanan olgularda mevcuttur (76).
2.6.11 Splenomegali, Hepatomegali
Ailevi Akdeniz ateşi hastalarının %30-50’sinde amiloidozdan bağımsız olarak splenomegali görülebilir. İnflamasyona sekonder olarak gelişir. Nadiren amiloidoza bağlı gelişebilir. Çocuk hasta grubuyla yapılan bir çalışmada splenomegali %34, hepatomegali %3 oranında bulunmuştur (77).
2.7 Laboratuar Bulguları ve Radyoloji
Ailevi Akdeniz ateşi için spesifik bir labaratuar bulgusu yoktur. Ataklar sırasında sık rastlanılan bulgular lökositoz, periferik yaymada sola kayma, eritrosit sedimantasyon hızında (ESH) artış ve akut faz reaktanlarında (AFR) artıştır. Akut faz reaktanları, C-reaktif protein (CRP), Serum Amiloid A (SAA), fibrinojen, haptoglobulin, C3 ve C4’tür. Atak geçtikten sonra bu değerler normal seviyelerine iner (5). Atak döneminde trombosit ve ferritin düzeylerinde yükselme görülmez (44). Otoantikorlar (antinükleer antikor (ANA), romatoid faktör (RF), antikardiyolipin antikorlar (ACA), antinötrofil sitoplazmik antikorlar (ANCA)) negatif veya düşük titrelerde pozitif olabilir (78).
Interlökin (IL)-1, IL-6 ve Tümor Nekrozis Faktör alfa (TNF-α) atak dönemlerinde hastalarda yüksek saptanırken, IL-6’nın atak arası dönemlerde de kontrol grubundan yüksek olduğu gösterilmiştir. Bunun atak arası dönemlerde de devam eden subklinik inflamasyonun göstergesi olabileceği düşünülmüştür (79,80). Atak arası dönemlerde yüksek seyreden diğer bir belirteç SAA olup subklinik inflamasyonu göstermede en iyi gösterge olduğu sonucuna varılmıştır. Proinflamasyon sitokinleri olan IL-17 ve IL-18 düzeyleri de AAA atakları sırasında artmaktadır (81). Ailevi Akdeniz ateşi hastalarında İnterferon-gama (IFN-γ) düzeyi normal bireylere göre daha yüksektir, ayrıca AAA atakları süresince anlamlı derecede artmaktadır (82).
Hastada amiloidoz gelişmemiş ise idrar analizi çoğu zaman normaldir. Ataklar sırasında geçici albuminüri ve mikroskopik hematüri olabilmektedir. Amiloidoz
varsa proteinüri görülebilir ve nefrotik düzeylere ulaşabilir. Ailevi Akdeniz ateşinde diğer labaratuar bulguları ise sinovyal sıvıda beyaz küre artışı vardır, ancak herhangi bir mikrobiyal etken üremesi görülmez (79,83).
Ailevi Akdeniz ateşine özgü herhangi bir görüntüleme bulgusu yoktur. Karın ağrısı atağı ile gelen hastalarda çekilen direkt karın grafilerinde ince barsaklarda dilatasyon ve hava sıvı seviyeleri izlenebilir. Çekilen karın tomografisinde mezenterik damarlarda vazokonstrüksiyon, mezenterik veya retroperitoneal lenfadenopati, ince barsaklarda dilatasyon ve minimal asit gibi nonspesifik bulgular görülebilir. Akut atak sırasında yapılan laparoskopi ya da laparotomilerde ödematoz ve hiperemik peritonu görmek mümkündür. Peritoneal biyopside steril nonspesifik inflamasyon izlenir. Kronik atakları olan bir hastada ise fibröz adezyonlar görülebilir (52,84).
Plevrit atağı ile gelen hastalarda en önemli bulgu, çekilen postero-anterior akciğer grafisinde kostofrenik açıda küntleşmedir. Daha masif efüzyonlarda aynı tarafta atelektaziler görülebilir (52). Perikarditlerde ise en iyi bulgu veren teknik ekokardiyografidir. Akciğer grafilerinde kardiyotorasik oranda artış, EKG’de ST-T değişiklikleri görülür (52).
2.8 Tanı
MEFV geni 1997 yılında klonlandıktan sonra sadece genetik test yaparak AAA tanısının konulabileceği düşünülmüştür. Bir süre sonra sadece genetik analizlerle tanının konulamayacağı veya dışlanamayacağı anlaşılmıştır (85). Günümüzde AAA hastalığın tanısında klinik bulgular, aile öyküsü ve moleküler tarama birlikte kullanılmaktadır. Diğer herediter periyodik ateş sendromlarının dışlanması ve kolşisine yanıt doğrultusunda karar verilir (86). Özellikle akut atak dönemlerinde lökositoz, ESH ve AFR’de artış ile ataksız dönemlerde bu bulguların normale dönmesi, atakların kısa süre sonra kendiliğinden tam düzelmesi tanıda önemli yere sahiptir (86,87).
Günümüze kadar birçok tanı kriterleri oluşturulmuşsa da bunlar içinde en sık kullanılan Tell-Hashomer tanı kriterleridir (61) (Tablo 3). Tell-Hashomer tanı kriterlerinin yanı sıra Livneh ve arkadaşlarının sonradan düzenlediği tanısal kriterlerde geçerliliğini sürdürmektedir (85) (Tablo 4).
Tablo 3: Tel-Hashomer tanı kriterleri (61) Major kriterler
1. Peritonit, sinovit veya plevritin eşlik ettiği tekrarlayan ateş atakları 2. Predispozan hastalık olmadan AA tipi amiloidoz olması
3. Sürekli kolşisin tedavisine anlamlı yanıt Minör kriterler
1. Tekrarlayan ateşli ataklar 2. Erizipel benzeri eritem
3. Birinci derece akrabalarda AAA varlığı AAA: Ailevi Akdeniz ateşi
2 major kriter veya 1 majorle ile 2 minör kriter varlığında kesin tanı, 1 major ve 1 minör kriter varlığında olası tanı konulabilir.
Tanısal problemler atipik bulgularla gelen olgularda daha fazla yaşanmaktadır. Bu durumlarda genetik analiz tanıda önemli olabilmektedir. Son yıllarda yapılan çalışmalarda, nedeni bilinmeyen ateşli olgularda veya etiyolojisi belirlenememiş nefrotik sendromlu olgularda AAA genetik analizi önerilmektedir (88). Fakat MEFV mutasyon analizlerinin yapılması bile tam olarak problemi çözememektedir. Tipik klinik bulguları olan fakat mutasyon saptanmayan olgularda mevcuttur. Bu tarz hastalarda MEFV mutasyonu saptanmasa da, hastada tipik klinik bulgular mevcutsa kolşisin tedavisi başlanması ve tedaviye yanıtın izlenmesi önerilmektedir. Eğer hasta, kolşisin tedavisine yanıt verirse, tedavi kesilip atakların tekrar ortaya çıkıp çıkmayacağı gözlenir. Eğer hasta kolşisin tedavisine yanıt vermiyorsa, diğer periyodik ateş sendromları araştırılmalıdır (5,86).
Tablo 4: Livneh ve arkadaşlarının önerdiği yeni kriterler (85). Majör Kriterler
Tipik ataklar (≥3 kez tekrarlayan aynı karakterde atak geçirmesi, atak süresinin 12-72 saat
olması, atağın ateşli olması ve ateşin de rektal ≥38 ºC olması) 1. Yaygın peritonit
2. Plörit (tek taraflı) veya perikardit
3. Monoartrit tutulumu (kalça, diz, ayak bileği) 4. Yalnızca ateş
Minör Kriterler
1. *İnkomplet abdominal ataklar 2. *İnkomplet göğüs atakları 3. *İnkomplet artrit atakları
4. Egzersizle ortaya çıkan bacak ağrısı 5. Kolşisine iyi yanıt
*İnkomplet ataklar
1. Vücut ısısının <38ºC olması
2. Sürenin daha uzun veya kısa olması (6 saat-1 hafta) 3. Karın ağrısı sırasında peritoneal bulguların olmaması 4. Lokalize abdominal ataklar
5. Spesifik eklemlerin dışındaki eklemlerin tutulumu Destekleyici Kriterler
1. Ailesinde AAA bulunması 2. Etnik köken
3. Atakların 20 yaşından önce başlaması 4. Atağın ciddi yatak istirahatı gerektirmesi
6. Ataklar arası belirtilerin olmaması
7. Geçici inflamasyonu gösteren anormal test cevabı (lökositoz, ESH, fibrinojen, SAA artışı)
8. Tekrarlayan proteinüri ya da hematüri
9. Gereksiz laparotomi veya apendektomi öyküsü 10. Akraba evliliği
AAA: Ailevi Akdeniz ateşi, ESH: Eritrosit sedimentasyon hızı, SAA: Serum amiloid A. Kesin tanı: ≥1 majör kriter veya En az 2 minör kriter veya 1 minör kriter + ≥ 5 destekleyici kriter (+)
Bazı yazarlar tarafından klinik belirti, bulgular ve aile öyküsü genetik tanıya daha üstün kabul edilmektedir. Bu hastalara kolşisin tedavisi başlanmaktadır. Dolayısı ile AAA tanısı günümüzde hala klinik verilere dayanan bir tanıdır (54).
2.8.1 Genetik Olarak İlişkili Hastalıklar
Aşağıda görülen hastalıklarda MEFV gen mutasyonuna karşı genetik bir yatkınlık olabileceği düşünülmektedir:
Romatoid Artrit: Özellikle Glu148Gln mutasyonu olmak üzere, romatoid
artritin klinik bulgularından bağımsız olarak MEFV de gen mutasyonu tespit edilmiştir (89,90).
Behçet Hastalığı: Behçet Hastalıklı bireylerde MEFV gen mutasyonu
gösterilmiştir (91). Hatta Behçet hastalığı ile AAA hastalığı birlikteliği venöz tromboz için bir risk olduğu da tespit edilmiştir (92).
Ülseratif Kolit: Bu hastalarda MEFV gen mutasyonunun sıklığının arttığı
özellikle epizodik artriti olan hastalarda gösterilmiştir. Bu hastalık sürecinde MEFV’in değişik etkilerinin olabileceği öne sürülmüştür (93,94,95).
2.8.2 Ayırıcı Tanı
Ailevi Akdeniz ateşi hastalığının tanısında ekartasyon önemlidir. Hastalığın tutulum yerine göre ayırıcı tanıda düşünülmesi gereken hastalıklar Tablo 5’te özetlenmiştir (52).
Tanı koyarken tekrarlayan inflamasyon atakları ile karakterize nadir görülen genetik hastalıklar grubu olan ‘’Periyodik Ateş Sendromları’’ dışlanarak tanı koyulmalıdır. Bu sendromlar: Hiper IgD Sendromu (HIDS), TNF-Reseptörü ile Asosiye Periyodik Sendrom (TRAPS), Muckle-Wells Sendromu (MWS), Ailesel Soğuk Otoinflamatuar Sendrom (Familial Cold Autoinflammatory Syndrom: FCAS), Kronik İnfantil Nörolojik Kutanöz Artropati Sendromu (Chronic Infantile Neurologic Cutaneous Arthropaty: CINCA), Piyojenik Ateş-Piyojenik Steril Artrit-Piyoderma Gangrenozum-Akne Sendromu (PAPA), Periyodik Ateş-Aftöz Stomatit-Farenjit-Adenopati (Periodic Fever, Aphtous Stomatitis, Pharyngitis, Adenopathy: PFAPA) olarak sayılabilir (2,96,97).
Tablo 5: Ailevi Akdeniz ateşi ataklarında ayırıcı tanı (52)
Febril ataklar Göğüs ağrısı atakları Skrotal atak Monoartrit PFAPA HIDS Crohn hastalığı Alerjik reaksiyon Siklik nötropeni Hodgkin lenfoma Nonhodgkin Lnf. Malarya Relapsing fever İnfeksiyoz plevroperikardit Otoimmün plöroperikardit Rekürren benign perikardit Plevropnomoni Rekürren pulmoner emboli Testis torsiyonu Epididimit Orşit Behçet hastalığı Gut / psödogut Palendromik romatizma Behcet Hastalığı Rekürren aftoz stomatit Rekürren artropati Spondiloartropati Juvenil kronik artrit İntermitant hidroartroz Münchausen’ sendromu
PFAPA: Periyodik Ateş, Aftöz Stomatit ve Adenopati, HIDS: Hiperimmünoglobulin D Sendromu
PFAPA (Periyodik Ateş, Aftöz Stomatit, Farenjit ve Adenopati Sendromu): Sıklıkla AAA’nın ateş ataklarından ayırt edilemez. Doğru tanı için
MEFV gen mutasyon analizi gerekebilir. Tedavide steroid etkilidir (97,98).
HIDS (Hiperimmünoglobulin D ve Periyodik Ateş Sendromu): Ateş
Ateş ve karın ağrısı atakları AAA’da olanlardan ayırt edilemez. Doğru tanı kolşisin etkinliği ve moleküler gen analiz testleri ile konur (97,98).
TRAPS (Tümör Nekroz Faktör (TNF) Reseptörü İlişkili Periyodik Sendrom): TNFR SF1A genindeki mutasyon sebebiyle oluşan otozomal dominant
kalıtımlı bir hastalıktır. Diğer adı Ailesel Hibernian ateşidir. Kliniğinde ateş, steril peritonit, eklem ağrısı, kas ağrısı, deri döküntüleri ve konjonktivit atakları vardır. Bazen amiloidozda gelişmektedir. Rekombinant TNF- reseptör analogları tedavide kullanılır. Ailevi Akdeniz ateşi’ne benzer klinik tablolar olabilmektedir. Ayırımda kalıtım şekli ve moleküler testler yardımcıdır (99).
ELA2 bağlı nötropeni: Konjenital ve tekrarlayan (döngüsel) nötropeniyi
içeren otozomal dominant kalıtımlı bir hastalıktır. Tekrarlayan ateş, deri ve orofarengeal inflamasyon, servikal lenfadenopati ile karakterizedir.
Konjenital nötropenili hastalarda ilk bir yaştan itibaren ishal, pnömoni, karaciğer, akciğer ve cilt altı dokularda derin apse gelişimi yaygındır. Bu hastalarda miyelodisplastik sendrom (MDS) ve akut miyeloid lösemi (AML) gelişme riski vardır (99).
Döngüsel nötropenide ise sellülit, özellikle perianal bölgede sellülit, nötropenik dönemde sık görülür. Nötropenik peryotlar arasında genellikle sorun yoktur ve belirtiler yetişkin dönemde artış gösterir. Lökosit elastazı kodlayan ELA2 geninin moleküler genetik testi klinik tanıda kullanılır (99).
Muckle-Wells Sendromu ve Ailevi Soğuk Ürtiker: Otozomal dominant
geçişli, CIAS1 genindeki mutasyon sonucu oluşan allelik bozukluklardır. Ürtiker, sağırlık ve renal amiloidoz ile karakterizedirler (99).
Tablo 6: Kalıtsal Otoinflamatuar Hastalıklar (99)
AAA HİDS TRAPS PAPA ASİS MWS CİNCA
Etnik Köken Türkler, Yahudile r Ermenile r Araplar Hollanda, Diğer Batı Avrupa İrlanda, İskoçya Kökenli Yok Kuzey Avrupa Kuzey Avrupa Yok Katılım Şekli OR OR OD OD OD OD OD Gen MEFV MVK TNFRSF1 A PSTPIP1 CIAS1/ NALP3 CIAS1/ NALP3 CIAS1/ NALP3 Etkin protein Pirin Mevalonat Kinaz TNF Reseptör
PSTPIP1 Kryopirin Kryopirin Kryopirin
Klinik Bulgu Yineleyen Ateş ve Poliserözi t atakları Yineleyen Ateş, Karın Ağrısı, Servikal LAP Yineleyen Ateş, Miyaliji, Döküntü, Karın Ağrısı Yineleyen Pyojenik Artrit ve Pyoderma Gangrenozu m Akne Soğuk İlişkili Ürtiker Atakları Ürtiker Atakları, Sensorinöra l İşitme Kaybı Kronik Menenjit , Artropati , Döküntü, Zeka Geriliği Atak 1-3 gün 3-7 gün >7 Gün Değişken < 24 Saat 1-2 gün Ataklarla Birlikte
idoz bilir nadir bilir Tedavi Kolşisin Statinler, Steroidler, TNF antagonist ler Nadiren Steroidler, TNF antagonist leri Steroidler TNF ve IL-1 antagonist leri Soğukta n Korunm a ve IL-1 antagon istler Steroidler, TNF antagonist leri Steroidle rTNF antagonis tler
AAA: Ailevi Akdeniz ateşi, HİDS: Hiperimmünglobülin D sendromu, TRAPS: Tümör nekrozis faktör reseptörü ilişkili periyodik sendrom, PAPA: Piyojenik artrit, piyoderma gangrenosum, akne ilişkili sendrom, ASİS: Ailesel soğuk ilişkili sendrom, MWS: Muckle-Wells sendromu, CİNCA: Kronik infantil nörolojik kutanöz artropati, OD: Otozomal dominant, OR: Otozomal resesif. TNF: Tümör nekrozis faktör, LAP: lenfadenopati
2.9 Amiloidoz
Ailevi Akdeniz ateşi hastalığının en önemli ve en korkulan komplikasyonu olan amiloidoz, ilk defa 1955 yılında amiloid nefropatisi modeli ile asemptomatik, proteinürik, nefrotik, azotemik, üremik evreler olmak üzere beş evre halinde rapor edilmiştir (100).
Amiloidoz, belli organlarda amiloid fibrillerinin ekstrasellüler olarak depolanması ile karakterize bir hastalıktır. Tüberkülozdan sonra en çok AAA hastalığında görülür (101). Amiloidozun birçok tipi olmasına rağmen en çok AL ve AA tipi amiloidoz görülür. Etiyolojisi multifaktöriyel olup primer (AL) ve sekonder (AA) (reaktif) tipleri tanımlanmıştır (102). Ailevi Akdeniz ateşi’nde sekonder (AA) tip amiloid birikimi sık görülür. AA proteini, karaciğerde sentezlenen yüksek dansiteli bir lipoproteinin bileşiğidir. Bir akut faz reaktanı olan serum amiloid A öncül proteininin parçalanması sonucu oluşur. Özellikle IL-1 ile ilişkili olan serum amiloid A, amiloid fibrillerin C-Terminal kısmına polimerizasyonu sonucu AA proteine dönüşür (103).
En fazla böbreklerde progresif olarak depolanan amiloidin en sık oluşturduğu klinik tablo nefrotik sendromdur. Son dönem böbrek yetersizliğine kadar
ilerleyebilen progresif nefropati ile karakterizedir. Hastalar genellikle normal tansiyona sahiptir ve hematüri gözlenmez (102). Hastaların mutlaka düzenli aralıklarla idrar tetkiki yaptırması gerekmektedir. Çünkü AAA’da amiloidoz gelişiminin erken dönemlerinde idrarda proteinüri görülmektedir. Ailevi Akdeniz ateşi olan hastalarda, hematürik bir idrar olmaksızın, sürekli proteinürinin varlığı amiloidozu düşündürmelidir. Ailevi Akdeniz ateşi olan 35 çocuk hastanın değerlendirildiği bir çalışmada proteinürinin, yaygın sistemik amiloidoz varlığının tek belirtisi olduğu ve proteinüri sonrası 5 yıllık sağ kalım oranının %20 olduğu bildirilmiştir (104).
Amiloidoz birikimi böbreklerin dışında gastrointestinal sistemde (malabsorpsiyon, diyare), karaciğerde (karaciğer enzim yüksekliği, hepatomegali, portal hipertansiyon), dalakta (splenomegali), kalpte (restriktif kardiomyopati, EKG bulguları, konjestif kalp yetmezliği, aritmi), tiroidte (hipotiroidi), sürrenal bezlerde (adrenal yetmezlik) ve testislerde fibriler proteinlerin depolanması gözlenebilir (100).
Amiloidoz, AAA’nın kliniğinde iki farklı şekilde ortaya çıkar:
Fenotip I. Klasik ataklarla seyreden klinik tablo ile birlikte amiloidoz vardır.
Fenotip II. Ailevi Akdeniz ateşi klinik bulguları olmadan ve amiloidozu açıklayacak
bir tablo olmadan hastada doğrudan amiloidoz vardır.
Hiçbir atak görülmeden, AAA kliniği oluşmadan renal komplikasyonların ortaya çıktığı Fenotip II olarak adlandırılan ve serozit nöbetlerinin eşlik etmediği bu tablonun AAA hastaları içinde insidansı %7 ile %25 arasında olduğu bildirilmiştir. Bazı verilerde ise hiç fenotip II hastasına rastlanmamıştır (105).
Amiloidoz oluşumunda her ne kadar inflamatuar cevap sorumlu olarak gösterilse de son yıllarda yapılan araştırmalar, AAA kliniği olmaksızın saptanan amiloidoz olguları(Fenotip 2), amiloidoz gelişiminin etiyopatogenezinde başka nedenlerin olduğunu düşündürmüştür. Bunlar arasında etnik köken, spesifik MEFV gen mutasyonu (özellikle M694V), ailede amiloidoz öyküsü, hastalığın şiddeti ve erkek cinsiyetin önemli rol oynadığı gösterilmiştir (105,106).
Uluslararası AAA Birliği, V726A gen mutasyonunun olduğu AAA hastalarında klinik şiddetin daha düşük olduğu ve amiloidozun daha az geliştiğini ve bu mutasyonun sıklıkla bulunduğu Ashkenazi Yahudileri, Dürziler ve Ermeniler’de amiloidoz gelişiminin az olmasından sorumlu olduğu öne sürülmüştür (107,108). Ancak V726A gen mutasyonunu homozigot veya birleşik heterozigot olarak taşıyan hastalarda da amiloidoz geliştiği bildirilmiştir (108). Amiloidozu olan Ashkenazi dışı Yahudi AAA hastalarında ise en yüksek MEFV gen mutasyon sıklığını Livneh ve ark. yaptıkları çalışmada 30 AAA’lı ve amiloidozlu hastanın değerlendirilmesiyle bunlardan 29 hastanın M694V homozigot mutasyon taşıdığını göstermiştir (108,109). Shohat ve ark. (110) Kuzey Afrika Yahudileri, Türkler ve Ermenilerden oluşan hasta grubunda M694V gen mutasyonunu homozigot olarak taşıyan 87 hastadan 18’inde (%21) amiloidoz olduğunu bildirmiştir.
Ailevi Akdeniz ateşinde kolşisin tedavisi kullanılmadan önce hastalarda amiloidoz gelişme ihtimali %60 iken, kolşisin tedavisi sonrası, düzenli tedavi alanlarda amiloidoz gelişme riski %5’ten az olarak bildirilmiştir. Buda kolşisinin amiloidoz gelişimini açık bir şekilde engellediğini göstermiştir (87,100).
Amiloidozda tanı doku biyopsisiyle konur. En fazla biyopsi yapılan yer böbreklerdir. Alternatif olarak rektal biyopsi ile de %70-80 oranında tanı konur. Ayrıca kemik iliği, subkutan yağ dokusu biyopsi alınabilecek diğer yerler arasındadır (85).
2.10 Şiddet skorlaması
Ailevi Akdeniz ateşi hastalığının şiddetinin değerlendirilmesinde günümüzde en fazla kullanılan skorlama sistemi Pras ve arkadaşlarının yaptığı skorlama sistemidir. Bu skorlama sisteminde hastalığın başlangıç yaşı, aylık atak sayısı, artritin akut ya da uzamış olma durumu, erizipel benzeri eritemin olup olmadığı, amiloidoz gelişip gelişmediği ve kullandığı kolşisin dozuna göre hastalar puanlandırılmakta ve bu puanlamaya göre hastalık şiddeti hafif, orta ve ağır şiddet olarak sınıflandırılmaktadır. Puanlamanın sayısal karşılığı ise 3-5 puan: hafif, 6-8 puan: orta, 9 ve üzeri puan: ağır olarak değerlendirilmektedir (26,111,112).
2.11 Tedavi
Kolşisin, Colchicum autumnale (acı çiğdem) ve Gloriosa superba (glory lily) İsimli bitkilerinden elde edilen nötral, lipofilik bir alkaloiddir. Akut gut artritinde uzun süredir kullanılmaktadır. Bunun dışında primer biliyer siroz, psöriazis, palmoplantar püstülozis ve birçok hastalığın tedavisinde de kullanılmaktadır (13,15,113).
İlk kez 1972’de Goldfinger tarafından AAA tedavisinde kolşisin kullanılmaya başlanmıştır (13). Ailevi Akdeniz ateşi hastalığında hem atakların sıklığını ve şiddetini azaltması, hem de hastalığın en önemli komplikasyonu olan amiloidoz gelişimini engellemesi açısından kolşisin, AAA tedavisinin temel taşı olmuştur (48,114).
Kolşisinin etki mekanizması intrasellüler mikrotübülleri etkileyerek lökosit adhezyon ve kemotaksisini bozar (115). Kolşisin 3 proteinle etkileşime girer;
Tubulin (α ve β-tubulin), hücrelerde bol miktarda bulunan ve birleşerek
mikrotübülleri oluşturan bir proteindir. Kolşisin, tubulin moleküllerine bağlanır ve mikrotübüllerin uzamasını engeller. Bu şekilde hücre iskeletinin yapısını bozar ve antimitotik etki ile birlikte sinyal iletim yollarını etkileyerek antiinflamatuar etki gösterir (115,116).
Sitokrom P450 3A4 (CYP3A4), kolşisin ve başka birçok ilacın
metabolizmasından sorumludur. CYP3A4 substratı veya inhibitörü olan diğer ilaçlarla birlikte kolşisin kullanılırsa, bu ilaçlar kolşisinin vücuttan atılımını azaltarak kolşisin toksisitesine sebep olabilir (117).
P-gp proteini, ATP bağımlı bir fosfoglikoproteindir. Hücre zarında bulunur.
Kolşisinde dahil birçok ilacın hücre dışına atılmasını sağlar. İlaç direncinden sorumludur (115,116,117).
Kolşisinin antiinflamatuar, antiamiloid, antimitotik, apoptotik etkilerinin yanı sıra, antifibrotik etkinliği de vardır. Kollajen sentezini inhibe edip kollajenaz