T.C.
EGE ÜNİVERSİTESİ
TIP FAKÜLTESİ
RADYOLOJİ ANABİLİM DALI
GASTROİNTESTİNAL DUVAR
KALINLAŞMALARINDA DUAL ENERJİ BT
İNCELEMENİN TANISAL KATKISI
Dr. İbrahim Emre ATASOY
DANIŞMAN:
Prof. Dr. Z. Nevra ELMAS
UZMANLIK TEZİ
İZMİR 2014
ÖZET
AMAÇ: Çalışmamızın amacı farklı keV değerlerinde elde olunan dual-enerji BT
görüntülerinde ve iyot haritalamasında saptanan iyot konsantrasyon değerlerinin
karşılaştırılarak gastrointestinal sistemde duvar kalınlık artışına neden olan patolojilerin benign-malign ayrımında ve kanser tespitinde dual-enerji BT’nin etkinliği ve tanısal katkısını araştırmaktır.
GEREÇ ve YÖNTEM: Nisan 2013-Ağustos 2013 tarihleri arasında abdominal BT
incelemesinin rutin portal faz görüntüleri Dual-enerji BT tekniği ile elde olunan ve radyolojik değerlendirme sonucunda gastrointestinal sistemde duvar kalınlaşması saptanan 196 hasta (216 lezyon) çalışmaya dahil edildi.
BT görüntüleri, dual enerji yöntemiyle 64-kesitli tek tüplü ÇKBT (Discovery 750 HD, GE Healthcare; Milwaukee, Wisconsin, ABD) kullanılarak elde edildi. Alınan görüntüler AW Gemstone Spectral Imaging (GSI) Viewer iş istasyonuna gönderildi ve dual-enerji programı kullanılarak, 40keV, 70keV, 140keV görüntüler ve iyot perfüzyon haritası elde edildikten sonra duvar kalınlaşmasının belirgin olduğu kesitte 40keV, 70 kev, 140 keV ve iyot haritası görüntülerinin her birinden 2x2 mm boyutta standart dairesel ROI
kullanılarak ölçümler yapıldı. İstatistiksel analizde, ROC eğrisi analizi ve Mann-Whithney U testi kullanıldı.
BULGULAR: Hastaların ortalama yaşı 61.4±16.6 yıldı. Mide yerleşimli lezyonların
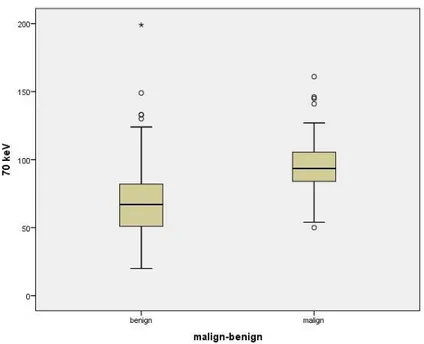
%49.3’ü benign, %50.7’si malign; ince barsak yerleşimli lezyonların %88.5’i benign, %11.5’i malign; kolon yerleşimli lezyonların ise %56.9’u benign, %43.1’i malign idi. Benign lezyonların 40 keV, 70 keV, 140 keV ve iyot perfüzyon haritası görüntülerdeki ortalama iyot konsantrasyon değerleri sırasıyla 166.7 HU, 69.6 HU, 38.7 HU, 16.5 mg/ml bulundu. Malign lezyonların ise 40 keV, 70 keV, 140 keV ve iyot perfüzyon haritası görüntülerdeki ortalama iyot konsantrasyon değerleri sırasıyla 247.3 HU, 95.7 HU, 47 HU, 25.4 mg/ml bulundu. Maligniteyi öngörmede 40 keV, 70 keV, 140 keV ve iyot perfüzyon haritasında sırasıyla sensitivite %83.8, %80, %65, %81.3; spesifite %75, %73, %60, %%74.3 bulundu.
SONUÇ: Dual enerji BT incelemesinde keV değerleri düştükçe iyot atenüasyonunda
belirginleşme olmakta ve bu duruma bağlı olarak yüksek derece iyot perfüzyonu gösteren neoplazik lezyonların HU değerleri belirginleşmektedir. Ayrıca iki materyal
dekompozisyon tekniği ile iyot perfüzyonu değerlendirildiğinde malign lezyonların benign lezyonlara kıyasla anlamlı ölçüde daha fazla perfüzyon gösterdiği anlaşılmaktadır.
ABSTRACT
The aim of our study is to evaluate malignancy potential of gastrointestinal system wall thickening by obtaining HU and iodine concentration values on different keV and iodine perfusion images.
Materials and methods: 196 patients (216 lesions) were included in this study. Portal
phase images of the patients were taken with GSI protocol. All patients had gastrointestinal system wall thickening.
CT images were obtained with single source dual energy MDCT (Discovery 750 HD, GE Healthcare; Milwaukee, Wisconsin, ABD). Images were evaluated in AW gemstone spectral imaging Workstation. Hounsfield unit values were obtained on 40, 70, 140 keV images. Iodine concentration values obtained on iodine perfusion images. Values were obtained using 2x2 mm ROI. ROC curve and mann-whitney U test were used in statistical analysis.
Findings: Mean age of patients was 61.4±16.6. %50.7 of gastric lesions were malignant.
%11.5 of small bowel lesions were malignant. %43.1 of colon lesions were malignant. 40 keV, 70 keV, 140 keV HU and iodine concentration values of benign lesions were 166.7, 69.6, 38.7 and 16.5 , respectively. 40 keV, 70 keV, 140 keV and iodine concentration values of malign lesions were 247.3, 95.7, 47 and 25.4 respectively. The sensitivity and specifity of 40 keV, 70 keV, 140 keV and iodine perfusion images in differentiating malign lesions were %83.8, %80, %65, %81.3; %75, %73, %60, %74.3 respectively.
Results: In two-material decomposition technique malignant lesions showed significantly
higher iodine perfusion compared to benign lesions. Attenuation of malign lesions becomes apparent in low keV values.
İÇİNDEKİLER ÖZET ABSTRACT İÇİNDEKİLER SİMGELER ve KISALTMALAR ŞEKİLLER RESİMLER TABLOLAR GRAFİKLER GİRİŞ 1.1. Çalışmanın Amacı GENEL BİLGİLER ve KAVRAMLAR
. 2.1. Mide Anatomisi
. 2.2. Midenin Prekanseröz lezyonları ve Mide Kanseri 2.2.1 Midenin Prekanseröz Lezyonları
2.2.2 Mide Kanseri
2.2.2.1 İnsidans 2.2.2.2 Etyoloji
2.2.2.3 Histopatoloji
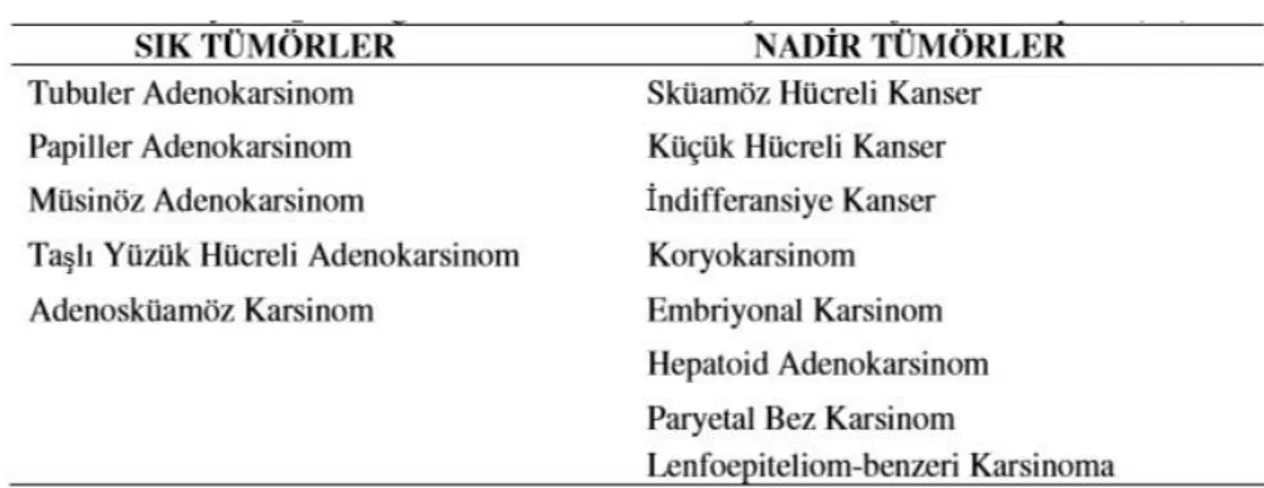
2.2.2.4 Mide Kanserinin Yayılım Şekilleri 2.2.2.5 Mide Kanserinde Evrelendirme 2.2.2.6 Diğer Mide Tümörleri
2.2.2.7 Mide hastalıklarının Tanısında Görüntüleme . 3.1. İnce barsak Anatomisi
. 3.2. İnce Barsak Patolojileri
3.2.1.1 Spesifik İnflamatuar Patolojiler
3.2.1.2 Nonspesifik İnflamatuar Patolojiler
3.2.2 Malabsorbsiyon
3.2.2 İnce Barsak Tümörleri 3.2.2.1 Benign Tümörler
3.2.2.2 Malign Tümörler 3.2.3 İnce Barsak Hastalıklarının Tanısında Görüntüleme
4.1. Kolon Anatomisi 4.2. Kolon Patolojileri
4.2.1 Kolonun Enflamatuar Hastalıkları 4.2.1.1 Kolonun Enfeksiyöz Hastalıkları
4.2.1.2 İdiyopatik Enflamatuar Barsak Hastalıkları
4.2.2 Kolon Polipleri ve Kolon Kanserleri
4.2.2.1 Kolon Polipleri 4.2.2.1.1 Adenomatöz Polipler 4.2.2.1.2 Juvenil Polipler 4.2.2.1.3 İnflamatuar Polipler 4.2.2.1.4 Hiperplastik Polipler 4.2.2.2 Kolon Kanserleri 4.2.2.2.1 Patoloji 4.2.2.2.2 Kolon Kanserlerinde Yayılım Şekilleri 4.2.2.2.3 Kolon Kanserlerinde Evrelendirme 4.2.2.2.4 Kolon Hastalıklarının Tanısında Görüntüleme . 5.1. Dual-enerji Bilgisayarlı Tomografi Fiziği
6. GEREÇ ve YÖNTEM 7. BULGULAR 8. OLGU ÖRNEKLERİ
9. TARTIŞMA ve SONUÇ 10. KAYNAKLAR
SİMGELER VE KISALTMALAR
2B İki boyutlu
3B Üç boyutlu
BT Bilgisayarlı tomografi
ca Kanser
ÇKBT Çok kesitli bilgisayarlı tomografi
DEBT Dual enerji bilgisayarlı tomografi
DLP “Dose length product”
FOV “Field of view”
GSI “Gemstone Spectral Imaging” HU Hounsfield ünitesi
iv İntravenöz
keV Kiloelektron volt
kV Kilo volt
mA Miliamper
MPR Multiplanar rekonstrüksiyon
mSv MiliSievert
PET-BT Pozitron emisyon tomografi – Bilgisayarlı tomografi
ROI “Region of interest”
SSD “Shaded Surface display”
tm Tümör
VNC Sanal kontrastsız, “Virtual noncontrast”
ŞEKİLLER
Şekil 2.1 Mide anatomisi
Şekil 2.2 Mide kanlanmasının MR Anjiografi görüntüsü
Şekil 2.3 Perigastrik lenf nodu istasyonları
RESİMLER
Resim 8.1. Sigmoid kolonda duvar kalınlaşması bulunan ve patolojik tanısı adenokarsinom olan olguda, iyot atenüasyon ölçümleri sırasıyla 40keV, 70keV, 140 keV ve iyot haritası değerleri; 208.7HU, 107.2HU, 41.5HU, 33.6mg/ml bulundu.
Resim 8.2. İleumda duvar kalınlaşması saptanan ve patolojik tanısı NET olan olguda, iyot atenüasyon ölçümleri sırasıyla 40keV, 70keV, 140 keV ve iyot haritası değerleri; 456.2HU, 150.8HU, 26.7HU, 55.2mg/ml bulundu.
Resim 8.3. İnce barsaklarda uzun segment duvar kalınlaşması saptanan olguda operasyon sonrası rezeksiyon materyali iskemik değişiklikler ve nekroz tanısı almış olup, iyot atenüasyon ölçümleri sırasıyla 40keV, 70keV, 140 keV ve iyot haritası değerleri; 105.1HU, 48.8HU, 31.4HU, 9.5mg/ml bulundu.
Resim 8.4. Opere mide adenokarsinomlu olguda anastomoz hattında barsak duvar kalınlığı olan alandan yapılan iyot atenüasyon ölçümleri sırasıyla 40keV, 70keV, 140 keV ve iyot haritası değerleri; 138.4HU, 58.5HU, 31.8HU, 13.4mg/ml bulundu. Bu bölgenin takiplerde regrese olduğu izlendi.
Resim 8.5. Anti-koagülan kullanımına bağlı intramural hematom saptanan olguda, iyot atenüasyon ölçümleri sırasıyla 40keV, 70keV, 140 keV ve iyot haritası değerleri; 185.7HU, 82.7HU, 44.7HU, 17.7mg/ml bulundu.
Resim 8.6. İnce barsakta duvar kalınlaşması saptanan ve patolojik tanısı desmoid tip ince barsak fibromatozisi olan olguda, iyot atenüasyon ölçümleri sırasıyla 40keV, 70keV, 140 keV ve iyot haritası değerleri; 162.7HU, 57.3HU, 26.1HU, 17.5mg/ml bulundu.
Resim 8.7. Transvers kolonda duvar kalınlaşması saptanan ve patolojik tanısı villöz adenoma zemininde gelişmiş adenokarsinom olguda, iyot atenüasyon ölçümleri sırasıyla 40keV, 70keV, 140 keV ve iyot haritası değerleri; 202.5HU, 85.6HU, 47.3HU, 20.2mg/ml bulundu.
Resim 8.8. Yalancı (+) olgu örneği. Aktif evre Chron hastalığı tanılı olguda, iyot atenüasyon ölçümleri sırasıyla 40keV, 70keV, 140 keV ve iyot haritası değerleri; 279.5HU, 105.3HU, 45.0HU, 29.8mg/ml bulundu.
Resim 8.9. Aktif ekstravazasyon ve intamural-intralüminal hematom saptanan olguda, iyot atenüasyon ölçümleri sırasıyla 40keV, 70keV, 140 keV ve iyot haritası değerleri; aktif ekstravazasyon için 99.6HU, 82.8HU, 78.5HU, 3.1mg/ml; intramural-intralüminal hematom için 390.7HU, 151.2HU, 67.2HU, 69mg/ml bulundu.
Resim 8.10. Kolonda diffüz duvar kalınlaşması saptanan ve patolojik olarak ilaç kullanımına bağlı olabilecek kolonda yangısal reaksiyon tanısı alan olguda, iyot atenüasyon ölçümleri sırasıyla 40keV, 70keV, 140 keV ve iyot haritası değerleri; 166.1HU, 67.3HU, 37.5HU, 17.0mg/ml bulundu. Resim 8.11. Psödotümöral lezyon olgusu. Barsak rezeksiyon uygulanmış olan olguda patolojisi kolon perforasyonu, serozal reaksiyon, yangısal bulgular, yağ nekrozu ve kanama alanları içeren psödotümöral oluşum şeklinde raporlandı. Yapılan ölçümlerde, iyot atenüasyon ölçümleri sırasıyla 40keV, 70keV, 140 keV ve iyot haritası değerleri; 143.2HU, 56.1HU, 16.5HU, 16.1mg/ml bulundu.
Tablo 2.1 Mide kanserinde Lauren sınıflaması
Tablo 2.2 Dünya Sağlık Örgütü’nün Mide kanseri için histolojik tümör tipleri
Tablo 2.3 Mide kanseri evre grupları
Tablo 7.1 Lezyonların dual-enerji ölçüm değerleri ortalaması
1.1 Çalışmanın Amacı
Gastrointestinal sistem kanserleri dünya genelinde yaygın olarak görülmektedir. Ülkemizde Sağlık Bakanlığı Kanser Savaş Dairesi tarafından bildirilen verilere göre erkeklerde solunum sistemi kanserlerinden sonra gastrointestinal sistem kanserleri ikinci sırada gelmektedir. Kadınlarda ise gastrointestinal sistem kanserleri; meme, ürogenital sistem ve solunum sistemi kanserlerinden sonra dördüncü sırada yer almaktadır. Gastrointestinal sistem kanserleri içinde mide kanserleri birinci sıradadır (1-3). İnce barsak maligniteleri ise oldukça nadir görülmekte olup gastointestinal sistem malignitelerinin sadece %1-2’sini oluşturmaktadır (4). Kolorektal kanserler gelişmiş ülkelerde ciddi morbidite ve mortaliteye yol açmaktadır. Amerika Birleşik Devletleri’nde en sık görülen üçüncü kanserdir ve kansere bağlı ölümlerde ikinci sırayı almaktadır. Avrupa’da kansere bağlı ölümlerde ikinci sıradadır (5,6).
Görüntüleme yöntemleri ile saptanan duvar kalınlık artışı gastrointestinal hastalıkların en önemli bulgularından biridir. Duvar kalınlık artışı normalin varyantı, benign gastrik ülser, gastrik karsinom, mideye invaze pankreas karsinomu, duodenal leomiyom, radyasyon enteriti, peritonit, kolonik karsinom, invajinasyon, divertikülit, enflamatuar barsak hastalığı, lenfoma gibi birçok sebebe bağlı olabilir (7). Gastrointestinal sistemde saptanan duvar kalınlık artışının geniş bir tanı spektrumuna sahip olması nedeniyle lezyonların özellikle benign-malign ayrımı tanısal anlamda önem taşımaktadır. ÇKBT, gastrointestinal sistemin duvar kalınlığının değerlendirilmesi açısından etkili bir görüntüleme yöntemidir. Duvar invazyonunun derecesi, komşu organlara invazyon, lenf nodu tutulumu ve uzak metastazları gösterebilmesi açısından preoperatif görüntüleme yöntemi olarak BT sık kullanılan görüntüleme yöntemidir (8). Dual enerji BT, ÇKBT’nin sağladığı avantajlar yanı sıra, iki veya üç materyal dekompozisyon tekniği ile mg/ml cinsinden iyot konsantrasyon değerini ölçerek dokunun iyot perfüzyonunu gösterebilmekte ve lezyonun kontrastlanma paterni hakkında fikir verebilmektedir (9-13).
Çalışmamızın amacı farklı keV değerlerinde elde olunan dual-enerji BT görüntülerinde ve iyot haritalamasında saptanan iyot konsantrasyon değerlerinin
karşılaştırılarak gastrointestinal sistemde duvar kalınlık artışına neden olan patolojilerin benign-malign ayrımında ve kanser tespitinde dual-enerji BT’nin etkinliği ve tanısal katkısını araştırmaktır.
GENEL BİLGİLER ve KAVRAMLAR 2.1. Mide Anatomisi
Sindirim borusunun (canalis alimentarius) en geniş kısmı olan mide karın boşluğunun sol üst kadranında yerleşmiş J şeklinde bir organdır. Özefagus ile duodenum arasında yerleşmiştir. Mide karın boşluğunun yukarı kısmında, diafragmanın altında, transvers kolon ve transvers mezokolonun üzerinde bulunur (14, 15). Mide; kardiya, fundus, korpus, antrum ve pilor olmak üzere beş bölgeye ayrılır. Kardiya; özofagus ile midenin birleşme yeridir. Fundus; kardiyanın solu ve üst kısmında kalan midenin en üst kısmıdır. Korpus; fundus ile incisura angularisden (midenin 1/3 alt ve orta kısmının birleştiği çentik) geçen yatay hat arasında kalan bölgedir. Bu yatay hat ile pilor arasında kalan bölüm antrumdur. Mideden duodenuma geçiş bölgesi ise pilordur (Şekil 2.1) (16).
Şekil 2.1. Mide anatomisi
Mide, yukarıda alt özofagiyal sfinkter, aşağıda ise pilor sfinkteri olmak üzere iki sfinkter ile kontrol altına alınmıştır. Alt özofagiyal sfinkter, kardiyanın hemen üzerindeki yüksek basınç bölgesinden oluşan gerçek bir sfinkter mekanizmasına sahiptir. Dinlenme halinde iken kapalıdır. Yukarıdan peristaltik dalga geldiği zaman açılarak, yutulan gıda veya salgının mideye girmesine izin verir. Yüksek basınç bölgesi, hem yutma hem dinlenme esnasında mide içeriğinin özofagusa kaçışını önler. Pilorik sfinkter, gerçek bir sfinkter olmadığı halde tam bir sfinkter gibi çalışır. Pilor bölgesindeki düz kas adalesinin
yoğunlaşması ile oluşmuştur. Pilor hem midenin boşalmasını düzenler hem de duodenumdaki içeriğin mideye kaçışını önler (16).
Midenin Arterleri Mide arterleriyel kanlanmasını 5 ana kaynaktan alır (Şekil 2.2)
(17).
1) Sol Gastrik Arter; trunkus çöliakusun bir dalı olup küçük kurvaturun üst kısmını kanlandırır,
2) Sağ Gastrik Arter; ana hepatik arterin dalı olup küçük kurvaturun kaudal kısmını besler,
3) Sağ Gastroepiploik Arter; gastroduodenal arterin dalı olup antrum ve alt gövdeyi besler,
4) Sol Gastroepiploik Arter; splenik arterin dalı olup üst gövdeyi besler,
5) Kısa Gastrik Arterler; splenik arterin dalları olup midenin fundusunu kanlandırır.
Midenin Venleri Midenin venleri genellikle arterlerine eşlik eder.
1) Sol Gastrik Ven; genellikle portal vene, bazen superior mezenterik vene dökülür,
2) Sağ Gastrik Ven; genellikle portal vene, bazen superior mezenterik vene dökülür,
3) Sağ Gastroepiploik Ven; genelde superiyor mezenterik vene dökülür,
4) Sol Gastroepiploik Ven,
Şekil 2.2. Mide kanlanmasının MR Anjiografi görüntüsü
Midenin Lenfatik Drenajı Midenin lenf damarları büyük ve küçük kurvatür
boyunca arterlerine eşlik eder. Sol gastrik lenf nodu grubu (10-20 adet) küçük kurvaturun arka üst kısmında sol gastrik arter düzeyinde yerleşiktir. Suprapilorik grup küçük kurvaturun en alt kısmında sağ gastrik arter düzeyinde (3-6 adet) yerleşiktir. Pankreatikosplenik grup (3-5 adet) fundus ve üst gövdenin lenfatiğini alır. 6-12 adet lenf nodu infrapilorik düzeyde gastroduodenal ve sağ gastroepiploik arter düzeyinde yerleşik olup pilorun lenfatiğini alır. Bu gruplar arasında yoğun yan bağlantılar bulunur (Şekil 2.3) (20).
Şekil 2.3. Perigastrik lenf nodu istasyonları: 1) Sağ Parakardiyal, 2) Sol Parakardiyal, 3)
Küçük kurvatur, 4) Büyük Kurvatur, 5) Suprapilorik, 6) İnfrapilorik lenf nodu istasyonları (20).
Midenin Sinirleri Midenin innervasyonu sempatik ve parasempatik sinirler
aracılığıyla olur. Parasempatik lifleri vagal sinirden, sempatik sinir lifleri çölyak pleksusdan gelir (16). Vagus sinirleri özofagusun lateralinden aşağıya inerek diafram seviyesinde sol (ön) ve sağ (arka) vagal kökleri yapar. Diafram seviyesinde ön vagus 1-2 dala ayrılarak özofagusun muskuler tabakasına yapışır (Şekil 2.4) (17). GE bileşke düzeyinde küçük dallar halinde küçük kurvatur kenarı boyunca ilerleyerek en sonunda Laterjet dallarını (Kaz Ayağı) oluşturmak üzere sonlanır (21). Vaguslar midenin hareketlerini ve mide bezlerinin çalışmasını arttırırlar. Sempatik sinirler ise mide hareketlerini inhibe ederken, pilor sfinkterini aktive ederler (16).
Şekil 2.4. Vagus sinirlerinin şematik görüntüleri (17).
2.2. Midenin Prekanseröz Lezyonları ve Mide Kanseri
2.2.1. Midenin Prekanseröz Lezyonları Prekanseröz olarak tanımlanan kanser
öncüsü lezyonlar bulunmaktadır. Bunlar; Kronik atrofik gastrit, intestinal metaplazi, pernisiyöz anemi, hipertrofik gastrit, mide polipleri, postgastrektomi, gastrik displazi, kronik peptik ülser ve Helikobakter pilori infeksiyonudur (22-27).
Kronik Atrofik Gastrit ve İntestinal Metaplazi Atrofik gastritte mukazal atrofi
ve sellüler hiperproliferasyon birliktedir. Kronik gastritte uzun süren iltihabi olay sonucu bezlerin tek tek hasarlanması ve bunun yerini bağ dokusunun alması ile atrofi gelişir. Mide kanserli olguların %80-90’ında atrofik gastrit söz konusudur. Atrofik gastritli olguların % 10’unda 10-20 yıllık süreçte mide kanseri gelişmektedir (28). İntestinal metaplazi ile mide karsinomu arasındaki ilişki yapılan çalışmalar ile desteklenmektedir.
Pernisiyöz anemi Pernisiyöz anemide görülen kronik otoimmün atrofik gastrit
mide karsinomu için belirgin bir risk faktörü olarak kabul edilmektedir. Bu grupda mide kanseri prevalansı %1-3’tür.
protein kaybettiren enteropatinin birlikte izlendiği nadir bir hastalıktır. Esas nedeni mide mukozasının mukus hücrelerinin aşırı çoğalmasıdır. Bildirilen 200 olgunun %15’inde mide kanseri saptanmıştır. Bu gerçek Menetrier hastalığının premalign bir durum olduğunu göstermektedir (29, 30).
Mide polipleri Mide polipleri genel olarak hiperplastik ve adenomatöz polip
olarak ikiye ayrılır.
Hiperplastik Polipler: Gastrik poliplerin %75-90’nı oluşturur.Bu polipler hasara uğrayan epitelin aşırı çoğalması ile oluşur. Etrafı salim doku ile sınır ayrımı net yapılamaz ve malign dönüşüm çok nadirdir. (31).
Adenomatöz Polipler: Gastrik poliplerin %8-25’ini oluşturur. Düz, papiller ve villöz bir şekilde büyüme eğilimi gösterirler. Malign dönüşüm %6-75’inde izlenebilir. 2 cm’nin üstündeki tümörler %30-60 oranlarına kadar ek kanseri barındırabilmektedir. 2 cm çapın üstüne çıktıkça malign dönüşüm riski artmaktadır (32).
Postgastrektomi Selim lezyonlardan dolayı yapılan gastrektomilerden sonra mide
kanseri insidansı artmaktadır. Daha çok Billroth II operasyonundan sonra görülen remnant mide kanseri süreyle doğrudan ilgilidir. Özellikle postoperatif 20 yıldan sonra riskin arttığı vurgulanmıştır. Remnant mide kanserinin safra ve pankreas salgıları ile özel olarak ilişkili olduğu gösterilmiştir (33-36).
Gastrik Displazi Displazi hafif, orta ve ağır olmak üzere üç aşamada değerlendirilmektedir. Displazi terimi prekanseröz lezyonu tanımlar. Ağır displazi erken mide karsinomlarında %40-100, ilerlemiş mide karsinomlarında %50-80, peptik ülserli vakalarda %1 oranında görülmüştür. Prospektif çalışmalarda hafif derecedeki displazinin %60-70 oranında gerilediği, orta derecede displazisi olanlarda %10-15, ağır derecede displazisi olanlarda ise %20-80 oranında karsinom geliştiği saptanmıştır (37, 38).
Kronik Peptik Ülser Kronik benign ülserler pratik olarak kanserleşmezler, ancak
kansere bağlı ülserler benign görünümde olabilmektedir. Son yıllarda geniş olgu katılımlı çalışmalarda, gastrik ülser tanısı konulanlarda 9 yıl izlemde gastrik kanser gelişme risk oranı 1.8 olarak saptanmıştır (39).
Helikobakter Pilori Dünya nüfusunun %50’si Helikobakter pilori (HP) ile enfekte
durumdadır. Epidemiyolojik pek çok çalışma HP ile mide kanseri arasında ilişki bildirmişlerdir. Son zamanlarda yapılan 13 ülkeyi ve 3000 hastayı kapsayan bir çalışmada HP ile enfekte olan kişilerde mide kanseri sıklığının 6 kat arttığı saptanmıştır. Gelişmekte olan ülkelerde 10 yaşına kadar tüm çocukların %50’sinin, 60 yaşına kadar ise neredeyse tüm toplumun bu organizma ile enfekte olduğu izlenmektedir (40-42). Helikobakter pilori enfeksiyonunun mide karsinogenezisi üzerine etkisi 3 yoldan olmaktadır (43).
2.2.2. Mide kanseri
2.2.2.1. İnsidans Dünyada erkeklerde 2. kadınlarda 4. en sık görülen kanserdir.
Mide kanseri insidansı orta yaşta ve erkeklerde daha yüksektir. Erkek/kadın oranı 2/1 dir. Türkiye’de tüm kanserler içinde erkeklerde ve kadınlarda 2. en sık görülen kanserdir. Türkiye’de saptanan kanserlerin erkeklerde %7.4 ve kadınlarda %6’sı mide kanseridir. (44, 45).
Mide kanseri insidansı coğrafi farklılıklar gösterir. Özellikle Japonya ve Kolombiya gibi bazı ülkelerde mide kanseri sıklığı diğer ülkelere göre daha fazladır. İnsidans ve mortalite düşük sosyo ekonomik sınıfta üst sınıftan 3 kez daha yüksektir. Mide kanseri endüstrileşmiş ülkelerden çok gelişmekte olan ülkelerin problemidir (46, 47). Irk ve cins mide kanserlerinde sağ kalımı ve tanı sırasındaki tümörün yaygınlığını etkilememektedir (48, 49).
2.2.2.2 Etyoloji Çevresel faktörler ve beslenmenin mide kanseri üzerine olan etkisi
uzun yıllar araştırılmıştır. Japonya, Kore, Kolombiya, İrlanda gibi ülkelerde mide kanseri diğer ülkelere göre daha sık görülmektedir (50-52). Çalışmalarda karbonhidrat, turşular, tuzlanmış et ve balık mide kanseri riskini arttırdığı, öte yandan süt, taze sebzeler, vitamin C tüketiminin artışının ise riski azalttığı gösterilmiştir. Besinlerde yağ oranının aşırı düşük ya da yüksek olması da kanser riskini yükseltmektedir (53,54). Mide kanserinin oluşmasında neden olduğu düşünülen diğer iki madde nitrit ve nitratlardır. Bu maddelerin artışının hipoklorhidri ile birlikte olduğu bildirilmiştir. Midenin hipo veya aklorhidri durumunda nitrit yapan bakterilerde artış olduğu gözlenmiştir (55). Genetik faktörlerin de mide kanserindeki rolü araştırılmıştır. Mide kanseri kan grubu A olanlarda sık olduğu
gözlenmiştir. Lynch sendromu II’de mide kanseri sık görülür. Ailesinde mide kanseri olanlarda 2-3 misli daha sık görülmesi ve ikizlerde de kanserin gözlenmesi genetik bir geçiş olabileceğini düşündürmektedir (56).
2.2.2.3. Histopatoloji Midenin ana kanser tipi adenokanserdir. Mide
adenokanserlerinin %30’u üst, %39’u orta, %26’ı alt kısımda, %5’i tüm midede izlenir (64). Mide adenokanserleri 2 bölümde incelenebilir:
1) Erken evre mide kanseri,
2) İleri evre mide kanseri.
Japonya’da mide adenokanserlerinin %40’ı erken evrede iken Avrupa ve Amerika’da bu oran %15’i geçmemektedir (57).
Erken evre mide kanserlerinde makroskopik özellikler Erken mide kanseri için
Japon Gastroenterolojik Endoskopi Derneği tarafından önerilen ve tüm dünyada kabul gören makroskopik klasifikasyonu kullanılmaktadır (58). 3 tipi vardır (59).
• Tip I: Polipoid (protrüze).
• Tip II: Mukozal yüzeyin pürüzsüz olması ile karakterize olmuş süperfisyal (yüzeyel) tip. Yüzeyden birkaç mm yükselmiş bir plak şeklinde olan tipi (Tip IIa). Mukozanın renginde sadece fokal bir değişiklik ile tanımlanmış olabilen flat (düz) tip (Tip IIb). Yüzeyden birkaç mm basılmış ve intakt veya minimal erode olmuş bir yüzeye sahip olan yüzeye göre depresse olmuş tip (Tip IIc).
• Tip III: Ülsere olan tip. Bu lezyonlar endoskopik olarak gözlendiği zaman, biyopsi yapıldığında yüksek bir kanser varlığı saptanmıştır.
İleri evre mide kanserlerinde makroskopik özellikler İlerlemiş gastrik
karsinomların makroskopik klasifikasyonunda ilk kez tanımlanan ve günümüzde de kullanılan Borrmann sınıflaması kullanılmaktadır (60).
• Tip II: Bir malign ülser veya kubbesinde bir ülserasyon bulunan fungiform tümörler (ülserovejetan).
• Tip III: İnfiltratif bir tabana sahip ülsere tümör.
• Tip IV: Mukozal bir kitle veya ülserasyon olmaksızın gastrik duvarın diffüz kalınlaşmasıdır.
Erken evre mide kanserlerinde mikroskopik özellikler Bu gruba boyutları ve
bölgesel lenf bezi tutulumuna bakılmaksızın lamina propria ve/veya submukozaya invazyon gösteren tümörler dahil edilmektedir. Tümörlerin %10’u multisentriktir. Sıklıkla midenin distalinde, küçük kurvatur boyunca yerleşim gösterirler. Genellikle 2 cm veya daha küçük boyutta karşımıza çıkmakla birlikte 8 cm boyuta ulaşan olgular da mevcuttur. Histolojik incelemede tüm karsinom tipleri görülebilir (60).
İleri evre mide kanserlerinde mikroskobik özellikler Mide mukozasının
hücresel çeşitliliği ve tümörlerin önemli bir kısmının intestinal metaplazi zemininde gelişmesi, bu tümörlerin oldukça geniş morfolojik spektrum göstermesine neden olmaktadır. Mide tümörlerinin histolojik sınıflandırılmasında günümüze kadar pek çok sınıflama ortaya atılmış olmakla birlikte, hiçbiri tümörlerin fenotipik ve genotipik özelliklerini tam anlamıyla yansıtmamaktadır. Bunlardan günümüzde kullanılanları Lauren (Tablo 2.1) ve WHO (Tablo 2.2) sınıflamalarıdır (61, 62).
Tablo 2.2. Dünya Sağlık Örgütü’nün Mide kanseri için histolojik tümör tipleri (63)
2.2.2.4. Mide kanserinin yayılması
Direkt Yayılım Tümörler vertikal olarak mide duvarı boyunca, horizontal olarak
ise proksimalde özofagusa, distalde duodenuma doğru yayılım gösterebilirler. Özofagus ve duodenuma invazyon direkt submukozal ve/veya subserozal yolla ya da submukozal lenfatikler yoluyla olduğunda yüzey mukoza normal görünümde izlenebilir. Bu nedenle cerrahi sınırların belirlenmesinde frozen section kullanımı zorunludur. Mide kanserleri direkt olarak pankreas, dalak hilusu, transvers kolon, karaciğer hilusu, omentum, diyafram ve karın duvarına yayılım gösterebilir (64).
Peritoneal Yayılım Tüm mide duvarı boyunca yayılıp serozaya ulaşan tümörler
peritoneal yayılım gösterebilirler. Diffüz tip kanserlerde periton yayılımı, intestinal tip’e oranla daha sıktır.
Peritoneal Yayılım; asit, omental implant, pelvik cul de sac ve bilateral over
tutulumu (Krukenberg tümörü) şeklinde karşımıza çıkabilir. Peritona yayılım gösteren tümörlerde, asit sıvısının sitolojik incelemesinde sıklıkla malign hücreler saptanır (64).
Hematojen Yayılım Hematojen yolla en sık karaciğere yayılım olur. Hematojen
yol ile de akciğer, kemik, adrenal bez, deri, over ve uterusa metastaz yapabilirler (64).
Lenfatik Yayılım Diffüz ve intestinal tümörlerde lenf yoluyla metastaz oranları benzerdir. Özellikle submukozal invazyonun olduğu, 4 cm’den büyük ve az diferansiye
tümörlerde lenfatik yayılım riski daha fazladır (64).
2.2.2.5. Mide Kanserinin Evrelemesi
TNM KLASİFİKASYONU (WHO-2000) (65)
1. Primer Tümör: Kanserin mide duvarına penetrasyonunun derecesini gösterir. X: Primer tümör değerlendirilemedi
T0: Primer tümör mevcut değildir
Tis: İnsitu Karsinom. Lamina propriaya invazyon göstermeyen intraepitelyal tümör Tl: Tümör lamina propria veya submukozada sınırlıdır
T2: Tümör muskularis propria veya subserozada sınırlıdır
T3: Tümör komşu dokulara (dalak, transvers kolon, diafragma, pankreas,
abdominal duvar, adrenal bez, böbrek, ince barsak, retroperitoneum) invazyon göstermeden serozayı geçmiştir
T4: Tümör komşu dokulara invazedir.
2. Nodal Tutulum: Büyük ve küçük kurvatur boyunca bulunan perigastrik lenf
nodları, çölyak, splenik, hepatik, sol gastrik arter boyunca uzanan lenf nodlarıdır. Diğer intraabdominal lenf nodları uzak metastaz olarak kabul edilmiştir.
NX: Regional lenf nodu tutulumu değerlendirilemedi. N0: Regional lenfnodu metastazı mevcut değildir. N1: Metastazlı regional lenf nodu sayısı 1-6 arasıdır. N2: Metastazlı regional lenf nodu sayısı 7-15 arasıdır. N3: Metastazlı regional lenf nodu sayısı 15’den fazladır. 3. Uzak Metastaz:
MX: Uzak metastaz değerlendirilemedi. M0: Uzak metastaz mevcut değildir. M1: Uzak metastaz mevcuttur.
Mide kanseri TNM sınıflamasına göre 4 evre grubuna ayrılmaktadır (Tablo 2.3) (65).
Tablo 2.3. Mide kanseri evre grupları (65).
2.2.2.6. Diğer Mide Tümörleri
Midenin Nöroendokrin Tümörleri İyi huylu, mukoza ve submukoza içinde
sınırlı, damar invazyonu yapmayan, fonksiyon yapmayan küçük tümörlerdir. Genellikle fundus mukozasında kronik atrofik gastrit zemininde ve hipergastrinemi ile birlikte enterokromafin benzeri (ECL) hücreli tümörlerdir (66).
Mide Lenfoması Mide lenfomaları mide kanserlerinin sadece %5’ini oluştururlar.
Ancak adenokarsinomadan sonra midenin en çok görülen kanser türüdür. Mideyi diffüz olarak infiltre eder. Gastrointestinal traktüs, lenfomaların en sık tuttuğu ekstranodüler bölgedir. Primer gastrointestinal lenfomaların %41-46’sı mideyi tutar, geri kalan da ince bağırsaklara yerleşir. Primer gastrik (non Hodgkin) lenfomalar B hücre tümörleri olup, mukoza ilişkili lenfoid doku’dan (MALT) kaynaklanır. (66).
Baryumlu İncelemeler Erken mide kanserinde radyolojik olarak en iyi tanı
medotu çift kontrastlı baryum incelemesidir. İleri evre tümörlerde polipoid, ülseratif veya infilitratif olabilirler. Ülsere karsinomlarda tümör kitlesi ülserasyonla yer değiştirmiştir. Malign ülserasyonlar kitle içinde intralüminal yerleşim gösterirken selim ülserasyonlar mide konturunun dışına taşma gösterir. Malign ülserleri çevreleyen tümör kitlesi komşu mide duvarı ile dar açı yapar. Mide mukoza kıvrımlarının tümör ile infilitrasyonu sonucunda bu kıvrımlarda düzensizlik ve kesinti izlenir. İnfiltran karsinomlar midede düzensiz daralma ve mukozada nodülarite gösterir. Mide kanserinin kolona invazyonu neticesinde oluşan gastrokolik fistüllerde saptanabilir (67).
Endoskopi (Gastroskopi) Gastroskopik inceleme, mide kanseri tanısı koymada
en önemli yöntemdir. Biopsi ile %80-85 oranında doğru sonuç alınmaktadır. Fırçalama ile alınan materyal ile doğruluk oranı %95’lere çıkmaktadır (67). Midenin 2 cm’den büyük adenomatöz poliplerinde %60 oranında kanserleşme görülmektedir. Bu nedenle midenin adenomatöz poliplerin endoskopik yöntem ile çıkarılması ve 2-4 yıl aralıklar ile takip edilmesi önerilmektedir (67). Amerikan Cerrahi Derneği'nin çalışmasında endoskopi ve biyopsi ile mide kanserlerinin %94’üne doğru tanı konma imkanı saptanmıştır (68).
Bilgisayarlı Tomografi (BT) Lümeni su, hava ya da kontrast madde kullanılarak
optimal olarak doldurulması sağlıklı mide duvar değerlendirilmesi için ön şarttır. Yetersiz lümen doldurulması durumunda mide duvarı normalden kalın olarak izlenir ve yanlış değerlendirilme yapılabilir. Genelde 400-700 cc arası bir hacim yeterli olur. Normalde mide duvar kalınlığı 5 mm’den daha az olmalıdır. Kardia bölgesinde duvardan oblik geçen kesitler alındığından biraz daha yüksek ölçümler elde edilebilir. BT lenf bezi metastazlarını ve pankreas invazyonunu belirlemede çok hassas değildir. Doğru evreleme oranı %60-80 arasında kabul edilmektedir (67).
Magnetik Rezonans Görüntüleme (MRG) Haraket artefaktları ile ticari olarak
piyasada satılan oral kontrast madde olmaması nedeni ile MRG’ın mide karsinomunu değerlendirmedeki rolü kısıtlıdır. Oral kontrast maddeler geliştirildikce ve hızlı çekim teknikleri ile MRG yakın zamanda daha fazla kullanılacaktır. (67).
invazyon derinliği net ortaya konabilir. EUS tümör ile fibrotik doku arasında ayrımı net yapamadığından bu bir dezavantajdır. EUS ile evreleme oranları %75 civarındadır. T2 lezyonlarda başarı oranı %38 iken, T1 ve T3 lezyonlarda bu oran %80-90’dır. EUS ile nodal tutulum teknik durum ve cerrahi deneyime göre %65 civarlarında saptanabilir (69).
3.1. İnce Barsak Anatomisi
İnce barsaklar sindirim kanalının pilordan ileoçekal valve kadar uzanan, kıvrımlar yapmış bölümüdür. Uzunluğu taze kadavrada yaklaşık 6–7 m olup canlılarda kas tonusu nedeniyle yaklaşık 4–5 m kadardır. Genişliği proksimalden distale doğru giderek azalır (proksimalde yaklaşık 4–5 cm, distalde yaklaşık 2–2.5 cm). Karın boşluğunun orta ve alt kısmında bulunur. Kalın barsağın oluşturduğu bir çerçeve içinde yer alır. Ön tarafta omentum majus ve karın ön duvarı ile komşudur. İnce barsak duodenum, jejunum ve ileum olmak üzere üç bölüme ayrılır.
Duodenum: İnce barsağın en kısa, en geniş çaplı, en kalın duvarlı ve en az hareket
eden parçasıdır. Pilordan başlar, açıklığı sola bakan bir yay çizdikten sonra solda 1–2. lomber vertebra seviyesinde fleksura duodenojejunaliste sonlanır. Uzunluğu yaklaşık 25 cm’dir. Normalde bir U veya yarım halka şeklinde olan duodenum kavsi içine pankreasın başı oturur. Duodenumun mezenteri yoktur. Duodenum dört parçadan oluşur:
Pars süperior: Duodenumun en hareketli bölümüdür. İlk yarısı intraperitonealdir ve diğer bölümlerine oranla daha geniştir. Bursa omentalisin bir bölümünü oluşturan bu geniş bölüme ampulla (bulbus) denir. Ampullayı örten periton parçaları omentum minusun hepatoduodenalis parçasını meydana getirir. Duodenumu karaciğere bağlayan bu periton plikasına ligamentum hepatoduodenalis denir. Pars süperiorun 2. yarısının arka yüzü peritonsuz olup karın arka duvarına yapışıktır.
Pars desenden: Bu bölümün ön yüzünü orta hizada mezokolon transversum çaprazlar. Bu mezo duodenuma gevşek areolar doku ile tutunmuş olup, üst ve alt kısmında kalan duodenum bölümlerinin ön yüzleri periton ile kaplıdır. Duktus koledokus ve duktus pankreatikus, duodenumun medial kenarında yan yana gelerek duodenum duvarına oblik
olarak girdikten sonra birleşerek ampulla hepatikopankreatika’yı oluştururlar. Ampullanın daralan ucu papilla duodeni majore (papilla vateri) açılır. Duktus pankreatikus minör (Santorini kanalı) papilla duodeni majörün 2 cm yukarısında bulunan papilla duodeni minöre açılır.
Pars horizontalis: 3. lomber vertebranın sağ tarafında başlar. Aortun ön tarafında pars asenden ile birleşir. Radiks mezenterinin çaprazladığı orta kısmı hariç ön yüzü peritonla kaplıdır. Arka kısmın sadece solda kalan küçük bir kısmı peritonla örtülüdür, diğer kısımları peritonsuzdur.
Pars asenden: Aortun önünde ve biraz sol tarafında yer alır. Duodenumun bu son bölümü ve fleksura duodenojejunalis ligamentum suspensorium duodeni (Treitz bağı) ile karın arka duvarına asılmıştır. Treitz bağı diaframın sağ krusundan başlar. Aşağıya doğru uzanarak fleksura duodenojejunalisin üst kısmına yapışır (70,71).
Jejunum ve İleum: Fleksura duodenojejunalisten başlayıp, ileoçekal valve kadar
devam eden bu iki bölüm yaklaşık 6–7 m uzunluğundadır. İnce barsağın bu bölümleri mezenter adı verilen iki katlı periton yaprağı vasıtasıyla karın arka duvarına asılır. Jejunum ve ileum mezenterin yapıştığı dar şerit şeklindeki sahalar haricinde periton ile kaplıdır. Duodenumun aşağısında kalan ince barsağın 2/5 proksimal kısmını jejunum, 3/5 distal kısmını ileum oluşturur. Bu iki bölüm arasında kesin bir sınır yoktur. Ancak görünüş ve yapı bakımından bazı farklılıklar vardır. Jejunum kıvrımları karın boşluğunun sol üst kısmında, ileum ise karın boşluğunun alt kısmında ve pelvis boşluğunda bulunur. Jejunum çapı yaklaşık 4 cm olup ileumdan daha geniştir. İleum çapı yaklaşık 3–3.5 cm olup ileoçekal valve doğru gidildikçe genişliği azalır. Jejunum kan damarlarından daha zengin olduğu için daha kırmızıdır. Mukozadaki plika sirkülarisler ileuma göre daha çok sayıda ve daha kalın olup sık yerleşimlidir. Duvarı ileum duvarından daha kalındır. Jejunumun damarları 1–3 kemer oluşturduktan sonra uzun damarlar şeklinde barsağa ulaşırlarken, ileumun damarları genellikle 4–5, bazen de daha fazla kemerler oluşturduktan sonra kısa dallar şeklinde barsağa ulaşır. Lenf folikülleri ileumun alt yarısında büyük ve çok sayıda bulunurken, jejunumda küçük ve az sayıda bulunur (70,71).
karın arka duvarına asar. Mezenterin karın arka duvarına yapışan kısmına radiks mezenteri denir. Radiks mezenteri 2. lomber vertebra sol tarafından başlayıp aşağı ve sağa doğru uzanarak sağ sakroiliak eklem seviyesinde sonlanır. Mezenterin iki yaprağı arasında jejunum, ileum, A-V. Mezenterika süperiorun jejunum ve ileuma giden dalları, sinirleri, lenf damarları ve bir miktar yağ dokusu bulunur (70).
İnce Barsağın Arterleri: Duodenumun arterlerini A. Gastroduodenalisin dalı olan
A.Pankreatikoduodenalis süperior ve A. Mezenterika süperiorun dalı olan A. Pankreatikoduodenalis süperiordan alır. Jejunum ve ileum arter dallarını superior mezenterik arterden alır. Sayıları 20 kadar olan bu dalların ilk 8–10 tanesi de ileuma gidip A. İliaka adını alır. Bu 20 kadar dalın hepsi A. Mezenterika superiordan çıktıktan az sonra mezenter içinde iki uç dala ayrılır. Bu uç dallar kendilerine komşu olan diğer uç dallarla kavis biçiminde anastomozlar yaparlar. Bu kavislerin konveks taraflarından tekrar dallar çıkar. Bunlar da uç dallara ayrılarak kendi aralarında anastomozlar yaparak ikinci bir kavis meydana getirirler. Böylece iki ile beş sıra halinde anastomozlardan oluşan arter kavisleri meydana gelir. İleumda arter kavisleri daha fazla sayıda olup daha karmaşık bir yapıya sahiptirler. Son arter kavislerinden çıkan vasa rektalar birbirleriyle anastomoz yapmazlar. Düz ve dik bir şekilde ilerleyerek mezenterde, jejunumda ve ileumda dağılırlar.
İnce Barsağın Venleri: İnce barsaktan dönen venöz kan V. Mezenterika superior
yolu ile V. Portaya dökülür.
Lenfatikleri: Lenf sisteminin başlangıcı villusların ortasındaki santral lenf
aralıklarıdır. Bunlar villusların dibinde ve submukozada bulunan lenf damar ağı ile birleşirler. Bu ağlardan çıkan lenf damarları mezenterin iki yaprağı arasındaki lenf ganglionlarına ulaşırlar. Bu ganglionlardan çıkan lenf damarları birleşerek trunkus intestinalisi yaparlar ve l. lomber vertebra hizasında sisterna şiliye dökülürler. Buradan başlayan en büyük lenf damarı olan duktus torasikus ise V. Kava süperiora dökülür.
İnce Barsağın Sinirleri:
Otonom sinir sisteminden, mezenterin iki yaprağı arasında ve arterlerin çevresinden gelirler. Sempatik lifler; superior mezenterik gangliondan, parasempatik lifler ise çöliak
ganglion aracılığı ile n. vagustan gelir. İnce barsak cidarına gelen bu sinir lifleri önce tunika muskularis tabakasında longitudinal ve sirküler kaslar arasında myenterik pleksusu (Auerbach), daha sonra submukoza tabakasında submukozal pleksusu (Meissner) meydana getirirler. Auerbach pleksusu barsağın peristaltik hareketlerini, Meissner pleksusu ise ince barsağın salgı fonksiyonunu idare eder. İnce barsağın ağrı duyusunu taşıyan afferent lifler, sempatik sinir lifleri ile birlikte medulla spinaliste 10–11–12. torakal ve l. lomber segmentlere gider. Bu nedenle ince barsaklardan gelen ağrılar 10–11–12. torakal ve l. lomber spinal sinirlerin yayıldığı göbek çevresi ile lomber bölgede hissedilir (70,71).
3.2 İnce Barsak Patolojileri 3.2.1 Enflamatuar Patolojiler
3.2.1.1 Spesifik Enflamatuar Patolojiler
Chron Hastalığı Crohn hastalığı, sıklıkla ince barsakları tutan, kronik, segmental,
transmural, inflamatuar bir hastalık olup ağızdan anüse kadar tüm gastrointestinal kanalı etkileyebilir. En sık terminal ileum ve proksimal kolon tutulur (72). Hastalığın nedeni bilinmemekle birlikte yeni yapılan araştırmalarda, bilinmeyen lüminal antijenlere anormal mukozal cevabı gösteren deliller bulunmuştur (73). Hastalık aynı anda birden fazla bölgeyi tutabilir. Lezyon alanları arasında sağlam barsak segmentleri bulunur. Treitz bağı ve ileoçekal valv arasındaki mezenterik ince barsak tutulduğunda radyolojik değerlendirme özel bir önem taşır. Çünkü bu alan endoskopik inceleme ile değerlendirilememektedir. Bu bölge patolojilerinin değerlendirilmesinde ince barsak pasaj grafisi, çift kontrast enteroklizis, BT enteroklizis ve MR enteroklizisten faydalanılır. Ancak mukozal yüzeyi baryumlu incelemeler (enteroklizis) daha ayrıntılı gösterdiği için hastalığın değerlendirilmesinde öncelikli olarak kullanılmaktadır. Crohn hastalığının radyolojik bulguları genellikle; erken dönem, ara, ileri dönem ve komplikasyonlar olarak değerlendirilir.
Enteroklizis incelemesinde erken dönemde granüler pattern ve aftöz ülserler tespit edilir. Ara dönemde aftöz ülserlerle birlikte duvarda kalınlaşma, mezenterik kenarda rijidite, antimezenterik kenarda “skalloping” şeklinde görünüm saptanmaktadır. İleri
dönemde; mural kalınlaşma ile birlikte transmural penetrasyon gösteren derin ve lineer ülserler izlenir. Derin ülserler ile arada kalan ödemli ve enflame mukoza Crohn hastalığı için karakteristik olan kaldırım taşı görünümünü (ülseronodüler patern) oluşturur. Ülser seviyesinde karşı barsak duvarında balonlaşma (pseudodivertikül) saptanabilir (74,75). Komplikasyonlar; striktür, fistülizasyon, abse formasyonu ve nadir olarak da tümör gelişimidir. Strüktürler radyolojik inceleme ile kolay tespit edilirler. Crohn hastalarında striktüre bağlı obstrüksiyon ve proksimal barsak dilatasyonu sık görülen belirtilerdendir. Fistüller tek veya çok sayıda olabilirler. Çoğunlukla terminal ileumdan başlayıp kolona geçerler (sıklıkla çekum veya sigmoid kolona). İleoileal veya ileovezikal fistüllerde daha az olmakla birlikte oluşabilirler. İleovaginal ve ileokutanöz fistüller ise çok nadir görülür. İnflamatuar polipler, sıklıkla sadece ince barsağın Crohn hastalığında görülür ve çoğunlukla küçük yuvarlak dolma defektleri şeklindedirler (76).
İntestinal Tüberküloz İntestinal tüberküloz gelişmiş batı ülkelerinde nadir bir
durum olup ülkemizde nispeten sık görülür. En sık tutulan bölge ince barsak ve özellikle ileoçekal alandır. Terminal ileumda ülserler ile birlikte huni biçimini almış kontrakte çekum görünümü karakteristiktir. Kronik enfeksiyon fibrozis ve obstrüksiyon ile sonuçlanır (74). Baryumlu incelemelerde ileoçekal tüberküloz sıklıkla kalınlaşmış, lümeni daralmış rijit terminal ileum olarak görülür. Tutulan bölgenin proksimalinde barsak dilatasyonu vardır. Sıklıkla çekum küçük, gergin ve kalınlaşmış olup, ileoçekal açı normal anatomik yapısını kaybetmiştir (77).
Back-wash İleitis Ülsertif kolitin ileoçekal valv ve terminal ileumu etkilemesidir.
Beraberinde genellikle tüm kolon tutulmuştur. Radyolojik olarak; genişlemiş ve rijit ileoçekal valv, terminal ileumda pilikalarda silinme ve granüler mukozal patern ile karakterizedir. Crohn hastalığının terminal ileum tutulumu ile karıştırılmamalıdır (78).
Yersinia İleitisi Etken bakteri Basillus Yersenia Enterokolika’dır. Enflamasyon
daha çok terminal ileumda oluşur. Semptomları; akut apandisite, morfolojik görünümü ise Crohn hastalığına benzer. Radyolojik değişiklikler, distal 20–30 cm'lik ileumla sınırlı olup sıklıkla semptomların kaybolmasından birkaç hafta sonraya kadar devam eder (79).
Çok sayıdaki biribirine dolanmış askaris, çocuklarda intestinal obstrüksiyona neden olabilir (74).
3.2.1.2 Nonspesifik İnflamatuar Patolojiler İskemik Hastalıklar
Akut İskemi: Akut iskemi önemli lümen daralması olmaksızın valvula konnivanteslerin kalınlaşması şeklinde bulgu verir. Yaklaşık 4–6 hafta sonra etkilenmiş barsak segmenti tamamen normale döner veya iskemi yerinde striktür gelişir (80).
Kronik İskemi: Arteryel orjinli kronik intestinal iskemi, çoğunlukla majör visseral arterlerin daralmasına bağlı olup barsaklarda genellikle bariz radyolojik değişikliklere neden olmaz. Mezenterik venöz oklüzyon intestinal iskeminin nadir bir nedeni olup (81), çoğunlukla mezenterin metastatik malignitelerine bağlı olarak oluşur.
İskemik Striktürler: Lokalize mezenterik vasküler emboli, strangülasyon veya travmaya bağlı oluşan intestinal iskemiyi takiben iskemik striktürler gelişebilir (82). Son zamanlarda romatoid vaskülite bağlı ince barsak iskemik striktürü de rapor edilmiştir (83).
Kronik Radyasyon Enteriti Radyasyon, vasküler endotelyal hücrelerde hasara yol
açar. Bu hasar intimal fibrozise neden olarak kronik intestinal iskemi oluşturur. (83). Radyasyon enteriti gelişmesi için geçirilmiş abdominal cerrahi veya peritonit sıklıkla predispozan bir faktördür (84).
Radyoterapi ile semptomların başlaması arasındaki geçen süre çok değişkendir. Semptomlar radyoterapi esnasında başlayabileceği gibi uzun yıllar sonra da ortaya çıkabilir (85).
Non-steroidal Anti-inflamatuar İlaç enteriti Non-steroid anti-inflamatuar ilaçlar
ince barsakta striktüre neden olabilirler. Bu striktürlerin makroskopik görünümleri tek bir geniş tabanlı fibröz striktürden multipl diafram benzeri stenotik lezyonlara kadar değişir (86,87).
göz tutulumu karakteristik bulgularıdır. Göz tutulumuna bağlı olarak üveit ve retinal vaskülit gelişebilir. Behçet'li hastaların %10-15'inde barsak tutulumu vardır ve en sık ileoçekal bölge etkilenir (88).
3.2.2 Malabsorbsiyon
Malabsorbsiyon, besin maddelerinin sindirim ve emilimindeki yetersizlik sonucu oluşan klinik tablodur. İntestinal ve ekstraintestinal çok değişik etyolojik nedenleri bulunmaktadır. En sık rastlanan intestinal neden ise çöliak hastalığıdır. Barsak emilim yüzeyinde destrüksiyona yol açan Crohn ve lenfoma gibi hastalıklar ile kısa barsak sendromu da malabsorbsiyonun diğer intestinal nedenlerindendir. Malabsorbsiyon olgularında tanı klinik, laboratuar, radyolojik ve histopatolojik bulguların birlikte değerlendirilmesiyle konulur. D-Xylose testi, dışkı yağ ölçümü, serum B12 düzeyi, solunum havası hidrojen ölçümü malabsorbsiyon tanısında kullanılan başlıca laboratuar yöntemleridir. Endoskopi ve biyopsi de diğer bir tanı yöntemidir. Crosby kapsülü ile jejunumdan alınan biyopsilerde histopatolojik olarak mukoza kalınlığını değiştirmeden, mukozada düzleşmeye neden olan villuslarda atrofi, kriptlerde hipertrofi ve lamina propriada hücre infiltrasyonu görülmektedir. Radyolojik inceleme yöntemleri baryumlu konvansiyonel pasaj grafileri veya enteroklizis ile çift kontrast incelemelerdir. Enteroklizis incelemesinde; jejunal plikalarda silinme ve seyrelme (ileizasyon), ileal plikalarda sıklaşma ve kabalaşma (jejunizasyon), duodenumda plikalarda seyrelme, kabalaşma ve düzensizlik, mukozada 1–3 mm boyutunda baryum içeren göllenmeler (mozaik patern) görülür (89,90).
3.2.3 İnce Barsak Tümörleri
İnce barsak tümörleri gastrointestinal traktusun bütün tümörlerinin %2'sinden azını oluştururlar. İnce barsağın benign ve malign tümörleri hemen hemen eşit sıklıkta görülürler. Sıklıkla semptom ve belirtileri aralıklı ve nonspesifiktir. Tanı, genellikle üst gastrointestinal kanal ve kolonda patoloji olmadığı ispat edildiğinde düşünülür (33).
3.2.3.1 Benign Tümörler
lipomlar ve hemanjiomlardır. Adenomatöz polipler ve leiomyomlar çok sık olup hemen hemen eşit sıklıkta görülürler. Nispeten daha az görülen benign tümörler ise; nörofibromlar, hamartomlar, lenfanjiomlar ve inflamatuar psödotümörlerdir.
Benign ince barsak tümörlü hastaların yaklaşık 1/5'inde klinik belirtiler gelişir. Buna karşın malign tümörlü hastaların %90'ında tümörle ilgili belirti ve semptomlar vardır. Bu nedenle benign tümörler sıklıkla otopside veya malign lezyonlara yönelik cerrahi operasyonlar sırasında tespit edilirler (91).
Leiomyom İnce barsakta en sık görülen benign tümördür. İntralüminal,
ekstralüminal ve halter şeklinde izlenebilir. İnce barsak leiomyomlarının en sık belirtisi kanamadır. İnvajinasyona da neden olabilirler (91,92).
Adenom Benign ince barsak tümörlerinin yaklaşık %25'ini oluştururlar ve
histolojik olarak tübüler veya villöz tipleri mevcuttur. Jejunum veya ileumdan ziyade sıklıkla duodenumda gelişirler. Adenomlar genellikle pediküllü olup intralüminal dolma defektleri şeklinde belirti verirler.
Lipom Genellikle ileum ve duodenumdan köken alırlar. İnvajinasyon veya
ülserasyona bağlı intestinal kanamaya neden olabilirler. Çoğunlukla intramural yerleşimlidirler. BT'de yağ dansitesinde kitle şeklinde izlenir.
Hemanjiom Küçük boyutlardaki hemanjiomlar baryumlu incelemelerle nadiren
tespit edilebilirler. Sıklıkla intralüminal veya intramural polipoid dolma defekti olarak görülmeleri için yeterli büyüklüğe ulaşmaları gerekir. İnce barsak hemanjiomları ilk olarak gastrointestinal kanama ile belirti verirler. Tuberoskleroz ve Turner sendromunda intestinal hemanjiomlar görülebilir.Osler-Weber-Rendu (Herediter hemorajik telenjiektazi) hastalarında küçük kavernöz hemanjiomlar görülebilir.
Polipozis Sendromları Benign ince barsak neoplazmları ile birlikte en sık görülen
sendrom, otozomal dominant geçişli Peutz-Jeghers sendromudur. Bu sendromda gastrointestinal hamartomlar, mukokutanöz melanotik maküllalar görülür. Hastaların %95'inde ince barsaklarda, %25'inde ise mide ve kolonda polipler oluşur. Peutz-Jeghers sendromunun klinik semptomları çoğunlukla ince barsağın geçici invajinasyonuna
bağlıdır. Malignleşme eğilimi nadirdir.
Cronkhite-Canada sendromunda bütün hastalarda mide ve kolonda benign kistik inflamatuar polipler oluşur. Hastaların yaklaşık yarısında ince barsakta da polipler bulunur. Alopesi, kutanöz hiperpigmentasyon ve tırnak atrofisi karakteristik ektodermal değişikliklerdir. Bu sendromda malabsorbsiyona bağlı ağır kronik ishal ve kaşeksi oluşabilir. İnce barsakta multipl adenomatöz polipler çoğunlukla Gardner sendromunun tipik kolonik polipozisi ile birliktedir. Familyal adenomatöz polipoziste ise ince barsak tutulumu son derece nadirdir (91,93).
3.2.3.2 Malign Tümörler
Adenokarsinom İnce barsağın primer adenokarsinomu duodenum ve jejunumdan
kaynaklanır. Hastaların 2/3'ü abdominal ağrı veya intestinal obstrüksiyon ile hekime başvururlar. Hastaların yarısından çoğunda kanama ve anemi, 1/3'ünde palpe edilebilen abdominal kitle vardır. Radyografik belirtiler, gastrointestinal kanalın diğer kısımlarında oluşan adenokarsinom belirtilerine benzer. Anüler infiltrasyon yapan tümörler çok sık olup barsak lümeninde düzensiz daralmalara, mukozal destrüksiyon ve omuz işereti bulgusuna neden olurlar. Daralmış barsak segmenti içerisine nodüler protrüzyonlar veya kitlede ülserasyon oluşabilir (91,94).
Lenfoma Lenfomalar, çocuklarda en sık görülen ince barsak maligniteleridir.
Erişkinlerde ise adenokarsinoma nispeten daha az görülür. İnce barsak lenfoması primer neoplazm şeklinde oluşabileceği gibi multisistemik hastalığın yayılımına bağlı olarak da gelişebilir. Abdominal ağrı ve obstrüktif semptomlar sıktır. Fakat adenokarsinoma göre şiddetleri daha azdır. İnce barsak lenfomasının farklı radyolojik görünümleri vardır. Hastaların yaklaşık %10- 20'sinde multipl lezyonlar oluşur ve bunların orjininin multisentrik ya da metastatik olduğunu belirlemek zordur. Nodüler formda değişik büyüklükte multipl nodüler intralüminal veya intramural dolma defektleri olarak görülürler. Barsak konturunda irregüler skalloping belirlenebilir. Fakat plikal ansın görünümü ve lümen çapı normaldir. Lenfomalar intralüminal polipoid bir kitle olarak görülebilir ve sıklıkla bu invajinasyon ile sonuçlanır. Diffüz intramural infiltrasyon sıklıkla barsak lümenini genişletir. Lenfomanın ekzoenterik formunda tümör ekstralüminal olarak
prolifere olur ve kitle içerisinde büyük ülserasyonlar ve fistüller oluşur. Mezenterik invazyon oluşumu, büyük ekstralüminal kitlelerin abdominal organlarda yer değişikliğine neden olmaları, dışarıdan basıya bağlı defektler ve barsak duvarına invazyon yapmaları ile belirlenir. BT, intraabdominal lenfomaların evrelemesinde önemli rol oynar. Mezenterik uzanımı, solid organ tutulumunu, intraperitoneal ve retroperitoneal lenfadenopatiyi belirlemede önemli faydalar sağlar (91,95).
Leiomyosarkom Yavaş büyüyen ekstralüminal kitleler şeklinde görülür ve komşu
barsak anslarını çevreye doğru iterler. Benign leiomyomlar ve leiomyosarkomlar benzer radyografik özellik gösterirlerse de, büyük düz kas tümörlerinde önemli ülserasyon ve fistül formasyonunun olması çoğunlukla maligniteye işaret eder. Diğer hücre tipli sarkomlar (fibrosarkom, liposarkom vb.) nadiren ince barsakta yerleşirler (91).
Karsinoid Tümör İnce barsak tümörlerinin 1/3'ünü oluşturan karsinoid tümörler
en sık görülen primer ince barsak tümörleridir. Bu tümörler mukozal kriptalardaki enterokromafin hücrelerinden orjin alırlar. Seratonin ve kinin peptitleri gibi değişik hormon üretme yetenekleri vardır. Karsinoid tümörler submukoza içerisinden dışarıya doğru büyüme eğilimi gösterirler. Bölgesel lenf nodu tutulumu ve uzak metastaz yapabilirler. Küçük boyuttaki karsinoid tümörler nadiren malign özellik gösterirler. Oysa 2 cm'den büyük çaplı tümörler büyük oranda malign özellik gösterip metastaz yaparlar. Genel olarak ince barsak karsinoidlerinin 1/3'ü multipldir, 1/3'ü metastaz yapar ve 1/3'ünde ikinci bir malignite vardır.
Hastaların çoğu asemptomatiktir. Semptomatik karsinoid tümörlü vakaların yaklaşık %90'ında bölgesel lenf nodu metastazı vardır. Taşikardi, diare, astım ve sağ kalp yetmezliği gibi spesifik semptomlar karsinoid sendromu oluştururlar (91,96).
Metastatik Tümörler İnce barsak metastazları, diffüz abdominal karsinomalı
hastalarda nispeten tesadüfi olarak tespit edilirler. Bu hastalarda tercih edilen ilk radyolojik tetkik genellikle BT'dir. BT mezenterik ve peritoneal kitleleri direkt olarak görüntüler. Barsak duvarındaki diffüz kalınlaşmayı veya metastatik kitleyi demonstre eder. Tümörün intraperitoneal yayılımı sıklıkla over veya gastrointestinal orjinli malignensilerde oluşur.
Serozal veya mezenterik metastazlar, barsağın konkav mezenterik kenarında kitle çentiklenmesi oluşturur. Oluşan dezmoplastik reaksiyona bağlı olarak mukozal kıvrımlarda kalınlaşma, barsak anslarında fiksasyon ve angülasyon, lümende daralma ve obstrüksiyon ortaya çıkabilir.
İnce barsağa hematojen metastazlar sıklıkla malign melanom, akciğer ve meme karsinomuna bağlı olarak oluşur. Embolik proçeslerin varlığında antimezenterik kenarda multipl submukozal nodüller görülür (91,97).
3.2.2 İnce Barsak Hastalıklarının Tanısında Görüntüleme
İnce barsak uzun ve kıvrımlı anatomik yapısından dolayı GİS’te incelenmesi en güç organdır. Teknolojik gelişmelere karşın ince barsak hastalıklarının tanısında halen güçlükler yaşanmaktadır. Sindirim sistemi hastalıklarında en kesin tanı yöntemi olan endoskopi ile ancak jejunumun proksimali ve terminal ileum incelenebilir. Diğer barsak segmentlerine endoskop ile ulaşmanın mümkün olmaması ve enteroskopinin hasta açısından konforsuz ve teknik açıdan zor olması nedeniyle rutinde kısıtlı olarak uygulanabilmiştir. Bu nedenle normal anatominin ve patolojilerin belirlenmesinde radyolojinin önemli bir yeri vardır.
Direk Batın Grafileri Direk batın grafileri özellikle akut batın olgularında
faydalıdır. Ayakta alınan grafilerde diafragma altındaki serbest hava ve hava-sıvı seviyelenmeleri saptanabilir. Yatarak alınan grafilerde barsaklara ait gaz dağılımı ile barsak anslarının genişliği değerlendirilir. Lateral dekübitus pozisyonda alınan grafilerde ise pnömoperitoneum daha kolay tespit edilir (74,98).
Baryumlu İnce Barsak Grafileri İnce Barsak pasaj Grafisi (İBPG)
Bu yöntemde yaklaşık 500 ml düşük yoğunlukta (%50’lik) baryum süspansiyonu oral yoldan verilir. Kontrast maddenin pilordan çekuma kadar pasajı izlenir. Ağızdan verilen baryum mideden boşalıncaya kadar, hasta prone ve sağ lateral dekübit pozisyonunda yatırılır. Amaç ince barsakta baryum sütununun kesintisiz bir şekilde devam
etmesini sağlamaktır. Pasaj süresi 1–6 saat arasında değişmektedir.
Transmural perforasyon şüphesi olan hastalarda ve ameliyat sonrası erken dönemde anastomoz hattından kaçak olup olmadığının değerlendirilmesi amacıyla uygulandığında suda eriyen kontrast maddeler kullanılmalıdır. Ancak iyotlu kontrast maddeler baryum kadar yoğun olmadığı için özellikle postoperatuvar küçük anastomoz kaçaklarını saptamayabilir. Buna rağmen İBPG, invaziv bir yöntem olmaması, kontur değişikliği yapan barsak hastalıkları ve fistülleri iyi göstermesi ayrıca fonksiyonel transit süresi hakkında bilgi vermesi nedeniyle yaygın olarak kullanılmaktadır (99–102).
Çift Kontrast İnce Barsak Pasaj Grafisi
Baryumlu ince barsak incelemesini takiben, barsak lümeni içinde çözülerek gaz yapan ajanların verilmesi ile inceleme yapılır. Kontrast maddenin çekuma ulaşması sonrasında oral yolla 700–1000 ml gaz oluşturacak miktarda efervesan ajan verilir. Hasta sol yan ve hafif trendelenburg pozisyonuna getirilerek gazın ince barsaklara geçmesi sağlanır. Gaz genellikle 10 dakika içinde terminal ileuma ulaşır. Supin pozisyonda çift kontrast ince barsaktan kompresyon radyografileri alınır. Bu teknik ile barsak anslarının birbirinden ayrılması, gerekli lümen distansiyonu sağlanması ve mukoza pili yapısın değerlendirilmesi İBPG’ye göre daha iyidir (91,101).
Retrograd İnce Barsak İncelemesi
Nadir kullanılan bir inceleme yöntemidir. Kolonun yeterli miktarda baryum ve su ile doldurulmasından sonra kontrast maddenin ince barsaklara reflüsü ile gerçekleşmektedir. Mekanik ileus ile dinamik ileusu ayırt etmekte ve distal obstrüksiyonların gösterilmesinde etkilidir. İleostomili hastalarda da retrograd infüzyon daha iyi tolere edilir (91).
Peroral Pnömokolon İncelemesi
Bu yöntemde ileoçekal bölgenin ayrıntılı çift kontrast görüntüleri elde edilir. İBPG incelemesi esnasında sağ kolon baryum ile dolduktan sonra, hastaya 1 mg İV glukagon enjekte edilir. Glukagon ileoçekal valvden havanın geri kaçışını kolaylaştırır ve ince
barsaklarda hipotoni oluşturur. Daha sonra hastaya rektal yoldan çekum distansiyonu gelişene kadar hava verilir. Bu şekilde ileoçekal bölgenin ve terminal ileumun çift kontrastlı görüntüleri elde edilir. Peroral pnömokolon incelemesi, inflamatuar ince barsak hastalığı şüphesi varlığında distal ileumu daha iyi değerlendirmek için, ayrıca pelvik adhezyon ve çekum patolojisi olan hastalarda İBPG’ye yardımcı olarak kullanılır (101).
Konvansiyonel Enteroklizis
Baryumlu ince barsak grafileri ile önceleri ince barsakların pozisyonu, uzunluğu ve pasaj zamanı değerlendirilmiş ancak süperpozisyonlar nedeniyle iyi görüntüler elde etmek mümkün olmamıştır (103). 1939 yılında başlayan tek ve çift kontrastlı inceleme denemeleri ve entübasyon teknikleri gelişerek 1978–79 yıllarında Herlinger tarafından modifiye edilmiş ve günümüzde de kullanılan “enteroklizis” yöntemi ortaya çıkmıştır. Nazojejunal entübasyon sonrası baryum ve metilselüloz verilerek yapılan çift kontrastlı bu inceleme, ince barsak hastalığı tanısında halen seçkin yöntem olarak kullanılmaktadır (103,104).
Anjiografi
Selektif olarak yapılan çöliak ve mezenterik anjiografiler, GİS’in akut ve masif kanamalarında hemoraji odağının yerinin ve nedeninin tesbitinde büyük rol oynar. Diğer taraftan iskemik barsak hastalıklarında tromboembolik arteryel oklüzyonu veya azalmış arteryel perfüzyonu saptamada da anjiografiden faydalanılır (105,106).
Sintigrafi
Alt GİS kanamalarında, Tc-99m ile işaretli sülfür veya eritrosit kullanılarak kanamanın lokalizasyonu saptanabilir. Meckel divertikülünün tanısında da sintigrafik incelemenin önemli bir yeri vardır. Son zamanlarda Tc-99m ile işaretlenmiş beyaz kürelerle gerçekleştirilen sintigrafik incelemelerin inflamatuar barsak hastalığının yayılımını saptamada doğru bilgiler sağladığı görülmüştür (107,108).
Ultrasonografi
İnce barsak hastalıklarının spesifik tanısında ultrasonografi (US) genellikle kullanılmaz. Ancak nonspesifik abdominal yakınmaları ve abdominal kitlesi olan
hastalarda ilk inceleme yöntemi olarak sıklıkla kullanılmaktadır (91). Gaz barsağın US ile incelemesinde önemli bir engeldir. Ancak barsak duvarı inflamasyon veya neoplazm nedeni ile infiltre olmuş ise bu bölge rijit olacağından genellikle gaz içermez. Henüz barsakta gaz distansiyonu oluşmamış erken evredeki barsak obstrüksiyonlarında, benign veya malign bir nedene bağlı barsak duvar kalınlaşması ile intrensek veya ekzofitik kitlesel lezyonların belirlenmesinde, mezenter yapraklarındaki kalınlaşma ve lenfadenopatilerin tespitinde US faydalı bir yöntemdir (109,110).
Doppler US; Barsak duvar kalınlaşmasının iskemik ve noniskemik nedenlerinin ayırıcı tanısında yardımcı bir tekniktir. Kalınlaşmış duvarda akım saptanmaması iskemiyi düşündürürken, artmış kan akımının saptanması ve beraberinde duvar yapısında değişikliklerin bulunması inflamatuar patolojilere yönlendirir. Ayrıca inflamatuar hastalıkların aktivitelerinin belirlenmesinde de faydalıdır (111).
Bilgisayarlı Tomografi Bilgisayarlı tomografi (BT) tekniğinde kaydedilen
ilerlemeler günümüzde yüksek rezolüsyonlu görüntülerin elde edilmesine, deneyim bilgisindeki artış da bu görüntülerin daha iyi yorumlanmasını sağlamaktadır. GİS radyolojisinde mukozal ve intralüminal lezyonların değerlendirilmesinde baryumlu çalışmalar temel inceleme yöntemidir. BT, lezyonların intramural ve ekstraintestinal komponentlerinin, mezenterik, peritoneal, retroperitoneal ve solid organ tutulumlarının değerlendirilmesinde önemli bilgiler sağlar (112).
BT enteroklizis, yeni uygulanmaya başlanan bir tekniktir. Nazojejunal entubasyonu takiben barsakların pozitif kontrast madde (su, metilselüloz, dilüe baryum süspansiyonu) ile distansiyonu sağlanarak inceleme yapılmaktadır. Bu teknik, daha önce abdominal operasyon hikayesi olan hastalarda oluşabilecek intermitant ince barsak obstruksiyonlarının, Crohn hastalığının komplikasyonlarının ve açıklanamayan gastrointestinal kanamalarının etyolojisinin araştırılmasında değerli bilgiler vermektedir (113).
Manyetik Rezonans Görüntüleme
kullanılmaya başlanan bir tetkiktir. Konvansiyonel MR cihazlarının çekim sürelerinin uzun olması, peristaltizm ve solunum artefaktından etkilenmesi nedeniyle ince barsaklar net değerlendirilememekteydi. Günümüzde hızlı görüntülemeye izin veren gelişmiş MR cihazlarının kullanılmaya başlanması ile ince barsaklar daha iyi değerlendirilebilmektedir. MRG’de iyi bir ince barsak tetkiki yapabilmenin ön şartı yeterli barsak distansiyonunun sağlanmasıdır. Bu da ancak enteroklizis yöntemi ile mümkün olabilmektedir.
Manyetik rezonans enteroklizis (MRE) incelemesinde; hastaya floroskopi ünitesinde nazojejunal kateter takılır. Bu işlemin hemen sonrasında hasta MR cihazına alınarak %0.5’lik metilselüloz solüsyonu MR uyumlu pompa ile verilir. Yeterli distansiyon sağlandığında görüntüleme yapılır. MRE’nin en sık kullanıldığı durumlar; Crohn hastalığı, ince barsak tümörleri ve intestinal obstrüksiyonlardır. Konvansiyonel enteroklizisten farklı olarak barsak duvarı, ekstraintestinal yapılar ve tüm abdomen içi direkt olarak değerlendirilebilir. Barsak anslarının süperpozisyonu sorun oluşturmaz. Pelvis posteriorunda yer alan barsak ansları daha kolay değerlendirilebilir. Kolon ansları da aynı anda incelenebilir. Hasta sadece floroskopi sırasında radyasyon alır. Pahalı ve zaman alıcı bir inceleme olması, barsak segmentlerinin hareketinin iyi değerlendirilememesi konvansiyonel enteroklizise göre dezavantajlarıdır (114,115).
4.1. Kolon Anatomisi
Kalın barsaklar ileoçekal valvden anüse kadar uzanır. Yaklaşık olarak 150 cm (120-200cm) uzunluğundadır.
İleumun kalın barsağa açıldığı kısımda ileoçekal valv vardır. Bunun açıldığı düzeyin altında kalan barsak parçasına çekum, üstünde kalan kısmına çıkan kolon denir. İleoçekal valv yarım ay biçiminde alt ve üst dudaklardan oluşur. Bunlar ön ve arka frenula ile birleşirler. Çekum gaz ile şiştiği zaman bunlar gerilerek birbirine yaklaşırlar. Böylelikle, çekum içeriğinin ince barsağa geri dönmesini çoğu kez önlerler. Çekum kalın barsağın en geniş aynı zamanda duvarları en ince yeridir. Çıkan kolon 12.5-20 cm uzunluğundadır. Ön, iç ve dış yüzleri periton ile örtülüdür. Arka yüzü karın arka duvarı ve sağ böbreğin alt kutbu
ile temas halindedir. Hepatik fleksura düzeyinde, çıkan kolon karaciğerin altına gelince keskin bir köşe ile sola aşağıya öne doğru döner. Arkada sağ böbreğin alt kutbunun ön yüzü ile komşudur.
Transvers kolon, 40-50 cm uzunluğundadır. İlk 10-12 cm’lik kısmında ön yüzünü periton örter. Arka tarafta sırasıyla, sağ böbrek, duodenumun inen parçası ve pankreas başına gevşek bağ dokusu ile yapışmış haldedir. Bundan sonraki kısımda transvers kolonun her yanı periton ile sarılır. Splenik fleksura, bu sağ köşeye göre daha dar bir açı yapar ve daha yukarıdadır. Ön yüzü periton ile örtülüdür. Arkada, sol böbreğin ön yüzü ile direkt temas halindedir. Frenikokolik ligament ile diyaframa bağlıdır.
İnen kolon aşağıya ve içe doğru inerek sol krista iliaka hizasına kadar gelir. Burada sigmoid kolon adını alır ve ön, iç ve dış yüzleri karın arka duvarından gelen periton ile örtülüdür. Arka yüzü sol böbrek, kuadratus lumborum kası ve transversus abdominis kası ile komşudur. Sigmoid kolon, inen kolon ile rektum arasındaki kolon segmentidir. Sol krista iliaka kenarından başlayıp 3. sakral vertebra hizasına kadar uzanır, ilyak ve pelvik kısımlara ayrılır. Uzunluğu 15-60 cm arasında değişir. Sakrumun 3.parçası önünde rektum ile birleşir. Periton sigmoid kolonun her tarafını sarar, ortada bir mezokolon oluşturur. Kolonun bölümleri ve anatomik detayları Şekil 4.1’de gösterilmiştir.