FERMENTASYONLA ETİL ALKOL ÜRETİMİ ÜZERİNE ÇÖZÜCÜ ETKİSİ
Tam metin
Şekil


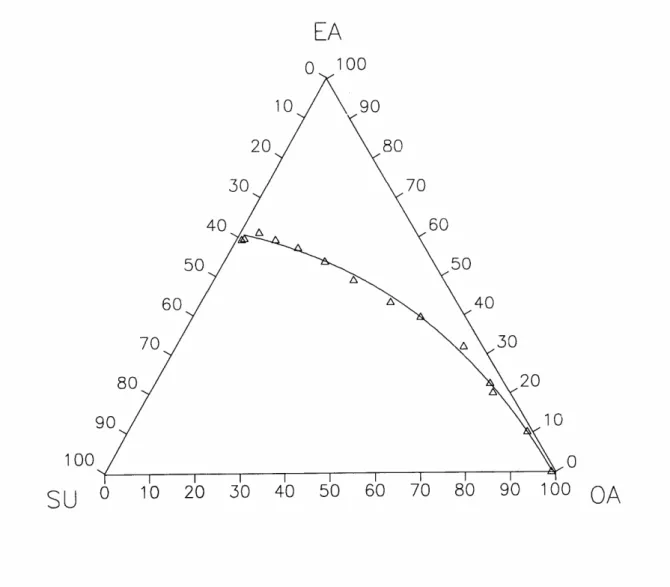
Benzer Belgeler
Cevdet Paşa 5 defa Adliye Nazırlığında bulunmuş ve pek çok kıymetli eserler vere, rek memlekete büyük hizmetlerde bulunmuş ve 1595 senesinde resmi ve
Bu çalıĢmayı yapmaktaki amacımız; yara yeri infiltrasyonunda kullanılan lokal aneste- zik ajanların yara iyileĢmesi üzerine etkilerinin ayrıntılı olarak incelenip etkin
Cumhurbaşkanı Kenan Evren, Yorgun Savaşçı filminin Milli Güvenlik Kurulu Genel Sekreterliği’nce Necdet Üruğ döneminde oluşturulan bir heyet
Gerçekleştirilen motor testleri neticesinde; dizel yakıtının, içersine % 20 etanol karıştırılan dizel yakıtının ve %15 ile %20 oranlarda gerçekleştirilen
Ayrıca hemofiliye bağlı spontan hematom; ekstremitenin uzun süre basınç altında kalması (aşırı dozda ilaç alımı ya da alkol alımı sonrası baygınlık vb.
The interesting aspect of the present case is that the patient was first considered to have confusion because of a history of ethyl alcohol intoxication with a period
• Kafa travması hikayesi olan , glaskow koma skalası 15 altında olan ; tedavi-gözlem sırasında mental durumda kötüleşme olan hastalara CT endikedir.. • Alkol veya ilaç
Alınan metil alkol miktarına bağlı olarak 4-15 ml dozda körlük ve 15- 100 ml dozda ölüm meydana