A. O. Vet. Fak. Dert:. 40 (4): 497-510 1993
vtRAL HASTALıKLARıN TEŞHİSİNDE
tMMUNOPEROKStDAZ
M. Çabaları Y. Akçaa
Im.munoperoksidase in the diagnosis oC viral disease.
Su~ary: Immıınoperoxidase assay is an alternative methodfor iden-tifying antigen and antiboriy, ıısed in eell eulture and histopathology studies an en{Yme-labeled antibody. In ıhis method, en{Yme eonjugated antibodies generate insoluble eolored products reacting with ehemieal substrate. This en{Ymatic reaetion can be visııalized by naked eye or by both of light and eleetron mic-roseope.
Özet: Jmmunoperoksidaz testi gerek histopatolojik gerekse hücre kültüTÜ [alışmalarında histo-kimyasal olarak antijen yada antikor tespitine yönelik ola-rak kullanılan alternatif bir yöntemdir. Bu yöntemde, enzim le konjuge edilen re-aktif/er substrat ile reaksiyona girerek renkli ürünler meydana getirmektedir. Bu enzimatik reaksiyon gö'zle yada basit bir ışık mikroskobu veya Elektron mikroskop ile değerlendirilebilmektedir.
Giriş
Enfeksiyöz hastalıkların tanısında, özellikle viruslar ve yavaş ço-ğalan bakterilerin kültürlerde üretilmeleri için uzun zamana ihtiyaç duyulduğundan, direkt etken izolasyonu Ye identifikasyonu yanısıra, Hemaglutinasyon İnhibisyon (HI), İndirekt Remaglutinasyon İnhi-bisyon (IRA), Agar jel presipitasyon (AGP), Komplement Fikzasyon (KF), İmmunoelektroforez (lE) gibi çok sayıda serolojik yöntem geliş-tirilmiştir (27).
Coons ve ark. (14) 1940 yılında fluorescein isothiocyanate ile işaretli antikorlar kullanarak dokular i~indeki antijenleri gösterme-yi başarmışlardiL Berenhaum 1958 yılında antikorları radyoaktif 1 Dr., Yüzüncü Yıl D., Veteriner Fakültesi, Viroloji Bilim Dalı., Van.
maddelerle işaretlemiş, Nakane ve Pierce'de 1966 yılında antikor-ların enzimlerk işaretlenebileceğini savunmuşlar vc denemelerinde başarılı olmuşlardır. Enzimlerk işaretleme yönteminde antijen-anti-kor reaksiyonu sonucu katı faza bağlanan enzim işaretli reaktiflerden yararlanılmaktadır. Değerlendirme enzim ile substratın oluşturacağı renk reaksiyonuna göre yapılıp, ortaya çıkan renkli ürünlerin miktarı, enzim işaretli re aktiflerin ve dolayısıyla katı faza bağlanan antijen veya antikor miktarını belirlemektedir (17, 27). Fluorescein isothioc-yanate ilc yapılan çalışmalarda özel mikroskoplara ihtiyaç duyulması, fluoresanmaddelerinzamanla aktivitelerini kaybetmeleri, ayrıca do-kularda bulunan otofluoresan özelliğin değerlendirmeyi güçleştirmesi Klcdeniyle, bu yöntemle sonuçların değerlendirilmesi subjektiftir (10, 2,4). Radyoaktif maddeler ile işaretli reaktiflerden yararlanılarak kulla-nılan Radioimmunoassay (RIA) 'in ise objektif bir tanı yöntemi olma-sına rağmen, radyoaktif maddelerin yarılanma süreleri, sonuçların de-ğcrlendirilmesindegama sayıcıları gibiözelaygıtların gerekliliği ve daha da önemlisi radyoaktif madde kullanımının sakıncaları bu duyar-lı yöntemin olumsuz taraflarıdır (13, 27). EnzimIerIc işaretleme yön-teminde, enzim işaretli reaktifkr uzun süre saklanabilmekte, sonuçlar b~liren renklcnmcnin şiddetine göre değerlendirilmektc ve direkt göz, basit bir İşık mikroskopu yada kolorometre iIc antijen veya antikorun respiti yapılabilmektedir (17, 24, 27). Bu üstüdükleri ncdeniyle virus, bakterı, mantar; parazit antijenleri ve antikorları yanında, immunog-lobulinler, serum proteinleri, tümör antijenleri gibi çeşitli maddelerin araştırılmasında enzimle işaretlemc yönteminden yararlanılmakta-dır (2, 7).
lmmunoperoksidaz yöntemi, enzimlerk işaretli reaktiflerin oluş-turdukları antijen-antikor kompleksinin histokimyasal olarak incelen-mesi esasınadayanır (2, 3, 4, 9, 24). Gerek histopatolojik çalışmalarda gerekse doku kültürü çalışmalarında immunoperoksidaz yönteminden yararlanılmakta ve kromojenIcrin meydana getirdikleri rcnkli ürünler ilc antijen yada ap.tikor tespitine gidilmektedir (2, 4, 12, 19, 24). An-!İjenlerin ultrastruktural lokalizasyonlarının saptanması amacıyla, İrnmunoperoksidaz ilc Elektron mikroskopi (EM) çalışmalarıda yapı-labilmektedir (13,24, 26). Eğer test materyalinin dilusyonları hazır-lanırsa, görülen en son renk dq'i;işiminin oluştuğu sulandırma basama-ğı o test materyalinin titresidir. Hesaplama Kaerber metodu vasıta-sıyla yapılır (8, 9).
VİRAL HAST.\L1KL\RI~ TEŞHİSİNDE İMMl'NOPEROKS1DAZ 499
Kuduzun teşhisi amacıyla yapılan bir çalışmada (1), direkt im-mur.operoksidaz (IP) ve fluorcsan antikor tekniği (FAT) karşılaştırıl-mış ve birbirir.e paralel sonu~Jar elde edildiği bildirilmiştir. Diğer bir çalışmada isc
(LO)
,direkt I P, direkt FAT ve Seller boyama yöntemleri kuduzun teşhisi amacıyla kullanılmış, FAT ve iP yöntemlerinin Sel-ler boyamadan daha duyarlı olduğu ve FAT'daki dezavantajlardan dolayı IP'nın FAT'ın yerini alabileceği savunulmuştur. Hyera ve ark. (8) Bovine viral diarrhea (BVD) virosu nötralizan antikodarının sap-tanması amacıyla Neutralizin.g peroxidasc-linked antibody (NPLA) \T Mikro nötralizasyon testlerini (MNT) kullanmışlar ve sonuçta test edilep. 425 sığır serumundan :t\PLA ilc%
48, MNT ile%
45'inin po-zitif olduğunu saptamışlardır.İmmunoperoksidaz yönteminde aşağıda belirtilen teknikler kulla-nılmaktadır (2, 8, 15, 16, 1, 24).
1 . Direkt yö~tem 2. İndirekt yöntem
3. Peroksidaz anti-peroksidaz (PAP) yöntemi
4. :"Jötralizasyon immunoperoksidaz yöntemi (NPLA)
j. Avidin-Biotin immunoperoksidaz yöntemi
a) Direkt Avidin-Biotin Peroksidaz Kompleks (ABC) yöntemi b) İndirekt ABC yöntemi
c) Avidin-Biotin işaretlerne yöntemi 6. İmmunoperoksidaz plak yöntemi
a) Direkt immunoperoksidaz plak yöntemi b) İndirekt immunoperoksidaz plak yöntemi
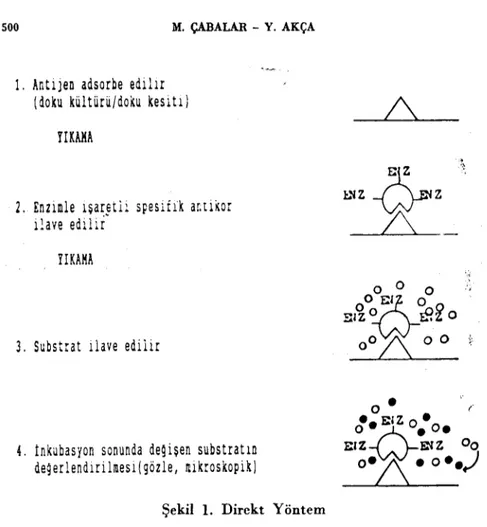
1. Direkt Yöntem
Antijene spesifik an.tikorlardan yararlanarak antijen varlığının ortaya konması esasına dayanır. Bu yöntemde spesifik antikor peroksi-daz ile kimyasalolarak bağlanır. Hazırlanan bu konjugat antijenle reaksiyona girerek, substratm ilavesiyle antijenin lokalize olduğu alan-larda renkli bir presipitat meydana getirir (Şekiıı). Meydana gelen rengir. şiddeti örnekteki <ıptijen miktarı ile orantılı olacaktıi". Duyarlı bir yöntem olmasına rağmen, her ar.tijen için spesifik bir antikora ihti. yaç göstermesi direkt yöntemin yaygın olarak kullanılmasını önlemek-te \'e indirekt yönönlemek-temin önemini artırmaktadır
cı,
2, 6, 10, 24).)1. AntıJen adsorbe edılır (doku kültürü/doku kesıtı)
YIKAMA
2. Enzımle ışaretli spesifik a~tıkor ılave edılir'
YIKAMA
3. Substrat ilave edilir
/\
~--ı:."iZ~Z7\
o o o o:>~ o ~1~~B~O001\
o o "4. !nkübasyon sonunda degişen substratın degerlendirilmesi(gözle, mıkroskopik)
Şekil
ı.
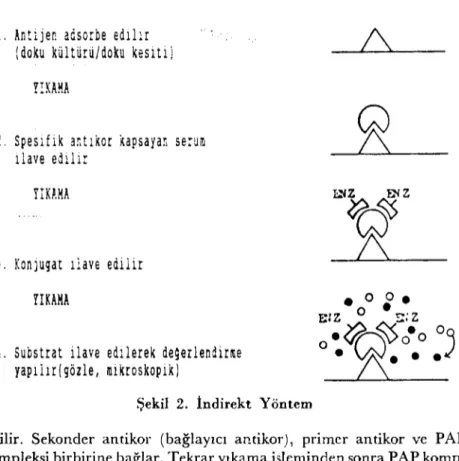
Direkt Yöntem 2. indirekt YöntemBu yöntemde, konjuge edilmemiş antikor numunede antijene bağ-larıır. Reaksiyona girmeyen maddelerin yıkama ışlemiyle ortamdan uzaklaştınlmasından sonra, konjuge edilmemiş antikora karşı elde edil-miş anti-antikorların işaretlenmesiyle hazırlanan spesifik konjugat ilave edilir. Konjugat ilk aşamada meydana gelen antijen-antikor komplek-sindeki antikora bağlarıır. Sonra bu lokalize reaksiyona substrat ilave edilir (Şekil 2). Meydana gelen ref'.gin şiddeti örnekteki antijen mikta-rı ile orantılıdır (2, 6, 24).
3. Peroksida::: Anti-Peroksida::: (PAP) Yöntemi
Bu yöntemde primer antikor, sekonder arıtikor ve PAP kompleks olmak üzere 3 reaktife ihtiyaç vardır. Primer antikor direkt olarak antijene bağlarıır. Yıkama işleminden sonra sekonder antikor ilave
VİRAL H..ASTALlKLARIN TEŞHİSİ~OE tMMUNOPEROKStOAZ 501
, Antijen adsorbe edılır
(doku kültürü/doku
kesıtı)
EKAMA
2.
Spesifık ar.tıkor kapsaya:. serum
ılave edılır
YIK.l.MA
3.
KonJugat ılave edilir
YIKAMA
4.
Substrat ilave edılerek de~erlendirme
yapılır(gözle,
ffiıkroskopık)
Şekil 2. İndirekt Yöntem
1\
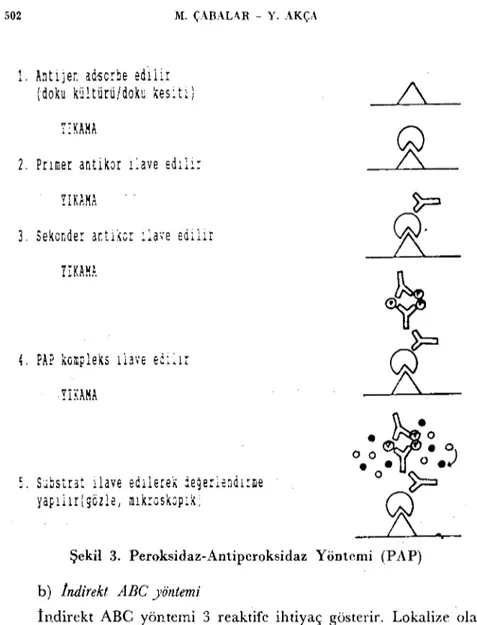
edilir. Sekonder antikor (bağlayıcı antikor), primer antikor ve PAP kompleksi birbirine bağlar. Tekrar yıkama işleminden sonra PAP komp-leks ve daha sonra da substrat ilave edilir. Test sonunda beliren ren-gin şiddeti numunedeki antijen miktarı ile orantılıdır (Şekil 3). Du-yarlı olması ve enzim ilc işaretli reaktifIere gerek olmaması bu yönte-min üstünlükleridir (2, 3, 4., 6, ll, 13, 24).
4. Avidin-Biotin lmmunoperoksida;::, Yöntemi
Avidin-Biotin ili~kisine dayanan bu yöntem, bir vitamin olan bio-tinin 4 molekülünün, glikoprotein olan avidin ile nonimmunolojik olarak birleşmesi esasına dayanır (2, 5, 21, 22).
a) Direkı Avidin-Biotin Peroksida;::, Kompleks (ABC) yöntemi
Bu yöntemde biotinle işaretli antikor direkt olarak antijene bağ-lanır. Reaksiyona girmeyen maddelerin yıkama ile ortamdan uzak.laş-tırılmasından sonra, avidin-biotin peroksidaz kompleks (ABC) ilave edilir. Substrat ilavesiyle antijenin lokalize olduğu danlar görünür hale gelir (2, 5, 2
ı,
22).ymMA
YIKAMA
2. Prımer antikor ı:ave edıl~:
o:-~~oı
• ~o • ..,
O~
~
.
Şekil 3. Pemksidaz-Antiperoksidaz Yöntemİ (PAP)
c SJbstrat ılave edılerek iegerlendı:me
yapılır(gözle, ffiıkrcskop:k,
1. Antı]e~ ad~c~be
edılir(doku k~ltürü!doku kes:tı)
3,
Sekcnder a~tı~cr ::a,e
edılır4. PA? kOffipleks ıla,e e::.ır
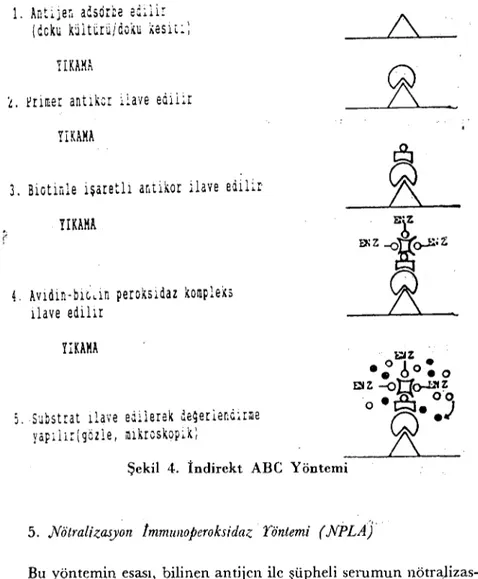
b) lndirekt ABC yöntemi
Indirekt ABC yöntemi 3 reaktife ihtiyaç gösterir. Lokalize olan antijen için spesifik primer antikor direkt olarak antijene bağlanır. Yıkama işleminden sonra biotirtle koııjuge edilmiş sekoıı.der antikor ve bunu takiben de ABC ilave edilir Dahasonra substrat ilave edilerek değerlendirme yapılır (Şekil 4) (2, 5, 21, 22).
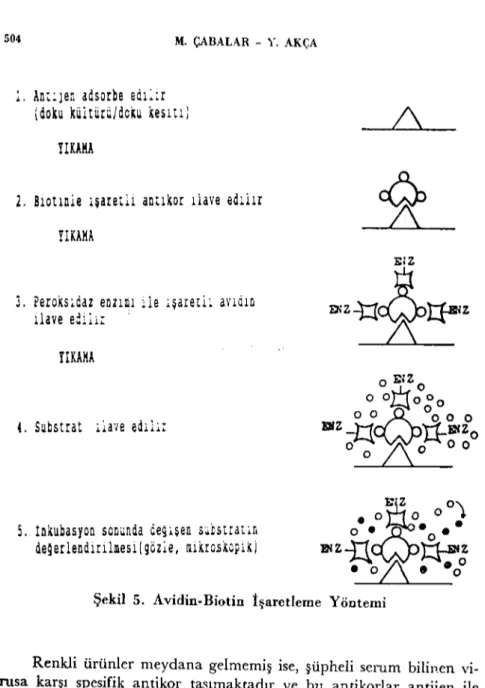
c) Avidin-Biolin /şaretlemc yöntemi
Bu yöntemde biotinle işaretlenmiş antikor direkt olarak antijene bağlanır. Yıkama işleminden sonra enzimlc koııjuge edilmiş avidin ilave edilir. Substrat ilavesiyle lokalize reaksiyon görünür hale getiri-lir (Şekil 5) (2, 21).
vtRAL HASTALıKLARı:'! TEŞHİst:'!DE tIDIUNOPEROKStDAZ 503
(
1.
Antije~
adsdrbee~~li:
(ccku k~lt~rüjdoku kesı~:;
YIKAMA
~. ~riffierantıkGr ılave edılır
YIKAMA3. Biotinle işaretlı autikor ilave edilir
YIKAMA
4,
Avıdin-bıt.ın peroksıdaz kompleKs
ılave ediln
YIKAMA
j,
Substrat ılave edilerek degerle~dır~e
yapılır(gczle, mıkrcskoplK;
Şekil 4. İndirekt ABC Yöntemi
1\
5. Nötralizasyon ImmUlıoperoksidaz Yiinlemi
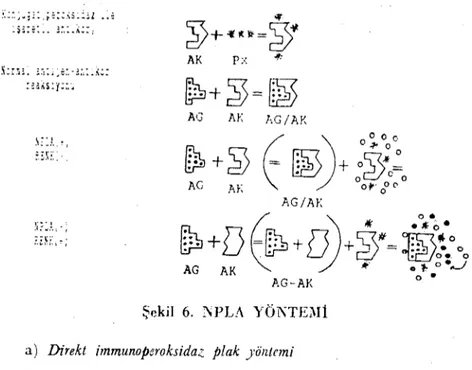
(NPLAY-Bu yöntemin esası, bilinen antijen ilc şüpheli serumun nötraJizas-yona bırakıldıktan sonra, nötralizasyonun meydana gelip gelriı~diği~, nin immunoperoksidaz ilc kontrol edilmesidir. Testin ilkaşaması olan nötralizasyondan sonra, l)ilinen virus ile şüpheli serum dilusyonlaİ'l hüc" re kültürüne inokule edilir. Daha sonra bu hüere kültürü antijene' spe-sifik konjugatla karşılaştırılır ve substrat ilavesiyle renkli ürünlerin meydana gelip gelmediğinin kontrolü yapılır (Şekil 6) (8,25).
Renkli ürünler meydana gelmiş ise; şüpheli serum bilinen virusa karşı spesifik antikor taşımamaktadır ve virus peroksidaz ile işaretli antikorla birleşmiş demektir.
l.
An~:)en
adsorbeedı~:r
(doku kültürü/dcıu ıesıtl)
YIKAHA
ı.
Bıotınle ışaretlı antıkor ılave edılır
YIKAMAJ.
Peroksidaz enzı~ı ıle işaretli avıdın
ılave e:ılı~YIKAMA
4. Substrat
ilave edı:i:
1\
5. lnkubasyon scn~nda degışen s~bstratın
degerlendırilmesı(gözle, mıkroskopıki
i;1
0'\ o o o ~•
•
FSZ-hd5~Z
• oZ'S ••
00Şekil 5. Avidin.Biotin İşaretlerne Yöntemi
Renkli ürünler meydana gelmemiş ise, şüpheli serum bilinen vi-nısa karşı spesifik antikor taşımaktadır ve bu antikorlar antijen ile birleştiğinden, peroksidaz ile işaretli antikodar antijen1c birleşmemiş demektir.
6. Jmmunoperoksidaz Plak Yöntemi
Hücre kültüründe, yarı katı vasatın etkisiyle, enfeksiyon yerinde lokalize olarak çoğalan vİrusun immunoperoksidaz yöntemi ile göste-rilmesi esasına dayanır (l3,
ı
5, 20).ytRAL HA~TALIKL\Rı!\ TEŞHt~t;'WE ıMML;;\OPEROK~ıDAZ 5(15 :::;.~..;~:.;~:~.\s..:;ı .. : : Ş ~::: -. :~.:.~::; S::.,L ,:::,,:: .. ":.:.,;: :'"'s:) ;:.~ S::,ı.,., ~.:;~::,. 1" •• 1 ;1: ~:'; •i :.:.~::\~;
Şekil 6. ı\PLA YÖKTEi\Iİ a) Direkt immunoperoksida;. plak )'ölltcmi
Bu yöntemde petrilerde üretilen hücre kültürlcril'.e ,'irus sulan-dırmasından inokule edilir ve inkuba~yona hırakılır. İnkııbasyop. so-nunda kültür vasatı uzaklaştırılır vc her bir pctriye vasat -]- agaroz karışımı hücre üzerine yayılarak dOi1uı~.caya. kadar bekletilir. Petrilcr içindeki donmuş agaroz 3.-4 gün sonra hücreye zarar vermeden uzak-l~tırılır. Fikzasyonu takiben ilave edilen konjugat aP.t~jerıle reaksiyona girecek ve substratın ilavesiyle virusun lokalize olduğu alanlarda sı-nırlı ve renkli üreme odakları görülecektir (I3, 20).
lı) Indirekt immunopcroksidaz plak )lontcmi
Bu yöntemde ilk aşamada antijen pleytlcri hazırlanır. Bnnun için önce pleytlerde hücre üretilir. S071ra virus inokule edilerek inkubasyo-na bırakılıf. İnkubasyon sonrası hücre üzeriEC' agaroz dökülür ve 4-5
gün sonra agaroz hücreye za,ar vermeden uzaklaştırılır. Fikzasyon-dan sonra plcytler kullanılana kadar -70'C'de 12ay süre ile muhafaza edilebilir. Gerektiğinde pleytlcr dondurlıeud",-ı çıkarılır, çözülür ve şüpheli serum ilave edilerek inkubasyona bırakılır. İI'.kubasyon sonrası ko~ıjugat, daha sonra da substrat solusyonu ilave edilerek değerlendir-me yapılır. Bu yö:,ltem, hücre kültürüne adapte edilebilen ve ürctilc-bilen viruslarla uygulanabilmektedir (I 6).
İmmunoperoksidaz yönteminin kullanımında çeşitli maddeler testin duyarlılığında roloynamaktadır. Bunlar,
Koııjııgrıt
Koııjugatın hazırlanmasında enzim (horseradislı peroxidasc: HRP), enzime doğal kurucu (işaretlcnecek antikor yada antijen) ve bağlanma için kullanılacak kimyasal maddeye (glu teraldehid, bcn-lOkinon) ihtiyaç vardır. Bağlanmada kullanılan maddeler aracılığı ile enzim ve immunoreaktiflerin (antikor, antijen) kovalcnt bağlan-maları sonucunda konjugat elde edilir. Bir enzim molekülü çok sayı-da substrat molekülü ile reaksiyona girerek r,~nkli ürünler oluşturur. Bu nedenle enzimle i~aretli reaktiflerin (konjugat) özellikleri test so-nucunu etkilediğinden, kullanılan enzimlerin kolay hazırlaıı.abilmele-ri, stabil ve yüksek aktiviteye sahip olmaları gerekir (5, 24, 27).
Peroksidrız
Peroksidaz 40.000 molekül ağırlığında bir hemaglikoproteindir. Peroksidazın küçük hacimli olması, pahalı olmaması ve çok stabil ol-ması kullanımını cazip hale getirmektedi.r. Konjugasyon sonunda peroksidazın aktivitesinde kayıp da az olmaktadır. Peroksidazın kulla-rumdaki dezavantajı ise spesifik substratlarının kansorejen özelliğe sahip olmalarıdır. Peroksidaz bitkisel dokularda bulunur ve ba5lıca kaynağı yabani turbdur (2, 26).
Avidin-Biotiıı
Konjugasyon sırasında reaktifin ve enzimin substratı bağlama böl-gelerinin bir bölümünde blokasyon meydana gelir. Bu durum konjuga-tın immunolojik ve .~n.zimatik aktivitesinde kayıplara neden olur. Bu tip aktivasyon kayıplarını önkycn kofaktör sistemler geliştirilmiştir. En ~:ok kullanılanı Avidin-Biotin. sistemidir. Biotin molekül ağırlığı 244 olan bir monokarboksilik asittir. Birçok mikroorganizma ve bitki yaprakları tarafından sentezleniL Yumurta bol miktarda biotin içe-rir. Avidinin ise molekül ağırlığı 70.000 olup, birbirine benzeyen 4 alt birimden oluşmuştur. Hcl' alt birim bir biotini bağlayabilir. Avidin ç.iğ yumurta akında bulunan bazik bir glikoproteindir (2, 5, 21).
Substl'a! Soluıyonları
Su bstratlar enzimlerle reaksiyona girerek immun kompleksin varlığını ortaya koyan maddelerdir. Enzimler su bs tran ürüne
dönüş-vtRAL HA~TALIKLARI:'\ TFŞHtsİi\'OE t:\BW'\OPERUKStOA7. 507
türerek katalizör görevi yaparlar. Enzim (E), Suhstrat (S), Ürün (Ü) ile gösterilirsc,
E
+
S - -- --~> E . S --- -- - -~- Ü+
E',' o
Enzim-ı.-uhstrat reaksiyonu ortamdaki enzim miktarına bağlıdır. Enzim (peroksidaz) tükenmez ve substratın (HzÜz) diğer molekülleri ile tekrar reaksiyona girerek daha çok renkli ürün meydana getirirler. Tek bir Horscradish pero:..:idasc (HRP) cp,zim molekülü bir dakikada substratın 100.000 molekülü ilc reaksiyona girerek gözle görülebilen ürün meydana getirebilmektedir (2, 24). HRP
+
H20Z - -o' HRP H:P2 t Elektron donor (elektron verici) rcnkli ürün -L HR P o H10Enzim reaksiyonunda elektron donor olarak kullanılan birkaç renk verici madde (kromojen) vardır ('rablo 1) (2, 4, 8, 9, 24).
Tablo
ı.
Substrat solusyonları ve oluşturdukları renkler. Enzim .--- Substr~ts()lusyoıı~_._---_._._---rt~-~k : 3,3 diaıııinobenzidin tctrahvdr()clıoloridı~' i (DAB)+
Hz02 • i Kahverengiı
, i ._---_._--- _..•.._---.._---3-aınino 9-cthy / carha,.;ole (AEC)
+
H20z:
Kırmızı ii
---.- ---_ ..._..-1
Peroksidaz 14-chlom ı-naphtol (Chloro-Naphtol)
. -+
HzOz MaviP-phcııylencdiaminc dihydrochlııridc.' ~
i pyrocatechol (Hanker- Yatcs)
-+
H20'? • Mavi-Siyahi
_____
.l
Or~~_~~_~idine(O_~~~~di~et-=t-~~~~~~=-l_~a~'i'=~-=i
Sonuç
Bu derlemede özellikle viral hastalıkların teşhisindc bütün dünya-da laboratuvar tanı yöntemi olarak kullanılan immunoperoksidaz tes-ti ilc ilgili farklı teknikler incelcnmiş YC hunlarınu ygulanabilirliklcri tartışılmıştır. Ayrıca immunoperoksidaz yöntemi diğer tanı yöntcmle-ri ilc de karşılaştırılmıştır.
Kavnaklar
1. Anjaria, J.M., Jhala, Ci. (1985). Immurıopernxidas€ rcaction ın di. (lgrıosis of rabies. Int.. .J. Zoon., 12: 267-<~75.
2. Bourne, ,LA. (1983). Handbook of im1llunopcroxide.~a staırııng mct-horis. Immunochemistry Lahoratory. Dako Corporation.
3. Cherringıon, J.M., Ghallli, H.V., Sawyer, M.M., Osburo, B.I. (1985). Delection of viral antijcns in bluetollque virus infeeted ovine tissue using thc peroxida.~c.antı:pl!roxidase tf!Clıniqııe. Am . .1. Vet. He~. ,J,6: 23:>6-~3:i9.
L (;imeııo, E.J., Nosetto, E.O., ~Iarıin, A.A., Galois, C,M., Ando, Y., Elchcverrigaray, M.E. (1987). Demostration of Equine Herpes Virus ( EHV-I) in histolo{{ical section and tiSSllC cu/tl/res by the peroxidase-antiperoxidase (PAP) tcchnique. J. Vet. Med., H: 74,O-ı,t2. ;). GucsdQn,
.ı.L.,
Ternynck, T., Avrameas, S. (1979). The use ofavidin-biotin intcraetion in immıınoen:ymatic tcehniques. J. of Histoche. and Cytoch., 27 (8):1131-1139.
6. I1ydel'man, E. (1979). imnııınoperoxidase tı!chnique in histopatlıology : ııpp/ications, methods und ı:orıtrofs. .Jonrnal af Clinical Patholagy, 32:971-978.
j. Hill, A.C. (1978). Demostration of Mycoplusıııas in tissue by the
immu-noperoxidase teehniqııe . .1. of inf. Disease., 137 (2): 152-154. 8. Byera, J.M.K., Liess, B., Fl'ey, H,R. (1987). A Direkt
Neutralizing-Peroxidase-Linked Antibody (Issay fot dR/edion and titration of anti-bQdies to Bovi,,~Viral /)ial'l'1ı()c(L6.rııs. J. Vet. Med., 34: 227-237. 9. Kalz, J.B., Kuheman, L., .Pemherton, J., Selımen, 1\1.,J. (1987).
De-teetion of bovine virus diarr/ıea virus in eell culture usiııg an immu-noperoxidase teehnigue. Vctf~rinary Micwbiology, 13:1:>3-157. 10. Kolwal, S., Narayan, K.G. (i 9R5). Direkt i mmruıopcroxidase test ın
the diagnosis of rabies -(in alternaÜve to fluOT'eseent antibody test. lut. J. ZOOIl., 12 (J): lJO--W).
ll. Macaerlney, L., MacarlDe)', C.M. (1986). Canine parvovirus: develop-ment of immunof/uorezcencc a"d imm.wzopernxiı1asc techniques. Res. Vet. Sci., 40: 201-208.
V1R.\J. TBSTALJKL.\HI" n:şnhti\"f)E İM~IF,OPEHOKSjDAZ 509
12. Miry, C., Ducatelle, R., Tboonen, H., Hoornes, J. (1983). Immııno-peroxidase study of canine distemper virus pneumonia. Res. Vet.
Sci., 34:1.15-11-8.
13. Moriarty, G.C., Michael, C.M., Sternberger, L.A. (1 9n). lJltrastruôtural immunocytochemisıry 1l'ith ımlabcled antibodie.~ and ıhr peroxidase-antiperoxidase ı:omplex. A technique more sensitivr than radioimmıı-noassay. J. Histochl'. aud Cytoclır., 21(9): 825-833.
14. Özcel, M.A. (1978). Immunofuloresans 1'1' parazitolojide uygulamasi, Ege Üniversitesi Tıp Fakültesi Yayını, No. 108,. Ege Üni. Bamn-evi.
15. Pan, I.C., Huang, T.S., Hess, W.R. (1982). iYen method of antihody deteetion by indirekt immunoperoxidase plaque stnining for serodiag" nosis of Afriean Sıvine Fever. J. Clinical Microbio., 16 (4):650-655. 16. Pan, I.C., Schimizu, M., Hess, W.R. (1978). African Sıvine Fever:
Mieroplaque assay by an' immunoperoxidase method. Am . .J. Vet. Res., 39 (3): 491-497.
ı
7. Piroid, R., Lombard, M. (1980). Les ınethodes immunoenzymatiqves et leurs applieations serologives. Revue Med. Vct., 131 (1): 25-42. 18. Rai, A., Prasad, I.J. (1980). Jmmunoperoxidase technique in rapid detection of Foot and JlI/ounth Disease t,irus. Indian J. Anim. Sci., 50 (ll): 957-960.19. Rodriguez, M., Heinlein, A.S., Ruiz, M., Metzler, A.E., Sehudel, A.A. (1989). Detection of bovine herpesvirus type 1 1Jia an immuno-peroxidase method, using monocional anıibodies. Am. J. Vet. Res.,
50 (5):619-621.
20. Sanders, G. (1991). Charakterisierııng zytopathogener und nichtzy-topathogener bioıypen unler Sıaırınıen / isolaten des B VD-virus in ei-nem lmmılnoplaque-tesı. IllHugural-Dissertation. TierartIiche Hoch-schule Hannover.
21. Su-ming, USU., Raine, L., Fanger, H. (1981). A comparaıive study of ıhe peroxidase-antiperoxidase method md an Avidin-Bioıin Conıp-lex meılwd for studying polypeptid hormon es wiıh Radioimmonoassay antibodies. Am. J. elin. Pathol. 75: 734.-739.
22. Su-ıning, HSU., Raine, L., Fanger, H. (1981). Use of avidin-bioıin-peroxidase complex (ABC) in immunoperoxidase ıechniques: A
parisoıı bptll'een A Be and Uıılabelad antibod)' (PA P) procedurps. ]. Histoch. and Cytneh., 29 (4): 577-,580.
23. Sutmoller, P., Cowan, K.M. (1974). The detl'ctl~ollof Foot-and ,UOIlIlth-Disease virus antigl'lls ı:n iı~rected ecU cultures by immıınoperoxic1use terhniqııes . .T. Gen. Vi ro!. , 23: 287-291.
24. Taylor, C.R. (1978). lmmlUloperoxidlıse techniques. Arclı. Patho!' Lab. :\1('(1., 102:113-]21.
2,5. Terptra, C., Bloemhraad,
:M.,
Gielkend, A.L.J. (1984). The lleutralizing peroxidase-linked assay for dptection of anıibid," againsı Sıdne Fel'er virus. Veterinary Microbiology 9:11 3--120.26. Ward, A.C.S., Kaerberle, M.L. (1984). Use of an immıınoperoxidase stain for the demostration of bOVl'neriml diıırhea virus by light and elec-tron mieroscopies. Am. ]. Vet. Hes., 4,5: 165-169.
27. Yolken, R.H., Leililter, F., Whitcomb, L., Davis, D., Mears, M.ı. (1983). Enzyme imlllunoassay for the diagntJsis oflJiml infeetions. Ann. N.Y. Aead. Sei., 420:37]-390.