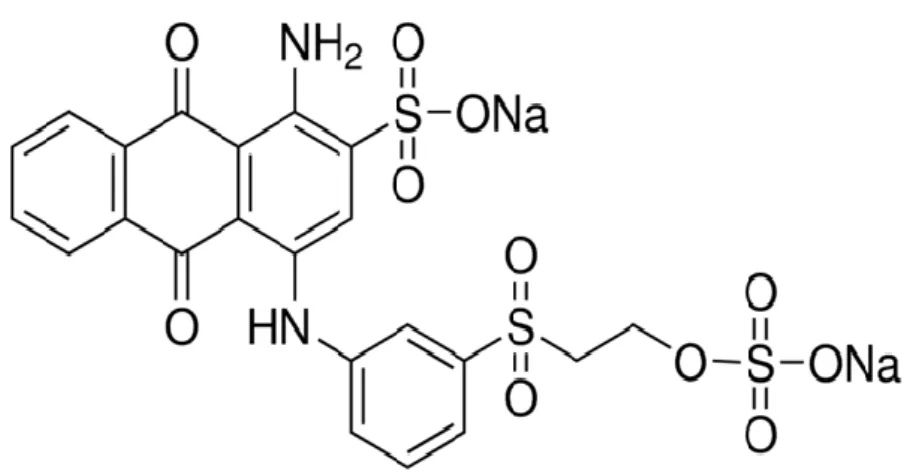
Farklı adsorbanlar kullanılarak atık sulardan reaktif boyaların gideriminde adsorpsiyon koşullarının araştırılması
Tam metin
Şekil
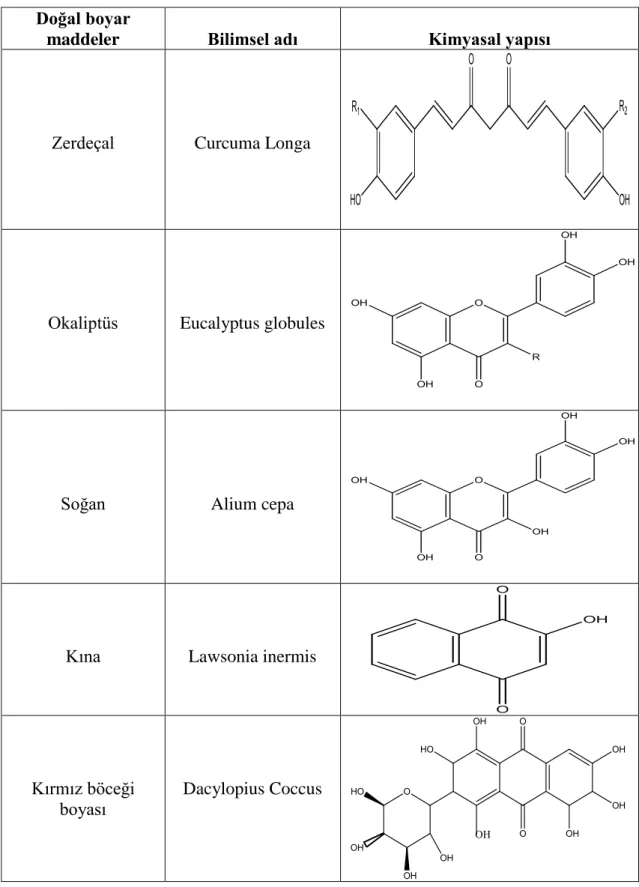
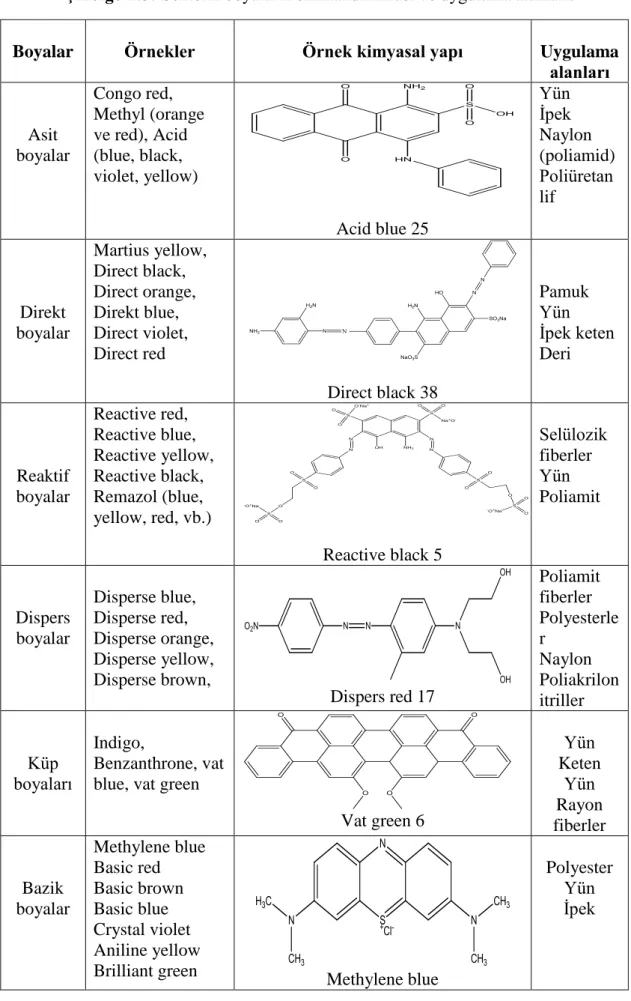
Benzer Belgeler
This work reports on the temperature- dependent performance of a monolithic microwave inte- grated circuit (MMIC): an AIGaN/GaN high electron mo- bility transistor
proposed models show that artificial neural networks can be used efficiently in the analysis and prediction of air quality.. The
Araştırmacı tarafından geliştirilen, çoktan seçmeli 20 maddelik “Geometrik Şekiller ve Cisimler Başarı ve Kalıcılık testi” nin geçerliliğini ve
(2008), “Bulanık Çok Kriterli Karar Verme Yöntemleri ve Uygulama” Pamukkale Üniversitesi, Sosyal Bilimler Enstitüsü, İşletme Ana Bilim Dalı, Sayısal Yöntemler
Bu sistemde hem klasik kolonda olduğu gibi kolonun altından hava verilmekte hem de pülpün jet hareketi ile atmosferden hava emilerek mikro kabarcık üretilmektedir..
In the direction of this purpose, this study focus on providing information on the characteristics of SMEs, motivations, stages, advantages and disadvantages of
Araştırmada “Sosyal bilgiler ve sınıf öğretmenliği bilim dallarında öğrenim gören bütün kademelerdeki adayların etkili birey yetiştirmede aile faktörüne
Za ten vefatında bilhassa Fransız gazete - leri büyük bir AvrupalI devlet adamı - nin zıyâından bahsederken Ali Paşa ' -.. Sadrazam Ali