T.C.
SELÇUK ÜNĠVERSĠTESĠ FEN BĠLĠMLERĠ ENSTĠTÜSÜ
TÜRKĠYE’DEKĠ GLYCYRRHIZA L. TÜRLERĠNĠN KROMATOGRAFĠK
YÖNTEMLERLE KĠMYASAL BĠLEġĠMLERĠNĠN VE ANTĠOKSĠDAN
KAPASĠTELERĠNĠN BELĠRLENMESĠ Yavuz Selim ÇAKMAK
DOKTORA TEZĠ Biyoloji Anabilim Dalı
EYLÜL-2011 KONYA Her Hakkı Saklıdır
iv
ÖZET DOKTORA TEZĠ
TÜRKĠYE’DEKĠ GLYCYRRHIZA L. TÜRLERĠNĠN KROMATOGRAFĠK YÖNTEMLERLE KĠMYASAL BĠLEġĠMLERĠNĠN VE ANTĠOKSĠDAN
KAPASĠTELERĠNĠN BELĠRLENMESĠ Yavuz Selim ÇAKMAK
Selçuk Üniversitesi Fen Bilimleri Enstitüsü Biyoloji Anabilim Dalı
DanıĢman: Prof. Dr. Abdurrahman AKTÜMSEK 2011, 113 Sayfa
Jüri
Prof. Dr. Abdurrahman AKTÜMSEK Prof. Dr. Ahmet DURAN Prof. Dr. Muhsin KONUK
Doç. Dr. Atilla ARSLAN Yrd. Doç. Dr. Haluk ÖZPARLAK
Glycyrrhiza L. (meyan) antik çağlardan beri geleneksel tıp içerisinde bulunan ve en yaygın kullanılan tıbbi bitkilerden birisidir. Bu çalışma Glycyrrhiza taksonlarının farklı kısımlarının (toprak üstü ve kök) antioksidan aktiviteleri, uçucu yağları ve yağ asidi kompozisyonu üzerine odaklanmıştır. Antioksidan kapasite testleri Glycyrrhiza taksonlarının methanol ekstraktlarının antioksidan aktivitesini değerlendirmek amacıyla yapılmıştır. Ekstraktlara antioksidan aktivitelerini belirlemek için total antioksidan kapasite (fosfomolibdat testi), β-karoten/linoleik asit test sistemi, serbest radikal süpürme etkinliği (DPPH), demir ve bakır iyonları indirgeme gücü (CUPRAC) olarak adlandırılan 5 farklı test sistemi uygulanmıştır. Her bir ekstraktın toplam fenolik ve flavonoid içerikleri de Folin-Ciocalteu reaktifi ve alüminyum klorid kullanılarak belirlenmiştir. G. glabra L. var. glabra L.‟nın toprak üstü kısımları en yüksek fenolik içerik (399.18±1.98 mg GAE/g), toplam antioksidan kapasite (342.66±5.34 mg AE/g), serbest radikal süpürme etkinliği (DPPH) ve demir indirgeme gücüne sahip olarak bulunmuştur. İlaveten G. glabra var. glabra‟nın köküde en yüksek flavonoid içeriğine (315.30±6.27 mg RE/g) sahiptir. G. iconica Hub.-Mor.‟nın kök ekstraktı en yüksek linoleik asit oksidasyon inhibisyonu göstermiştir. Bakır indirgeme gücü metodunda, G. glabra L. var. glandulifera (Waldst. Et Kit.) Boiss.‟nın toprak üstü kısmı diğer taksonlardan önemli oranda yüksek bulunmuştur. Genel olarak Glycyrrhiza taksonlarında toplam fenolik içerik ve çeşitli antioksidan aktiviteleri arasında pozitif bağlantı gözlenmiştir.
Glycyrrhiza taksonlarının toprak üstü ve kök kısımlarından elde edilen uçucu yağlar Gaz Kromatografisi Kütle Spektroskopisi (GC-MS) sistemleri ile analiz edilmiştir. Major bileşenler hexanal, β-pinene, furan-2-pentyl, benzaldehyde, 4-terpineol, 1-pentylcyclobutene, acetophenone, α-caryophyllen, naphtalene, 1-phenyl-1H-pyrazol-3-amine, m-cresol, nerolidol, hexahydro farnesyl acetone, E-neryl
v
linalool, 1-tetracosanol, p-hexylacetophenone, phytol, 4-pyridinecarbonitrile, dimethylamine ve n-hexadecanoic acid olarak belirlenmiştir.
Bu taksonların yağ asidi profilleri Gaz kromatografisi Alev İyonlaşma Dedektörü (GC-FID) ile incelenmiş ve 22 yağ asidi belirlenmiştir. Palmitik, linoleik ve linolenik asitler temel yağ asidi bileşenleri olarak tespit edilmiştir.
Bu çalışmanın sonuçları Glycyrrhiza taksonlarının toprak üstü ve kök kısımlarının metanol ekstraktlarının güçlü antioksidan aktiviteleri ve faydalı yağ asidi profillerinden dolayı kolay elde edilebilir doğal antioksidanların kaynağı olarak, muhtemel gıda katkısı olarak veya farmakolojik endüstride kullanılabileceğini göstermiştir.
Anahtar Kelimeler: Antioksidan, Glycyrrhiza L., kromatografik teknikler, Türkiye, uçucu yağ
vi
ABSTRACT
Ph.D THESIS
DETERMINATION OF CHEMICAL COMPOSITION BY USING CHROMATOGRAPHIC TECHNIQUIES AND ANTIOXIDANT CAPACITIES
OF GLYCYRRHIZA L. SPECIES IN TURKEY
Yavuz Selim CAKMAK
THE GRADUATE SCHOOL OF NATURAL AND APPLIED SCIENCE OF SELÇUK UNIVERSITY
DOCTOR OF PHILOSOPHY IN BIOLOGY
Advisor: Prof. Dr. Abdurrahman AKTUMSEK
2011, 113 Pages
Jury
Prof. Dr. Abdurrahman AKTUMSEK Prof. Dr. Ahmet DURAN Prof. Dr. Muhsin KONUK Assoc. Prof. Dr. Atilla ARSLAN Asst. Prof. Dr. Haluk OZPARLAK
Glycyrrhiza L. has been one of the most widely used medicinal plants and found in traditional medicine since antiquity. This study focused on antioxidant activities, essential oils and fatty acid compositions of different parts (the aerial and root) of Glycyrrhiza taxa. The antioxidant capacity tests were designed to evaluate the antioxidant activities of methanol extracts of Glycyrrhiza taxa tested. The extracts will be executed for their possible antioxidant activities by five different test systems namely total antioxidant capacity (phosphomolibdat assay), β-carotene/linoleic acid test system, free radical scavenging (DPPH), ferric and cupric ion reducing power (CUPRAC). Total phenolic and flavonoid concentrations of each extract were also determined by using both Folin-Ciocalteu reagent and aluminum chloride. The aerial part of G. glabra L. var. glabra L. was found to possess the highest total phenolic content (399.18±1.98 mg GAE/g), total antioxidant capacity (342.66±5.34 mg AE/g), free radical scavenging (DPPH) and ferric reducing power. Additionally the root of G. glabra var. glabra displayed the highest total flavonoid content (315.30±6.27 mg RE/g). The root extract of G. iconica Hub.-Mor. showed the highest inhibition of linoleic acid oxidation. In cupric ion reducing power assay, the aerial part of G. glabra L. var. glandulifera (Waldst. Et Kit.) Boiss. was significantly higher than other taxa. Positive correlation was generally observed between total phenolic content and various antioxidant activities in Glycyrrhiza taxa.
The essential oil from aerial parts and roots of Glycyrrhiza taxa was analyzed by gas chromatography mass spectroscopy (GC-MS) systems. The major components identified were hexanal,
β-vii
pinene, furan-2-pentyl, benzaldehyde, 4-terpineol, 1-pentylcyclobutene, acetophenone, α-caryophyllen, naphtalene, 1-phenyl-1H-pyrazol-3-amine, m-cresol, nerolidol, hexahydro farnesyl acetone, E-neryl linalool, 1-tetracosanol, p-hexylacetophenone, phytol, 4-pyridinecarbonitrile, dimethylamine and n-hexadecanoic acid.
Fatty acid profiles of these taxa were also examined by GC-FID and 22 fatty acids were identified. Palmitic, linoleic and linolenic acid were detected as the main components.
The results of this study have shown that the methanol extracts of aerial parts and roots of Glycyrrhiza species can be used as an easily accessible source of natural antioxidants and as a possible food supplement or in pharmaceutical industry due to their strong antioxidant activities and beneficial fatty acid profiles.
Keywords: Antioxidant, chromatographic techniques, essential oil compound, fatty acid
viii
ÖNSÖZ
Selçuk Üniversitesi Fen Fakültesi Biyoloji Bölümü Fizyoloji-Biyokimya Araştırma Laboratuarında yürütülmüş olan bu doktora tez çalışmasında Glycyrrhiza L. (meyan) türlerinin kimyasal bileşimi ve antioksidan kapasiteleri araştırılmıştır.
Tez konumu belirleyen ve çalışmam süresince rehberlik eden, destekleyen ve tavsiyeleriyle beni yönlendiren danışman hocam Prof. Dr. Abdurrahman AKTÜMSEK‟e içtenlikle teşekkür ederim. Arazi çalışmalarını planlayarak çalışma materyali olan bitki örneklerini toplayan ve teşhis edilmesini sağlayan saygıdeğer hocam Prof. Dr. Ahmet DURAN‟a ve Arş. Gör. Özlem ÇETİN‟e teşekkürü borç bilirim.
Özellikle yağ asidi analizleri sonuçlarının değerlendirilmesi konusunda yardımcı olan ve faydalı tavsiyeleriyle tezimin oluşmasına katkı sağlayan değerli hocam Arş. Gör. Dr. Gökalp Özmen GÜLER‟e teşekkür ederim.
Örneklerin analize hazırlanma aşamaları olan numunelerin öğütülmesi, ekstraksiyonları ve deneysel çalışmalarımın her aşamasında yardımını gördüğüm arkadaşım Arş. Gör. Gökhan ZENGİN‟e teşekkür ederim.
Ayrıca çalışmalarım süresince maddi ve manevi her türlü konuda yanımda olup desteğini esirgemeyen başta babam Mesut ÇAKMAK ve annem Safiye ÇAKMAK olmak üzere aileme ve nişanlım Arş. Gör. Emel KUNDUZ‟a, lisansüstü eğitimim süresince bana evlerini açan eniştem ve teyzeme sonsuz teşekkürlerimi sunarım.
Yavuz Selim ÇAKMAK KONYA-2011
ix ĠÇĠNDEKĠLER ÖZET ... iv ABSTRACT ... vi ÖNSÖZ ... viii ĠÇĠNDEKĠLER ... ix SĠMGELER VE KISALTMALAR ... xi 1. GĠRĠġ ... 12 2. KAYNAK ARAġTIRMASI ... 15 2.1. Serbest Radikaller ... 15
2.2. Serbest Radikallerin Hastalıklarla İlişkisi ... 18
2.3. Antioksidanlar ... 19
2.4. Antioksidan Kapasite Tayin Metotları ... 22
2.4.1. Toplam Fenolik Madde Tayini (Folin-Ciocalteu Yöntemi) ... 23
2.4.2. Toplam Flavonoid Madde Tayini ... 23
2.4.3. Toplam Antioksidan Kapasite Testi (Fosfomolibdat Testi) ... 24
2.4.4. β-karoten/Linoleik Asit Emülsiyon Sistemi ... 24
2.4.5. DPPH (2,2-difenil-1-pikrilhidrazil) Yöntemi (Serbest Radikal Süpürme Etkinliği) ... 24
2.4.6. Demir İndirgeme Gücü ... 25
2.4.7. CUPRAC Testi ... 25
2.5. Uçucu Yağlar ... 26
2.6. Bitkisel Yağlar ... 28
2.7. Fabaceae Familyası ve Glycyyrhiza L. Cinsi ... 29
3. MATERYAL VE YÖNTEM ... 31
3.1. Çalışmada Kullanılan Glycyrrhiza Türleri ve Özellikleri ... 31
3.2. Bitkisel Ekstraktların Hazırlanması ... 33
3.3. Antioksidan Kapasitenin Belirlenmesinde Uygulanan Metotlar ... 33
3.3.1. Toplam Fenolik Madde Tayini (Folin Yöntemi) ... 33
3.3.2. Toplam Flavonoid Madde Tayini ... 34
3.3.3. Toplam Antioksidan Kapasitenin Belirlenmesi ... 34
3.3.4. β-karoten/Linoleik Asit Emülsiyon Sistemi ... 35
3.3.5. DPPH Süpürme Etkinliği ... 35
3.3.6. Demir İndirgeme Gücü ... 36
3.3.7. CUPRAC Metodu ... 36
3.4. Bitkilerin Yağ Asidi Komposizyonlarının Belirlenmesi ... 37
3.4.1. Bitkilerden Yağın Ekstrakte Edilmesi ... 37
3.4.2. Yağ Asitlerinin Metil Esterlerinin Hazırlanması ... 37
3.4.3. Numunelerin Gaz Kromatografi Cihazında Yağ Asidi Analiz Koşulları ... 37
x
4. ARAġTIRMA SONUÇLARI VE TARTIġMA ... 39
4.1. Antioksidan Kapasite Metotlarına Ait Sonuçlar ... 39
4.1.1. Toplam Fenolik Madde Tayini (Folin Yöntemi) ... 40
4.1.2. Toplam Flavonoid Testi ... 44
4.1.3. Toplam Antioksidan Kapasite ... 47
4.1.4. β-karoten/Linoleik Asit Emülsiyon Sistemi ... 49
4.1.5. DPPH Süpürme Etkinliği ... 51
4.1.6. Demir İndirgeme Gücü ... 63
4.1.7. CUPRAC Metodu ... 73
4.2. Uçucu Yağ Analizlerine Ait Sonuçlar ... 76
4.3. Yağ Asidi Analizlerine Ait Sonuçlar ... 84
5. SONUÇLAR VE ÖNERĠLER ... 93
5.1. Sonuçlar ... 93
5.2. Öneriler ... 94
KAYNAKLAR ... 95
xi SĠMGELER VE KISALTMALAR Simgeler Açıklama mg miligram g gram nm nanometre dk dakika ml mililitre cm santimetre µg mikrogram ºC derece santigrat M molar Kısaltmalar DPPH 2,2-difenil-1-pikrilhidrazil CUPRAC Bakır indirgeme gücü metodu GAE Gallik asit eşdeğeri
AE Askorbik asit eşdeğeri
RE Rutin eşdeğeri
GC-MS Gaz kromatografi-kütle spektorskopisi GC-FID Gaz kromatografi-Alev iyonlaşma dedektörü AIDS Edinilmiş bağışıklık eksikliği sendromu
ATP Adenozintrifosfat
DNA Deoksiribonükleik asit
SH Sülfidril bağı
KOAH Kroner obstrüktif akciğer hastalıkları
SOD Süper oksit dismutaz
GPx Glutatyon peroksidaz
CAT Katalaz
BHA Bütillenmiş hidroksianisol BHT Bütillenmiş hidroksitoluen TBHQ Tersiyerbutil hidrokinon
PG Propilgallat
LDL Düşük yoğunluklu lipoprotein (Low Density Lipoprotein)
DHA Dokosa hekzaenoik asit
EPA Eikosa pentaenoik asit ALA Alfa linoleik asit
UV Ultra viole
IUPAC Uluslararası temel ve uygulamalı kimya birliği (The International Union of Pure and Applied Chemistry)
1. GĠRĠġ
İnsanoğlu tarih boyunca besin, ilaç, yağ ve diğer pek çok kullanışlı ürünü elde etmek amacıyla bitkisel ürünleri kullanmıştır. Meyve ve sebze gibi bitkisel ürünlerin tüketiminin yüksek olduğu bir diyet ile pek çok kronik hastalık riskinin düşmesi arasında bir ilişki bulunmaktadır (Block ve ark., 1992; Ness ve Powles, 1997). Bitkisel ürünlerin tüketiminin artırılmasının sağlık açısından faydalı olduğunun çok eski çağlardan beri bilinmesine rağmen bu faydalı etkiden hangi özel bileşenlerin sorumlu olduğu pek bilinmemekteydi. Ancak günümüzde bitkilerin bileşiminde bulunan birçok ürün daha fazla ilgi çekmekte, bunların faydaları ve kullanım alanlarının araştırıldığı çalışmaların sayısı her geçen gün artmaktadır. Bitkiler lipidler, basit ve kompleks karbohidratlar, proteinler, mineraller ve insan beslenmesi için önemli sekonder metabolitlerin iyi bir kaynağıdır. Bunlara ek olarak bitkilerin kimyasal bileşiminde bulunan fitokimyasallar gibi bazı maddelerin sağlık açısından faydaları son zamanlarda oldukça ilgi çekmektedir (Heber, 2004). Fakat 19. yüzyılın başlarına kadar bitkilerdeki bu aktif bileşenler izole edilememiştir. Doğal bitkisel bileşenlerin kimyasal yapıları ancak bu yüzyılın sonlarında belirlenebilmiştir. Son 50 yılda yeni kimyasal teknolojilerin geliştirilmesiyle biyolojik bileşenlerin belirlenmesi, izolasyonu ve sentezi mümkün hale gelmiştir. Bitkiler ve onların çeşitli kısımlarından elde edilen bileşenler boya, koku, tat verici, hastalıkların tedavisi gibi birçok amaçla kullanılmaktadır.
Organizmada gerçekleşen kimyasal süreçler, özellikle oksidasyon süreci, serbest radikallerin oluşmasına neden olur. Yüksek derecede reaktif olan serbest radikaller biyomoleküllerle kolayca reaksiyona girerek hücrelere zarar verebilecek toksik özellikte bileşikler oluşturabilir (Finaud ve ark., 2006). Serbest radikal, atomik ya da moleküler yapılarda çiftlenmemiş tek elektron bölümlerine verilen isimdir. Bu radikaller genellikle kararsız bir yapıya sahiptir ve bazı maddelerle kolayca reaksiyona girerek toksik etkisi yüksek yeni bileşikler meydana getirebilirler (Sen, 2001). Bu radikallerin oluşumu oksidasyon süreci gibi endojen kaynaklı olabileceği gibi başlıca sigara, alkol, çevresel kirlenme, ozon ve ilaçlar gibi ekzojen kaynaklı da olabilir. Serbest radikaller doku hasarı ve patolojik olgularda önemli rol oynamaktadır. Tüm radikallerin biyolojik sistemlerde birikmesi oksidatif zararlara neden olur. Aerobik koşullarda aşırı doymamış yağ asidi içeren lipitler, proteinler, nükleik asitler ve karbohidratlar serbest radikallerin rol oynadığı reaksiyonlarla okside olurlar. Bu durum kanser başta olmak üzere kalp hastalıkları, artrit, Parkinson ve Alzheimer gibi nörodejeneratif hastalıklara neden
olmaktadır (Christen, 2000). Antioksidanlar serbest radikallerle etkileşerek bunların hücrelere zarar vermelerini önlerler. Günümüzde antioksidan özelliği keşfedilen birçok farklı madde vardır. Bu antioksidan maddelerin bir kısmını vücutta doğal olarak bulunan enzim sistemleri oluştururken, bir kısmını da diyetle alınan özellikle bitkisel orijinli antioksidanlar oluşturmaktadır (Pokorný, 2007).
Diyette tüketilen yağ asitleri kardiovasküler hastalıklar, kanser, diabet ve dejeneratif hastalıkların gelişimine katkıda bulunan önemli bir faktör olabilmektedir (Connor, 2000; Tapiero ve ark., 2002). Bitkilerin yağ asidi bileşimi özellikle hayvansal yağlarda yüksek oranda bulunan doymuş yağlara oranla daha yüksek oranda tekli ve çoklu doymamış yağ asidi içermelerinden dolayı genellikle sağlıklı olarak kabul edilir. Özellikle bitkisel kaynaklı yağların bileşiminde bol miktarda bulunan aşırı doymamış yağ asitleri ve bunların ω3 ve ω6 yağ asitleri olarak bilinen izomerleri pek çok hastalığa neden olan olumsuz etkileri önemli ölçüde önleyen ve sağlık üzerine olumlu etkilere sahip yağ asitleridir. ω6 yağ asitlerinin ana kaynağı özellikle linoleik asit içeren mısır ve soya fasulyesi yağları gibi bitkisel yağlardır (Kirshenbauer, 1960). ω3 yağ asitleri ise keten tohumu, ceviz ve özellikle planktonlar ile yağlı balıklar gibi su ürünlerinde bulunur. ω6 yağ asitleri organizmada oldukça önemli rolleri olan eikosanoidlerin öncül molekülü olması bakımından önemlidir. ω3 yağ asitleri büyüme ve gelişmede, beyin gelişiminde, kardiovasküler hastalıkların önlenmesinde büyük öneme sahiptirler. Balıklar ve diğer deniz ürünleri bu yağ asitlerinin önemli kaynakları olmasına rağmen diğer kaynakları arasında bulunan bitkisel ürünlerde oldukça dikkat çekicidir (Meyer ve ark., 2003). Bu duruma bağlı olarak özellikle bitkilerin yağ asidi komposizyonun tespiti ve bu yağ asitlerinin yeni kaynaklarının belirlenmesine yönelik çalışmalar oldukça hız kazanmıştır. Bitkisel yağlar gıda olarak tüketilmeleri yanında kozmetik ürünlerin bileşiminde katkı maddesi olarak ve yakıt olarak ekonomik açıdan da büyük önem taşıyan ve giderek genişleyen bir kullanım alanına sahiptir.
Uçucu yağlar aromatik bitkiler tarafından üretilen güçlü bir kokuyla karakterize olan doğal ve kompleks uçucu bileşenlerdir. Uçucu yağların tıbbi özelliklere ve güzel kokulu bileşenlere sahip olduğu bilinmektedir. Bütün bu özellikler sayesinde bitkiler doğada zararlılardan korunmayı, canlıları cezp etmeyi ve bu sayede polen ve tohumlarını yayarak nesillerinin devamlılığı konusunda tahmin edilenin de üstünde bir başarı sağlamaktadırlar (Bakkali ve ark., 2008). Bitki uçucu yağları antibakterial, antiviral, antifungal, antiinflamatuvar ve antioksidan özellik gibi önemli biyolojik etkilere sahip olmalarından dolayı farmakolojik açıdan da önem taşımaktadırlar. Ayrıca
kozmetik alanında bazı ürünlerin bileşiminde kullanılıyor olmaları ticari bir değer de katmaktadır.
Fabaceae familyası ılıman, subtropik ve tropik bölgelerde geniş yayılış göstermektedir. Bu familyada yaklaşık 730 cins ve 19.400 tür bulunur ve çiçekli bitkilerin üçüncü büyük familyasıdır (Wojciechowski ve ark., 2004). Glycyrrhiza cinsi dünyada yaklaşık 20 tür ile temsil edilmektedir (Polhill ve Raven, 1981; Sümbül ve ark., 2003). Bu familyaya ait ve tıbbi yönüyle tarih boyunca hep ilgi çekici bir bitki olan
Glycyrrhiza cinsi dünyada Amerika, Avrupa kıtası, Çin, Nepal, Tayvan, Rusya,
Pakistan, Kıbrıs ve Türkiye‟de yayılış göstermektedir. Türkiye‟de ise 8 takson ile temsil edilmektedir. Bunlardan 4‟ü endemik olup endemizm oranı %50‟dir. Ülkemizde “meyan” olarak adlandırılan bitki antik çağlardan beri geleneksel ilaç olarak en yaygın kullanılan bitkilerden biridir. Bitkinin kullanımının izlerine antik Asur, Mısır, Çin ve Hindistan kültürlerine kadar rastlanmaktadır (Armanini ve ark., 2002; Fiore ve ark., 2005). Modern tıpta meyan ekstraktları ilaçlardaki acı ve kötü tadı maskelemek amacıyla tat verici ajan olarak, soğuk algınlığında öksürük söktürücü olarak kullanılmaktadır. Japonya‟da 60 yıldan fazla bir zamandır kronik hepatit, AIDS, Herpes gibi pek çok virüs hastalığının tedavisinde kullanılmaktadır (Takahara ve ark., 1994). Ülkemizde de hemoroit, karın ağrısında kaynatılarak çayı içilmektedir (Sezik ve ark., 2001).
Bu tez çalışmasında dünyada ve ülkemizde tıbbi amaçlarla kullanılan
Glycyyrrhiza cinsinin ülkemizde yayılış gösteren tüm taksonlarının (G. aspera hariç)
yağ asidi kompozisyonu, uçucu yağ bileşimi ve antioksidan kapasiteleri belirlenerek elde edilen sonuçlara göre kullanılan türlerin sağlık açısından önemleri ortaya konularak gıda ve farmakoloji endüstrisi açısından bir hammadde kaynağı olup olmayacağının değerlendirilmesi amaçlanmıştır.
2. KAYNAK ARAġTIRMASI
2.1. Serbest Radikaller
Oksijenin insan yaşamı için vazgeçilmez olduğu bilinmektedir. Solunum yoluyla alınan oksijenin büyük bir kısmı (yaklaşık %90) elektron taşıma sistemi, kalan kısmı ise diğer oksijen gerektiren reaksiyonlarda kullanılmaktadır. Elektron taşıma zincirinde son elektron alıcısı olan moleküler oksijen suya indirgenir. Bu yolda oksijen molekülünün kuvvetli oksitleyici gücü, ATP‟nin yüksek enerjili fosfat bağı haline dönüştürülür.
Moleküler oksijen dış orbitallerinde paylaşılmamış iki elektron içerir. Bu elektronlar, spinleri aynı yönde ve farklı orbitallerde iken minimum enerji seviyesindedirler. Oksijen çeşitli fiziksel ve kimyasal etkenlerle oksijen radikallerini oluşturabilir. Serbest radikaller yüksek bir enerji girişi gerektiren bir elektron transferiyle üretilir. Bu radikal diğer radikallerle veya moleküllerle reaksiyona girerek yeni radikalleri oluşturabilir (Sen, 2001). Serbest radikaller yapılarında çiftlenmemiş elektrona sahip moleküllerdir ve kararsız bir yapıları vardır. Bu radikaller reaktif bazı maddelerle reaksiyona girerek toksik etkilere neden olan yeni bileşikler meydana getirebilmektedirler. Serbest radikaller reaktif oksijen türleri, reaktif nitrojen türleri ve reaktif kükürt türleri şeklinde sınıflandırılabilir (Çizelge 2.1). Reaktif oksijen türleri yapılarında oksijen radikali içeriğine sahip radikallerdir. Reaktif nitrojen türleri ve reaktif sülfür türleri ise reaktif oksijen türleriyle reaksiyonlar sonucunda oluşabilmekte veya reaktif oksijen türlerinin oluşumunu artırabilmektedirler (Finaud ve ark., 2006). Ancak, immunite ve oksidatif stres gibi temel fizyolojik olaylara yol açan grup süper oksijen radikalleri olduğu için genelde serbest radikaller denildiğinde bunlar kastedilmektedir. Reaktif oksijen türleri denildiğinde özellikle süperoksit radikali (O2•-), hidrojen peroksit (H2O2) ve hidroksil radikali (OH•) akla gelmektedir.
Süperoksit radikali oksijene (O2) bir elektron eklenmesiyle oluşur ve yüksek reaktiviteye sahiptir.
O2 + e- → O2•-
Süperoksit radikali Fenton reaksiyonu ve Haber-Weiss reaksiyonu aracılığıyla hidrojen peroksitin geçiş metalleri (demir ve bakır) ile ayrışması sonucu yüksek reaktif özelliğe sahip hidroksil radikalini oluşturur. Bu reaksiyonlar şu şekilde gerçekleşmektedir (Finaud ve ark., 2006);
a) O2•- + H+ → O2•H
b) O2•H + O2•- + H+ → H2O2 + O2 c) Fe+3 + O2•- → Fe+2 + O2
d) Fe+2 + H2O2 → Fe+3 + OH• + OH
-Çizelge 2.1. Serbest radikallerin sınıflandırılması ve temel etkileri (Finaud ve ark., 2006)
Serbest Radikal Kısaltma Temel Etki
Reaktif Oksijen Türleri Lipid oksidasyonu ve peroksidasyon, Protein oksidasyonu, DNA hasarı Süperoksit radikali (O2•-)
Ozon (O3)
Singlet Oksijen (1O2)
Hidrojen Peroksit (H2O2)
Hidroksil Radikali (OH•) Hipoklorik Asit (HOCl) Hipobromik Asit (HOBr) Alkoksil Radikali (RO•) Peroksi Radikali (ROO•) Hidroperoksil Radikali (ROOH•)
Reaktif Nitrojen Türleri Lipid peroksidasyonu, DNA hasarı, Proteinlerin oksidasyonu
Nitrik Oksit (NO•)
Azot Dioksit (NOO•)
Peroksinitrik (ONOO•)
Nitroz asit (HNO2)
Nitrozil katyonu (NO+) Nitroksi anyonu (NO-)
Nitroz asit (HNO2)
Diazot tetraoksit (N2O4)
Peroksinitril asit (ONOOH) Nitronyum katyonu (NO2+)
Alkilperoksi nitrit (ROONO)
Reaktif Sülfür Türleri Protein oksidasyonu, DNA hasarı, Reaktif oksijen türleri oluşumu Thiyl Radikali (RS•)
Hidrojen peroksit, Fenton reaksiyonunun birinci ve ikinci safhalarında (a ve b) özetlenmektedir. Bu reaksiyon asidik ortamda oluşur ve süperoksit dismutaz enzimi tarafından katalizlenir.
SOD
Hidrojen peroksit bir serbest radikal değildir çünkü paylaşılmamış elektrona sahip değildir. Ancak onun reaktif oksijen türlerini oluşturma kapasitesi ve toksik olması dolayısıyla bir reaktif oksijen radikali olarak düşünülmektedir.
Lökositlerde bulunan miyeloperoksidaz enzimi sayesinde hidrojen peroksitten en güçlü fizyolojik oksidanlardan ve antimikrobiyal ajanlardan biri olan hipoklorik asit (HOCl) oluşmaktadır (Hampton ve ark., 1998).
Hidroksil radikali (OH•) ise Fenton reaksiyonunun son ürünüdür. Hidroksil aşırı reaktif ve en toksik reaktif oksijen türüdür. Bu serbest radikale karşı özgün olan bir antioksidan bulunmamaktadır. Bu radikal özellikle lipid peroksidasyonuna ve protein oksidasyonuna neden olmaktadır (Leewenburgh ve ark., 1999).
Reaktif nitrojen türlerinden en önemlisi nitrik oksit (NO•) radikalidir. Nitrik oksit serbest radikal olmasına rağmen seçici bir reaktiviteye sahiptir. Bu radikal ağırlıklı olarak süperoksit anyonu (O2
•-) ve moleküler oksijen (O2) gibi radikal türleri, ferrik (Fe+3) ve ferroz (Fe+2) demir gibi paramanyetik metal iyonlarıyla reaktif hale gelmektedir (Stamler ve ark., 1992; Kharitonov ve ark., 1994; Eiserich ve ark., 1995; Pryor ve Squadrito, 1995; Rubbo ve ark., 1996).
Alifatik tioller organizmada yüksek konsantrasyonlarda bulunmaktadır. Proteinlerin yapısında bulunan –SH grubu pH değişimine bağlı olarak kolaylıkla tiolat anyonuna dönüşebilmektedir. Tiolat anyonu ise demir ve bakır gibi geçiş metallerinin varlığında reaktif sülfür türü olan thyl radikallerinin (RS.
) oluşumuna yol açmaktadır. RSH + Cu2+ → RS. + Cu+ + H+
Bu thyl radikalleri oksijenle (O2) birleştiğinde güçlü reaktiviteye sahip hale gelmektedir.
RS. + O2 → RSO2. Ayrıca oluşan thyl radikali ferrik (Fe+3
) demiri ferroz (Fe+2) demire indirgeyerek Fenton reaksiyonu ile reaktif oksijen türlerinin oluşmasına neden olmaktadır (Spear ve Aust, 1994; Pieri ve ark., 2003). Bunun dışında thyl radikali lipid moleküllerinin bileşiminde bulunan yağ asitlerinin cis-trans izomerizasyonunu da katalize etmektedir (Ferreri ve ark., 2005).
2.2. Serbest Radikallerin Hastalıklarla ĠliĢkisi
Serbest radikallerin aşırı üretimi sonucu oksidatif stres denilen durum ortaya çıkmaktadır. Oksidatif stres DNA, lipoproteinler, lipidler ve proteinler gibi hücre membranı ve diğer yapılarda görev alan yapısal moleküller üzerinde değişikliklere ve ciddi zararlara neden olabilmektedir (Young ve Woodside, 2001; Droge, 2002; Wilcox ve ark., 2004; Pacher ve ark., 2007). Oksidatif stresin yaşlanmanın yanı sıra kanser, kardiyovasküler hastalıklar, nörolojik hastalıklar, pulmoner hastalıklar, romatoid artrit, renal rahatsızlıklar, göz rahatsızlıkları gibi pek çok hastalıkla ilişkisi bulunmaktadır.
İnsanlarda kanserin gelişimi çeşitli iç ve dış uyaranlar aracılığıyla hücresel ve moleküler düzeyde gerçekleşen değişiklikleri içeren kompleks bir süreçtir. Oksidatif DNA hasarının kanser gelişimine neden olduğu kanıtlanmıştır (Valko ve ark., 2004; Valko ve ark., 2006; Valko ve ark., 2007). Kardiyovasküler hastalıkların nedenleri yüksek tansiyon ve kolesterol, düşük fiziksel aktivite, sigara, diabet, stres gibi birçok faktöre bağlıdır (Bahorun ve ark., 2006; Chatterjee ve ark., 2007; Ceriello, 2008). Ancak son zamanlarda oksidatif stresin aterosklerozis, iskemi, hipertansiyon, kardiak hipertrofi gibi kardiyo vasküler hastalıkların oluşumunda destekleyici rol oynadığına dair önemli kanıtlar elde edilmiştir (Droge, 2002; Bahorun ve ark., 2006; Ceriello, 2008). Alzheimer, Parkinson, multiple sklerozis, hafıza kaybı ve depresyon gibi sinirsel hastalıklarla oksidatif stresin ilişkisinin araştırıldığı bir çok çalışma mevcuttur (Christen, 2000; Halliwell, 2001; Butterfield, 2002; Singh ve ark., 2004). Klinik ve deneysel çalışmalar nöronların kaybı ve akıl hastalığının ilerlemesinde oksidatif zararların kilit rol oynadığını göstermiştir (Christen, 2000). Alzheimer hastalarının beyninde bulunan toksik bir peptit olan β-amiloid oksidatif stres sonucu üretilir ve nörodejeneratif ilerlemede önemli bir rol oynamaktadır (Butterfield, 2002). Özellikle dış etmenlerin (sigara, çevre kirliliği vb.) etkisiyle ortaya çıkan hastalıklardan olan kronik obstrüktif akciğer hastalığı (KOAH) ve inflamatuvar akciğer hastalıkları solunum sisteminin normal fonksiyonlarını gerçekleştirebilmesini kısıtlayan veya engelleyen hastalıklardır. Bu hastalıkların sistemik ve lokal kronik inflamasyonlar ve oksidatif stresle alakalı olduğuna dair önemli kanıtlar elde edilmiştir (Caramori ve Papi, 2004; Guo ve Ward, 2007). Oksidanlar transkripsiyon faktörleri (NF-kappa B ve AP-1 vb.) ve farklı kinazların aktivasyonu aracılığıyla inflamasyonu artırabilmektedirler (MacNee, 2001; Hoshino ve Mishima, 2008). Romatoid artrit eklem ve dokuların kronik inflamasyonuyla karakterize bir otoimmun hastalıktır (Mahajan ve Tandon, 2004;
Walston ve ark., 2006; Valko ve ark., 2007). Hastalığın esası ve gelişimi inflamasyonun olduğu yerde reaktif oksijen ve reaktif azot türlerinin üretiminden dolayıdır. Oksidatif stres nefrit, kronik böbrek yetmezliği ve proteinüri gibi böbrek rahatsızlıklarında da etkili olmaktadır. Gentamisin, siklosporin, takrolimus, bleomisin, vinblastin gibi ilaçların nefrotoksisitesi bunların lipid peroksidasyonu vasıtasıyla oluşan oksitadif stresten kaynaklanmaktadır (Sadeg ve ark., 1993; Massicot ve ark., 1997; Galle, 2001). Oksidatif stres, gözler ve görme fonksiyonunu da olumsuz yönde etkileyebilmektedir. Serbest radikallerin etkisi altında lens yüzeyine kristal proteinlerin bağlanmasına ve birikmesine bağlı olarak katarakt oluşumu görülebilmektedir (Meyer ve Sekundo, 2005). Oksidatif stresin gebelik süresince de çeşitli problemlere neden olabildiği belirlenmiştir. Gebelik sürecindeki kontrollerde ileri seviyede gebelik toksisemisine (eklampsi) neden olabilen hipertansiyon ve fetal büyümenin sınırlanması durumunun gelişimini de kapsayan bir takım hastalıklar gözlenmiştir. Bazı araştırmalar bu hastalıkların nedenleri arasında reaktif oksijen ve reaktif nitrojen türlerinin rolü olduğunu göstermiştir (Braekke ve ark., 2006; Myatt, 2006; Biri ve ark., 2007; Hracsko ve ark., 2008).
2.3. Antioksidanlar
Çeşitli kaynaklardan gelen serbest radikallere maruz kalmak organizmanın bir dizi savunma mekanizması geliştirmesine neden olmuştur (Cadenas, 1997). Serbest radikaller ve onların neden olduğu oksidatif strese karşı geliştirilen antioksidan savunma mekanizmaları oldukça önemlidir.
Antioksidanların önemli bir kısmı mikroorganizmalar, mantarlar, bitkiler ve organizmanın kendisi gibi canlı sistemler tarafından doğal olarak sentezlenmektedir. Bunlar doğal antioksidanlar olarak adlandırılmaktadır ve tercih edilen antioksidan kaynakları olarak kabul edilmektedirler (Pokorný, 2007). Doğal antioksidanlar enzimatik ve enzimatik olmayan antioksidanlar olarak iki gruba ayrılabilir. Önemli enzimatik antioksidanlar süperoksit dismutaz (SOD), glutatyon peroksidaz (GPx) ve katalazdır (CAT). Enzimatik antioksidanlar organizmanın kendini korumak amacıyla ürettiği ve biyokimyasal süreçlerde üretilen serbest radikallerin zararlı etkilerinden korunma mekanizmasıdır. Normal şartlar altında, bu antioksidanların aktiviteleri ve hücre içi seviyeleri arasında bir denge vardır. Bu denge organizmanın hayatta kalabilmesi için esastır (Valko ve ark., 2007). Enzimatik olmayan antioksidanlar ise
askorbik asit (C vitamini), α tokoferol (E vitamini), glutatyon (GSH), karotenoidler ve flavonoidlerdir (Larson, 1988). Diyetle alınan antioksidanlar endojen kaynaklı antioksidanlara oksidatif stresin etkilerinin ortadan kaldırılması konusunda yardımcı olarak önemli bir rol oynamaktadırlar. Antioksidanların diğer üretim yolu ise bunların endüstriyel olarak sentezlenmesidir. Bu şekilde üretilen antioksidanlar sentetik antioksidanlar olarak adlandırılmaktadır. Doğal antioksidanların tersine sentetik antioksidanların insan sağlığı açısından güvenilirliği tartışmalıdır (Jadhav ve ark., 1996). Sentetik antioksidanlar özellikle hazır gıdalarda yaygın olarak kullanılmaktadır. Bunun temel nedeni deodorizasyon veya kızartma gibi sıcaklık uygulamaları ve uzun depolama şartları altında gıdalarda lipid oksidasyonu sonucunda serbest radikal oluşumunun önlenmesi ve beslenmeyle alınan gıdalar aracılığıyla organizmada oluşabilecek serbest radikal düzeyini düşürerek ortaya çıkabilecek hastalıklara karşı korumaktır (Pokorný, 2007). Sentetik antioksidanlardan en önemlileri BHA (bütillenmiş hidroksianisol), BHT (bütillenmiş hidroksitoluen), TBHQ (tersiyerbutil hidrokinon) ve PG (propilgallat)‟ dir. Ancak günümüzde sentetik antioksidanların bazı toksik etkilere sahip olduğunun belirlenmesi sonucu doğal antioksidanlara olan ilgi giderek artmaktadır (Jadhav ve ark., 1996).
Antioksidanların alımında fenolik ve flavonoid içeriği yüksek olan bitkisel ürünlerin tüketilmesi tavsiye edilmektedir. Pek çok bitkisel üründe kuru madde ağırlığının %0.5-5 düzeyinde fenolik bileşik içermesi dolayısıyla bunların iyi birer antioksidan kaynağı olduğu söylenebilir (Chung ve ark., 1998). Fenolik maddeler yapılarında hidroksil grubu içeren en az bir aromatik halka ile buna bağlı bir veya daha fazla hidroksil grubuyla karakterizedir. Fenoller, basit fenoller, benzoik asit, fenilopropanoidler ve flavonoidler gibi farklı gruplara ayrılabilmektedir (Rice-Evans ve ark., 1996; Solecka, 1997; Chaudiere ve Ferrari-Iliou, 1999). Fenolik bileşikler yüksek metal şelatlama eğilimine sahiptir. Yapılarında bulunan hidroksil ve karboksil grupları özellikle demir ve bakır iyonları bağlama kabiliyetine sahiptir (Jung ve ark., 2003). Bu şekilde demir iyonlarını inaktive ederek reaktif oksijen türlerinin en önemli kaynağı olduğu düşünülen Fenton reaksiyonu aracılığıyla süperoksit oluşumunu durdurabilmektedir (Rice-Evans ve ark., 1996).
Şekil 2.1. Fenolün Yapısı
Flavonoidler bitkilerin büyük bir çoğunluğunda bulunan polifenolik bileşenlerdir. Kimyasal yapılarına göre 4000‟den fazla flavonoid tanımlanmıştır. Bunlar, flavanoller, flavanonlar, flavonlar, izoflavonlar, kateşinler, antosiyaninler ve proantosiyaninler olarak sınıflandırılabilir. Flavonoidler serbest radikal süpürme ve antioksidan özellikleri sayesinde kanser ve yaşlanmayı önlemede oldukça kullanışlı farmakolojik özelliklere sahiptir (Sharma, 2006).
2.4. Antioksidan Kapasite Tayin Metotları
Sentetik antioksidanların zararlı etkileri göz önüne alındığından bunların yerine geçebilecek doğal antioksidan kaynaklarının belirlenmesine yönelik çalışmalarda çok çeşitli kimyasal metotlar kullanılmaktadır. Bu metotların bir kısmı radikal süpürme etkinliği (DPPH, ABTS vb.), bir kısmı geçiş metallerinin indirgenmesi (demir indirgeme gücü, CUPRAC testi), bir kısmı ise lipid oksidasyonun inhibe (β-karoten/linoleik asit test sistemi, Ferrik thiosiyanat metodu) edilmesine dayanmaktadır. Son zamanlarda birçok yeni metod geliştirilmesine rağmen bitkilerin antioksidan etkinliklerini tümüyle yansıtan etkin ve verimli bir metod geliştirilememiştir. Bu neden antioksidan kapasite belirleme üzerine yapılan çalışmalarda özellikle yukarıda isimleri belirtilen metotlar uygulanarak net ve kesin bir yorumlama yapılabilir (Karadag ve ark., 2009; Prior ve ark., 2005).
Antioksidan kapasite üzerine yalpan kimyasal testler genel olarak iki genel grupta toplanabilir:
1. Hidrojen atomu transferine dayalı testler (HAT) 2. Elektron transferine dayalı testler (ET)
Hidrojen atomu transferine dayalı testler hidrojen veren stabil bir bileşik tarafından ortamdaki serbest radikalin süpürülmesi temelinde gerçekleşir.
AH +X• XH+A•
Hidrojen transferine dayalı testler ortam pH‟ı ve solvente bağlı olup oldukça kısa sürede tamamlanana testlerdir. Hidrojen transferine dayanan testler genel olarak ABTS gibi serbest radikal oluşturucu, bir oksitlenebilen prob ve bir antioksidan içermektedir. Bu gruptaki testlere örnek olarak β-karoten/linoleik asit test sistemi, oksijen radikali absorblama kapasitesi (ORAC) ve total antioksidan yakalana antioksidan potansiyeli (TRAP) verilebilir (Prior ve ark., 2005).
Elektron transferine dayalı testler ise bir antioksidan bileşikten elektron transferi ile metaller, karboniller veya radikallerin indirgenmesine dayanmaktadır.
Elektron transferine dayanan testlerde temel iki eleman vardır: antioksidan ve oksidan. Oksidan molekül antioksidandan bir elektron alarak renk değişimi meydana getirir. Meydana gelen bu renk değişimi antioksidan molekülün konstrasyonu ile ilişkilidir. Elektron transferine dayanan testlere örnek olarak : Toplam fenolik madde tayini (Folin yöntemi), DPPH testi ile demir ve bakır indirgeme güçleri örnek olarak verilebilir (Huang ve ark., 2005).
2.4.1. Toplam Fenolik Madde Tayini (Folin-Ciocalteu Yöntemi)
Bitkilerde bok miktarda bulunan fenolik bileşiklerin içeriği antioksidan kapasitenin oluşumunda en önemli katkıyı yapan bileşenlerdendir (Apak ve ark., 2007). Folin-Ciocalteu metodu bitkisel ekstraktların toplam fenolik madde içeriğini ortaya koymada en yaygın kullanılan metotlardan birisidir. Metodun esasını suda ve organik çözücülerde çözünmüş olan fenolik bileşiklerin folin reaktifi ile alkali ortamda renkli kompleksler meydana getirmesi oluşturur (Singleton ve Rossi, 1965). Metot kolay uygulanabilir ve tekrarlanabilir olması ve diğer metotlarla korelasyon göstermesi gibi avantajlarından dolayı yaygın olarak kullanılmaktadır. Ancak folin reaktifini sadece fenolik maddeler tarafından değil aynı zamanda fenolik olmayan bazı bileşikler tarafından da indirgenebilmektedir. Bu nedenle bu metot spesifik bir metot olarak kabul edilmemektedir. Bu duruma uygun olarak metotun total fenolik içeriği tümüyle yansıtmadığı belirtilmektedir. Sonuçlar genellikle standart fenolik maddeler olan gallik asit veya kateşine eş değer olarak verilmektedir.
2.4.2. Toplam Flavonoid Madde Tayini
Flavonoidlerin antioksidatif özellikleri serbest radikal üretmekten sorumlu enzimlerin inhibisyonu, demir ve bakır iyonlarının şelatlanması, serbest radikallerin süpürülmesi gibi pek çok farklı mekanizmadan dolayıdır (Benavente-Garcia, 1997). Flavonoidler yapılarına bağlı olarak bilinen bütün reaktif oksijen türlerini süpürme yeteneğindedirler. Toplam fenolik içeriğin miktarı AlCl3 metodu kullanılarak belirlenebilmektedir (Chang ve ark., 2002).
2.4.3. Toplam Antioksidan Kapasite Testi (Fosfomolibdat Testi)
Bu metot aynı zamanda fosfomolibdat metodu olarak da isimlendirilir. Metodun esası fenolik bileşiklerin asidik ortamda Mo (VI)‟yı Mo (V)‟e indirgemesi ve bunu takiben oluşan yeşil renkli fosfat/Mo (V) kompleksinin oluşmasına dayanmaktadır. Oluşan bu kompleks 695 nm‟de maksimum absorbans göstermektedir. Bu testin sonuçları antioksidan etkinliği bilinen maddelere eşdeğer olarak (mg/g, mg/ml) verilmektedir. Bu amaçla özellikle askorbik asit ve α-tokoferol kullanılmaktadır. Bu metot özellikle basitliği ve kullanılan reaktiflerin ucuzluğundan dolayı total antioksidan kapasitenin tayininde alternatif bir metot olarak kullanılmaktadır (Prieto ve ark., 1999).
2.4.4. β-karoten/Linoleik Asit Emülsiyon Sistemi
Linoleik asitin oksidasyonu diallik metil gruplarından hidrojen atomlarının koparılmasına bağlı olarak peroksil serbest radikallerinin üretimine yol açar (Laguerre ve ark., 2007). Meydana gelen bu serbest radikaller doymamış bir molekül olan β-karoten‟nin okside olmasına neden olur. Sonuç olarak turuncu renkli olan β-β-karoten‟nin rengi açılır ve bu durum spektrofotometrik olarak incelenir. Metotta ortama ilave edilen bitkisel ekstrakların bu renk açılmasına ne oranda inhibe ettiği hesaplanır ve inhibisyon oranın yüksek olması antioksidan etkinliğin güçlü olduğunun bir göstergesidir. Metot ayrıca çözücü ve pH‟dan etkilenmeden oldukça kısa sürede gerçekleşmektedir (Apak ve ark., 2007).
2.4.5. DPPH (2,2-difenil-1-pikrilhidrazil) Yöntemi (Serbest Radikal Süpürme Etkinliği)
DPPH radikali uzun ömürlü bir azot radikali olup oldukça koyu mor bir renge sahiptir. Bu test sisteminde mor renkli olan radikal antioksidan veya indirgeyici bir bileşik tarafından indirgenerek sarı renkli hidrazine dönüşür. Antioksidanların bu indirgeme kapasiteleri 515-528 nm aralığında absorbansdaki azalmayla gözlenir (Brand-Williams ve ark., 1995). Metot özellikle basitliği, hızlı olması ve spektrofotometre dışında spesifik bir araç getirmemesi nedeniyle antioksidan kapasite tayin çalışmalarında en sık kullanılan yöntemlerdendir (Fukumoto ve Mazza, 2000). Bununla birlikte metodun bazı eksik yönleri rapor edilmiştir. Bunlardan biri DPPH‟in organik çözücülerle özelliklede alkolik solusyonlarda çözülmesi buna karşılık sulu
sistemlerde çözünmemesidir (Huang ve ark., 2005). Bu durum özellikle hidrofilik antioksidanların yorumlanmasına sınırlamalar getirmektedir. Ayrıca kullanılan radikalin biyolojik bir radikal olmaması oksijen ve azot radikallerinin süpürme yeteneğini bire bir yansıtmamaktadır. Metodun sonuçları genellikle IC50 olarak nitelendirilen serbest radikalin yarısını süpüren konsantrasyon belirlenerek yorumlanmaktadır. IC50 değerinin düşüklüğü radikal süpürme etkinliğinin yüksekliğini gösterir (Brand-Williams ve ark., 1995).
2.4.6. Demir Ġndirgeme Gücü
Antioksidan kapasite tayininde kullanılan diğer bir metot olan indirgeme gücünde yüksek absorbans yüksek indirgeme potansiyelini göstermektedir. Metotta asidik ortamda antioksidan fenolik bileşiklerin [K3Fe(CN)6] içindeki Fe (III)‟ün Fe(II)‟ye indirgenmesine dayanmaktadır. İndirgeme reaksiyonu sonucu oluşan Prusya mavisi renkli kompleks 700 nm‟de maksimum absorbans göstermektedir. Antioksidan maddelerin etkinliğine bağlı olarak Prusya mavisi renk yeşil ile mavi arasında değişmektedir. Absorbansın artması indirgeme gücünün yüksekliğini gösterir (Mathew ve Abraham, 2006).
2.4.7. CUPRAC Testi
CUPRAC testi Apak ve ark. (2006) tarafından geliştirilmiştir. Metot bir örnekteki mevcut antioksidanlar tarafından Cu (II)‟nin Cu (I)‟e indirgenmesi esasına dayanmaktadır. CUPRAC metodunda renk oluşumuna neden olan oksidan olarak Cu(II)-neokuproin belirteci kullanılır. Test, pH 7‟de antioksidan içeren numune ile CuCl2 çözeltisi, neokuproin ve amonyum asetatın karışımının 30 dk inkübasyonu sonucunda 450 nm‟de absorbansının okunmasını içerir.
Bu metot hem suda hem de yağda eriyen antioksidan bileşiklerin fizyolojik pH şartlarında bakır(II)-Nc kompleksini bakır(I)-Nc kompleksine indirgemesi bakımından son zamanlarda oldukça fazla kullanılan bir metottur. Ayrıca reaksiyonun fizyolojik pH‟a oldukça yakın pH‟da gerçekleşmesinden dolayı metodun sonuçlarının fizyolojik koşulları yansıtma olasılığı oldukça fazladır (Apak ve ark., 2007).
İlave olarak metodun sonuçlarının toplam fenolik madde ve özellikle demir indirgeme gücü ile yüksek oranda korelasyon göstermesi metodun bir avantajı olarak düşünülebilir (Ozturk ve ark., 2007).
2.5. Uçucu Yağlar
Uçucu yağlar bitkiler tarafından üretilen ve distilasyon gibi fiziksel yöntemlerle bitkinin tamamı veya bir kısmından izole edilen uçucu bileşenlerin kompleks bir karışımıdır. Uçucu yağın temel bileşenleri üç biyosentetik yol ile oluşturulmaktadır. Bunlar; sesquiterpenleri oluşturan mevalonat yolu, mono ve diterpenleri oluşturan metileritritol yolu ve fenilpropenlere giderken şikimik asit yoludur (Franz ve Novak, 2010). Bu uçucu bileşenlerin pek çoğu çeşitli ekolojik fonksiyonlara sahiptir. Uçucu bileşenler bitkinin metabolizmasını düzenleyen haberciler, herbivorlara karşı savunma ürünleri veya tozlaşmayı sağlayan böcekleri kendine çekmeye yarayan cezp ediciler olarak hareket edebilirler (Harrewijn ve ark., 2001).
Uçucu yağlar genellikle geleneksel farmakopenin büyük önem taşıdığı tropikler ve Ortadoğu gibi sıcak kuşakta yetişen çeşitli aromatik bitkilerden elde edilmektedir. Aromatik bitkilerin sürgün, yaprak, çiçek, gövde, tohum, meyve ve kök gibi bütün kısımlarında sentezlenebilmektedir. Bakterisit ve fungisit özelliklerinden dolayı farmakolojide ve gıdalarda kullanımı sentetik kimyasal ürünlere alternatif olarak yaygınlığı giderek artmaktadır (Bakkali ve ark., 2008). Uçucu yağlar presleme ve buhar distilasyonu gibi yöntemler kullanılarak elde edilmektedir. Kullanım amacına göre farklı ekstraksiyon yöntemleri bulunmaktadır. Örneğin parfüm yapımında kullanım için lipofilik çözücüler veya süperkritik karbondioksit ile ekstraksiyon tercih edilmektedir. Ekstraksiyon ürünleri iklim, toprağın bileşimi, bitkinin farklı bölgeleri, yaş ve vejetatif siklusun farklı safhalarına göre değişebilmektedir (Masotti ve ark., 2003; Angioni ve ark., 2006). Bu nedenle, sağlıklı bir karşılaştırma yapabilmek için araştırmanın niteliğine göre incelenecek türlerin toplandığı iklim, toprak yapısı, organları gibi parametrelerden bazıları aynı olmalıdır.
Günümüzde yaklaşık 3000 uçucu yağ bileşeni bilinmektedir. Bunlardan 300 kadarı ticari olarak değer taşıyan sektörler için oldukça önemlidir. Uçucu yağlar veya onların bazı bileşenleri parfümler, makyaj ürünleri, hijyen ürünleri, dişçilik, tarım, temizlik ürünlerinde, gıda katkıları ve koruyucuları olarak kullanılmaktadır. Örneğin d-limonen, geranil asetat, d-carvon gibi bileşenler parfüm, krem, sabun, gıdalar için katkı
maddeleri olarak ticari ürünlerde tercih edilmektedir (Bakkali ve ark., 2008). Ayrıca uçucu yağlar bitkisel yağlarla karıştırılarak aromaterapide masaj yağları olarak da kullanılmaktadır. Bazı uçucu yağların sistemik hastalıklar veya organ fonksiyon bozukluklarını tedavi etmesi gibi tıbbi özelliklere sahip olduğu görülmüştür (Hajhashemi ve ark., 2003; Perry ve ark., 2003; Silva ve ark., 2003). Bitkinin türüne göre genellikle birkaç bileşen major düzeyde bulunurken diğerleri düşük düzeylerde bulunmaktadır. Genellikle bu major bileşenler uçucu yağın biyolojik özelliklerini belirlemektedir. Uçucu bileşenler biyosentetik orijinlerine göre iki farklı gruba ayrılır. Birinci grup terpenler ve terpenoidlerden diğer grup ise aromatik ve alifatik bileşenlerden oluşmaktadır (Croteau ve ark., 2000; Betts, 2001; Bowles, 2003; Pichersky ve ark., 2006). Terpenler izopren olarak adlandırılan beş karbon tabanlı (C5) ünitelerin pek çoğunun birleşmesi sonucu oluşmaktadır. Buna bağlı olarak terpenler, hemiterpenler (C5), monoterpenler (C10), sesquiterpenler (C15), diterpenler (C20), triterpenler (C30) ve tetraterpenler (C40) olarak sınıflandırılmaktadırlar. Oksijen içeren terpenler ise terpenoidler olarak adlandılır. Aromatik bileşenler fenilpropandan türer ve terpenlerden daha düşük sıklıkla oluşmaktadır. Aromatik bileşenler aldehit, alkol, fenoller, metoksi türevleri ve metilen dioksi bileşenlerinden oluşmaktadır (Bakkali ve ark., 2008).
Uçucu yağlar çok fazla sayıda bileşen içermesinden dolayı spesifik hücresel hedeflere sahip değillerdir (Carson ve ark., 2002). Tipik lipofiller olarak hücre duvarı ve sitoplazmik memranlardan geçer ve farklı polisakkarit yapıları, yağ asitleri ve fosfolipidleri etkileyerek geçirgenliği bozmaktadır. Sitotoksisitesi membran zararını içerir ve bu özelliği sayesinde antimikrobiyal etki göstermektedir. Bakterilerde membranın geçirgenliğini etkileyerek iyon kaybı sonucu membran potansiyelinin düşmesine, proton pompasının çökmesine ve ATP havuzunun boşalmasına neden olabilmektedirler (Knobloch ve ark., 1989; Helander ve ark., 1998; Di Pasqua ve ark., 2006; Turina ve ark., 2006). Uçucu yağlar sitoplazmayı yoğunlaştırabilir (Gustafson ve ark., 1998), lipid ve proteinlere zarar verebilirler (Ultee ve ark., 2002; Burt, 2004). Hücre duvarı ve membranlarının zarar görmesi makromoleküllerin sızmasına ve lizise neden olabilir (Juven ve ark., 1994; Gustafson ve ark., 1998; Cox ve ark., 2000; Lambert ve ark., 2001; Oussalah ve ark., 2006). Ökaryotik hücrelerde de membran potansiyelini düşürerek mitokondriyal membranların depolarizasyonuna neden olabilir ve iyonik Ca++ döngüsünü etkileyebilirler (Richter ve Schlegel, 1993; Novgorodov ve Gudz, 1996; Vercesi ve ark., 1997).
Günümüze kadar yapılan pek çok çalışma ile uçucu yağların mutajenlerin hücre içine girişini engellediği (Kada ve Shimoi, 1987; Shankel ve ark., 1993), hücre antioksidan enzimlerinin aktivasyonu veya mutajenler tarafından üretilen serbest radikalleri süpürerek onların inaktivasyonunu sağlaması sonucu (Hartman ve Shankel, 1990; Sharma ve ark., 2001; Ipek ve ark., 2005) antimutajenik özellik gösterdiği belirlenmiştir. Ayrıca sıcak iklimlerde uçucu yağca zengin bitkilerde uçucu yağların hızla buharlaşarak yüzeylerin soğumasını sağladığı ve bitkinin su kaybını önlediği anlaşılmıştır (Manville ve ark., 1989).
2.6. Bitkisel Yağlar
Bitkilerin yağ asidi bileşimi doymuş yağlara oranla daha yüksek oranda tekli ve çoklu doymamış yağ asidi içermelerinden dolayı genellikle sağlıklı olarak kabul edilir. Buna bağlı olarak bitkisel ürünlerin tüketiminin artırılması tavsiye edilmektedir. Lipidler gıdaların önemli bileşenlerindendir. Lipidlerin varlığı, miktarı ve kompozisyonu yalnızca lezzet bakımından değil aynı zamanda beslenme ve kalitenin korunması açısından da önemlidir. Gıdalarda bulunan lipidlerin çok düşük seviyesi bile daha lezzetli ve tatmin edici bir tadın ortaya çıkmasında etkilidir. Ayrıca bütün dokulardaki hücre membranlarının yapısal materyali olarak iş görmesi yanında esansiyel yağ asitlerini ve yağda eriyen vitaminleri sağlaması açısından da oldukça önemli bir role sahiptir (Gurr ve James, 1975). Birçok yağ asidi normal biyolojik fonksiyonlarda, sağlık ve tarımla ilişkili büyük problemlerde önemli rol oynar (King, 1970; Hansen, 1990). Bitkilerdeki yağ asitlerindeki çeşitlilik besinsel, endüstriyel ve farmakolojik amaçlarla kullanılmasına ek olarak taksonomik ve filogenetik çalışmalarda kullanışlı bir araç haline gelmiştir (Vickery, 1971).
Lipid molekülündeki yağ asitlerinin tipi ve miktarı, bu yağ asitlerinin dağılımı ve pozisyonu onun fiziksel, kimyasal ve fonksiyonel özelliklerini belirler (Dugan, 1976). Bu nedenle yağ asidi kompozisyonunun bilinmesi yeni gıda ürünleri geliştirmeye yardımcı olabilecektir. Bazı orta zincir uzunluğuna sahip yağ asitleri (C12-C18) antimikrobiyal özelliğe sahiptir (Jay, 1986; Beuchat ve Golden, 1989). Ticari bitkisel ürünlerin major yağ asitleri genellikle laurik (12:0), miristik (14:0), palmitik (16:0), stearik (18:0), oleik ( 18:1), linoleik (18:2) ve linolenik (18:3) asit oluşturmaktadır. Bunlardan palmitik, oleik ve linoleik asit en yüksek oranlarda bulunan yağ asitleridir.
Genel olarak, bitkisel kaynaklardan elde edilen lipidler oda sıcaklığında sıvı haldedir ve hayvansal yağlara oranla doymuşluk oranı daha düşüktür (Hitchcock ve Nichols, 1971). Gelişmiş ülkelerde tüketilen yağın kalorisine göre sağlığa etkisi daha büyük önem taşımaktadır. Tüketilen yağ miktarı, yağın içeriğindeki doymuş yağ miktarı ile kolesterol seviyesi ve kardiyovasküler hastalıklar arasında ilişki olduğu bilinmektedir. Özellikle ω3 yağ asitlerinin LDL (Kötü) kolesterol seviyesini düşürerek kalp hastalıkları başta olmak üzere kanser, hipertansiyon ve otoimmünite hastalıklarını önlediği bilinmektedir. Besinsel ω3 yağ asitlerinden en önemlileri dokosahekzaenoik asit (DHA), eikosapentaenoik asit (EPA) ve α-linolenik asit (ALA)‟dır. Bunlardan EPA ve DHA balıklarda yüksek oranda bulunmaktadır (Connor, 2000; Tapiero ve ark., 2002) ve vücut tarafından doğrudan kullanılmaktadır. ALA bitkisel ürünlerden özellikle kabuklu meyvelerde bulunur ve vücutta DHA ve EPA‟ya dönüştürülmektedir. Soya ve kanola yağında da ALA oldukça yüksek oranlarda bulunmaktadır. ω3 ve ω6 çoklu doymamış yağ asitleri insan vücudunda sentezlenemez ve besinlerle dışarıdan alınması gerekmektedir. Diyetimizdeki ω6 yağ asitlerinin kaynağı özellikle bitkisel yağlar ve tahıllar gibi bitkisel kaynaklardır. ω3 bitkilerde ve deniz kaynaklı ürünlerde bulunan uzun zincirli doymamış yağ asitleridir (Friedman ve Moe, 2006). Bu yağ asitleri bitkisel ürünlerden özellikle sert kabuklu meyvelerde (ceviz vb.) ve tohumlarda yaygın olarak bulunmaktadır (Namiki, 2007). ω3 ve ω6 yağ asitlerinin diyetteki uygun düzeylerde alınması önemlidir ve bunların sağlığa katkıları birlikte alınmalarıyla daha önemli düzeylerdedir (Logan, 2004).
ω3 yağ asitleri doymuş yağ asitlerinin aksine romatoid artritin tedavisi (Rennie ve ark., 2003) ve kan basıncını düzenleyerek koroner kalp hastalıklarını önleme (Freeman, 2000) gibi sağlık açısından faydalı etkilere sahiptir. Ayrıca antiinflamatuar özelliklerinden dolayı inflamatuara bağlı barsak, egzama ve sedef gibi hastalıkların tedavisinde de kullanılmaktadır (Cleland ve ark., 2003).
2.7. Fabaceae Familyası ve Glycyyrhiza L. Cinsi
Fabaceae (Leguminosae=Baklagiller) çiçekli bitkilerin üçüncü büyük familyasıdır. Türkiye Florasında 69 cins ve 1000‟den fazla türle temsil edilmektedir (Davis, 1970; Davis ve ark., 1988; Seçmen ve ark., 1989). Bu familyaya ait olan ağaç, çalı ve otsu bitkilerin büyük bir çoğunluğu önemli ekonomik değere sahiptir ve genellikle ılıman, subtropik ve tropik bölgelerde yayılış göstermektedir (Hickey ve
King, 1997). Familya, Mimosoideae, Caesalpinioideae ve Papilionoideae alt familyalarına ayrılmaktadır.
Baklagiller binlerce yıldır kültüre edilmektedir ve dünya çapında bir çok bölgede geleneksel diyette önemli rol oynamaktadır (Grela ve ark., 1999; Prati ve ark., 2007). Tohumları protein, nişasta, bazı yağ asitleri, vitamin ve mineral gibi besleyici içeriğiyle zengin bir gıda kaynağıdır (Morrow, 1991; Souci ve ark., 2000; Trosyznska ve Ciska, 2002). Sağlık üzerine faydalı etkilere sahip olan yağı iyi bir yağ kaynağı olabileceği düşünüldüğünden araştırmacıların ilgisini çekmektedir (Siriamornpun ve ark., 2006). Fabaceae‟nin bazı türleri yüksek protein içeriğiyle insanlar ve hayvanlar için ucuz bir protein kaynağıdır (Chang ve Satterlee, 1979; Platt, 1980).
Fabaceae familyasına ait ve çok yıllık bir bitki olan Glycyrrhiza cinsinin bütün türlerine genel olarak meyan adı verilmektedir. 10-120 cm yükseklikte, çok yıllık, rizomlu, mavimsi mor çiçekli bitkilerdir. Tatlı olan kökleri tedavide ve meyan şerbeti hazırlamakta kullanılır. Bu şerbet özellikle Diyarbakır ve Urfa gibi ülkemizin Güney Doğu Anadolu Bölgesindeki illerde yaygın olarak tüketilmektedir. Kökler genellikle G.
echinata ve G. glabra‟dan elde edilmektedir (Baytop, 1984). Bir sap etrafında simetrik
olarak dizilmiş olan yaprakçıklar ile terminal yaprakçık birleşik yaprağı teşkil eder (Oğuz, 1972). Bol çiçek açar. Çiçek salkımı 15 cm uzunluğuna kadar erişen bir eksen etrafında gevşek ve homojen olarak bulunur (Rechinger, 1957; Oğuz, 1972).
Meyan antik çağlardan beri geleneksel ilaç olarak en yaygın kullanılan bitkilerden biridir. Meyan kökü en zengin biyolojik olarak aktif bileşik kaynaklarındandır (Roth, 2004). Bitkinin kullanımının izlerine antik Asur, Mısır, Çin ve Hindistan kültürlerine kadar rastlanabilir (Armanini ve ark., 2002; Fiore ve ark., 2005). 6000 yılı aşkın süredir Çin‟de tıbbi amaçlarla kullanılmaktadır (Vaya ve ark., 2004). Meyan köküyle ilgili bildirilen tıbbi ve faydalı etkiler antibakteriyel, ülser, anti-tümör, anti-aterosklerotik, anti-inflamatuar ve antioksidan etkileri içermektedir (Shibata, 2000; Kitagawa, 2002; Vaya ve ark., 2004). Köklerden izole edilen bazı flavonoidlerin oksidasyona karşı güçlü antioksidan aktivite sergilediği görülmüştür (Gordon ve An, 1995). Kökün ana bileşenleri olan glycyrrhizin ve glycyrrhetinic asit klinik olarak hiperlipidemi, arterosklerozis ve alerjik inflamasyonun tedavisinde kullanılmaktadır (Lin ve ark., 2005).
3. MATERYAL VE YÖNTEM
3.1. ÇalıĢmada Kullanılan Glycyrrhiza Türleri ve Özellikleri
Çalışmada kullanılan Glycyrrhiza taksonları florada belirtilen lokalitelerden çiçeklenme dönemlerinde toplanmıştır. Türkiye‟de doğal olarak yetişen Glycyrrhiza taksonlarının dördü endemiktir (Chamberlain, 1970; Sümbül ve ark., 2003) . Üzerinde çalışma yapılan bitkilerin toplayıcı adı, numarası ve toplandığı lokalite bilgileri Çizelge 3.1‟de verilmiştir.
Çizelge 3.1. Glycyrrhiza taksonlarının toplayıcısı, numarası ve lokalite bilgileri
Bitkinin Adı Toplayıcı ve No. Yükselti Tarih Lokalite
G. asymmetrica Hub.-Mor. Ö. Çetin-1038 30 m 09.06.2011
Antalya: Antalya-Aksu arası, Aksu‟yu 1 km geçince
G. echinata L. Ö.Çetin-1043 20 m 11.06.2011
Antalya: Serik, Boğazak köyü, yol kenarı-tarla kenarı G. flavescens Boiss. subsp.
antalyensis Sümbül et al. Ö.Çetin-1030 & A.Duran 5 m 13.03.2011
Antalya: Kemer- Tekirova-Çıralı arası, antik yol
G. flavescens Boiss. subsp.
flavescens Ö.Çetin-1031 & A.Duran 930 m 8.04.2011
Antakya: radar yolu, Kisecik köyü yukarısı
G. glabra L. var. glabra Ö.Çetin-1036 & A.Duran 448 m 20.05.2011
Kahramanmaraş: Aksu nehrine varmadan, tarla kenarı
G. glabra L. var. glandulifera
(Waldst. Et Kit.) Boiss. Ö.Çetin-1027 & A.Duran 570 m 15.06.2010
Gaziantep-Şanlıurfa Otobanı, Nizip ayrımı
G. iconica Hub.-Mor. Ö.Çetin-1026 & A.Duran 992 m 01.06.2010
Konya: Sarayönü Gözlü çiftliği, Gözlüye varmadan
Endemik türler Glycyrrhiza iconica (Konya), Glycyrrhiza flavescens subsp.
flavescens (Hatay, Mersin, Adana), G flavescens subsp. antalyensis Sümbül, Ö. Tufan,
O.D. Düsen & R.S. Göktürk (Antalya) ve G. asymmetrica (Antalya)‟dır. Glycyrrhiza
glabra var. glabra, Glycyrrhiza glabra var. glandulifera, Glycyrrhiza echinata türleri
geniş yayılışlı olmasına rağmen ülkemizde sadece bir lokaliteden (Kahramanmaraş-Ceyhan Vadisi) bilinmektedir. Bu tür en son 1930‟lu yıllarda toplanmış olup araştırmamızda bu lokalitede yapılan arazi çalışmalarında bulunamamıştır. Bitkinin çevresel faktörler ve inşa edilen baraj nedeniyle yok olduğu düşünülmektedir. Dolayısıyla çalışma G. aspera hariç 7 takson olarak yürütülmüştür.
Şekil 3.1. Glycyrrhiza asymmetrica Şekil 3.2. Glycyrrhiza echinata
Şekil 3.5. Glycyrrhiza glabra var. glandulifera Şekil 3.6. Glycyrrhiza iconica
3.2. Bitkisel Ekstraktların Hazırlanması
Bitki örneklerinin toprak üstü ve kök kısımları ayrı ayrı incelenmiştir. Toprak üstü kısımları bitkinin gövde, yaprak, çiçek ve meyve gibi bütün kısımlarını içermektedir. Bitkisel örnekler toplanıp gölgede kurutulduktan sonra değirmende iyice toz haline getirildi. Toz haline gelen örneklerden antioksidan analizler için yaklaşık 15 g tartılıp literatürlerde en sık karşılaşılan çözücü olan metanol ile sokslet aparatında 6-8 saat süreyle antioksidan kapasite testleri için ekstraksiyon işlemine tabi tutuldu.
3.3. Antioksidan Kapasitenin Belirlenmesinde Uygulanan Metotlar
3.3.1. Toplam Fenolik Madde Tayini (Folin Yöntemi)
Bitki ekstraktlarının konsantrasyonu 2 mg/ml olacak şekilde hazırlandı. Standart olarak kullanılacak olan gallik asidin ise 100 µg/ml konsantrasyonu stok olarak hazırlandı ve bu konsantrasyondan seyreltme ile beş farklı konsantrasyon elde edildi. Bitkisel drogların her bir konsantrasyonundan 200 µl ayrı deney tüplerine alındı. Daha sonra her bir tüpe 1 ml Folin-Ciocalteu reaktifi ilave edildi. Ardından her bir tüpe 2 ml %7.5‟lik Na2CO3 çözeltisinden eklendi ve toplam hacim 7 ml olacak şekilde saf su ilave edildi. Karışımlar oda sıcaklığında karanlıkta 2 saat bekletildikten sonra 765 nm‟de absorbansları ölçüldü. Tüm antioksidan kapasite tayin testlerinde spektrofotometrik ölçümler Shimadzu UV-1800 spektrofotometre cihazı kullanılarak gerçekleştirildi. Aynı
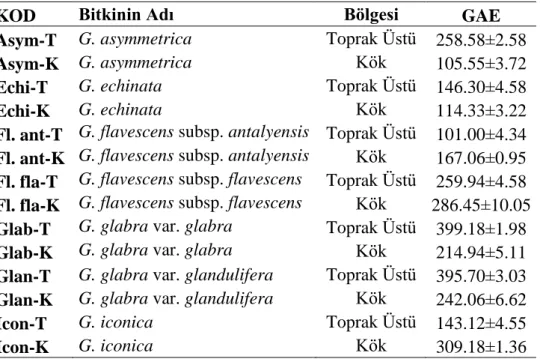
işlemler standart olarak kullanılan gallik asit için de tekrarlandı. Bitkilerin fenolik madde içeriği gallik asit eş değeri (mg GAE/g) olarak verildi (Slinkard ve Singleton, 1977).
3.3.2. Toplam Flavonoid Madde Tayini
Bitki ekstraktlarındaki toplam flavonoid içeriği spektrofotometrik olarak belirlenmiştir. Buna göre %2‟lik AlCl3‟ün metanolik çözeltisinden 1 ml alınarak aynı hacimde ve 2 mg/ml konsantrasyondaki bitki ekstraktı ile karıştırıldı. 10 dakika bekledikten sonra 415 nm‟de karışımın köre karşı absorbansı belirlendi. Aynı işlemler standart flavonoid olan rutin için de yapılarak rutine ait kalibrasyon eğrisi çizildi. Sonuçta ekstraktların toplam flavonoid madde içerikleri rutin eş değer (mg RE/g) olarak verildi.
3.3.3. Toplam Antioksidan Kapasitenin Belirlenmesi
Metodun esası Mo(VI)‟nın Mo(V)‟e indirgenmesi ve asidik ortamda yeşil renkli fosfat/Mo(V) kompleksinin oluşumuna dayanır. Metotta öncelikle bitki ekstraktlarının konsantrasyonları 2 mg/ml olacak şekilde çözeltileri hazırlandı. Standart olarak ise askorbik asit 500 µg/ml ile 31.25 µg/ml arasında beş farklı konsantrasyonda kullanıldı. Metotta kullanılacak reaktif çözeltisi aşağıdaki gibi hazırlandı:
0.6 M H2SO4 çözeltisi: 0.83175 ml H2SO4 alınır ve 24.18825 ml saf su üzerine sızdırılarak ilave edildi.
28 mM Na2HPO4.12H2O çözeltisi: 0.025 gr Na2HPO4.12H2O tartılıp hacmi saf su ile 25 ml‟ye tamamlandı.
4 mM Amonyum molibdat çözeltisi: 0.123585 gr amonyum molibdat tartılıp
hacmi saf su ile 25 ml‟ye tamamlandı.
Bu şekilde hazırlanan çözeltiler bir mezürde karıştırılarak reaktif çözeltisi hazırlandı. 1 mg/ml konsantrasyonunda bitkisel çözeltilerden 0.3 ml bir tüpe alındı ve bunun üzerine reaktif çözeltisinden 3 ml eklendi. Tüpler kuvvetlice karıştırılıp 95 °C‟de 90 dakika inkübe edildi. İnkübasyon sonunda çözeltilerin absorbansı 695 nm‟de okundu. Aynı işlemler standart antioksidan olarak kullanılan askorbik asit için de yapıldı. Antioksidan aktivite askorbik asit eşdeğeri (mg AE/g) olarak hesaplandı (Prieto ve ark., 1999).
3.3.4. β-karoten/Linoleik Asit Emülsiyon Sistemi
Bitkisel materyal ve standart antioksidanlar 200 µg/ml konsantrasyonda hazırlandı. Metotta öncelikle emülsiyon çözeltisi hazırlandı. Bunun için 1 mg β-karoten 2 ml kloroformda çözüldü. Bu karışıma 50 µl linoleik asit ve 200 mg Tween 40 eklendi. Karışım iyice karıştırıldı. Kloroform rotary evaporatörde 40 °C‟de iyice uçuruldu. Kalan kısım üzerine 200 ml saf su eklendi. Böylece emülsiyon çözeltisi hazırlanmış oldu.
1 mg/ml konsantrasyonundaki bitkisel droglar ve standart maddelerden 350 µl alındı ve bunların üzerine 2.5 ml emülsiyon çözeltisinden ilave edildi. Emülsiyon çözeltisi eklenir eklenmez absorbansları 490 nm‟de okundu. Daha sonra tüpler 50 °C‟de 120 dakika inkübe edildi. Ayrıca bitkisel materyalin yerine 350 µl metanol eklenip bunun üzerine de 2.5 ml emülsiyon çözeltisi ilave edilerek kontrol çözeltisi hazırlandı. Kontrol çözeltisinin absorbansı da emülsiyon çözeltisi eklenir eklenmez okundu ve aynı şekilde 50 °C‟de 120 dakika inkübe edildi (Sokmen ve ark., 2004).
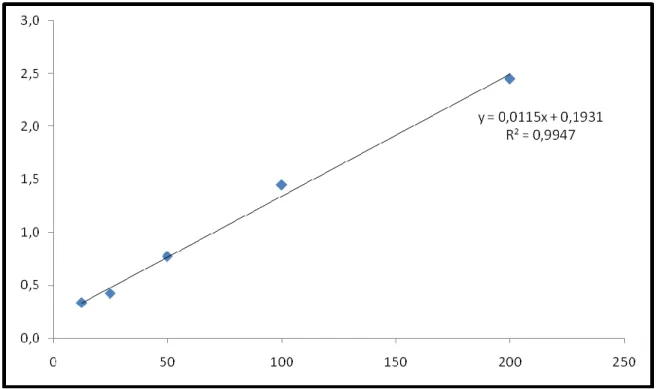
120 dakika sonunda renk açılım oranı hesaplandı. R= ln(A/B)/t A: Başlangıç absorbansı
B: 120 dakika sonundaki absorbansı t: 120 dakika
Bu eşitlikten inhibisyon değeri yani antioksidan aktivite hesaplandı. İnhibisyon değeri= ((Rkontrol-Rörnek)/ Rkontrol)x100
Ayrıca her bir bitkisel drog ve BHT için bağıl antioksidan aktivite de hesaplandı.
3.3.5. DPPH Süpürme Etkinliği
Bitkisel drogların farklı konsantrasyonlarda çözeltileri hazırlandı. Bunun için öncelikle 400 µg/ml konsantrasyonluk ve daha sonrasında seyreltme ile dört farklı konsantrasyonda çözeltiler elde edildi (400-100 µg/ml). Sentetik antioksidanlar olan BHT ise 200 µg/ml ile 3.125 µg/ml konsantrasyonları arasında beş farklı konsantrasyonda hazırlandı. DPPH çözeltisi ise 6x10-5
M konsantrasyonda hazırlandı ve bundan seyreltme ile kalibrasyon eğrisi için beş farklı konsantrasyon elde edildi.
Farklı konsantrasyonlardaki bu bitkisel çözeltilerden 0.5 ml alınıp bunun üzerine 6x10-5 M konsantrasyondaki DPPH çözeltisinden 3 ml ilave edildi. Tüpler ağızları
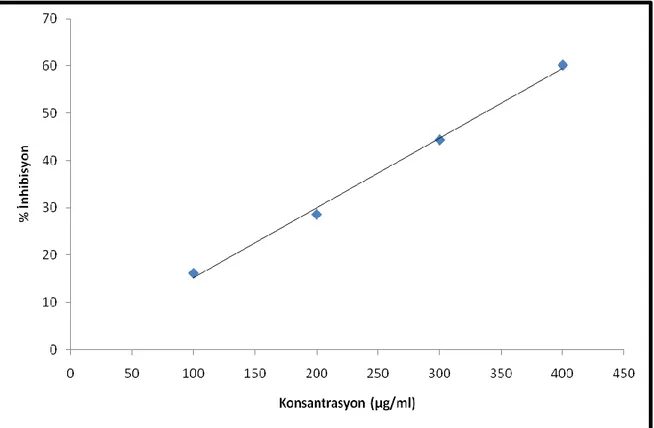
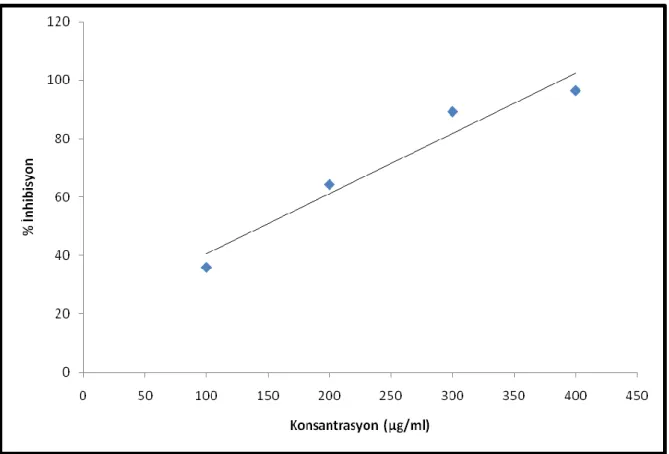
kapatılıp kuvvetlice karıştırıldıktan sonra oda sıcaklığında karanlıkta 30 dakika bekletildi. Bu süre sonunda absorbanslar 517 nm‟de okundu. Bitkisel çözeltilerin ve standart maddelerin inhibisyonu aşağıdaki denklemden hesaplandı:
İnhibisyon(%)=((Akontrol-Aörnek)/Akontrol)x100
Bitkisel çözeltiler ve standart maddelerin konsantrasyon inhibisyon grafiği çizilerek buradan DPPH radikalinin yarısını süpürebilen konsantrasyon hesaplandı (IC50). IC50 değerinin düşük olması antioksidan kapasitenin yüksek oluşunu göstermektedir (Sarikurkcu ve ark., 2008).
3.3.6. Demir Ġndirgeme Gücü
Bu metotta bitkisel ekstraktların 1000 µg/ml ile 50 µg/ml konsantrasyonları kullanıldı. Standart olarak aynı konsantrasyonlarda BHT hazırlandı. Farklı konsantrasyonlardaki bitkisel çözeltilerden 2.5 ml alındı. Bunun üzerine 0.2 M pH 6.6 2.5 ml fosfat tamponu ve %1‟lik 2.5 ml potasyum ferrisiyanür eklendi. Tüpler 50 °C‟de 20 dakika inkübasyona bırakıldı. İnkübasyon sonrası tüplerin üzerine 2.5 ml %10‟luk TCA ilave edildi. Tüpler iyice karıştırıldıktan sonra üst kısımlarından 2.5 ml başka bir tüpe aktarıldı. Bu tüpün üzerine de 2.5 ml saf su ve 0.5 ml %0.1‟lik FeCl3 çözeltisi eklendi.
Çözeltilerin absorbansları 700 nm‟de okundu (Oyaizu, 1986). Absorbans arttıkça indirgeme gücü de artış göstermektedir.
3.3.7. CUPRAC Metodu
10-2 M Cu(II) klorür çözeltisi;. CuCl2.2H2O‟den 0.4262 g tartılarak su ile 250 ml‟ye tamamlanarak hazırlandı.
Amonyum asetat tamponu; 1 M (pH=7). NH4Ac‟dan 19.27 g tartılarak su ile 250 ml‟ye tamamlanarak hazırlandı.
Neokuproin çözeltisi: 7.5x10-3 M, Neokuproin (2,9 dimethyl 1-10 phenantroline)‟den 0.039 g tartılarak %96‟lık etil alkolle 25 ml‟ye tamamlanarak hazırlandı.
Bitki ekstraktlarının 400 µg/ml ile 25 µg/ml arasındaki beş farklı konsantrasyonları kullanıldı. Metotta öncelikle her bir deney tüpüne 1 ml CuCl2.2H2O, 1 ml amonyum asetat, 1 ml neokuproin çözeltileri ile 0.6 ml saf su eklenir. Daha sonra