ÖZET
Doktora Tezi
KALİKS[4]ARENLERİN HOMOKİRAL AMİT TÜREVLERİNİN SENTEZİ ve ENANTİYOMERLERİN TANINMASINDA KULLANILMASI
Erdal KOCABAŞ Selçuk Üniversitesi Fen Bilimleri Enstitüsü
Kimya Anabilim Dalı
Danışman: Prof. Dr. Abdulkadir SIRIT 19 Ekim 2007, Sayfa: 118
Jüri:
Prof. Dr. Mustafa TOPRAK Prof. Dr. A. Dinçer BEDÜK
Prof. Dr.Mustafa YILMAZ Prof. Dr. Bedrettin MERCİMEK
Prof. Dr. Abdulkadir SIRIT
Bu çalışmada p-t-bütilkaliks[4]aren ve kaliks[4]aren’in kiral sekiz yeni amit türevi (5-8, 9-12); 5,11,17,23-tetra-ter-bütil-25,27 dietoksikarbonilmetoksi-26,28- dihidroksi kaliks[4] aren (3) ve 25,27 dietoksikarbonilmetoksi-26,28-dihidroksi kaliks[4] aren (4) ile 2- amino-1-butanol, fenil glisinol, 3-fenil-1-amino-propanol ve (1S,2S)-(+)-2-amino-1-(4-nitrofenil)-1,3-propandiol amino alkolleri tepkimeye sokularak elde edilmiştir. Kaliks[4]arenin kiral amit türevleri kiral aminlerin moleküler tanınma çalışmalarında ve amino asitlerin faz transfer ekstraksiyonunda kullanılmıştır. Ayrıca bu bileşiklerden 10 ve
12’ nin feniletil amin ve 1,2-propandiol guestlerine karşıkiral tanınma özellikleri 1H NMR spektroskopisi kullanılarak incelenmiştir.
Gerçekleştirilen tüm reaksiyonlar İTK ile izlenmiş ve elde edilen ürünler kolon kromatografisi ile saflaştırılarak yapıları IR ve 1H NMR, 13C NMR ve FAB MS teknikleriyle aydınlatıldıktan sonra kiral bileşiklerin optik çevirme açıları ölçülmüştür.
Anahtar Kelimeler: Kaliks[4]aren; homokiral amit, Enantiyomerik ve moleküler
ABSTRACT
Ph. D. Thesis
THE SYNTHESIS OF HOMOCHIRAL AMIDE CALIX[4]ARENE DERIVATIVES AND THE USE OF THEIR FOR RECOGNITION OF
ENANTIOMERS Erdal KOCABAŞ Selcuk University
Graduate School of Natural and Applied Science Department of Chemistry
Supervisor: Prof. Dr. Abdulkadir SIRIT
19 October 2007, Page: 118
Jury:
Prof. Dr. Mustafa TOPRAK Prof. Dr. A. Dinçer BEDÜK
Prof. Dr. Mustafa YILMAZ Prof. Dr. Bedrettin MERCİMEK
Prof. Dr. Abdulkadir SIRIT
In this study, eight novel chiral amide derivatives of calix[4]arene and
p-tert-calix[4]arene (5-8, 9-12) have been synthesized from the reaction of
5,11,17,23-tetra-ter-butyl-25,27 diethoxycarbonylmethoxy-26,28-dihydroxy calix[4] arene (3) ve 25,27 diethoxycarbonylmethoxy-26,28-dihydroxy calix[4] arene with 2- amino-1-butanol, phenyl glycinol, 3-phenyl-1-amino-propanol and (1S,2S)-(+)-2-amino-1-(4-nitrophenyl)-1,3-propanediol, respectively. Chiral amide derivatives of calix[4]arene and p-tert-calix[4]arene have been used for molecular recognition of chiral amines and also phase transfer extraction of some selected α-amino acids. Moreover chiral recognition capability of 10 ve 12 compounds towards the guests; phenylethyl amine and 1,2-propanediol by 1H NMR spectroscopy was investigated.
The reactions were monitored by TLC and pure compounds were obtained after crystallysation, column chromatography or both. The structures of synthesized compounds were identified by IR, 1H NMR 13C NMR ve FAB MS and optical rotation measurements were also included.
Keywords: Calix[4]arene; homochiral amide; Enantiomeric and molecular
ÖNSÖZ
Bu çalışma, Selçuk Üniversitesi Eğitim Fakültesi Kimya Eğitimi Anabilim Dalı öğretim üyelerinden Prof. Dr. Abdulkadir SIRIT danışmanlığında hazırlanarak, Selçuk Üniversitesi Fen Bilimleri Enstitüsü’ ne Doktora Tezi olarak sunulmuştur. Bu çalışma aynı zamanda S. Ü. Bilimsel Bilimsel Araştırma Projeleri Koordinatörlüğü tarafından FBE 2004/081 no lu proje olarak desteklenmiştir.
Doktora tez konusunun seçiminde, hazırlanmasında ve çalışmamın her safhasında yardımlarını esirgemeyen, beni bilgi ve tecrübeleriyle yönlendiren değerli danışman hocam Sayın Prof. Dr. Abdulkadir SIRIT’ a saygı ve şükranlarımı sunarım.
Çalışmalarım boyunca devamlı yardım ve desteklerini gördüğüm Fen Edebiyat Fakültesi Kimya Bölümü Öğretim Üyelerinden Sayın Prof. Dr. Mustafa YILMAZ’ a, Selçuk Üniversitesi Rektör Yardımcısı ve aynı zamanda Tez İzleme Komitesi’nin üyesi olan Prof. Dr. A. Dinçer BEDÜK’ e saygı ve şükranlarımı sunarım.
Tezimin her aşamasında yardım ve desteklerini gördüğüm değerli hocam Yrd. Doç. Dr. Sabri ALPAYDIN’ a ve çalışma arkadaşlarım Yrd. Doç. Dr. Ayşegül KARAKÜÇÜK İYİDOĞAN’ a ve Arş. Gör. Mustafa DURMAZ’ a, Doktora Öğrencisi Selahattin BOZKURT’ a, Selçuk Üniversitesi Eğitim Fakültesi Kimya Eğitimi Anabilim Dalı’ndaki ve Fen-Edebiyat Fakültesi Kimya Bölümü’ndeki diğer hocalarıma ve Araştırma Görevlisi arkadaşlarıma teşekkür ederim.
Son olarak eşim Hilal’e, bana gösterdiği sonsuz sevgi, destek ve sabır için teşekkür ediyorum
Erdal KOCABAŞ
İÇİNDEKİLER ÖZET...ii ABSTRACT... iv ÖNSÖZ... vi İÇİNDEKİLER ...vii ŞEKİLLER LİSTESİ... ix
ÇİZELGELER LİSTESİ... xiv
1. GENEL BİLGİLER... 1
1.1. Kaliksarenler ... 2
1.2. Kaliksarenlerin Adlandırılması ... 2
1.3. Kaliksarenlerin Yapısı ve Sentezi ... 4
1.3.1. Tek Basamaklı Sentez...4
1.3.2. Çok Basama Sentez……….6
1.3.3. Asit Katalizörlü Kaliksaren Sentezi………8
1.4. Kaliksarenlerin Konformasyonları... 8
1.5. Fonksiyonlandırılmış Kaliksarenlerin Sentezi ... 10
1.6. Kaliksarenlerin Fiziksel Özellikleri ... 14
1.6.1. Erime Noktaları……….14
1.6.2. Çözünürlükleri………..14
1.6.3. HPLC de ayrılmaları……….14
1.6.4. Kaliksarenlerin pKa değerleri………15
1.6.5. Kaliksarenlerin Dipol Momentleri………16
1.6.6. Kaliksarenlerin IR Spektrumları………...17
1.6.7. 1H-NMR Spektrumları………..17
1.7. Kaliksarenlerin Kullanım Alanları... 19
1.7.1. Kaliksarenlerin Enzim Mimik Olarak Kullanılması……….19
1.7.2. Kaliksarenlerin Molekül veya İyon Taşıyıcı Olarak Kullanılması……...20
1.7.3. Kaliksarenlerin Enantiyomerlerin Tanınmasında Kullanılması…………26
1.7.4. Kaliksarenlerin Kromatografide Kullanılması………..30
1.7.5. Kaliksarenlerin Katalizör Olarak Kullanılması………34
1.7.6. Kaliksarenlerin Nanoteknolojide Kullanılması………37
1.8. Aminoasitler ve Aminoalkoller... 38
2. KAYNAK ARAŞTIRMASI ... 41
3. MATERYAL VE METOT... 64
3.1. Kullanılan Kimyasal Maddeler ve Çözücüler... 64
4.2.4. 25,27 dietoksikarbonilmetoksi-26,28-dihidroksi kaliks[4] aren (4) 69 4.2.5. Kaliks[4]arenin kiral diamid türevlerinin sentezi için genel prosedür
(5-12)………...69 Bileşik 5 ... 70 Bileşik 6 ... 70 Bileşik 7 ... 71 Bileşik 8 ... 72 Bileşik 9 ... 72 Bileşik 10 ... 73 Bileşik 11 ... 74 Bileşik 12 ... 74 4.3. Sıvı-Sıvı Ekstraksiyonu... 75
4.3.1. Aminoasit Pikrat Çözeltilerinin Hazırlanması………..76
4.4. Log – Log Grafik Analizleri ... 76
4.5. 1H NMR ile Enantiyomerik Tanınma Çalışması... 77
5. ARAŞTIRMA SONUÇLARI VE TARTIŞMA... 78
5.1. Çalışmanın Amacı... 78
5.2. Kaliksarenin Kiral Amit Türevlerinin Sentezi ... 80
5.3. Amino Asit Metil Esterlerinin Ekstraksiyonu... 86
5.4. Enantiyomerik ve Moleküler Tanınma Çalışmaları... 89
5.5. 1H NMR Spektrumu ile Kiral Tanınma ve Kompleksleşme Çalışmaları ... 95
6. SONUÇ VE ÖNERİLER... 100
7. KAYNAKLAR ... 101
8. EKLER... 109
ŞEKİLLER LİSTESİ
Şekil 1.1. Supramoleküllerin yapısı (Siklodekstrinler, crown eterler, kaliksarenler).. 1
Şekil 1.2. p-alkilkaliks[n]arenlerin numaralandırması... 3
Şekil 1.3. Siklik tetramerlerin sentezi... 4
Şekil 1.4. Kaliksarenlerin tek basamaklı sentezi ... 5
Şekil 1.5. Birbiriyle yaklaşık olmayan çok basamaklı sentez... 6
Şekil 1.6. [3+1] kondenzasyonuyla sentez... 7
Şekil 1.7. [2+2] kondenzasyonuyla sentez... 7
Şekil 1.8. Kaliks[4]arenlerin konformasyonel izomerleri... 9
Şekil 1.9. Kaliks[4]arenin p-konumunun ve fenolik OH’larının şematik gösterimi.. 11
Şekil 1.10. Kinonmetit yoluyla aminokaliks[4]arenlerin sentezi……….. 12
Şekil 1.11. p-t-butilkaliks[4arenin fenolik –OH ve para pozisyonları üzerinden fonksiyonlandırılması……….13
Şekil 1.12. p-tert-butil kaliks[n]aren karışımının HPLC’ de yürütülmesi( piklerin üzerindeki rakamlar n sayısını ifade etmektedir.)………...15
Şekil 1.13. p-t-butil kaliks[4]arenin CDCl3’deki 1H-NMR spektrumu... 18
Şekil 1.14. Açiltransferaz aktivite gösteren kaliks[4]aren türevleri. ... 19
Şekil 1.15. 12-17 bileşiklerinin katalize ettiği p-nitrofenil benzoat (PNB) ve asetat (PNA)………..19
Şekil 1.16. Metalloenzimler için etkili kaliks[6]aren yapısı ... 20
Şekil 1.17. p-alkilkaliks[4]aren’ in kompleks oluşturma mekanizması………21
Şekil 1.18. Kiral kaliks[4](azoksa)crown-7 bileşiğinin sentezi………..22
Şekil 1.19. Kiral kaliks[4](azoksa)crown-7 türevinin Li+ ve geçiş metali katyonlarıyla yaptığı kompleksleşmenin mekanizması ... 23
Şekil 1.20. Kaliks[4]aren diamid türevlerinin kromat anyonuyla yaptığı muhtemel etkileşme……….24
Şekil 1.24. Çalışmanın genel sentez çalışması ve kiral tanımada kullanılan
karboksilik asitler... 29
Şekil 1.25. (a) 2a’nın 1H NMR spekrumu(5 mM) (b) 2a (5 mM) ve 3a (20 mM) arasındaki kompleksin spektrumu (c) 2a (5 mM) ve 3a (92 mM) arasındaki kompleksin spektrumu (d) 2b (5 mM)’nin spektrumu (e) 3b (5 mM)’nin spektrumu (f) 2b (5 mM) ve 3b (5 mM) arasındaki kompleksin spektrumu………29
Şekil 1.26. N(O,S)-TFA-D,L-amino asit metil esterlerinin gaz kromatografisi ile enantiyomerlerine ayrılması………..30
Şekil 1.27. Çalışmanın genel sentez şeması………..31
Şekil 1.28. Çalışmada kullanılan kaliksaren ve resorsinaren durgun fazları……….32
Şekil 1.29. İncelenen analitlerin yapıları………...32
Şekil 1.30. p-tert-butil kaliks[6]-1,4-benzocrown-4 bağlı durgun fazın sentez şeması...33
Şekil 1.31. Krom (III)/p-tert-butil kaliks[4]aren bileşiği için muhtemel monomerik (a) ve dimerik (b) yapılarının şematik gösterimi………34
Şekil 1.32. Çalışmada gerçekleştirilen aldol reaksiyonu ve katalizör olarak kullanılan kaliksaren türevleri………..35
Şekil 1.33. Silika yüzeyine immoblize edilen p-t-bütilkaliks[4]arenin aromatik bileşikleri adsorbsiyonu………..37
Şekil 1.34. Amfiphilik kaliksaren türevlerinin yapıları………..38
Şekil.1.35. 1-7 nolu aminoasitlerin yapıları……….39
Şekil 1.36. 8-11 nolu aminoasitlerinin yapıları………..40
Şekil 2.1. Dikromat anyonlarının ekstraksiyonu için kullanılan kaliks[4]aren diamit türevleri ... 41
Şekil 2.2. 5 – 10 reseptörlerinin dikromat ekstraksiyon yüzdeleri ... 41
Şekil 2.3. Kaliks[6]arenin kiral türevleri………. 42
Şekil 2.4. 5-(4-isothiocyanatophenyl)-10,15,20-tris-(dimethyl)-calix[4]phyrin-(1,1,1,1)’ in sentezi ve reaksiyonları………...44
Şekil 2.5. (a) Bu4NF’ nin artan konsantrasyonlarda ilavesinin 2 numaralı bileşiğe etkisini gösteren kısmi 1H-NMR spektrumu. (b) florür anyonlarının varlığında görülen piklerdeki kaymalar………...45
Şekil 2.7. 1H NMR spektrumu ( 499.885 MHz, CDCl3, 298 K, her biri 15 mmol L-1):
(a) saf (±)-4 (b) kompleks 1-2- (±)-4... 47 Şekil 2.8. 1H NMR spektrumu ( 499.885 MHz, CDCl3, 298 K, her biri 15 mmol L-1):
(a) saf (±)-5 (b) kompleks 1-2- (±)-5... 48 Şekil 2.9. CDCl3 içersinde kaliks[6]aren varlığında tripropil amin (a) ve piperidinin
(b) 1H NMR spektrumu ( Ortadaki sayılar ilave edilen molar equivalant kaliks[6]aren miktarını göstermektedir)... 48
Şekil 2.10. (a) 100% HNO3/CH2Cl2–CH3COOH, rt (45%); (b) SnCl2·2H2O, etanol,
refluks (87%); (c) triphosgene/toluen, reflux ; (d) CH2Cl2 (61%); (e) 100%
HNO3/CH2Cl2–CH3COOH, rt (30%); (f) SnCl2·2H2O, etanol, refluks (88%); (g)
triphosgene/toluen, refluks ; (h) CH2Cl2/çok seyreltik, rt (15%), (i) 1,4-phenylene
diisocyanate/CH2Cl2, rt (84%) ... 50
Şekil 2.11. (a) Br2/CHCl3, rt (95%); (b) PrI/NaH, DMF, rt (87%); (c) (i) BuLi/THF,
-78 °C; (ii) DMF; (iii) su (56%); (d) NaClO3/sulfanilik asit, rt (75%); (i)
(COCl)2/CCl4, refluks, (ii) 8, CH2Cl2/çok seyreltik, rt (10%) ... 52
Şekil 2.12. Genel sentez şeması... 53 Şekil 2.13. Çalışmada sentezlenen kiral hostlar ve kullanılan guestler ... 54 Şekil 2.14. ( R)-1 in asetondaki 2X10-5 M çözeltisinin absorpsiyon spektrumu (a) saf haldeki (b) 10-3 R-MBA (c) 10-2 R-MBA (d) 10-3 S-MBA (e) 10-2 S-MBA, ve ( S)-1 in asetondaki 2XS)-10-5 M çözeltisinin absorpsiyon spektrumu (f) saf haldeki (g) 10-3 S-MBA (h) 10-2 S-MBA (i) 10-3 R-MBA (j) 10-2 R-MBA... 55
Şekil.2.15. (A) Rasemik propandiol (B) S-propandiol ile 3 etkileşmesi (C)
R-propandiol ile 3 etkileşmesi (D) rasemik ile 3’ün etkileşmiş hali (E) rasemik ile 1’in etkileşmiş hali (F) rasemik ile 4’ün etkileşmiş hali 25 derecede CDCl3 içinde…….56
Şekil.2.16. (A) Rasemik SerOMe; (B) Rasemik SerOMe ile 2 nolu host molekül (C) 2 nolu host molekül NMR spektrumları ... 57 Şekil.2.17. Kiral ve akiral aminlerin kompleksleşmesinde kullanılan kaliksarenin
4 mol dm-3) 1.4-7.0×10-2 mol dm-3 (R)-Ph-Et’ in eklenmesi ile gözlenen spektral
değişimler... 59
Şekil 2.20. Genel sentez şeması. (i) – (iii) (S)-(-)-1-Phenylethylamine, (R)-(-)-1-cyclohexylethylamine or (R)-(-)-2-heptylamine, CHCl3/MeOH, refluks ... 62
Şekil 2.21. (a) 4 nolu bileşiğin kloroform içerisindeki çözeltisinin UV-Vis spektrumu (8.33×10-4 mol dm-5). (b) 25°C’ de 4 nolu bileşiğin kloroformdaki çözeltisine (8.33×10-4 mol dm-5) 0.33-2.17×10-2 mol dm-3 (D)-Phe-OMe.HCl in eklenmesi ile gözlenen spektral değişimler... 62
Şekil. 4.1. Kaliks[4]arenin kiral diamid türevleri için genel sentez şeması. i) AlCl3, fenol, toluen ii) EtBrOAc, K2CO3, aseton iii) kiral amino alkol, toluen, metanol.... 66
Şekil 5.1. p-t-bütilkaliks[4]arenin sentezi………..78
Şekil 5.2. p-t-bütilkaliks[4]arenin dealkilasyonu………78
Şekil 5.3. p-t-bütilkaliks[4]arenin diester türevinin sentezi………79
Şekil 5.4. Kaliks[4]arenin diester türevinin sentezi………79
Şekil 5.5. 5 bileşiğinin sentezi………...……….80
Şekil 5.6. 6 bileşiğinin sentezi………81
Şekil 5.7. 7 bileşiğinin sentezi………82
Şekil 5.8. 8 bileşiğinin sentez şeması……….82
Şekil 5.9. 9 bileşiğinin sentezi………83
Şekil 5.10. 10 bileşiğinin sentezi………84
Şekil 5.11. 11 bileşiğinin sentezi………85
Şekil 5.12. 12 bileşiğinin sentezi………85
Şekil 5.13. Seçilen amino asit metilesterleri HCl tuzları………...86
Şekil 5.14. D-SerOMe ile ligand 8 nin 25 ˚C’ de diklormetandan su fazına ekstraksiyonu için log [D] ve log [L] grafiği………..88
Şekil 5.15. Kaliksarenin kiral diamit türevleri ile amino asite ait amonyum katyonunun muhtemel etkileşimi………89
Şekil 5.16. Seçilen kiral aminler………90
Şekil 5.17. 25°C’ de 5b nolu bileşiğin kloroformdaki çözeltisine (2.5×10-4 mol dm-3) 1.4-7.0×10-2 mol dm-3 (S)-CHEA’ in eklenmesi ile gözlenen spektral değişimler... 90
Şekil 5.18. 6 ve (S)-CHEA’ in CHCl3’da 25°C’de host–guest kompleksleşmesi için tipik Benesi-Hildebrand grafiği... 91
Şekil 5.19. 6 nolu bileşik ve (S)-CHEA’ in CHCl3 içerisindeki host–guest
kompleksleşmesi için ln K’ya karşı 1/T grafiği ... 92
Şekil 5.20. 1H NMR deneylerinde kullanılan guest moleküllerinin kimyasal yapıları.. ... 95
Şekil 5.21. 10 ve 12 reseptörlerinin ve bu reseptörlerin guestlerin eşit molar karışımlarıyla yaptıkları komplekleşmenin kısmi 1H NMR spektrumu(herbiri10 mM) 25 ºC’de CDCl3 içerisinde 400 MHz’de. (A) host 10; (B) ras-FEA ile host 10; (C) ras-FEA; (D) ras-FEA ile host 12; (E) host 12 ... 96
Şekil 5.22. (A) Rasemik 1,2-propandiol bileşiğinin 1H NMR spektrumu (a, 10 mM); (B) S-1,2-propandiol bileşiğinin 1H NMR spektrumu (10 mM); (C) R-1,2-prpopandiol bileşiğinin 1H NMR spektrumu (10 mM); (D) host 10 varlığında ( 10 mM) CDCl3 içerisinde 25 ˚C’ de………98
Şekil 8.1. 6 bileşiğinin 1H NMR spektrumu ... 110
Şekil 8.2. 6 bileşiğinin 13C NMR spektrumu ... 111
Şekil 8.3. 7 bileşiğinin 1H NMR spektrumu ... 112
Şekil 8.4. 7 bileşiğinin 13C NMR spektrumu ... 113
Şekil 8.5. 8 bileşiğinin 1H NMR spektrumu ... 114
Şekil 8.6. 8 bileşiğinin 13C NMR spektrumu ... 115
Şekil 8.7. 10 bileşiğinin 13C NMR spektrumu ... 116
ÇİZELGELER LİSTESİ
Çizelge 1.1. Kaliks[4] arenler, lineer trimerler ve monomerlerinin pKa değerlerinin
karşılaştırılması ... 16
Çizelge 1.2. Kaliks[4]arenlerin dipol momentleri ... 16 Çizelge 1.3. Kaliks[4]arenlerin konformasyonlarına ait 1 H NMR spektrumları... 17
Çizelge 1.4. Ligandlarla metal pikratlarının sıvı –sıvı ekstraksiyon yüzdeleri……..22 Çizelge 1.5. Kaliks[4]aren diester türevlerinin aminoliz reaksiyon……...24 Çizelge 1.6. Ligandlarlaa metal pikratların ekstraksiyonu……….26
Çizelge 1.7. Seçilmiş amino asit metil esterleri ile 1,2,3 ve 4a ‘ün ekstraksiyon yüzdeleri... 28
Çizelge 1.8. 1 ile 2a’ nın 3a ürününü vermek üzere gerçekleşen aldol reaksiyonu...35 Çizelge 1.9. NaOH çözeltisi içersinde çeşitli aktif metilen bileşiklerinin C
alkillemeleri ... 36
Çizelge 2.0. Amino asit metilesterlerinin 16 ve 17 ligandlarıyla ekstraksiyon
yüzdeleri... 42
Çizelge 2.2. Aminoalkollerin 16 ve 17 ligandlarıyla ekstraksiyon yüzdeleri... 43 Çizelge 2.3. CD3CN içersinde TFA veya kaliks[4]aren varlığında ve yokluğunda
amin hidrojenlerinin kimyasal kayma değerleri (δ ppm)………....46
Çizelge 2.4. CH3CN içersinde kaliks[4]aren ve aminlerin titrasyonu sonucunda elde
edilen Kp değerleri ... 46
Çizelge 2.5. CDCl3 içersinde bir equimolar kaliks[6]aren varlığında çeşitli
aminlerdeki protonlar için kimyasal kayma relaksiyon zaman değerleri... 49
Çizelge 2.6. 298 K de ve CH3CN içersinde alifatik aminler ve kaliks[6]aren
monoanyonu arasındaki reaksiyonlar için denge sabiti değerleri ... 49
Çizelge 2.7. Farklı molar oranlarında TFA, kaliks[6]aren, p-tert-butil kaliks[6]aren
ve asitlerin varlığında ve nötral yapıdaki aminlerin 1H NMR kimyasal kayma değerleri………...50
Çizelge 2.8. 6, 10, 11 ve 17 nolu reseptörlerin seçilmiş anyonlara karşı
kompleksleşme sabiti Kc değerleri.
Çizelge 2.9. Kiral aminler ile ( R)-1 ve (S)-1 kaliks crownların reaksiyonu için denge
sabitleri... 55
Çizelge 2.10. Rasemik guestlerin (a-b) host molekül (1-4) varlığında ve yokluğunda
25 ˚C’ de CDCl3 veya CDCl3 + d6-DMSO içerisinde 1H kimyasal kaymaları (ppm)57
Çizelge 2.11. 1 ve 2 nolu bileşiklerin amino asit esterleri ekstraksiyon değerleri…58 Çizelge 2.12. 1 – 3 reseptörleriyle kiral guest bileşiklerinin kloroform içerisinde 25
˚C’de yaptığı kompleksleşmeler için bağlanma sabitleri (K), enantiyoseçicilikler (KR/KS) ve termodinamik parametreler... 60
Çizelge 2.13. 1 – 3 nolu bileşiklerin akiral guest bileşikleriyle kloroform içerisinde
25 ºC’de yaptığı kompleksleşmeler için bağlanma sabitleri (K) ve termodinamik parametreler... 61
Çizelge 2.14. 1 – 4 nolu bileşiklerin D/L-amino asit esterleri guest bileşikleriyle
kloroform içerisinde 25 ºC’de yaptığı kompleksleşmeler için bağlanma sabitleri (K), enantioselektiviteleri (KD/KL) ve termodinamik parametreler... 63
Çizelge 5.1. 7,8,10,11, 12 ile seçilmiş α-amino asit metil esterlerinin ekstraksiyon değerleri………..87
Çizelge 5.2. 5-8 ve 10-12 reseptörleriyle kiral guest bileşiklerinin kloroform
içerisinde 25 ˚C’de yaptığı kompleksleşmeler için bağlanma sabitleri (K), enantiyoseçicilikler (KR/KS) ve termodinamik parametreler………..80
Çizelge 5.3. 25 ºC de CDCl3 içersinde kaliks[4]aren diamidleri 10 ve 12 ile
ras-feniletilaminin komplekleşmesineki kimyasal kayma değerleri... 97
Çizelge 5.4. 25 ºC de CDCl3 içersinde kaliks[4]aren diamidleri 10 ile rasemik
1,2-propandiol bileşiğinin komplekleşmesineki guest’in kimyasal kayma değerleri ... 99
Çizelge 5.5. 25 ºC de CDCl3 içersinde kaliks[4]aren diamidleri 10 ile rasemik
1. GENEL BİLGİLER
Supramoleküler Kimya da birinci ve ikinci kuşak olarak anılan crown eterler ve siklodekstrinlerden sonra üçüncü kuşak olarak tanımlanana kaliksarenler, glukoz birimlerinden oluşan siklodekstrinler ve etilen birimlerinden oluşan crown eterlere benzer olarak fenol ve metilen birimlerinden oluşan metasiklofan sınıfına ait bileşiklerdir (Şekil 1.1.) (Gutsche 1989). Bu bileşiklerin sahip olduğu özelliklerin yanında artı özelliklere de sahip olan kaliksarenler büyük miktarlarda sentezlenebilir ve çok kolay fonksiyonlandırılabilirler. Sabit halka yapıları nedeniyle de metal iyonlarını ve nötral molekülleri seçici olarak taşıma özeliğine sahiptirler. Bu yüzden sentez ve uygulama alanları büyük önem kazanmaktadır (Karaküçük 2006).
O OH O H OH O O OH O H O OH O O OH OH O O H O OH OH O O H O OH O H O H O O OH O H OH n O O O O O O OH HO OH OH R R R R n n
1.1. Kaliksarenler
Kaliksarenler, bilerek veya bilmeyerek 1870 yıllardan beri sentezlenmektedir. Özel bir alan olarak ilgilenilmesi ise 1940 yıllarda olmuştur. Tekararlanabilir sentezi ve kesin yapısının tayini ise ancak 1980’ li yıllarda gerçekleştirilebilmiştir. Supramoleküler ve biomimetik davranışa sahip olan makrosikliklerin bu sınıfı oldukça uzun bir geçmişe sahiptir. İlk sentezi 1872 yılında Alman organik kimyacı Adolph Von Baeyer tarafından gerçekleştirilmiştir (Thurman 1982). Daha sonraları Baekeland 20. yüzyılın başlarında yine fenol türevi olarak katı ve esnek bir reçine elde etmiş ve bu reçineye bakalit adı verilmiştir(Baekeland 1908). 1941 yılında Zinke ve ark. p-t-butilfenol ve formaldehiti NaOH varlığında etkileştirmiş ve sonunda 340 derece erime noktasına sahip, yüksek molekül ağırlıklı ve çözünürlüğü az olan bir ürün elde etmişlerdir (Zinke 1944). 1955 yılında Cornforth tarafından kaliksarenin alkil eterlerinin antituberkular etkileri ile ilgili bir çalışma yayınlanmıştır ama kaliksarenlerin özelliklede kaliks[4]arenlerin sentezi için gerekli optimum şartlar ve yapı tayini Gutsche tarafından belirlenmiştir. Günümüze kadar kaliksarenlerin sentezi ve uygulama alanları ile ilgili yüzlerce yayın, rewiev ve kitap yazılmıştır. Özetle tanımlamak gerekirse; kaliksarenler, fenolik boşluğa sahip metilen köprüleri birbirine bağlı fenol halkalarından oluşan fenol türevli 2,6 metasiklofanlardır (Karaküçük 2006).
1.2. Kaliksarenlerin Adlandırılması
bileşikler olması sebebiyle de Patrick ve Egan (1977), tarafından siklofan bileşiklerine benzerliklerinden dolayı “Metacyclophane” olarak adlandırılmışlardır.
Kaliksarenlerin, IUPAC tarafından da kabul edilen pratik ve kısa adlandırılması ise bu bileşiklerin yapısı tam olarak aydınlatılmış ilk sentezini gerçekleştiren Gutsche (1978) tarafından yapılmıştır. Gutsche bu makrosiklik bileşikleri “Calix Creater” olarak bilinen yunan vazosuna benzettiği için
“Calix[n]arenes” olarak adlandırmıştır. Burada “Calix” kelimesi yunanca da vazo
anlamında olan “chalice” kelimesinden gelmektedir. “Arene” ise aromatik halkayı ifade etmektedir. “n” harfi ise yapıdaki aromatik halka sayısını ifade etmektedir.
IUPAC ‘ a göre kaliksarenlerin sistematik adlandırılması için numara sistemi kullanılmıştır. Şekil. 1.2.’ de görülen, kısa ve pratik adı p-tert butil-kaliks[4]aren olan bileşik “5,11,17,23-tetraalkil-25,26,27,28-tetrahidroksi kaliks[4]aren” olarak adlandırılır. R R R R R R OH OH OH OH O H O H 35 17 11 23 29 1 2 3 4 5 6 7 8 37 38 39 40 41 42 OH OH R R HO OH R R 1 2 3 4 5 6 7 8 11 17 23 25 26 27 28 9 10 12 13 14 15 16 18 19 20 21 22 24
1.3. Kaliksarenlerin Yapısı ve Sentezi
Makrosiklik kaliksarenler p-substitue fenoller ve formaldehitin aşağıda belirtilen prosedürlerden biri ile p-substitue fenoller ve formaldehitin kondensasyonundan elde edilebilmektedir.
1.3.1. Tek Basamaklı Sentez
Makrosiklik kaliksarenlerin yapısı ilk defa 1941 yılında Zinke ve Ziegler tarafından açıklanmıştı. Onlar p-substitue fenoller ve formaldehiti bir baz varlığında ve yüksek sıcaklıkta muamele etmişler ve sonuçta Şekil 1.3 ‘de gösterildiği gibi yüksek erime noktasına sahip siklik tetramerik yapılar elde etmişlerdir.
OH R CH2O -OH CH2 OH R 4 + + H2O
R=metil, siklohekzil, t-butil, fenil, izobutil....vb. Şekil.1.3. Siklik tetramerlerin sentezi
Bununla birlikte elde edilen ürünler karışıktı ve tekrarlanabilir verimler elde edilememişti. Hatta Zinke ve Ziegler (1944) oluşan bu ürünlerin konformasyonel özelliklerini ve enzim mimik özellik gösterebilecek uygun madde olma
p-tert-butil fenolden yola çıkılarak; çözücüler, bazlar, reaktanların oranları ve diğer şartlar değiştirilerek siklik tetramer, hekzamer ve oktamer yapıları yüksek bir verimle Şekil.1.4’ de gösterildiği gibi elde edilmiştir.
OH CH2O CH2 OH 4 OH CH2O CH2 OH 6 OH CH2O CH2 OH 8 + + H2O 4 4 0,045 eq NaOH
difenil eter , refluks 4
+ + H2O 6 6 0,34 eq KOH ksilen , refluks 6 %50 %85 + + H2O 8 8 0,03 eq NaOH ksilen , refluks 8 %65
1.3.2. Çok Basamaklı Sentez
Kaliksarenler para pozisyonlarının hepsinde aynı substituentlerin kullanılmasıyla tek basamaklı olarak sentezlendiği gibi farklı substituentler kullanılarak da çok basamaklı olarak sentezlenebilmektedir. Birbiriyle yaklaşık olmayan sentez tipinde başlangıç maddesi olarak o-bromo-p-alkil fenol kullanılarak gerçekleştirilen kondensasyon basamakları sonucunda hidroksi metil grupları bağlı lineer oligomer yapılar elde edilir. Bu lineer ürünün dehalojenasyonundan sonra çok seyreltik şartlar altında halkalaşma gerçekleşir (Şekil.1.5).
OH R 1 Br2 OH R 1 Br CH2O OH R 1 Br OH OH R 2 OH R 1 Br OH R 2 OH OH R 1 Br OH R 2_3 OH OH R 4 CH2 OH R 1_4 4 OH
-basamağından daha önce gelir. Böhmer ve ark.(eyıl) para pozisyonlarında farklı substituentler bulunan kaliksarenleri sentezlemek için çoğunlukla TiCl4/dioxane
şartlarında [3+1], [2+2] ve [2X1+2X1] kondenzasyonlarını etkili bir şekilde kullanmışlardır. OH R 1 OH O H OH R 1 R 3 R 2 OH R 4 Br Br TiCl4 ,dioxane reflux OH OH HO OH R 1 R 3 R 2 R 4 R1 (R3) R2 R4 tert-Bu tert-Bu CH3 CH3 CH3 CH3 tert-Bu tert-Bu Br tert-Bu Br NO2 CH3 Cl tert-Bu Br CH3 CH3
Şekil. 1.6. [3+1] kondenzasyonuyla sentez
OH OH HO OH R 1 R 3 R 2 R 4 OH R 2 OH R 1 OH R 3 OH R 4 Br Br TiCl4 ,dioxane reflux
1.3.3. Asit Katalizörlü Kaliksaren Sentezi
p-alkilfenol ile formaldehitin reaksiyonunun asidik şartlar altında
gerçekleştirilmesi halinde çok yüksek verimlerle lineer oligomerler oluşmasına rağmen, çok düşük verimlerle halkalı oligomer elde edilmiştir (Ludwig 1986). Bununla birlikte p-t-bütilfenol ile s-triokzan, kloroformda p-toluen sülfonik asit varlığında oldukça yüksek verimli kaliksarenler sentezlenebilmektedir (Gutsche 1990). Bazik ortamdaki reaksiyon şartların tersine, asit katalizörlü ortamda saf bir halkalı oligomer yüksek verimlerle elde edilememiştir. Bunun yerine halkalı tetramer ve daha çok aromatik halkaya sahip (7, n > 8) kaliksarenler, bazik ortamda daha büyük verimler ile elde edilebilmektedir.
1.4. Kaliksarenlerin Konformasyonları
Serbest fenolik hidroksil grupları içeren kaliksarenlerin hepsi oda sıcaklığında çözelti içersinde konformasyonel olarak hareketlidir. İlk defa Cornforth ve ark. (1955) kaliksarenlerin konformasyonel izomeriye sahip olduğunu fark etmişlerdir. Gutsche bu izomerleri, koni, kısmi koni, 1,2 karşılıklı ve 1,3 karşılıklı olarak tasnif etmiştir (Şekil 1.8.).
OH O H OH OH Koni OH OH OH OH Kısmi Koni 1,3-Karşılıklı OH OH OH OH OH HO OH OH 1,2-Karşılıklı Şekil.1.8. Kaliks[4]arenlerin konformasyonel izomerleri
Birbirlerine en uygun uzaklıkta bulunan serbest hidroksil gruplarına sahip kaliksarenlerin kristal yapılarının hepsi katı durumdayken koni konformasyonuna sahiptir. Burada hidroksil grupları arasındaki molekül içi hidrojen bağlarından dolayı yapı bu konformasyonda kararlı haldedir.
Kaliksarenler 1H-NMR spektroskopisinden çok rahat görüleceği üzere çözelti içersinde koni konformasyonu dışında da bulunabilir. p-tert-butil kaliks[4]arenler koni konformasyonu için 1H-NMR spektroskopisinde Ar-H, -OH ve C(CH
3)3
protonları singlet verirken köprüdeki metilen gruplarının her bir hidrojeni için ise bir çift dublet verir. Zaten kaliksaren konformasyonlarının yapıları da özellikle bu metilen köprülerindeki sinyallere bakılarak tespit edilir.
Konformasyonlar; sentezde kullanılan çözücü, bazdaki metalin atom çapı ve reaksiyon sıcaklığına bağlı olarak farklılıklar gösterebilir. Eğer sentezde çözücü olarak kaliksaren türevleri ile kompleks oluşturan aprotik çözücüler (toluen, brombenzen, karbontetraklorür….vs.) kullanılırsa konformasyon dönüşüm hızının azaldığı görülmüştür. Aprotik çözücülerin tersine aseton, asetonitril, piridin gibi protik çözücüler kullanıldığında ise bu tip çözücülerin molekül içi hidrojen bağını zayıflatmalarından dolayı konformasyon dönüşüm hızı artar. Kaliksarenlerin
sentezinde kullanılan bazın metalinin atom çapıda konformasyonda etkilidir. Eğer sentezde atom çapı küçük (NaH, Na2CO3,….vs.) bir metale sahip baz kullanılırsa
koni konformasyonu, atom çapı daha büyük bir baz (Cs2CO3 gibi) kullanılırsa 1,3
karşılıklı konformasyonun da kaliksarenler elde edildiği görülmüştür (Iwamoto 1990). Kaliksarenlerin konformasyonları sıcaklığa bağlı olarak da değişiklik göstermektedir. Örneğin; p-t-butilkaliks[4]arenin koni konformasyonunda 10 derecede metilen protonları bir çift dublet verirken 60 derecede çok keskin bir singlet verir (Gutsche 1985). Kaliksarenler fonksiyonlandırılırken yapıya bağlanan moleküllerde konformasyonu etkiler. Eğer yapıya p-pozisyonu veya fenolik -OH kısmından hacimli gruplar bağlanırsa konformasyon dönüşüm hızı en aza indirilmiş olur (Arnaud-Neu,1992). Yine yapının her bir aril halkasına molekül içi köprüler kurulmasını sağlayacak crown eter grupları bağlayarak konformasyon dönüşüm hızı en aza indirilebilir (Takeshita 1995).
1.5. Fonksiyonlandırılmış Kaliksarenlerin Sentezi
Kaliksarenler fenol hidroksi gruplarının bulunduğu fenolik -OH veya diğer adıyla narrow rim kısmından ve aril halkasına göre para pozisyonundaki t-butil gruplarının bulunduğu p-pozisyonu veya diğer adıyla wide rim kısmından fonksiyonlandırılabilirler.
OH OH OH HO OH O H HO OH 4 Geniş kısım, p- pozisyonu Dar kısım, fenolik -OH bölgesi
Şekil 1.9. Kaliks[4]arenin p-konumunun ve fenolik OH’larının şematik gösterimi
Fenolik –OH kısmından fonksiyonlandırma, eter, ester, keto, fosfin ve metal boşluklarını içine almaktadır. Reaksiyon şartları ve reaksiyona giren maddeler değiştirilerek seçici lower rim fonksiyonlandırılması gerçekleştirilebilir. α – halokarbonil bileşikleriyle gerçekleştirilen türevlendirme özel bir öneme sahiptir çünkü bu fonksiyonlandırma sonucu elde edilen ester, amid, asit ve keton türevleri iyonofor olarak kullanılabilirler. Yine OH gruplarının H (Shinkai 1994), SH (Gutsche 1995), Br (Biali 1996), Cl (Biali 1996), NH2 (Shinkai 1992, Biali 1995),
CH3 (Biali1997) gibi gruplarla yer değiştirmesiyle değişik türevler elde edilebilir.
Fenil halkasındaki para pozisyonunda bulunan t-butil gruplarının uzaklaştırılmasıyla kaliksarenlerin para pozisyonundan türevlendirilmeleri çok çeşitli ve kolay olarak yapılabilmektedir. Bu tür türevlendirmeye örnek olarak en çok bromlama(Gutsche 1985, Atwood 1990), iyotlama(Ungaro 1990), nitrolama(Reinhoudt 1992), sülfolama(Gutsche 1985, Manabe 1986), klorsülfolama(Reinhoudt 1993), klor metilleme(Ungaro 1989, Shinkai 1993), açilleme(Gutsche 1986), diazonyum tuzları bağlama(Manabe 1989) ve formilasyon(Ungaro 1991) içeren elektrofilik substitusyon reaksiyonları verilebilir Gutsche ve Nam(1988) tarafından yayınlanan sekonder bir aminle aminometillemeyi içeren p- kinon metit yolu ise çok kullanışlı bir metotdur (Şekil 1.10.). Bu yöntem sonucunda elde edilen p-tert-
tetrakis(siyanometil)kaliksaren çok iyi bir başlangıç maddesidir. Örneğin siyano grupları amino gruplarına(Gutsche 1988) indirgenebilir veya hidrolizle karboksil gruplarına(Gutsche, yayınlanmamış çalışma) çevrilebilir. Kaliksarenin allil eterlerinin düzenlenmesiyle elde edilen p -Claisen metodu özellikle büyük hacimli kaliksarenlerin sentezi için çok uygundur(Gutsche 1985). Mesela 1,3-bis(trimetilsillil)üre kullanılarak bu metotla çok büyük hacimli bis kaliksarenler elde edilebilir(Gutsche, yayınlanmamış çalışma). Bu metot özellikle bis kaliksaren sentezi için kolaylık sağlamasına rağmen henüz daha tam olarak araştırılmamıştır.
OH 4 HCHO (CH3)2NH OH 4 NMe2 CH3I O 4 CH3NMe3 H O 4 CH2 OH 4 CN BH3 OH 4 NH2 CN -CN
OH Bu 4 4 OH H 4 OH R 4 OH R 4 OH R 4 OH R Bu 4 OR Bu 4 OR R=SO3H R=NO2 R=Br R=CH2CH2NH2 R=CHO R=CH2CH2CN R=CH=NOH R=CH2CH2OH R=CH2CH2N3 R=CH2COH R=CH2CN R=CH2OCH3 R=CH3 R=CH2N3 R=CH3 R=CH2CH3 R=C6H5 R=CH3 R=CH2COR R=CH2COONH2 R=CH2COOR R=CH2C6H5 R=COCH3 R=COC6H5 p-Kinonmetit metodu t t t Fenolik -OH p-pozisyonu Elektrofilik Substitusyon p-Claisen Çevrilmesi p-Klormetilasyon Metodu Dealkilasyon
Williamson Eter Sentezi Esterleşme
Şema 1.11. p-t-butilkaliks[4arenin fenolik –OH ve para pozisyonları üzerinden
1.6. Kaliksarenlerin Fiziksel ve Kimyasal Özellikleri
1.6.1. Erime Noktaları
Kaliksarenler yüksek erime noktasına sahiptir. Hemen hemen hepsinin erime noktası 300˚C’nin üzerindedir(Gutsche 1981). Bununla birlikte kaliksarenler türevlendirilerek erime noktaları düşürülebilir veya yükseltilebilir. Örneğin kaliksarenlerin ester veya eter türevlerinin erime noktaları genellikle 220 ˚C civarındadır(Böhmer 1987).
1.6.2. Çözünürlükleri
Kaliksarenlerin bilinen bütün formları birçok organik çözücüde az çok çözünmektedir. Fakat genellikle suda çözünmezler(Gutsche 1989). Bu özelliğide saflaştırma, izolasyon ve karakterizasyonda zorluklara neden olmaktadır. Bununla birlikte kaliksarenlerin hemen hemen hepsi çözeltilerinde spektroskopik ölçümlere müsaade edecek kadar kloroform, diklormetan, DMSO, DMF ve piridin gibi çözücülerde çözünürler.
1.6.3. HPLC de ayrılmaları
Şekil.1.12’de bir örneğinin görüldüğü gibi özellikle reverse phase HPLC tekniği kaliksarenlerin ayrılması için kullanılabilecek çok kullanışlı bir tekniktir. Lower riminde fosforil grupları taşıyan kaliksarenler bu teknikle ayrılabilir(Kalchenko,1997). Kiral kaliksarenler ise kiral kolonlar kullanılarak
Şekil.1.12. p-tert-butil kaliks[n]aren karışımının HPLC’ de yürütülmesi( piklerin
üzerindeki rakamlar n sayısını ifade etmektedir.)
1.6.4. Kaliksarenlerin pKa değerleri
Kaliksarenler monomerik fenol birimlerinden daha güçlü asidiktirler. Reinhoudt ve Shinkai ile çalışma arkadaşları hem potansiyometrik hemde spektrofotometrik metotları kullanarak SO2N(CH2CH2OH) veya NO2 grupları taşıyan
kaliks[4]arenlerin pK değerlerini ölçmüşlerdir. Bu kaliks[4]arenlerin monomer ve trimer yapılarıyla pKa değerlerinin karşılaştırılmış hali Çizelge 1.1. de verilmiştir.
Çizelge 1.1. Kaliks[4] arenler, lineer trimerler ve monomerlerinin pKa değerlerinin karşılaştırılması. Bileşik pK1 pK2 pK3 pK4 4 SO2N(CH2CH2OH)2 0.8±0.3 9.7±0.1 Yak. 12.5 >14 Lineer trimer 4.71±0.05 8.27±0.05 11.61±0.1 Monomer 8.25±0.03 4NO2 2.9±0.3 10.9±0.1 12.3±0.2 >14
Lineer trimer 3.6±0.1 10.6±0.1 Yak. 12.5
Monomer 8.67±0.03
1.6.5. Kaliksarenlerin Dipol Momentleri
Bu konuda yapılan en önemli çalışmada Çizelge.1.2. de görüldüğü gibi upper rim ve lower riminde farklı gruplar bağlı dokuz tane kaliks[4]aren türevinin dipol moment değerleri verilmiştir. Bu çalışmadan da anlaşılacağı gibi belirtilen şartlar dahilinde dipol moment koni > kısmi koni > 1,2 karşılıklı > 1,3 karşılıklı şeklinde sıralanmaktadır(Mendoza,1993).
Çizelge.1.2. Kaliks[4]arenlerin dipol momentleri
Fenolik -OH p- pozisyonu Konformasyon Dipol moment, D
OH t-Bu Koni 4.19
OPr NO2 Koni 13.8
OPr NO2 Kısmi koni 6.7
OPr NO2 1,3 karşılıklı 0.0
1.6.6. Kaliksarenlerin IR Spektrumları
Kaliksarenlerin IR spektrumları incelendiğinde parmak izi bölgeleri(900-1500 cm-1) aynıdır. Ayrıca fenolik –OH gruplarına ait titreşim pikleri 3150-3300 cm
-1 de görülür. Bu spektrumlar molekül içi hidrojen bağlarından dolayı yayvandır.
1.6.7. 1H-NMR Spektrumları
Kaliksarenlerin yapı tayininde ve konformasyonlarının belirlenmesinde en çok kullanılan metot 1H-NMR spektroskopisidir. Fenolik –OH gruplarına ait hidrojenlerin piki 10 ppm civarında olması gerekirken molekül içi hidrojen bağlarının perdeleme etkisinden dolayı yukarı alana kaymıştır ve bir singlet verir. Para pozisyonundaki tersiyer bütil gruplarına ait hidrojenler yüksek sıcaklıklarda singlet verirken düşük sıcaklıklarda bir çift dublet verir. Aril halkaları arasındaki metilen köprüsü hidrojenlerinin pikleri ise konformasyona göre değişir ve 3.0-4.5 arasındadır(Çizelge 1.3.).
Çizelge 1.3. Kaliks[4]arenlerin konformasyonlarına ait 1 H NMR spektrumları
Konformasyon ArCH2Ar protonlarına ait sinyaller Koni Bir çift dublet
Kısmi koni İki çift dublet (1:1) veya bir çift dublet ve bir singlet (1:1) 1,2 karşılıklı Bir singlet ve iki dublet (1:1)
1,3 karşılıklı Bir singlet
Şekil.1.13. p-t-butil kaliks[4]arenin CDCl3’deki 1H-NMR spektrumu
Katı fazdaki kaliksarenlerin konformasyonları X-ray kristalografisinden yararlanılarak bulunabilir. Kaliksarenlerin türevlerinin molekül kütlesini belirlemek için kullanılan FAB MS tekniğinden de kaliksarenlerinin yapısının belirlenebilmesi için faydalanılabilinir.
1.7. Kaliksarenlerin Kullanım Alanları
1.7.1. Kaliksarenlerin Enzim Mimik Olarak Kullanılması
Kaliksarenler enzim mimik özellik gösterebilecek şekilde uygun gruplarla fonksiyonlandırılırsa enzimin aktif bölgesini oluşturarak substratların katalitik olarak ürünlere dönüşmesini sağlayabilir.
Dospil ve ark. (2001), kaliks[4]arenin upper rimi üzerine farkı pozisyonlarda imidazol grupları bağlamışlar ve tampon çözeltisi içersinde p-nitrofenil ester
bileşiğinden p-nitrofenolü elde etmek için açil transferaz enzimine benzer şekilde katalizör olarak kullanmışlardır.
N N OR OR O H OR N N N N OR OR O H OH N N N N OR OR O H OR 12 (R = H; 70%) 13 (R = Bz; 72%) 14 (R = H; 90%) 15 (R = Bz; 85%) 16 (R = H; 70%) 17 (R = Bz; 81%)
Şekil 1.14. Açiltransferaz aktivite gösteren kaliks[4]aren türevleri.
O O2N R O OH O2N MeOH/H2O yada MeOH/MeCN Katalizör R = Ph, PNB R = Me, PNA
Şekil 1.15. 12-17 bileşiklerinin katalize ettiği p-nitrofenil benzoat (PNB) ve asetat
Reinaud ve ark. (2002), kaliks[6]aren türevlerini sentezlemişler ve bunların bakır komplekslerini oluşturmuşlardır. Oluşturdukları bu yapı metalloenzimlerde aktif merkeze substrat kanal girişi için güzel bir model örneğidir. (Şekil.1.16)
Şekil.1.16. Metalloenzimler için etkili kaliks[6]aren yapısı.
1.7.2. Kaliksarenlerin Molekül veya İyon Taşıyıcı Olarak Kullanılması
Kaliksarenler farklı konformasyonları ve yapılarında bulunan halka boşluğu sayesinde iyonları ve küçük nötral molekülleri tersinir olarak tutabilirler. (Şekil.1.17.) Bu kompleksler endo- ve ekzo- kompleksler şeklindedir.
R R R R
OH
OH OH
HO
Nötral Guest (Konuk)
İyonik Guest (Konuk)
veya
Endo- Kompleks
Ekzo- Kompleks Host (Ev sahibi)
+
R R R R OH OH HO OH R R R R OH OH HO OHŞekil 1.17. p-alkilkaliks[4]aren’ in kompleks oluşturma mekanizması
Bu komplekslere örnek p-t-butilkaliks[4]arenin benzen, ksilen, toluen ve anisol gibi çözücülerle verdiği tersinir moleküler kompleksler verilebilir. Kaliksarenlerin organik moleküllerle verdiği komplekslerin 250°C’ nin üzerinde bile uzaklaştırılamaması çok sağlam kompleksler verdiğini göstermektedir. Kaliksarenler fenolik -OH gruplarındaki hidrojenlerin güçlü bazların etkisiyle iyonlaşabilmesi zayıf asidik karakterde olduğunu gösterir. Bundan dolayı aminlere proton vererek kompleks yapabilirler (Gutsche, 1987).
Kaliksarenler hem polar hem de apolar bölgeler içerirler. Kaliksarenlerin polar bölgesi alkoller, esterler, eterler ve amid gruplarının oksijenleri arasına metal iyonlarını bağlayabilen bir boşluktan oluşur. Metal iyonlarıyla kaliksarenlerin kompleksleşmesiyle ilgili ilk çalışma Izatt ve ark.(1983) tarafından gerçekleştirilen alkali metal iyonlarının özelliklede Cs+ iyonunun kaliksarenleri kullanarak sulu fazdan organik faza taşınmasını inceledikleri çalışmadır.
Sırıt ve ark (2005), koni konformasyonunda yeni bir kiral kaliks[4](azoksa)crown-7 türevini sentezlemişler ve alkali, toprak alkali ve geçiş metallerinin sıvı-sıvı ekstraksiyonu çalışmalarında kullanmışlardır (Şekil 1.18.)
OH OH O O O O OMe OMe OH OH O O O O N N O O O Ph Ph H H 5 6
Şekil 1.18. Kiral kaliks[4](azoksa)crown-7 bileşiğinin sentezi
Ekstraksiyon sonuçlarına bakıldığında diğer alkali metaller arasından Li+
metal katyonunun sulu fazdan organik faza çok yüksek miktrada taşındığı ve geçiş metalleri için bu kaliksaren türevinin iyi ekstraksiyon yeteneğine sahip olduğu tespit edilmiştir (Çizelge 1.4.).
Çizelge 1.4. Ligandlarla metal pikratlarının sıvı –sıvı ekstraksiyon yüzdeleri
Ekstrakte edilen metal pikrat yüzdesi (%)
Ligand Li+ Na+ K+ Cs+ Co2+ Cu2+ Cd2+ Ni2+ Pb2+ Hg2+ 5 <1.0 <1.0 <1.0 <1.0 <1.0 <1.0 <1.0 3.7 22.3 29.2
6 22.9 1.0 8.7 <1.0 42.2 61.5 47.3 26.3 82.3 83.3
H H O OH OH O O O O N N O O Ph Ph M nPic n+ OH OH O O O O N N O O O Ph Ph H H Li Pic +
Şekil 1.19. Kiral kaliks[4](azoksa)crown-7 türevinin Li+ ve geçiş metali katyonlarıyla yaptığı kompleksleşmenin mekanizması
6 nolu bileşiğin Li+ katyonunu büyük oranda sulu fazdan organik faza taşımasının nedenini muhtemelen kaliksaren boşluğunun bu katyonun geometrik yapısına uygun olması şeklinde açıklamışlardır. Kaliksarene bağlı bulunan crown yapısındaki üç tane oksijen atomunun elektrostatik olarak Li+ katyonuyla etkileşmesi sonucu küçük iyon çapına sahip olan katyon bu boşluğa girerek yapının sabit kalmasını sağlar. Daha büyük atom çapına sahip geçiş metallerinde ise etkileşim yapıda bulunan beş oksijen ve iki azot atomuyla olmaktadır (Şekil 1.19.).
Kaliksarenlerin anyonlarla yapılan kompleksleşme çalışmaları katyonlarla yapılan kompleksleşme çalışmalarına göre daha azdır. Anyonlarla yapılan çalışmalarda genellikle reseptör olarak kaliksarenlerin amid türevleri kullanılmıştır(Beer, 1995). Kaliksarenlerin kompleks yapma gücünü anyonun büyüklüğü ve hidrojen bağlama etkiler. Ayrıca kullanılan anyonların lewis bazları olması da kaliksarenlerin kompleks yapmasını kolaylaştırır.
Sırıt ve ark.(2006), yaptıkları bir çalışmada kaliks[4]arenin diamid türevlerini sentezlemişler ve bu bileşiklerin dikromat anyonu ile farklı pH’ larda yapılan ekstraksiyonunda düşük pH’ larda bileşiklerin dikromat anyonunu ekstrakte ederken yüksek pH’ larda bu etkinin azaldığı görülmüştür.
Şekil 1.20. Kaliks[4]aren diamid türevlerinin kromat anyonuyla yaptığı muhtemel
etkileşme.
Sırıt ve ark. (2007), yaptıkları başka bir çalışmada p-tert-butil kaliks[4]aren ve kaliks[4] aren diester türevlerini çeşitli primer aminlerle reaksiyona sokarak kaliksarenin mono ve diamid türevlerini sentezlemişler. Çalışmada türevlerin sentezine sterik engel ve reaksiyon süresinin etkisini ince tabaka kromatografisi ve HPLC tekniklerini kullanarak incelemişlerdir. Ayrıca alkali metallerle ekstraksiyonunu gerçekleştirmişler ve özellikle yayına göre 8 nolu amid türevinin Sr+2 ile Cs+ iyonlarına karşı seçici davrandığı gözlenmiştir.
Çizelge 1.5. Kaliks[4]aren diester türevlerinin aminoliz reaksiyonu
Ürün Başlangıç
Materyali Süre(Saat) Monoamit Verim(%) Diamit Verim(%)
1 72 3 61 10 22 1 72 4 55 11 23 1 192 3 19 10 74 1 192 4 12 11 73 1 72 - - 12 72 1 72 - - 13 74 2 72 - - 6 79
Çizelge 1.6. Ligandlarlaa metal pikratların ekstraksiyonu
Ekstrakte edilen Pikrat Tuzu
Bileşik Li+ Na+ K+ Cs+ Mg2+ Ca2+ Sr2+ Ba2+ 3 1.93 <0.1 1.2 <0.1 5.92 1.67 2.1 2.34 4 1.12 <0.1 0.9 1.21 7.04 1.88 <0.1 3.71 5 <0.1 <0.1 <0.1 <0.1 3.94 2.54 <0.1 4.3 6 9.2 0.4 6.5 4.0 6.0 5.9 8.1 14.3 7 <0.1 <0.1 <0.1 <0.1 <0.1 <0.1 <0.1 <0.1 8 40.0 41.1 43.4 76.9 25.8 23.3 73.7 32.9 9 95.6 93.8 95.3 94.2 88.4 90.7 91.9 91.4 10 4.05 <0.1 <0.1 0.3 5.63 1.67 <0.1 3.13 11 <0.1 <0.1 <0.1 <0.1 <0.1 <0.1 <0.1 <0.1 12 38.4 41.7 44.2 68.8 40.3 24.9 45.3 32.0 13 98.0 95.4 96.4 97.1 93.4 95.7 95.3 94.3
a Sulu faz, [metal nitrat]= 2.5 X 10-5 M; organik faz, diklormetan, [ligand]= 1 X 10-3
1.7.3. Kaliksarenlerin Enantiyomerlerin Tanınmasında Kullanılması
Kirallik moleküllerin davranışını ve aktivitesini belirler. Doğadaki biyolojik moleküller enantiomerlerin sadece birinden meydana gelmiştir. Örneğin bütün aminoasitler L-formundadır. Bu yüzden özellikle ilaçlarda kullanılan maddelerden bir tanesinin bir enantiomeri iyileştirici özellik gösterirken diğer enantiomeri vücuda zarar verebilir. Bu nedenle özellikle aminler,amino alkoller ve amino asitler gibi kiral bileşiklerin enantiomerik tanınması oldukça önemlidir.
Kiral kaliksaren türevlerini kullanılarak bugüne kadar kiral tanınma, enantiomerik ayırma ve enantiomerik tanınma ilgili pek çok çalışma yapılmıştır. He ve ark. (2002), (L)-valinden türetilen kiral kaliks[4](aza)crownları sentezlemişler ve bu bileşikleri 1H NMR ve 13C NMR yardımıyla tartarik asit dibenzoat ve amigladik asit gibi bazı asitlerin kiral tanınmasında kullanmışlardır (Şekil 1.19.).
Yılmaz ve ark. 2006 yılında yaptıkları bir çalışmada yeni kiral kaliks[4]aren triamid türevlerini sentezlemişler ve bu türevlerin sıvı-sıvı ekstraksiyon metoduyla seçilmiş amino asit metil esterlerine karşı ekstraksiyon özelliklerini incelemişlerdir.
Şekil 1.22. Çalışmanın genel sentez şeması.
Çizelge 1.7. Seçilmiş amino asit metil esterleri ile 1,2,3 ve 4a ‘ün ekstraksiyon yüzdeleri.
Ligand D-AlaOMe L-AlaOMe D-PheOMe L-PheOMe D-TrpOMe L-TrpOMe
1b <0.1 <0.1 <0.1 <0.1 <0.1 <0.1
2 <0.1 <0.1 <0.1 <0.1 <0.1 <0.1
3 54.1 56.5 71.3 68.5 68.4 69.7
4 59.5 57.4 65.8 67.5 62.6 68.3
a Sulu faz, {amonyum pikrat] = 2 X 10-5 M; organik faz, diklormetan, [ligand]= 1 X 10-3 M;
25 °C; 1 saat.
b Organik faz olarak kloroform kullanıldı.
Yapılan çalışmada 1 ve 2 nolu reseptörlerin seçilen aminoasit metil esterleri için iyi bir ekstraktant özelliği göstermediği görülmüştür. Fakat 3 ve 4 nolu reseptörlerin iyi seçicilik özelliği göstermesede iyi bir ekstraktant olduğu gözlenmiştir.
Zhang ve ark. (2004) gerçekleştirdikleri bir çalışmada p-tert-butil kaliks[4]arenin lower rim kısmına optikçe saf α,β amino alkolleri bağlayarak rasemik mandelik asit, 2,3 dibenzoil tartarik asit ve 2-hidroksi 3-metil bütirik asit için kiral tanıma çalışmalarını yapmışlardır. Ayrıca NMR spektroskopisi ile de kararlılık sabitlerini hesaplamışlardır.
Şekil 1.24. Çalışmanın genel sentez çalışması ve kiral tanımada kullanılan
karboksilik asitler.
Şekil 1.25. (a) 2a’nın 1H NMR spekrumu(5 mM) (b) 2a (5 mM) ve 3a (20 mM) arasındaki kompleksin spektrumu (c) 2a (5 mM) ve 3a (92 mM) arasındaki
kompleksin spektrumu (d) 2b (5 mM)’nin spektrumu (e) 3b (5 mM)’nin spektrumu
1.7.4. Kaliksarenlerin Kromatografide Kullanılması
Schurig ve ark. (1999) yaptıkları çalışmada Şekil 1.25. de gösterildiği gibi kirasil kaliks türevini sentezlemişler ve bu bileşiği GC’ de kiral durgun faz olarak kullanarak alanin, valin, lösin vb. gibi amino asitlerin N-(triflorasetil) metilesterlerini enantiyomerlerine ayırmışlardır (Şekil 1.26.).
Şekil 1.27. Çalışmanın genel sentez şeması
Jira ve ark. 2002 yılında durgun faza bağlı kaliksaren ve resorsinaren türevlerini HPLC’ de kolon dolgu maddesi olarak kullanmışlar ve thioxanthene, dibenz[b,e]oxepin’ in cis ve trans izomerlerini ayırma çalışmalarını gerçekleştirmişlerdir.
Şekil 1.28. Çalışmada kullanılan kaliksaren ve resorsinaren durgun fazları. N N S OH CF3 N N S OH Cl N S CF3 O N
flupentiksol klopentiksol kloropprotiksen doksepin
Şekil 1.29. İncelenen analitlerin yapıları.
Liu ve ark. 2004 yılında yaptıkları çalışmada p-tert-butil kaliks[6]-1,4-benzocrown-4 bağlı durgun fazının sentezi ve karakterizasyonunu gerçekleştirmişler ve bu polimer yapıyı sıvı kromatografide aromatik bileşiklerin ayrılması için kullanmışlardır.
OH OH ClCH2CH2OH NaOH OCH2CH2OH OCH2CH2OH SO2Cl C H3 OCH2CH2OTs OCH2CH2OTs 6 K2CO3, Toluene O O O O 6 O Si OH O C H2 O (CH2)3 Si OMe OMe
OMe toluen, trietilamin refluks, N2 O Si O Si (CH2)3 O CH2 O toluen, NaH katalizör, refluks O Si O Si (CH2)3 O CH2 CH OH CH2 O 6 O O 1 (OH)6 1 (OH)4 2 + + 2 (OH)3
p-tert-butil-kaliks[6]-1,4-benzocrown-4-bağlı silikajel durgun fazı 3-glisidoksipropil bağlı faz
Şekil 1.30. p-tert-butil kaliks[6]-1,4-benzocrown-4 bağlı durgun fazın sentez şeması.
Zuo ve ark. (2004), aminosilanla türevlendirilmiş p-tert-butil kaliks[4]aren türevini hazırlayıp aktive edilmiş silika jelle etkileştirilerek p-tert-butil kaliks[4]aren türevinin durgun fazını ede etmişlerdir. Sıvı kromatografide bu durgun faz polar ve apolar ve aromatik bileşikler, temel aromatik bileşikler ve bazı izomerlerin ayrılması için kullanılmıştır. Özellikle alkil benzenlerin ayrılmasında Kromasil-C18-SiO2 kolon
1.7.5. Kaliksarenlerin Katalizör Olarak Kullanılması
Kim ve ark. (2004), yeni bir krom (III)/p-tert-butil kaliks[4]aren/ alkil amonyum katalizör sistemi hazırlamışlar ve bu sistemi etilenin polimerizasyonunda kullanmışlardır. Yaptıkları çalışmalar sonucunda bu sistemin etilenin polimerizasyonu için çok aktif ve uygun olduğu bulunmuştur.
Şekil 1.31. Krom (III)/p-tert-butil kaliks[4]aren bileşiği için muhtemel monomerik
(a) ve dimerik (b) yapılarının şematik gösterimi.
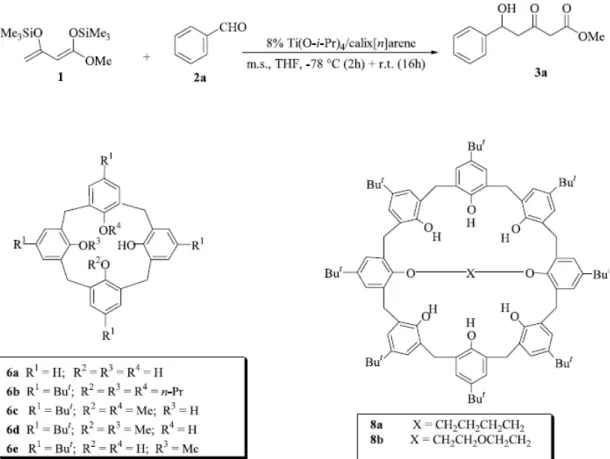
Neri ve ark. 2003 yılında yaptıkları çalışmada benzaldehitle Chan’in dieninin aldol kondensasyonu reaksiyonu sadece %8 mol kaliks[n]aren/Ti(O-i-Pr) içeren
Şekil 1.32. Çalışmada gerçekleştirilen aldol reaksiyonu ve katalizör olarak kullanılan
kaliksaren türevleri.
Çizelge 1.8. 1 ile 2a’ nın 3a ürününü vermek üzere gerçekleşen aldol reaksiyonu
Giriş Kaliks[n]aren Verim (%)a
1 6 77 2 7 96 3 8 56 4 Ti(O-i-Pr)4 4 5 6a 95 6 6b 10 7 6c 17 8 6d - 9 6e 69 10 8a 44 11 8b 58b
a Verimler 1H NMR analizinden elde edildi. b Çözücü olarak toluen kullanıldı.
Aktif metilen bileşikleri, alkoller ve fenollerin alkil halojenürlerle NaOH çözeltisi içersindeki alkilleme reaksiyonları hiçbir çözücü ilavesine ihtiyaç duymaksızın gerçekleşebilir. Hirai ve ark. (2000) upper riminde trimetilamonyometil grupları ihtiva eden suda çözünen kaliks[n]aren türevlerini faz transfer katalizörü olarak kullanmışlar ve iyi verimlerde alkilleme ürünleri elde etmişlerdir.
Çizelge 1.9. NaOH çözeltisi içersinde çeşitli aktif metilen bileşiklerinin C
alkillemeleri R 1 R 2 Br R 1 R 2 R R 1 R 2 R R R OH + TACnM + + 4 N NaOH 3 mL 4.0 mmol 3 4 2 R = 1-C10H7CH2 Saflaştırılmış verim (%)
Giriş R1-CH2-R2 (mmol) Katalizör
(% mol) Şartlar 3 4 2
1[a]
CH3COCH2COCH3 (12.0) Yok 60°C,0.5s 11 (+az miktar) [b] 0 0
2[a]
CH3COCH2COCH3 (12.0) TAC6M
(1.0) 60°C,0.5s 50 (+2)
[b] Az miktar 0
3[a]
CH3COCH2COCH3 (12.0) TAC6M
(1.0) 60°C, 2 s 88 (+3b) [b] 3 0 4[a] C6H5COCH2CN (12.0) TAC6M (1.0) 60°C, 2 s 82 12 miktarAz [c] 5[a] C6H5COCH2CN (4.8) TAC6M (1.0) 60°C, 2 s 69 22 Az miktar [c] 6 C6H5CH2CN (12.0) TAC4M (1.0) 70°C, 10 s 90 8 0 7 C6H5CH2CN (4.8) TAC4M (1.0) 70°C,10 s 68 19 13 8 2-ClC6H4CH2CN (4.8) TAC4M (1.0) 60°C,10 s 84 0 0 9 C6H4-1,2-(-CH=CH-CH2-) (4.8) TAC(1.0) 4M 70°C,10 s 74 [d] Az miktar[e] 4 (+6)[c] 10[f] 1-C 10H7CH2CN (4.8) Yok 70°C, 2 s 21 0 0 11[f] 1-C 10H7CH2CN (4.8) TAC4M (1.5) 70°C, 2 s 58 0 Az miktar 12[f] 1-C 10H7CH2CN (4.8) TAC6M (1.0) 70°C, 2 s 66 0 Az miktar 13[f] 1-C 10H7CH2CN (4.8) TAC8M (0.75) 70°C, 2 s 78 0 Az miktar 14[f] 1-C 10H7CH2CN (4.8) TAC6M (1.0) 70°C, 5 s 91 0 Az miktar
1.7.6. Kaliksarenlerin Nanoteknolojide Kullanılması
Son yıllarda yapılan bir çalışmada silika yüzeyine kaliks[4]arenin tek adımda immobilizasyonu gerçekleştirmiş olup, silikanın aktifleştirilmiş yüzeyine silikon grupları bağlanarak yüzeyde bulunan tetrahedral silikon atomları ve kaliksarenlerin fenolik oksijen grupları ile kararlı bir yapı teşekkül edilmiştir (Katz 2002). Silika yüzeyine immobilize edilen kaliksarenlerin konuk olarak hareket edebilen organik bileşiklerin adsorpsiyonu araştırılmıştır (Şekil 1.31.).
Si O Si O Si O O silika yüzeyi O O O H O Si Si O Si O Si O O silika yüzeyi O O O H O Si R R Guest Adsorpsiyonu
Şekil 1.33. Silika yüzeyine immoblize edilen p-t-bütilkaliks[4]arenin aromatik
bileşikleri adsorbsiyonu
Stirling ve ark. (1996), ester grupları taşıyan kaliks[8]aren monolayerlarının kararlı ve seçici bir şekilde alkali metalleri sırasıyla Cs>Rb>Na>K şeklinde transport ettiğini gözlemlemişlerdir.
Bilewicz ve ark.(1998), feniletil grubu ve L(-) norefedrin ile türevlendirilmiş kiral kaliks[4]resorsinaren türevlerini sulu çözelti/hava yüzünde monolayer olarak dizayn etmişlerdir.
Zhu ve ark. 2004 yılında yaptıkları çalışmada D-fenilalanin veya L-fenilalanin içeren sulu fazın yüzeyinde ve saf suyun yüzeyinde kiral bisiklik
guanidinyum taşıyan amfiphilik kaliksaren türevlerinin monolayerları film balans ölçümlerinden faydalanarak çalışıldı.
Şekil 1.34. Amfiphilik kaliksaren türevlerinin yapıları.
1.8. Aminoasitler ve Aminoalkoller
Protein yapımında kullanılan 20 genel α-aminoasit kiral olmayan glisin dışında belki de asimetrik sentez için en çok kullanılan kiral başlangıç maddeleri sınıfını oluşturur. Aminoasitlerin sahip olduğu fonksiyonel grup birçok yolla kullanılabilir. Aminoalkoller ise karboksil grubunun indirgenmesiyle kolayca türetilebilir ve aminoalkoller de kiral başlangıç maddeleri olarak kullanılabilirler.
Aminoalkolün amino grubu ve alkol grubu üzerinden tepkimeye girerek şelat oluşturabilirler. Birçok asimetrik reaksiyonda sterik etki nedeniyle stereokontrol
ile hem de mikrobiyolojik proseslerle yüksek enantiomerik saflıkta, çoğunlukla (S)-enantiomeri olarak (sistein için (R) (S)-enantiomeri) elde edilirler. Bu nedenle doğal olmayan zıt enantiomerler her zaman pahalıdır. Buna göre (R)-asparaginin fiyatı (S)-enantiomerinin 2 katı olmasına rağmen bu oran arjinin için 400:1’dir. Her iki enantiomerin de istenmesinin nedeni bir çok işlemde ürünün zıt enantiomerlerinin geçişine izin vermesidir. Halkalı yapıda bir aminoasit olan (S)-prolin (6) birçok asimetrik proseste yönlendirici etkide bulunmasına rağmen doğal kaynaklardan (R)-prolini elde etmek oldukça güçtür. Bu problemi çözmek için dolaylı kaynak olan ve pahalı olmayan (R)-glutamik asitten elde edilen (R)-proglutamik asit (7) kullanılarak (R)-prolin elde edilebilir.
N H2 CO2H H, N H2 CO2H CH2Ph H, N H2 H, OH N H2 CH2Ph H, OH N H2 H, N H H CO2H NH H CO2H O Pri Pri Pri OBut (1) (2) (3) (4) (5) (6) (7)
Şekil.1.35. 1-7 nolu aminoasitlerin yapıları.
Aminoasitlerin hidrokarbon yan zincirleri olanları (alanin, valin, lösin, izolösin, fenil alanin, fenilglisin) sterik yönlendirme etkisi için çok fazla kullanılmasına rağmen, diğer fonksiyonel gruplu olanları özellikle OH (serin, treonin), NH2 (lisin, ornitin), SH (sistein), CO2H (aspartik asit, glutamik asit)
CONH2 (asparajin, glutamin) aminoaside ilaveten yan zincir fonksiyonlandırması
kullanılarak daha geniş bir alanda kullanılabilir. Burada yer alan bu aminoasitler gerçektir ve birçok kiral bileşiğin asimetrikliğinin ilk kaynağıdır. Bunlar kiral yardımcı, reaktif ve katalizör olarak uygun bir kullanıma dönüştürülebilmeleri için bazı basamakları kullanmaya ihtiyaç duyarlar.
Yukarıda bahsedilen aminoasitlerden türeyen amino alkollere ilave olarak iki amino alkol geniş olarak kullanılır. Bunlardan birisi doğal olarak meydana gelen bitki alkoloidi, (1R,2S)-efidrin (8) ve (9) nolu (S,S)-aminodiol bileşiği de bir antibiyotik olan kloramfenikolün mikrobiyolojik olarak üretiminden yan ürün olarak elde edilir. Her iki bileşikte de komşu karbonlardaki stereojenik merkezler oldukça yararlıdır ve amino asitlerden (S,S)-izolösin (10) ve (2S,3R)-treoin (11) de de bu özellik vardır. (12) nolu (R)-aminoalkol ise enantiomerik saf olarak mevcuttur.
NHMe Me H OH H Ph NH2 H OH H Ph OH Me N H2 Et H H CO2H Me N H2 OH H H CO2H (8) (9) (10) (11)
2. KAYNAK ARAŞTIRMASI
Sırıt ve ark. (2007) yaptıkları bir çalışmada kaliks[4]aren diesterlerinin aminolizi ile yeni p-t-bütilkaliks[4]aren ve kaliks[4]aren diamit türevlerini sentezlemişler (Şekil 2.1.) ve bu bileşiklerin Cr2O72-/HCr2O7- anyonlarıyla
kompleksleşme özelliklerini araştırmışlardır (Şekil 2.2.).
OH OH O O R R R R O O OEt OEt OH OH O O R R R R O O NH NH R' R' 3 - 4 5 - 10 3: R = But 4: R = H 5: R = But, 6: R = H, 7: R = But, 8: R = H, 9: R = H, 10: R = H, R' = a R' = a R' = b R' = b R' = c R' = d N R': a b c d O N N
Şekil 2.1. Dikromat anyonlarının ekstraksiyonu için kullanılan kaliks[4]aren diamit
türevleri 1,52,5 3,54,5 5 6 7 8 9 10 0 20 40 60 80 100 pH % E
Yılmaz ve grubu (2006) tarafından yapılan başka bir çalışmada ise, 5,11,17,23,29,35-tert-butil-37,38-dimetoksi-39,40,41,42-(p-tosiletoksi)kaliks[6]aren
15 D-/L- fenilalaninol ile kuru THF içerisinde etkileştirerek
p-tert-butilkaliks[6]arenin kiral türevleri (16 ve 17) sentezlenmiş (Şekil 2.3.) ve bunların bazı amino asit metilesterleri ve amino alkollere karşı ekstraksiyon özellikleri sıvı – sıvı ekstraksiyon tekniği ile araştırılmıştır (Çizelge 2.1. ve Çizelge 2.2.).
2 OR 4 OMe R = CH2CH2OTs THF D-fenilalaninol THF L-fenilalaninol 2 O 4 OMe N H O H H N H O H H O 2 4 OMe 15 16 17
Şekil 2.3. Kaliks[6]arenin kiral türevleri
Çizelge 2.0. Amino asit metilesterlerinin 16 ve 17 ligandlarıyla ekstraksiyon
yüzdeleria
Ligand L-AlaOMeb D-AlaOMe L-PheOMe D-PheOMe D-TrpOMe L-TrpOMe
Amino alkol grupları taşıyan kiral p-tert-bütilkaliks[6]aren türevleri bazı aminoasit metil esterleri ve amino alkollere karşı ekstraksiyon ve kiral tanıma özelliklerini araştırmak amacıyla sentezlenmiştir. Kiral kaliks[6]aren türevleri 16 ve
17 her ne kadar kullanılan tüm amino asit ve amino alkoller için mükemmel
ekstraktantlar olsa da herhangi bir kiral seçicilik gözlenmemiştir.
Çizelge 2.1. Aminoalkollerin 16 ve 17 ligandlarıyla ekstraksiyon yüzdeleria
Ligand D-Phegly L-Phegly (R)-Hyd-Me-Pyr (S)-Hyd-Me-Pyr
16 92.3 72.5 89.1 90.4
17 83.5 87.6 84.4 91.2
a Sulu faz, [amonyum pikrat] = 2.0 × 10-5 M; organik faz, diklormetan, [ligand] = 1.0 × 10-3 M; 25°Cde, 1 saat.
Sushil ve ark. (2007) gerçekleştirdikleri bir çalışmada kaliks[4]arenin pirol türevlerini sentezlemişler ve bu bileşiklerin hem NMR hem de UV-visible spektroskopisi ile çeşitli anyonlarla (F-, Cl-, Br-, I-, HSO4-) kompleksleşmelerini
N N NO2 CHO N N N N NO2 N N N N NH2 N2H4 / Pd / C EtOH reflux N N N N NCS RNH2 / DCM N N N N N H NHR S N N N N N H N H S O O x N N N N N N H S O R' R'CH(NH2)COOMe/DCM/TEA O O x NH2 H H + H H H i) TFA/DCM, rt.72h ii) DDQ H H H 1,1-thiocarbonyldipyridone / DCM, rt. 1 h. H H H H H H (2) (3) (4) R=allyl (5) R=Ph (6) R=t-Bu (7) R=Bn (8) rt. 1 h. H H H H H H R'=Bn (9) R'=i-Pr (10) rt. 1h /DCM rt. 2h (11)
Şekil 2.5. (a) Bu4NF’ nin artan konsantrasyonlarda ilavesinin 2 numaralı bileşiğe
etkisini gösteren kısmi 1H-NMR spektrumu. (b) florür anyonlarının varlığında görülen piklerdeki kaymalar.
Nachtigall ve ark. (2002), kaliks[4]aren ve alifatik aminler arasındaki denge ilişkisi ve kompleksleşmeyi kalorimetrik ve spektrofotometrik metotla ölçmüşler, tuzlarının yapıları NMR spektroskopisi ile çalışmışlardır.
Çizelge 2.2. CD3CN içersinde TFA veya kaliks[4]aren varlığında ve yokluğunda
amin hidrojenlerinin kimyasal kayma değerleri (δ ppm).
Amin Hidrojen Bir asidin varlığında δ (ppm) değeri
Serbest TFA Kaliks[4]aren
n-Hekzilamin α-CH2 2.57 2.91 2.93 İso-propilamin CH 3.00 3.45 3.45 CH3 0.99 1.27 1.29 tert-butilamin CH3 1.07 1.35 1.39 Piperazine CH2 2.67 2.94 2.95 Dietilamin CH2 2.56 2.99 3.01 CH3 1.02 1.24 1.23
Çizelge 2.3. CH3CN içersinde kaliks[4]aren ve aminlerin titrasyonu sonucunda elde
edilen Kp değerleri. Amin Kp logKp Kpa n-Hekzilamin 18 1.26 (18.26)b İso-propilamin 15 1.18 tert-butilamin 10 1.00 18.14 Piperazin 32 1.51 Morfolin 0.5 -0.29 16.61 Piperidin 204 2.31 18.92 Dietilamin 139 2.14 18.75
![Şekil 1.9. Kaliks[4]arenin p-konumunun ve fenolik OH’larının şematik gösterimi](https://thumb-eu.123doks.com/thumbv2/9libnet/4788854.92191/26.892.176.749.123.435/şekil-kaliks-arenin-konumunun-fenolik-larının-şematik-gösterimi.webp)
![Çizelge 1.1. Kaliks[4] arenler, lineer trimerler ve monomerlerinin pK a değerlerinin karşılaştırılması](https://thumb-eu.123doks.com/thumbv2/9libnet/4788854.92191/31.892.165.809.189.392/çizelge-kaliks-arenler-lineer-trimerler-monomerlerinin-değerlerinin-karşılaştırılması.webp)
crown-7 türevinin Li + ve geçiş metali katyonlarıyla yaptığı kompleksleşmenin mekanizması](https://thumb-eu.123doks.com/thumbv2/9libnet/4788854.92191/38.892.194.762.131.393/şekil-kiral-türevinin-geçiş-katyonlarıyla-yaptığı-kompleksleşmenin-mekanizması.webp)
![Şekil 1.20. Kaliks[4]aren diamid türevlerinin kromat anyonuyla yaptığı muhtemel etkileşme](https://thumb-eu.123doks.com/thumbv2/9libnet/4788854.92191/39.892.251.741.132.389/şekil-kaliks-diamid-türevlerinin-anyonuyla-yaptığı-muhtemel-etkileşme.webp)



![Şekil 1.30. p-tert-butil kaliks[6]-1,4-benzocrown-4 bağlı durgun fazın sentez şeması.](https://thumb-eu.123doks.com/thumbv2/9libnet/4788854.92191/48.892.178.781.128.839/şekil-kaliks-benzocrown-bağlı-durgun-fazın-sentez-şeması.webp)