T.C.
EGE ÜNİVERSİTESİ TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI
Prof. Dr. Fehmi AKÇİÇEK
AKUT BÖBREK HASARLANMALI HASTALARDA
NÖTROFİL-LENFOSİT ORANI
VE BAZAL KARAKTERİSTİKLERİN
PROGNOZ ÜZERİNE ETKİSİ
UZMANLIK TEZİ
Dr. Tuğba KİP TEYMUR
TEZ DANIŞMANI
Doç. Dr. Devrim BOZKURT
ÖNSÖZ
Ege Üniversitesi Tıp Fakültesi İç Hastalıkları Anabilim Dalı’nda sürdürdüğüm uzmanlık eğitimim süresince bilgi, deneyim ve hoşgörüsünden yararlandığım, hiçbir zaman desteğini esirgemeyen Anabilim Dalı Başkanı sayın Prof. Dr. Fehmi Akçiçek’e,
Bu tezin hazırlanmasındaki yol göstericiliğinden, bilgi ve tecrübelerinden yararlandığım ve eğitimime sağladığı katkılardan dolayı tez danışmanım sayın Doç. Dr. Devrim Bozkurt’a ve Nefroloji Bilim Dalı Başkanı Prof. Dr. Hüseyin Töz’e,
İç Hastalıkları eğitimim boyunca verdikleri destek ve eğitimime sağladıkları katkılar
nedeniyle bütün İç Hastalıkları öğretim üyelerine, uzmanlarına, birlikte çalıştığım tüm asistan arkadaşlarıma, İç Hastalıkları AD bünyesinde çalışan tüm hemşire ve personellere,
Özveri ve hoşgörüleri ile bugünlere gelmemi sağlayan, hayatımın her döneminde varlıklarından güç aldığım sevgili ailem ve eşime sonsuz teşekkürü bir borç bilirim.
Dr. Tuğba KİP TEYMUR
İ
ÇİNDEKİLER
ÖNSÖZ ... ii İÇİNDEKİLER ... iii ŞEKİL VE TABLO DİZİNİ ... v SİMGELER VE KISALTMALAR ... vi ÖZET ... viii ABSTRACT ... ix 1.GİRİŞ VE AMAÇ ... 1 2.GENEL BİLGİLER ... 32.1.Akut Böbrek Hasarlanması ... 3
2.1.1.Glomerüler filtrasyon hızı ve serum kreatinini ... 3
2.1.2.Oligüri ve anüri ... 3
2.1.3.Akut tübüler nekroz (ATN) ... 4
2.1.4.Akut böbrek yetmezliği ... 5
2.1.5.RIFLE kriterleri ... 5
2.1.6.Akut böbrek hasarlanması ... 6
2.1.7.Çalışmalarda RIFLE kriterleri ... 7
2.1.8.ABH tanımının kısıtlı yanları ... 7
2.1.9.ABH tanım ve sınıflandırılması ... 7
2.1.10.Bazal SCr değerinin tahmin edilmesi ... 12
2.1.11.Klinik değerlendirme ... 14
2.1.11.1.Psödo ABH ... 14
2.1.11.2.Atipik ABH ... 14
2.2.Yoğun bakım hastalarında akut böbrek hasarlanması ... 15
2.3.Sistemik inflamasyon ve akut böbrek hasarlanması ilişkisi ... 17
2.3.1.Sepsiste ve septik şokta renal hemodinamik değişiklikler ve sistemik mediatörler ... 19
2.4.Klinikte nötrofil-trombosit lenfosit oranı ve inflamasyon ilişkisi ... 24
2.4.1.Kardiyovasküler hastalıklarda NLO ... 25
2.4.2.Kanser NLO ilişkisi ... 26
3.MATERYAL METOD ... 29
3.1.Çalışma tasarımı ve hastalar ... 29
3.2.Hesaplamalar ... 30
3.3.İstatiksel analiz yöntemleri ... 30
4.BULGULAR ... 31
5.TARTIŞMA ... 41
5.1.Çalışmamızın güçlü yanlar ve limitasyonları ... 44
Ş
EKİL VE TABLO DİZİNİ
Şekil 1. RIFLE kriterleri
Şekil 2. Sepsiste akut renal yetmezliğe yol açan mekanizmalar Şekil 3. Final NLO, NLO değişimi ve NLO % değişimi
Şekil 4. Final NLO, NLO ve NLO % değişimi için ROC analizi
Tablo 1. ABH evrelemesi
Tablo 2. ABH tanı ve sınıflamasında RIFLE ve AKIN kriterlerinin karşılaştırılması Tablo 3. ABH’nın hızlı tanı ve spesifik tedavi gerektiren nedenleri ve tanı testleri Tablo 4. Tahmini bazal Scr değerleri
Tablo 5: Tüm çalışma grubunun bazal demografik laboratuvar karakteristikleri (n=96) Tablo 6. ABH etyolojisi
Tablo 7. Kardiyovasküler hastalık öyküsü ve komorbiditeler Tablo 8. Diyaliz ihtiyacı olan ve olmayan hastalar
Tablo 9. Diyaliz endikasyonu
Tablo 10. Sağ kalan ve ölen hasta sayısı Tablo 11. Mortalite nedenleri
Tablo 12. Mortalite prediktörleri
Tablo 13. Kohort hastalarında NLO değişimi
SİMGELER VE KISALTMALAR
ABD : Amerika Birleşik Devletleri
ABH : Akut Böbrek Hasarlanması
ABY : Akut Böbrek Yetmezliği
ACE inh : Anjiotensin Konverting Enzim inhibitörü
ADH : Anti Diüretik Hormon
ADQI : Acute Dialysis Quality Initiative, Akut Diyaliz Kalite İnsiyatifi
AKIN : Acute Kidney Injury Network, Akut Böbrek Hasarı Ağı
APACHE 2 : Acute Physiology and Chronic Health Evaluation 2,Akut Fizyoloji ve Kronik Sağlık Değerlendirmesi 2
ATN : Akut Tübüler Nekroz
C3a : Kompleman 3a
C5a : Kompleman 5a
C5b : Kompleman 5b
CRP : C Reaktif Protein
D-ABH : Diyaliz gerektiren akut böbrek hasarlanması
DİK : Dissemine İntravasküler Koagülasyon
eCrCl : Tahmini kreatinin klirensi
eGFR : Tahmini glomerüler filtrasyon hızı
ESRD : End Stage Renal Disease, Son Dönem Böbrek Hastalığı
GFR-GFH : Glomerüler Filtrasyon Hızı
HR : Hazard oranı
hsCRP : Yüksek Duyarlı C Reaktif Protein
IL : İnterlökin
iNOS : İndüklenebilir Nitrik Oksit Sentetaz
KAE : Koroner Arter Ektazisi
KBH : Kronik Böbrek Hastalığı
KBY : Kronik Böbrek Yetmezliği
KDIGO : Kidney Disease Improving Global Outcomes
MCP-1 : Monosit Kemotaktik Proteini 1
MDRD : Modification of Diet in Renal Disease, Renal Hastalıkta Diyet Modifikasyonu Çalışması
mg/kg/s : Miligram/kilogram/saat micL : Mikrolitre micromol/L-µmol/L : Mikromol/litre ml/dak : Mililitre/dakika ml/kg/saat : Mililitre/kilogram/saat mmHg : Milimetre civa
NLO-N/L : Nötrofil/Lenfosit Oranı
NO : Nitrik Oksit
PAF : Trombosit Aktive Edici Faktör
PG : Prostoglandin
RIFLE : -risk –injury –failure –loss –end stage renal disease baş harflerinden oluşan akronim
RRT : Renal Replasman Tedavisi
SCr : Serum kreatinini
SDBY : Son Dönem Böbrek Yetmezliği
SOFA : Sepsis-related Organ Failure Assessment, Sepsis ilgili organ yetersizliğinin değerlendirilmesi
TLO-T/L : Trombosit/Lenfosit Oranı
TNF : Tümör Nekrozis Faktör
TXA2 : Tromboksan A2
VIP : Vazoaktif İntestinal Polipeptid
ÖZET
GİRİŞ VE AMAÇ:
Son zamanlarda daha çok akut böbrek hasarlanması (ABH) olarak adlandırılmaya başlanan akut böbrek yetmezliği, yoğun bakım hastalarında kardiyovasküler sistem komplikasyonları, enfeksiyon, morbidite ve mortalitenin temel nedenlerinden biridir.
Nötrofil lenfosit oranı (NLO), birçok hastalıkta etkinliği gösterilmiş, yeni ve kolay ölçülebilir bir inflamasyon göstergesidir. Sistemik inflamasyon, ABH ve hasta mortalitesi birbirleriyle yakın ilişkili kavramlardır. İnflamasyonun erken saptanması ve takip edilebilmesi, ABH’ye bağlı hasta mortalitesini azaltabilir.
YÖNTEM:
Bu retrospektif çalışmada 96 ABH tanılı hasta incelendi. Hastaların demografik özellikleri, yeni inflamasyon belirteci olarak NLO ve rutin biyokimyasal incelemeler; başvuru anı, taburculuk ve poliklinik takipleri olarak kaydedildi. Sonuçlar istatistiksel olarak değerlendirildi.
BULGULAR:
Hastaların takip periyodunda NLO değişimlerindeki azalma poliklinik takiplerinde de, özellikle yaşayanlar için, daha belirgindir. Taburculuk anındaki NLO bağımsız bir mortalite öngörücüsüdür. Kesme noktası olarak NLO ≥10 değeri, %73 sensitivite ve %87 spesifitede (HR: 7.31, 95% CI: 3.36-15.91; p<0.001) anlamlı mortalite öngörücüsüdür. NLO’daki takip peryodunda günlük 1 birim azalma hastane mortalitesinde %30 azalma ve günlük %1’lik azalma hastane mortalitesinde %15’lik azalmaya karşılık gelmektedir. Diğer parametrelere oranla en anlamlı mortalite öngörücüsüdür.
SONUÇ:
Hastane izleminde NLO değişimi, hasta sağ kalımının anlamlı bir takip parametresi olabilir.
SUMMARY
INTRODUCTION:
Acute renal failure, currently named as acute kidney injury (AKI); is one of the most leading cause of cardiovascular failure, infections, morbidity and mortality in intensive care unit (ICU) patients. An easily measurable parameter, ratio of neutrophil and lymphocyte counts (NLR), is the novel inflammatory marker in various clinical conditions. Systemic inflammation, AKI and patients’ mortality can occur in combined fashion, to detect inflammation timely or screening may reduce the high rates of patients’ mortality due to AKI.
METHODS
In this retrospective report, 96 AKI patient were recruited. Demographical properties, non traditional inflammation marker neutrophil-to-lymphocyte ratio (NLR) and routine biochemical analysis on admission (baseline), at discharge (final) and after discharging during outpatient clinic follow-up (last follow-up) were included in statistical analysis.
RESULTS
Thre was a trend toward to decrease in NLR values in patients who alive even in outpatient clinic fallow-up. Final NLR was significantly correlated with mortality. The cut-off value for final NLR, ≥10, is significant mortality predictor which has 73% sensitivity and 87% specifity (HR: 7.31, 95% CI: 3.36-15.91; p<0.001). Every 1 point decrease per day of NLR during hospitalization decreases likelihood of mortality 30% and every 1 percentage decrease from baseline per day during hospitalization decreases likelihood of mortality 15%. Several models including variations of variables above revealed that best predictor of mortality is absolute NLR change during hospitalization.
CONCLUSION:
NLR change during hospital course may be a screening tool for patients’ outcome.
1.
GİRİŞ VE AMAÇ
Son yıllarda akut böbrek yetmezliği (ABY) kavramı üzerine yeniden incelemeler yapılmıştır. Akut böbrek hasarlanmasında böbrek fonksiyonlarının göreceli olarak hafif hasarlandığı, ABH’nin idrar çıkış miktarındaki ve kan kimyasındaki değişikliklerle açığa çıktığı, ciddi klinik sonuçlara işaret ettiği öne sürülmektedir [1-5]. Birçok rewiev ve textbook bölümünde böbrek fonksiyonlarındaki ciddi azalma, beraberinde ciddi azotemi ve genellikle oligüri veya anüri olduğu vurgulanmıştır. ABY’nin kesin biokimyasal tanımlanması için bir öneri hiç yapılmamıştır ve ABY tanı kriteri veya klinik tanımlaması üzerine fikir birliği sağlanamadığından birçok değişik tanımı mevcuttur.
Akut Diyaliz Kalite İnsiyatifi (ADQI) grubunca akut renal fonksiyon bozukluğu tanımlaması ve sınıflandırması için bir sistem geliştirilmiştir [6]. Baş harfleri RIFLE’dir (-risk [risk] –injury [hasar] –failure [yetersizlik] ve 2 sonuç sınıflaması –loss [kayıp] –end stage renal disease [son dönem böbrek yetmezliği]). Renal fonksiyonlardaki akut değişiklikleri kapsamlı bir şekilde tanımladığından RIFLE kriterlerinin ABY’nin ötesine geçmektedir. ‘Akut böbrek hasarlanması (ABH)’ terimi renal fonksiyonlardaki minör değişikliklerden renal replasman tedavisi (RRT) gerektiren bozukluklara kadar geniş bir spektrumu oluşturan sendromu tanımlamaktadır [7]. Bu nedenle RIFLE kriterlerince tanımlanan ABH konsepti yeni bir bakış açısı yaratmaktadır.
ABH; ne ATN ne de böbrek yetmezliğidir. Bunun yerine; her ikisini de ve ayrıca daha az ciddi durumları da kapsar. ABH; spesifik böbrek hastalıkları (örn. Akut intersitisyel nefrit, akut glomerüler ve vaskülitik böbrek hastalıkları), spesifik olmayan durumlar (örn. İskemi, toksik hasarlanma), ekstrarenal patolojiler (örn. Prerenal azotemi ve akut postrenal obstrüktif nefropati) gibi birçok etyolojiyi kapsayan geniş bir klinik sendromdur. Aslında bir sendrom olarak gerçek böbrek hasarı olmayan ancak fizyolojik taleplere göre rölatif fonksiyonel hasarlanması olan hastaları da içerir. ABH sınıflaması yaparken bu tip hastaları dahil etmek önemlidir çünkü, bu hastalar erken müdahaleden kesinlikle karlı çıkacaklardır. ABH’ye hastanelerin dahili, cerrahi, pediatri, onkoloji kliniklerinde ve yoğun bakım ünitelerinde (YBÜ) sık rastlanır. Tabiatına bakılmaksızın uzun ve kısa vadede olumsuz sonuçlar için bir prediktördür. Tüm dünya çapında tanı, tarama, tedavi ve diyalize gidişi önlemeye, ABH sonuçlarını iyileştirmeye ihtiyaç vardır [8].
Geleneksel kılavuzlarda bu konu hakkında bilgi bulunmamaktadır. ABH’nin erken tanı, ayırıcı tanı ve prognozunda serum kreatinin değeri (SCr) dışındaki diğer biyomarkırların rolü incelenmelidir. ABH riski veya ABH’ye progresyon riskini öngören biyomarkırlar, ABH sonrası düzelmeyi veya ölüm ve uzun dönem RRT ihtiyacını öngören biyormarkırların tespiti için yeni araştırmalara ihtiyaç vardır.
Çalışmamızda son dönemde yapılan araştırmalarda hastalık prognozları hakkında değerli bilgiler sunduğu düşünülen trombosit/lenfosit oranı (TLO) ve nötrofil/lenfosit (NLO) oranının diğer geleneksel inflamasyon markırları da kullanılarak ABH’lı hastalarda morbidite ve mortalite prediktörü olarak incelenmesi planlandı. Bu çalışmada Ocak 2010 – Aralık 2013 yılları arasında Ege Üniversitesi İç Hastalıkları Kliniği’ne başvuran akut böbrek hasarlanmalı hastaların klinik özellikleri, böbrek fonksiyonları, diyaliz ihtiyaçları, rutin biokimyasal testleri ve TLO - NLO yönünden retrospektif olarak araştırılması amaçlanmıştır.
2.
GENEL BİLGİLER
2.1.Akut böbrek hasarlanması
Son yıllarda akut böbrek yetmezliği (ABY) kavramı üzerinde bir çok inceleme yapılmıştır. ABY’nin akut geliştiği, böbreğin göreceli olarak hafif hasarlandığı veya böbrek fonksiyonlarının hafif bozulduğu, idrar çıkış miktarındaki ve kan kimyasındaki değişikliklerle açığa çıktığı, ciddi klinik sonuçlara işaret ettiğini gösterilmiştir [1-5].
Geleneksel olarak birçok rewiev ve textbook bölümünde böbrek fonksiyonlarındaki ciddi azalma, beraberinde ciddi azotemi ve genellikle oligüri veya anüri olduğu vurgulanmıştır. Son yıllarda böbrek fonksiyonlarındaki ılımlı bir azalmanın bile kritik hastalar [2] ve kontrast nefropatisinde [5] potansiyel bir öneminin olduğu üzerinde durulmaktadır.
2.1.1. Glomerüler filtrasyon hızı ve serum kreatinini
Böbrek fonksiyonlarını en iyi gösteren belirtecin glomerüler filtrasyon hızı olduğu oldukça kabul görmüştür. Buna karşın GFR ölçümü zordur ve genelde kreatinin gibi endojen filtrasyon belirteçlerinden tahmini bir hesaplama yapılır. Serum kreatininde (SCr) >0.3 mg/dl’lik (>26.5 mikromol/l) artış mortalite ile ilişkilidir [1]. SCr’deki bu küçük değişikliklerin hastane mortalitesini neden arttırdığı tamamen açık değildir. Olası nedenler; volüm yüklenmesi, üremik bileşenlerin retansiyonu, asidoz, elektrolit bozuklukları, enfeksiyon riskinde artış ve anemi gibi azalmış böbrek fonksiyonlarının istenmeyen etkileridir [9]. Ayrıca SCr’deki bu değişimler mortalitede artışa neden olan ölçülemeyen diğer değişikenlere bağlı da olabilir. Böbrek fonksiyonlarında ciddi azalmalar da daha kötü sonuçlarla ilişkili olma eğilimindedir.
2.1.2. Oligüri ve anüri
İdrar çıkışı hem böbrek fonksiyonlarını hem de tübüler hasarlanmayı gösteren duyarlı
bir biyomarkırdır. İdrar çıkışı, GFR ve tübüler hasarlanma arasında karmaşık bir ilişki vardır. Örneğin; tübüler fonksiyonlar bozulmamışsa oligüri daha derin olabilir. Hipovolemi ve
toplayıcı kanallar suya tamamen geçirgen hale gelir. Medullanın iç kısımlarındaki konsantrasyon mekanizmaları da destek verir ve idrar volümü azaltılmış, idrar konsantrasyonu arttırılmış olur. Tam tersi, tübüller hasarlandığında maksimum konsantrasyon yeteneği bozulur ve idrar volümü normal olabilir (ör: nonoligürik böbrek yetmezliği). Oligüri ve azotemi bozulmamış tübüler fonksiyonu gösteren güçlü bir kanıttır. Bununla birlikte; bu ‘benign’ veya prerenal azotemi olarak yorumlanmamalıdır. Bozulmamış tübüler fonksiyon, renal hastalıkların (ör: glomerulonefritler) çeşitli formlarında özellikle erken dönemlerde görülebilir. Sepsis; YBÜ’lerinde ABY’nin en sık nedenidir ve idrar bulgularında karakteristik değişikliklere neden olmadan böbrek fonksiyonlarını değiştirebilir [10,11]. Bu anormallikleri ‘prerenal’ olarak sınıflandırmak şüphesiz yanlış kararlar alınmasına neden olur. Son olarak; oligüri ve anüri renal tübüler hasar sonucu oluşabileceği gibi üriner trakt obstrüksiyonu ve total arteriyel veya venöz oklüzyona bağlı da oluşabilir. Bu koşullar böbreğin hızlı ve geri dönüşü olmayan hasarına neden olabileceği için hemen tanım ve değerlendirme yapmak gerekir.
2.1.3. Akut tübüler nekroz (ATN)
Memeli böbrekleri uzamış sıcak iskemiyi takiben reperfüzyona maruz kaldığında proksimal tübüllerde nekroz gelişir [12]. Hayvan deneylerinde distal nefron tutuluşu minimaldir [13]. Bu hayvanlarda ciddi ABY gelişir. Aslında ‘akut tübüler nekroz’ terimi bu koşullardaki morfolojik değişimleri tam olarak yansıtmamaktadır [14]. Bunun yerine; ATN terimi tübüler bütünlüğü sağlayabilecek ancak glomerüler filtrasyonu muhafaza edemeyecek kadar yeterli renal perfüzyonu tanımlamak için kullanılmıştır. 1950’lerden günümüze renal biyopsi verilerinde [15] ciddi organ disfonksiyonu yerine limitli parankimal taviz [14] olduğu belirtilmektedir. Bu nedenle ATN sendromunu geleneksel olarak çalışılan hayvan modelleri ile izah etmek yetersizdir. Son zamanlarda araştırmacılar renal hasara neden olan endotel disfonksiyonu, koagülasyon anormallikleri, sistemik inflamasyon ve oksidatif stresin rolünü araştırmaya ağırlık vermiştir [16]. Örneğin, arteriyel hasarı olan hastalarda (örn. rüptüre anevrizma, akut diseksiyon) hayvan modellerindeki gibi uzamış sıcak iskemiye bağlı hasar görülür. Ancak bu olgular ABH’li hastaların sadece ufak bir bölümünü oluşturmaktadır ve ironik olarak bu hastalar genelde ATN’yi araştıran çalışmalardan dışlanır.
2.1.4 Akut böbrek yetmezliği
ABY terimi ilk kez William Heberden tarafından 1802’de ‘ischuria renalis’ olarak tanımlanmıştır [17]. 20. yüzyılın başlarında ABY ‘acute Bright’s disease’ olarak William Osler’s Textbook for Medicine (1909) isimli kitabında da tanımlanmıştır; Toksik ajan, gebelik, yanık, travma veya böbrek operasyonu sonucu geliştiği belirtilmiştir. 1. Dünya Savaşı sırasında ‘savaş nefriti’ [18] olarak isimlendirilmiş ve birçok yayında bu şekilde rapor edilmiştir. 2. Dünya Savaşı döneminde Bywaters ve Beal ‘crush sendromu’ raporlarını yayınlayana kadar unutulmuştur [18]. Homer W. Smith ‘akut böbrek yetmezliği’ terimine girişte itibarlı biri olarak kabul edilir ve ‘The Kidney – Structure and Function in Health and Disease’ (1951) isimli kitabında ‘travmatik yaralanmalarla ilişkili akut böbrek yetmezliği’ bölümü mevcuttur.
Maalesef bu zamana kadar ABY’nin kesin biokimyasal tanımlanması için bir öneri yapılmamıştır. ABY tanı kriteri veya klinik tanımlaması üzerine fikir birliği sağlanamadığından birçok değişik tanımı mevcuttur. Literatürde en az 35 ABY tanımlaması mevcuttur [20]. Bu karmaşık durum ABY’nin insidans ve klinik önemi konusunda geniş varyasyonlara neden olmaktadır. Kullanılan tanımlamalara göre YBÜ hastalarının %1.25’inde ABY görülürken mortalite oranları da %15-60 arasında değişmektedir [21-23].
2.1.5. RIFLE kriterleri
Akut Diyaliz Kalite İnsiyatifi (ADQI) grubunca oluşturulmuş bir konsensus tarafından akut renal fonksiyon bozukluğunun tanımlaması ve sınıflandırılması için bir sistem geliştirilmiştir [6]. Bu sistem Şekil 1’de özetlenmiştir. Baş harfleri RIFLE’dir (-risk [risk] – injury [hasar] –failure [yetersizlik] ve 2 sonuç sınıflaması –loss [kayıp] –end stage renal disease [son dönem böbrek yetmezliği]). 3 ciddiyet derecesi SCr (serum kreatinin) veya idrar çıkışı temel alınarak tanımlanmıştır. 2 sonuç kriteri de böbrek fonksiyon kaybının süresi göz önünde bulundurularak tanımlanmıştır.
Şekil 1: RIFLE kriterleri
2.1.6. Akut böbrek hasarlanması
Renal fonksiyonlardaki akut değişlikler daha kapsamlı bir şekilde tanımladığından RIFLE kriterleri ABY’nin ötesine geçmektedir. ‘Akut böbrek hasarlanması’ (ABH) terimi renal fonksiyonlardaki minör değişikliklerden renal replasman tedavisi (RRT) gerektiren bozukluklara kadar geniş bir spektrumu oluşturan sendromu tanımlamaktadır [7]. RIFLE kriterlerince tanımlanan ABH konsepti yeni bir bakış açısı yaratmaktadır. ABH; ne ATN, ne de böbrek yetmezliğidir. Aslında bir sendrom olarak gerçek böbrek hasarı olmayan ancak fizyolojik taleplere göre rölatif fonksiyonel hasarlanması olan hastaları da içerir. ABH sınıflaması yaparken bu tip hastaları da tanımlamaya dahil etmek ilgi çekicidir. Bu hastalar erken müdahaleden kesinlikle yarar göreceklerdir. ABH hem hasarlanma hem de bozulmayı içerir. Sadece renal yetmezlikli veya diyalize giren hastalara odaklanmaktansa, hastane mortalitesi ile yakından ilişkili ABH bizi bu hastalıkla ilgili düşüncelerimizi değiştirmeye itmektedir. ABH; sıvı, elektrolit, asit baz ve hormonal düzenlemede derin değişimlere neden
olur. ABH’lı birçok hastada multisistem organ yetmezliği zaten vardır. YBÜ’deki ciddi sepsisli hastaların sonlanımları ABH’nın erken rezolüsyonu ile yakından ilişkilidir. ABH’nın hızlı düzelmesi prognoz için basit bir markır olabilir [24].
2.1.7. Çalışmalarda RIFLE kriterleri
ABH hastalarını sınıflamak için bir araç olarak kullanılan RIFLE kriterleri ile 2010 yılının başından itibaren bir milyon hasta incelenmiştir [25-28]. ABD [28], Avrupa [29,30] ve Avustralya’dan [25] incelenen büyük serilerde binlerce hasta tutarlı bir tablo çizmiştir. Hastaların %47’sinde sepsis tetikleyici faktördür. RIFLE sınıflaması; renal fonksiyonların düzelmesi, RRT gerekliliği, sağ kalan hastalar için hastanede kalış süresi ve hastane mortalitesi için kullanışlı prediktif bilgiler sunmaktadır [31]. RIFLE sınıflamasındaki artışla hastane mortalitesindeki artış arasında lineer bir ilişki söz konusudur. RIFLE R sınıfı hastaları bile ABH geliştirmemiş hastalara göre 3 kat daha mortal seyretmektedir [5]. ABH ciddiyetindeki artış komorbiditeden bağımsız ölüm riskinde artış ile ilişkilidir [28].
2.1.8. ABH tanımının kısıtlı yanları
Maalesef dışlama kriterleri halen sınırlıdır. ABH tanımı ve sınıflaması için harcanan çabaya rağmen uygulamada tutarsızlıklar vardır [26, 27]. Çalışmaların az bir kısmında idrar çıkışı da kriterlere dahil edilmiştir [9, 29] ve birçok çalışmada başlangıç SCr değeri zaten yüksek olan hastalar dışlanmıştır. ABH vakalarının yaklaşık üçte birinin toplumdan kazanıldığı için birçok çalışmada doğru insidans verisi sağlanamamaktadır. Gelecekte keşfedilecek renal hücre hasarlanması biyomarkırları tarafından ABH’li yeni hastalar saptanabilir ve hastalar daha erken evlerde tanımlanabilir.
2.1.9. ABH tanım ve sınıflandırılması
ABH böbrek yapı ve fonksiyonunu etkileyen bir dizi durumdur. ABH böbrek fonksiyonlarındaki ani azalma olarak tanımlanmıştır. ABH; spesifik böbrek hastalıkları (örn. Akut intersitisyel nefrit, akut glomerüler ve vaskülitik böbrek hastalıkları), spesifik olmayan
durumlar (örn. İskemi, toksik hasarlanma), ekstrarenal patolojiler (örn. Prerenal azotemi ve akut postrenal obstrüktif nefropati) gibi birçok etyolojiyi kapsayan geniş bir klinik sendromdur. Birden fazla koşul aynı hastada aynı zamanda varolabilir. Epidemiyolojik kanıtlar, düzelebilecek erken evre ABH’nın bile artmış ölüm riski gibi önemli klinik sonuçlar doğurabileceğini desteklemektedir [2, 5]. Bu nedenle ABH akut akciğer hasarlanması veya akut koroner sendrom gibi düşünülebilir. ABH böbrek kaynaklı veya böbrek dışından gelen strese bağlı olabilir. ABH’nın hastalık belirtilerinin ortaya çıkış şekli ve klinik bulguları, etiyolojisi ne olursa olsun oldukça benzerlik gösterir. ABH bir sendrom olarak hem direk böbrek hasarı hem de böbrek fonksiyonlarındaki akut bozulmayı kapsar. ABH tedavisinin altta yatan etiyolojiye yönelik yapılması genel kabul gören bir kavramdır.
ABH sık görülür ve olanaklar dahilinde tedavi edilebilirdir. Böbrek fonksiyonlarında en ufak akut bir bozulmanın bile kötü bir prognozu vardır. ABH’nın erken tanı ve tedavisi sonuçlarda iyileşme sağlayabilir. SCr ve idrar çıkışına dayanan iki benzer tanımlama (RIFLE ve AKIN) önerilmiş ve kabul görmüştür.
ABH aşağıdakilerden biri olarak tanımlanmıştır:
- SCr’de 48 saat içerisinde ≥0.3 mg/dl (≥26.5 µmol/L) artış veya;
- SCr’de son 7 gün içerisinde bazale göre ≥1.5 kat artış veya;
- İdrar miktarının 6 saat boyunca <0.5 ml/kg/saat olması.
ABH ciddiyetine göre şu şekilde evrelendirilmiştir (Tablo 1).
Tablo 1. ABH evrelemesi
Evre Serum Kreatinin İdrar Çıkışı
1 Bazale göre 1.5-1.9 kat artış
veya
≥0.3 mg/dl (≥26.5 µmol/L) artış
<0.5 ml/kg/saat 6-12 saatte
2 Bazale göre 2.0-2.9 kat artış
<0.5 ml/kg/saat
≥12 saat boyunca
3
Bazale göre 3 kat artış veya
SCr ≥4.0 mg/dl veya
Başlangıçta RRT veya <18 yaş hastalarda
eGFR’nin <35 ml/dk/1.73 m2 olması
Anüri ≥12 saat veya
<0.3 ml/kg/saat 24 saat boyunca
Böbrek yapı ve fonksiyonlarını etkileyen durumlar sürelerine bağlı olarak akut veya kronik etkiler oluşturur. ABH bir dizi akut böbrek hastalığından veya bozukluğundan biridir. ABH diğer akut veya kronik böbrek hastalığı/bozukluklarıyla beraber veya tek başına ortaya çıkabilir. Oysa, kronik böbrek hastalığı iyi belirlenmiş bir kavramsal model ve tanımlamadır [32-34]. ABH kavramı göreceli olarak daha yenidir ve halen gelişmektedir.
GFR’nin, hastalık ve sağlık durumlarında, böbrek fonksiyonlarını en iyi gösteren belirteç olduğu yaygın olarak kabul edilmiştir. SCr’de ve idrar çıkış miktarındaki değişiklikler de GFR’deki değişikliklerin yerine kullanılmaktadır. Klinik uygulamada GFR’deki ani düşme, SCr’de yükselme veya öligüri ile değerlendirilir. Renal hasarlanmanın erken tanı ve tahmini için daha sensitif ve spesifik biyomarkırlara ihtiyaç olduğu hakkında genel bir fikir birliği vardır. ADQI tarafından öne sürülen RIFLE kriterleri ilk uluslararası, disiplinlerarası konsensus kriteridir. Pediatrik popülasyon için daha uygun olan modifiye kriterler de öne
sürülmüştür (pRIFLE) [35]. SCr’deki küçük değişiklikler RIFLE tarafından
yakalanamamaktadır. Bu nedenle AKIN kriterleri ile birlikte değerlendirme yapılması sensitiviteyi arttıracaktır. (Tablo 2).
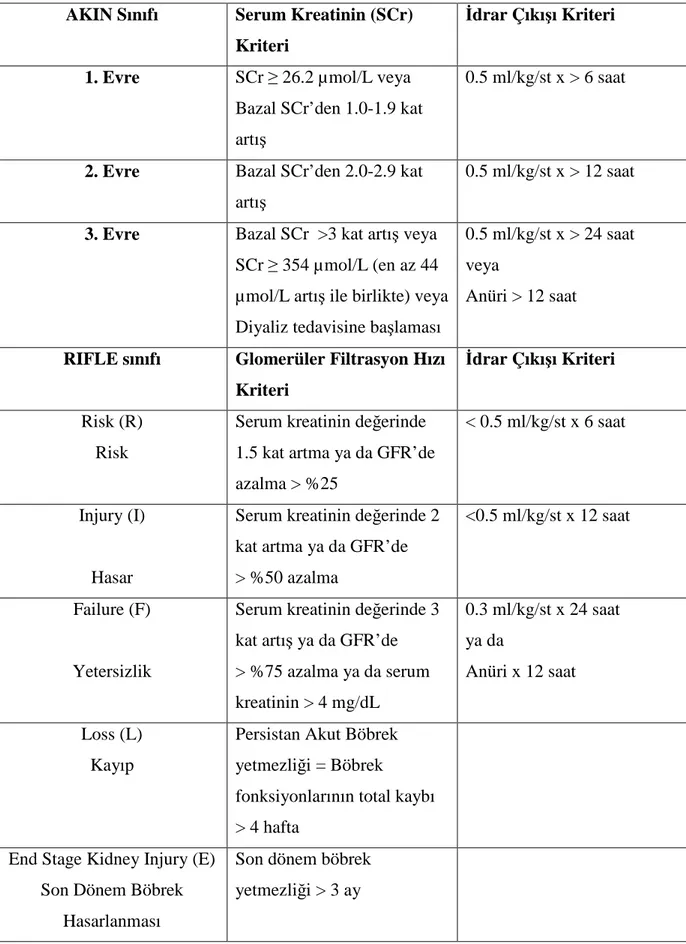
Tablo 2. ABH tanı ve sınıflamasında RIFLE ve AKIN kriterlerinin karşılaştırılması. AKIN Sınıfı Serum Kreatinin (SCr)
Kriteri
İdrar Çıkışı Kriteri
1. Evre SCr ≥ 26.2 µmol/L veya Bazal SCr’den 1.0-1.9 kat artış
0.5 ml/kg/st x > 6 saat
2. Evre Bazal SCr’den 2.0-2.9 kat artış
0.5 ml/kg/st x > 12 saat
3. Evre Bazal SCr >3 kat artış veya SCr ≥ 354 µmol/L (en az 44 µmol/L artış ile birlikte) veya Diyaliz tedavisine başlaması
0.5 ml/kg/st x > 24 saat veya
Anüri > 12 saat
RIFLE sınıfı Glomerüler Filtrasyon Hızı Kriteri
İdrar Çıkışı Kriteri
Risk (R) Risk
Serum kreatinin değerinde 1.5 kat artma ya da GFR’de azalma > %25
< 0.5 ml/kg/st x 6 saat
Injury (I)
Hasar
Serum kreatinin değerinde 2 kat artma ya da GFR’de > %50 azalma
<0.5 ml/kg/st x 12 saat
Failure (F)
Yetersizlik
Serum kreatinin değerinde 3 kat artış ya da GFR’de > %75 azalma ya da serum kreatinin > 4 mg/dL 0.3 ml/kg/st x 24 saat ya da Anüri x 12 saat Loss (L) Kayıp
Persistan Akut Böbrek yetmezliği = Böbrek
fonksiyonlarının total kaybı > 4 hafta
End Stage Kidney Injury (E) Son Dönem Böbrek
Hasarlanması
Son dönem böbrek yetmezliği > 3 ay
RIFLE ve AKIN kriterleri hastanede yatmakta olan hastaların artmış ölüm riski ve/ya RRT ihtiyacını ortaya çıkaran gruplamalar yapabilmektedir [2, 5, 25, 28-30]. ABH evrelemesi yapmak; evredeki artışla ölüm riski ve RRT ihtiyacındaki artış korele olduğu için uygun bir yaklaşımdır [2, 5, 25, 28-31]. Ayrıca ABH düzeldikten sonra bile uzun vadede kardiyovasküler hastalık, KBH ve mortalite gelişme riskinde artış olduğu da kanıtlanmıştır [36-38]. Sensiviteyi arttırmak amacıyla ABH’lı hastaları hem RIFLE hem de AKIN kriterlerini birlikte kullanarak değerlendirmek mantıklı olacaktır [29].
Evrelemede hastalar kendilerini en yüksek evreye yerleştiren kritere göre evrelendirilmelidir. Bu nedenle kreatinin ve idrar çıkışına göre değişik evrelere giren hastalar girdikleri en yüksek evreye göre evrelenir. Orjinal RIFLE kriterlerine göre yapılmış yayınlardaki GFR değişiklikleri SCr’deki değişimleri tam olarak karşılamamaktadır. SCr’nin ölçülebilir, GFR’nin ise ancak tahmin edilebilir olması nedeniyle kreatinin kriteri ABH tanısı ve evrelemesi için idrar çıkışı ile birlikte kullanılmalıdır.
ABH tanımlaması ortalama ölçülere sahip erişkinler için geliştirişmiş RIFLE ve AKIN
kriterlerini temel alır. Kreatinin bazlı tanımlamada SCr >4.0 mg/dl (>354 µmol/L) ise hasta otomatik olarak Evre 3’e kabul edilir. Daha küçük pediatrik hastalar için bu tanımlama problem oluşturur. İnfant ve çocukların düşük kas kitleleri olduğundan 4.0 mg/dl gibi bir SCr değerine ulaşmaları mümkün olmayabilir. Bu nedenle modifiye RIFLE ABH kriterleri, tahmini kreatinin klirensi (eCrCl) baz alınan Schwartz formülüne dayanarak geliştirilmiştir.
İdrar çıkışının tanı ve evrelemede kullanılması daha az değerli bir kriterdir. Örneğin
GFR aniden sıfıra düşerse SCr’deki ölçülebilen artış saatler içinde olacaktır ancak idrar çıkışı hemen etkilenecektir. İdrar çıkışının SCr’ye teorik olarak avantajı cevabın hızıdır. İlaç etkileri (örn. ACE inh.), sıvı dengesi ve diğer faktörleri içeren, hasta bireye özgü klinik değerlendirmeye ihtiyaç duyulur. Obez hastalar için bazen normal idrar çıkışı ABH kriteri olabilir. SCr ile idrar çıkışının ABH tanısında kullanıldığı çalışmalarda sadece SCr kullanılmasının birçok hastanın gözden kaçmasına neden olduğu belirtilmiştir. İdrar çıkışı kriterinin kullanılması çelişkili vakaların sayısını azaltır.
Hasta yönetimi mutlaka hastalığın nedenine yönelik yapılmalıdır. ABH nedeninin mümkün olduğunca belirlenmesi önemlidir. Özellikle azalmış böbrek perfüzyonu, akut glomerülonefrit, vaskülit, intersitisyel nefrit, trombotik mikroanjiopati ve idrar yolu obstrüksiyonu acil tanı ve spesifik tedavi gerektirir.
Tablo 3. ABH’nın hızlı tanı ve spesifik tedavi gerektiren nedenleri ve tanı testleri.
ABH’nın hızlı tanı ve spesifik tedavi gerektiren nedenleri
Önerilen tanı testleri
Azalmış böbrek perfüzyonu Volüm durumu ve üriner tanı belirteçleri
Akut glomerülonefrit, vaskülit, intersitisyel nefrit, trombotik mikroanjiopati
İdrar sedimenti değerlendirmesi, serolojik
testler, hematolojik testler
İdrar yolu obstrüksiyonu Böbrek ultrasonu
Nedeni tespit etmek her zaman mümkün değildir ve neden belli olsa da spesifik bir tedavisi olmayabilir. ABH sendromlu hastalardan spesifik böbrek hastalığı olanlar (örn. Glomerülonefritler) için spesifik tedaviler mevcuttur. Bu nedenle ABH’nin altta yatan nedeni mutlaka araştırılmalıdır.
SCr’nin ABH riski altındaki hastalarda sık aralıklarla ölçülmesi tanı koyma hızı ve doğruluğu açısından oldukça yararlıdır. Yüksek risk altındaki veya ABH şüphesi bulunan hastalarda bu nedenle sık SCr ölçümlerinin yapılması önerilmektedir.
2.1.10. Bazal SCr değerinin tahmin edilmesi
Birçok hasta güvenilir bir bazal SCr değeri kaydı olmadan ABH ile başvurur. Bazal SCr değeri Renal Hastalıkta Diyet Modifikasyonu Çalışmasının (Modification of Diet in
Renal Disease Study- MDRD) bazal eGRF’yi 1.73 m2 başına 75 ml/dk olarak kabul eden bir
denklemi yardımıyla tahmin edilebilir (Tablo 4). Bu uygulama yakın zamanda geçerli kabul edilmiş olup ayrıca RIFLE yöntemini kullanan ABH epidemiyoloji çalışmalarının birçoğunda da kullanılmıştır.
Tablo 4. Tahmini Bazal Scr Değerleri [6]
Yaş (yıl) Zenci Erkekler mg/dl (µmol/L) Diğer erkekler mg/dl (µmol/L) Zenci kadınlar mg/dl (µmol/L) Diğer Kadınlar mg/dl (µmol/L) 20-25 1.5 (133) 1.3 (115) 1.2 (106) 1.0 (88) 25-29 1.5 (133) 1.2 (106) 1.1 (97) 1.0 (88) 30-39 1.4 (124) 1.2 (106) 1.1 (97) 0.9 (80) 40-54 1.3 (115) 1.1 (97) 1.0 (88) 0.9 (80) 55-65 1.3 (115) 1.1 (97) 1.0 (88) 0.8 (71) >65 1.2 (106) 1.0 (88) 0.9 (80) 0.8 (71)
Tahmini glomerüler filtrasyon oranı = 75 (ml/dk/1.73m2 )= 186 x (serum kreatinin [Scr]) – 1.154 x
(yaş) – 0.203 x (0.742 kadın ise) x (1.210 zenci ise) = exp(5.228 – 1.154 x In[Scr]) – 0.203 x In(yaş) –
(0.299 kadın ise) + (0.192 zenci ise)
Tablo 4’te çeşitli yaş, cinsiyet ve ırk kategorileri için geriye dönük hesaplamalarla elde edilmiş tahmini SCr aralıkları gösterilmektedir. Bazal SCr değerinin bilinmediği durumlarda tahmini SCr değeri kullanılabilir ancak KBY varlığında kullanılması yanıltıcı olabilir. Genellikle KBY varlığında bazal bir SCr değeri vardır. Ancak ne yazık ki birçok KBY vakasına tanı konulmamıştır ve bu nedenle gerçekte tanısı belirlenememiş KBY olan bir hastanın bazal SCr değerinin tahmin edilmesi ABH olarak fişlenme riski oluşturabilir. Ayrıca KBY ve ABH birlikte bulunabilir. Eldeki tüm klinik verileri kullanarak (laboratuvar, görüntüleme, hikaye ve fizik muayene) hem kesin bir tanıya hem de kesin bir tahmini bazal SCr değerine ulaşmak mümkün olabilir. Hastane yatışı sırasında elde edilen en küçük tahmini SCr değeri genellikle bazale eşit veya daha büyüktür (masif sıvı resütasyonuna sekonder hemodilüsyon izlenen vakalar dışında). Bu SCr değeri ABH tanısı ve evrelemesi için kullanılmalıdır.
2.1.11. Klinik değerlendirme
Tanımlama ve sınıflama sistemleri tartışılırken ABH’nın klinik tanısı için bir taslak sağlanmıştır. Burada bahsedilenlerden klinik muhakemeyi tamamen kullanma veya hariç tutma gibi bir sonuç çıkarılmamalıdır. Vakaların büyük kısmı hem ABH tanı kriterlerine hem de klinik muhakememize uysa da ABH’lı her vaka önerilen tanımlamaya uymaz. Ancak istisnalar çok nadirdir.
2.1.11.1. Psödo ABH
Laboratuvar testleriyle tanı koyulan diğer hastalıklar gibi (örn: Hiponatremi), laboratuvar verileri yorumlanırken dikkatli olunmalıdır. En önemli örnek laboratuvar hatalarıdır. Hatalı laboratuvar değerleri hastalık tanısında kullanılmamalı ve şüpheli laboratuvar sonuçları tekrar çalışılmalıdır. Diğer bir örnek de farklı laboratuvarlardan elde edilen farklı SCr ölçümleridir. ABH tanımında SCr için en az iki ölçüm gerekmektedir. Gelecekte SCr ölçümünün uluslararası standardizasyonu ile laboratuvarlar arası fark nedeniyle oluşan varyasyonlar elimine edilebilecektir. Farklı laboratuvarlardan gelen değerleri yorumlarken dikkatli olunmalıdır. Ayrıca diyet ve aktiviteye göre SCr’de %10’a varan oranda günlük değişimler olabilir. Endojen kromojenler (örn: Bilirubin, askorbik asit, ürik asit), egzojen kromojenler ve ilaçlar da (örn: Sefalosporinler, trimetoprim) kreatinin ölçümünde hatalara neden olabilir. İdrar çıkışı için de benzer bir problem mevcuttur. Özellikle sondası olmayan hastalar ve YBÜ dışında takip edilen hastaların idrar çıkış miktarları genelde kayıt altına alınmaz veya hatalı kayıtlar olabilir. Kilo bazlı kriterler obez hastalarda hiçbir böbrek anormalliği olmamasına rağmen ABH tanısı koydurabilir.
2.1.11.2. Atipik ABH
Tanı alamayan ABH olguları da ayrı bir problem olarak karşımıza çıkmaktadır. Örneğin, bir hastada büyük miktarlarda intravasküler sıvı uygulaması sonrası SCr yanlış olarak düşük saptanabilir [39]. Benzer olarak, masif kan transfüzyonu yapıldığı durumlarda SCr değeri hastanın böbrek fonksiyonlarını yansıtmaktan çok donörünkini yansıtıyor olabilir. Bu olgularda oligüri de beklenen bir sonuç değildir. Bu nedenle birçok hasta aslında kendi
resusitasyonu veya transfüzyonu ile SCr’de yanıltıcı düşüşlerin olacağı konusunda dikkatli olmalıdır, bu durumlarda normal değerler ABH’yı dışlatmaz. Kreatinin üretimindeki değişimler iyi bilindiği üzere kas yıkımınında artışa neden olan ve kaslarda zayıflık ile giden hastalıklarda görülebilir. Kreatinin üretimi ayrıca sepsiste azalmış kas perfüzyonuna bağlı azalmış olabilir.
2.2. Yoğun bakım hastalarında akut böbrek hasarlanması
ABH, ciddi hastalığa sahip hastalarda yaygın bir bulgu olup yoğun bakıma kabulün sık nedenlerinden biridir. Gerek böbrek fonksiyonlarının ileri dönemde kaybı, gerekse altta yatan hastalıkların gidişatını kötü etkilemesi nedeniyle önem arz etmektedir. Hastalığın ciddiyetini de yansıtabilir, bilinmeyen bağımsız bir risk faktörü de olabilir. ABH sonrası, serum kreatinin ölçümleriyle normal renal fonksiyonlarına kavuşmuş görünen hastalarda bile ileriki dönemlerde SDBY gelişme riski oldukça artmıştır [40]. Bu hastalarda serum kreatinin değerleriyle saptanamayacak renal fonksiyon kayıpları olabilir [41]. ABH’li hastalarda %4-6 oranında diyaliz gerektiren (D-ABH) görülür [42, 30]. Ayrıca hastaların karakteristikleri ve ilişkili organ disfonksiyonuna bağlı olarak %25 ile %90 arasında değişen mortalite oranları ile bağlantısı vardır [43].
SDBY (kronik diyaliz veya renal transplantasyon gerektiren) maliyetlerde ciddi bir artış ve yaşam kalitesinde azalma yaratır [44]. D-ABH, SDBY için önemli bir risk faktörüdür [38, 45]. YBÜ hastalarında ABH’ye bağlı SDBY gelişimi; uzun dönemde nadiren kalıcı olmaktadır. Bu durum özellikle D-ABH epizodu sonrası renal fonksiyonlarında yeterli iyileşme olanlarda geçerlidir [46].
Yakın zamanda yapılmış, geniş popülasyona sahip uluslararası bir kohortta D-ABH ve YBÜ’de yatan diğer hastalarının kısa ve uzun dönemde SDBY gelişme riski kıyaslanmıştır. YBÜ taburculuğu sonrası 90 gün hayatta kalan 107.973 hastanın %2.8’i YBÜ takipleri esnasında D-ABH geliştirmiştir. D-ABH nedeniyle YBÜ’ne kabulden itibaren 90 gün sağ kalan hastaların 10’da birinden fazlasında 5 yıllık takipte SDBY gelişmiştir, diğer YBÜ hastalarında bu oran 200’de birden azdır. Bu nedenle YBÜ hastalarında, D-ABH epizodu YBÜ’ne yatıştan itibaren 5 yıllık dönemde SDBY gelişmesi için önemli bir risk faktörüdür. Diğer YBÜ hastaları ile kıyaslama yapıldığında bu risk aşikardır; gruplar arasında rölatif riskin en yüksek olduğu
hasta grubu kronik böbrek hastalığı olmayan genç hastalardır. Kronik böbrek hastalığı olan hastalarda D-ABH’den bağımsız olarak artmış SDBY gelişme riski vardır [46].
İsveç’te yapılmış bir çalışmada YBÜ’deki D-ABH’li hastalarda SDBY’nin kısa
vadede riski %9.4 iken 90 gün–7 yıl periyodunda % 3.4 olarak bulunmuştur [47]. Yine literatürden diyaliz tedavi yoğunluğunun araştırıldığı randomize bir denemede daha düşük oranlar tahmin edilmiştir. D-ABH hastalarının %5.6’sının akut diyaliz sonrası 90 günlük dönemde hala diyalize bağımlı olduğu gösterilmiştir [48]. Akut diyaliz gerektiren ancak renal fonksiyonlardaki düzelme nedeniyle diyalize devam edilmeyen hastalarda da artmış SDBY riskinin gösterildiği bir Kanada ve ABD çalışmasının sonuçları da benzerdir [38, 45]. Ayrıca küçük gruplar içeren birkaç çalışmada da hastaların %4.2 - %28.9’u akut diyaliz sonrası 90-180. günlerde hala diyalize bağlı olarak saptanmıştır [49-54]. Bu büyük varyasyon YBÜ popülasyonundaki ve bazal renal fonksiyonlardaki farklılıklar ile açıklanabilir.
YBÜ hastaları arasında D-ABH kısa ve uzun vadede SDBY gelişmesi için önemli bir risk faktörüdür. Bu nedenle YBÜ’deki D-ABH gelişen hastalarda taburculuk sonrası sistematik bir hasta takibi uygulanmalıdır ve profilaktik stratejiler geliştirilmelidir [46].
ABH, SDBY ve normal renal fonksiyona sahip hastaların yoğun bakım mortalitelerini değerlendiren bir çalışmada ABH ve SDBY hastalarındaki benzer hastalık yaygınlık skorlarının aksine; RRT gereksinimi duyulan ABH hastalarındaki mortalite oranları kronik diyaliz hastalarınınkinden beş kat, normal renal fonksiyonlara sahip hastalarınkinden ise on kat fazla saptanmıştır [55]. Başka bir çalışmada yine benzer olarak; RRT gerektiren ABH’lı hastalarda SDBY hastalarına kıyasla yaş, hastalıklarının yaygınlık derecesi ve organ disfonksiyon sayılarının eşit olduğu durumlarda, yoğun bakım ve hastane mortalite oranlarının yaklaşık iki kat fazla olduğu bulunmuştur [56].
Kritik hastalığa sahip RRT tedavisi altındaki 1847 ABH hastası ve 797 yoğun bakım bağımlı SDBY hastasını karşılaştıran büyük bir retrospektif veri tabanı analizi sonucunda benzer sonuçlar alınmıştır. SDBY hastalarının yoğun bakım ve hastane mortaliteleri RRT tedavisi altındaki ABH hastalarının yaklaşık olarak yarısıdır. Beklenildiği gibi organ yetmezliği sayısı arttıkça her iki gruptaki yoğun bakım mortalite değerleri de artar. Ancak iki nonrenal organ yetmezliği görülen durumda mortalite artışı RRT tedavisi altındaki ABH hastalarında belirgin derecede daha yüksek bir orana sahiptir (%75’e kıyasla %25.6). ABH
hastalarında SDBY hastalarına kıyasla hem yoğun bakım hem de hastane kalış süreleri de belirgin derecede daha yüksektir [56-58].
İlginç olarak, SDBY nedeniyle ciddi hastalığı olanlar sıklıkla yoğun bakıma alınırlar
ve bu hastaların sonuçları normal renal fonksiyonu olanlardan daha kötü gibi görünse de, prognozları RRT gerektiren ABH hastalarından daha iyidir. ABH hastalarının YBÜ’lerindeki izlemde morbidite ve mortalitelerinin SDBY hastalarına oranla çok daha yüksek bulunması esas belirleyicinin böbrek fonksiyon kaybından ziyade altta yatan hastalığın komorbiditeleri ile primer olarak ilişkilidir [43].
Literatürdeki yayınların çoğu, RRT alması gereken ABH hastalarının yoğun bakım ve hastane sonuçlarının, kritik hastalığı olan kronik diyaliz hastalarınkine kıyasla belirgin derecede kötü olduğunu işaret etse de; iki küçük çalışmada tanı ve hastalık yaygınlık skorları uyuşan, sürekli RRT alan, ABH ve SDBY hastalarının yoğun bakım ve hastane/90 gün mortalite değerlerinin benzer olduğu rapor edilmiştir [59, 60].
ABH hastaları kronik diyaliz hastalarına kıyasla daha fazla mekanik ventilasyon ve vazopressör ilaç tedavisi almaya eğilimlidirler. Bu durum hastalık yaygınlık skorlarının eşit olduğu durumlarda ve ayrıca RRT modu açısından kontrol edildiğinde dahi aynı şekildedir [56, 58, 61]. Bu bulgular bu grubun mortalite oranlarının yüksek olma nedenini açıklayabilir.
2.3. Sistemik inflamasyon ve akut böbrek hasarlanması ilişkisi
Sepsis, gelişen tıbbi bilgilerimiz doğrultusunda patogenezinin daha iyi anlaşılmasına ve antimikrobiyal tedavi alanındaki ilerlemelere rağmen önemini koruyan, erken tanı koyulmadığı ve septik şok geliştiği takdirde mortal seyreden, abartılı inflamatuvar yanıt ile karakterize bir durumdur. Prognozu belirleyen en önemli faktörlerden biri multiple organ tutulumudur.
“Sistemik inflamatuar yanıt sendromu”; şu parametrelerden iki veya daha fazlasının bulunması halinde tanı koyulan klinik bir durumdur: Vücut ısısının 38 °C’nin üzerinde veya 36 °C’nin altında olması; Kalp hızının 90/dak’nın üzerinde olması; Solunum hızının 20/dak’in üzerinde veya arteryel karbondioksit basıncının 32 mmHg’nın altında olması; lökosit
%10’un üzerinde genç hücre olması. Bu bulgular enfeksiyona bağlı geliştiyse tabloya “sepsis” denir. Sıvı resüsitasyonuna rağmen hipotansiyon ve hipoperfüzyon mevcutsa “septik şok”, hemostaz dış müdahale olmadan sağlanamıyorsa da “multi organ yetmezlik sendromu” mevcuttur [62].
ABH etyolojisinde sepsis ve septik şok en önemli nedenler arasında kabul edilmektedir. Sepsis ve septik şokta prognozu belirleyen en önemli faktörlerden biri de ABH’dir. ABH genellikle multiple organ yetmezliğinin bir parçası olarak karşımıza çıkar. ABH patogenezinde renal hipoperfüzyon, iskemi, lokal ve sistemik mediyatörler, nötrofil endotel etkileşimleri ve mikrovasküler trombozlar suçlanmaktadır [63]. Sepsis ve şoktaki bir hastada renal fonksiyon bozukluğu kreatinin klirensine azalma, serum kreatininde yükselme, oligüri ile tanınır [64].
Sepsiste klinik tabloya genellikle akut tübüler nekroz; nadiren kortikal nekroz, glomerülonefrit veya interstisyel nefrit hakimdir. Septik ABY histolopatolojisi üzerine yapılan bir derlemede, hastaların %22’sinde akut tübüler nekroz saptandığı, ancak esas yaygın histopatolojik bulgunun spesifik olmayan tübülointerstisyel renal değişiklikler olduğu bildirilmiştir. Genel düşüncemizin aksine septik ABY histopatolojik bulgularının tamamen normal bulgular ile şiddetli ATN arasında değişebildiği ve ATN’nin sık olmadığı kanısına varılmıştır [65].
Sepsise sekonder gelişen akut böbrek yetmezliğinin daha iyi anlaşılabilmesi için sepsiste kan akımı, renal hemodinami, sistemik ve lokal mediyatörler ve bunların etkileri bilinmelidir [66]. (Şekil 2)
Şekil 2. Sepsiste akut renal yetmezliğe yol açan mekanizmalar [63]
2.3.1. Sepsiste ve septik şokta renal hemodinamik değişiklikler ve sistemik mediatörler
Organizma ciddi bir enfeksiyona endojen mediyatörler aracılığı ile yanıt verir. Başlıcaları kompleman sistemi, serbest oksijen radikalleri, eikozanoidler, sitokinler, plazminojen aktivatör faktör, vazoaktif moleküller, koagülasyon sistemi ve fibrinolitik sistemdir. Sepsiste akut renal yetmezlik gelişimiyle ilgili hipotezlerde renal hipoperfüzyon, reperfüzyon hasarı, nötrofil endotel etkileşimleri, mikrovasküler trombozlar, lokal ve sistemik mediyatörler ile endotel hasarı üzerinde durulmaktadır [66, 67].
Deneysel çalışmaların çoğunda normal hemodinamiye rağmen azalmış GFR ve renal kan akımı saptanmıştır. Sepsiste sistemik vazodilatasyon olmasına, kardiyak outputtaki artışa rağmen selektif renal vazokonstrüksiyon mevcuttur [68]. Bazı çalışmalarda ise septik
durumda renal kan akımı azalmadan da böbrek yetmezliği tablosu gelişmiştir [69]. Gerçek renal plazma akımındaki artışa rağmen azalmış efektif akım anatomik veya fizyolojik şantları düşündürmektedir. Kortikal ve jukstamedüller vasküler şantlar kuramı ortaya atılmıştır [68]. Arter ve ven arasındaki kapalı bileşkelerin açılmasının da sorumlu olduğu iddia edilmiştir.
Endotoksemi ile salınan sitokinlerce arttırılan NO sentezi, arteriyel vazodilatasyon ve sistemik vasküler dirençte azalmaya neden olur. Baroreseptörler tarafından santral sinir sistemi uyarılması gerçekleşir ve renin anjiotensin aldosteron sistemi aktive olur. Artmış kalp debisine rağmen gelişen renal vazokonstriksiyon, azalmış plazma akımı ve filtrasyon fraksiyonu sonucu ABY’ye zemin hazırlanır [63, 70]. Endotoksemi renal hipoperfüzyondan bağımsız olarak enerji metabolizmasını da bozmaktadır [68, 71].
Sepsiste norepinefrin, anjiyotensin II ve vazopressin seviyeleri artar. Yüksek anjiyotensin II seviyeleri postglomerüler vazokonstriksiyon, filtrasyon fraksiyonunda artış, mezangial hücre kontraksiyonu, sempatik sistem aktivasyonu ve intrarenal vazodilatör prostoglandinlerde artış gibi etkilerle patogeneze katkıda bulunur [66].
Temelde afferent arteriolar direncin etkilendiği, efferent arteriolar direncin aynı kaldığı, glomerüler hidrostatik direncin arttığı gösterilmiştir. Hiperdinamik sepsis modelinde ise preglomerüler vazokonstriksiyon olduğu ve efferent arteriolde değişiklik olmadığı görülmüştür.
Sepsis poliürisi önemli bir sıvı kaybı nedenidir [72]. Sepsis poliürisi, renal yetmezliğin poliürik evresinden farklıdır. Sepsis poliürisi dört mekanizma ile açıklanmaya çalışılmıştır: 1-Azalmış tübüler onkotik basınç [73], 2-Laktik asidoz ve sepsise bağlı yan ürünlere sekonder artan ozmotik aktivite ve diürez [74], 3-Olası diyabet insipit modeli (sepsis poliürisinin zaman zaman ADH’ya yanıt vermesi) [75], 4-Aldosteron reseptör blokajının da poliüriyi etkilemesi belirleyicidir [76].
Böbrekten salınan vazodilatatör ve vazokonstrüktör ajanlar arasındaki bu dengesizlik intrarenal vazokonstrüksiyon lehine işler; glomerüler perfüzyon, filtrasyon hızı ve yüzeyi azalır. Sistemik hipotansiyon ve intrarenal vazokonstrüksiyona bağlı olarak sepsisin erken döneminde prerenal ABY tabloya hakimken tablo ilerledikçe uzun süreli renal iskemiye bağlı tübüler hücre hasarı ve akut tübüler nekroz meydana gelir [63].
Lokal mediatörler
1-Sitokinler (TNF, IL-1, IL-2, IL-6, IL-8, IL-13, MCP-1)
Sitokinlere bağlı hasara böbreklerin çok duyarlı olduğu düşünülmektedir. Sitokinler, glomerül kapillerlerinde nötrofil agregasyonu ve toksik madde salınımını arttırır, mezangial hücrelerden reaktif oksijen metabolitleri açığa çıkmasına sebep olurlar. Renal plazminogen aktivatör inhibitörü salgılatarak fibrinolizi engellerler. Deneysel endotoksemi modellerinde renal yapılarda granülosit artışı saptanır. Granülositlerden salgılanan proteazlar, oksijen serbest radikalleri ve vazoaktif maddeler bölgesel renal iskemi ve hasar gelişiminde önemli faktörlerdir [77].
Glomerül endotel ve mezangial hücrelerde PAF, endotelin1, adenozin gibi vazokonstriktör ve nitrik oksid (NO), PGE2 gibi vazodilatör maddelerin sentezlerini arttırırlar. Hayvan modellerinde önemli renal hasar yaptıkları ve TNF alfa’nın direk olarak endotel mezangial hücre hasarı yaptığı gösterilmiştir [78]. Endotoksinler glomeruler mezenkimal hücrelerden TNF salınımını uyarırlar [79]. TNF alfa nötralizasyonu, lipopolisakkarit ilişkili böbrek yetmezliği gelişimini önleyebilmektedir [80]. TNF ve sepsis ilişkili ABY arasındaki bu bağlantının ortaya konması sepsis sırasındaki böbrek hasarından, toksik immünolojik mekanizmaların, hemodinamik faktörlerden daha önemli rol oynadığını düşündürmektedir.
2-Adezyon molekülleri
Sepsiste adezyon molekülleri; sitokinler, trombosit aktive edici faktör, komplemanlar, oksijen radikalleri gibi maddelerce düzenlenmektedir. Adezyon molekülü monoklonal antikorlarının, deneysel çalışmalarda ABY için protektif olduğu gözlenmiştir [81].
3-Serbest oksijen radikalleri
Prostoglandin ve nitrik oksit metabolizmasını etkileyerek renal vazokonstrüksiyona neden olurlar [68].
4- Tromboksan A2 (TxA2)
Endotoksin, anjiyotensin II, vazopressin, IL-1, PAF ve serbest oksijen radikalleri TxA2 sentezini artırır. Hayvan çalışmalarında TxA2 infüzyonunun renal kan akımını azalttığı, afferent arteriol vazokonstriksiyonu yaptığı, filtrasyon fraksiyonunu azalttığı gösterilmiştir. Ayrıca trombosit agregasyonu ve trombozlardan sorumludur [77].
5-PGF2a benzeri maddeler:
Serbest oksijen radikalleri üzerinden selektif renal vazokonstriksiyon yaparlar ve sepsiste renal fonksiyon bozukluğuna katkıda bulunurlar [77].
6-PGE2, PGI2:
Endotoksinlerce PGE2 ve PGI2’nin renal üretimi arttırılır, iç korteks ve medullaya giden kan akımı artar. Kan akımının düzenlenmesinde koruyucu etkileri olduğu görülmüştür [68, 82].
7-Lökotrienler
Lökotrienlerin efferent arteriolde vazokonstriksiyon, glomerüler filtrasyon hızında azalma, renal kan akımında azalma ve mezangial hücre kontraksiyonu etkileri saptanmıştır. Lökotrien antagonistlerinin böbrekte iskemik hasarı azalttığı bildirilmiştir [68, 83].
8-Trombosit aktive edici faktör (PAF)
PAF salınımı endotoksinlerce uyarılır. Vazokonstriktör bir maddedir ve kemotaksis, nötrofil aktivasyonu, intravaskuler koagulasyona katılır. PAF inhibitörlerinin hayvan modellerinde renal fonksiyonlarda düzelme sağladığı görülmüştür [68, 84].
9-Endotelin-1
Endotelinin salınımı; TNF, endotoksin, vazopressin, anjiyotensin II tarafından uyarılır. Renal arterioller endotelin-1’in vazokonstriktör etkisine duyarlıdır. Hem afferent hem de efferent arteriolde siddetli vazokonstriksiyona yol açar. Renal kan akımını ve filtrasyon fraksiyonunu azaltır. PAF’ın mezangial üretimini ve TxA2’nin endotelden salınımını arttırır. Reaktif bir şekilde PGE2, NO, PGI2 seviyelerinde de artışa sebep olur. Antiendotelin-1 monoklonal antikorlar endotoksine bağlı GFR azalmasını kısmen bloke eder [77, 85].
10-Nitrik oksit (NO):
Uyarılabilir NO-sentaz (iNOS) ile NO aşırı üretiminin sepsisteki sistemik vazodilatasyondan sorumlu major mekanizma olduğu düşünülmektedir. Endotelde, vasküler kas hücresinde, makrofajda, mezangial hücrede iNOS aktivitesi saptanmıştır. iNOS; endotoksin, TNF, IL-1 ile uyarılır. Ayrıca aktive nötrofillerin kendileri de bir NO kaynağıdır. Lokal NO üretimi renal kan akımı düzenlenmesinde önemli bir mediyatördür. Preglomerüler
hücre ilişkilerini bloke eder ve böylece trombosit agregasyonunu ve oksidan salınımını engeller. Hayvan modellerinde NO inhibisyonunun; proteinüride artış, GFR’de azalma ve glomerüler tromboza sebep olduğu gösterilmiştir [77, 86].
11-Adenozin
İskemide endotel ve mezangial hücre hasarı sırasında yüksek enerjili fosfatların yıkımı
ile ortaya çıkan kuvvetli bir vazokonstriktördür. Reaktif oksijen metabolitlerini bloke eder. TNF'nin mezangial hücrede adenozin salınımını artırdığı gösterilmiştir [68, 86].
12-Lazaroid, Pentoksifilin
Sepsiste renovasküler dirençte araşidonik asit metabolizmasından kaynaklanan bir artış vardır. Pentoksifilin ve U74389G (antioksidan özellikli bir madde) gibi maddelerin araşidonik asit metabolizmasını düzenleyerek sepsiste koruyucu etkilerinin olabileceği gösterilmiştir [77, 87].
13-Monosit kemoatrektan proteini (MCP-1)
Sepsiste sitokin üretiminin düzenlenmesinde, endojen monosit kemoatrektan proteininin de organizmayı koruyucu yeri vardır [68, 88].
14-Vazoaktif intestinal polipeptid (VIP)
Sepsiste protektif ve sağkalımı arttırıcı etkileri vardır. Mast hücre reaktivitesini önleyerek septik şokta tedavi amaçlı kullanılabileceği düşünülmektedir [68, 89].
15-IL-13
Sepsisteki sitokinlerin salınımını ve üretimini azaltarak koruyucu rol oynadığı hayvan deneylerinde gösterilmiştir [67].
16-Komplemanlar
C3a ve C5a vasküler geçirgenliği arttırır, lökosit PAF sentezini arttırır. C5a ve C5b lökositlerin endotele adezyonunu aktive eder [90].
Sonuç olarak; sepsiste otoregülasyon mekanizmalarının bozulması (sistemik kan basıncı 60 mmHg altına düşmediği sürece böbrek otoregülatuvar mekanizmalarla filtrasyon basıncını ayarlar), sitokinler, tromboz ve kanama, vazodilatasyon ve vazokonstrüksiyon, oksidasyon ve redüksiyon, katabolik ve anabolik aktivite arasındaki dengesizlik ve enzim
aktivitelerindeki düzensizlik tam olarak aydınlatılmamış mekanizmalarla organ fonksiyon bozukluğuna yol açar, böbrek fonksiyon kaybı gelişir [63].
Sepsis-akut böbrek hasarlanması ilişkini irdeleyen çalışmaların sayısı arttıkça patogenezi hakkındaki bilgilerimiz daha da netlik kazanacaktır. Mortalitesi yüksek bir sorunun tedavi olanaklarının geliştirilmesi sağlanacaktır.
2.4. Klinikte nötrofil-trombosit lenfosit oranı ve inflamasyon ilişkisi
Son zamanlarda inflamasyondaki akut durumu yansıtan nötrofil yüksekliğini ve akut fizyolojik stresle gelişen lenfopeniyi yansıtan bir orandan sıkça bahsedilmeye başlanmıştır. Nötrofil ve lenfositin oranı (NLO) ile elde edilen bu indeks, çalışmalarda diğer inflamatuvar belirteçler ile birlikte değerlendirilip inflamatuvar durum hakkında diğer belirteçlerle korele bulunmuştur [91]. NLO rutin tam kan sayımı üzerinden hesaplanabilen bir parametre
olduğundan ucuz, günlük kullanımı kolay bir parametredir.
Yüksek nötrofil sayısının inflamasyon, düşük lenfosit sayısının genel sağlıktaki kötü durumunun ve fizyolojik stresin bir göstergesi olduğu bilinmektedir [91].
Dolaşımdaki lökositlerin strese karşı verdikleri fizyolojik yanıt nötrofil sayısında artış ve lenfosit sayısında bir düşüşe neden olduğundan bu iki alt grubun birbirine oranı bir inflamasyon belirteci olarak kullanılmaktadır [92-94].
NLO’nun birçok klinik durumda, sağkalım tahmininde yararlı olduğunu gösteren kanıtlar gün geçtikçe çoğalmaktadır. NLO toplumdan kazanılmış enfeksiyonu olan hastalarda bakteriyemi gelişiminin tahmin edilmesinde kullanılabilir. Bir çalışmada appendisit
şüphesinde artmış nötrofil lenfosit oranının, artmış beyaz küre sayısından daha duyarlı olduğu
gösterilmiştir [95, 96].
İnflamatuvar yanıt sırasında dolaşımdaki lökositlerin oranlarında değişiklikler olur.
Nötrofiliye relatif lenfopeni eşlik eder. Nötrofil/lenfosit oranı inflamatuvar yanıtın basit bir belirteci olarak öne sürülmektedir. APACHE 2 (Acute Physiology and Chronic Health Evaluation II) ve SOFA (Sepsis-related Organ Failure Assessment) gibi sepsis skorlarıyla değerlendirildiğinde bu oran hastalığın şiddeti ve prognozuyla uyumlu bulunmuştur ve “nötrofil
hastalarda da kötü prognozun bir göstergesi olduğu saptanmıştır. NLO’daki yükselmeyle birlikte akut koroner sendromlarda mortalite oranının arttığı gösterilmiştir [95, 97].
Nötrofili, akut miyokard infarktüsü ile başvuran hastalarda akut dekompanze kalp yetmezliği ile ilişkili olup buna ek olarak rölatif lenfopeninin kalp yetmezliğinde mortalite için bağımsız bir öngördürücü olduğu gösterilmiştir. Bir tümörde T lenfositlerin bulunması lezyona karşı belirgin bir immün yanıtın göstergesidir. Yeni veriler bir kolorektal tümörde düşük lenfosit sayısının kötü prognozla ilişkili olduğunu göstermektedir. NLO’nun, kolorektal ve over kanserlerinde survey üzerine prognostik bir faktör olduğu gösterilmiştir [98, 99]. Preoperatif NLO’nun kolorektal kanserde kötü prognozlu hastaların belirlenmesinde kullanılacak basit bir yöntem olabileceği öne sürülmüştür [100].
Trombositler de; endotelyal hücreler, dendritik hücreler, T lenfositler, nötrofiller ve mononükleer fagositlerin de olduğu birçok hücre grubu ile etkileşim halindedir. Son çalışmalarda bu etkileşimin arter duvarında inflamasyonu başlattığı ve şiddetlendirdiği yönüne bulgular saptanmıştır [101]. Ayrıca trombositoz bazı kanserlerde düşük sağkalım için bağımsız bir risk faktörü olarak belirtilmiştir [102].
2.4.1. Kardiyovasküler hastalıklarda NLO:
Lökositler inflamasyonun temel hücrelerindendir. Kardiyovasküler hastalıklarda inflamatuvar sürecin rolü bilinmektedir, bu süreçte lökositler ve alt tipleri de istenmeyen
olaylardan sorumlu tutulmaktadır [103]. Birçok çalışmada lökosit sayısı ve tiplerinin
kardiyovasküler sonuçları önceden tahmin etmede önemli birer inflamatuvar markır olduğu, nötrofil/lenfosit oranının kardiyovasküler olay ve mortalite ile ilişkili olduğu gösterilmiştir [104-107].
KAH, AKS:
Ateroskleroz evrelerinde inflamatuvar sürecin önemli bir rol oynadığı bilinmektedir [108]. KAH’li hastalarda NLO’nun kardiyak olay ve mortaliteyi öngördürdüğü gösterilmiştir [109]. Akut koroner sendromda da stres ile ilişkili kortizol salınımına bağlı olduğu düşünülen göreceli lenfopeninin ise miyokart enfarktüsü geçiren hastalarda erken belirteçlerden biri olduğu, yüksek NLO’nun koroner ateroskleroz ilerlemesinin bağımsız bir öngördürücüsü olduğu daha önceki
çalışmalarda gösterilmiştir [110]. Lökosit sayısının akut miyokart enfarktüslü hastaların erken dönem mortalitesinin önemli bir prediktörü olduğu belirtilmiştir [103].
NLO perkütan koroner girişim geçiren ST yükselmeli miyokart enfarktüslü hastalarda,
erken dönem risk sınıflamasında önemli bir belirteçtir [111].NLO, ST yükselmeli miyokart
enfarktüslü hastaların uzun dönemde de kardiyovasküler olay riskinde artışla ilişkilidir [112]. Koroner ektazi:
Yapılan çalışmalarda anevrizma oluşumunda inflamasyonun rolü tespit edilmiş, koroner ektazilerin (KAE) patogenezinde de inflamasyon varlığı araştırılmıştır [113].
İnflamasyon belirteçlerinden C-reaktif protein (CRP), sitokinler ve adezyon molekülleri
KAE’li hastalarda sağlıklı bireylere göre daha yüksek bulunmuştur [114, 115]. İzole koroner arter ektazisi olan hastalar ile normal koroner arterleri olan olgular NLO açısından değerlendirilmiş, NLO’nun koroner arter ektazisi ile olan bağımsız ilişkisi gösterilmiştir. KAE’li hastalarda kontrol grubuna kıyasla NLO’da anlamlı oranda yükseklik saptanmıştır. Yüksek NLO koroner arter ektazisi varlığı ve ciddiyetiyle ilişkilidir [104].
2.4.2. Kanser NLO ilişkisi:
Kanser ve inflamasyon ilişkisi bir yüzyıl önce keşfedilmiştir. Bir dizi çalışmada NLO ve TLO’nun kanser hastalarının prognozu ile ilişkili olduğu belirtilmiştir [100, 116-119]. Yüksek NLO’nun bazı malign tümörlerde prognostik bir belirteç olduğu daha önce yapılan çalışmalarda belirtilmiştir. Kolorektal, gastrik, hepatoselüler, pankreas, böbrek, akciğer kanserlerinde mortalitenin güçlü bir prediktörüdür [120]. Preoperatif NLO hastanın inflamasyon durumu, klinik evresi ve surveyi hakkında önemli bilgiler sunmaktadır.
İnflamasyon ve yüksek NLO kötü prognozla ilişkili saptanmıştır [102].
Kolorektal kanser:
İmmun sistem, tümor kompleksi ile tetiklenen bir sistemdir. Yapılan çalışmalarda
düşük lenfosit sayısı ile kötü kolorektal kanser prognozu arasında ilişki saptanmıştır. NLO’nun preoperatif kolorektal kanser prognozunu gösteren kolay bir metod olduğu belirtilmiştir [100].
Gastrik kanser:
Gastrik adenokarsinomlu hastalarda preoperatif yüksek NLO tümör progresyonu ve kötü prognoz ile ilişkili saptanmıştır. Ayrıca trombositoz da gastrik adenokanser ve özefagus kanserinde düşük survey için bağımsız bir risk faktörüdür [102].
Küçük hücre dışı AC kanseri:
Artmış nötrofil sayısı küçük hücre dışı akciğer kanserinde de azalmış sağkalım için bağımsız bir risk faktörü olarak saptanmıştır [121].
Meme kanseri:
N/L oranının > 3.3 olması ve lenfopeni, meme kanserli hastalarda kısa-uzun dönem mortalitenin bağımsız bir prediktörüdür. Kanser rekürrensi ve postop mortaliteyle ilişkili güçlü bağımsız bir prognostik faktördür. Ayrıca tümör büyüklüğü ve hastanın yaşı ile ilgili de bilgiler sunmaktadır. Diğer lökosit parametreleri (nötrofil, lenfosit, lökosit sayıları) ile
kıyaslandığında bu konuda üstünlüğü gösterilmiştir [120].
Testis tümörü:
Testise sınırlı ve testis dışına yayılmış hastalarda bakılan N/L oranları arasında istatistiksel anlamlı bir fark saptanmamıştır [122].
Pankreas kanseri:
Pankreatik duktal adenokanser vakalarında preoperativ N/L oranı bir prognostik faktör olarak saptanmasına karşılık T/L oranında böyle bir ilişki saptanmamıştır [123].
2.4.3. Diğer hastalıklarda NLO:
Eroziv özofajit:
Yakın zamanda yapılan bir çalışmada, erozif özofajit ile erozif olmayan özefajit olgularında NLO karşılaştırılması yapılmış ancak gruplar arasında NLO açısından fark saptanmamıştır [124].
Fournier gangreni:
Yüksek NLO ve TLO’nun Fournier gangreni vakalarında hastalık prognozu hakkında güçlü parametreler olduğu saptanmıştır. Debridman sayısında artış, hastanede kalış süresinde uzama, maliyette artış ve artmış mortalite ile istatistiksel olarak anlamlı bir ilişki saptanmıştır [125].
Akut apendisit:
Mutlak lökosit sayısı her türlü enfeksiyonla birlikte artmaktadır. Apendisitte asıl etkenin bakteriler olduğu düşünüldüğünde, bakteriyel enfeksiyonlara duyarlılığı daha belirgin olan nötrofil sayısının mutlak lenfosit sayısına oranın apendisit tanısı açısından daha değerli bilgiler vereceği öngörülmüştür [126]. Literatürdeki çalışmaların sonuçları incelendiğinde NLO’nun diğer laboratuar tetkiklerine oranla daha değerli bilgiler verdiği görülmüştür. NLO’nun, apendisit tanısı için yüksek hassasiyete sahip bir tetkik olduğu gösterilmiştir [127]. Nonalkolik yağlı karaciğer hastalığı:
Nonalkolik karaciğer hastalığı inflamasyon ve artmış oksidatif stresle ilişkili bir hastalıktır. NLO da inflamatuvar olaylar ve fizyolojik stresle ilgili bilgiler sunan bir parametredir. Non alkolik steatohepatitte fibrozisi, ciddi histolojik hastalığı öngörmede yüksek NLO kullanılabilecek non invaziv bir markırdır. Basit steatozlu hastalara göre non alkolik steatohepatitte daha yüksek değerler gözlenmiştir [128].
SDBY:
SDBY hastalarında hsCRP, IL-6, TNFα, pentraksin gibi inflamasyon markırlarının serum seviyeleri yüksek seyreder [129-131]. NLO hem periton hem de hemodiyaliz hastalarında artmış inflamasyonla yakından ilişkilidir [132]. NLO SDBY hastalarında inflamasyonu gösteren potansiyel bir markırdır. Son çalışmalarda TLO ve NLO; TNFα, IL-6 gibi inflamasyon markırları ile pozitif korele saptanmıştır. TLO, SDBY hastalarında NLO ile kıyaslandığında inflamasyonu göstermede daha üstün saptanmıştır [133].


![Tablo 4. Tahmini Bazal Scr Değerleri [6]](https://thumb-eu.123doks.com/thumbv2/9libnet/3041206.2794/22.892.99.797.163.604/tablo-tahmini-bazal-scr-degerleri.webp)





