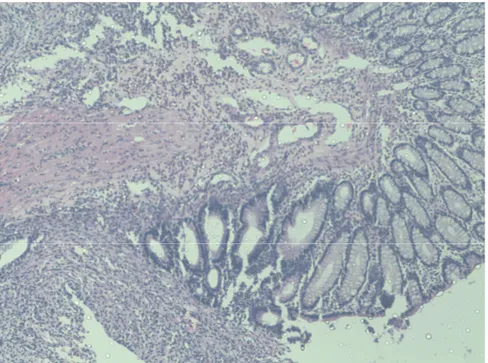
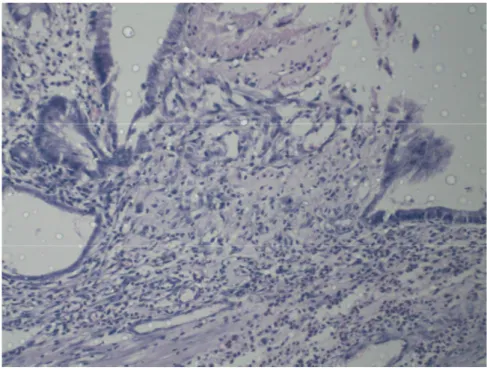
Deneysel kolon anastomoz modelinde, Ghrelinin anastomoz iyileşmesine etkisi
Tam metin
Şekil
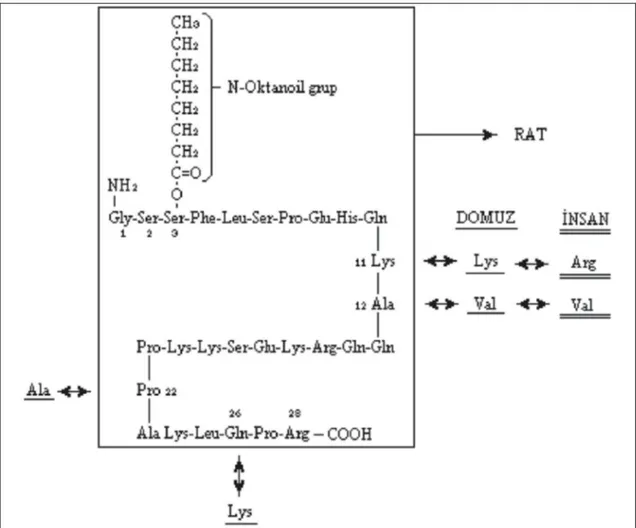
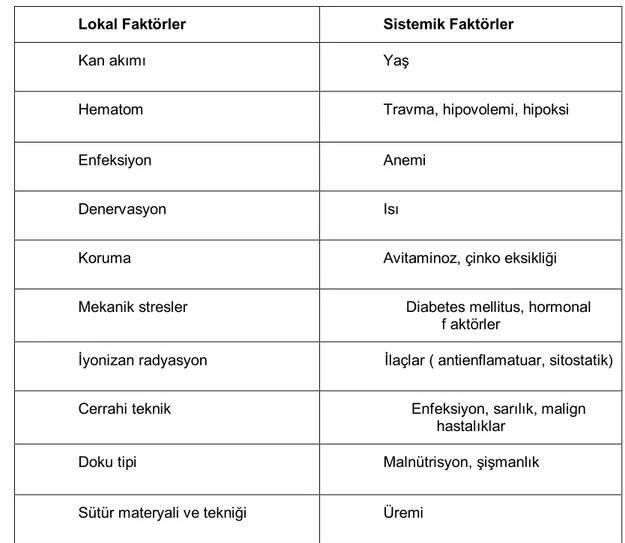
Outline
Benzer Belgeler
(12), uterus içi antibiyotik tedavisi yapılan kısraklarda yapılmayanlara göre; ilk tohumlamadaki gebelik oranlarının benzer, üreme sezonu sonrası gebelik oranlarının
Gazyağcı, Gazyağcı, Kılıç, Çelebi, Babür, Öcal ● Amasya İlinde Kanin Leishmaniasis / Canine Leishmaniasis in Amasya Province.. Kocatepe Vet J (2008) 1: 69-71
[6] Etekli (flanged) teknik olarak adlandırılan bu modifiye Bentall işleminde oluşturulan kompozit greftte mekanik kapak tübüler greftin alt ucundan 1 cm kadar
Daha önce yapılan çalışmalar da göz önüne alındığında, PA indeksi ameliyat öncesi düşük olan hastaların iki yönlü kavopulmoner anastomoz sonra- sı pulmoner kan
Bu çalýþmanýn amacý, sleeve lobektomi uyguladýðýmýz olgulardaki anastomoz tekniklerini, morbidite ve mortalite oranlarýný gözden geçirmektir.. Materyal
The key hypothesis of this study is that teachers are the primary stakeholders of schools and their awareness and participation in the management and accountability of sources
For Phase data generation, there are four components of the study element, namely qualitative approach, neo-narrative process, visual research methodology and object
2552 The beta CAPM results estimated in the model can be used to estimate Weighted Beta CAPM for the whole banking industry with the application of market value of each joint