T.C.
DĠCLE ÜNĠVERSĠTESĠ TIP FAKÜLTESĠ
ÇOCUK SAĞLIĞI VE HASTALIKLARI ANABĠLĠM DALI
KARBAMAZEPĠN VE VALPROĠK ASĠT ĠLE TEDAVĠ EDĠLEN EPĠLEPSĠLĠ ÇOCUKLARDA, SERUM LĠPĠDLERĠ VE KARACĠĞER
FONKSĠYON TESTLERĠNĠN ĠNCELENMESĠ
UZMANLIK TEZĠ
Dr.Nilüfer OKUR
TEZ DANIġMANI
Prof. Dr.Mehmet Ali TAġ
ĠÇĠNDEKĠLER
TEġEKKÜR 2 TABLOLAR DĠZĠNĠ 3 ġEKĠLLER VE GRAFĠKLER DĠZĠNĠ 4 SĠMGELER VE KISALTMALAR DĠZĠNĠ 5 GĠRĠġ VE AMAÇ 7 GENEL BĠLGĠLER 9 GEREÇ VE YÖNTEM 37 BULGULAR 40 TARTIġMA 46 SONUÇLAR VE ÖNERĠLER 55 ÖZET 57 ABSTRACT 59 KAYNAKLAR 61TEġEKKÜR
Uzmanlık eğitimim süresince bilgi ve tecrübelerinden yararlandığım değerli hocalarım; Anabilim Dalı BaĢkanımız Prof. Dr. M. Ali TAġ, Prof. Dr. Kenan HASPOLAT, Prof. Dr. Celal DEVECĠOĞLU, Prof. Dr. Aydın ECE, Prof. Dr. Murat SÖKER, Prof. Dr. M. Fuat GÜRKAN, Prof.Dr. Ahmet YARAMIġ, Doç. Dr. Mehmet BOġNAK, Doç. Dr. Mehmet KERVANCIOĞLU, Doç. Dr. Selahattin KATAR, Doç. Dr. Fatma ÇELĠK, Yrd. Doç. Dr. M. Nuri ÖZBEK, Yrd. Doç. Dr. Ayfer GÖZÜ PĠRĠNÇĠOĞLU, Yrd. Doç. Dr. Mustafa TAġKESEN, Yrd. Doç. Dr. Sultan MENTEġ ECER’e Ģükranlarımı sunarım.
Tez çalıĢmamın planlaması, yönlendirilmesi ve hazırlanmasında katkılarından dolayı tez hocam Prof. Dr. Mehmet Ali TaĢ ve tezimin istatistiksel olarak değerlendirilmesi aĢamasında bilgilerinden faydalandığım Prof. Dr. Yusuf Çelik’e en içten dileklerimle teĢekkür ederim.
Bunun yanında, tezimin yazım aĢamasında benden desteğini ve hoĢgörüsünü esirgemeyen sevgili eĢim Dr. Nurettin OKUR’a ve aileme, beĢ yıl boyunca mesai ve nöbetlerde pek çok Ģeyi paylaĢtığım diğer tüm doktor arkadaĢlarıma, ayrıca kliniğimizin hemĢire ve personellerine teĢekkür ederim.
Dr. Nilüfer OKUR Diyarbakır–2008
TABLOLAR DĠZĠNĠ
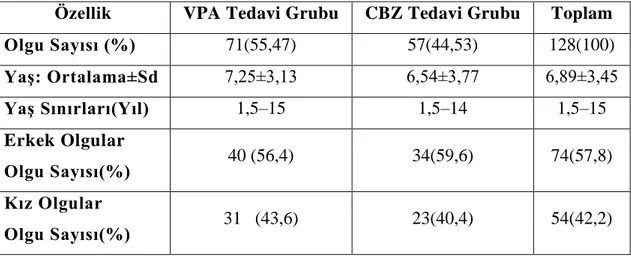
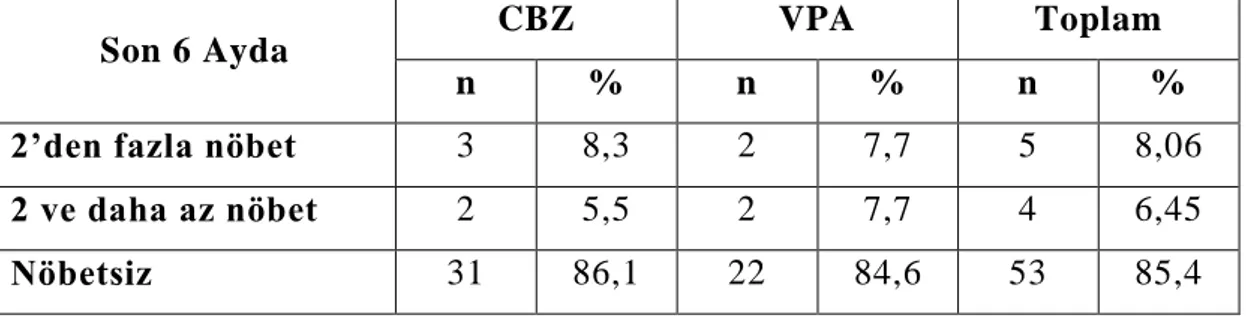
SAYFA Tablo–1 : Olguların, sayı, yaĢ ve cinsiyet dağılımları 40 Tablo–2 : Antiepileptik tedavi altında nöbet tekrar oranları 42 Tablo–3 : AEĠ kullanımı sonrası görülen yan etkiler 43 Tablo–4 :
VPA grubunda serum lipidlerinde tedavi süresine bağlı
değiĢiklikler 44
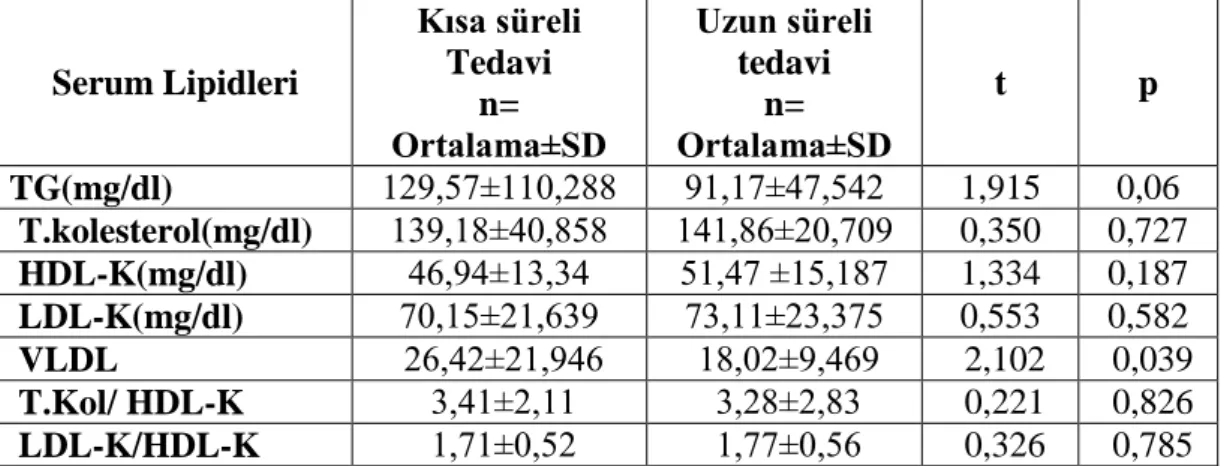
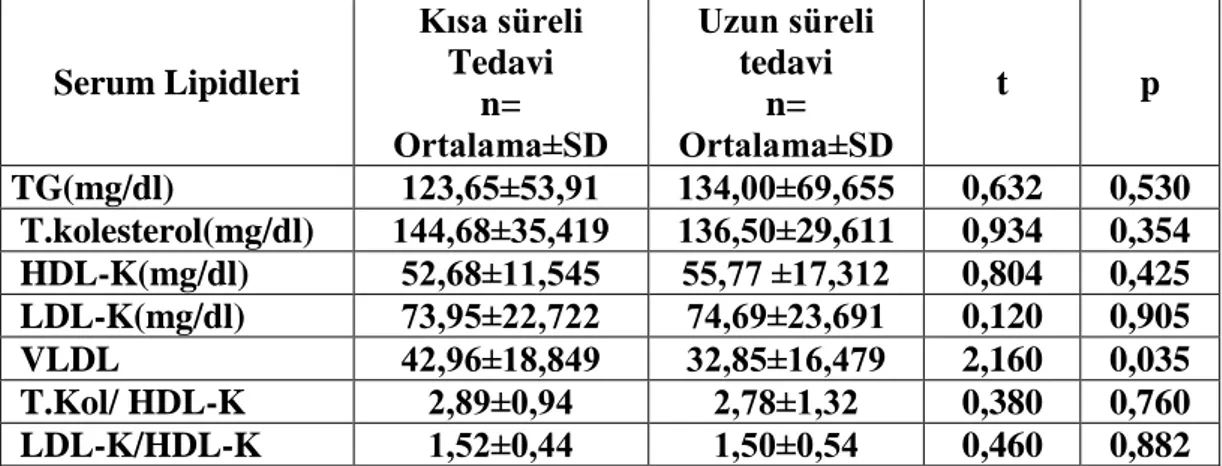
Tablo–5 : VPA tedavisi alan hastaların karaciğer fonksiyon testleri 44 Tablo–6 : CBZ grubunda serum lipidlerinde tedavi süresine bağlı değiĢiklikler 45 Tablo–7 : CBZ tedavisi alan hastaların karaciğer fonksiyon testleri 45
ġEKĠLLER DĠZĠNĠ
SAYFA ġekil –1 : Antiepileptik bir ilacın yutulmasından klinik etkilerinin
Kolesterol Biosentezi 18 ġekil –2 : Antiepileptik tedavi altında nöbet tekrar oranları 28
ġekil –3 : Lipoprotein Molekülü 29
ġekil –4 : Lipoprotein Metabolizması 34
KISALTMALAR
EEG :ElektroensefalogramILAE :Uluslararası Epilepsi Ġle SavaĢ Ligi GABA :Gama amino butirik asit
MSS :Merkezi sinir sistemi AEĠ :Antiepileptik Ġlaç PHT :Fenitoin
CBZ :Karbamazepin LTG :Lamotrijin
MSS :Merkezi Sinir Sistemi VPA :Valproik asit
PB :Fenobarbital GPT :Gabapentin PRM :Pirimidon LEV :Levetirasetam VGB :Vigabatrin FBM :Felbamat
SLE :Sistemik lupus eritematozus OXC :Okskarbazepin
GABA :Gama Amino Butirik Asit TPM :Topiramat
ASHK :Aterosklerotik kalp hastalıkları LCAT :Lesitin kolesterol açil transferaz VLDL :Çok düĢük dansiteli lipoprotein IDL :Orta dansiteli lipoprotein TG :Trigliserid
LP :Lipoprotein
LDL :DüĢük dansiteli lipoprotein ġM :ġilomikron
HDL :Yüksek dansiteli lipoprotein LPL :Lipoprotein lipaz
Apo :Apoprotein SYA :Serbest yağ asitleri FL :Fosfolipid
GGT :Gamaglutamil transaminaz ALP :Alkalen fosfataz
SGOT :Serum glutamik okzalo transaminaz SGPT :Serum glutamik piruvat transaminaz AST :Aspartat aminotransferaz
ALT :Alanin aminotransferaz PT :Protrombin zamanı
INR :Uluslararası normalleĢtirilmiĢ oran LGS :Lennox –Gastaut Sendromu
GĠRĠġ VE AMAÇ
Nöbet ve konvülziyon beyindeki anormal elektrik aktivite sonucu oluĢan motor hareket veya davranıĢta belli bir süreliğine oluĢan paroksizmal değiĢikliktir. Nöbetler pediatrik yaĢ grubunda sıktır ve çocukların yaklaĢık %10’unda görülür. Çocuklardaki nöbetlerin 1/3’ünden azı epilepsiye bağlıdır. Epilepside nöbetler beyinde tekrarlayarak tetiklenir. Epilepsinin kümülatif yaĢam boyu insidansı %3’tür ve vakaların yarısından fazlası çocukluk çağında baĢlar (1).
Ġlaç tedavisi nöbetli hastalığı olan çocukların çok büyük bir çoğunluğu için esas tedavi biçimidir (2). Çocukluk çağı epilepsilerinin tedavisinde ilk tercih edilen ilaçlardan biri valproik asit, diğeri de karbamazepindir. Altta yatan patolojiye bağlı olarak uzun yıllar, hatta bazen ömür boyu kullanmaları gereken bu ilaçlar büyüme – geliĢme dönemindeki çocuklarda uygulanırken daha da dikkatli izlem gerektirir. Çünkü kullanmakta olduğumuz antiepileptik ilaçlar birçok endojen maddede olduğu gibi karaciğerde metabolize edilirler ve karbamazepin, fenobarbital, difenilhidantoin gibi bazı antiepileptik ilaçlar aynı zamanda karaciğerde enzim aktivasyonu yaparlar. Karbamazepin de enzim aktivasyonu yaparak baĢta kendi metabolizması olmak üzere karaciğerde safra asitleri, kolesterol, lipidler, bilirubinler, glukokortikoid hormonlar, D ve K vitamini gibi bu enzimlerle aktive olan pek çok endojen maddenin metabolizmasını etkiler (3).
Ateroskleroza bağlı kalp hastalıkları, ABD baĢta olmak üzere pek çok ülkede ölüm nedenlerinin baĢında gelmektedir. Aterosklerozun artık hayatın ilk yıllarından itibaren baĢladığı bilinmektedir. Aterosklerozu hazırlayan birtakım risk faktörleri ortaya konmuĢ, bunlardan kaçınmanın ateroskleroz insidansını azalttığı çeĢitli çalıĢmalarda bildirilmiĢtir. Bu risk faktörlerinden en önemlilerinden birisi hiperlipidemilerdir (4).
Antiepileptik ilaçların serum lipid ve lipoprotein seviyelerini yükselttiği birçok araĢtırmacı tarafından saptanmıĢtır (5.6.7.8.9.10.11.12). Fakat bu ilaçların HDL-K’de artıĢ yaparak aterosklerotik kalp hastalıklarında koruyucu bir faktör olarak rol oynayabileceğini belirten raporlar da vardır (13,14).
Bu çalıĢma ile çocukluk çağı epilepsilerinde ilk seçenek olarak yaygın ve uzun süre kullanılan antiepileptik ajanlardan karbamazepin ve valproik asidin ;serum lipidleri ve karaciğer fonksiyonları üzerine etkilerini ve ateroskleroz üzerinde predispozan bir faktör olup olmadığını saptamak istedik.
GENEL BĠLGĠLER
EPĠLEPSĠLER GiriĢ:
Epilepsi terimi, ortak özelliği yalnızca, epileptik nöbetler olarak bilinen paroksismal olayların ortaya çıkmasına yatkınlık Ģeklindeki birçok duruma, kabaca uygun düĢer. Epilepsi sözcüğü yunanca tutmak yakalamak anlamına gelen kelimeden türetilmiĢtir. Sözcüğün iki anlamı vardır: Bir yandan eski çağların görüĢleri olan, tanrılar ve cinlerin neden olduğu, nöbetler ve ataklarla görülen hastalıkları iĢaret etmektedir (15). Diğer taraftan yakalamak kelimesinin epilepsi hastaları için objektif olarak haklı bir yönü de vardır; çünkü ataklar aniden oluĢur, karĢı konulamazlar ve hastanın nöbetten ve bunun sonuçlarından kaçınma Ģansı yoktur (15).
Epilepsi tarihçesi M.Ö. 2080 yılındaki Asurlular, Ġbraniler, Babiller dönemine ait epileptik kiĢilerle ilgili sosyal yaĢamı düzenleyen kayıtlara dayanır. Ġlk mantığa dayalı değerlendirmeler ünlü hekimler Hipokrat ve Galeneus dönemine aittir. Ġlk kez 1857’de bromid tedavi amacıyla kullanılmaya baĢlanmıĢ, ancak yan etkileri nedeniyle daha sonra bırakılmıĢtır. 19. yüzyıl sonlarında H.Jackson ve William Gowers tanı ve tedavi konusunda modern bir çığır açmıĢlardır (16).
Tanımlamalar:
Epilepsi terimi, sadece spesifik nörofizyolojik bir mekanizmaya bağlanabilen özel tipteki ataklar için uygundur. Beyin fonksiyonlarını etkileyen epizodik ataklarla karakterize her hastalık epilepsi değildir. Jackson’un klasik tanımlamasına göre; ''epilepsi, gri maddenin, zaman zaman ortaya çıkan, ani, aĢırı, hızlı ve lokal boĢalımlarının adıdır''.
Epileptik nöbetler ya da ataklar, az ya da çok yaygın bir grup serebral nöronun anormal aĢırı aktivitesi sonucu ortaya çıkan geçici klinik olaylardır. Epileptik nöbetler genelde kısadır, birkaç saniye veya dakika sürerler; tamamen motor ve diğer beyin fonksiyonlarının da etkilenebildiği davranıĢ görüntülerinin aniden ortaya çıkıĢı ile dikkati çekerler. Epileptik nöbetin kökenindeki anormal ve aĢırı nöronal aktivite, hem atağı meydana getiren klinik olaylar ve hem de klinik
nöbetlerle aynı anda çekilen elektroensefalogramdan (EEG) oluĢur. Tüm olgularda, epileptik nöbet bir ya da daha çok beyin fonksiyonunun paroksismal düzensizliği ile sonuçlanır. Bu ataklar, EEG aktivitesinde, ister yaygın, isterse lokalize olsun geçici paroksizmal değiĢiklikler olarak tanımlanan epileptik deĢarjı oluĢtururlar. EEG kaydı Jackson tarafından ileri sürülen anormal, aĢırı nöronal aktivitenin en kesin kanıtıdır. Epileptik deĢarjın ana özellikleri yüksek amplitüdlü ve ritmik olmasıdır (15). Epileptik deĢarj, birden fazla, değiĢik nöronal kaynaktan oluĢan bir ağdan doğan inhibitör ve eksitatör uyarıların etkileĢimi sonucunda meydana gelen kompleks bir fenomendir (17).
Çocukluk Çağı Epilepsilerine YaĢın Etkisi:
Çocuklarda yaĢ, büyüme ve geliĢme faktörleri sadece epilepsinin geliĢip geliĢmemesini belirleme konusunda değil, nöbetlerin klinik ve elektriksel görünümleri ve hangi tip nöbet hastalıkları ile karĢılaĢılabileceği konusunda da birinci dereceden önemlidir. Herkes tarafından kabul görmese de, genel olarak hastalığın prognozunu belirlemede en önemli faktör olarak kabul edilir. YaĢın status epileptikusun sonucu üzerine de etkisi vardır. Ġki-üç yaĢından küçük çocuklarda sekeller daha büyüklere göre sıktır. Antiepileptik ilacın emilmesi, proteine bağlanması, klirensi ve zahiri yarı ömrü yaĢamın farklı dönemlerinde değiĢir. Genellikle yenidoğan döneminde antikonvülzanların metabolizması yavaĢtır ve bebeklerde kolaylıkla intoksikasyon oluĢur. Nöbetlerin klinik dıĢa vurumlarının yaĢ ile değiĢmesinin altında yatan fizyopatolojik değiĢiklikler iyi anlaĢılamamıĢtır. YaĢ ile artan sinaptik bağlantıların karmaĢıklığı, inhibitör ve buna karĢı gelen eksitatör sistemlerin geliĢimlerinin değiĢik seviyeleri ve nörotransmitter sentezindeki değiĢiklikler özellikle önemlidir (18).
Sınıflama:
Çocukluk yaĢlarında baĢlayan epilepsilerin klinik bulgularındaki değiĢkenlik, terminolojide ve klinisyenler arası iletiĢimde zorluklara yol açmıĢtır. Ortak bir tanımlama ve sınıflama ilk kez 1970’de Gestaut tarafından yapılmıĢtır (19). Yakın
dönemde epileptoloji alanındaki ilerlemelerin sonucu olarak, nöbetleri sınıflandırmada yeni yaklaĢımlara ihtiyaç duyulmasını anlamak kolaydır (18). Uluslararası Epilepsi Ġle SavaĢ Ligi (ILAE), büyük ölçüde epileptik sendromların tanımlanmasını esas alan epilepsiler ve Epileptik Sendomların sınıflandırmasını kabul etmiĢtir (18).
Epilepsi ve Epileptik Sendromların Uluslararası Sınıflandırması;(20) ĠDAE (1989)
I. Lokalizasyonla ĠliĢkili (Fokal, Lokal, Parsiyel) Epilepsiler ve Sendromlar
A.Ġdiopatik (baĢlangıç yaĢına göre)
1) Sentrotemporal diken bulgusu veren çocukluk çağı selim epilepsisi 2) Oksipital-paroksizmal çocukluk çağı epilepsisi
3) Primer "okuma" epilepsisi B. Semptomatik
1) Kojewnikow sendromu (kontinü parsiyel epilepsi) 2) Belirli uyanlarla geliĢen epilepsiler (örn: refleks epilepsi) 3) Temporal lob epilepsisi (amigdalohipokampal, lateral)
4) Frontal lob epilepsisi (singulat, anterior frontopolar, orbitofrontal, dorsolateral, operkular, motor korteks)
5) Pariyetal lob epilepsisi 6) Occipital lob epilepsisi C.Kriptojenik fokal epilepsiler II. Generalize epilepsiler
A.Ġdiopatik(baĢlangıç yaĢına göre)
1) Selim familyal neonatal konvulziyonlar 2) Selim neonatal konvulziyonlar
3) Çocukluk çağı selim myoklonik epilepsisi 4) Piknolepsi
5) Jüvenil absans
6) Jüvenil myoklonik epilepsi(impulsif petit mal) 7) Uyanınca geliĢen tonik-klonik(grand mal)epilepsi
8) Belirli uyanlarla geliĢen tonik-klonik (grand mal)epilepsi
9) Yukanda sımflandınlmayan diğer generalize idiopatik epilepsiler
B.Kriptogenetik/semptomatik (yaĢ sırasına göre)
1) West sendromu (infantil spazm, Blitz-Nick-Salaam Krampfe) 2) Lennox-Gastaut sendromu
3) Myoklonik-astatik nöbetli epilepsi 4) Myoklonik absanslı epilepsi C.Semptomatik
a) Nonspesifık sebepler
1) Erken myoklonik ensefalopati
2) Supresyon "bursf'lü erken infantil epileptik ensefalopati
3) Yukarıda sımflandırılmayan diğer semptomatik generalize epilepsiler b) Spesifik sendromlar
Komplike hastalık durumlarında görülen epileptik konvülziyonlar
III. Fokal ya da jeneralize olduğu belirlenemeyen epilepsiler A.Hem jenerejize hem de fokal konvülsiyonlar
1) Neonatal konvülziyonlar
2) Çocukluk çağı ağır myoklonik epilepsisi
3) YavaĢ dalgalı uykuda beliren sürekli diken dalga bulgusu 4) Edinsel epileptik afazi (Landau-Kleffiıer sendromu)
B. Açıkça generalize ve fokal bulgu gösterenlerin dıĢındakiler IV. Diğer konvulziyon türleri
A. Çevresel nedenlere bağlı konvulziyonlar 1) Febril konvulziyonlar
2) Ġzole epileptik status
Epidemiyoloji:
Epileptik nöbetler pediatrik yaĢ grubunda en sık görülen nörolojik hastalıktır ve % 3–5 sıklıkla meydana gelir. Epilepsi populasyonun % 0,5-1’inde görülür ve vakaların % 60’ı çocukluk çağında baĢlar (21). Tüm insidans ve prevelans araĢtırmalarında en yüksek rakamlar hayatın ilk bir yılı için bildirilmiĢtir. YaĢamın ilk 5 yılında oran kızlarda hafifçe yüksek olmakla birlikte tüm yıllar ele alındığında erkeklerde epilepsi görülme oranı daha yüksektir (22,23).
Fizyopatoloji:
Merkezi sinir sisteminde denge halinde bulunan eksitatör ve inhibitör aktiviteyi sağlayan sistemlerden birincisinde artma, ikincisinde azalma sonucu nöronal uyarılabilirlik artar (24). Epileptik nöbetler sırasında sinir hücrelerinin aktivitesi üzerine, inhibitör ve eksitatör etkideki normal denge bozulmuĢtur. Ġnhibitör aktivitenin azalması epileptik aktivitenin azalmasında önemli bir faktördür (25,26). Epilepside görülen klinik tablo korteks ya da subkortikal yapılarda belirli bir nöron grubu veya tamamının uyarılabilirliğinin artmasına bağlıdır (27). Nöronlarda eksitasyon, membranın Na+ ve Ca++’a, inhibisyon ise Cl- ve K+’a geçirgenliğin artmasına bağlıdır. Nöromediatörler ise kendilerine ait reseptörlerin pre veya postsinaptik membranda kenetlendiği, iyon kanallarının açıklığını veya açılıp kapanma frekansını değiĢtiren maddelerdir. Nöromediatörler, inhibitör gama amino butirik asit (GABA) erjik, adenozinerjik ve eksitatör glutamerjik sistemler olmak üzere üç grupta etkilerini gösterirler(24 ). Ġdiopatik epilepsi dıĢında anormal deĢarjı baĢlatan faktörler somut olarak vardır; lokal dolaĢım bozuklukları, lokal metabolizma bozuklukları, herhangibir bölgedeki skatris dokusu, atrofi, inflamasyon, tümör, apse vb. normalden daha fazla elektriksel aktiviteye sahip olan bu hücre grubuna ‘’epileptojenik odak’’ denir (27). Serebral kortekste kronik epileptojenik foküs, uzak bölgelerde anormal nöronal aktiviteye neden olurlar.
EPĠLEPSĠ TEDAVĠSĠ
Tedavinin Genel Prensipleri:
Epilepsi tedavisi ancak, her hasta özelinde uygulanacak genel bir yaklaĢım stratejisi olarak düĢünülebilir. Çocukluk çağı epilepsilerinin tedavisi, yalnızca nöbetlerin ve diğer paroksismal nörofizyolojik fonksiyon bozukluklarının önlenmesinden daha geniĢ kapsama sahiptir (2). Tekrarlayan nöbetler, hastaların bireysel ve toplumsal yaĢamlarında ağır kesintilere yol açarlar ve kontrole alınmamıĢ epilepsisi olan çocukların ve gençlerin hem fizik güvenlikleri hem de tümüyle yaĢam kaliteleri kesinlikle tehlikeyle karĢı karĢıyadır. Epilepsili hasta gruplarında ölüm, özellikle de ani ölüm insidansı, genel nüfusta görülenden daha yüksektir (2).
AĢikar nöbetlerin ortaya çıkardığı belli sorunlara ek olarak zahiri subklinik epileptik aktivite bazı hastaların zihinsel iĢleyiĢini derinden bozabilmektedir (2). Subklinik epileptik aktivitenin, en azından bazı hastalarda, istenmeyen etkileri olabilmektedir. Çok sayıda yayın, izole paroksizmlerin ve kısa EEG boĢalımlarının kognitif süreçlerin akıĢını engelleyici olabileceğini göstermektedirler (2). Bunlara ek olarak, belli koĢullarda tekrarlayan kısa nöbetler bir beyin hasarına yol açabilmekte ve sık nöbetlerin ve/veya EEG deĢarjlarının tekrarlayan uyarması baĢlı baĢına bir status epileptikusa varabilmektedir (2). Bu yüzden nöbetlerin ve epileptik aktivitenin diğer etkilerini önleyebilmek için her türlü mantıklı çaba gösterilmelidir. Nöbetleri olan çocuklarda eğer nöbetin tekrarlama ihtimali yüksekse tedavi kesinlikle gereklidir. Subklinik epileptik aktivitesi olan hastalarda ise antiepileptik tedavi endikasyonlarının belirlenmesi daha güçtür. ''EEG’nin tedavisi'' bir ilke olarak, semptomu olmayan hastalarda önerilmez. Bunla birlikte paroksismal EEG deĢarjları olan bir çocukta kognitif güçlükler ya da gerileme ortaya çıktığında, tedavi düĢünülebilir (2). Bununla birlikte, nöbetlerin ve özellikle de devamlı EEG deĢarjlarının kontrolü hastaların entelektüel kapasitelerinden ödün vererek elde edilmemelidir. Bütün antiepileptik ilaçların (AEĠ) davranıĢ ve/veya öğrenme süreçleri üzerinde olumsuz etlileri olabilmekte (2) ve ağır bir tedavi dikkatte ve kognitif yeteneklerde ciddi bir eksikliğe yol açabilmektedir (2). Tedavi bu nedenle, normal ailesel ve sosyal yaĢamla uyuĢabilir olmalıdır. Bir çok çocuk için sosyopsikolojik faktörler yalnızca nöbet önleme sorunlarından çok daha ağır
basmaktadır. Epilepsinin, basitçe nöbetlerden oluĢan bir tablodan çok öte bir kavram olduğunu, her hasta özelinde çok kapsamlı bir tedaviyi planlarken, klinisyenin devamlı akılda tutması gerekmektedir. Tedavinin amacı hastanın yaĢam kalitesinin bütününde iyileĢme sağlamaktır. Epilepsinin hastaların yaĢamına hakim olacak dereceye varan, hatta bazı olgularda en önemli ilgi ve mazeret gösterme odağını oluĢturan kronik bir hastalık olması dolayısıyla, hastadaki nöbetin kontrolü, yararsız olabilmekte, hatta olumsuz etki bile yapabilmektedir (2). Neticede epilepsi tedavisinin temel amacı, nöbetlerin tam olarak kontrol altına alınmasıdır. Epilepsi tanısı kesin konulmadan antiepileptik tedaviye baĢlanmamalıdır. Primer epilepsilerin nedeni tam anlaĢılamadığından, tedavi, nedeni ortadan kaldırmak değil, nöbetleri önlemeye yöneliktir (28). Ayrıca epileptik nöbetlerde büyük önemi olan ailesel yatkınlığı düzeltmek de mümkün değildir (29,30).
Epilepsi tedavisinin üç esası vardır:
Ġ. Nöbetleri ortadan kaldırmak ya da olabildiği derecede sıklığını azaltmak, ii. Uzun süreli tedavi ile ilgili ortaya çıkabilen yan etkilerden kaçınmak, iii. Çocuklarda hastalığın aldığı normal günlük yaĢantı ve sosyal özellikleri geri kazandırmak (28).
Tedavi Seçenekleri:
AEĠ (antiepileptik ilaç)’ler epilepside en sık kullanılan tedavi seçeneğidir. Bütün AEĠ’lerin potansiyel bazı yan etkileri bulunduğuna ve tedavideki en önemli hedeflerden birinin ilaca bağlı istenmeyen etkiler oluĢturmaksızın nöbetleri kontrol altına almak olduğuna göre, bu ilaçların kullanılma endikasyonları dikkatle hesap edilmelidir(2). Adrenokortikotropik hormon ve steroidler özel endikasyonlarda antiepileptik araçlar olarak kullanılabilmekte ve mutad AEĠ’lerden daha etkili olabilmektedir(2). Daha yeni ilaçlar, konvansiyonel AEĠ’lerle karĢılaĢtırıldıklarında, kesinlikle daha tolere edilebilir bulunurlar ancak potansiyel yan etkileri de ihmal edilemez düzeydedir(2). Nöbet baĢlama yaĢı, nöbet sıklığı, EEG verileri ve görüntüleme incelemelerinin bulguları dahil, hastanın özellikleri, hekimin sendrom tanısına ulaĢmasını sağlayan ve her hasta özelinde daha uygun AEĠ’yi seçmesine olanak veren tanı göstergelerini oluĢturur. Bununla birlikte, AEĠ’lerin özgüllüğü nispeten sınırlıdır ve ilaçla tedaviye sıklıkla, esas nöbet tipi için uygun olan geniĢ
aktivite spektrumuna sahip etkili bir ilaçla baĢlanır. Gerçekten de, birçok antiepileptik maddenin belli bir epilepsi biçimi için benzer ya da aynı özelliği bulunmaktadır. Bu nedenle, ilacın sonuçta oluĢturacağı yan etkileri ve pratik uygulamadaki güçlükleri tedavide kullanılacak bu maddenin seçiminde esas rolü oynar (2). Ġlaçla oluĢan nöbetlerdeki artıĢ sıklıkla tanınmayan ya da dikkatten kaçan bir klinik sorundur. Bu fenomenin prevalansını değerlendiren ve mekanizmalarını araĢtıran daha ileri çalıĢmalara gerek varsa da, mevcut verilerin gözden geçirilmesi Ģu iki ayrı sürecin olayla iliĢkisini iĢaret etmektedir: (a) ilaç entoksikasyonunun spesifik olmayan belirtileri aĢırı dozlara ya da polifarmasiye veya, (b) özel epilepsi tipleri ya da belli epilepsi sendromları üzerinde ilacın özel ters bir etkisine bağlıdır (2). Karbamazepinin özellikle idiyopatik jeneralize epilepsili hastalarda bir dizi nöbeti (miyoklonik ve absans) açığa çıkardığı ya da arttırdığı bildirilmiĢtir. Diğer taraftan yakın tarihli bir yayında fokal epilepsilerde ilaçlara bağlı Ģiddetlenmenin nadir olduğu ileri sürülmektedir (2). Fenitoin ve vigabatrin de jeneralize nöbetlerin Ģiddetlenmesi ile iliĢkilendirilmiĢ, gabapentin ise miyoklinik kasılmaların açığa çıkmasıyla bağlantılı bulunmuĢtur. Benzodiazepinlerin özellikle Lennox-Gastaut sendromu (LGS) olan hastalarda tonik nöbetleri açığa çıkardığı bildirilmiĢtir (2).
Tıbbi Tedavi:
Nöbetleri olan epilepsili kiĢilerde doğal gidiĢ, hastadan hastaya ve aynı hastada farklı zamanlarda önemli ölçülerde değiĢmektedir. Hastaların çoğunda artmıĢ epileptik duyarlılık uygun dozlarda kullanılan antiepileptik maddelerle azaltılabilmekte ya da baskılanabilmektedir (2). Gençlerde ve eriĢkinlerdeki yakın incelemeler ilk seçilecek ya da ikinci seçilecek bir antiepileptik ilaç ile monoterapide, nöbetlerin kabaca %60’ının kontrol altına alındığının, oysa geri kalanlarının bir veya birçok kombinasyona dirençli olduğunu göstermiĢtir. Bununla birlikte yeni ilaçların çoğu eski bileĢiklerden daha iyi tolere edilirler(2).
AEĠ’lerin etkinliği ve etki tarzı hakkındaki günümüzdeki bilgilerin en büyük kısmı hayvanlardan elde edilmiĢtir. Epileptogenez tek bir nöronda oluĢmamakta ancak, yüksek frekanslı diken boĢalımı patlamalarını oluĢturma yatkınlığını, kalıtımsal ya da edinsel olarak kazanmıĢ nöron havuzlarında doğmaktadır (2). Bu patlamalar aksonlar boyunca iletilmekte ve yeterli hacimde sinir dokusu aktive
edildiğinde klinik bir nöbetle sonuçlanmaktadır. Bu nedenle klinik nöbetler, ya irkiltici nöronal havuzun eksitabilitesi düĢürülerek ya da epileptojenik diken patlamalarının havuzdan yayılması engellenerek önlenebilirler. Kullanılan ilaca bağlı olarak, mekanizmalardan biri ya da diğeri çalıĢabilmektedir; fakat patlamanın yayılmasının önlenmesi geleneksel antikonvülzanların çoğunluğu için karakteristiktir (2). Antikonvülzan ilaçlar beyinde genellikle özel reseptörlere bağlanırlar. Genel olarak ilacın etkisinin büyüklüğü ilaç molekülleri tarafından iĢgal edilen reseptör bölgelerinin sayısı ile iliĢkilidir(2). Örneğin PTH, CBZ ve lamotrijin (LTG) seçimli olarak sodyum kanalları üzerinde etki ederler, böylece nöronal aksiyon potansiyellerinin tekrarlayan ateĢlemesini engelleyerek, sonuçta epileptik aktivitenin yayılmasını inhibe etmektedirler. Diğer ilaçlar öncelikli olarak sinaptik iletimi etkiler görünmektedir. Bu etki presinaptik olabileceği gibi sinaptik veya postsinaptik de olabilmektedir. Antikonvülzan maddelerle tedavi uzun süre amprik olarak sürdürülmüĢtür. Beden sıvılarında ilaçların çok küçük miktarlarını ölçme tekniklerinin geliĢtirilmesi sayesinde, yakın yıllardaki klinik farmakokinetik ilerlemelerle ilaçların metabolizmasının doğru incelenmesini mümkün kılmıĢtır. Optimal kan düzeyleri kavramı sıklıkla yanlıĢ yorumlanmıĢtır; öyle ki, pek çok hekim tedavi aralığı dıĢındaki kan ilaç düzeylerinin değersiz olduğuna ve bir AEĠ’nin bütün kullanımlarında bu tedavi aralığındaki kan düzeylerinin hedeflenmesi gerektiğine inanmaktadır. Tedavi aralığı tek tek hastalardan çok, yalnızca topluluklara uygulanan istatistik bir kavramdır. Bazı hastalarda bireysel tedavi aralığının alt ve üst sınırları kabul edilmiĢ sınırların dıĢına çıkabilmektedir. Klinik olarak kontrole alınmıĢ hastalarda, eğer ilaç toksisitesinin klinik kanıtları yoksa bu değerler tedavi aralığının veya optimalin dıĢında olsalar bile, tedavi değerine eriĢmek için çaba sarf edilmemelidir. Kan düzeyleri, bir ilacın yutulması ile farmakodinamik etkilerinin gerçekleĢeceği etki noktası arasında meydana gelen farmakokinetik olaylar zincirinde yalnızca bir halkadır. Önemli olan bundan dolayı ilacın merkezi sinir sisteminde (MSS) reseptör noktalarındaki konsantrasyonudur. Bir ilacın optimal aralığı kavramı, ancak ilacın reseptörlerine irreversibl olarak bağlanmaması ve/veya aktif metabolitleri olmaması durumunda geçerlidir. Bu durumda CBZ’nin ve benzodiazepinlerin kan düzeylerinin belirlenmesi tartıĢmaya açıktır; çünkü bu maddelerin aktif metabolitleri vardır ve diğer ilaçların etkilenmeleriyle bu
metabolitlerin düzeyleri arttığında, metabolitler klinik olarak son derece önem kazanır (2). AEĠ’lerin kan düzeyleri bir dizi sürecin sonucudur. (Ģekil 1)
ġekil 1: Antiepileptik bir ilacın yutulmasından klinik etkilerinin görünmesine kadar geçen ardıĢık basamakların Ģematik gösterilmesi.
Antikonvülzanların pek çoğu ağızdan kullanılmakta, hızlı ve genellikle tümüyle emilmektedir. Ġlaçlar emildikten sonra dolaĢıma geçerler. Kanda değiĢik oranlarda proteinlere bağlanırlar. Ġlaçların proteine bağlanma derecesi serbest ilaçların düzeyi ile sabit denge içindedir. Reseptör bölgelerine ulaĢabilmek üzere, yalnızca serbest fraksiyon kan beyin bariyerini geçebilmektedir. Bir ilacın serbest fraksiyonu çeĢitli etmenler tarafından değiĢtirilebilir. Ġlki, ilacın bağlandığı noktalardan baĢka bir ilaç ya da bilirubin ve serbest yağ asitleri gibi, baĢka bir kimyasal madde tarafından ayrılması ile oluĢur. Diğer faktörler arasında gebelik ve yaĢ (örn. çocukluk ve yaĢlılık) yer almaktadır. Ġlaçların dağılımı maddenin, özellikle
lipit çözünürlüğüne bağlı, zahiri dağılım hacmi ile değiĢmektedir. Benzodiazepinler gibi, bazı AEĠ’ler bedenin toplam sıvı hacminden daha büyük dağılım hacimlerine sahiptirler; bu durum doku elemanlarına bağlandıklarını, hücrelerin içine aktif taĢınmalarını ya da depolanma bölgelerinde toplandıklarını göstermektedir. Diğer AEĠ’lerin toplam beden sıvı hacmine eĢit ya da yakın dağılım hacimleri vardır; oysa valproik asit (VPA) hücre dıĢı sıvısına yakın bir dağılım hacmine sahiptir (2 ) .
Antikonvülzan ilaçlar Ģu iki mekanizmaya uyarak bedeni terk ederler; Ġnaktif ya da daha az sıklıkla, aktif metabolitlere biyotransformasyon ile ve böbrekler, incebağırsak, ter ve gözyaĢı yoluyla atılımı ile. ''Biyotransformasyon’’, baĢlıca karaciğerin mikrozomal aktivitesi sonucu oluĢan bir enzimatik süreçtir (2). Bazı ilaçlar bu sistemi inhibe, diğerleri aktive eder. Fenitoin, fenobarbital ve karbamazepinin bu sistemi aktive ettiği gösterilmiĢtir. Biyotransformasyonda en önemli organ karaciğerdir, en önemli enzim fraksiyonu da mikrozomal enzimlerdir (31,32).
Mikrozomal enzim indüksiyonu, mikrozomal bir enzimin substratı olan bir madde tarafından, bu enzimin sentezinin arttırılması sonucu enzimatik etkinliğin artması olayıdır. Enzimlerin miktarının artmasına p 450 sitokromunun ve benzeri hemli proteinlerin artması eĢlik eder. Deney hayvanlarında mikrozomal enzim indüksiyonu esnasında karaciğer hücrelerinde endoplazmik retikulumda hiperplazi ve karaciğer hücrelerinde büyüme saptanmıĢtır (33,34).
Bu aktivite; sırasıyla, hastanın genetik yapısına ve cinsiyetine olduğu kadar, diyet ve ilaç metabolize eden mikrozomal enzim sistemini indükleyen diğer ilaçların etkilemesi gibi, bir dizi dıĢ etkiye de bağlıdır. EtkileĢme, bir ilacın metabolizmasının bir diğeri tarafından değiĢik mekanizmalar aracılığıyla baskılanması aracılığıyla da olur (2). Bir ilacın atılması, idrarın pH derecesi, idrar akımı ya da glomerüler filtrasyon hızı gibi etkenler tarafından değiĢtirilebilmektedir(2).
Bir ilacın zahiri plazma yarı-ömrü, önceki plazma düzeyi değerinin %50’sine düĢmesi için geçen zaman olarak tanımlanır (2). Toplam ilaç (serbest, artı proteine bağlı fraksiyon) kan seviyesi yerine, serbest ilaç fraksiyonlarının kan düzeylerinin belirlenmesi ile bu güçlüklerden bazıları ortadan kaldırılabilmektedir (2). Ancak
böyle bir belirleme için uygulanan teknik daha karmaĢıktır. Bu nedenle, AEĠ’lerin serbest düzeylerinin ölçümünü yapma, gebelik, hipoalbüminemi ve hepatik ya da renal yetmezlik gibi özel koĢullar dıĢında, toplam düzeyin belirlenmesi yerine geçememiĢtir.
Ġlacı metabolize eden mikrozomal enzimlerin indüksiyonu ilaç etkileĢimine yol açabilir. Çocuklardaki değiĢkenliğin ek ve önemli bir kaynağı hastanın yaĢıdır. YaĢ, ilaç metabolizmasının her yönünü etkilemektedir. CBZ dıĢında, AEĠ’lerin emilimi genellikle, küçük çocuklarda ve gençlerde eriĢkinlerden daha hızlıdır. BaĢlıca antikonvülzanların yarı-ömürleri yeni doğmuĢ bebeklerde yaĢamın ilk 1–3 haftası boyunca oldukça uzundur ve bu dönemden sonra, yaĢamın ilk 2–3 ayı sırasında dramatik olarak azalır. YaĢamın ilk günleri sırasında tekrarlayan dozlarda antikonvülsanları alan yenidoğanlarda entoksikasyonların sık, buna karĢılık, sonraki birkaç gün ya da haftalar içinde uygun tedavi düzeylerini sürdürmenin neden güç, hatta imkânsız olduğunu açıklamaktadır (2).
Bütün antiepileptik maddeler, hastanın etkinliklerini önemli ölçüde engelleyebilen yan etkiler oluĢtururlar. Bu etkiler bilinç bozukluğu ile birlikte olan ya da nadiren ölüme yol açan akut entoksikasyonlardan, değiĢken gösterilerin sergilendiği sinsi kronik toksisiteye ve hafif fakat bazen hastayı psikolojik ve sosyal bakımdan özürlü hale sokan akne ve aĢırı kilo alma ya da kilo kaybı gibi yan etkiler kadar bir dizi oluĢtururlar. Alerjik ve idiyosenkratik reaksiyonlar da sıktır ve nadiren ölümlerden sorumludurlar. Antikonvülzanların kognitif etkileri özellikle can sıkıcıdır ve bazılarında (örn.PB) diğerlerinden (örn.sodyum valproat, CBZ ve GPT) daha belirgin olsa bile, olumsuz kognitif ve davranıĢsal etkileri tümüyle olmayan ilaç bulunmamaktadır. Genç kızlarda uzun süreli tedavi önerileceği zaman, bu tedavinin doğurganlık yaĢına uzadığında teratojenite olasılığının da dikkate alınması gerekmektedir (2). Daha eski AEĠ’ler (benzodiazepinler, PHT, PB, CBZ ve valproat), dudak ve damak yarıklığı ve kalp defektleri de dahil, major fetal malformasyon riski taĢırlar.
Bazı olgularda AEĠ’ler paradoksal olarak nöbetlerin sıklığında artıĢa yol açabilirler. CBZ absans epilepsili ve juvenil miyoklonik epilepsili hastalarda kontendikedir. Fakat bazı olgularda, diğer mevcut ilaçlara dirençli tonik-klonik
nöbetlerin kontrolü için kullanılması gerekebilir. VGB ve GPT tipik absansların ve/veya miyoklonianın sıklığındaki artıĢtan sorumlu olabilmektedir (2).
Antiepileptik ilaçların seçimi:
Ġlaç seçimi öncelikle hastanın yaĢadığı nöbetin tipine bağlıdır. Bununla birlikte, belli herhangi bir ilacın, özel bir nöbet türü için özgünlüğü yoktur ve yalnızca genel bir yöneliĢe olanak verir.
Genel olarak, etkinlik dikkate alındığında, AEĠ’ler aĢağıdaki üç geniĢ kategoriye ayrılabilirler:
(a) Yalnızca jeneralize non-konvülzif nöbetlere (absanslar) ve belli miyoklonik nöbetlere karĢı etkili olanlar; bu kategoriye etosüksimid ve iliĢki bazı ilaçlar ve dionlar girmekte;
(b) Jeneralize ya da parsiyel olsun, geniĢ bir dizi nöbete etkili olanlar; bu grupta benzodiazepinler, sodyum valproat, LTG, TPM ve muhtemelen LEV yer almakta
(c) Daha çok parsiyel nöbetler üzerinde etkisi olanlar kategorisinde GPT, VGB, tiagabin, PB, PHT ve iliĢkili maddeler, PRM, CBZ ve feneturid bulunmaktadır (2).
Fenobarbital ve Fenitoin
Fenobarbital (PB) ve fenitoin (PHT) ilk kuĢak AEĠ’lere dahildir. .PB tonik-klonik ve fokal nöbetlere etkili bir antikonvülzandır. Ġlaç, absans ve atonik nöbetlere ve infantil spazmlara etki etmez; hatta bu nöbetleri ağırlaĢtırabilir. Çocuklarda sıklıkla davranıĢ bozukluklarına yol açtığı görülür. Bellek sorunlarının eĢlik ettiği ve okul performansını tehlikeye sokan kognitif iĢlev bozuklukları daima bildirilmiĢtir. PHT parsiyel ve jeneralize tonik-klonik nöbetlerin tedavisi için tercih edilen ilaç olarak kalmıĢtır. Akut toksik etkileri doza bağımlıdır (örn.ataksi, nistagmus, koordinasyon bozuklukları) ve nispeten sıktır. Gingiva hiperplazisi, hirsutismus ve yüzün kaba görünüĢ alması gibi kronik ters etkileri, ilaç kronik tedavi amacıyla ve özellikle çocuklara önerileceği zaman akılda tutulmalıdır. Uzun süreli kullanımında nöropatolojik değiĢiklikler ve serebellar dejenerasyon oluĢabilmektedir (2).
Karbamazepin
Karbamil grubu içeren bir iminostilben türevi olup kimyasal olarak trisiklik antidepresanlara benzer. 1960’larda keĢfinden sonra önceleri trigeminal nevraljilerde, antiepileptik olarak ise 1974’den itibaren kullanılmaya baĢlanmıĢtır (35) . CBZ, VPA ile birlikte, ikinci kuĢak AEĠ’ler arasında yer alır. Bunların PHT, PB, PRM gibi daha eski ilaçlara göre daha az nörotoksisiteye sahip oldukları düĢünülmektedir. Parsiyel epilepsileri olan çocuklar için ilk basamak ilacı olarak önerilir (2). CBZ, sadece ağız yoluyla kullanılan bir AEĠ’tır. Tablet ve süspansiyon formu vardır. Emilimi yavaĢtır, maksimum konsantrasyonu 4–8 saat sonra oluĢur. Tok karınla alınması sonucu yüksek çözünebilme özelliğine bağlı olarak daha hızlı emilebilir fakat biyoyararlanımı değiĢmez. Albüminden daha çok diğer proteinlere olmak üzere plazma proteinlerine %70–80 oranında bağlanır. Tükrük, beyin omurilik sıvısı, gözyaĢı CBZ konsantrasyonu serum konsantrasyonu ile benzerdir (24,36). Titrasyon hızı daima yavaĢ olmalıdır, orta dozajları bile yeterli olabilir. Sık rastlanan ters etkileri arasında ataksi, diplopi ve deri döküntüsü yer alır (2). Yapıca imipramide benzediği için ağız kuruluğu, midriazis, yakın görmede bozulma ve idrar retansiyonu gibi yan etkiler yapabilir. Gastrointestinal yan etkiler; bulantı, kusma, karın ağrısı, iĢtahsızlık, diyare, bazen kabızlık (24). Alerjik yan etkiler olguların %8-10’unda ortaya çıkar. Tedavi baĢlangıcında ortaya çıkan yan etkilerin 1/3’ünü oluĢtururlar ve daha sonra azalırlar. Çok hafif döküntülerden eritrodermi, eksfoliyatif dermatit, toksik püstüloderma, SLE benzeri tablo, Stevens-Johnson sendromu ve toksik epidermolizis büllosa gibi ciddi durumlara kadar değiĢik döküntüler oluĢabilir (24,37). Çocuklarda %10 olguda tedavinin ilk ayında sınırda lökopeni bildirilmiĢtir. Nadiren trombositopeni ve aplastik anemi bildirilmiĢtir (37). Nadir olarak jeneralize lenfadenopati ve kan tablosuyla birlikte ağır febril döküntü yapabilir. Seyrek olarak hipertansiyon, sol kalp yetmezliği ve kardiyovasküler kollaps bildirilmiĢtir (24). Karaciğer mikrozomal enzim indüksiyonu yaptığı için safra asitleri, kolesterol, lipidler, steroid hormonlar, tiroid hormonları, bilirubinler gibi pek çok endojen madde ile dıĢarıdan alınan ilaçların metabolizmasını etkiler (37). Teratojenik olabilir (24,37). Çocuklardaki semptomatik ya da kriptojenik jeneralize tonik-klonik ve absans nöbetlerinde artıĢ ve atonik ve miyoklonik nöbetlerde kolaylaĢma yaptığı bildirilmiĢtir (2).
Sodyum Valproat
Sodyum valproat, (VPA) zamanın deneyiminden geçmiĢ yerleĢmiĢ bir antikonvülzandır. GeniĢ spektrumlu bir AEĠ olup, her türlü nöbetlerin tedavisi için kullanımı önerilmektedir ve nöbetleri ağırlaĢtırma bakımından son derece düĢük potansiyele sahiptir. Miyoklonik ve absans nöbetleri için ilk seçim ilacıdır ve Lennox-Gastaut ve Davet sendromu gibi, ağır epilepsi sendromlarının kombinasyon tedavilerinde, hemen daima sistemli bir Ģekilde kullanılmaktadir. Kilo alma ve tremor oldukça sık görülen yan etkilerdir. VPA karaciğer hastalığı, ciddi karaciğer fonksiyon bozukluğu ve mitokondrial hastalıkları olanlarda önerilmemelidir. VPA tedavisi sırasında mutad karaciğer enzimleri ölçümü sık yapılan bir uygulamadır ve ekseriya transaminazlarda biraz yükselme saptanır. Bu bulguların karaciğer yetmezliğini önceden göstermesi bakımından değeri yoktur ve hepatotoksisite tanısı, daha çok bulantı, kusma, iĢtahsızlık ve letarji dahil, klinik bulguların erken fark edilmesine dayanır. En yüksek ölümcül toksisite riski 3 yaĢından daha küçük bebeklerde bulunmaktadır ve buna göre, bu yaĢ grubunda mümkün oldukça VPA kullanımından kaçınmak gerekir. Potansiyel olarak ölümcül akut hemorajik pankreatit bildirilmiĢ olup, bu olasılık karın ağrısı, bulantı, kusma ve iĢtahsızlık ile ortaya çıkan olgularda araĢtırılmalıdır. TPM ile birlikte kullanılmasının, VPA’ya bağlı hiperamoniamik ansefalopati için bir risk olduğu bildirilmiĢtir (2). VPA’nın yağ asidi metabolizması ile yarıĢtığı bazı deneysel çalıĢmalarla desteklenmiĢtir. Valproat alımından 2–4 saat sonra karaciğerdeki lipid kontenti artmaktadır (38,40). Lipid birikimi daha çok periportal alanda olmakta, böylece lipid metabolizmasını etkilediği düĢünülmektedir (39,40). Nörolojik yan etkiler; sedasyon, uyuĢukluk, tremor, ataksi görülebilir (24). Trombosit agregasyonunu inhibe ederek kanama zamanını uzatır, fibrinojen düzeyini düĢürebilir. Geçici saç dökülmesi doza bağlıdır ve olasılıkla çinko eksikliği sonucu oluĢur. Teratojenik olabilir. Dismorfizm, spina bifida, belirgin immatürite yapabilir (24). Titrasyonu yavaĢ yapılmalıdır (günde 10 ila 15 mg/kg, haftalık aralıklarla günde 30 ila 50 mg/kg’a kadar) ve günlük iki doz olarak verilmesi önerilir (2). Yarı ömrü 7-17 saattir. Terapötik serum konsantrasyonu 50–100 µg/ml’dir (28,36,41).
Lamotrijin
GeniĢ spektrumlu bir AEĠ olan LTG, kimyasal bakımdan diğer antikonvülzanlara benzemez. Kısmen voltaj-bağımlı ve kullanıma bağımlı sodyum kanallarında blok yaparak etki etmekte, böylece nöronal membranı stabilize etmektedir. LTG’nin hem ekleme tedavisinde hem de monoterapide etkili olduğu kanıtlanmıĢtır. ÇeĢitli çalıĢmalarda LTG ile bağlantılı, genellikle hafif ve orta derecedeki belli baĢlı ters etkiler arasında ataksi, bulantı, CBZ varlığında daha sık görülen sersemlik ve çift görme, valproatın varlığında daha sık ortaya çıkan tremor yer almaktadır. Ġlaçla tedavi edilen hastaların %5’inde deri döküntüsü oluĢur, fakat düĢük dozda baĢlayıp, birkaç hafta içinde yavaĢ yükseltmekle bunun sıklığı en aza indirilebilinir (2).
Gabapentin
GABA’nın kimyasal bir türevi oan GPT’nin, inhibitör sinaptik reseptörlerde GABA’nın etkisini taklit edeceği düĢünülmüĢtü. Bununla birlikte, daha sonraki incelemeler, GPT’nin, GABA’nın sentezini ve vesiküler olmayan açığa çıkıĢını artıran etkisi olmasa bile, GABAa ve GABAb reseptörleri üzerinde etkisi olmadığını göstermiĢtir ve bu bakımdan muhtemelen birden çok etki mekanizmasına sahip olduğu sanılmaktadır. GPT tipik ve atipik absansları artırabilmektedir. Ciddi ters etkileri son derece nadirdir. Çocuklarda ve özellikle de kronik epilepsisi ve statik ansefalopatisi olanlarda, akut baĢlayan saldırganlık, hiperaktivite ve atak davranıĢla Ģekillenen davranıĢsal değiĢiklikler bildirilmiĢtir. Kilo alımı nadir değildir (2).
Topiramat
TPM birden çok farmakolojik etkiye sahiptir. Ġlaç voltaj-bağımlı sodyum iyon kanallarını modüle ve GABA iletili inhibitör nöro-transmisyonu potansiyalize eder. PHT ve CBZ gibi enzim indüksiyonu yapan AEĠ’ler ile birlikte kullanıldığında, TPM’nin klirensinde iki ile üç misli artıĢa yol açması beklenir ve bu etkileĢim klinik bakımdan etkilidir. TPM’nin en önemli ters etkisi kognitif iĢlev bozukluğu olmuĢtur; bozukluk zihinsel yavaĢlama ve kelime bulma güçlüğü Ģeklinde ortaya çıkar ve oldukça anlamlıdır. Diğer yan etkiler kilo kaybı ve parestezilerdir (2).
Okskarbazin
OXC aslında bir ön-ilaçtır. Ġlacın parsiyel baĢlayan nöbetler üzerinde monoterapi olarak etkinliği, CBZ kadar PHT ve VPA’nın etkinliğine de denktir. OXC ile tedavi edilen çocukların %25’inden fazlasında görülen hiponatreminin klinikle uyumluluğu nadirdir (2). OXC parsiyel nöbetlerin kontrolü için önerilir.Yan etkileri arasında uyuklama, baĢağrısı, sersemlik, bulantı, apati ve deri döküntüsü yer almaktadır.
Levetirasetam
LEV, etki mekanizması henüz belirlenememiĢtir. Lokalizasyonla bağlantılı epilepsilerde, ek tedavi olarak LEV’nin etkinliği çok merkezli üç incelemede saptanmıĢtır. Ġlaç iyi tolere edilir, fakat uyuklama görece sık görülen yan etkidir(2).
Vigabatrin
VGB, inhibitör nörotransmitter olan GABA’yı katalize eden GABAtransaminaz enzimini geri dönüĢsüz olarak baskılayan bir maddedir. Ġlaç eriĢkinlerdeki ve çocuklardaki parsiyel epilepsilerin tedavisinde son derece etkili olduğu gibi, infantil spazmlar dahil diğer epilepsilerin tedavisinde de etkili olmaktadır. Ġlaç enzim indüksiyonu yapmamakta ve ilaçların çoğu ile anlamlı bir etkileĢime girmemektedir. Sedasyon, kilo alma, yorgunluk en sık görülen yan etkilerdir (2).
Felbamat
FBM, özellikle sekonder jeneralize epilepsili hastalarda etkili olması bakımından ilginç bir ilaçtır. YaĢamı tehtid edici aplastik anemi ve hepatotoksisite görülebilir.
LĠPĠDLER
Lipidler biyolojik yaĢamın ana bileĢenlerinden biridir. Tüm hücre ve organellerin membranlarının yapısında bulunurlar. Sinir liflerinin izolasyonu, vücudun soğuktan korunması yanı sıra hormonların biyosentezi, enerji deposu ve metabolik yakıt olması gibi birçok önemli görevleri vardır (42). Ġnsan plazmasındaki baĢlıca lipidler; kolesterol, trigliserid (TG), fosfolipid (FL), kolesterol esterleri (KE), serbest yağ asitleridir (SYA). Lipidler hidrofob özelliğe sahip olduklarından suda çözünmeyen veya çok az çözünen organik moleküllerdir. Lipidler, hücrelerin bütünlüğünü koruyan ve sitoplazmanın özgül organeller halinde bölümlere ayrılabilmesini sağlayan hücre zarının yapısında yer alırlar (43). Lipidler plazmada apoproteinler ile birleĢip lipoproteinleri oluĢturarak hedef dokulara taĢınabilirler (42,44).
Lipid türleri
1)Yağ asitleri:a) DoymuĢ yağ asitleri (Çift bağı olmayan)
b) DoymamıĢ yağ asitleri (Bir veya daha fazla çift bağı olan)
Dokulardaki yağ asitleri, kompleks lipidleri oluĢturmak üzere diğer lipidlerle esterleĢtirilirler. Bunlar kanda serbest yağ asitleri ve albümine bağlı Ģekilde ya da kompleks lipidler halinde lipoproteinler üzerinde taĢınırlar. Yağ asitleri kolaylıkla sağlanabilen enerji kaynaklarıdır. Ayrıca kompleks lipidlerin biyosentezinde de kullanılmaktadır(11).
2)Kompleks Lipidler
a) Trigliseridler: En çok bulunan kompleks lipidlerdir (11). Bir molekül gliserol ile esterleĢmiĢ 1, 2 veya 3 molekül yağ asitinin birleĢmesinden oluĢurlar. Diyet ile alınabildikleri gibi vücutta da sentez edilebilirler. Plazmada lipoproteinler içinde taĢınırlar. Hücrelerde yağ damlacıkları Ģeklinde depolanırlar. Bu lipid damlacıkları vücudun ana enerji deposudur. Çünkü indirgenme potansiyelleri çok yüksektir. TG’ler, karaciğerde hepatik lipaz, dokularda LP-lipaz ve hormona duyarlı lipaz ile hidrolize edilerek
gliserol ve yağ asitlerine parçalanırlar. Gliserol karaciğerde fosforillenip ya tekrar TG sentezine, ya glikolize ya da glukoneogeneze katılır. Yağ asitleri eritrosit, beyin ve sürrenal medullası dıĢındaki doku hücrelerinde oksitlenerek enerji elde edilmesinde kullanılırlar (42, 44, 45).
b) Kolesterol: Yirmiyedi karbonlu bir siklopentanoperhidrofenantren bileĢiğidir. Kolesterol vücuda steroid hormonlar, D vitamini ve safra asitlerinin sentezi için sterol iskeleti sağlar. Vücutta tüm hücre membranlarının önemli bileĢenidir. Bu özelliği ile eritrosit membranlarını hemolizden korur, nöron membranı stabilizasyonunu sağlar. Her gün barsaklardan safra asitleri ve yağların varlığında 300–500 mg kolesterol emilir. Ayrıca günde yaklaĢık emilen miktar kadar kolesterol %90’ı karaciğerde olmak üzere vücutta sentezlenir. Plazma kolesterolünün 2/3’ü yağ asitleri ile esterleĢmiĢ halde bulunur. Yarı ömrü 8 gündür (3, 44). Kolesterol dolaĢımdan iki Ģekilde temizlenir:
1) Safla asitlerine çevrilme ve feçeĢle nötral steroid Ģeklinde atılma. 2) Steroid hormon sentezi ve katabolizma ürünlerinin idrarla atılması. Çekirdekli hücre içeren dokuların çoğunda özellikle karaciğer, sürrenaller, deri, bağırsaklar, testis ve aortada kolesterol sentez edilir (46). (Ģekil 2)
ġekil 2: Kolesterol Biosentezi
Plazma Lipoproteinleri:
Barsaklardan absorbe edilen ve karaciğerde sentezlenen temel lipidler, TG ve kolesterol suda, dolayısıyla plazmada erimezler; glukoprotein yapısındaki apoproteinlerle birleĢerek hidrofilik lipoproteinleri (LP) oluĢtururlar.(Ģekil 3) Böylece hedef dokulara taĢınabilirler (3,44,45,47,48). Plazma lipoproteinleri ilk kez 1920 yılında Frenchman Macheboeuf tarafindan tanımlanmıĢtır. Lipid ve protein içeriklerinin amonyum sülfat ile presipite olduğu gösterilmiĢtir. 1940' larda Ondey ve arkadaĢları lipoproteinleri ayırmak için Cohn fraksiyon tekniğini denemiĢlerdir (49).
ġekil 3: Lipoprotein Molekülü
Lipoproteinler yüksek moleküler ağırlıklı partiküller ve suda çözünmeyen nonpolar lipidlerden oluĢur. Lipoprotein yapısında fosfolipidlere ek olarak yüzeyde birkaç tane anesterefiye kolesterol ve protein vardır. Bunlara apolipoproteinler denir. Bunlar lipoproteinlerin metabolik etkinliklerinde anahtar rolü oynar (50). Plazmada bulunan lipid ve apoproteinlerden oluĢan, küresel yapıda makromoleküllerdir. Küresel yapının santral kısmında non-polar lipidler (TG, kolesterol esterleri, kolesterol), dıĢ kısmında ise polar lipidler (fosfolipidler, esterleĢmemiĢ kolesterol) ve apolipoproteinler (apoproteinler) bulunur (11). Lipoproteinlerin esas görevi suda çözünmeyen lipidlerin (TG ve kolesterol esterleri), suda çözünebilir polar bir kabukla (fosfolipid, apolipoprotein, serbest kolesterol) sarılmıĢ halde plazmada taĢınmasıdır (5,8,12). Apoproteinlerin görevi; hidrofobik lipidlerin suda eriyebilme özelliklerini, metabolizmada izleyecekleri yolu belirlemektir (7). Lipoproteinler vücutta baĢlıca iki yerde oluĢur:
1) Günlük ekzojen yağ tüketimi, sindirimi ve emilimi sonrası lümende 2) Endojen yağlardan karaciğerde
LP’ler farklı oranlarda TG, kolesterol ve FL içermeleri nedeniyle Ģilomikronlar (ġM), çok düĢük dansiteli lipoproteinler (VLDL), orta dansiteli LP’ler (IDL), düĢük dansiteli lipoproteinler (LDL) ve yüksek dansiteli lipoproteinler (HDL) olmak üzere 5 temel gruba ayrılırlar (3,44,47,48).
Plazmada dört grup lipoprotein bulunur:
1) ġilomikronlar: Besinlerle alınan lipidleri taĢıyan en büyük çaplı, en düĢük dansiteli LP’lerdir. Plazma klirensleri bir saatten azdır. 12 saatlik açlıktan
sonra kanda bulunmazlar. Elektroforezde hareket etmezler (41,42,44,48). Barsak mukoza hücrelerinde üretilir ve besinsel trigliserid, kolesterol esterleriyle, barsakta yapılan ilave lipidleri periferik dokulara taĢırlar. Plazma lipoproteinlerinin en büyük olanıdır. Dansitesi 0.93 gr/ml olup plazmanın ultrasantrifüjüyle kolaylıkla ayrılabilir, içeriğini % 98–99 lipidi, bunun % 85– 90 kadarını TG, % 1-2'sini protein oluĢturur (51).
2) VLDL (pre B lipoprotein): Dansitesi 1.063g/ml' dir. Karaciğerde sentezlenir ve bir kısımda besinlerden elde edilir.
3) LDL (B lipoprotein): Çoğu plazmada VLDL den oluĢur. Fakat bir miktar karadğerde de sentezlendiği düĢünülmektedir. Dansitesi 1.020–1.063 gr/ml. dir.
4) HDL (alfa lipoprotein): Dansitesi 1.021 gr/ml. Alfa globulin ile taĢınır. Karaciğerde sentezlenir.
VLDL (Very Low Density Lipoprotein):
Endojen olarak karaciğerde üretilir. Apo B100 içerir. Trigliserid primer lipid içeriğidir. Aynı zamanda kolesterol, kolesterol ester ve fosfolipid bulunur. VLDL'
nin en önemli fonksiyonu kolesterol transportu ve endojen trigliserid üretimidir (50). Elekrtoforezde pre –β bölgesinde kalır (42,44,45,47).
IDL
Doğrudan sentez edilmez, Ģilomikron ve VLDL'nin metabolizmaları sırasında oluĢur. LPL enzimi aracılığı ile VLDL'nin LDL'ye dönüĢümü sırasında, ara ürün olarak meydana gelir. Normal koĢullarda, plazmada çok düĢük düzeylerde bulunur. EĢit miktarda TG ve kolesterol içerir. Fonksiyonunun kolesterolün katabolize olması için karaciğere taĢınması olduğu düĢünülmektedir. Karaciğer ve incebarsak mukozal hücrelerinden salgılanır. Apolipoproteinlerden apo B–100 ve E'yi tutar. IDL yüksekliğinin erken koroner ve periferik damar hastalığında predispozan olduğu düĢünülmektedir (52).
LDL (Low Density Lipoprotein):
LDL’ de Apo B100 proteinine sahiptir ve kütlesinin % 25' ini oluĢturur. LDL, VLDL ‘nin yıkılmasından ya da direkt sentez yolu ile elde edilir. Plazmada taĢınmasını
sağlayan apoprotein B, E karaciğerde ya da ekstrahepatik organlarda bulunur. LDL’ nin % 43' ü B ve E reseptörlerine bağlanır. LDL apoproteininin yarı ömrü iki buçuk gündür. LDL’ nin birinci fonksiyonu steroid hormonu ve hücre membran sentezi için hücrelere kolesterol taĢımaktır. Bu hücrelerin yüzey membranlannda LDL reseptörü denen protein molekülleri bulunur. Bu LDL reseptörlerinin sayısı kandaki LDL’ nin majör göstergesidir. Reseptörlerin aktivite ve sayılan hayatın erken döneminde yüksektir. YaĢla birlikte azalma eğilimi gösterir. YaĢam boyu kolesterol ve doymuĢ yağlardan zengin diyet LDL reseptör aktivitesinin kronik supresyonuna yol açabilir. Hepatositler LDL reseptörleri içerir ve LDL bu reseptörlere bağlanır, endositoz ile alınır. Sıklıkla LDL reseptörleri hücre yüzeyinde yenilenirler. LDL kolesterol esterleri lizozomlarda lizozomal kolesterol esteraz ile hidrolize edilir. Sağlıklı insanlarda LDL’ nin % 70' i reseptörlere bağlanır.
LDL metabolitleri dolaĢımdan retiküloendotelyal sistem tarafindan uzaklaĢtırılır. Bu yola "scavenger-cell pathway" denir (53). Bu hücre reseptörlerine "asetil LDL reseptör" denir. Modifiye LDL oluĢur. Bu yolda normal LDL hücreleri bulunmaz. Okside ve modifiye LDL, makrofaj ve düz kaslarda kolesterol ve kolesterol ester Ģeklinde yığılır.
Aterosklerotik plak geliĢmesine yol açar (53).
HDL (High Density Lipoprotein):
HDL’ nin klinik önemini anlamak için metabolizmasını, sentez ve katabolizmasını anlamak gerekir. HDL metabolizması hakkındaki ilk bilgileri Eisenberg tanımlamıĢtır (49). HDL plazmada proteinler ile bir araya gelmektedir. Majör proteinler karaciğer ve bağırsaklarda sentez edilmektedir (50).
HDL 70-100 amstrong boyutunda 200.000-400.000 dalton ağırlığında makromoleküler protein-lipid kompleksidir. Dansitesi 1.063–1.021 gr/ml dir. Analitik ultrasantrifujdeki yerlerine göre HDL2 ve HDL3 diye ikiye ayrılırlar. HDL % 50 protein % 50 lipid içerir. Lipidlerin %32' si kolesterol esterleri, % 5' i serbest kolesterol, %55' i fosfolipid ve %8' i trigliseriddir. Protein içeriğinin % 70' i apo Al, % 20' si apo AII’dir (50). Apoproteinler immünaffinite kromotografi yöntemi ile gösterilir, üç tiptir. Apo A–1 only, apo Al, apo AH ve erich lipoproteindir.
HDL karaciğerde ve bağırsaklarda sentez edilir ve salgılanır (54). Bağırsak kökenli HDL apoprotein C içermez, yalnızca apoprotein A vardır. Çünkü apoprotein C yalnızca karaciğerde sentez edilir. Karaciğer tarafindan oluĢturulan olgunlaĢmamıĢ HDL apoprotein ve serbest kolesterol içeren disk Ģeklinde fosfolipid tabakasından oluĢur. Bu disk lesitin kolesterol acil transferaz (LCAT) tarafindan aynĢtınlır. Nikkile ve arkadaĢları HDL döngüsünü Ģekil 3 ile tanımlamıĢlardır (49).
HDL konsantrasyonları kolesterolün temizlenmesinin etkinliğini yansıttığından koroner ateroskleroz ile ters orantılıdır. HDL hücre yüzeyinden kolesterolün alımını kolaylaĢtırır. Kolesterol katalaz enzimi "lesitin cholesterol acyltransferaz" için bir substrat gibi kullanılır. Bu enzimatik reaksiyonun kofaktörü HDL'nin majör apoproteini Al’
dir.
HDL kolesterol seviyelerinin normal değerleri "Lipid Research Clinic Prevalence Study" tarafindan düzenlenmiĢtir. Klinik gözlem ve çalıĢmalar artan koroner kalp hastalıklarında HDL kolesterol seviyesinin düĢük olduğunu göstermiĢlerdir. Bu korelasyon yaklaĢık 30 yıl önce gözlemlenmiĢtir. Framingham HDL kolesterol ve koroner kalp hastalıkları insidansı hakkında 12 yıl devam eden bir çalıĢma yapmıĢtır ve göstermiĢlerdir ki HDL kolesterol koroner kalp hastalıklarında önemli koruyucu bir faktördür. "Lipid Research Clinic Primary Prevention Trial" tarafindan 7–10 yıllık bir sürede yapılan çalıĢmada HDL’ nin koroner kalp hastalıkları için koruyucu bir faktör olduğu saptanmıĢtır (55,56).
KarĢılaĢtırmalı olarak yapılan çalıĢmalarda HDL kolesterol seviyelerinin trigliserid seviyelerine bağlı olduğu görülmüĢtür. Koroner kalp hastalıklarına karĢı en fazla koruyuculuğu HDL 2 yapar (49,57).
Aterojenik indeksler: (T.Kolesterol/HDL-K, LDL-K/HDL-K)
Ateroskleroz hayatın erken yıllarında baĢlar.1915 yılında Saltykow '' çocukluk çağında ve gençlikte arterlerde özellikle aortadaki yağlı dejenerasyon hemen hemen bir Ģey değildir, ancak aterosklerozun baĢlangıcıdır'' diyerek bu konuya ilk yaklaĢımı yapmıĢtır (58).
Serum lipidlerinin ateroskleroz yapısı etkilerinin belirlenmesinde, aterojenik lipidlerin (T.kolesterol, LDL-K) anti aterojenik HDL-K’e oranı, tek tek T.kolesterol ve
LDL-K düzeylerinin ölçülmesinden daha önemlidir (59,60). Epidemiyolojik, klinik ve anjiografik çalıĢmalar ile aterosklerozun belirlenmesinde prediktif değerleri olan aterojen indeksler elde edilmiĢtir. Yüksek T.kolesterol/HDL-K, LDL-K/HDL-K, HDL3/HDL2, apoAll/apoAl, apoB/apoAı indeksleri artmıĢ ateroskleroz riskini göstermektedir (44,49).
Plazma Lipid Metabolizması ve Transportu
ġM’lar diyet ile alınıp barsaklardan absorbe edilen TG ve KE’lerini alıp duktus lenfatikuslardan dolaĢıma geçerler. DolaĢımda yapısındaki apo A1 ve ll’yi verip HDL-K’den apo C ve apo E alır. Kapiller endotel yüzeyindeki lipoprotein lipaz (LPL) tarafından hidroliz edilir ve yapısındaki TG’i hücrelere verir. Geriye kalan Ģilomikron kalıntıları karaciğere taĢınarak hepatik lizozomlarca hidrolize edilir. Açığa çıkan kolesterol hücre içinde kullanılır. Böylece ġM’lar diyetle alınan TG’leri periferik dokulara, kolesterolü ise karaciğere taĢırlar (3,44,47,48).
Karaciğerde sentezlenen VLDL TG’i yapısına alarak kana salınır. Kapillerlerden geçerken endotel LPL’ı ile TG’i dokulara bırakır. Bu arada apoproteinlerini de apoB 100 hariç kaybeder ve kolesterolce zengin VLDL kalıntıları da denen IDL’ler oluĢur. IDL’lerin yarısı karaciğer tarafından tutularak LDL’ye dönüĢtürülür. Böylece IDL’nin apoproteinine hepatositin tüm kolesterol içeriği yüklenerek plazmaya salınır (47,48).
Kolesterolün büyük bir kısmı sentezle oluĢurken az bir kısmı diyetle salınır. Kolesterol plazmadan safra asitlerine çevrilme ve feçesle nötral steroid Ģeklinde atılma ve steroid hormon sentezi ve katabolizma ürünlerinin idrarla atılması Ģeklinde iki Ģekilde atılır (61). Karaciğerde oluĢan VLDL kolesterolü plazmaya taĢır. Kolesterolün büyük kısmı VLDL’den oluĢan LDL’de bulunarak plazmada lipoprotein Ģeklinde taĢınır. Bir miktar kolesterol LCAT tarafından HDL’ye dönüĢtürülür. Kolesterol HDL ve LCAT ile ester halinde ekstrahepatik dokulardan karaciğere taĢınır (50,62).(Ģekil 4)
KARACĠĞER FONKSĠYON TESTLERĠ
Karaciğer lipit metabolizmasında önemli bir rol oynar. ġM kalıntılarını dolaĢımdan temizler ve VLDL’leri sentezler. IDL hepatik lipaz ile LDL’ye çevrilir. Hepatositler üzerinde çok yoğun olarak LDL reseptörleri bulunur. HDL prekürsör partikülleri ve bunları fonksiyonel hale getiren lesitin kolesterol açil transferaz (LCAT), serbest yağ asitlerinden keton cisimleri, kolesterolden safra asitleri, steroid ve D vitamini sentezi de karaciğerde olur. DıĢarıdan vücuda alınan ilaçların çoğu karaciğerde biyotransformasyona uğrayarak aktif ya da inaktif hale gelirler (63). YaĢamın erken evresinde yağ asidi oksidasyonu glikojenoliz ve glukoneogenezi tamamlayan önemli bir enerji kaynağı sunar. Kısmen karaciğerdeki kısıtlı ketogenez kapasitesine bağlı olarak yenidoğan bebekler uzamıĢ açlığa görece tahammülsüzdür. YaĢamın ilk birkaç gününde karaciğerin yağ asitlerini okside etme yeterliliğinde hızlı bir olgunlaĢma görülür. YaĢamın erken döneminde süt kalorinin en büyük kaynağını sunar; bu yüksek yağ, düĢük karbonhidratlı gıda, kan Ģeker seviyelerinin idamesi için aktif glukoneogenezi zorunlu kılar. Glukoz sunumu kısıtlı olduğunda endojen yağ asitlerinden keton cismi üretimi karaciğerdeki glukoneogenez için enerji ve beyin metabolizması için baĢka bir seçeneğini sağlar. Karbonhidrat bol olduğunda, karaciğer trigliseridleri üretir. Yağ lipoproteinleri içeren metabolik süreçler baskın olarak karaciğerdedir; karaciğerin olgunlaĢmamıĢ veya hastalığı, yağ düzeylerini ve lipoproteinleri etkiler (21). Konjugasyon reaksiyonları (ilaçları ve metabolitleri safra ile atılabilecek Ģekillere dönüĢtürülebilen) reaksiyonlar da karaciğer mikrozomal enzimleri tarafından yürütülür. Yenidoğan bebeklerde konjuge olmayan bilirubin kolaylıkla atılabilir, glukoromid konjugatına dönüĢtüren ve bilirubin atılımında hız kısıtlayıcı enzim olan UDP glukronil transferaz aktivitesi düĢüktür (21). AĠE hepatotoksisitesi doza bağlı, ilaç hipersensitivitesi ya da VPA’da olduğu gibi aberran ilaç metabolizmasına bağlı olarak idiosinkrazik tipte olabilir. CBZ’ye bağlı hepatotoksisite sıklıkla 3–4.haftada, VPA’e bağlı hepatotoksisite ilk 90 günde ortaya çıkar. AEĠ tedavisine baĢlanılmadan önce ve ilaç tedavisinin ilk birkaç ayı boyunca rutin karaciğer fonksiyonlarının düzenli aralarla en az ayda bir kez kontrolü gerekir (63,65).
Bir karaciğer hastalığı Ģüphesinin taranması veya doğrulanması için sıklıkla kullanılan labaratuar testleri; bilirubin, gamaglutamil transferaz (GGT) , alkalen fosfataz (ALP) ve transaminazlar; alanin aminotransaminaz (ALT), aspartat aminotransaminaz (AST) kontrol edilir (24,63).
Viral hepatit, ilaç veya toksinle baĢlatılan karaciğer hastalığı Ģok, hipoksemi veya metabolik hastalıktaki akut karaciğer hasarı (parankimal hastalık) en iyi Ģekilde serum aminotransferaz düzeylerindeki belirgin artıĢlarla yansıtılır. Alanin aminotransferaz (ALT) karaciğere özgü iken, aspartat aminotransferaz (AST) karaciğere ek olarak diğer organlardan da türer. Hem AST hem de ALT seviyelerindeki en belirgin yükseklikler, akut karaciğer hücre hasarı ile görülebilir-birkaç bin katlık bir yükselme; akut viral hepatit, toksik hasar, hipoksi ve hipoperfüzyondan kaynaklanabilir. Kolestaz (tıkayıcı sarılık) safra bileĢenlerinin serum içerisine geri kaçıĢını içerir; total veya konjuge serum bilirubin düzeyleri ve serum safra asitleri yükselmiĢtir (21). Serum GGT yüksekliği hepatoselüler hastalıkta orta dereceli, obstrüktif hastalıkta ise daha fazladır. GGT karaciğer, böbrek ve pankreasta bulunur. Mikrozomal bir enzimdir. AEĠ’ler GGT sentezini indükler. AEĠ kullanımında %90 olguda GGT yükselmektedir (63,64,66). Karaciğerin yapım iĢlevini serum albümin ve protein düzeyleri ve protrombin zamanı (PT) veya uluslar arası normalleĢtirilmiĢ oran (INR) yansıtmaktadır (21). Alkalen fosfataz (ALP) karaciğer, kemik, ince barsaklar, plasenta ve böbreklerde bulunur. Serum ALP’nın çoğu hepatobiliyer ve osteoblast orijinlidir. Fizyolojik olarak kemik büyümesine bağlı olarak özellikle sütçocukluğu ve puberte döneminde serum ALP’ı yüksektir. Normal değeri yaĢa ve cinsiyete bağlıdır (66,67).
GEREÇ VE YÖNTEM
AraĢtırmanın TürüBu araĢtırma, epilepsi nedeni ile izlenen, CBZ veya VPA monoterapileri ile tedavi edilen çocuklarda bu ilaçların bu ilaçların serum lipidleri ve karaciğer enzimleri üzerindeki etkilerinin gözlenmesi amacıyla ilaçların kullanım sürelerine göre serum lipit ve karaciğer fonksiyon testlerinin karĢılaĢtırıldığı prospektif bir çalıĢmadır.
AraĢtırmanın Yapıldığı Yer
ÇalıĢma Dicle Üniversitesi Tıp Fakültesi (DÜTF) Çocuk Sağlığı ve Hastalıkları Anabilim Dalı, Çocuk Nöroloji Polikliniği’nde epilepsi tanısı ile izlenen, CBZ veya VPA tedavisi alan hastalar alındı. Tüm hastalar interiktal dönemde, rutin kontrol döneminde iken incelendiler.
AraĢtırmanın Evreni ve Örneklemi
1 Eylül 2000–1 Eylül 2008 tarihleri arasında DÜTF Çocuk Sağlığı ve Hastalıkları Anabilim Dalı Çocuk nöroloji polikliniğinde izlenen, 1 -15 yaĢ arasında epilepsi tanısı alan toplam 1125 hasta araĢtırmanın evrenini oluĢturur. AraĢtırma grubundaki hastaların ailelerine bilgi verilerek izinleri alındı. ÇalıĢma koĢullarını karĢılayan toplam 128 hasta çalıĢmaya katıldı.
ÇalıĢmaya alınan hastalar için koĢullar;
a) Epilepsi tanısı almıĢ olan çocuk hastalar,
b) Epilepsi dıĢında baĢka hastalık tanısı almayanlar (kraniyal patolojiler dahil),
c) Tekli CBZ veya VPA tedavisi alan ve bu ilaçları 3 aydan daha kısa veya 1 yıldan daha uzun süredir kullanan hastalar,
d) BaĢka bir hastalık nedeniyle düzenli ilaç kullanmayan e) Metabolik hastalık belirti ve Ģüphesi olmayan
f) Kan ilaç düzeyi normal sınırlarda izlenen hastalar çalıĢmaya alındı.
Bu koĢullar altında CBZ ve VPA kullanan hastalar kendi aralarında ilacı 3 aydan daha kısa süre ve 1 yıldan daha uzun süre ilacı kullananlar olmak üzere iki gruba ayrıldı.
Veri Toplama
AraĢtırmanın yapılması amacıyla çalıĢmaya katılan hastalardan 8–12 saatlik açlık sonrası sabah saat 08.00–09.00 arasında 5 ml venöz kan alınmıĢtır. Alınan kan örnekleri DÜTF Biyokimya Laboratuarı’nda çalıĢılmıĢtır. Alınan kan örneklerinden çalıĢılan biyokimyasal parametreler;
Total Kolesterol: Abbott firmasının enzimatik yöntemi ile çalıĢan hazır kiti kullanılarak Architect C 16000 otoanalizöründe çalıĢılmıĢtır. Kolesterol esterleri enzimatik olarak kolesterol esteraz ile kolesterol ve serbest yağ asitlerine hidrolize olur. Serbest kolesterol kolesterol oksidaz ile okside edilir. Meydana gelen hidrojen peroksit hidroksibenzoik asit ve 4-aminoantipirin ile birlikte quinoneimine oluĢumu esasına dayanır.
Trigliserid: Abbott firmasının gliserol fosfat oksidaz kalorimetrik metoduna dayalı kiti ile Architect C 16000 otoanalizöronde çalıĢılmıĢtır. Trigliseridler enzimatik olarak lipaz tarafından yağ asitlerine ve gliserole hidrolize edilirler. Peroksidaz ile katalize edilen bir renkli reaksiyonda,H2O2 kırmızı renkli bir boya oluĢturmak için 4-aminoantipirin (4-AAP) ve 4-klorofenol (4-CP) ile reaksiyona girer. Bu boyanın absorbansı örnekteki trigliserid varlığının konsantrasyonu ile orantılıdır.
HDL-K, LDL-K: Direk plazma veya serumda direk HDL kolesterol konsantrasyonu ölçülür. LDL-K Friedewald Formülü’ne göre hesaplanmıĢtır: LDL-K:Total kolesterol-(TG/5+HDL).
Karaciğer Fonksiyon Testleri: Abbott firmasının Architect C 16000 otoanalizöründe AST, ALT, GGT, ALP, T.biluribin, D.bilirubin, Ġndirek bilirubin, laktat dehidrogenaz ve albümin hazır kitlerle çalıĢılmıĢtır.
Ġstatisitksel Analiz
Sürekli değiĢkenlerin ortalama ve standart sapma değerleri ( X ± SD) tanımlayıcı istatistikler olarak kullanıldı. Ġki grubun karĢılaĢtırılmasında '' iki bağımsız grup ortalamasını karĢılaĢtıran Student’s t testi ''kullanıldı. Test aĢamasında hipotezler çift yönlü kabul edilerek, yanılma olasılığı p< 0.05 olduğunda önemli farklılık kabul edildi. Ġstatistik analizler; SPSS 15,0 for Windows (SPSS, Inc. Chicacgo, ILL,USA) paket programı kullanılarak yapıldı.
AraĢtırmanın Sınırlılıkları
AraĢtırmada planlanan örneklem sayısı; bazı hastaların dahil etme kriterlerine uymamaları, katılmayı kabul etmemeleri nedeniyle azaltılmak zorunda kalınmıĢtır. Bu Ģekilde olgular özellikle karbamazepin grubunda olmuĢtur.
ÇalıĢma grubunda yer alan olguların çocukluk yaĢ grubunda olmalarına bağlı olarak, izlemi yapılan labaratuar verilerinin alt ve üst sınırları tüm olgular için eĢit değildir. Ancak bu araĢtırma grubundaki toplam hasta sayısı, yaĢ sınırlarına göre grup oluĢturmak için yeterli sayıda değildir.
Literatürde çocuklarda yapılan araĢtırmalar oldukça kısıtlı olduğundan daha çok eriĢkinlerde yapılan çalıĢmalar ile karĢılaĢtırma yapılmıĢtır.