T. C.
EGE ÜNİVERSİTESİ TIP FAKÜLTESİ
FİZİKSEL TIP VE REHABİLİTASYON ANABİLİM DALI
NÖROPATİK AĞRISI OLAN HASTALARDA QST FENOTİPLERİ İLE FONKSİYONEL MANYETİK REZONANS GÖRÜNTÜLEME (fMRI)
PATERNLERİNİN İLİŞKİSİ
Uzmanlık Tezi Dr. Göksel Tanıgör
Tez Danışmanı Prof. Dr. Simin Hepgüler
ii İçindekiler ÖNSÖZ ... iv ÖZET ... v ABSTRACT ... vii TABLOLAR ... ix KISALTMALAR ... x GİRİŞ VE AMAÇ ... 1 1. GENEL BİLGİLER ... 2
1.1 SERVİKAL DİSK BOZUKLUKLARI VE RADİKÜLOPATİ ... 2
1.1.2 Servikal bölge anatomisi ... 2
1.1.3 Boyun ağrısı ... 7
1.1.4 Servikal disk bozuklukları ... 9
1.1.5 Servikal radikülopati ... 12
1.2 NÖROPATİK AĞRI ... 14
1.2.1 Nöropatik ağrı patofizyolojisi ve mekanizmaları ... 16
1.2.2 Nöropatik ağrıda öykü, semptom ve bulgular ... 20
1.2.3 Nöropatik ağrıda tanısal süreç, QST ve tanısal teknikler ... 21
1.2.4 Nöropatik ağrı tedavisi ... 25
1.2.5 Fonksiyonel manyetik rezonans görüntüleme ... 30
2. GEREÇ VE YÖNTEM ... 32
2.1 Katılımcıların özellikleri ... 32
2.2 Hastaların değerlendirilmesi ve ölçütler... 34
2.3 İstatistiksel yöntem ... 42
3. BULGULAR ... 42
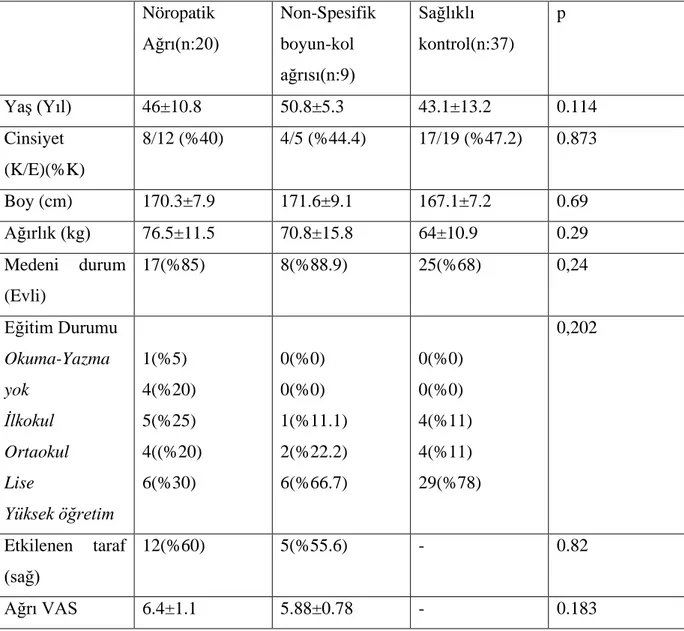
3.1 Demografik özellikler ve hastalık özellikleri ... 43
3.2 Hastaların QST değerlerinin karşılaştırılması ... 45
iii
4. TARTIŞMA... 56
5. SONUÇ...65
6. KAYNAKLAR ... 66
7. EKLER ... 82
EK-1 Olgu rapor formu ... 82
iv ÖNSÖZ
Uzmanlık eğitimim boyunca hem meslek eğitimimde, hem de bireysel anlamda bana her konuda büyük destek ve katkıları olan, yol gösteren başta anabilim dalı başkanımız sayın Prof. Dr. Yeşim KİRAZLI olmak üzere, değerli hocalarım Prof. Dr. Berrin DURMAZ, Prof. Dr. Simin HEPGÜLER, Prof. Dr. Yeşim AKKOÇ, Prof. Dr. Arzu ON, Prof. Dr. Kazım ÇAPACI, Prof. Dr. Cihat Öztürk Prof. Dr. Sibel EYİGÖR, Prof. Dr. Funda ATAMAZ ve Doç. Dr. Hale KARAPOLAT’a içtenlikle teşekkür ederim.
Ayrıca, tezimin her aşamasında destek ve yardımlarını gördüğüm tez danışmanı sayın hocam Prof. Dr. Simin HEPGÜLER’e şükranlarımı sunarım.
Çalışmanın gerçekleştirilme sürecindeki emeklerinden dolayı Ege Üniversitesi Tıp Fakültesi Radyoloji Anabilim Dalı Nöroradyoloji Bilim Dalı Öğretim Üyesi sayın hocam Prof. Dr. Cem Çallı ve Ege Üniversitesi Tıp Fakültesi Anestezi Anabilim Dalı Algoloji Bilim Dalı Öğretim Üyesi sayın hocam Prof. Dr. Meltem Uyar’a teşekkürlerimi sunarım. Tezimin istatistiğinde yardımcı olan Sayın Doç. Dr. Timur KÖSE ve Dr. Onur ÖZYURT’a teşekkür ederim. Tez çalışmam boyunca vaktini ve yardımlarını esirgemeyen Sayın Uzm. Dr. İdris Köken’e ve onunla geçirebilecekleri değerli zamanlarını bu çalışmaya vermeyi kabul eden ailesine teşekkür ederim.
Uzmanlık eğitimim süresince daima destek ve dostluklarını gördüğüm tüm doktor arkadaşlarıma, kliniğimizin tüm fizyoterapist, hemşire, teknisyen ve personeline teşekkür ederim.
Çalışmada yer almayı kabul ederek bana değerli zamanlarını ve incelemeler sırasında katılım ve anlayışlarını eksik etmeyen değerli hastalarımız ve gönüllülerimize teşekkür ederim.
Tüm eğitim yaşamım boyunca beni yalnız bırakmayarak her konuda destek olan sevgili annem Zeynep Aysan Tanıgör ve sevgili babam Mehmet Emin Tanıgör’e sonsuz teşekkürlerimi sunarım.
En mutlu ve en çaresiz anlarımı paylaştığım, tüm zorluklarda hep yanımda olan, gerek fikirleri, gerekse manevi desteği ile hayatıma anlam katan değerli eşim Ezgi Karagöz Tanıgör’e sonsuz teşekkür ederim.
Dr. Göksel Tanıgör İZMİR, 2020
v ÖZET
Amaç: Bu çalışmanın amacı nöropatik ağrı ile giden servikal radikülopatilerde QST ve fMRG değişikliklerinin ve aralarındaki ilişkilerin belirlenmesidir. Çalışmanın bir diğer amacı ise QST değerlendirmesine göre hiperaljezik veya hipoestezik olarak belirlenen hastalarda fMRG bulgularında farklılık olup olmadığını değerlendirmektir.
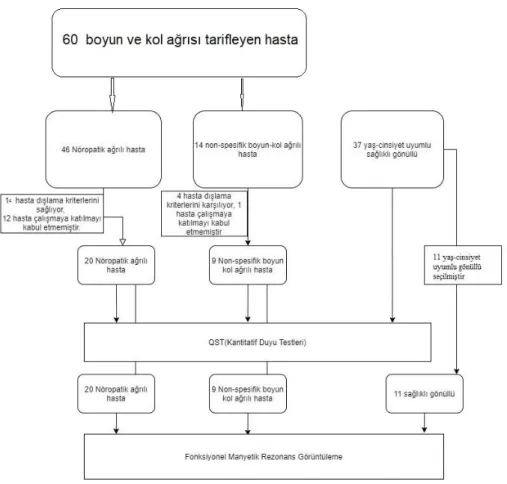
Gereç ve yöntem: Çalışmaya nöropatik ağrılı(NA) (n:20), nöropatik olmayan boyun-kol ağrılı (NNA)(n:9) ve sağlıklı gönüllüler (n:37) olmak üzere 66 katılımcı dahil edilmiştir. Katılımcıların sosyodemografik ve klinik verileri alındıktan sonra PainDetect (PD) anketi uygulanmış, ardından QST analizi ve toplam 40 hastaya her iki ekstremitenin ayrı ayrı sensoryal olarak uyarımını içeren fMRG tetkiki gerçekleştirilmiştir.
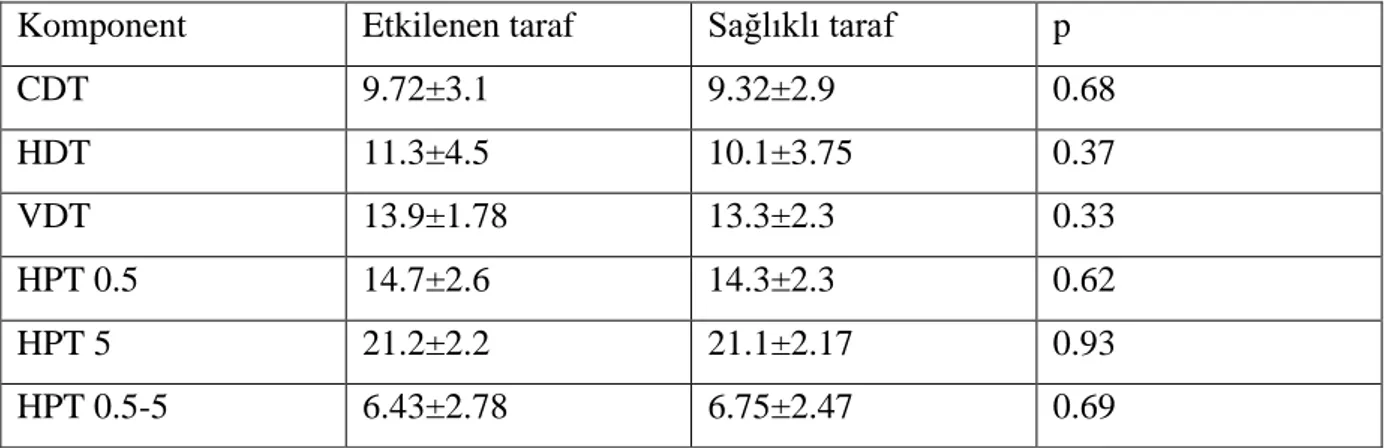
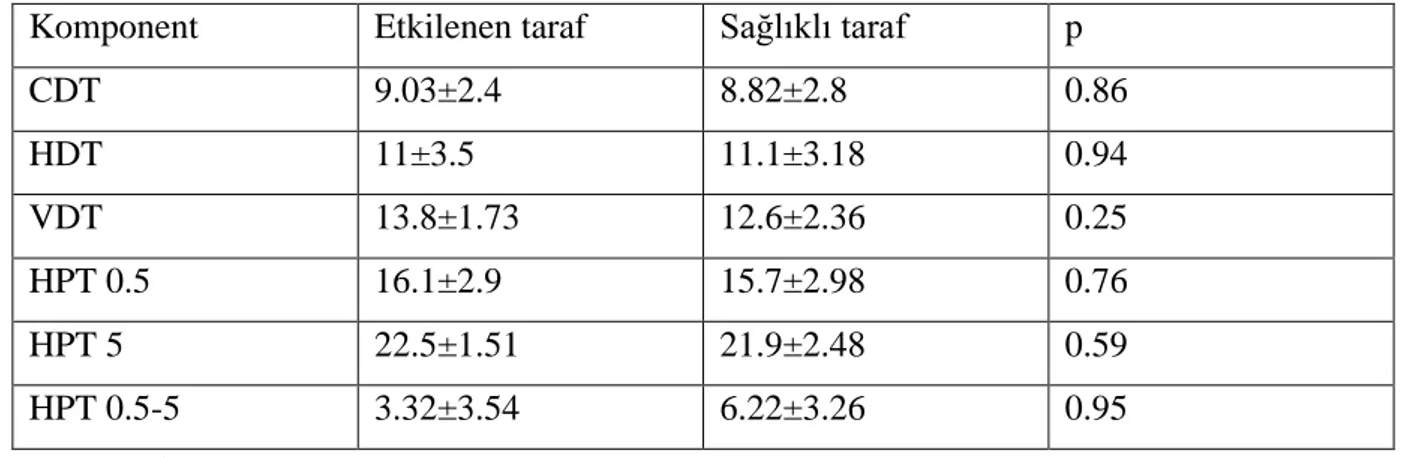
Bulgular: Çalışma sonucunda QST’de ağrı tarifleyen hasta gruplarında QST’nin komponentleri olan CDT(Soğuk tespit eşiği), HDT(Sıcak tespit eşiği), VDT(Vibrasyon tespit eşiği) ve HPT(Sıcak ağrı eşiği) değerlerinde iki ekstremite(ağrılı ve ağrılı olmayan) arasında fark saptanmamıştır (p>0,05).
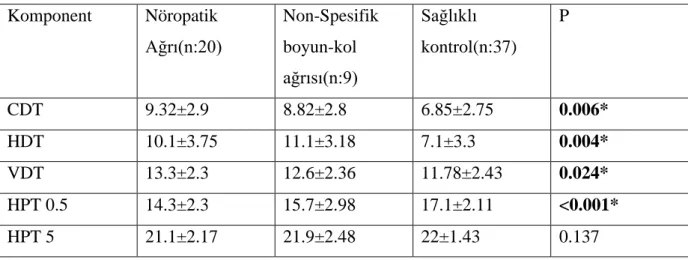
Gruplar arası analizlerde duyusal eşiği gösteren CDT, HDT ve VDT testleri, NA ve NNA gruplarında sağlıklı gönüllülere göre daha yüksek, ağrı eşiğini gösteren testlerden HPT 0.5 testi ise düşük saptanmıştır(p<0.05). Bu değişiklikler hem ağrı tariflenen, hem de tariflenmeyen ekstremitelerde gösterilmiştir.
fMRG sonuçlarında sol taraflı NA tarifleyen hastalarda sağlıklı gönüllülere göre frontal pol ve superior frontal gyrus bölgelerinde daha düşük BOLD yanıtı izlenmiştir(p<0.05).
QST’ye göre hipoestezik NA grubunda, sağlıklı gönüllülere göre, ağrısız ekstremitelerinde daha düşük bir somatosensoryal korteks aktivitesi saptanmıştır(p<0.05). QST’ye göre tek taraflı hiperaljezik NA grubunda ağrılı tarafta daha düşük bir somatosensoryal korteks aktivitesinin yanında, hiperaljezi bilateral ise operculum ve insular kortekste de daha düşük BOLD aktivitesi saptanmıştır(p<0.05).
Sonuç: NA ve NNA hastalarının QST değerlerinin sağlıklı gönüllülere göre farklılıklar gösterdiği saptanmıştır. Nöropatik ağrılı hastalarda QST ile özellikle iki taraflı hiperaljezi tespit edilen
vi hastaların santral sinir sisteminde fMRG ile uyarım sonucu kronik ağrı ile ilişkilendirilmiş olan bölgelerde aktivite artışı saptanırken, alt grup olmaksızın tüm hasta gruplarının karşılaştırmasında anlamlı bir farklılık gösterilememiştir.
NA’lı hastalarda kantitatif duyu testlerindeki değişikliklere santral fonksiyonel değişiklikler de eşlik ederken, NNA hastalarda bu değişiklikler gözlenmemiştir.Bu bulgular özellikle duyusal değişikliklere sebep olan nöropatik ağrıda santral mekanizmaların da rolü olduğunu düşündürmektedir.
Çalışma servikal radikülopatili hastalarda nöropatik ağrı ile ilişkili periferik ve santral değişiklikleri inceleyen ilk çalışma niteliğindedir. Ancak bu ince ve detaylı mekanizmaların aydınlatılabilmesi için daha fazla çalışmaya ihtiyaç vardır.
vii ABSTRACT
Objectives: The aim of this study is to determine QST and fMRG changes and show their possible relationships in cervical radiculopathy patients with neuropathic pain. Another aim of the study is to evaluate whether there is a difference in fMRI findings in patients who are determined as hyperalgesic or hypoesthetic according to the QST assessment.
Materials and methods: 66 participants were included in the study, including neuropathic pain (NA) (n: 20), non-neuropathic neck-arm pain (NNA) (n: 9) and healthy volunteers (n: 37). After obtaining the socio-demographic and clinical data of the participants, the PainDetect (PD) questionnaire was performed, followed by QST analysis and fMRI examination, which included sensory stimulation of both extremities in a total of 40 patients.
Results: Analyses between painful and non-painful extremities yielded no differences in CDT (Cold detection threshold), HDT (Hot detection threshold), VDT (Vibration detection threshold) and HPT (Heat pain threshold) with QST, in all groups (p> 0.05).
CDT, HDT and VDT tests, which showed sensory thresholds, were found to be higher in the NA and NNA groups compared to healthy volunteers, and HPT 0.5 test was found to be lower in the tests showing pain threshold (p <0.05) in the intergroup analyses. The changes described were found in both painful and non-painful limbs.
In patients who described left-sided NA in the fMRI results, a lower BOLD response was observed in the frontal pol and superior frontal gyrus regions compared to healthy volunteers (p <0.05).
In the hypoesthetic NA group, a lower somatosensory cortex activity was found in non-painful limbs compared to healthy volunteers (p <0.05). In the unilateral hyperalgesic NA group a lower somatosensory cortex activity was found on the painful side, and if the hyperalgesia was bilateral, a lower BOLD activity was also found in the operculum and insular cortex (p <0.05).
Conclusion: The QST values of NA and NNA patients were shown to be different compared to healthy volunteers. An increased fMRI activity was detected in regions associated with chronic pain in patients with bilateral hyperalgesia, but no significant difference was observed in the intergroup analyses including all patients, regardless of the QST findings.
viii While changes in the quantitative sensory tests in patients with NA were accompanied by central functional changes, these changes were not observed in NNA patients. These findings suggest that central mechanisms also play a role in neuropathic pain causing sensory changes.
The study is the first study to examine peripheral and central changes associated with neuropathic pain in patients with cervical radiculopathy. However, more studies are needed to clarify these fine and detailed mechanisms.
ix TABLOLAR
Tablo 1: Boyun ağrısı etyolojisi Tablo 2: Nöropatik ağrının sebepleri
Tablo 3: Nöropatik ağrıda pozitif ve negatif semptomlar Tablo 4: Hastaların demografik ve klinik özellikleri Tablo 5: Nöropatik ağrılı hastaların ağrı özellikleri
Tablo 6: Nöropatik ağrılı hastalarda etkilenen taraf ile sağlam taraf arası QST karşılaştırması Tablo 7: Non spesifik boyun ve kol ağrılı hastalarda etkilenen taraf ile sağlam taraf arası QST karşılaştırması
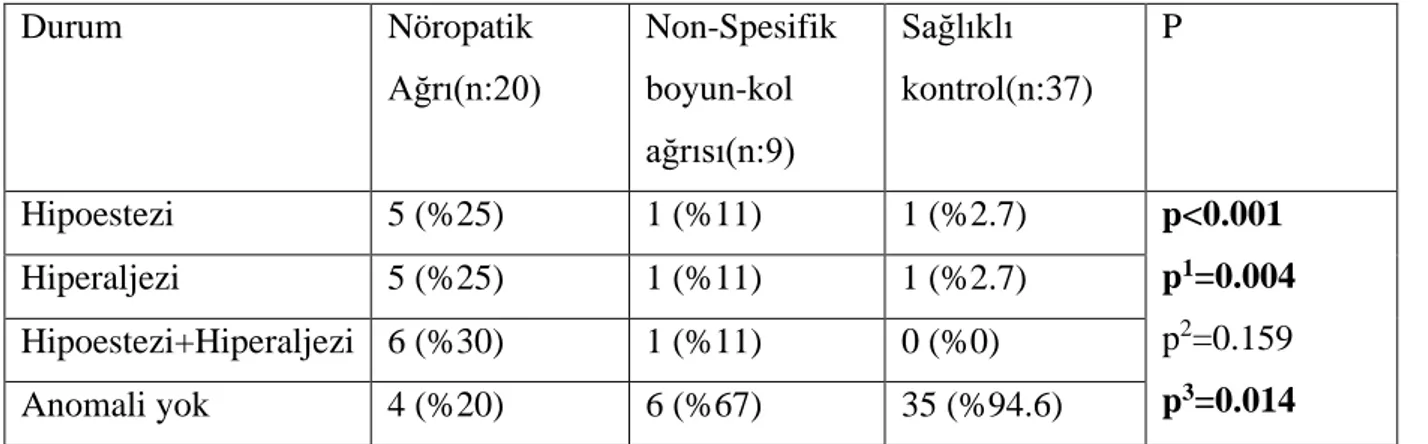
Tablo 8: Ağrılı taraflarla, kontrol QST değerlerinin gruplar arası karşılaştırılması Tablo 9: Sağlam taraflarla, kontrol QST değerlerinin gruplar arası karşılaştırılması Tablo 10: Gruplarda tanımlanan hipoestezi ve hiperaljezi sıklıkları
FİGÜRLER Şekil 1: Çalışmanın akış şeması
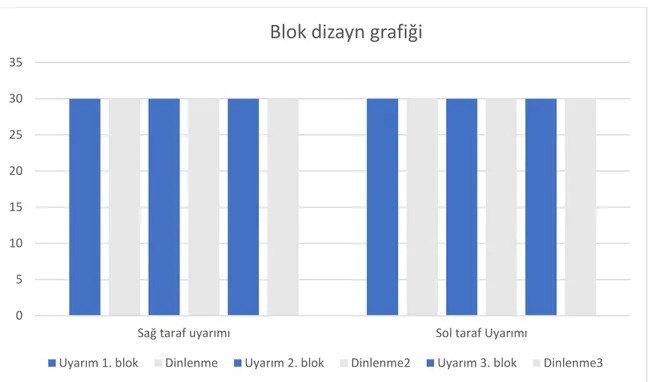
Şekil 2: Blok dizayn grafiği
Şekil 3: Sağ ekstremitenin etkilendiği nöropatik ağrılılar ile sağlıklı grupta, sol el aktivasyonu ile elde edilen BOLD yanıtları
Şekil 4: Sol ekstremitenin etkilendiği nöropatik ağrılılar ile sağlıklı grupta, sol el aktivasyonu ile elde edilen BOLD yanıtları
Şekil 5: Hipoestezi saptanan nöropatik ağrı grubunda, şikayetin olmadığı tarafın uyarımı ile elde edilen BOLD yanıtları
Şekil 6: Her iki tarafta hiperaljezi saptanan nöropatik ağrı grubunda, şikayetin olmadığı tarafın uyarımı ile elde edilen BOLD yanıtları
Şekil 7: Her iki tarafta hiperaljezi saptanan nöropatik ağrı grubunda, şikayetin olduğu tarafın uyarımı ile elde edilen BOLD yanıtları
Şekil 8: Lezyonun olduğu tarafta hiperaljezi saptanan nöropatik ağrı grubunda şikayetin olduğu tarafın uyarımı ile elde edilen BOLD yanıtları.
1
KISALTMALAR
ASL: Arteral Spin Labeling (Arteryal dönüş etiketlemesi) ATP: Adenozin Trifosfat
BOLD: Blood Oxygen Level Dependent (Kan oksijen seviyesine bağlı yanıt) CDT: Cold Detection Threshold (Soğuk tespit eşiği)
HDT: Heat Detection Threshold (Sıcak tespit eşiği) HPT: Heat Pain Threshold(Sıcak ağrı eşiği)
VDT: Vibration Detection Threshold (Vibrasyon tespit eşiği) DN4: Douleur Neuropathique 4 (4 Soru Nöropatik Ağrı Anketi) fMRG: Fonksiyonel Manyetik Rezonans Görüntüleme
GABA: Gama Amino Bütirik Asit
GRE: Gradient Refocused Echo (Değişken yeniden odaklanmalı yankı)
LANSS: Leeds Assessment of Neuropathic Symptoms and Signs (LANSS ağrı skalası) LEP: Laser Evoked Potentials (Laser uyarımlı potansiyeller)
MMP: Matriks metalloproteinaz
NPQ: Neuropathic Pain Questionnaire (Nöropatik Ağrı Anketi)
NPSI: Neuropathic Pain Symptom Inventory (Nöropatik Ağrı Semptom Envanteri) NSAİİ: Non-steroidal Anti-İnflamatuvar İlaçlar
NNBKA: Non-nöropatik boyun-kol ağrısı
PDQ: PainDETECT Questionnaire (PainDETECT anketi) QST: Quantitative Sensory Testing (Kantitatif Duyu Testi) SNRI: Serotonin-Norepinefrin Gerialım İnhibitörü
TRPV: Transient potential cation channel V member 1 (Geçici potansiyel katyon kanalı 1)
1
GİRİŞ
Nöropatik ağrı çoğunlukla merkezi sinir sistemi veya periferik sinir sisteminin herhangi bir yerinde oluşan sinir hasarı veya iletim bozukluğu sonucu oluşan, diğer duyusal veya motor fonksiyon bozukluklarının da eşlik edebildiği bir ağrı tipidir. Uluslararası Ağrı Çalışmaları Birliği (IASP) tarafından somatosensoriyel sistemdeki lezyon veya hastalığa bağlı olarak ortaya çıkan ağrı olarak tanımlanmaktadır (1). Diğer ağrı türlerinden farklı olarak nöropatik ağrılar tedaviye çoğunlukla daha dirençlidir ve kronikleşmeye meyillidir(2).
Servikal radikülopati, nöropatik ağrı ile seyredebilen birçok patolojiden birisidir. Servikal radikülopati, boyundaki sinir köklerinin irritasyon veya basısı sonrası üst ekstremitedeki motor kayıpları ve eşlik eden duyusal bozuklukları ifade eder. Yapılan çalışmalarda gerek servikal, gerekse lomber bölgede radiküler etkilenmeyi düşündürecek disk patolojilerinde nöropatik ağrı komponentinin %30-50 arasında olduğu saptanmıştır(3, 4).
Son dönemlerde yapılan araştırmalarda nörolojik testlerin standardize edilmesi ve tekrarlanabilmesi amacıyla çeşitli teknikler geliştirilmiştir. Bu tekniklerden birisi de QST (Quantitative Sensory Testing)’dir (5). QST duyusal muayene uygulamalarının standardize edilmiş, kimileri dijitalize platformlar aracılığı ile uygulanan, verilen stimulusların şiddet ve özelliklerinin ölçülebildiği bir testtir. İçeriğinde sıcak, soğuk, titreşim ve dokunma duyusu gibi farklı duyu modaliteleri ölçülür. QST ağrının özellikleri ve eşlik eden duyusal değişikliklerin yanında ek istatistik yöntemler ile ortak özellikler gösteren ağrı profillerinin fenotiplendirilmesini de sağlar. Ağrı fenotiplemesi için birçok sınıflama bulunsa da, temel bakış açısı fonksiyon kazancı ve kaybı üzerinedir. Özellikle hiperaljezi ve hipoestezi varlığı bu fonksiyonel değişikliklerde temel alınan ölçütlerdir. Farklı QST fenotiplerinin farklı tedavilere daha iyi yanıt verdiği de gösterilmiştir(6). Farklı mekanizmalar ile oluştuğu düşünülen bu fenotiplerin merkezi sinir sisteminde oluşturduğu yansımalar hakkında yapılan çalışma sayısı azdır, çalışmalarda çoğunlukla periferik patofizyoloji ön planda değerlendirilmiştir.
Beyindeki fonksiyonun değerlendirilmesi için kullanılmakta olan yöntemlerden birisi fMRG (Fonksiyonel Manyetik Rezonans Görüntüleme)’dır. fMRG temel olarak fonksiyon gerçekleştirmekte olan bölgedeki kan akımındaki değişikliklerin ölçümüne dayanır(7). Kan akımında oluşan artış sonucu bölgesel oksijen seviyelerinde meydana gelen değişiklik BOLD (Blood Oxygen Level Dependent) yanıtını geliştirmektedir. Periferik sinir sistemindeki
2
ağrıların farklı lifler ve yolaklar ile iletildiği düşünüldüğünde bu farkların kortikal düzeylere yansıması da muhtemeldir(8).
Nöropatik ağrıda fMRG kullanımı ile ilgili birçok çalışma mevcuttur (9). Buna rağmen servikal disk bozukluğu seyrinde gelişen nöropatik ağrıya özgü bir çalışma yer almamaktadır, çalışmaların çoğunda ağrı etyolojisi heterojenite göstermektedir. Bunun yanında nöropatik etkilenimin olmadığı kronik ağrılı hastaları inceleyen çalışmalar da literatürde mevcuttur(10). Bu çalışmanın amacı nöropatik ağrı komponenti bulunan servikal radikülopatilerde QST ve fMRG bulgularını sağlıklı gönüllüler ve nöropatik olmayan boyun-kol ağrılı hastalar ile karşılaştırmaktır. Çalışmanın bir diğer amacı ise QST’ye göre hiperaljezik veya hipoestezik olarak belirlenen hastalarda fMRG ile var olabilecek farklı santral bulguları değerlendirmektir.
Servikal Bölge Anatomisi Kemik yapılar
Boyun omurgası, yedi omurdan oluşmuştur ve öne doğru' lordoz' adı verilen bir eğime sahiptir. Komplike bir eklem yapısına sahiptir ve omurganın en hareketli bölümüdür. Başın dengede durmasını ve hareket etmesini sağlar.
Boyundaki omurga kemikleri, servikal(cervical) vertebranın baş harfi olan C ile başlayan, ardından da bir rakam ile yukarıdan aşağıya sıralarının ifade edildiği bir isimlendirmeye sahiptir(C1-C7).
Bu kemiklerden C1 diğer adıyla Atlas, diğer vertebralardan farklı bir şekle sahiptir, massa lateralis denilen yapılar aracılığı ile kafa kemikleri ile eklem yapar. C1 vertebrasının spinöz çıkıntısı yoktur. Atlas kemiğinin yapısı Resim 1’de gösterilmiştir.
3
Resim 1: C1 vertebra (Atlas)(11)
C2’nin diğer adı Axis’tir, temel özelliği dens axis adı verilen çıkıntı aracılığıyla Atlas ile eklem yapmasıdır. Axis Resim 2’de temel yapıları ile gösterilmiştir.
Resim 2: C2 vertebranın anatomisi(11)
C3 ve C7 arasında kalan vertebralar, servikal vertebraların tipik özelliklerini taşırlar. Korpuslarının yanında unsinat çıkıntı denilen çıkıntılar yer almaktadır. Vertebral arkuslarının
4
pedikülleri üzerinden yana doğru transvers çıkıntılar bulunur. Bu transvers çıkıntılarda oluklar vardır ve bu oluklardan spinal sinirler geçer. Transvers foramenlerin içerisinden ise vertebral arterler, venler ve sempatik sinirler geçmektedir. C7’yi farklı kılan özellik ise spinöz çıkıntısında çatallanmanın olmaması ve diğer servikal vertebralardan daha uzun bir spinöz çıkıntıya sahip olmasıdır(12). Bu özelliği ile vertebra prominens (belirgin-çıkıntılı) ismini alır. Servikal vertebranın yapısı Resim 3’te gösterilmiştir.
Resim 3: Servikal vertebradaki önemli yapılar(11)
Eklemler ve ligamanlar:
C1 ve oksiput arasında bulunan atlanto-oksipital eklemin temel görevi fleksiyon-ekstansiyon ve lateral fleksiyon hareketlerinin gerçekleştirilmesidir. Bunun yanında bu eklemin çevresinde birçok ligaman bulunur, bu ligamanların görevi hem destek olmak, hem de spinal kordu korumaktır(13).
C1 ve C2 arasında ise birbirinden bağımsız 3 eklem bulunmaktadır. Bu eklemler başın rotasyonuna, atlantoaksiyal eklem ise fleksiyon ve ekstansiyonuna katkıda bulunurlar. Eklemin stabilitesi, başta transvers ligaman olmak üzere ligamentöz yapılar ile sağlanır. Bu eklemde intervertebral disk yoktur. C1-C2 ekleminin aksine diğer servikal vertebralar arasında disk bulunur. İntervertebral diskin periferi anulus fibrozus adı verilen bağ dokusu fibrillerinden oluşur. Merkezinde ise nükleus pulpozus adı verilen yumuşak kıkırdak yapı yer alır. Nükleus pulpozus esasen embriyonik dönemde notokordun artığıdır. Büyük ölçüde mukopolisakkaritlerden oluşur. İntervertebral diskin temel görevi şok absorbsiyonudur. Vasküler yapılar yalnızca periferde bulunur. Merkez ise difüzyon yolu ile beslenir(13).
5
Vertebralar arasında birçok ligaman bulunur. Korpusların önü ve arkasından sırasıyla anterior longitudinal ligaman ve posterior longitudinal ligaman geçer. Bunun dışında arkuslar arasında ligamentum flavum uzanır. Nuchal ligaman ise oksipital protuberensten başlayıp C7’nin spinöz çıkıntısına kadar uzanır ve başın taşınmasını sağlar(14).
Vertebraların posterior bölgesinde ise faset eklemler (zigapofizial) yer almaktadır. Bu vertebraların superior ve inferiorartiküler prosesleri tarafından oluşturulan bir eklem türüdür. Kapsüllü bir eklem yapısı olan faset eklemler, boyunda horizontal uzanım gösterir ve her yöne harekette katkıda bulunurlar.
Kaslar
Servikal omurga çevresindeki kaslar için birçok sınıflandırma bulunmakla beraber ön, yan ve arka bölüm kasları olmak üzere 3 temel grupta incelenebilirler. Boyun kaslarının bir kısmı Resim 4’de gösterilmiştir.
6
Resim 4: Boyun kasları(11)
Ön grup kasları prevertebral kaslar ismini alırlar. M Longus Colli, M Longus Capitis ve M Rectus Capitis öndeki kas gruplarıdır. M Longus Colli’nin temel görevi servikal fleksiyon iken, M Rectus Capitis’in lateral bölümü lateral fleksiyonu sağlar. Bu kasların innervasyonu temel olarak C1 ve C2 spinal sinirler ile gerçekleşir.
Yan grupta bulunan kaslar; anterior, medius ve posterior olmak üzere üç grupta incelenen skalen kaslardır. Yüzün karşı tarafa çevrilmesi sırasında boynun aynı yöne çekilmesinde görev aldıkları gibi inspirasyona da yardımcı olurlar. Ön gruptan farklı olarak innervasyonları C4-C8’den sağlanır.
Arka grup derin kaslar ise M Rectus Capitis Posterior (major ve minor), M Obliquus Capitis Superior ve İnferiordur. C1’in dalı olan Suboksipital sinir ile innerve olur. Bu kasların
7
üzerinde ise M Splenius Capitis ve Colli cervicis kasları yer alır. Ekstansiyon ve rotasyonda görevli olan bu kasların daha yüzeyel kısmında M Trapezius ve M Levator Scapulae yer alır (14).
Boynun innervasyonu
İntervertebral foramenlerden toplam 8 çift servikal sinir çıkar. Bu sinirlerin kökeni medulla spinalis’ten gelen ön ve arka dallardır. Spinal sinirler hem duyu, hem de motor lifler taşır. Çıktıkları seviyeye göre yukarıdan aşağıya C1’den C8’e kadar isim alırlar.
Spinal sinirlerin posterior dal lifleri arka bölgedeki kasların innervasyonunu sağlarken, anterior dal lifleri ön yüzdeki kaslara ek olarak ekstremitelerdeki kasların da innervasyonunu sağlar. C1-C4 arası spinal sinirlerin anterior lifleri baş boyun derisi ve servikal derin kasları innerve eder. Ayrıca C4 siniri C3 ve C5 ile birlikte frenik siniri innerve ederek solunuma da yardımcı olur. C5 ve T1 arası lifler ise brakial pleksusu oluşturur. Brakial pleksus ekstremitelerdeki kasların innervasyonunu sağlar(15).
Boynun fonksiyonel anatomisi
Boyun bölgesi omurganın en hareketli bölgesidir. Fleksiyon, ekstansiyon, iki yöne lateral fleksiyon ve rotasyonları gerçekleştirebilir. Bu hareketler boynun farklı bölgelerinde, farklı oranlarda ortaya çıkar, ancak neredeyse her seviye her tip harekete belirli oranda katılır. Fleksiyon ve ekstansiyonun temel olarak gerçekleştiği eklemler atlanto-oksipital eklem ile birlikte C5-C7 arası vertebralardır. Lateral fleksiyonlar ise C3-5 arasında diğer bölgelere göre daha fazla gerçekleşir. Rotasyonu temel olarak gerçekleştiren eklem ise atlanto-aksiyel eklemdir (14).
Boyun hareketleri ile birlikte foraminal açıklıklarda değişiklikler meydana gelir. Örneğin intervertebral foramenler fleksiyonda açılırken, ekstansiyonda kapanır. Lateral fleksiyonda ise fleksiyonun olduğu taraftaki foramenler daha dar, karşı taraf ise daha geniş olarak gözlenir (12).
Boyun ağrısı
İnsanların üçte ikisi, yaşamlarının en az bir döneminde boyun ağrısı tarifler ve boyun ağrısı prevalansı orta yaşta en yüksektir(16). İngiltere kaynaklı bir ankette kadınların %25’i, erkeklerin ise %20’si halihazırda boyun ağrısı tariflemiştir (17). Başka bir araştırmada ise insanların %34’ü geçmiş senede en az bir kez boyun ağrısı bildirmiştir (18). Sırt ağrısı ile birlikte boyun ağrısı, dünyada kas iskelet sistemi için birinci basamaktan gelen konsültasyon
8
sebeplerinde en üst sıradadır (19). Boyun ağrısı ile ilgili çalışmalar çoğunlukla hasta beyanına dayalıdır. Buna rağmen boyun ağrısının bireyler, işverenler ve sağlık hizmetleri üzerinde ağır bir yük oluşturduğuna dair önemli kanıtlar mevcuttur (20).
Boyun ağrısı nedenleri
Boyun ağrısı nedenlerinin önemli bir kısmı kas-iskelet sistemi kökenli patolojilerdir (21). Boyun ağrısının birçok olası nedeni vardır, ancak kesin nedenini belirlemek her zaman mümkün olmayabilir. Bunun nedeni, fizik muayenenin ve görüntüleme testlerinin her zaman ayırıcı tanıda net sonuçlar verememesidir. Ek olarak, sıklıkla görüntüleme testlerinde görülen dejeneratif kemik ve eklem değişiklikleriyle ağrının şiddeti her zaman ilişkili değildir. Bir kişide herhangi bir muayene, görüntüleme veya laboratuvar anomalisi olmaksızın boyun ağrısı olması mümkündür. Benzer şekilde görüntülemede önemli anormalliklere rağmen hastalar çok hafif derecede ağrı tarif edebilir.
Boyun ağrısının temel sebepleri Tablo 1’de sıralanmıştır. Tablo 1: Boyun ağrısı etyolojisi(22)
• 1. Mekanik Ağrı
• Servikal strain/sprain
• Whiplash sendromu
• Dejeneratif disk hastalığı
• Servikal disk hernisi
• Servikal spondiloz
• DISH(Diffüz İdiopatik Skeletal Hiperostoz)
• Servikal segmental disfonksiyon
• 2. Enfeksiyon • Brusella • Tüberküloz • 3. Tümörler • 4. Diğer Hastalıklar • Romatizmal hastalıklar
• Miyofasiyal ağrı sendromu
9 • Paget hastalığı • 5. Konjenital Anomaliler • Servikal kot • Blok vertebra • Spina bifida • 6. Torasik Çıkış Sendromları • Servikal kot
• Skalenius anterior sendromu
• Kostaklavikular sendrom
• Hiperabduksiyon sendromu
Servikal disk bozuklukları
Servikal disk bozuklukları tüm toplumlarda yaygın görülen bir hastalık grubudur ve boyunda ağrı, hareket kısıtlılıkları, duyusal ve motor kayıp yakınmalarıyla ilişkili olabilir. Bu konuda literatürdeki ilk yayınlar 20. Yüzyıl başlarında ortaya çıkmış olup dahili ve cerrahi yönetimi konusunda birçok aşamalar kat edilmiştir(23). Bununla birlikte günümüzde bu bozuklukların ve sebep oldukları komplikasyonların yönetimi için çalışmalara olan gereksinim çok fazladır. Servikal disk bozukluklarının sıklığı genellikle yaş ile birlikte artış gösterir ve disk dejenerasyonunun yaşlanmanın normal bir parçası olduğu düşünülmektedir. Christe ve ark. (24) yapmış oldukları çalışmada, 50 yaş üzeri disklerde radyografik görüntülere yansımasa bile histolojik olarak dejeneratif değişikliklerin sık görüldüğünü göstermiştir. Bunun yanında yapısal MRG çalışmalarında 40 yaşın altındaki kişilerde disk bozuklukları %25 civarı görülürken, 40 yaşın üzerindeki serilerde % 60-62 oranında en az bir seviyede disk bozukluğu tespit edilmiştir (25, 26). Semptomatik servikal disk bozukluğu insidansı bir kohortta 83.2/100000 olarak belirlenmiştir, erkeklerde kadınlara göre daha sık saptanmıştır (107.3’e karşılık 63.5/100000) (27).Servikal disk bozukluklarında en sık etkilenen diskler C5-C6 ve C6-C7 olup, bu etkilenimin yaş ile arttığı da dikkat çekmektedir. Ayrıca lomber disk dejenerasyonu varlığı da servikal etkilenim için bir risk faktörü olarak görülmüştür (28). Yine de çoğu hastada servikal dejenerasyonun lomberdeki süreçten daha geç başladığı düşünülmektedir.
10
İntervertebral diskler avasküler yapılardır, diskin beslenmesi kartilaginöz uç plaklardan difüzyon aracılığı ile gerçekleşir. Nükleus pulpozus genç erişkinlerde %85-90 civarı sıvı içeren jelatinimsi bir yapıdır ve geri kalan kısmında kollajen ve proteoglikanlar bulunur. Yaş ile birlikte bu sıvı miktarı azalır ve görece olarak kollajen ve proteoglikanlar artar. Anülüs fibrozusta ise yaklaşık %60-70 civarında su bulunmaktadır ve geri kalanı kollajen ağırlıklıdır. Nükleus pulpozustan farklı olarak sıvı içeriği yaş ile belirgin değişiklik göstermez. Yaşın dışında genetik yatkınlık, sigara içmek, kronik yüklenme, ateroskleroz ve cerrahi öykü gibi faktörler de dejenerasyonu etkiler (29-31). Dejenerasyon sürecinde çoğu inflamatuvar sitokinler arasında yer alan birçok molekülün etkili olduğu görülmüştür. Örneğin interlökin 1 ve tümör nekroz faktörü alfanın disk dejenerasyon süreci ile ilişkisi saptanmıştır (32, 33). Genetik ile ilişkili faktörlerde ise kollajeni kodlayan genlerdeki farklılıklar ilişkilendirildiği gibi, metalloproteinazlardan MMP3, D vitamini reseptörü ve agrekan gibi proteinleri kodlayan genlerin de disk dejenerasyonu ile ilişkisi olduğu düşünülmektedir(34). Yine ikizler üzerinde yapılan çalışmalarla disk dejenerasyonuna genetik yatkınlık kanıtlanmıştır (35). Ayrıca, MMP-3 üretimini düzenleyen genin promotör bölgesinde yaygın olarak bir polimorfizm (5A ve 6A alelleri) de saptanmıştır (36).
Disk dejenerasyonu sürecinde temel adımlardan birisi disk içeriğindeki sıvı kaybıdır. Sıvı kaybındaki temel mekanizma proteoglikan ve kollajen yıkımıdır. Yıkım ile birlikte disk matriksinde ozmotik basınçta düşmeler meydana gelir. Sıvı kaybının ardından intervertebral disk aralığında daralma oluşur, eklem dizilimleri bozulmaya başlar. Eklemlerdeki bozulma ve disk aralığındaki daralma kemik yapılar ve diskler üzerinde artmış bir makaslama stresine sebep olur. Makaslama stresi faset eklemler başta olmak üzere birçok yapıda dejeneratif değişiklikleri hızlandırır. Dejenerasyon ilerledikçe yumuşak dokulardaki yüklenme de artar(37).
Diskler iyileşirken intervertebral diskin kondrositleri matriksi sentez eder ve matriks metalloproteinazlar (MMP'ler), disintegrin ve metaloproteinaz (ADAMS) dahil olmak üzere degradatif enzimler üreterek ve aktive ederek mevcut matriksi parçalar. Proteoglikan oluşumu ve matriksin yapım-yıkım döngüsü ergenlikte en üst düzeydedir ve genellikle bundan sonra azalır.
Hasarlı intervertebral diskler yüksek derecede katabolik sitokin konsantrasyonuna, MMP aktivitesine ve skar dokusuna sahiptir. Annulus fibrosus yaralanırsa nükleus pulposus, yaralı annulus fibrosustan kaçabilir. Yaralı bir anulusun iyileşme süreci dejeneratif değişiklikler ile sonuçlanır.
11
Disklerde oluşan dejeneratif süreçler birçok semptom ile ilişkili olabilir. Bu semptomlar diskin yapısındaki bozulmalar ile ilişkili olabildiği gibi bozulmuş ve yer değiştirmiş disklerin çeşitli yapılara hasar vermesiyle de ortaya çıkabilir.
İntervertebral diskler esas olarak sinuvertebral sinirler aracılığı ile innerve olurlar, bunun yanında ventral ramus veya ramus communicanstan da doğrudan sinir dalları alırlar. Normal bir diskte anulus fibrozusun dış katmanlarında innervasyon mevcut iken diskin içinde ve nükleus pulpozusta innervasyon yoktur. Disk protrüzyonu sürecinde dış yırtıklar bu innervasyon sebebiyle ağrıya neden olabilir. Bunun yanında intervertebral disklerdeki bozulmalar posterior elemanlarda sekonder bir dejenerasyona yol açabilir. Faset eklemlerde ortaya çıkan dejeneratif değişiklikler de ağrı ile ilişkili olabilir. Özellikle ileri yaştaki hastalarda diskojenik ağrıya nazaran faset eklemlerdeki değişikliklerin önem arz ettiği lombervertebralarda gösterilmiştir, bu durumun servikal diskler için de geçerli olması kuvvetle olasıdır (38).
Servikal disk bozukluklarında çoğunlukla yakınma boyun ağrısı ile başlar. Temel olarak tipik bulgular; boyun ağrısı ve servikal omurga eklem hareket açıklığında azalmadır. Bunun dışında hastalar baş ağrısı ve omuz ağrısı ile de kliniklere başvurabilir. Boyun ağrısı kadınlarda daha sık görülür ve orta yaşlarda pik yapa(39). Boyun ağrısı ile gelen hastalarda yapılan bir çalışmada ağrı kaynağının öncelikle faset eklemler olduğu (%55), bunu diskojenik ağrı (%16) ve lateral atlantoaksiyal eklem ağrısının (%9) izlediği tespit edilmiştir(40).
Boyun ağrısının yanında disk bozuklukları radikülopatiye de sebep olabilir. Radiküler tutulumda ağrının dermatomal yayılması ve nöropatik vasıfta olması beklenir. Bunun yanında kuvvet kaybı, atrofi, derin tendon reflekslerinde azalma gibi motor problemler ile ağrı dışı parestezi veya hiperestezi gibi duyusal değişiklikler de söz konusu olabilir. Dejeneratif bozukluklara bağlı radiküler tutulumun en sık sebebi disk hernileri olmakla beraber spondilotik osteofitler veya ligaman hipertrofileri gibi çevresel değişiklikler de radiküler etkilenime sebep olabilir. Fleksiyon ve ekstansiyon hareketlerinde en hareketli bölge C4-6 arası omurgalardır. Bu da C5-6 ve C6-7 seviylerindeki disk protruzyonlarının en sık görülmesine sebep olur(41). İlgili seviyelerdeki disk protruzyonları söz konusu olduğunda hastalarda biceps, ön kolun radyal kısmı ve parmak uçlarına yayılan nöropatik ağrı görülebilir. Bunun yanında bilek ekstensörleri, dirsek fleksör ve ekstensörlerinde kuvvet kaybı söz konusu olabilir, brakioradyal refleks ve triceps refleksi zayıflayabilir. Bu hastaların bir kısmına dermatomal ağrı ve paresteziler eşlik edebilir. Disk herniasyonlarının muayenesinde; servikal kas spazmı, hareket kısıtlılığı, Spurling bulgusu pozitifliği,
12
dermatomal ve myotomal uyumlu duyusal ve motor defisitler, refleks kaybı görülebilir. Özellikle bu şikayetler valsalva manevrasıyla veya başın etkilenen tarafa fleksiyonu, rotasyonu ve başın aksiyal yönde bastırılmasıyla ortaya çıkarılabilir. Bunun yanında bazı hastalarda omuz abduksiyonu semptomları azaltmaktadır.
Boyun ağrısı ve radikülopatinin yanında servikal disk bozuklukları doğrudan spinalkorda bası yaparak myelopati tablosuna sebep olabilir. Myelopati tablosu posterior longitudinal ligaman ossifikasyonu, spondilotik süreçler ve disk herniasyonunun doğrudan etkisi ile ortaya çıkabilir. Radikülopatiye göre klinik olarak iyileşmeler daha nadirdir. Hastalarda progresyon söz konusu olabilir, bu progresyon birkaç hafta içinde hızlı olarak oluşabildiği gibi genellikle aylar-yıllar içerisinde yavaş olarak ilerleyebilir (42).
Servikal radikülopati
Dejeneratif süreçler sonucu oluşan radikülopati çoğunlukla disk herniasyonu veya spondilozis sürecine eşlik eder. Bunların yanında tümör, travma, sinovyal kistler ve dural arteriovenöz fistüllerde de bu tablo gözlenebilir.
Radikülopati ile ilgili ilk tarifler 1800’lü yılların başında kendi ismiyle anılan hastalığın ilk tarif edildiği yayında Parkinson tarafından yapılmıştır, ancak etiyoloji konusunda bazı hatalar mevcuttur(43). Ardından 20. Yüzyılın başında Dejerine tarafından da benzer klinik tarifler yapılmıştır, ancak Elliott’un 1926 yılında nöral foraminal stenozlar sonucu radikülopati tarifi etiyolojiyi belirlemek açısından önem arz etmektedir(44, 45). Zamanla radikülopati konusundaki yayınlar hızla artmıştır.
Servikal radikülopati konusunda yapılan çalışmalarda insidans; ABD’de her 100 000 erkekten 107’sinde ve kadınların 63.5'inde olarak tespit edilmiştir. En sık etkilenen kökler C6 ve C7 kökleridir(27).
Nörolojik etkilenim durumunda ikinci motor nöronları taşıyan spinal sinir köklerinin iyileşme şansı mevcuttur, radikülopatiler de zamanla iyileşebilir. Servikal radikülopatili hastaların önemli bir kısmında 2-3 ay içerisinde semptomlarda gerileme gözlemlenir. Yaklaşık %10-15’lik kısmında ise parsiyel iyileşme söz konusudur(46). Buna rağmen bazı hastaların cerrahi müdahaleler de dahil olmak üzere iyileşmeleri, herhangi bir girişim olmaksızın iyileşmesi mümkün olmamaktadır(47).
13
Servikal radikülopatiye sebep olarak sert ve yumuşak disk olmak üzere iki çeşit disk bozukluğu mekanizması tanımlanmıştır. “Sert disk” mekanizmasında spondilozis ve bu süreçte oluşan osteofitler ve faset hipertrofisi radikülopatiye sebep olmaktadır. Disk sıvı içeriğini ve yüksekliğini kaybetmiş, yüklenmedeki dengesizlik spondilozis mekanizmasını tetiklemiştir. Dejeneratif süreçler sonucu nöral foraminal ve spinal kanalda daralmalar meydana gelebilir. Bunun dışında “yumuşak disk” mekanizması söz konusu olduğunda etkilenen diskte nükleus pulposus herniye olmuştur ve ilgili kökler etkilenmiştir. Bu mekanizma özellikle genç hastalarda daha sıktır. 40-60 yaş arası hasta gruplarının büyük kısmı yumuşak disk nedeniyle radikülopati yaşarken, daha ileri yaşlarda sert disk mekanizması ön plana geçer. Tüm bunların dışında bazı hastalarda mekanizmadan bağımsız olarak ikili etkilenim (double crush) de söz konusu olabilir. Hastaların küçük bir kısmında kök ve bu kökün dal verdiği sinirlerden biri tuzak nöropatiler nedeniyle etkilenebilir(48). Servikal radikülopatinin ayırıcı tanısında çoğunlukla periferal nöropatiler bulunur. C5 seviyesi gibi üst seviyelerde rotator manşet kasları etkilenimi söz konusu olmakla birlikte, C6-7 seviyelerinde karpal tünel sendromu, CC6-7 ve C8 seviyelerinde ulnar sinir tutulumları, posterior ve anterior interosseöz sinirlerin etkilenimleri ayırıcı tanıya girer. Bunun dışında radikülopati sebebi olarak bahsedilen tüm etkenler de ayırıcı tanıda belirlenmelidir.
Servikal radikülopati, disk patolojilerinin en sık C5-6 ve C6-7 seviyelerinde görülmesinden dolayı C6 ve C7 düzeylerinde diğer düzeylere nazaran daha sık görülür. Bu seviyelerde disk herniasyonları gerçekleşerek radiküler etkilenime sebep olduğunda klinik, etkilenen köke göre farklılık gösterir. C6 etkilenimi ön planda olduğunda duyusal etkilenim kolun anterioru, başparmak ve işaret parmağın radial tarafında beklenirken, motor etkilenim biseps, supinator ve el bileği ekstansörlerinde beklenir. Derin tendon refleks değerlendirmesinde biseps ve brakioradyal reflekslerde zayıflama görülebilirken, hastalar başparmak ve işaret parmağını kapsayan parestezik alanlar tarif eder. C7 etkilenimi olduğunda ise duyusal etkilenim kolun ve ön kolun laterali, işaret, orta ve yüzük parmakta beklenirken, motor etkilenim triseps ve el bileği fleksörlerinde, bazen de el bileği ekstansörlerinde beklenir. Derin tendon refleks muayenesinde triseps refleksinde azalma gözlenebilir. Hastalar işaret parmağı, orta parmak ve yüzük parmağındaki parestezilerden yakınır.
Servikal radikülopatinin tanısal sürecinde görüntülemelerin önemi büyüktür. Direkt grafiler kemik yapılardaki dejenerasyonu, disk aralıklarındaki değişimleri ve bunlara bağlı nöral foraminal stenozları gösterebilir. Bunun dışında MRG kemik yapıların yanı sıra yumuşak
14
dokulardaki değişimleri, ligaman ossifikasyonlarını, disk yapısındaki bozuklukları ve omurilikteki sinyal değişimlerini de gösterebilir.
Kemik yapıları görüntülemede üstün olan bilgisayarlı tomografinin de radikülopati etyolojisini araştırmada yeri olmakla beraber MRG daha öncelikli olarak tercih edilmektedir. Yine de MRG sonuçları klinik öykü ve muayene eşliğinde değerlendirilmelidir, zira semptom yaratmadığı halde MRG ile birçok dejeneratif değişiklik patolojinin kaynağı olarak yanlış yorumlanabilmektedir(49).
Elektrofizyolojik çalışmaların da radikülopati teşhisinde önemli bir yeri vardır. Elektromyografi ve sinir iletim çalışmaları özellikle klinik öykü ve muayene görüntüleme ile uyumsuz olduğunda tanıya gidişte yardımcı olabilir(50). Bunun yanında periferik nöropati gibi etkilenimler söz konusu olduğunda ayırıcı tanıyı sağlamada yardımcıdır. Yine de elektrofizyolojik çalışmalar özellikle yalnızca nöropatik ağrı söz konusu olduğunda her zaman bulgu vermeyebilir. Bunun temel sebebi elektrofizyolojik çalışmalarda geniş çaplı liflerin etkileniminin gösterilmesi, ancak tutuldukları zaman nöropatik ağrıya sebep olabilecek daha küçük çaplı liflerin etkilenimin bu çalışmalarda bulgu vermemesidir(51).
Servikal dejeneratif disk bozukluklarına bağlı gelişen radikülopatilerin önemli bir kısmı yalnızca konservatif tedavi ile gerileyebilir. Konservatif tedavi seçenekleri arasında nonsteroid antiinflamatuvar ilaçlar, miyorelaksanlar, kortikosteroidler, fizik tedavi yöntemleri, ortezleme(boyunluk) ve gereğinde opioidler ve nöropatik ağrı varsa ona yönelik ilaç tedavisi yer almaktadır(42).
Cerrahi tedavi çoğunlukla progresif motor fonksiyon kaybı, konservatif tedaviye yanıt vermeyen şiddetli ağrısı olan hastalarda tercih edilmektedir(52). Cerrahi yaklaşımda anterior veya posterior yaklaşımlar yer almaktadır. Bu yaklaşımlar ile dekompresyon cerrahisi ve ek olarak füzyon uygulanabilir. Bunun dışında servikal disk artroplastisi de tercih edilebilecek bir tedavi seçeneğidir(53).
NÖROPATİK AĞRI
Nöropatik ağrı tarih boyunca birçok tanıma sahip olmuş bir klinik durumdur. Nöropatik ağrının en güncel tanımı; somatosensoryel sistemi etkileyen bir patoloji veya lezyon nedeniyle ortaya çıkan ağrı biçimidir(1). Somatosensoryal sistem dokunma, basınç, ağrı, sıcaklık, pozisyon, hareket ve vibrasyonun algılanmasını sağlar. Bu algılamayı termoreseptörler,
15
mekanoreseptörler, kemoreseptörler, pruriseptörler ve nosiseptörler aracılığıyla alarak spinal korda taşır. Sinyallerin büyük kısmı talamusta işlenerek serebral kortekse iletilir. Bu yolakları etkileyebilecek lezyonlar veya patolojiler sonucu iletimde bozulmalar ortaya çıkabilir. Nöropatik ağrı ile ilişkilendirilmiş patolojiler arasında birçok neden mevcut olup, bu nedenler Tablo 2' de gösterilmektedir. Yine de bu hastalıklara sahip tüm bireylerde nöropatik ağrı gelişmeyebilir. Nöropatik ağrı diğer ağrı tiplerine nazaran mekanizmasından dolayı belirgin farklılıklar taşır, bu farklılıklar tanı ve tedavide de farklılığa neden olur.
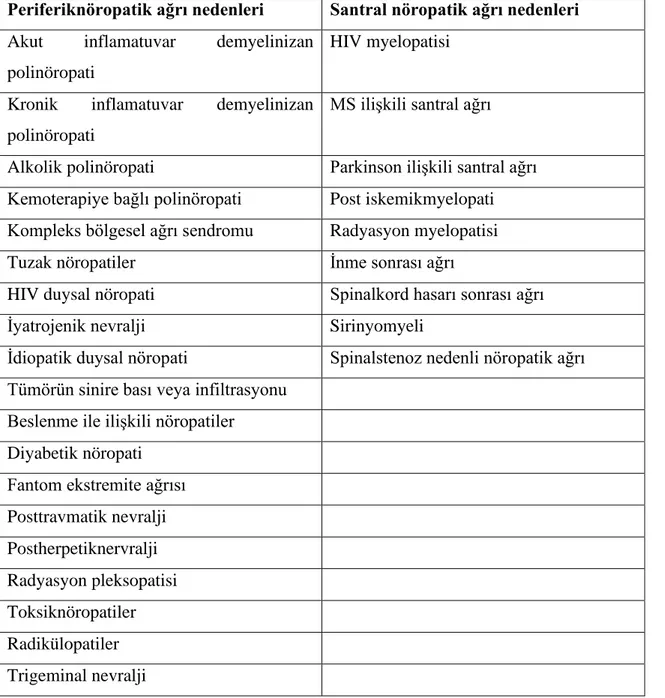
Tablo 2: Nöropatik ağrının sebepleri (54)
Periferiknöropatik ağrı nedenleri Santral nöropatik ağrı nedenleri Akut inflamatuvar demyelinizan
polinöropati
HIV myelopatisi
Kronik inflamatuvar demyelinizan polinöropati
MS ilişkili santral ağrı
Alkolik polinöropati Parkinson ilişkili santral ağrı Kemoterapiye bağlı polinöropati Post iskemikmyelopati Kompleks bölgesel ağrı sendromu Radyasyon myelopatisi
Tuzak nöropatiler İnme sonrası ağrı
HIV duysal nöropati Spinalkord hasarı sonrası ağrı İyatrojenik nevralji Sirinyomyeli
İdiopatik duysal nöropati Spinalstenoz nedenli nöropatik ağrı Tümörün sinire bası veya infiltrasyonu
Beslenme ile ilişkili nöropatiler Diyabetik nöropati
Fantom ekstremite ağrısı Posttravmatik nevralji Postherpetiknervralji Radyasyon pleksopatisi Toksiknöropatiler Radikülopatiler Trigeminal nevralji
16
Nöropatik ağrı ile ilgili epidemiyolojik verinin elde edilmesi oldukça zordur, zira bu klinik tablo birçok hastalığın seyrinde görülebilmektedir. Bu nedenle çoğu veri hastalıklara spesifik çalışmalar aracılığı ile elde edilmektedir. Bununla birlikte, nöropatik ağrı taramasını sağlayan Doleur Neuropathique 4, PainDETECT vb ölçeklerin artmasıyla birlikte toplumda kronik ağrılı, nöropatik komponenti olan hastaların prevalansının %7 ile 10 arasında olduğu gösterilmiştir. Özellikle kadınlarda (kadınlarda %8 iken erkeklerde %5.7’dir) ve 50 yaş üzerinde (50 yaş üzerinde %8.9 iken altında %5.6’dır) sıklığı daha fazladır (55).
Nöropatik ağrı birçok nedenden kaynaklanabilir. Santral patolojiler somatosensoryal yolakları etkilerken, periferik tutulumlu hastalıklar duyusal A beta, A delta ve C liflerini tutarlar. Özellikle öncelikli olarak tutulan lifler küçük, myelinsiz C lifleridir. Periferik tutulumlu hastalıklar; generalize tutulum ve fokal tutulum olarak sınıflandırılabilir. Generalize nöropatik ağrı ile karakterize hastalıklar arasında diyabetes mellitus, HIV enfeksiyonu, kemoterapi, otoimmun nöropatiler, inflamatuvar nöropatiler ve kanal bozuklukları yer almaktadır. Bu tip hastalıklarda ağrının tipik dağılımı eldiven çorap tarzında olup, distaldeki en ufak çaplı liflerin tutulumu gözlenir(56). Yine de sistemik doğalarından ötürü bu hastalıklarda özellikle duyusal gangliyonlarda tutulum söz konusu olursa şikayetler daha proksimalde ortaya çıkabilir. Fokal tutulumlu nöropatiler arasında ise postherpetik nöralji, post operatif sinir hasarı, servikal ve lomber radikülopatiler, kompleks bölgesel ağrı sendromu ve trigeminal nöralji yer almaktadır(57). Bu hastalıklarda ağrı etkilenen sinirin dağılım alanı ile uyumludur.
Nöropatik ağrı patofizyolojisi ve mekanizmaları
Nöropatik ağrının patofizyolojisinde birçok mekanizma mevcuttur. Temel mekanizmalar ağrı sinyallerinde değişimler, iyon kanallarındaki değişiklikler, ikincil nosiseptif nöronlardaki yanıt ve inhibitör modülasyonlarda görülen bozulmalardır.
Periferik nöropatiler duyusal sinirlerin elektriksel özelliklerini etkiler, merkezi uyarıcı ve inhibitör sinyallerin dengelerinde bozukluklara sebep olur. Bunun sonucu olarak spinal kordda dorsal boynuz nöronlarında disinhibisyon ve fasilitasyon mekanizmalarında değişimler meydana gelir. Hayvan çalışmalarında periferden merkezi sinir sistemine dek gerek fonksiyon kaybı, gerekse fonksiyonel kazanım ile ilişkili birçok değişiklikler tanımlanmıştır. Bu değişikliklerin gerçekleştirildiği deneklerde uyaranlara karşı hipersensitivite, spontan ağrı tetiklenmeleri gibi özellikler keşfedilmiştir(58). Bunların dışında afferent liflerde ektopik aktiviteler de gerçekleşebilir. Özellikle ektopik aktiviteler sinir
17
hasarına bağlı nöropatik ağrılarda önemli bir yere sahiptir. Hasarlanan C tipi liflerin mikronörografi ile incelenmesi bu liflerde spontan aktivite ve buna bağlı ağrıların oluşabileceğini göstermiştir(59).
İyon kanallarındaki değişimler de nöropatik ağrı ile ilişkilidir. Herediter kanalopatilerin bir kısmının nöropatik ağrı ile ilişkili olduğu bilinmektedir. Sodyum, kalsiyum ve potasyum kanallarında meydana gelen bozulmalar ağrı iletiminde fonksiyonel değişikliklere sebep olmaktadır. Örneğin dıuyusal nöronların spinal korddaki sonlanmalarında sodyum kanal sayısı ve eksitabilitesindeki artış, artmış sinyal iletimi ve nörotransmitter salınımına sebep olmaktadır. Potasyum kanallarındaki fonksiyonel kayıplar, ağrı iletim modülasyonunu bozabilir. Kalsiyum kanalları da çoğunlukla spinal kord düzeyinde nörotransmitter salınımında ve nosiseptif uyarıcı sinapsların fonksiyonunda artışa sebep olabilir. Bu kanallardaki fonksiyonel değişiklikler hasarlı sinirdeki ektopik iletimler ile birleştiğinde sensoriyel kayıplara eşlik eden nöropatik ağrı meydana gelir.
İnhibitör mekanizmaların kaybı nöropatik ağrının hem patofizyolojisi, hem de tedavi seçenekleri açısından önemli bir mekanizmadır. Nöropatik ağrı söz konusu olduğunda gama aminobutirik asit (GABA) salınımı gerçekleştiren inhibitör ara nöronlarda fonksiyonun azalması aşırı uyarılmışlığa katkıda bulunur(60). Ara nöronlardaki bu disfonksiyon inhibitör ve eksitatör dengelerin eksitatör taraf lehine bozulmasına yol açar. Böylece beyin anormal duyusal girdiler alır. Talamus ve korteks ile birlikte limbik sistem de bu uyarılma sürecine dahil olur ve hastalarda anksiyete, depresyon ve uyku problemleri ortaya çıkabilir. Singulat korteks ve amigdalanın nöropatik ağrı ile seyreden komorbiditelerde önemli bir yere sahip olduğu da gösterilmiştir. Bu bölgelerden ağrı modulasyonunda önemli bir yeri olan periakuaduktal gri maddeye birçok bağlantı uzanmaktadır, bu bağlantılar ağrı algısının değişmesine katkıda bulunurlar(61). Serotonin ve noradrenalin aracılığı ile yönetilen inhibitör mekanizmalar da GABA aracılı mekanizmalar gibi önemlidir. Noradrenerjik alfa 2 reseptörlerinin fonksiyonları azalırken, 5HT2 ve 5HT3 serotonerjik reseptörler baskın duruma geçer. Nöropatik ağrıda gerçekleştiği gösterilmiş olan mekanizmalar Resim 5’te özetlenmiştir.
18
Resim 5: Nöropatik ağrıda gerçekleşen santral ve periferik sinir sistemindeki değişiklikler(8) Nöropatik ağrı her insanda farklı şiddet ve özellikte ortaya çıkar. Buna tedavi yanıtları da dahildir. Bu farklılığa esas olan durumun santral sinir sisteminde olduğu düşünülmektedir. Ağrı yanıtları santral sinir siteminde modüle edilir. Ağrı sinyali dorsal kök gangliyonu aracılığı ile medulla spinalise iletildiği seviyeden itibaren çeşitli modülasyonlara uğrar. Bu süreçte kimi seviyelerde baskılanırken, kimilerinde daha da şiddetli olarak iletilebilir. Nöropatik ağrı söz konusu olduğunda birçok hastada ağrı olduğundan daha şiddetli bir şekilde iletilmektedir. Diğer bir deyişle bu hastalarda ve birçok ağrı sendromunda ağrı modülasyonu
19
sağlıklı popülasyona nazaran daha etkisizdir(62). Bunun yanında nöropatik ağrıda asendan yollar aracılığı ile ağrılı stimulasyonların şiddetlendirildiği de saptanmıştır(63). Araştırmalar açısından hangi hastaların ne tip ağrı modülasyonuna sahip olduğu, teorik açıdan farklı tedavi seçeneklerini de getirebilir. Özellikle ağrı iletiminin artmış olduğu hasta popülasyonlarında GABA üzerinden etki eden ajanların daha etkili olduğu düşünülürken, noradrenalin gibi inhibe edici modülasyonların etkinliğinin azaldığı hastalarda serotonin-noradrenalin geri alım inhibitörleri (Serotonine-Noradrenaline Reuptake Inhibitor-SNRI) daha uygun tedavi seçenekleri olabilir. Günümüzde bu profili tespit edecek güvenilir ve klinikte kullanılabilir bir yöntem mevcut değildir. Ağrı modülasyonunu tedavide kullanmanın bir diğer önemi de gerek nöropatik ağrı, gerekse diğer ağrı tiplerinde kronik ağrı etkeninin ortadan kaldırılmasıdır. Ağrı sebebi var olduğu sürece modülasyon devam edecek, bu modülasyon mevcut ağrının giderek daha kötü hissedilmesine yol açacak ve kronik ağrı ile ilişkilendirilmiş birçok ağrı dışı semptom ortaya çıkacaktır. Bu nedenle ağrının kontrol edilmesi kritik bir öneme sahiptir. Ağrı modülasyonunun klinikteki bir diğer ilginç, ancak temel yansıması da beklenti ile ortaya çıkan analjezidir. Bu prensip başta plasebo etkisi olmak üzere birçok tedavinin etkinliği açısından önemlidir. Plasebo etkisinin yanında, etkili olduğu kanıtlanmış ajanların hastaya sunum şekli bile ağrı tedavisinin etkinliğini değiştirebilir. Colloca ve arkadaşları (64), 2004 yılında yapmış oldukları bir çalışmada anestezik bir ajan olan lidokaini bir grup hastaya, bunun bir anestezik olduğunu ve ağrıyı azaltacağını, diğer gruba ise aynı ajanı, bir kontrol ilacı olarak tanıttığında ilk grubun belirgin olarak daha yüksek bir analjezi elde ettiğini göstermiştir. Bu bulgular, çalışmalarda hastaya yaklaşımın ne kadar dramatik etkiler yaratabileceğini düşündürmektedir. Ağrı modülasyonu ile ilgili gelecekte yapılacak çalışmalar, yeni yaklaşım stratejilerinin geliştirilmesine de yardımcı olacaktır.
Periferik mekanizmalar gibi santral sinir sistemindeki mekanizmalar da nöropatik ağrı gelişiminde önemli bir role sahiptir. Özellikle A beta ve A delta afferent liflerinin sinaps yaptığı, merkeze sinyalleri taşımakla görevli nöronlarda sinir hasarı ile birlikte değişiklikler oluşur ve verilen uyarılar merkeze daha çok nöron tarafından iletilir veya kortikal temsil alanlarında genişleme söz konusu olabilir(65). Bu duruma santral sensitizasyon adı verilir. Afferentlerden sürekli olarak salınan uyarıcı nörotransmitterler aşırı derecede N metil D aspartat (NMDA) ve alfa amino 3 hidroksi 5 metil 4 izoksazole propionik asit (AMPA) salınımı ile karakterize postsinaptik değişikliklere sebep olabilir. Bu değişiklikler gerçekleştiğinde talamik nöronal aktivite artar, bu da allodini veya hiperaljezi gibi durumlara
20
yol açabilir(9). Nörotransmitterler dışında çevresel nöron dışı hücrelerin de bu süreçte yer aldığı düşünülmektedir(66).
Nöropatik ağrıda öykü, semptom ve bulgular
Nöropatik ağrılı hastalarda detaylı bir öykü esastır. Ağrının niteliği, şiddeti ve yayılımının sorgulanması gerekir. Nöropatik ağrıyı ifade ederken hastalar farklı ifadeler (yanıcı, batıcı, elektrik çarpması, sıcak, soğuk vb) kullanabilirler(67).
Sinir trasesi boyunca hasar veya somatosensoryal yolaklarda hasar görülür ise duyusal defisitler ortaya çıkabilir. Tutulan liflerin özelliklerine göre defisitler değişkenlik gösterebilir. Kalın lif veya dorsal kolon tutulumunda mekanik, pozisyonel veya vibrasyonda değişiklikler görülürken, ince lifler veya spinotalamik yol tutulumunda ağrı-ısı duyularında kayıp ön planda olabilir(68).
Nöropatik ağrı varlığında etkilenen alanda sıklıkla duyusal değişiklikler saptanır(69). Hastalar bu ağrıları spontan veya uyaran ile tetiklenen olarak tanımlayabilirler. Spontan ağrılar bir uyarandan bağımsız olarak ortaya çıkar, hastalar ağrılarını batıcı, zonklayıcı veya elektriklenme gibi tarifler. Ağrı şiddeti değişkendir. Allodini ve hiperaljezi ise uyaran ile ortaya çıkan fenomenlerdir. Allodini ağrılı olmayan bir uyaranın hastada ağrıya sebep olmasıdır(dokunma gibi). Hiperaljezi ise normalde ağrılı olan bir uyaranın olduğundan daha şiddetli bir ağrıya sebep olmasıdır(70).
Nöropatik ağrıda ortaya çıkan bu defisit ve fenomenler negatif ve pozitif semptomlar olarak adlandırılır. Nöropatik ağrıda görülen pozitif ve negatif semptomlar tablo 3’te verilmiştir.
Tablo 3: Nöropatik ağrıda pozitif ve negatif semptomlar(71)
Pozitif Semptomlar Negatif Semptomlar
Spontan ağrı: Stimulus olmadan ağrı hissi Hipoestezi: Stimulasyona karşı azalmış his Allodini: Normalde ağrı oluşturmayan bir
uyarana karşı ağrı hissi
Anestezi: Total his kaybı
Hiperaljezi: Ağrılı bir uyarana karşı artmış ağrı hissi
Hipoaljezi: Ağrıya karşı azalmış yanıt
Disestezi: Rahatsız edici anormal his, spontan veya uyarılmış olabilir
21
Parestezi: Anormal his, spontan veya uyarılmış olabilir
Yine nöropatik ağrıya nosiseptif ağrının eşlik etmesi sık görülen bir durumdur. Bu nedenle iyi bir öykü ve muayene, bu komponentleri belirlemede kritiktir. Komponentlerin şiddetinin belirlenmesi tedavi planlanması için de önemlidir.
Nöropatik ağrıda fizik muayene
Nöropatik ağrılı hastalarda duyu muayenesi ön planda olmak üzere iyi bir nörolojik muayene yapılması esastır. Duyusal fonksiyon bozuklukları pozitif ve negatif semptomlar ile seyredebilir. Bu semptomların her biri için fizik muayene yapılmalıdır. Hipoestezi, hiperestezi, hiperaljezi ve allodini ile ilgili testler, standart nörolojik muayeneye eklenmelidir. Sinir hasarı söz konusu olduğunda hastalarda motor değişiklikler, otonomik değişikler ve reflekslerde değişiklikler görülebilir(54). Bu değişikliklerin birlikte değerlendirilmesi, lezyonun lokalizasyonuna da yardımcı olabilir (Periferik sinir, pleksus lezyonu spinal kord veya serebrum gibi). Bunlar dışında nöropatik ağrı hastanın uykusunu, duygu durumunu ve yaşam kalitesini etkileyebilir(72). Bu nedenle klinisyenler ağrının bu yönlerini de göz önünde bulundurmalıdır.
Nöropatik ağrıda tanısal süreç
Nöropatik ağrının tanısı ile ilgili birçok yöntem ve öneri getirilmekle beraber, en güncel ve en çok kabul gören tanımlardan biri DFNS (Alman Nöropatik Ağrı Araştırma Ağı)’ nin 2016 yılında önermiş olduğu tanımdır(73). Bu konseptte nöropatik ağrı olası (possible), muhtemel (probable) ve kesin (definite) olmak üzere üç seviyede tanımlanmıştır. Hastalığın öyküsünde nöropatik ağrı düşündürebilecek bir durum söz konusu ise bu olası (possible) nöropatik ağrıdır. Öyküde bunu düşündürebilecek ögeler; ağrının nörolojik bir lezyon ile uyumlu olması veya nöroanatomik bir dağılıma uymasıdır. Yine ağrının yanma, batma, elektrik çarpması veya dokunmaya hassasiyet gibi nitelikler taşıması da öyküyü destekler. Olası nöropatik ağrıya eşlik eden klinik bir duyusal işaret varlığında(nörolojik muayene, kantitatif duyu testi gibi) bu ağrının tanımı muhtemel (probable) nöropatik ağrı olacaktır. Muhtemel nöropatik ağrının kesin nöropatik ağrı niteliğini alabilmesi için objektif bir test ile kanıtlanmış olması gereklidir. Bu objektif test tanıya göre değişmekle beraber nedensel olan lezyonun gösterildiği bilgisayarlı tomografi, manyetik rezonans görüntüleme olabilir. Bunun dışında sinir hasarının gösterildiği bir deri biyopsisi, lazer uyarılmış potansiyellerdeki (LEP) değişiklikler veya
22
herediter eritromelaljide olduğu gibi genetik testler tanı amacıyla seçilebilir. Bir ağrı kesin nöropatik ağrı tanısına ulaşabilmekle beraber, bu onun diğer ağrı tiplerinden tamamen ayrıldığını göstermez. Mekanik veya inflamatuvar karakterdeki ağrılar nöropatik ağrıya eşlik edebilir ve birden fazla ağrı türü iç içe geçebilir, hatta esas ağrı karakteri nöropatik ağrıdan çok diğer tiplere de ait olabilir. Bu nedenle ayırıcı tanının özenle yapılması gereklidir(74). Her ne kadar çoğu araştırmada öncelikli olarak bu tanım kullanılsa da klinik pratikte ve araştırmaların da önemli bir kısmında nöropatik ağrıyı tanımlamak için geliştirilen anketlerin de önemli bir yeri vardır. Bu anketler sayesinde toplumda etiyolojisinden bağımsız olarak nöropatik ağrılı hastaları taramak olasıdır. Hatta bazı cut-off noktalarının belirlenmesi ile yüksek oranlarda nöropatik ağrı tanısı koyabilmek mümkün olmuştur. Çoğu anket hasta bildirimine dayalı olmakla beraber anketlerin bir bölümünde klinik ve hasta muayenesine dayalı kısımlar da mevcuttur. Güncel anlamda doğruluğu kanıtlanmış ve tarama amaçlı yaygın kullanılan anketler arasında PainDETECT, LANSS (Leeds Assessment of Neuropathic Symptoms and Signs), DN4 (Douleur Neuropathique 4), NPQ (Neuropathic Pain Questionnaire), NPSI (Neuropathic Pain Symptom Inventory) yer almaktadır.
PainDETECT 2004 yılında geliştirilip 2006 yılında yayınlanmış, DFNS tarafından geliştirilmiş bir nöropatik ağrı tarama aracıdır(4). Birçok dile çevrilmiş ve Türkçe geçerlilik ve güvenilirliği de gerçekleştirilmiştir (75). 7 adet duyusal semptom ile ilgili derecelendirilmiş soru ve ağrının yayılımına ve zamanına dair iki sorudan oluşan bir ankettir. Ağrıyı nöropatik dışı, olası nöropatik ve nöropatik olarak 3 sınıfta inceler. 12 puanın altında nöropatik ağrı olası değildir, 12-19 puan arası olası nöropatik ağrı olarak sınıflandırılır. 19 puanın üzerindeki hastalarda nöropatik ağrı söz konusudur. Klinik incelemeler ile karşılaştırıldığında sensitivite ve spesifitesinin sırasıyla %85 ve %80 olduğu tespit edilmiştir. DN4, 4 temel bölüm ve 10 sorudan oluşan bir ankettir (76). 7 soru ağrı kalitesi ile ilişkili olup, 3 soru ise klinik değerlendirme üzerine kuruludur. Hem hasta, hem klinisyen görüşünü içerir. Nispeten basit olmasından dolayı sık tercih edilmektedir. 4 puanın üzerindeki skorlar nöropatik ağrı ile ilişkilidir. %90 spesifitesi olduğu bildirilmiştir(77). Türkçe geçerlilik ve güvenilirliği de gerçekleştirilmiştir(78).
LANSS (Leeds Assessment of Neuropathic Symptoms and Signs) da nöropatik ağrının taranması için hazırlanan ölçeklerden birisidir(79). İçeriğinde semptom ile ilgili 4 sorunun yanında bir inspeksiyon bulgusu (deri görünümü) ve iki fizik muayene bulgusu mevcuttur. Türkçe geçerlilik ve güvenilirliği Yücel ve ark (80) tarafından gerçekleştirilmiştir.
23
NPQ (Neuropathic Pain Questionnaire) toplam 7 duyusal semptom, 3 provoke edici faktör ve ağrının hastaya olan subjektif etkisinin 2 soruda sorgulandığı bir ölçektir(81). Sensitivite ve spesifitesi sırasıyla %66 ve %74 olarak görülmüştür. Türkçe versiyonu mevcut olup, geçerlilik ve güvenilirliği de kanıtlanmıştır (82).
NPSI (Neuropathic Pain Symptom Inventory) ağrının özelliklerine ait 10, zamansal dağılıma ait 2 ve klinik ile ilişkili 5 boyuta sahip bir envanterdir (83). Günümüz itibarıyla literatürde Türkçe versiyonu yer almamaktadır. Ağrının çok boyutlu değerlendirmesine olanak sağlayan envanterlerdendir.
Nöropatik ağrıda tanısal teknikler
Kantitatif Duyu Testi (QST-Quantitative Sensory Testing)
Kantitatif duyu testleri (QST) periferik ve merkezi, nosiseptif ve nonnosiseptif sistemleri değerlendirmek amacıyla oluşturulmuş standardize testlerdir. Diğer metodlara üstünlük olarak farklı lif tiplerinde (A beta, A delta ve C) fonksiyon kaybı veya kazanımını değerlendirebilmektedir. QST için dünyada birçok sistem düzenlenmiştir. Bunlardan en yaygın kullanılmış olanı Case IV (WR medicalelectronics, Maplewood, USA) olmakla beraber testleri gerçekleştirebilecek, standardize edilmiş birçok sistem mevcuttur. Son dönemlerde DFNS tarafından araştırmalarda kullanılmak üzere 13 parametrelik bir QST seti ve uygulama ilkeleri belirtilmiştir. Bu Case IV’un içerisindeki temel 4 komponentin yanında yönergeleri belirlenmiş standart bir ekipman ile gerçekleştirilen 9 ayrı komponent içerir. Testlerin her biri için normal aralıklar tanımlanmakla beraber, her ne kadar uygulama yönergeleri standardize de olsa, toplumlar ve araştırıcılar arası değişkenlikler görülmesi olasılığı mevcuttur(84). QST tekniklerinde hedeflenen; duyu gibi sübjektif bir modaliteyi imkanlar dahilinde objektif hale getirmektir. Yine de tüm gelişmelere ve standardizasyonlara rağmen duyu hasta beyanına dayalıdır ve kesin nesnelliğe ulaşmak beklenen hedefler arasında yer almamaktadır.
CASE IV içeriğinde sıcaklığı hissetme eşiği (Warmdetectionthreshold-WDT), titreşimi hissetme eşiği (Vibration detection threshold-VDT), Soğuk hissetme eşiği (Cold detection threshold-CDT) ve ısıya karşı ağrı sensitivitesi (heat sensitivity for pain- HSP) komponentleri yer almaktadır. Tüm uyarılar bilgisayar aracılığı ile standart seviyelerde defalarca denenerek hastaya hissedip hissetmediği sorulur ve kumanda aracılığı ile yanıt alınır. Tüm bu
24
denemelerin sonucunda bu modalitelere karşı hastanın ne kadar hissettiği, ne kadarını hissetmediği ölçülür ve bir eşik değeri çıkar. Bu eşik değer yaş, cinsiyet, boy, kilo ve yandaş hastalıklar ile değişkenlik gösterebilir. Eşik değerlerinde kontralateral tarafa veya yaş-cinsiyet uyumlu referans değerlerine göre farklılıklar görülmesi anlamlı kabul edilir. Ağrı mekanizmalarında lezyon tek taraflı bile olsa santral değişiklikler işin içerisinde yer alabilmektedir. Bu nedenle lezyon tek taraflı bile olsa yalnızca kontralateral tarafın kontrol olarak seçilmesi bazı hatalara sebep olabilir, özellikle bu durum santral plastisiteye bağlı hiperaljezi durumu söz konusu olduğunda daha belirgindir (85). Bu durum özellikle daha önceki yayınlarda kontralateral tarafın kontrol amaçlı alınması ile ilişkili öneriler ile bir tezat oluşturmaktadır(86). Bunun yanında farklı merkezler ve toplumlardan elde edilmiş olan QST verilerinin referans olarak belirlenmesi hususunda da bazı tartışmalar mevcuttur. 2016 yılında Avrupa’da farklı merkezlerden DFNS’nin yönergesine göre uygulanan testlerde referans değerler arasında heterojenite düşük saptanmış ve belirli yönergeler ve standardize testler söz konusu olduğunda farklı birimlerden katkıların olduğu geniş veri tabanlarının bu konuda yararlı olabileceği düşünülmüştür(84). Elde bu veriler olmakla beraber dünyanın farklı merkezlerindeki çalışmalar kendi toplumlarına göre bu referans aralığının dışında değerler de belirtebilmektedir (87).
Lazer uyarımlı potansiyeller (LASER Evoked Potentials -LEP)
Lazer uyarımlı potansiyeller (LEP) ağrı ile ilişkili fonksiyonlar için en güvenilir nörofizyolojik tekniklerden biri olarak kabul edilmektedir(86, 88). Genel olarak sinir iletim çalışmaları veya somatosensoryaluyarlımlı potansiyeller (SEP) gibi standart nörofizyolojik çalışmalar A beta liflerini test etmekte olup, ağrı ile ilişkilendirilmiş A delta ve C liflerine dair bilgi vermemektedir. Bununla birlikte nöropatik ağrıda sinir iletim çalışmaları ve EMG’nin önemi büyüktür, özellikle klinik tanı şüpheli olduğunda veya ayırıcı tanıda bazı patolojiler yer aldığında bunların dışlanması, veya büyük lif etkilenimi de söz konusu ise doğru tanıya gidilmesi açısından kullanılmaktadır (89). Lazer uyarımlı potansiyeller, özellikle A delta ve C liflerini uyarmaktadır(90).
Klinik kullanım için de yaygınlaşmakta olan LEP’ler nosiseptif yolların etkilenimi söz konusu olduğunda alınamayabilirler, düşük amplitüd veya yüksek latansa sahip olabilirler. Nöropatik ağrı değerlendirmesinde ısıya yönelik LEP’ler sık kullanılmaktadır, bunun yanında ağrı ile ilişkili uyarılmış potansiyellerin de kullanımı mevcuttur(91).
25
Deri biyopsisi
Küçük sinirlerin hasarını inceleme söz konusu olduğunda deri biyopsisi en hassas yöntem olarak görülmektedir(92). Özellikle deri altındaki serbest sinir uçlarının büyük bir kısmı C liflerinden oluşur, A delta liflerinin myelin kılıflarını kaybederek serbest biçimde sonlanmaları ise nadirdir. Bu durum biyopsinin C liflerini daha iyi değerlendirmesini sağlar. Yine de nöropatik ağrıda biyopsinin yeri de tartışmalıdır. Çünkü kimi çalışmalar periferal nöropati varlığında dahi intradermal sinir uçlanının korunabildiğini göstermiştir(93).
Korneal konfokal mikroskopi
Sistemik tutulumlu nöropatiler söz konusu olduğunda korneanın in vivo olarak özel mikroskoplar ile incelenmesi myelinsiz C lifleri ve küçük myelinli A delta liflerini gösterebilir(94). Ancak günümüzde maliyeti ve yaygın olmaması nedeniyle klinik pratikteki kullanımı sınırlıdır. Bunun yanında korneanın yapısı nöropati dışı sistemik hastalıklar tarafından da etkilenebilir. Tüm bu nedenler nedeniyle nöropatik ağrı ve korneal konfokal mikroskopinin ilişkisi konusunda kanıt düzeyi oldukça sınırlıdır(95).
Nöropatik ağrının tedavisi
Birçok patolojide olduğu gibi nöropatik ağrıda da öncelikli yönetim amacı, ortaya çıkışını engellemek olmalıdır. Ancak bu çoğu durumda mümkün değildir. Yine de sağlıklı bir yaşam tarzı, uyku ve beslenme bu süreçte ağrının yönetimi için yararlı olabilir. Bunların yanında nöropatik ağrı nedenlerinin doğru tanısı ve yönetimi şarttır. Örneğin diyabetes mellitus hastası bir bireyin şeker regülasyonunun sağlanması nöropatiyi yavaşlatabilir. Aşılama programları herpes zoster virüsünün yayılımını azaltarak postherpetik nevralji sıklığını düşürebilir. Tüm bu verilere paralel olarak tedavide hedef, altta yatan patolojinin mümkün ise tedavisidir. Nöropatik ağrı varlığında çoğunlukla altta yatan patolojiyi yok etmek mümkün değildir. Bu nedenle yönetimin de temelini semptomatik yaklaşım oluşturur. Temel bakış açısı öncelikli olarak noninvazif ve farmakolojik tedavilerin başlanması, bunların yetersiz olduğu noktalarda sinir bloğu, cerrahi veya nöromodülasyon gibi ileri tekniklerin önerilmesidir. İlk basamak