BEZMİALEM VAKIF ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ
ZEYTİN YAPRAĞI EKSTRAKTININ İNSAN HEPATOSELÜLER KARSİNOMA HÜCRELERİNDE TİROZİN KİNAZ, İNSÜLİN RESEPTÖR-1, GLUT4 VE GLUT2 PROTEİN EKSPRESYON SEVİYELERİ ÜZERİNE ETKİLERİNİN ARAŞTIRILMASI
YÜKSEK LİSANS TEZİ Burçin KASAP
Biyoteknoloji Anabilim Dalı Biyoteknoloji Programı
Tez Danışmanı: Prof. Dr. Abdurrahim KOÇYİĞİT
BEZMİALEM VAKIF ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ
ZEYTİN YAPRAĞI EKSTRAKTININ İNSAN HEPATOSELÜLER KARSİNOMA HÜCRELERİNDE TİROZİN KİNAZ, İNSÜLİN RESEPTÖR-1, GLUT4 VE GLUT2 PROTEİN EKSPRESYON SEVİYELERİ ÜZERİNE ETKİLERİNİN ARAŞTIRILMASI
YÜKSEK LİSANS TEZİ Burçin KASAP
(150305123)
Biyoteknoloji Anabilim Dalı Biyoteknoloji Programı
Tez Danışmanı: Prof. Dr. Abdurrahim KOÇYİĞİT
ii
Bezmialem Vakıf Üniversitesi, Sağlık Bilimleri Enstitüsü’nün 150305123 numaralı Yüksek Lisans Öğrencisi Burçin KASAP, ilgili yönetmeliklerin belirlediği gerekli tüm şartları yerine getirdikten sonra hazırladığı “Zeytin Yaprağı Ekstraktının İnsan Hepatoselüler Karsinoma Hücrelerinde Tirozin Kinaz, İnsülin Reseptör-1, GLUT-4 ve GLUT-2 Protein Ekspresyon Seviyeleri Üzerine Etkilerinin Araştırılması” başlıklı tezini aşağıda imzaları olan jüri önünde başarı ile sunmuştur.
Tez Danışmanı : Prof. Dr. Abdürrahim KOÇYİĞİT Bezmialem Vakıf Üniversitesi
Jüri Üyeleri :
Teslim Tarihi : 09.04.2018 Savunma Tarihi : 18.04.2018
Doç Dr. Şehabettin SELEK Bezmialem Vakıf Üniversitesi
Prof. Dr. Ata ALTURFAN İstanbul Üniversitesi
iii
iv ÖNSÖZ
Tez çalışmalarım esnasında bilgilerinden ve tecrübelerinden yararlandığım değerli danışman hocam Prof. Dr. Abdürrahim KOÇYİĞİT’e çok teşekkür ederim.
Tezimi yazarken gerek kurallar hakkında gerekse laboratuar çalışmalarımda fazlasıyla destek olan hocam Eray Metin GÜLER ve Ersin KARATAŞ’a çok teşekkür ederim.
Çalışmamın uygulama kısmında yardımcı olan Hümeyra Nur KALELİ, Derya ARAS, Merve TOPACA’ya teşekkür ederim.
Tez çalışmamın uygulama kısmını gerçekleştirirken teknik cihazları kullanmada yardımcı olan ve laboratuar malzemelerinin teminini gerçekleştiren Mustafa KARABONCUK’a teşekkür ederim.
Hayatımın her döneminde koşulsuz sevgi ve şefkatle yanımda olan, bana inanıp güvenen, arkamda hep destek olan sevgili kardeşim Burak Kasap, çok kıymetli annem Zeynep Kasap ve babam Ömer Kasap’a tüm kalbimle teşekkürlerimi sunarım. Bu tez, Bezmiâlem Vakıf Üniversitesi Bilimsel Araştırma Projeleri Komisyonu Başkanlığı tarafından 6.2016/57 numaralı proje ile desteklenmiştir.
Nisan 2018 Burçin KASAP
v BEYAN
Bu tez çalışmasının kendi çalışmam olduğunu, tezin planlanmasından yazımına kadar bütün safhalarda etik dışı davranışımın olmadığını, bu tezdeki bütün bilgileri akademik ve etik kurallar içinde elde ettiğimi, bu tez çalışmasıyla elde edilmeyen bütün bilgi ve yorumlara kaynak gösterdiğimi ve bu kaynakları da kaynaklar listesine aldığımı, yine bu tezin çalışılması ve yazımı sırasında patent ve telif haklarını ihlal edici bir davranışımın olmadığını beyan ederim.
vi İÇİNDEKİLER Sayfa ÖNSÖZ ... iv BEYAN ... v İÇİNDEKİLER ... vi KISALTMALAR ... viii TABLO LİSTESİ ... x ŞEKİL LİSTESİ ... xi ÖZET... xiii SUMMARY ... xv 1. GİRİŞ VE AMAÇ ... 1 2. GENEL BİLGİLER ... 4
2.1 Diabetes Mellitus Tarihçesi ... 4
2.2 Diabetes Mellitusun Tanımı ... 4
2.3 Diabetes Mellitusun Tipleri ... 5
2.3.1 Tip I Diyabet ... 5
2.3.2 Tip II Diyabet ... 6
2.4 Diabetes Mellitus Belirtileri ... 6
2.5 İnsülin Yapısı ... 7
2.5.1 İnsülin reseptörü ve etki mekanizması ... 7
2.5.2 İnsülinin karbonhidrat metabolizması üzerine etkileri ... 8
2.6 Diabetes Mellitus Epidemiyolojisi ... 10
2.7 Fitoterapinin Tarihçesi ... 10
2.7.1 Fitoterapi tedavisi ve seçenekler ... 11
2.8 Olea europae L.’nin Bilimsel Sınıflandırılması ... 11
2.8.1 Oleuropein ... 12
2.8.2 Zeytin yaprağının tıbbi özellikleri ... 13
2.8.3 Olea europaea L’nin antioksidan aktivitesi ... 14
2.8.4 Olea europaea L’nin fenolik madde içeriği ... 14
2.8.5 Olea europaea L.’nin antidiyabetik ve hipoglisemik etkisi ... 16
2.9 İnsan Hepatoselüler Karsinoma Hücrelerinin Özellikleri ... 17
2.10 Kanser ve Diyabet İlişkisi... 18
2.11 Tirozin Kinaz ... 19
2.12 Antioksidan Tayin Yöntemleri ... 20
2.12.1 Difenil pikril hidrazil (DPPH) yöntemi ... 20
2.12.2 Kuprak yöntemi ... 21
2.12.3 Troloks eşiti antioksidan kapasite yöntemi ... 21
2.13 Yüksek Basınçlı Sıvı Kromatografisi (HPLC) ... 21
vii 3. GEREÇ VE YÖNTEM ... 24 3.1 Gereç ... 24 3.1.1 Cihazlar ... 24 3.1.2 Kullanılan kimyasallar ... 25 3.2 Yöntem ... 27
3.2.1 Zeytin yaprağının ekstresinin eldesi ... 27
3.2.2 Farklı çözücülerde hazırlanan zeytin yaprağı ekstrelerinde HPLC ile oleuropein miktar tayini ... 28 3.2.2.1 Kullanılan ekipmanlar ... 28 3.2.2.2 Standart çözeltiler ... 28 3.2.2.3 Kromatografik koşullar... 28 3.2.2.4 Kalibrasyon ... 28 3.2.2.5 Oleuropein RP-HPLC metodu ... 29
3.2.3 Total fenolik içerik ... 29
3.2.4 Total flavanoid içerik ... 29
3.2.5 Prooksidan aktivite ... 29
3.2.6 2,2 ' -diphenyl-1-picrylhydrazyl (DPPH) radikal giderim aktivite yöntemi ... 30
3.2.7 Bakır indirgeyici antioksidan kapasite (KUPRAK) ... 31
3.2.8 ABTS radikal katyon yakalama aktivitesi ... 31
3.2.9 Hepatoselüler karsinoma hücrelerinin canlılık testi ... 32
3.2.10 Hepatoselüler karsinoma hücrelerinin apoptoz ölçümü ... 32
3.2.11 Hücre içi reaktif oksijen türlerinin miktar tayini ... 32
3.2.12 Western blot analizi ... 33
3.2.13. İstatistiksel analiz ... 34
4. BULGULAR ... 35
4.1 Oleuropein Konsantrasyonları ... 35
4.2 Total Fenolik İçerik ... 37
4.3 Total Flavanoid İçerik ... 38
4.4 Prooksidan Aktivite Tayini ... 39
4.5 Difenil Pikril Hidrazil Reaktif Ölçümü ... 40
4.6 Kuprak metodu ... 41
4.7 ABTS (2,2'-Azinobis [3-ethylbenzothiazoline-6-sulfonic acid) ... 42
4.8 Zeytin Yaprağı Ekstresi Miktarı ve Hücre Canlılığı ... 43
4.9 Apoptoz ... 45
4.10 Hücre İçi Reaktif Oksijen Türleri ... 49
4.11 Western Blot Analizi ... 50
5. TARTIŞMA ... 53
6. SONUÇ VE ÖNERİLER ... 63
KAYNAKLAR ... 64
viii KISALTMALAR
ABTS : 2,2′-azinobis-3-ethylbenzothiazoline-6-sulfonic acid ACE : Asetonitril
ADA : American Diabetes Association AMPK : AMP-activated protein kinase
AO : Akridin orange
AOA : Antioksidan aktivite AOK : Antioksidan kapasite APS : Amonyum persülfat BHA : Bütil hidroksi asetat
BHT : Bütillendirilmiş Hidroksi Toluen BSA : Bovin Serum Albumin
CAT : Katalaz CO2 : Karbondioksit CuCl2 : Bakır(II) Klörür DCM : Diklorometan ddH2O : İyonu giderilmiş su dh2O : Distile su DM : Diabetes Mellitus DMSO : Dimetil sülfoksit DNA : Deoksiribonükleik asit DPPH : Difenil pikril hidrazil DSO : Dünya Sağlık Örgütü
EB : Etidyum bromür
ET : Elektron transferi
EtOH : Etanol
FCR : Folin Ciocalteu Reaktifi
g : Gram
GAE : Gallik asit eş değeri
GDPH : Glukoz 6 fosfat dehidrogenaz GLUT 2 : Glukoz Taşıyıcı Protein Tip 2 GLUT 4 : Glukoz Taşıyıcı Protein Tip 4 GPx : Glutatyon Peroksidaz
GTB : Glukoz tolerans bozukluğu
H2DCF-DA : 2′,7′-Dichlorodihydrofluorescein diacetate
H2O : Su
H2O2 : Hidrojen peroksit
HAT : Hidrojen atomu transferi HBA1C : Hemoglobine bağlanmış glikoz HCC : Hepatosellüler Karsinoma HepG2 : İnsan Karaciğer kanser hücresi
HPLC : Yüksek Performanslı Sıvı Kromatografisi HRP : Horseradish peroksidaz
ix
IGF-I : İnsülin benzeri büyüme faktörü 1 Irs-1 : İnsülin Reseptör Protein 1
JNK : c-Jun N-terminal kinase KCl : Potasyum Klörür
KH2PO4 : Potasyum dihidrojen fosfat
LDL : Low Density Lipoprotein MetOH : Metanol
mg : Miligram
ml : Mililitre
MT : Metallotiyonin Na2CO3 : Sodyum karbonat
Na2HPO4 : Di sodyum hidrojen peroksit
NH4AC : Amonyum asetat
PBS : Phosphata buffered salin PBST : Phosphate buffered saline PVDF : Polyvinylidene floride
RIPA : Radio Immuno Precipitation Assay RNA : Ribonükleik asit
ROS : Reaktif oksijen türleri RTK : Reseptör tirozin kinaz SDS : Sodyum dodesil sülfat
SDS-PAGE : Sodyum dodesil sülfat poliakrilamid jel elektroforezi SOD : Süperoksit dismutaz
SPSS : Sosyal bilimler için statistik programı STZ : Streptozotosin
TAC : Toplam antioksidan kapasite TAT : Tamamlayıcı alternatif tedavi TBST : Tris-buffered saline
TCA : Trikloroasetik asit
TEAC : Troloks Eşiti Antioksidan Kapasite TEMED : Tetramethyl ethylene diamine
TK : Tirozin kinaz
TURDEP : Türkiye Diyabet Epidemiyoloji Çalışma Grubu UDPG : Uridin difosfoglukoz
UHY-ME : Ulusal Hastalık Yükü ve Maliyet Etkililik
UV : Ultraviyole
VEGF : Vasküler endotelyal büyüme faktörü WHO : World Health Organization
°C : Celsius
µg : Mikrogram
x TABLO LİSTESİ
Sayfa
Tablo 2.1 : Zeytin yaprağı ekstraktında bulunan fenolik maddelerin miktarları. ... 15
Tablo 3.1 : Kullanılan cihazların listesi. ... 24
Tablo 3.2 : Kullanılan kimyasalların listesi. ... 25
Tablo 3.3 : Prooksidan aktivite ölçümü için kullanılan kimyasallar ve zeytin
yaprağı ekstresi miktarları. ... 30
Tablo 3.4 : Çeşitli dozlarda verilen zeytin yaprağı ekstresinde DPPH antioksidan
aktivite tayini için kullanılan miktarlar. ... 31
Tablo 3.5 : Protein ekspresyon analizinde elektroforez için yükleme tamponu
içeriği. ... 33
Tablo 3.6 : Protein ekspresyon analizinde elektroforez için ayırma jeli içeriği. ... 34
Tablo 4.1 : Ekstraktların oleuropein içeriklerini gösteren tablolar. ... 35
Tablo 4.2 : Ekstrelerin organik çözücülerdeki ortalama oleuropein miktarları
(DCM:Diklorometan, ACE:Asetonitril, MetOH:Metanol). ... 35
Tablo 4.3 : Hepg2 hücrelerine farklı dozlarda verilen ekstrelerin canlılık yüzdeleri. ... 43
Tablo 4.4 : Hepg2 hücrelerinin canlılık, nekrotik, apoptotik yüzdeleri. (V:Viability,
A:Apoptotik, N:Nekrotik) ... 45
Tablo 4.5: Hepg2 hücrelerine verilen farklı dozlardaki zeytin yaprağı ekstresi
xi ŞEKİL LİSTESİ
Sayfa
Şekil 2.1 : Proinsülin zincir yapısı. ... 7
Şekil 2.2 : İnsülinin glukoz metabolizmasına etkisi. ... 8
Şekil 2.3 : İnsülinin karbonhidrat metabolizması üzerine etkisi. ... 9
Şekil 2.4 : Oleuropein yapısı.... 12
Şekil 2.5 : Oleuropein ile ilgili bileşiklerin kimyasal yapıları. ... 13
Şekil 2.6 : Diyabette oksidatif stresin artış metabolizması. ... 15
Şekil 2.7 : Oksidatif stresin hiperglisemi ile bağlantısı. ... 16
Şekil 2.8 : Sinyal iletim mekanizmasında tirozin kinaz rolü. ... 19
Şekil 2.9 : Membran temelli immün tespit yöntemi. ... 23
Şekil 4.1 : Farklı organik çözücülerle yapılan ekstraksiyon sonucu seri grafik. ... 36
Şekil 4.2 : Farklı organik çözücülerle gerçekleştirilen oleuropein konsantrasyonu (**:p<0.01) ... 36
Şekil 4.3 : Metanol, asetonitril, diklorometan, etanol organik çözücüleriyle yapılan ekstraksiyonlardaki fenolik içerik. (*:p<0.05) (DCM:Diklorometan, ACE:Asetonitril, MeOH:Metanol, EtOH:Etanol). ... 37
Şekil 4.4 : Farklı konsantrasyonlarda çözücülerle yapılan ekstraksiyondaki fenolik içerik. ... 38
Şekil 4.5 : Zeytin yaprağı ekstresinin dört farklı organik çözücüdeki flavanoid içerikleri.(*:p<0.05)(DCM:Diklorometan, ACE:Asetonitril, MeOH:Metanol, EtOH:Etanol) ... 38
Şekil 4.6 : Farklı konsantrasyonlarda çözücülerle yapılan ekstraksiyondaki flavanoid içerik. ... 39
Şekil 4.7: Zeytin yaprağı ekstresinin metanol, asetonitril ve diklorometan çözücülerindeki prooksidan aktivitesi. ... 39
Şekil 4.8 : Farklı organik çözücülerle yapılan ekstraksiyonun % inhibisyon değerleri. ... 40
Şekil 4.9 : Zeytin yaprağı ekstrelerinin yüzde inhibisyonlarının grafikleri. ... 41
Şekil 4.10 : Kuprak metoduyla organik çözücülerle yapılan ekstraksiyon yüzdeleri. ... 41
Şekil 4.11 : ABTS yöntemiyle yapılan ekstraksiyonun yüzde inhibisyon değerleri. ... 42
Şekil 4.12 : Çeşitli dozlarda zeytin yaprağı ekstresi verilen Hepg2 hücrelerinin canlılık değerleri. (-> :Aralığındaki değerler dahil) (*:p<0.05 **:p<0.01 ***:p<0.001) ... 44
Şekil 4.13 : Apoptoz ölçüm sonucunda görünen canlı hücreler. (Yeşil:canlı) ... 46
Şekil 4.14 :Apoptoz ölçüm sonucunda görünen nekrotik ve canlı hücreler. (Kırmızı:nekrotik, Yeşil:canlı) ... 47
Şekil 4.15: Apoptoz ölçüm sonucunda görünen apoptotik, nekrotik ve canlı hücreler. (Kırmızı:nekrotik, Turuncu:apoptotik, Yeşil:canlı) ... 47
Şekil 4.16 : Hepg2 hücrelerinin verilen çeşitli dozlarda zeytin yaprağı ekstresi sonucunda canlılık, apoptotik ve nekrotik değerleri. (*:p<0.05)(Yeşil:canlı, Kırmızı:nekrotik, Sarı:Apoptotik hücreler) ... 48
xii
Şekil 4.17 : Hücre içi reaktif oksijen türleri (*:p<0.05 **:p<0.01). ... 49
Şekil 4.18 : Zeytin yaprağı ekstresinin farklı dozlarında Hepg2 hücrelerindeki
reseptör oranları. (*:p<0.05 **:p<0.01 ***:p<0.001) ... 51
Şekil 4.19 : Hepg2 hücrelerindeki tirozin kinaz, Irs-1 reseptörleri ve Glut 4, Glut 2
xiii
ZEYTİN YAPRAĞI EKSTRAKTININ İNSAN HEPATOSELÜLER KARSİNOMA HÜCRELERİNDE TİROZİN KİNAZ, İNSÜLİN RESEPTÖR-1, GLUT4 VE GLUT2 PROTEİN EKSPRESYON SEVİYELERİ ÜZERİNE ETKİLERİNİN ARAŞTIRILMASI
ÖZET
Zeytin ağacı dünyadaki en dayanıklı ağaçlardandır. Yaprağı asırlardır yeryüzünde halk tarafından çeşitli hastalıkların tedavilerinde kullanılmaktadır. Zeytin yaprağının içerdiği, antioksidan özelliklere sahip olan yüz kadar farklı kimyasal madde günümüzde çeşitli kanser tiplerine sahip olan hastalarda ve Tip II diyabet hastalarında medikal tedaviye destek amaçlı kullanılmaktadır. Diyabetli bireylerde hipergliseminin karsinogenezde rol oynayan moleküller, antiapoptotik mekanizmalar, hücresel migrasyon ve invazivlik aracılığıyla kanser biyolojisine katkıda bulunduğu düşünülmektedir. İnsülin direnci sonucu ortaya çıkan inflamatuvar sitokinler hepatosteatoza yol açarak hepatoselüler karsinomlara zemin hazırlamaktadır. Tip II Diyabet, toplumun giderek yaşlanmasına ve sağlıksız beslenme tarzına bağlı olarak hızla artan, tedavi edilmediğinde morbidite, mortalitenin yükselmesine neden olan yaygın kronik bir hastalıktır. Günümüzde tedavisi için kimyasal kökenli ilaçların yanında bitkisel ürünler de kullanılmaktadır. Diyabetin bitkisel tedavisinde yaygın olarak kullanılan zeytin yaprağının önemli etken maddesi olan ‘oleuropeinin’ diyabetli bireylerde sıkça görülen kalp yetmezliği, damar tıkanıklığı gibi komplikasyonları önlediği; ayrıca zeytin yaprağında bulunan fenolik bileşiklerin damar içi plak oluşumunu engellediği ve bireylerde kan glukoz seviyesinde anlamlı düşüş sağladığı çeşitli çalışmalarla gösterilmiştir. Ancak etki mekanizmaları ile ilgili yeterince bilgi mevcut değildir.
Bu proje ile amacımız zeytin yaprağı ekstresinin in vitro hücre kültürü ortamında insan hepatoselüler karsinoma (HepG2) hücreleri üzerinde insülin reseptör protein (Irs-1), tirozin kinaz reseptörlerinin, GLUT-4 ve GLUT-2 transport proteinlerinin ekspresyonları üzerine etkilerini araştırmaktır.
Bu amaçla, zeytin yaprağı %70 metanol, / %30 su karışımı ile ekstrakte edildi ve liyofilizatörde liyofilize edildikten sonra %0.1 dimetilsüfoksit (DMSO) ile çözülerek, total fenol ve flavonoid içerikleri fotometrik yöntem ile belirlendi. Oleuropein konsantrasyonları HPLC (yüksek performanslı sıvı kromatografisi) metoduyla analiz edildi. Analiz sonuçlarından sonra farklı konsantrasyonlarda dilüe edilen zeytin yaprağı ekstraktının farklı konsantrasyonları Hücre kültürü ortamında Hepg2 hücreleriyle muamele edilip 24 saat inkübe edildi. Ardından sitotoksisite testi luminometrik ATP seviyesi tayini ile, reaktif oksijen türleri (ROS) florometrik yöntem ile analiz edildi. Elde edilen hücre lizatlarından IRS-1, Tirozin kinaz, GLUT-4 ve GLUT-2 protein ekspresyon seviyeleri Western Blot tekniği ile analiz edildi. İstatistiksel analizle de deney ve kontrol hücre gruplarının değerlendirilmesi yapıldı.
xiv
Zeytin yaprağı ekstraktının düşük konsantrasyonlarda (10µg/ml’ye kadar) proliferatif etki gösterdiği, 10 µg/ml’nin üzerinde doza bağımlı olarak sitotoksik etkinin arttığı, aynı şekilde 10 µg/ml’ye kadar ROS seviyelerinin düştüğü, 10 µg/ml üzerinde doza bağımlı arttığı, ROS ile hücre canlılığı arasında negatif güçlü ilişkinin olduğu tespit edildi. Protein ekspresyon analizi sonucunda zeytin yaprağı ekstresinin glukozun hücre içine girişini sağlayan reseptörlerin ve transport proteinlerin ekspresyonunu artırdığı, maksimum artışın 10 µg/ml dozunda gerçekleştiği görüldü.
Sonuçta, geleneksel olarak kullanılan zeytin yaprağı ekstresinin, hücre içine glukoz girişini sağlayan reseptörler ve transport proteinlerin ekspresyonunu artırdığı, dolayısıyla Tip II Diyabet’in tedavisinde kullanılabileceği kanaatine varıldı.
Anahtar kelimeler: Tip 2 Diyabet, zeytin yaprağı, insan karaciğer kanser hücresi, GLUT-2, GLUT4, tirozin kinaz, IRS-1
xv
RESEARCH OF THE IMPACT WHICH OLİVE LEAF EXTRACT CAUSES IN HUMAN HEPATOCELULAR CARSINOMA CELLS THAT INVOLVES TYROSİNE KİNASE,
INSULIN RECEPTOR-1, GLUT4 AND GLUT2 PROTEIN EXPRESSION LEVELS
SUMMARY
Olive tree is one of the most durable tree on earth. The leaf of olive tree have been used by folks in the treatment of various diseases. The reason why olive leaf is commonly used as a supplement in the recovery process of Type II Diabetes and various cancers is because it involves hundreds of antioxidant chemicals. Hyperglycemia in individuals with Diabetes is considered to be beneficial for cancer biology thanks to the molecules in carcinogenes, antiapoptothic mechanisms, cell migration and invasion. Inflammatuar cytokines, which formed due to insulin resistance, leads to hepatosteatosis which may cause hepatocelular carcinom after. Type II Diabetes is a widespread chronic disease that leads morbidity and mortality to rise when the population is getting untreated, increasing rapidly due to the age of the population and the unhealthy diet. Today, both chemical and herbal products are widely used for treatment. 'Oleuropeinin', an important ingredient of olive leaf, prevents complications such as heart failure, vascular occlusion, which are common in diabetic individuals; also phenolic compounds existing in the olive leaf block the formation of intravenous plaque and result in a significant decrease in blood glucose levels of individuals. However, there is insufficient information on the mechanisms of action.
The aim of this project is to investigate the effects of olive leaf extract on the expression of insulin receptor protein (Irs-1), tyrosine kinase, GLUT-4 and GLUT-2 receptor proteins on human hepatocellular carcinoma (HepG2) cells on in vitro cell culture medium.
For this purpose, olive leaf was extracted with 70% methanol / 30% water mixture and lyophilized in lyophilizer and then dissolved with 0.1% dimethylsulfoxide (DMSO), total phenol and flavonoid contents were determined by photometric method. Oleuropein concentrations were analyzed by HPLC (viability test). After the analysis results, different concentrations of the olive leaf extract diluted and they were treated in HepG2 cell culture medium and incubated for 24 hours. The cytotoxicity test was then analyzed by luminometric ATP level assay and reactive oxygen species (ROS) were analyzed by fluorometric assay. Within the obtained cell lysates; IRS-1, tyrosine kinase, GLUT-4 and GLUT-2 protein expression levels were analyzed by Western Blot technique. Statistical analysis also assessed the experimental and control cell groups.
It was determined that the olive leaf extract has a proliferative effect at low concentrations (up to 10 mg / ml) and it has an increase in cytotoxicity proportionally with dose (after 10mg/ml). Also, ROS levels were decreased until 10mg/ml and then proportionally increases proportionally (after 10 mg/ml) with dose. There was a strong negative correlation between ROS and cell viability. Protein expression
xvi
analysis revealed that olive leaf extract promoted the expression of glucose receptors and transport proteins, with a maximum increase of 10 μg / ml.
As a result, it has been concluded that the conventionally used olive leaf extract can be used in the treatment of diabetes mellitus. It also increases the expression of receptors and transport proteins that provide glucose entry into the cell.
Key Words: Type 2 diabetes, olive leaf, human hepatocellular carsinoma, GLUT-2, GLUT-4, tyrosine kinase, IRS-1
1 1. GİRİŞ VE AMAÇ
Zeytin, dünyanın çeşitli bölgelerinde yaygın olarak bulunan uzun ömürlü bir ağaçtır. Zeytin yaprağı yüz yıllardır kullanılan geleneksel tedaviye katkı sağlayan bitkiler arasında bulunmaktadır. Akdeniz diyetinin önemli bir bileşeni olan zeytinyağı gibi geleneksel tedavi seçenekleri arasında yer alan zeytin yaprağının da, sahip olduğu özellikler nedeniyle modern tıpta günümüzün önemli sağlık problemlerinden olan çeşitli kanserler ve diyabet gibi bazı hastalıkların tedavisinde kullanılabileceği düşünülmektedir. Zeytin yapraklarından elde edilen oleuropeinin oksidatif stres, enzimatik ve nonenzimatik antioksidanlar üzerine etkileri oleuropeinin hiperglisemi ve oksidatif stresi inhibe etme potansiyeli olduğu ve oksidatif stresle ilişkili komplikasyoların önlenmesinde faydalı olabileceği gösterilmiştir [1]. Zeytin yaprağının serbest radikalleri nötralize etme yeteneğinin iyi bilinmesi, özellikle reaktif oksijen ve nitrojen türlerinin insan vücudunda oluşturduğu hasarı azaltan fenolik antioksidan bileşiklere sahip olması, yaşlanma belirtilerini ve hücre degradasyonunu azaltarak birçok dejeneratif hastalığı önleyebilmesi onu geleneksel tedavide tercih edilen bitkiler arasında bulundurmaktadır. Oksidatif hasarın, kalp damar hastalıkları, kanser, diyabet ve diğer kronik hastalıkların riskinde bir artış ile ilişkili olduğu bilinmektedir [2]. Diabetes Mellitus (DM), gelişmiş toplumlarda sıklıkla en sık rastlanılan endokrinolojik hastalıktır. Günümüzde, birçok gelişmiş ve gelişmekte olan ülkede, epidemik hastalık olarak kabul edilmekte ve çoğu gelişmiş ülkenin, ilk beş ölüm nedeni arasında dördüncü sırada yer almaktadır. DM, genetik ve immün yapının neden olduğu bir seri patalojik olaylar sonucu, pankreas beta hücrelerinden salgılanan insülin hormonunun, mutlak veya göreceli azlığı ya da etki gösterememesi sonucu karbonhidrat, protein ve yağ metabolizmasında bozukluklara yol açan, hemen hemen tüm sistemlerde komplikasyonlara neden olan, kronik, hiperglisemik, metabolik bir hastalıktır [3,4]. Diyabetik hastalarda serbest oksijen radikallerinin ve lipid peroksidasyonunun önemli derecede arttığı ve oksidatif stresin; diyabet etiyolojisinde ve ilerlemesinde rolü olduğu bilinmektedir [5]. Biyolojik sistemlerde serbest radikal oluşumu, normal metabolik olayların seyri esnasında görüldüğü gibi, organizmada bazı yabancı maddelerin (ksenobiyotikler) metabolize
2
edilmesi sırasında ve organizmanın radyasyon gibi dış etkenlere maruz bırakılmasıyla da meydana gelebilir. Serbest radikallerin zararlı etkilerine karşı organizmada koruyucu mekanizmalar vardır. Bu mekanizmalardan bir kısmı serbest radikal oluşumunu, bir kısmı ise oluşmuş serbest radikallerin zararlı etkilerini önler. Bunu antioksidanlar aracılığıyla yapmaktadır. Dünya üzerinde farklı bitki türleri üzerinde bu bitkilerin terapötik etkinlikleriyle ilgili birçok araştırma yapılmaktadır. Güneş ışığı ve oksijenin neden olduğu oksidatif stresi kontrol etmek amacıyla bitkilerin antioksidan özellikleriyle ilgili çeşitli çalışmalar yapılmaktadır ve yeni antioksidan kaynakları aranmaktadır [6,7].
DM’nin görülme sıklığının ve tedavi masraflarının fazla olması, bunun yanı sıra kesin tedavi yönteminin henüz geliştirilememiş olması onu gündemde olan bir araştırma konusu yapmaktadır. Bu sebeple bu hastalığın tedavisi için birçok araştırma yapılmakta ve yeni tedavi yöntemleri aranmaktadır. Bazı araştırıcılar yüksek antioksidan içerikli bitkilerin ekstrelerini diyabet hastalığında denemişler ve oksidatif stresi baskılamaya çalışmışlardır. Zeytin yaprağının da bu bağlamda (Olea
europaea L.) geleneksel antidiyabetik ve antihipertansif bitkisel bir ilaç olduğu ileri
sürülmektedir. Zeytin yaprağının güçlü antioksidan etkiye sahip olduğu hayvan deneyleriyle de gösterilmiştir [8]. Bugüne kadar yapılan çalışmalarda zeytin yaprağının önemli bir etken maddesi olan ‘oleuropeinin’ diyabetli bireylerde sıkça görülen kalp yetmezliği, damar tıkanıklığı gibi komplikasyonları önlediği; ayrıca zeytin yaprağında bulunan fenolik bileşiklerin damar içi plak oluşumunu engellediği ve bireylerde kan glukoz seviyesinde anlamlı düşüş sağladığı gösterilmiştir. Ancak etki mekanizmalarına dair yeterince bilgi mevcut değildir [8].
Projemiz kapsamında elde edilecek zeytin yaprağı ekstrelerini Hepg2 hücreleri ile muamele ederek, glukoz metabolizmasını etkileyen ve özellikle glukozun hücre içerisine girişini kontrol eden reseptör ve transport proteinler üzerine araştırmalar yapılmıştır.
Bu çalışma; kontrol ve deney grubu insan hepatoselüler karsinoma hücrelerine çeşitli dozlarda verilen zeytin yaprağı ekstresinin, terapötik etkinlikleri konusunu ve aynı zamanda glukozun hücre içine girişini sağlayan reseptörlerin ve transport proteinlerin moleküler mekanizmalarını anlamamızı sağlayacak ve günümüzde tedavi seçeneklerine dair çeşitli yaklaşımlar olan Tip II Diyabetli hastalar için, zeytin
3
yaprağı ekstresinin, hücre içine glukoz girişini sağlayan reseptörleri ve transport proteinleri aynı zamanda bunların protein ekspresyonunu ne derece etkilediği hakkında bilgi verecek, medikal tedaviye desteğini de kanıtlayarak gelecekte moleküler düzeyde yapılacak çalışmalara ışık tutacaktır. Bu çalışma ile uzun dönemde diyabetli hastaların dışarıdan insülin alma oranları azaltılmaları konusunda yardımcı olacağı düşünülmektedir. Belirlenecek olan uygun dozda zeytin yaprağı ekstreleri sayesinde diyabetli hastalarının medikal tedavilerinin yerine geçmesi öngörülmektedir. Uzun dönemde dışarıdan ithal edilen anti diyabetik ilaçlara bağımlı olan ülkemizde, geleneksel tıpta kullanılan zeytin yaprağının kullanımının modern tıbbın araştırma yöntemleri ile araştırılması optimizasyonunun sağlanması ile diyabet hastalarında antidiyabetik olarak kullanılması yolu ilaç tüketiminin azaltılması, hedeflenen somut yararlar arasındadır.
4 2. GENEL BİLGİLER
2.1 Diabetes Mellitus Tarihçesi
Diabetes Mellitus (DM), geçmişten günümüze bilinen bir hastalıktır. DM ile ilgili en eski kayıtlar, M.Ö. 1500 yıllarında Mısır’da yazılmış Ebers papirüsünde yer almıştır. Bu papirüste sık idrara çıkmayla seyreden bir durum bulunur. “Diabetes” kelimesini, ilk kez Kapadokya’da M.S. 2. yüzyılda Areteus kullanmıştır. Areteus, diyabeti, idrar miktarında artış, aşırı susama ve kilo kaybının olan bir hastalık olarak tanımlamıştır. 1625 yılında Thomas Willis bu hastaların idrarlarının tatlı olduğunu belirtmek için “mellitus” şeklinde eklemiştir. Hindistan’da Ayurveda’da diyabetli hastaların idarının tatlı olduğunu bu yüzden böcek, sinek ve karıncaların, bazı insanların idrarını yaptığı yerlere toplandığını belirtmiştir. 1776 yılında Matthew Dobson idrarın tatlı olmasının diyabet hastalarının kanlarındaki ya da idrarlarındaki şeker miktarının artışı yüzünden oluştuğunu kanıtlamıştır [9]. Diyabet hastalarının idrarının tatlı olduğu 17. yüzyılda İngiliz bir doktor olan Thomas Willis tarafından yeniden keşfedilmiştir [10]. Geçmişten günümüze kadar şekerin karaciğerde glikojen olarak depo edilmesinden, insülin elde edilmesi, alfa ve beta polipeptid zincirlerinden oluşup 51 aminoasit içeren yapıda olması ve 3 boyutlu yapısının ortaya konmasına dair birçok yol kat edilmiştir [10].
Hastalığın etiyopatogenezi ile ilgili pek çok bilgi ise 1900’lü yıllarda edinilmiştir. Günümüzde immünolojik ve genetik çalışmalar sürdürülmektedir. Yaygın görülen bir endokrin ve metabolik hastalık olan DM, batı toplumlarında önde gelen ölüm nedenlerindendir [3].
2.2 Diabetes Mellitusun Tanımı
DM, hiperglisemi ile karakterize, karbonhidrat, protein ve lipit metabolizmalarının bozukluğu ile seyreden, kronik bir hastalıktır. Hastalığın ilerlediği sıralarda mikrovasküler, makrovasküler ve nöropatik komplikasyonlar gelişebilmektedir. Pankreas insülin salgılanmasının yetersizliği, insülin eksikliği veya insülin
5
molekülündeki yapısal bozukluklar sonucunda oluşan bu hastalık, etiyolojisi, genetik ve klinik tablosu ile karmaşık özellikte olan bir sendromdur [3,4]
2.3 Diabetes Mellitusun Tipleri
Diyabet oluşmadan önceki aşamada kişinin kan glikoz değerleri normalin üzerinde görülüp kan glikoz düzeyleri tanı koymak için yeteri kadar yüksek olmadığı durumlarda prediyabettir. American Diabetes Association (ADA) tarafından diabetes mellitus 4 tip olarak sınıflandırılmıştır [11].
Tip 1 Diyabet: Pankreas tarafından vücutta insülin hormonunun üretiminin yetersiz ya da hiç olmaması sonucunda gelişen diyabet tipidir. İmmünolojiktir.
Tip 2 Diyabet: İnsülin yetersizliği ile ilişkili ve insülin direnci sonucu gelişen diyabet tipidir.
Gestasyonel Diyabet: Gebelik sırasında gelişen diyabet tipidir. Gebelik sonrası gestasyonel diyabet olan kadınların %5-10’unda Tip 2 diyabet gelişir.
Diğer Tipler: Beta hücre ya da insülin fonksiyonunda genetik bozukluklar, pankreas hastalıkları, endokrin hastalıklar, enfeksiyonlar, ilaçlar ve diğer kimyasal maddelerin neden olduğu diyabet tipleridir.
2.3.1 Tip I Diyabet
İnsüline bağımlı, -İnsulin Dependent Diyabetes Mellitus (IDDM) - diyabet olarak tanımlanabilir. Bu tip diyabet total veya kısmi insülin eksikliği olarak tanımlanır. Polidipsi, poliüri, zayıflama ve ketoasidoz gibi semptomları gösterir. Hiperglisemi ve ketoasidoz oluşumunu engellemek amacıyla insülin tedavisine gereksinim göstermektedir. Bu tipte pankreasın insülin salgılayan β-hücrelerinin virüs kaynaklı enfeksiyonlar veya otoimmünitedeki değişimlerden dolayı tahrip olduğu gösterilmiştir [12].
Diabetes mellituslu bireylerin yaklaşık % 10-15’i Tip І diyabetiktirler. Semptomlar (örneğin; poliüri, polidipsi ve hızlı kilo kaybı) genellikle akut olarak ortaya çıkar. Diyabetik bireylerde pankreas adacık beta hücreleri kaybı görüldüğü için insülin yetersizliği mevcut olduğundan yaşamlarını sürdürebilmek ve ketozu önlemek için insüline bağımlıdırlar. Genellikle bu hastalık çocukluk ve genç erişkinlikte en fazladır. Yaklaşık olarak % 75’inde hastalık 30 yaşından önce başlar [13].
6 2.3.2 Tip II Diyabet
Bu tip diyabet daha çok yetişkinlerde görülmektedir bu sebeple, ergin tipi diyabet, sekonder (ikincil) diyabet, insüline bağımlı olmayan diyabet denir. Genellikle orta yaşın üzerindeki yaşlarda görülmeye başlamış olsa da son dönemlerde genç erişkinlerde ve çocukluk çağında da görülmeye başlamıştır [14].
Tip II diyabetli bireylerde 2 grup altında tanımlanabilir. Birincisi; insülinin periferik dokuları etkileme yeteneğindeki azalmadır. Bu azalma insülin direnci olarak isimlendirilir ve bazı araştırmacılar tarafından primer patolojik olay olarak düşünülmektedir. Diğeri beta hücre disfonksiyonudur. Bu, insülin direncini dengelemek için yeterli insülin üretmede pankreasın yetersizliğidir. Böylece hastalıkta önce insülinin göreceli yetersizliği oluşur ve sonra mutlak insülin eksikliği gelişir. İnsülin direnci ve insülin sekresyonundaki temel moleküler bozukluklar çevresel ve genetik faktörlerin kombinasyonundan kaynaklanmaktadırlar [13].
Bu tip diyabette beta hücrelerinde insülin oluşumu, salınımı, depo edilmesi ve beta hücrelerinin sayısı normaldir. Kandaki insülin düzeyi azalmış, normal ya da yüksek olabilir. Asıl bozukluk, insülinin etkilediği hedef hücrelerde insülin reseptör sayısının azlığı ya da hücre içinde postreseptör düzeyde insülin etkinliğinin azalması ve insüline karşı direnç gelişmesinden kaynaklanmaktadır. Bunun sonucu olarak glukoz hücrelere yeterince giremez ve hücrelerde glukoz kullanılamadığından bu tür diyabet gelişir. Az miktarda salgılanan insülin, kan glukozunu normal düzeyde tutmasa da yağları depo edecek düzeydedir. Bu nedenle genellikle kilo artışı vardır. Ağır bir enfeksiyon ya da hastalık durumunda hastalar komaya girebilir [15,16].
2.4 Diabetes Mellitus Belirtileri Poliüri
Polifaji Polidipsi Yorgunluk
Kuru ve kaşıntılı cilt Bulanık görme
Sık sık enfeksiyon gelişmesi
7 2.5 İnsülin Yapısı
İnsülin, vücuttaki bütün dokuları etkileyen glukoz, amino asitler, lipidler gibi besin maddelerinin hücre içinde tutulup depolanmasını sağlayan ve hemeostazına katkıda bulunan antikatabolik bir hormondur. İnsülin, pankreas langerhans adacıklarında bulunan hücrelerde üretilir ve ada içerisinde yaklaşık olarak %70 oranında bulunur. İnsülin A ve B polipeptid zincirinden oluşmuş 51 amino asit içeren bir yapıya sahiptir. A7, B7, A20 polipeptid zincirlerini B19 zincirine bağlayan, iki disülfit köprüsü ile birleşmiştir. Üçüncü bir zincir içi disülfit köprüsü ile de A zincirinde 6. Ve 11. Amino asitleri birleştirir. A ve B zincirinde sırası ile 21 ve 30 amino asit yer almaktadır. İnsan insülin geni, 11. Kromozomun kısa olanında yerleşmiştir. Molekül ağırlığı 5808 daltondur. Domuz insülini insan insülininden, B zincirinin C terminalinde threonin yerine alanin gecmesiyle farklı iken, sığır insülini 3. amino asidin pozisyonuyla farklıdır [20,21]. Proinsülin zincir yapısı Şekil 2.1’de gösterilmektedir [22].
Şekil 2.1 : Proinsülin zincir yapısı. 2.5.1 İnsülin reseptörü ve etki mekanizması
İnsülinin çizgili kas, miyokard, karaciğer ve yağ hücrelerinde kendine özgü spesifik reseptörleri vardır. İnsülin reseptörü hücre membranında bulunur. Aminoasit transport sistemiyle veya glukoz transport sistemiyle bağlıdır. Bu reseptör uyarıldığı zaman glukoz, aminoasitler hücre içine girer. İnsülin reseptörü, iki alfa ve iki beta alt ünitesinden oluşur. İki alfa alt ünitesi membranın dış yüzüne bakar, hormonu tanıma bölgesidir. İki beta alt ünitesi ise membrana gömülmüş şekildedir, tirozin protein kinaz aktivitesine sahiptir. İnsülin dış yüzdeki alfa ünitelerine bağlanır, internalize
8
edilir, kinaz aktivitesi uyarılır. Kinaz aktivitesi, reseptör proteinini ve hücre içi diğer proteinleri fosforile ederek aktivitelerini değiştirir ve böylece biyolojik cevapları oluşturur [23].
İnsülin reseptörünün fosforilasyon substratları olarak çeşitli intraselüler proteinler tanımlanmıştır. Üzerinde en çok çalışılmış olan insülin reseptör substratı 1 veya IRS-1'dir. Fosforilasyon sonucu IRS-1 aktive edildiğinde birçok olay tetiklenir ve diğer enzimlerin de aktivasyonu sonucu insülinin etkileri oluşturulur [24]. IRS-1 aktif hale geçince, fosfoinozitol-1,3-kinaz'ı aktifleştirir. Bunu sonucunda GLUT-4 glukoz taşıyıcısı transloke olur ve glukoz hücre içine alınır Böylece GLUT-4’ler hücre içindeyken translokasyon sonucu membrana yerleşirler. Tirozin kinaz aktivitesi ile başka pek çok protein/enzim de aktive edilir. Çekirdekteki transkripsiyon olayları tetiklenir. İnsülin reseptör etki mekanizması Şekil 2.2’de gösterilmiştir [25,26].
Şekil 2.2 : İnsülinin glukoz metabolizmasına etkisi.
2.5.2 İnsülinin karbonhidrat metabolizması üzerine etkileri
İnsülinin en iyi bilinen etkisi plazma glukoz konsantrasyonunu azaltmaktır. İnsülin glukozun çizgili kaslar, miyokard ve yağ dokusu hücreleri içine girişini arttırır. Hücrelere glukoz girişi kolaylaştırılmış difüzyon olayı ile (GLUT-4 taşıyıcısı kullanılarak) olur. İnsülin translokasyon yaptığı gibi, taşıyıcı moleküllerin sayısında da artmaya neden olur. GLUT-1 ve GLUT-2 nin de insülinle uyarıldığını bilinmektedir. Glukozun hücre içine alınmasından sonra bir takım mekanizmalarda
9
kullanılmasını sağlar. Hücre içine giren glukoz, hekzokinaz enzimi tarafından fosfatlanır. Oluşan glukoz-6-fosfat hücre membranından geçemediği için dışarı çıkamaz. İnsülin bu maddenin glikoliz yolağı üzerinden laktik asite kadar yıkılmasını hızlandırır. Ayrıca glukoz-6-fosfataz enzimini inhibe ederek bu maddenin glukoza dönüşümünü inhibe eder. Ayrıca bu maddenin gliseraldehit-3-fosfat (gliserol fosfat)'a dönüşümünü stimüle eder. Bu madde lipit metabolizması açısından önemli. Bu maddenin (glukoz-6-fosfat'ın) glukuronik asit yolağında önce uridindifosfoglukoz (UDPG)'a dönüştürülmesini ve daha sonra glikojen sentaz enzimini indükleyerek (sentezini, miktarını arttırarak) glikojen oluşumunu stimüle eder. Glikojenez olayını artırır. İnsülin glikojen yıkılması olayı (glikojenoliz)'nı inhibe eder (amaç glikozu glikojen deposu şeklinde tutmak). İnsülinin karbonhidrat metabolizması üzerine etkileri Şekil 2.3’te gösterilmiştir [27].
Şekil 2.3 : İnsülinin karbonhidrat metabolizması üzerine etkisi.
Bu olay katekolaminler, glukagon, glukokortikoidler ve büyüme hormonu tarafından aktive edilir. İnsülin bu hormonların bu etkisini inhibe eder İnsülin glukoneogenezi, yani aminoasitlerden glukoz yapımı olayını azaltır. Bütün bu etkiler kan glikozunu azaltıcı etkiye katkıda bulunur [28].
10 2.6 Diabetes Mellitus Epidemiyolojisi
Diyabetli hastaların %90-97’sini Tip 2 diyabetli hastalar oluşturmaktadır. Gelişmekte olan ülkelerde diyabet prevelansının hızla artacağı düşünülmektedir. World Health Organization (WHO) verilerine göre diyabetik hasta sayısı Hindistan’da günümüzde 19 milyon iken 2025 yılında 57 milyona, Çin’de 16 milyondan 38 milyona çıkacağı tahmin edilmektedir. Pakistan, Endonezya ve Meksika’da bu anlamda önemli artışların görüleceği ülkelerdendir. Bu artış doğrultusunda DM dünyanın en önemli halk sağlığı sorunlarından biri haline gelmiştir [29]. 2003 Ulusal Hastalık Yükü ve Maliyet Etkililik (UHY-ME) Çalışması Hane Halkı Araştırmasında diyabet insidansı toplamda yüzbinde 3820, erkeklerde 3210.2 ve kadınlarda 4280.1 olarak bulunmuştur. Türkiye’de ulusal düzeyde ölüme neden olan ilk 10 hastalığın yüzde dağılımı incelendiğinde diyabet %2.2 ile 8. sırada yer almaktadır. Diyabet tüm yaş gruplarında %1.9 ile ulusal düzeyde sakatlığa uyarlanmış yaşam yıllarına neden olan 12. hastalıktır [29].
DM’nin prevalans ve insidansı, coğrafi bölge, ırk ve yaşa göre farklılıklar göstermektedir. Türkiye Diyabet Epidemiyoloji Çalışma Grubu (TURDEP) 2002 yılında ülkemizde Tip 2 DM prevalansını %7,2; Glukoz Tolerans Bozukluğu (GTB) prevalansını ise %6,7 olarak açıklamıştır [30]. TURDEP II çalışma sonuçlarına göre Türk erişkin toplumunda diyabet sıklığının %13.7’ye ulaştığı görülüp 12 yılda diyabet sıklığı %90 artmıştır [31]. Dünya Sağlık Örgütü verilerine göre; 2009 sonu itibari ile tüm dünyadaki diyabet nüfusu 285 milyon iken bu sayının 2030 yılında tüm dünyadaki diyabetli birey sayısının 438 milyona ulaşacağı düşünülmektedir. Düşük ve orta gelirli ülkelerde ise bu oranın tüm diyabetlilerin %80’inden fazla olacağı yönündedir. Bu sayının %90-95’i Tip II, yani insüline bağımlı olmayan diyabettir [32].
2.7 Fitoterapinin Tarihçesi
M.Ö. 3000 yıllarında Mezopotamya’dan Hititlere, Grek uygarlığından Roma Bizans uygarlığına, İslam ve Selçuklu uygarlığından Osmanlı uygarlığına kadar birçok tıp adamı yetişmiş ve çeşitli bitkisel yöntemler kullanmışlardır. Çağdaş tıp döneminde, tamamlayıcı ve alternatif tedavi (TAT) yöntemleri kullanımı gelişmekte olan ve endüstrileşmiş birçok ülkede artmıştır. ‘’Fitoterapi (phytos=bitki, therapy=tedavi)’’, doğal bitkileri kullanarak hastalıkları tedavi etme yöntemidir. Bitkiler insanların
11
hayatı için ve hastalıkların tedavisinde kullanımları sebebiyle önemli canlılardır. Besin, yakacak ve giyecek elde etmede insanlar bitkilerden büyük ölçüde yararlanmışlardır [33]. Ülkemizdeki sıklığı bilinmemekle birlikte çok sayıda hasta tıbbi tedavilerin yanı sıra bitkisel tedavilere de başvurmaktadır [34]. Bitkilerin kimyasal ve biyolojik etki zenginliğinden “insan sağlığı” için akılcı bir şekilde yararlanılabilmesi önemlidir. İzole edilen saf bileşen tedavide kullanılabilir. Bitki ekstreleri içerisinde bileşenlerin “Ekstre” halinde sinerjistik/antagonistik etkileşmelerle, terapötik etkileri artabilir, yan etki profili azaltılabilir. Bu tip formülasyonlar kullanılarak daha etkin ve sürekli tedavi cevabı sağlanabilmesi mümkün olabilmektedir [35].
2.7.1 Fitoterapi tedavisi ve seçenekler
Tamamlayıcı ve alternatif tedaviler (TAT), Amerikan Ulusal Tamamlayıcı ve Alternatif Tıp Merkezi tarafından “standart tıbbi tedavilerin dışında kalan çeşitli sağlık bakım sistemleri, uygulamaları ve ürünleri” olarak tanımlanmaktadır. Alternatif tıbbın amacı, hastalığı meydana getiren genetik, sosyal, çevre, iş faktörleri ve organdaki bozukluktan etkilenen diğer organsal fonksiyonel değişiklikleri bunun oluşturduğu psikolojik ve ruhsal farklılaşmaları birlikte değerlendirerek bunlara çözüm aramaktır [36].
2.8 Olea europae L.’nin Bilimsel Sınıflandırılması
Alem : Plantae Bölüm : Magnoliophyta Sınıf : Magnoliopsida Takım : Lamiales Familya : Oleaceae Cins : Olea Tür : O. Europae
12 2.8.1 Oleuropein
Zeytin meyvesinin ilk dönemlerinde meyvede daha fazla bulunan, olgunlaşmanın ilerlemesi ile zamanla metabolize olarak miktarı azalan ve meyveye acılık veren bir maddedir [37,38,39,40]. Zeytin yaprağında en çok bulunan biyoaktif bileşik oleuropein ve rutindir. Oleuropein doğada en yoğun olarak zeytin yapraklarında bulunmaktadır [1,37,38,39,40,41].
Oleuropein ilk kez 1908 yılında Bourquelot ve Vintilesco tarafından tespit edilmiştir [8]. Yapısı ise 1960 yılında tanımlanabilmiştir. Oleuropein molekülünün kimyasal yapısı Şekil 2.4’te gösterilmiştir [8,42].
Şekil 2.4 : Oleuropein yapısı. Oleuropein;
Antimikrobiyal Antioksidatif Antiatherojenik
Yüksek antioksidan potansiyeli
Hipotansif aktivitesi (Kan basıncını düşürücü)
Antienflamatuvar etkisi (5- lipoksigenaz enzimini inhibe ederek)
Kardiyopropektif (LDL oksidasyonu inhibisyonu ve trombosit-kan hücresi aggregasyonu)
Hipoglisemik (Kan şekeri düşürücü)
13 Antiviral (HIV vrüsüne karşı etkili) Stostatik (McCoy hücrelerine karşı)
Mollusisidal (Salyangozlara karşı olan toksik etki) Endokrinal-hormonal
Enzim modülatörü [43].
Oleuropein ile ilgili bileşiklerin kimyasal yapıları Şekil 2.5’te gösterilmiştir [44].
Şekil 2.5 : Oleuropein ile ilgili bileşiklerin kimyasal yapıları.
2.8.2 Zeytin yaprağının tıbbi özellikleri
Zeytin yaprakları tanen, uçucu yağ, organik asitler ve rezin taşır. 1960 yılında, Panizzi ve arkadaşları acı bir glikozid olan oleuropeini zeytin yapraklarından izole etmişlerdir. Daha sonra bu maddenin bir fenolik bileşik olduğu iridoid gruba ait olduğu göstermişlerdir [45]. Bu ayrıca zeytinde de mevcuttur. Oleuropein zeytin ağacında, yaprakta, tomurcukta, meyvede, odunda ve ağaç kabuğunda da bulunmaktadır. Zeytin yaprakları ortalama her gramında 60-90 mg (kuru ağırlık) oleuropein içermektedir. İlaveten önemli seviyede içerdiği elenoik asidin glikozidik esteri ve hidroksitirizol, oleuropein ve onun hidrolize ürünleri olan oleuropein aglycone, elenoik asit, beta-3,4 dihidroksifenetil alkol ve metil-o-metil elelonat, biyolojik olarak ilgi çeken moleküllerdir [29].
14 2.8.3 Olea europaea L’nin antioksidan aktivitesi
Reaktif oksijen ve nitrojen türleri; detoksifikasyon, kimyasal sinyalizasyon, enerji gereksinimi ve bağışıklık fonksiyonları için gereklidir. Onlar sürekli olarak insan vücudunda üretilir ve SOD, GPx ve CAT gibi endojen enzimler tarafından kontrol edilir. Bu reaktif türlerin aşırı bir üretim olursa, dış oksidant maddelere maruz kalma ya da savunma mekanizmasında anormal bir durum ve çeşitli biyomoleküllerde (DNA, lipidler, proteinler) hasar meydana gelebilir. Bu hasar kardiovasküler, kanser ve diğer kronik hastalıkların artan riskiyle ilgilidir. Antioksidanlar bu hasarı önlerken, aynı zamanda diyetle alınan antioksidanların artışı kronik hastalıkların riskini düşürür. Kardiovaskular hastalıklara ve belli kanserlere karşı sebze ve meyvelerdeki zengin diyetlerin koruyucu etkileri kısmi olarak antioksidanlara bağlıdır [8].
2.8.4 Olea europaea L’nin fenolik madde içeriği
Yapılan çalışmalarda zeytin yaprağı ekstraktında bulunan temel fenolik maddelerin oleuropein ve onu takiben hidroksitirosol olduğu belirlenmiştir [8]. Zeytin yaprağı ekstraktında belirleyici fenolik maddenin oleuropein olmasına rağmen oluropeinin saf haldeki antioksidan kapasitesi sınırlıdır. Ancak zeytin yaprağı ekstraktının antioksidan kapasitesi güçlü bir antioksidan olan hidroksitirosol ile yakın, C ve E vitamininden ise çok daha yüksek düzeydedir. Bu durum iki farklı şekilde açıklanabilir [8].
1. Oleuropein ekstrakt içerisinde kendisinden çok daha güçlü olan hidroksitirosole parçalanmaktadır ve ekstraktın toplam antioksidan kapasitesini yükseltmektedir.
2. Ekstrakt içerisindeki fenolik maddeler sinerjistik etki göstermektedir. Zeytin yaprağındaki fenolik maddeler ve miktarları Tablo 2.1’de gösterilmiştir.
15
Tablo 2.1 : Zeytin yaprağı ekstraktında bulunan fenolik maddelerin miktarları.
Fenolik Maddeler % miktar (kuru temel) TEAC (mM)
Ekstrakt - 1,58 ± 0,06 Olueropein 24,54 0,88 ± 0,09 Hidroksitirosol 1,46 1,57 ± 0,12 Lutelin-7-glukosit 1,38 0,71 ± 0,04 Apigenin-7-glukosit 1,37 0,42 ± 0,03 Verbaskosit 1,11 1,02 ± 0,07 Tirosol 0,71 0,35 ± 0,35 Vanilik asit 0,63 0,67 ± 0,09 Diosmetin-7-glukosit 0,54 0,64 ± 0,09 Kafeik asit 0,34 1,37 ± 0,08 Luteolin 0,21 2,25 ± 0,11 Rutin 0,05 2,75 ± 0,05 Diosmetin 0,05 1,42 ± 0,07 Vanilin 0,05 0,13 ± 0,01 Kateşin 0,04 2,28 ± 0,04
Diyabette oksidatif stresin artış metabolizması Şekil 2.6’da gösterilmiştir.
Şekil 2.6 : Diyabette oksidatif stresin artış metabolizması [46].
Metabolik stres oksidatif olayların artmasına neden olmaktadır. Diyabet komplikasyonlarının gelişimini kolaylaştıran bu durum, yapısal ve fonksiyonel hasarı oluşturmaktadır. Normalde çok düşük olan HbA1C düzeyinin kan konsantrasyonu, yüksek kan glukozu ile seyreden kişilerde total hemoglobinin %12 kadarına veya
16
daha üzerine çıkabilmektedir. Ortalama eritrosit ömrü 120 gün olduğundan HbA1C düzeyleri son dört aylık süreyi kapsayacak şekilde dolaşımdaki kan şeker düzeyi için iyi bir gösterge olmaktadır [47,48].
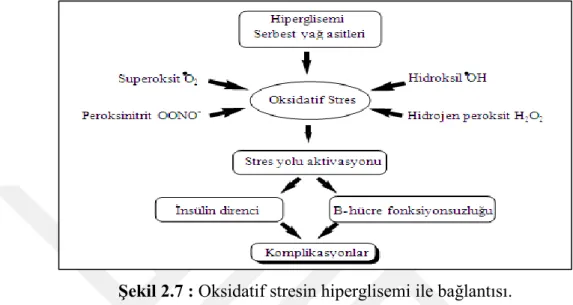
Oksidatif stresin hiperglisemi ile bağlantısı Şekil 2.7’de gösterilmiştir [47].
Şekil 2.7 : Oksidatif stresin hiperglisemi ile bağlantısı.
Hiperglisemideki aşırı oksidatif stresin vasküler duvarlarda ve plazmada lipit peroksidasyonunu artırmasıyla aterosklerozis oluşumu arasında ilişki olduğu tespit edilmiştir. Ayrıca diyabette vasküler ve diğer komplikasyonların sebebi olarak sigara, hipertansiyon ve dislipitemi gibi faktörler gösterilmektedir. Bazı araştırıcılar bu risk faktörlerinin oksidatif stresi artırarak diyabetin patofizyolojisine ve komplikasyonların gelişimine katkıda bulunduğunu bildirmektedirler [48].
2.8.5 Olea europaea L.’nin antidiyabetik ve hipoglisemik etkisi
Zeytin yaprakları, antidiyabetik ve antihipertansif bir bitkisel ilaç olarak bilinir [49]. Aynı zamanda diyabetik hiperglisemi, hipertansiyon ve bulaşıcı hastalıkları tedavi etmede kullanılır, hipertansiyon ve diyabet için geleneksel bir tedavi olarak tanımlanır [50]. Diyabette oleuropeinin hipoglisemik etkisini açıklamak için iki mekanizma ileri sürülmektedir [2].
1. Glukoz kaynaklı insülin salınımını etkileme potansiyeli 2. Periferik glukoz alınımını artırma etkisi
17
Alloxan ile diyabet oluşturulan tavşanlarda oleuropeinin antioksidan ve hipoglisemik etkileri incelenmiştir. Tavşanlar 16 hafta boyunca oleuropein ile tedavi edilmiş. Tedaviden sonra oleuropein ile tavşanların kan glukoz seviyelerinin önemli bir şekilde azalttığı ve oleuropinin diyabet ve hipoglisemiyi engellemede faydalı olabileceğini belirtilmiştir [2].
Diyabetik ratlara yemlendikten sonra zeytin yaprağı ekstresi verilerek kan glukozundaki değişmeleri incelenmiş ve hem luteolin hem de alealonik asitin yemlenme sonrası diyabetik ratlardaki kan glukozunun artmasını engellediğini tespit edilmiştir [50].
2.9 İnsan Hepatoselüler Karsinoma Hücrelerinin Özellikleri
Hepg2 (insan hepatoselüler karsinoma) hücre hattı, Amerika’da bulunan beyaz ırka sahip 15 yaşında erkek bireyin farklılaşma gösteren hücrelere sahip olan hepatoselüler karsinoma örneğinden hazırlanmıştır. Hepg2 hücrelerinin diğer hücre hatlarına göre kültüre edilmesi daha kolay olduğu için oldukça avantajlı yönleri bulunmaktadır. Aynı zamanda bu yönleri nedeniyle in vitro modellemelerde yaygın olarak kullanılmaktadır. Bu avantajlı yönlere bakılacak olursa; biyosentetik özelliklerinin normal hepatositlere benzerliği, hücre yüzey reseptörlerini koruyabilmesi, plazma proteinlerinin büyük bir kısmını üretebilmesi, metal ve organik bileşiklere maruz kaldığında metallotiyonin (MT) oluşturması, yüksek-düşük yoğunluklarda lipoproteinlerin sentezlenmesi, serumsuz besiyerinde üretilmesi durumunda ise karaciğere özel çeşitli serum proteinlerini üretebilmesi, sitokrom p450 (CYP450)‟ ye bağımlı monooksijenaz enzimlerine sahip olması ve glukuronat-sülfatla birleşme tepkimelerini gerçekleştirebilmesi sonucu 14 detoksifikasyon işlemlerinde gerekli olan normal biyotransformasyon etkinliklerinin çoğunu yapmakta ve dolayısıyla in vitro toksisite modellemesi olarak yaygın kullanılmaktadır [51]. Hepg2 hücreleri birçok bitki sitotoksisitesi araştırmalarında da kullanılmıştır [52-53]. Bu çalışmada karaciğer kanser hücrelerinde insülin transport proteinleri olan Glut tiplerinin çoğunun çalışılabilmesi ve daha çok hücre soyu üretilmesi gibi özellikleri nedeni ile Hepg2 hücreleri kullanılmıştır.
18 2.10 Kanser ve Diyabet İlişkisi
Diyabet ve kanser tüm dünyada yüksek ölçüde mortalite ve morbidite oranları olan en önemli sağlık sorunları arasında yer almaktadır. Diyabete benzer şekilde kanser prevalansı da gün geçtikçe artmaktadır ve mortalite sıralamasında 2. basamakta yer almaktadır [54]. Geçmişten günümüze yapılan tüm çalışmalar, diyabet ile kanserin ortak patogenetik mekanizmaları olduğunu ve diyabetli bireylerde sağlıklı bireylere oranla bazı kanser tiplerinin daha sık görüldüğünü desteklemektedir. Bunun yanında diyabet tedavisinde kullanılan bazı ajanların da kanser riskini arttırdığına dair bulgular mevcuttur. Her iki hastalık arasındaki ilişkiye dair ilk bulgu 1934’te diyabetli hastalarda pankreas kanseri sıklığının diyabet olmayan bireylere kıyasla daha yüksek olduğunun fark edilmesi ile elde edilmiştir [55]. Sonrasında çeşitli klinik ve epidemiyolojik araştırmalarda diyabetli bireylerde çeşitli hematolojik malinitelerin riskinde artış görülmüştür. Risk artışının pankreas, karaciğer ve endometrium kanserinde en yüksek olduğu belirlenmiştir. Birçok epidemiyolojik çalışmada, tip 2 diyabetin hepatoselüler karsinoma gelişme riskini 2-3 kat arttırdığı gösterilmiştir [56,57]. Risk hepatit C ve hepatit B’li olgularda en yüksek olarak belirlenmiştir [58,59]. Karaciğerin ven yoluyla endojen insüline en fazla maruz kalan organlardan biri olması, hiperinsülinemi durumunda uyarılan insülin benzeri büyüme faktörü 1 (IGF-1)’in karaciğerde hücresel proliferasyonu arttırarak apoptozu inhibe etmesi ve karsinogenezi tetiklemesi nedeniyle gerek in vitro gerekse in vivo çalışmalar bulunmaktadır [60,61]. Hipergliseminin karsinogenezde rol oynayan anahtar yolaklardaki moleküller (epidermal büyüme faktörü, protein kinaz C, peroksizom proliferatör-aktive reseptörler, siklin-bağımlı kinaz 2), antiapoptotik mekanizmalar, hücresel migrasyon ve invazivlik (E-kaderin, reaktif oksijen radikalleri, çinko) üzerinden kanser biyolojisine katkıda bulunduğu düşünülmektedir [62]. Bunun yanında insülin direnci sonucu ortaya çıkan inflamatuvar sitokinler hepatosteatoza yol açarak HCC’ye zemin hazırlamaktadır [63]. Ayrıca diyabet tedavisinde kullanılan insülin salgılatıcı bazı antidiyabetik ajanların kanser riski oluşturduğuna dair çalışmalar da mevcuttur. Yakın zamanda yayınlanan ve sülfonilürelerin kullanıldığı 18 çalışmayı içeren bir analizde sulfonilüre kullanımının kanser riskini arttırdığı belirtilmiştir [64]. Bununla birlikte, çalışmaların bazılarında insülin direnci üzerinden etki gösteren oral antidiyabetik ajan olan metforminin insülin-duyarlılaştırıcı ajanlar dışındaki diğer antidiyabetiklere kıyasla kanser riskini azalttığı bildirilirken, bazı çalışmalarda da etkisi olmadığı belirtilmiştir [65,66,67].
19 2.11 Tirozin Kinaz
Tirozin Kinaz (TK), protein fosforilasyonunu sağlayan protein kinaz ailesine mensup bir enzimdir. Kinazlar yoluyla proteinlerin fosforilasyonu, sinyal iletim mekanizmasında önemli rol oynar. Sinyal iletimi hücrelerin çoğalması ve apoptozisi gibi işlevleri kontrol ettiğinden, burada meydana gelen değişimler kanser gelişiminde ve metastazlarda önemli rol oynar. TK’lar bulundukları yere göre 2 gruba ayrılır; membran yerleşimli (reseptör) ve sitoplazmik yerleşimli (non-reseptör). Membranda yerleşenlere reseptör tirozin kinazlar (RTK) denir. Bu reseptörler arasında insülin reseptörü, büyüme faktörleri reseptörleri ve efrin reseptörleri örnek gösterilebilir [68]. Bilinen yaklaşık 2000 kinaz arasında, 90'dan fazla TK insan genomunda bulunmaktadır. Bunların hücresel aktivitelerde (büyüme, diferensiyasyon, metabolizma, adezyon, motilite, ölüm vs.) önemli rolü vardır. Birçok RTK, gen mutasyonu veya kromozom translokasyonu nedeniyle değişime uğrayarak kanser gelişimde etkin rol oynar. Bu patolojik durum kısaca aşırı-ekspresyon olarak da tanımlanabilir [69]. Sinyal iletim mekanizmasında tirozin kinazın rolü Şekil 2.8’de gösterilmiştir.
20 2.12 Antioksidan Tayin Yöntemleri
Antioksidan kapasitesini ölçmek için çok sayıda yöntem geliştirilmiştir [70]. Bu yöntemlerde antioksidan kapasite (AOK); reaksiyon termodinamiği ile ölçülürken antioksidan aktivite (AOA); reaksiyon kinetiği oranı ile ilişkilendirilerek ölçülür. Bu metotların en geniş kabul gören sınıflandırma şekli hidrojen atomu transfer (HAT) temelli ve elektron transfer (ET) temelli analiz yöntemleridir [71]. HAT temelli yöntemler genel olarak azo bileşiklerin bozulması ile oluşan peroksil radikalleri için antioksidan ve substratın rekabetine dayanan rekabetli reaksiyonlardır. ET temelli yöntemler antioksidanın oksidanı indirgenme yeteneğini renk değişimi ile ölçer. [70]. HAT reaksiyonları; çözücü, pH etkisinden bağımsızdır ve kısa bir sürede gerçekleşir. ET reaksiyonları; çözücü, pH'a bağlı olarak ve daha yavaş şekilde gerçekleşirler [72].
2.12.1 Difenil pikril hidrazil (DPPH) yöntemi
Bu metot ilk olarak Brand-Williams ve arkadaşları tarafından 1995 yılında geliştirilmiştir sonrasında yapılan çalışmalarda Sanchez ve arkadaşları tarafından 1998 yılında farklı olarak kullanılmaya başlanmıştır [73]. DPPH (2,2-difenil-1- pikrilhidrazil) ticari olarak elde edilebilen stabil organik nitrojen radikalidir [74]. DPPH radikal süpürme kapasitesi analiz yöntemleri ekstraktların antioksidan içeriğini ölçmede yaygın olarak kullanılan bir yöntemdir [75]. Bu yöntem de temel olarak antioksidan tarafından DPPH serbest radikaline proton transferi reaksiyonu 517 nm’de absorbansın azalmasına sebep olur. Bu süreç görünür alanda spektrofotometre ile absorbans sabit olana kadar takip edilmesi prensibine dayanmaktadır [70]. DPPH radikali metanolik çözeltide okside formunda yaklaşık 520 nm’de en yüksek absorbansa sahip bir kimyasaldır. Bu yöntem basit, hızlı ve birçok örneğin radikal süpürme aktivitesini gözlemlemek için farklı örneklerin çözünürlüklerine elverişli bir metot olarak belirlenmiştir. Ancak ışığa, oksijene ve kirliliğe olan hassasiyeti bu metodun kullanımında sınırlamalara sebebiyet vermektedir [75].
21 2.12.2 Kuprak yöntemi
Cu (II) İyonu İndirgeyici Antioksidan Kapasite (KUPRAK) Yöntemi İlk olarak Apak ve arkadaşları tarafından geliştirilmiştir. Temelde 2,9- dimetil-1, 10-fenantrolin (Neokuproin Nc)’in Cu (II) ile oluşturduğu bakır (II)-neokuproin kompleksinin (Cu(II)-Nc), 450 nm’ de en yüksek absorbans veren bakır (I)- neokuproin (Cu(I)-Nc)’e indirgenme yeteneğinden yararlanılarak antioksidan kapasite hesaplanmaktadır [76]. KUPRAK yönteminin toplam antioksidan kapasite (TAC) analizinde diğer transfer yöntemlerinden ayırıcı avantajı kolay pH ayarlaması, reajanların kolay kullanılabilmesi ve stabil olması, düşük maliyetli ve basit olması, hidrofilik antioksidanların yanında lipofilik antioksidanlara da uygulanabilmesidir [71].
2.12.3 Troloks eşiti antioksidan kapasite yöntemi
Troloks Eşiti Antioksidan Kapasite (TEAC veya ABTS) Yöntemi ilk olarak Miller ve arkadaşları tarafından gösterilmiş [77] olup daha sonra yapılan çalışmalarla Re ve arkadaşları tarafından da geliştirilmiştir [78]. TEAC analizi 2,2’-azinobis (3-etil-bezotiazolin 6 sulfonat) (ABTS) radikal katyonunun antioksidanlar tarafından absorbansının engellenmesi temeline dayanır. TEAC’ın karakteristik dalga boyu 660, 734 ve 820 nm’de en yüksek absorbansı yapar [79]. Radikal katyon formunda üretilen ABTS, temel spektrofotometrik olarak çeşitli maddelerin toplam antioksidan kapasitesini ölçmek için uygulanır. Deneyler renksiz sıvı potasyum persülfit ile ABTS’nin oksidasyonu aracılığında ABTS’deki renk üretimini içermekte olup hem lipofilik bileşenlere hem de hidrofilik bileşenlere uygulanabilir. ABTS çözeltisi seyreltilir ve 10 dakika içinde absorbansı ölçüldükten sonra 1 ml çözeltiler ile farklı konsantrasyonlardaki ekstraktların ilk hazırlanan karışımları ölçülür. Trolox, vitamin E’nin suda çözünen kısmı olup referans standart olarak kullanılır. Analiz bitkilerin antioksidan özelliklerini belirlemek için kullanılmaktadır [73].
2.13 Yüksek Basınçlı Sıvı Kromatografisi (HPLC)
Son zamanlarda yeni kolon dolgu maddelerinin geliştirilmesiyle HPLC metodu biyomoleküllerin ayrılmasında yaygın olarak kullanılmaktadır. Böylece birçok molekülü yapısal ve işlevsel olarak analiz etmek için biyomoleküller kısa sürede
22
saflaştırılmaktadır. Günümüzde HPLC’nin modern olarak kullanılan sıvı kromatografilerine göre önemli üstünlükleri bulunmaktadır. Kolonları yeniden doldurulmadan ve yenilenmeksizin sürekli kullanılabilmesi, tekrarlanabilirliğinin oldukça yüksek olması, verilerin analizinin kolaylıkla otomatikleştirilmesi;büyük boyutlardaki ayırım süreçlerine uygulanması sebebiyle diğer klasik yöntemlere göre, ayrıştırma ve analiz hızı oldukça yüksektir [80].
2.14 Western Blot Tekniği
1979 yılında Towbin ve arkadaşları tarafından bulunan bu tekniğe protein blotlama ya da Western blotlama ismi verilmiştir. “Western blot” ya da “Immunoblott” tekniği, antikor tespitinin özgüllüğü ile jel elektroforezinin çözünürlüğünü bir araya getiren bir yöntemdir. Blotlama tekniği, bir antijenin moleküler ağırlığı, varlığı ve miktarı, antijen izolasyonunun etkinliği gibi protein antijenlerinin önemli özelliklerini belirlemede kullanılabilir. Kompleks bir örnek içerisinde düşük miktardaki proteinlerin tespit edilmesi ya da protein sentezi görüntülenmesi için kullanılır. “Western blot”, protein karışımının jel elektroforezi ile ayrıştırıldıktan sonra uygun bir membrana transfer edilmesi prensibine dayanır. Protein spesifik olarak işaretli antikor veya antijenle reaksiyona girmektedir. Şekil 2.9’da gösterilmiştir. Bu yöntem ile spesifik bir proteinin moleküler ağırlığı bilgisi ve işlenmiş ürünlerden izoformların ayırımı mümkündür. Protein uygun bir membrana transfer edildikten sonra görüntüleme için boyanabilir, N ucundan sekanslanarak direkt olarak tanımlanabilir, kütle spektrofotometri ya da immüntespit yapılabilir [81,82].
23
24 3. GEREÇ VE YÖNTEM
3.1 Gereç 3.1.1 Cihazlar
Tez çalışmasında kullanılan cihazlar Tablo 3.1’de yer almaktadır. Tablo 3.1 : Kullanılan cihazların listesi.
Cihaz Adı Marka Kullanım Amacı
Otomotik Pipetler Thermo,
Eppendorf Tüm moleküler çalışmalarda kullanılmıştır. Distile su cihazı Sartorius Stedim Tüm moleküler çalışmalarda kullanılmıştır.
Santrifüj Nüve, NF 400
Yüksek hızda (maksimum: 14000 rpm) ayrıştırma gerektiren tüm çalışmalarda kullanılmıştır (Hettich). Düşük hızda ve büyük hacimde ayrıştırma gerektiren tüm çalışmalarda kullanılmıştır (Nüve).
Vortex Stuart Küçük hacimdeki sıvı karışımlarını homojen hale getirmede kullanılmıştır.
Buzdolabı (+4) Uğur Örnekler, belirli kit çözeltileri, tampon ve stok çözeltilerin saklanmasında kullanılmıştır. Derin dondurucu
(-20˚C, -80˚C) Uğur, Haier
Örneklerin uzun süreli saklanmasında kullanılmıştır.
pH metre Mettler Toledo Tampon çözeltilerin pH ayarlamasında kullanılmıştır.
Liyofilizatör Christ Ekstrelerin kalan su içeriğinden arındırılması amacıyla kullanılmıştır.
Evoporatör Boeco Ekstrelerdeki çözücülerin uçurulması amacıyla kullanılmıştır.
Hassas Terazi GR 200 Numunelerin tartılmasında kullanılmıştır.
Balon Joje Hanna
Instruments
Standart çözeltilerin hazırlanmasında kullanılmıştır.
Membran Filtre Fılmtec HPLC analizine zeytin yaprağı ekstresini hazır hale getirmede kullanıldı. Çeker Ocak Stuart Kalan çözücüden ekstreyi uzaklaştırmada
kullanılmıştır.
25
Tablo 3.1 (devam) : Kullanılan cihazların listesi.
Cihaz Adı Marka Kullanım Amacı
Florometrik
Kültür Flaskları Jet Biofil
Hücre içi ROS tayininde hücrelerin ekilmesinde kullanılmıştır. Vilber Lourmat Görüntüleme cihazı Collégien, Fransa
Protein ekspresyon analizinde görüntülerdeki bantların piksel yoğunluğunu tespit etmede kullanılmıştır.
Spektrofotometre Thermo Western Blot analizinde kullanılmıştır. Floresan
Mikroskop Cnoec
Hücre canlılık ve apoptoz tayininde hücre sayımında kullanılmıştır.
3.1.2 Kullanılan kimyasallar
Tez çalışmasında kullanılan kimyasallar Tablo 3.2’de yer almaktadır. Tablo 3.2 : Kullanılan kimyasalların listesi. Kimyasal Adı Marka Kullanım Amacı
PBS Sigma
Aldrich
Tüm çalışmalarda kullanılan fizyolojik tampon olarak kullanılmıştır.
TEMED Sigma
Aldrich
SDS-PAGE analizinde jellerin
hazırlanmasında ve proteinleri denatüre etmede kullanılmıştır.
SDS Sigma
Aldrich
SDS-PAGE jellerinin hazırlanmasında kullanılmıştır
APS Sigma
Aldrich
SDS-PAGE jellerinin hazırlanmasında kullanılmıştır
Coomassie blue boyası R250
Sigma Aldrich
SDS-PAGE jellerinin boyanmasında ve protein ölçümlerinde kullanılmıştır Hidroklorik asit Sigma
Aldrich
Tampon çözeltilerin pH ayarlamalarında kullanılmıştır.
Sodyum hidroksit Sigma Aldrich
Tampon çözeltilerin pH ayarlamalarında kullanılmıştır.
Glut 2 Antikoru Cell
Signaling Western Blot yönteminde kullanılmıştır. Glut 4 Antikoru Cell
Signaling Western Blot yönteminde kullanılmıştır. Tirozin Kinaz
Antikoru Santa Cruz Western Blot yönteminde kullanılmıştır. İnsülin Reseptör
Protein -1Antikoru Santa Cruz Western Blot yönteminde kullanılmıştır. Sekonder Antikor Cell



![Şekil 2.6 : Diyabette oksidatif stresin artış metabolizması [46].](https://thumb-eu.123doks.com/thumbv2/9libnet/3571079.19519/32.892.163.789.136.565/şekil-diyabette-oksidatif-stresin-artış-metabolizması.webp)