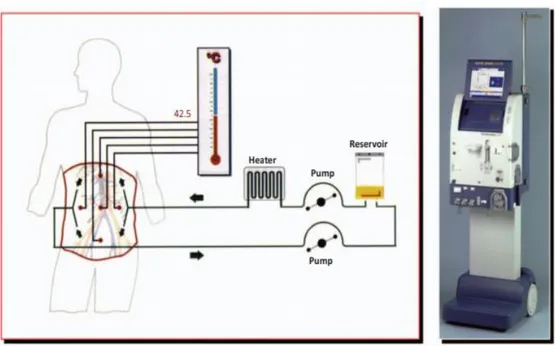
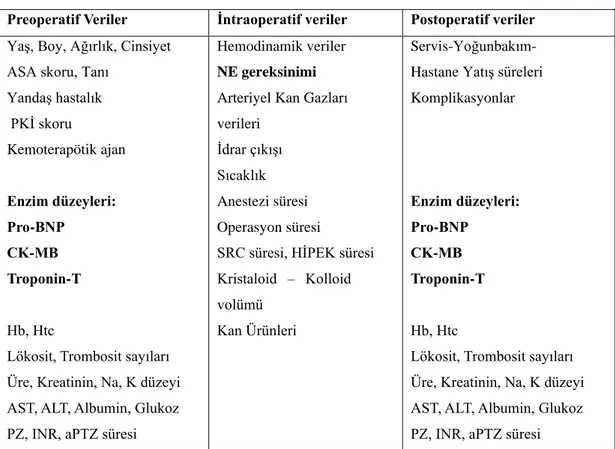
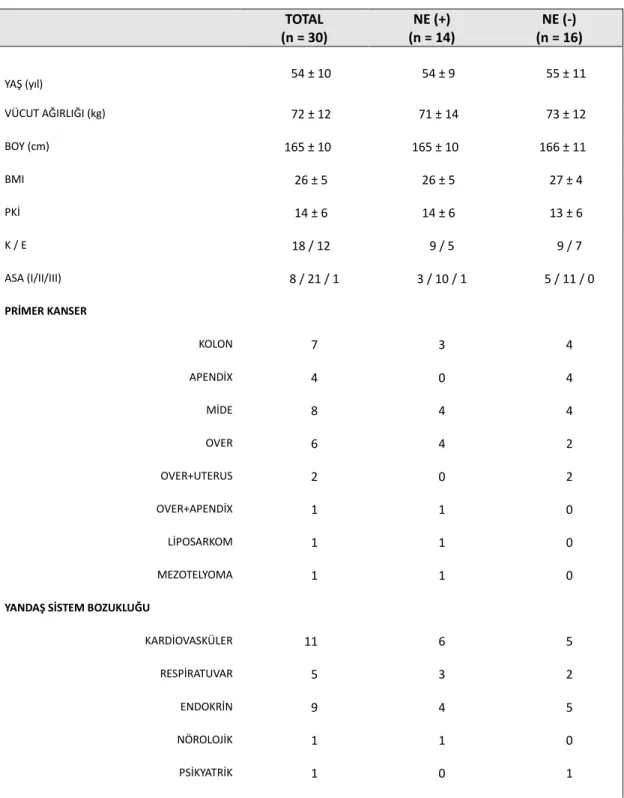
Sitoredüktif cerrahi ve hipertermik intraperitoneal kemoterapi geçiren hastaların kardiyovasküler durumlarının PRO-BNP, CK-MB ve Troponin-T ile değerlendirilmesi
Tam metin
Şekil

Outline
Benzer Belgeler
Sonuç: Çalışmamıza göre akut myokart infarktüsü tanısı konan hasta serumlarında troponin I’nın özgüllüğü troponin T’den daha yüksek, troponin T’nin duyarlılığının
Sonuç olarak; minor myokardiyal hasarın en iyi göstergelerinden biri olan troponin-I'in preeklamptik gebelerde yüksek saptanması, preeklamptik gebeliklerde kardiyak
Bu yazıda; overin seröz karsinomuna bağlı peritoneal karsinomatozisde, sitoreduktif cerrahi ve hipertermik intraperitoneal kemoterapi sonrası nadir görülen cilt
Bu nedenle, akut miyokard infarktüsündeki kompleman aktivasyonunun, infarkt alan›n›n büyüklü¤ünü göstermede ve do¤rudan tedavi hedeflerini araflt›rmada, CK- MB düzeyi
Olgular›m›zda CK ve CK-MB düzeyindeki yük- sekli¤in klinik ve EKG ile uyumlu olmamas›, CK-MB aktivite ölçümünün total CK aktivitesini aflacak düzey- de yüksek
sonuçlarındaki küçük değişikl ikler metod ve hasta populasyonunu farklılığı yla ilgili olabilir. Bununla birlikte, bu serilerdeki ortak nokta -çalışmamızdaki
Bu çalışmanın amacı, akut miyokard infarktüsü ge- çiren hastalarda Tn-T'nin salınma eğrisini belirlemek ve klasik olarak kullanılan CK-MB ile karşılaş..
Sonuç olarak, gerek SAP gerekse UAP olarak kabul edilen hastaların önemli bir bölümünde, rutin klinik ve laboratuar yöntemlerle saptanamayan mikroin- farktüslerin