T.C.
DİCLE ÜNİVERSİTESİ TIP FAKÜLTESİ Nöroloji Anabilim Dalı
SEREBROVASKÜLER HASTALIKLARDA S-100 PROTEİN ,
NÖRON SPESİFİK ENOLAZ DÜZEYLERİNİN NÖROLOJİK DEFİSİT
VE PROGNOZLA İLİŞKİSİ
(UZMANLIK TEZİ)
TEZ YÖNETİCİSİ
Prof. Dr. NEBAHAT TAŞDEMİR
Dr. ALİ AKÇİÇEK
ÖNSÖZ
Nöroloji uzmanlık eğitimim boyunca mesleki bilgi, beceri ve
deneyimleriyle bana önderlik ederek bilimsel ufkumu genişleten tez
konusunun seçiminde ve çalışmaların yürütülmesinde yardımlarını
esirgemeyen sayın Prof. Dr. Nebahat TAŞDEMİR’e Nöroloji uzmanlık
eğitimimde büyük emekleri geçen Sayın Doç. Dr. M. Ufuk ALUÇLU’ya
ve tezimin hazırlanmasında katkı, bilgi ve tecrübelerinden yararlandığım
Sayın Yrd. Doç. Dr. Yusuf TAMAM’a
ve
Tüm çalışma arkadaşlarıma
TEŞEKKÜR EDERİM
DR. ALİ AKÇİÇEK
KISALTMALAR
ACA: A. Cerebri Anterior ASA: Anterior Spinal Arter
AICA: A. Cerebellaris Anterior İnferior AVM: Arteriyovenöz Molformasyon AF: Atrial Fibrilasyon
BA: Baziler Arter
BDH: Beyin Damar Hastalıkları BT: Bilgisayarlı Tomografi
BBT: Beyin Bilgisayarlı Tomografi CAD: Koroner arter darlığı
CBF: Beyin Kan Akımı
CVR: Serebrovasküler Direnç CPP: Serebral Perfüzyon Basıncı CCA: A. Carotis Communis CI: Cerebral İnfarktüs CRP: C-reaktif Protein GİA: Geçici İskemik Atak ICA: A. Carotis İnterna İKH: İntakraniyal Hemoraji KAH: Koroner Arter Hastalığı KKY: Konjestif Kalp Yetmezliği KVH: Kardiovasküler Hastalık LACI: Lakunar İnfarktüs
LVH: Sol Ventrikül Hipertrofisi Mİ: Miyokard İnfarktusu
MRG: Manyetik Rezonans Görüntüleme
NINDS: National Institute of Neurological Disorders and Stroke NIHS: National Institutes of Health Stroke Scalae
NNE: Non-Nöronal Enolaz NSE: Nöron Spesifik Enolaz NVAF: Nonvalvüler Atrial Fibrilas
OCSP: Oxfordshire Toplumda İnme Projesi Sınıflandırması NVAF: Nonvalvüler Atrial Fibrilasyon
PACI: Parsiyel anterior sirkülasyon infarktı PET: Pozitron Emisyon Tomografisi PCA: A. Cerebri Posterior
PICA: A. Cerebellaris Posterior İnferior POCS: Posterior Sirkülasyon Infarktı SAK: Subaraknoid kanama
SKA: Serebral kan akımı
SOR: serbest oksijen radikalleri SVH: Serebrovasküler Hastalık
TACI: Total Anterior Sirkülasyon İnfarktı TNF alfa: Tümör Nekroz Faktör alfa
TOAST : Trial of Org 10172 in Acute Stroke Tr WHO: Dünya Sağlık Örgütü
İÇİNDEKİLER ÖNSÖZ KISALTMALAR ŞEKİLLER VE GRAFİKLER TABLOLAR 1. GİRİŞ VE AMAÇ 1 2. GENEL BİLGİLER 3
2.1 Serebrovasküler Hastalıkların Tanımı 3
2.2 Serebrovasküler Hastalıkların Epidemiyolojisi 4
2.3 Serebrovasküler Hastalıkların Vasküler Anatomisi 5
2.4 Serebrovasküler Hastalıkların Fizyolojisi 8
2.5 Serebrovasküler Hastalıkların Patojenez ve Sınıflandırması 10
2.6 Strokun Risk Faktörleri 17
2.7 Geçici İskemik Atak (GİA) 23
2.8 Serebral İnfarkt 23
2.9 İntraserebral kanama 24
2.10 Strokun Sonuçları, Etkileri, Gidişi 33
2.11. İnme skalaları 35
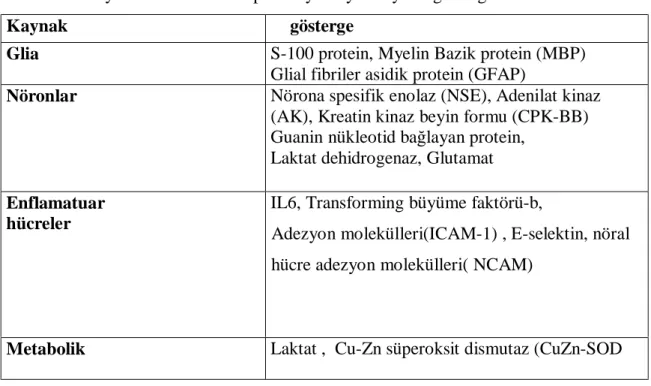
2.12 Nörolojik hasarlanmanın biyokimyasal göstergeleri 39
2.13. Protein S-100 40
2.14. Nöron Spesifik Enolaz (NSE) 43
2.15. İnterlökin-6 46
3. MATERYAL METOD 48
3.1 Çalışma Grubu 48
3.2. İnme Fenotipinin Belirlenmesi 48
3.3 Yapılan İncelemeler 49 3.4 İstatistiksel değerlendirme 50 4. BULGULAR 51 5. TARTIŞMA 64 6. ÖZET 71 7. SUMMARY 73 8. KAYNAKLAR 75
ŞEKİLLER VE GRAFİKLER
NO Şekiller sayfa
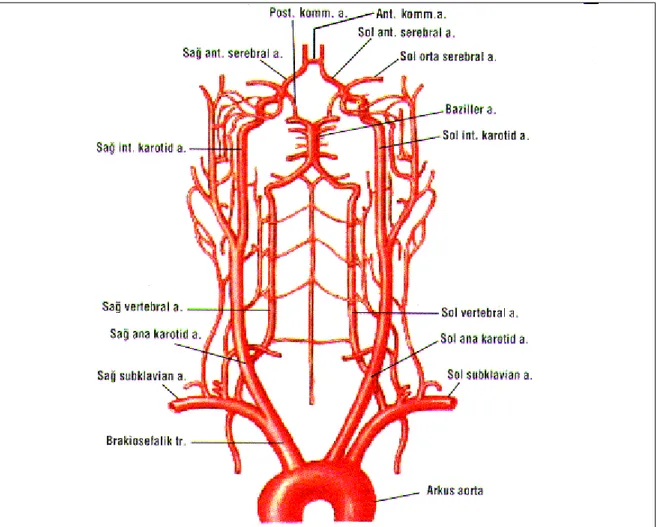
Şekil 1 Karotid ve vertebral arterlerin boyundaki seyri 7
Şekil 2 Beyinin alt yüzünün arterleri ve Willis halkası 8
NO Grafikler
Grafik 1 Hastalar ile kontrol grubunun demografik verileri. 53
Grafik 2 Hastalar ile kontrol grubunun S100 düzeyleri. 53
Grafik 3 Hastalar ile kontrol grubunun NSE düzeyleri. 53
Grafik 4 Hastalar ve kontrol grubunun IL-6 düzeyleri. 53
Grafik 5 İskemik inme hastalarında NİH skalası. 54
Grafik 6 iskemik inmede eks ve taburcu olan hastalarda S-100 düzeyleri. 55
Grafik 7 iskemik inmede eks ve taburcu olan hastalarda NSE düzeyleri. 55
Grafik 8 İskemik inmede eks ve taburcu olanlarda IL-6 düzeyleri. 56
Grafik 9 Oxfordshire sınıflandırmasına göre S100 ve NSE düzeyleri 56
Grafik 10 İskemik inmede NİH skalasına göre S100 ve NSE düzeyleri. 57
Grafik 11 Hemorajik inmede NİH skalasına göre S-100 ve NSE düzeyleri. 58
Grafik 12 Hemorajik inme hastalarında NİH skalası. 59
Grafik 13 Hemorajik inmede eks ve taburcu olanlarda S-100 ve NSE düzeyleri. 60
Grafik 14 Hemorajik inmede eks ve taburcu olanların IL-6 düzeyleri. 61
Grafik 15 Supratentoryal ve infratentoryal tüm günlerde S100 ve NSE düzeyleri. 62
TABLOLAR
NO sayfa
Tablo 1 National Institute of Neurological Disorders and Stroke- NINDS. 3,4
Tablo 2 Serebral kan akımını etkileyen faktörler. 9
Tablo 3 İskemik inmede inflamasyonun etki mekanizmaları. 13
Tablo 4 İskemik inmede TOAST sınıflandırması. 14
Tablo 5 İskemik inmenin diğer etyolojileri. 16
Tablo 6 İnme risk faktörlerinin sınıflandırılması. 18
Tablo 7 Serebral İnfarkt Sendromları. 24
Tablo 8 Primer İntraserebral Kanamada Lokalizasyon. 33
Tablo 9 NIH inme skalası. 36
Tablo 10 İnmeli hastalarda inme skalaları ve klinik özelliklerine göre prognoz. 37
Tablo 11 Barthel İndeksı. 38
Tablo 12 Beyin hasarlanmasının potansiyel biyokimyasal göstergeleri. 39 Tablo 13 NSE’nin değişik insan ve sıçan dokularındaki miktarları. 44
Tablo 14 NSE ve NNE’nin beyin dokularında dağılımı. 45
Tablo 15 Hastalar ile kontrol grubunun sosyodemografik verileri ve inme risk faktörleri. 52 Tablo 16 Hastalar ile kontrol grubunun S-100 ve NSE düzeyleri. 52
Tablo 17 İskemik ve kontrol grubunda İL-6 düzeyleri. 53
Tablo 18 İskemik inme hastalarında eks ve taburcu olan hastaların NİH skalasına göre değerlendirilmesi .
54 Tablo 19 İskemik inme hastalarının S-100 protein ve NSE düzeyleri. 55
Tablo 20 İskemik inmede IL-6 düzeyleri. 55
Tablo 21 Oxfordshire sınıflandırmasına göre S100 ve NSE düzeyleri. 56 Tablo 22 İskemik inmede NİH inme skalasına göre S100 ve NSE düzeyleri . 57 Tablo 23 Hemorajik inmede NİH İnme skalasına göre S100 ve NSE düzeyleri. 58 Tablo 24 Hemorajik inme hastalarında eks olan ve taburcu olan hastaların NİH skalasına
göre değerlendirilmesi.
59 Tablo 25 Taburcu olan ve eks olan hemorajik inme hastalarının S100 protein ve
NSE düzeylerinin karşlaştırılması.
60 Tablo 26 Hemorajik inmede taburcu ve eks olanlarda İL-6 düzeyleri. 60 Tablo 27 Supratentoryal ve infratentoryal hemorajik inmeli hastalarda NSE ve
S100 protein düzeyleri.
61
Tablo 28 1. ve 3. ayda barthel indeksi. 62
1. GİRİŞ VE AMAÇ
İnme, beynin bir bölgesinin, iskemi veya kanama sonucu kalıcı veya geçici olarak etkilenmesi ve/veya beyni ilgilendiren bir yada daha fazla kan damarlarının primer patolojisi olarak tanımlanır. İnme tüm dünyada en önemli mortalite ve morbidite sebeplerinden biridir. Koroner kalp hastalığı ve tüm kanserlerin ardından üçüncü sıklıkta gelen ölüm nedenidir. Tüm inmeler içinde iskemik inme % 70-80, İntra-Serebral Kanama % 7-15 ve Subaraknoid Kanama ise % 2-8 oranında görülür. Son yıllarda serebrovasküler hastalıklarda ölüm oranı %50 kadar azalma göstermiştir. Bunun en önemli sebebi, inmenin tedavisindeki gelişmeler, risk faktörlerinin belirlenmesi ve bunların oluşturduğu komplikasyonlarla mücadele esasına dayanmaktadır.
Bilgisayarlı Beyin Tomografisi ve Magnetik Rezonans Görüntüleme gibi modern nöroradyolojik görüntüleme teknikleri iskemik ve hemorajik inme yerini ve hacmini belirlemede yardımcı olur. Ancak tekrarlanan nöroradyolojik görüntülemeler pratik değildir. Beyin hasarlarında S100 protein, Nöron spesifik enolaz, interlökin-6, myelin bazik protein, glial fibrik asit proteinin kan seviyesini ölçüm tekniği bize daha az riskle daha sık deneme imkanı ve beyin hasarlanmasının ciddiyetini göstermede, hızlı tanı konmasına ve erken tedaviye olanak sağlamaktadır.
100 asidik bağlayıcı bir proteindir.100 Protein iki alt birimden oluşmuştur (αveβ). S-100 ββ yüksek konsantrasyonlarda astrosit ve schwan hücrelerinde bulunur. Nöron Spesifik Enolaz ise 2- fosfogliseratı fosfoenol pruvata çeviren glikolitik bir enzimdir. Üç immünolojik subünitesi bulunur. (α,β,γ ) Dimerik αα formu glial hücreler için spesifiktir. İnterlökin-6 farklı dokuların büyümesi ve farklılaşmasını sağlayan,çok çeşitli fonksiyonları bulunan bir sitokindir.
Son dönemde yapılan çalışmalarda
Serumda interlökin-6, Nöron spesifik enolaz ve S-100 proteinlerinin ölçümü: 1-Hasara uğrayan dokuların daha çok glial ya da nöronal mı olduğunun tahmininde 2-Hastalık prognozunun saptanmasında
3-Hasar büyüklüğü ve uygulanılacak tedavi stratejisinin belirlenmesinde 4-Hastalıkların ayırıcı tanısında
5-Tedavi etkinliğinin değerlendirilmesinde faydalı oldugu belirtilmiştir. Bu çalışmada;
Hemorajik ve iskemik inme geçiren hastalarda akut dönemde (1.,2., 3. ve 10. günlerde) seri olarak bakılan serum Nöron spesifik enolaz, S100 protein,interlökin-6 ölçümü;
a- National Institutes of Health Stroke skalası ve Barthel skorları kullanılarak prognozla olan ilişkisinin tespiti ve mortalite üzerine etkisini araştırmak,
b) Lezyon büyüklüğü ve inme tipi ile ilişkisini araştırmak,
2. GENEL BİLGİLER
2. 1. Serebrovasküler Hastalıkların Tanımı
Serebral inme dünya ölüm istatistiklerine göre ölüm sebepleri arasında kalp hastalıkları ve kanserden sonra üçüncü morbidite nedeni olarak yer almaktadır. Nörolojik hastalıklar içinde en sık görülen hastalık grubunu oluşturur (1). Bilindiği gibi Dünya sağlık organizasyonu (WHO) inmeyi “hızla gelişen serebral işlevlerin fokal veya global bozukluğuna bağlı klinik bulgular olup, 24 saat veya daha uzun sürme veya ölüm gelişmesi” olarak tanımlamaktadır (2). Amerikan Nörolojik Bozukluklar ve İnme Ulusal Enstitüsü (National Institute of Neurological Disorders and Stroke (NINDS)) serebrovasküler hastalığı şu şekilde tanımlamıştır; Bir beyin bölgesinin, iskemi veya kanama sonucu kalıcı veya geçici olarak etkilenmesi ve /veya beyni ilgilendiren bir ya da daha fazla kan damarının primer patolojisidir (3).
Tablo-1: Amerikan Nörolojik Bozukluklar ve İnme Ulusal Enstitüsü (National Institute of Neurological Disorders and Stroke- NINDS) tarafından yapılan Serebrovasküler Hastalıkların Sınıflaması .1990
A- Asemptomatik
B- Fokal beyin disfonksiyonu 1- Geçici iskemik atak
a. Karotid sistemde
b. Vertebrobaziler sistemde c. Her ikisinde
d. Lokalize edilemeyen e. Olası geçici iskemik atak 2- İnme a. Geçici profil 1) ilerleyen 2) Daha da kötüleşen 3) Stabil strok b. İnme tipi 1) Beyin hemorajisi 2) Subaraknoid hemoraji
3) Arteriovenöz malformasyona bağlı intrakraniyal hemoraji 4) Beyin infarktı
(1) Trombotik (2) Embolik (3) Hemodinamik b) Klinik sınıflama (1) Aterotrombotik (2) Kardiyoembolik (3) Laküner (4) Diğerleri
c) Semptom ve belirtilerin dağılımı (1) Internal karotid arter (2) Medial serebral arter (3) Anterior serebral arter (4) Vertebrobaziler sistem (a) Vertebral arter (b) Baziler arter
(c) Posterior serebral arter C- Vasküler Demans
D-Hipertansif Ansefalopati
2. 2. Serebrovasküler Hastalıkların Epidemiyolojisi
Türkiye’de ülke genelini kapsayan inmeyle ilgili kapsamlı bir çalışma yoktur. Çok merkezli Türk strok çalışması sonuçlarına göre (1996) Türkiye’de nüfusa göre oranlandığında her yıl yeni 125.000 inme olgusu görüldüğü tahmin edilmektedir. Çok merkezli Türk strok çalışmasında olguların %71,2’si iskemik %28,8’i hemorajik bulunmuştur. Batı ülkelerinde iskemik inme %85, hemorajik inme %15 bulunmuştur (4). İnmenin epidemiyolojisini araştırırken coğrafya ve toplumların kendine ait özellikleri (yaş, cinsiyet, ırk gibi) önem kazanmaktadır. Özellikle risk faktörlerinin giderilmesi, koruyucu tedavi yönünden büyük önem taşımaktadır. Özdemir ve arkadaşlarının (2000) Türkiye’de inmenin risk faktörleri yönünden yaptıkları çalışma sonuçlarına göre inmeli olgularda en önde gelen risk faktörünün Hipertansiyon (HT) olduğu (infarktlarda %62.7, hemorajilerde %79.2) dikkati çekmektedir. Ülkemizde hemorajik tip inmenin batı ülkelerine göre yüksek bulunması HT ile yeterli mücadele yapılamaması ile ilişkili olabilir (5).
2.2.1. İnme İnsidansı
İnme olaylarının epidemiyolojisini incelemede en geçerli verilerden bir tanesi de insidans verileridir. Kristensen B. ve ark. insidans çalışmasında ideal kriterleri şöyle tanımlamıştı; İnmenin tanımı iyi yapılmalı, geçiçi inme atağı(GİA) dışlanmalı,
populasyonda sınırlama yapılmaksızın incelenmeli, inme kayıtları iyi tutulmalı , ilk atak olmalı, yaşlara göre insidans incelenmeli (6).
Nencini ve arkadaşları (7). 15-45 yaş arası inme insidansını 10/100,000 kişi olarak bildirmişlerdir. 45 yaşından önce inme insidansını tahmin etmek zordur. Çünkü inmelerin ancak %3-5’ini oluşturmaktadır (8).
15 yaştan önce perinatal dönem dışındaki inme İnsidansı 2,7/100000 olarak tahmin edilmektedir (9). 55-64 yaşlarda insidans 170-360/100.000; 65-74 arası 490-890/100000; 75 yaşından sonra 1350-1790/100000 kişidir (4,10,11). Kadınlarda 55-64 yaş arası inme insidansı erkeklere göre 2-3 kat daha azdır (9). 85 yaşa doğru bu fark azalmaktadır. Kış aylarında inmenin arttığı görülmektedir (12).
2.2.2. İnme Prevalansı
İnme prevalansı inmesi olan olguların insidansına ve yaşayabilen hastalara bağlıdır. Yaşın ilerlemesi ile artar. Örneğin inmeli hastaların %75'i 65 yaş üzerindedir. Batı ülkelerinde inme prevalansı 8-20/1000’dir (13,14). Yapılan epidemiyolojik çalışmalar, inme sonrası yaşam oranının da yükseldiğini göstermektedir (9,10). Amerika Birleşik Devletleri'nde(A.B.D) yapılan çalışmada inmeden bir sene sonraki yaşam süresi 1970-73'te %49 iken, 1979-80 arası %62'ye çıkmıştır (14). İntraserebral kanama (İSK) sonrası yaşam oranı, iskemik inmelere göre daha belirgin artmıştır. Bunun nedeni olasılıkla, tedavi yöntemlerinin ve bakım koşullarının gelişmesidir (12). Burada önemli olan, sekonder komplikasyonların önlenmesi ve iyi bakımın sağlanmasıdır (15).
ABD’de yapılmış çalışmalardan elde edilen bilgilere göre bu ülkede inmeden sonra hayatta kalan hasta sayısı 4 milyondur, ayrıca her yıl için 600.000 rekürren ya da yeni inme oluşmaktadır (17,16). 65 yaş üzerinde gelişmiş ülkelerde tüm ölümlerin %10 kadarı inmeyle ilgili olabilir. ABD.’de her yıl için inme mortalitesi 50-100/100.000'dir, ancak son dönemlerde inme mortalitesinde azalma bildirilmektedir (16,18).
2.3. Serebrovasküler Hastalıkların Vasküler Anatomisi
Beyin; iki serebral hemisferden ve derindeki büyük yapıları (bazal ganglion ve talamusu, kortekse çıkan ve korteksten inen beyaz madde yollar ve sıvı ile dolu
ventriküler sistemi) saran serebral korteksten oluşur. Serebral korteks frontal, pariyetal, temporal ve oksipital loplara ayrılır. Serebrumun orta beyin, pons ve medullayı içeren derin yapıları beyin köküne bağlanır.
Serebral hemisferler kanını internal karotis arterden alır. Sağ arteria karotis komminis brakiyosefalik gövdeden köken alır ve sol arteria karotis komminis arkus aortadan köken alır. Her iki arteria karotis komminis boyunda mandibula açısının hemen altında ikiye ayrılır ve beyine giden arteria karotis interna ile yüze giden arteria karotis eksternayı oluşturur (Şekil 1). İnternal karotis arter petroz kemik ve kavernöz sinüsü geçerek oftalmik arteri oluşturup dallara ayrılarak göze doğru yol alır. Anterior korodial arter dalı orta serebral ve anterior serebral arterlere ayrıldığı yerden hemen önce internal karotis arterden köken alır. Anterior koroidal arter mediyal temporal loba kan sağlar. Orta serebral arter frontal, pariyetal ve temporal lopları içeren serebral hemisferlerin lateral yüzeyinin dolaşımını sağlar. Orta serebral arterin horizontal bölümünden gelen küçük dallar -lentikülostriat arterler - bazal ganglionun derindeki yapılarını ve internal kapsülle kan sağlar; bu yapı korteks ve alttaki yapılar arasındaki beyaz maddeden oluşan ana bağlantı yoludur. Anterior serebral arter frontal, pariyetal ve temporal lopları içeren serebral hemisferlerin mediyal yüzeyine kan sağlar.
Beyin kökünün kanını iki vertebral arter sağlar (Şekil 1); bu arterler her iki tarafta da subklavyen arterlerden köken alır ve birleşerek baziller arteri oluştururlar. Posterior inferior serebellar arter proksimal intrakranyal vertebral arterden köken alarak inferior serebellum ve lateral medullanın kan dolaşımını sağlar. Anterior serebellar arter ve süperior serebellar arter baziller arterden köken alır ve baziller arterden çıkan küçük arterlerle beyin kökü ve serebellumun geri kalan bölümüne kan sağlar. Baziller arterin uç dalları posterior serebral arterleri oluşturur ve bu arterler talamus ile birlikte pariyetal ve temporal lopların posterior bölümlerine ve oksipital loba kan sağlar.
Majör bir damar tıkandığı zaman kollateral anastomozlardan oluşan yoğun bir ağ beyinin primer kan desteğinden yoksun alanlarını besler. Ana kollateral kanal beyinin tabanındaki Willis halkasından oluşur (Şekil 2). İki karotis arter anterior komminis arterler boyunca birbirleri ile bağlantılar oluşturur. Posterior serebral arterle birlikte iki karotis arter posterior komminis arterin de katılımıyla serebral ve vertebrobaziller dolaşımlar arasında kollateral bir yol oluşturur. İnternal karotis arter tıkandığı zaman eksternal karotis arter ve İnternal karotis arter arasında kollateral kanallarda oluşabilir. Eksternal karotis arterin supraorbital dalından gelen kan internal karotis arteri doldurmak için oftalmik arter boyunca geriye doğru akabilir ve eksternal karotis arterin meningeal dalları serebral arterlerin distal dalları ile anastomozlar yapabilir. Beyin dolaşımında
hemisferlerin orta bölümündeki orta ve anterior serebral arter alanlarının birleşim yerinde serebral arterlerin distal dallarının ortak akım alanlarında ve posterior pariyetal lopta orta ve posterior serebral arterlerin birleşim alanında boşalma havzaları oluşur. Perfüzyon basıncındaki ani düşüşlerde, bu alanlar iskemiye daha açık alanlardır (19).
Şekil 2. Beyinin alt yüzünün arterleri ve Willis halkası
2.4. Serebrovasküler Hastalıkların Fizyolojisi
Metabolik olarak vücuttaki en aktif organlardan biri olan beynin bu aktiviteyi sağlayabilmek için zengin bir kan akımına gereksinimi vardır. Normalde total kan volümünün %20’sini, glukozun %17’sini kullanan beyin akciğerler tarafından absorbe edilen oksijeninde %20 kadarını kullanmaktadır. Beyin total olarak dakikada 750-800 ml kan kullanıp 46 ml kadar oksijen tüketimi yapmaktadır. Serebral kan akımı (SKA) 100 gr beyin dokusu için ifade edilir ve normalde ortalama 50ml/dak‘dır. Gri cevherde SKA ortalama 70-80ml/100gr/dak iken beyaz cevherde 30ml/100gr/dak’dır (20). Her iki karotis arter dakikada 350 cc, vertebrobaziler sistem ise 150-200cc kanı beyine taşır. Birkaç dakikalık işlev bozukluğu sonucunda bile oksijen ve glikoz azalıp kritik seviyelere inebilir. Beyin dokusu bu maddeleri depolayamadığından ve metabolizması çok yüksek olduğundan serebral dolaşımda 6-10 saniyelik kritik düzeyde bir duraklama geriye dönüşümlü nöronal metabolik bozukluğa ve bilinç yitimine neden olur. Serebral dolaşımda 30 saniyelik bir kesilme beyin metabolizmasında değişikliğe yol açarken, 5 dakika sonra irreversibl beyin dokusu yıkımı ve serebral enfarktla sonlanabilecek anoksi
başlar (21,22). Serebral kan akımını etkileyen faktörler Tablo-2 ‘de gösterilmiştir (23).
Tablo 2: Serebral kan akımını etkileyen faktörler. 1- Serebral metabolizma hızı
2-Pa O2 3- Pa CO2 4-Viskozite 5- Ateş
6- İntrakranial basınçta değişme 7- Barbitüratlar
8- Vazoaktif ilaçlar
9- Sistemik arteriyel kan basıncı
Arterioller, oksijen ve karbondioksit kısmi basınçlarının değişikliklerine aşırı duyarlıdır. PaO2' nin ileri düzeyde düştüğünde ve PaCO2 arttığında arterioller genişler ve
serebral kan akımı artar. PaCO2 azaldığında ve ekstrasellüler Ph arttığında arterioller
kasılır ve kan akımı azalır. PaO2 değişiklikleri karşıt etkilidir. Fokal serebral aktivite,
ekstremite hareketi oluştuğu zaman meydana gelmekte ve uygun bölgede metabolizma hızlanmaktadır, buna uygun olarak lokal kan akımı da artmaktadır. Serebrovasküler patolojilerde bu kompansatuvar mekanizmalar ortadan kalkar.
Kemoregülatuar faktörlerin dışında ateş, intrakranial basınç değişiklikleri, anestezik ajanlar ve vazoaktif ilaçlar beyin kan akımını etkileyebilmektedir. Vücut ısısındaki her 1 derecelik düşüş serebral metabolizma hızında %6-7' lik bir azalma ortaya çıkartmaktadır. Hipotermi hem beynin elektrofizyolojik fonksiyonları için, hem de hücrelerin yapısal olarak bütünlüğünü devam ettirebilmeleri için gerekli olan enerji ihtiyacını azaltmaktadır. Vücut ısısının yaklaşık 20 dereceye yaklaştığı hipotermide EEG'de tam bir baskılanma görülmektedir. Hiperterminin serebral fizyoloji üzerine etkisi hipoterminin tam tersidir. Vücut ısısının 42 dereceye kadar olan artmalarında, hem serebral metabolizma, hem de serebral kan akımını arttırmaktadır. Hiperterminin toksik etkisi için eşik değer kabul edilir. 42 dereceden sonra enzimlerin fonksiyonlarında bozulma ve protein yıkımı görülebilmektedir. İntrakranial basınç, serebral perfüzyon basıncını etkileyerek serebral kan akımında değişikliğe neden olur. İntrakranial basıncın yükselmesi serebral perfüzyon basıncını düşürmektedir. Barbitüratlarda, serebral metabolizma ve nöronal aktiviteyi azaltarak beynin enerji gereksinimini düşürürler ve sonra da serebral kan akımını azaltırlar (23).
2.5. Serebrovasküler Hastalıkların Patojenez ve Sınıflandırması 2.5.1. Patojenez
Nöronal disfonksiyon serebral kan akımı 22ml/100gr/dak düzeylerinde oluşmaya başlar. 12ml/100gr/dak’nın altına düşmesi durumunda ise nöronal ölüm meydana gelir. Beyin enerji depolama kapasitesi düşük olan bir organdır. Komplet bir iskemide depolanmış enerji hücreyi ancak 3 dakikada koruyabilir. İskemik inmelerin çoğunda komplet iskemi alanı küçük olup çevresindeki inkomplet iskemi alanı ise büyüktür. Bu alanlarda kollateral akım sayesinde hücrelerde morfolojik değişiklikler oluşmamıştır. Ancak irreversibl harabiyet açısından riskli bir alandır. Bu alana penumbra denir. Penumbra belli bir terapotik zaman aralığında uygun tedavi yaklaşımları ile kurtarılabilir bir beyin dokusudur. Penumbra alanı dinamiktir. Bu alanda iskeminin şiddet ve süresine bağlı olarak dokuyu infarkta götüren çok kompleks nöronal, glial ve vasküler olaylar rol almaktadır. Protein sentezi süprese olmuş ancak ATP azalmamıştır. Elektrofizyolojik olarakta aktif bir alandır.
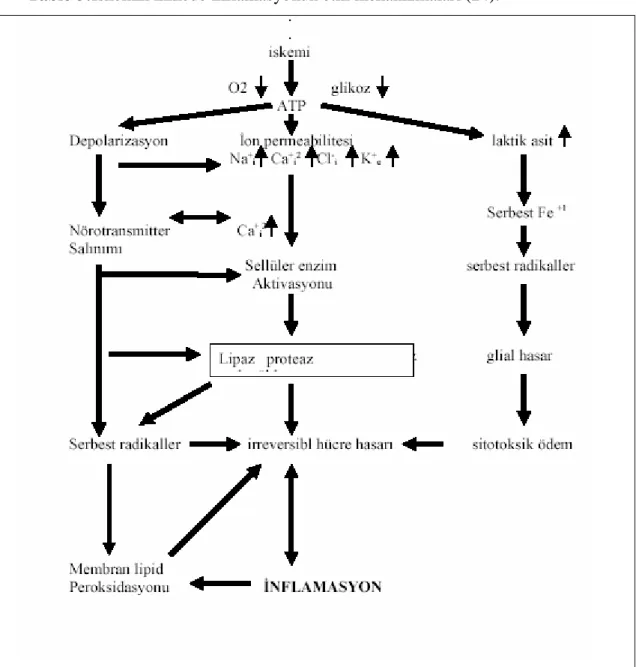
İskemik dokuda biyokimyasal kaskadın birçok kademeleri vardır. Yapılan çalışmalar nöron ölümüne yol açan başlıca 4 fazın oluştuğunu götermektedir.
1- Eksitotoksisite (dakikalar içinde).
2- Perinfarkt depolarizasyon (dakikalar, saatler içinde). 3- İnflamasyon (saatler günler içinde).
4- Apopitoz, nekroz (günler içinde).
Bu fazlarda rol oynayan majör mediyatörler intrasellüler sitozolik kalsiyumun kontrolsüz yükselişi, serbest radikallerin artışı ve asidozdur ( tablo 3).
Glutamat Eksitotoksisitesi:
Beyinde iskemi ve birçok nörödejeneratif hastalıkta glutamat reseptörlerinin aşırı aktivasyonu nöronal harabiyete ve nöron ölümüne yol açar. Bu duruma glutamat eksitotoksisitesi denir. İntrasellüler konsantrasyonu ekstrasellüler konsantrasyonundan daha çok olan glutamat, astrosit ve nöronlar içine sodyuma bağımlı olarak taşınır; iskemiye maruz kalan nöronlarda ise dakikalar içinde ATP azalması ile birlikte oluşan nöronal membran depolarizasyonu bu sistemi etkileyerek glutamatın ekstrasellüler konsantrasyonunun artmasına yol açar. Ekstrasellüler konsantrasyon 2-5 μmol/lt’ye ulaşırsa glutamat eksisitotoksisitesi ve buna bağlı nöronal harabiyet oluşur. Ekstrasellüler glutamat artışı N-metil-D-aspartat (NMDA) ve non NMDA reseptörlerinin aşırı aktivasyonuna yol açar. Eksitotoksisiteden esas sorumlu olan NMDA reseptör aktivasyonudur. NMDA reseptör kanalı normalde magnezyum ile bloke durumdadır.
İskemi ile nöronal memran depolarizasyonu oluşunca voltaja bağımlı bu kanal açılarak nöron içine Na, Cl ve H2O’nun girmesine neden olur, hücrede şişme meydana gelir.
Aktivasyonun uzun sürmesi durumunda nöron içine kalsiyum girerek kalsiyuma bağlı enzimleri aktive olmasına ve gecikmiş hücre ölümüne neden olur.
Kalsiyum sitotoksisitesi:Normalde ekstrasellüler kalsiyum konsantrasyonu intrasellüler konsantrasyondan 104-105 kat daha yüksektir. İskemide oluşan ATP kaybı ile hızlı olarak masif intrasellüler kalsiyum artışı olur. İntrasellüler kalsiyum artışı nöron içinde kalsiyuma bağımlı birçok enzimin aktive olmasına neden olur. Bu enzimler protein kinaz C, protein kinaz 2, fosfolipaz A2, proteaz, protein fosfataz, nitrik oksit sentetaz (NOS), endonükleaz ornitin dekarboksilaz ve ksantin oksidazdır. Bu enzimlerden fosfolipaz A2’nin aktivasyonu araşidonik asit ve platelet aktive edici faktör (PAF) oluşmasına neden olur. PAF glutamat salınımını arttırır, araşidonik asit ise glutamatın astrositler ve nöronlara geri alınımını inhibe eder. Böylelikle her ikisi de glutamat nörotoksisitesine yol açarlar ve oksidatif stresi arttırırlar.
Oksidatif stres:İskemide; reperfüzyonda nöronal harabiyetin mekanizmasında öne sürülen teorilerden biri de hücre içinde serbest oksijen radikallerinin oluşması ve ani oksidatif strestir. Oksijen molekülünü ilgilendiren serbest radikallere serbest oksijen radikalleri (SOR) denir. SOR iskemi, nörodejeneratif hastalıklar gibi birçok hastalığın patofizyolojisinde rol oyanmaktadır. Başlıca üç çeşit SOR vardır; süperoksit anyonu, hidrojen peroksit ve hidroksil radikali. Hidroksil radikali ortamda serbest demir varlığında oluşur ve çok reaktiftir. Hücre içi ve dışı antioksidan savunma sistemleri vardır. Hücre içinde SOR’lerinin aşırı artışı durumunda bu savunma sistemleri yetersiz kalır. Özellikle hücredeki intrasellüler kalsiyum artışı ile aktive olan enzimlere bağlı gelişen SOR artışı nörondaki oksidatif stresin esas nedenidir. İskemide beyinde hem parankim hem de vasküler endotelde serbest radikaller açığa çıkar.
İnflamasyon:
Yapılan deneysel çalışmalar iskemik inmede zedelenen beyin dokusunda saatler içinde inflamatuar bir reaksiyonun tetiklendiğini ve bu durumun semptomların ortaya çıkışından sonraki günlerde de devam etmekte olduğunu göstermiştir. İskemik dokunun lökositler tarafından infiltrasyonu ile mikroglia ve astrositlerden inflamatuar cevabın önemli bir göstergesi olan sitokinler tümür nekroz faktör-α (TNF alfa), interlökin 1 (IL1a) açığa çıkar. Sitokinler endotel hücreleri, lökositler ve plateletlerden İntrasellüler adeyon molekülü (ICAM-1), Endotelyal lökosit adezyon molekülü (ELAM-1), selektin, integrin salınımını arttırır. Bundan sonraki evrede ise;
1- Endotele yapışan lökositlerin eritrosit akımını bloke ederek akım hızını yavaşlatması.
2- Aktive lökositlerden salınımı artan proinflamatuvar sitokinler, oksijen radikalleri ve proteazlar.
3- Lökositlerde fosfolipaz aktivasyonu ile lökotrienler, prostoglandinler, eikosanoidler ve platelet aktive edici faktörlerin yapımının artması iskemik doku harabiyetini daha da arttırarak nöron ölümüne neden olabilir.
Enflamatuar hücreler nöronlar üzerinde oksijen serbest radikalleri oluşturarak ve indüklenen nitrik oksit sentaz (iNOS) ile siklooksijenaz (COX2) aktivasyonu sağlayarak direk olarak toksik etkiye neden olabilirler. iNOS fokal iskemi modellerinde iskemiden 12-48 saat sonra yükseldiği ve bu artışa NO ve peroksinitrit artşının eşlik ettiği gösterilmiştir. iNOS inhbitörlerinin ise deney hayvanlarında infarkt boyutunu küçülttüğü saptanmıştır.
Sonuç olarak iNOS iskemik harabiyetin gecikmiş progresyonunda önemli bir faktördür.
Apopitoz: Apopitoz yavaş gelişen genetik kontrol altında oluşan programlanmış hücre ölümüdür ve hücre kendi ölümünde aktif rol oynayan proteinleri sentez etmektedir. Apopitoza yol açan farklı uyarılar ölüm programını aktif hale getirmektedir. Hücre içinde kalsiyumun ve serbest radikallerin artışı apopitozu indüklerken spesifik gen transkripsiyolarına ve protein sentezlerine neden olmaktadırlar. Apopitozun spesifik moleküler belirleyicisi olan kaspaz adı verilen proteolitik enzimler apopitotik hücre ölümünün oluşmasında önemli rol oynarlar. Kaspaz inhibitörlerinin verildiği deneysel fokal iskemi modellerinde iskemik hasarın azaldığı gösterilmiştir. Apopitozda hücrelerde kaspaz aktivasyonu dışında DNA fragmantasyonu ve Bax/Bcl-2 (apoptotik gen/prototipik antiapoptotik geni) oranında artış saptanmıştır (24).
Tablo 3:İskemik inmede inflamasyonun etki mekanizmaları (24).
2.5.2. Sınıflandırma
İskemik inmeli hasta grubunu alt tiplere ayırma konusunda halen bir fikir birliğine varılmamıştır. Yaygın olarak kullanılan sınıflandırmalar da hastaların değerlendirilmesi ve tedavi yöntemi için yol gösterse de her yönü ile yeterli olmaktan uzaktırlar. Bugün için en sık kullanılan etyolojiyi temel alan sınıflamadır. Etyolojiyi temel alan sınıflandırmalardan en yaygın kullanılanı, klinik bulguların yanı sıra etyolojiye de yer veren 1993 yılında yayınlanan Trial of Org 10172 in Acute Stroke Treatment (TOAST) çalışmasında kullanılan sınıflandırmadır (Tablo 4) (25).
Tablo 4: İskemik inmede TOAST sınıflandırması.1993 1. Aterosklerotik enfarkt (Büyük damar hastalığı), 2. Kardiyoembolik enfarkt
3. Laküner enfarkt (Küçük damar hastalığı) 4. Diğer belirlenen etyolojiler
5. Sebebi belirlenemeyenler (Kriptojenik)
TOAST sınıflandırılmasında adı geçen hastalıklar şunlardır; 1. Aterosklerotik İnfarkt (Büyük Damar Hastalığı)
Tüm iskemik inme hastalarının %14-40 kadarından sorumludur (17,18). NINDS kriterlerine göre major intrakranyal veya ekstrakraniyal serebral arterleri tutan aterosklerotik lezyonlara bağlı olarak ortaya çıkan serebral enfarkt olarak tanımlanır. Geniş damarların birindeki aterosklerotik plak sonucunda progresif stenoz ile geniş arteryel oklüzyon oluşabilir. Aterosklerotik plaklar karotis arter ve vertebrobaziler sistemin herhangi bir noktasında oluşabilir. Fakat en sık ana karotis arter bifurkasyonu ile eksternal ve internal karotis arterlerde görülür. Ayrıca orta ve ön serebral arterlerden ve vertebral arterlerden orijin alabilir (16).
Majör damarların oklüzyonu ya da şiddetli stenozu distal kısımda perfüzyon yetersizliği ve infarkt oluşturur. İnfarktın oluşumu kollateral akımla da ilgilidir. Stenozun derecesi ve perfüzyonun azalması multipl faktörlere bağlıdır. Aterosklerotik stenoz ya da oklüzyon, embolik mekanizma üzerinden de serebral infarkta neden olabilir. Bu durumda proksimalde yerleşmiş ateromatöz lezyondan çıkan emboli, diğer sağlıklı dalları oklüde ederek arteryel ağacın daha distalinde lokalize olur. Embolik fragman, stenoze ya da ülsere, etkilenmiş ekstrakraniyal arterlerden çıkabilir. Herhangi bir majör serebral arterin kökünde stenoz olabilir ayrıca oklüzyon internal karotid arterin gövdesinde de görülebilir ve bu durumlarda embolik fragman oluşturabilir. Hatta oklüde karotisin üstünde anterograd olarak trombüs gelişebilir.
2. Kardiyoembolik Enfarkt
Kardiyak kaynaklı trombüsden köken alan kardiyoembolizm önemli bir inme nedenidir. İskemik serebrovasküler hastalık nedenleri arasında, aterotrombotik mekanizmalardan sonra ikinci sırada yer alır, %15 ile %30 kadarından sorumludur (16,17).Trombüsten küçük bir partikül kopup kan dolaşımına geçerek küçük bir artere, genelde distal intrakraniyal dallara gidebilir. Trombüsten embolizasyonun yanı sıra diğer tip partiküller de (neoplazm, yağ, hava ve diğer yabancı madde partikülleri) embolize
olabilir. Kardiyak embolizmin en sık nedenleri; valvüler kalp hastalıkları (mitral stenoz, mitral regurjitasyon, romatik kalp hastalıkları), intrakardiyak trombüs (anterior MI sonrası, sol ventrikül duvarını etkileyen trombüs, atriyal fibrilasyonlu (AF) hastalarda sol atriyal apendikste trombüs), ventriküler ya da septal anevrizma ve kardiyomyopatilerdir. Kardiyak kan akımının yavaşlaması da intrakardiyak trombüs formasyonu için artmış eğilim yaratır. Diğer serebral embolizm kaynakları; atrial miksoma, marantik endokardit ve şiddetli mitral kapak prolapsusudur. Embolizm, majör serebral arterlerin farklı bölümlerini veya serebral yüzeyel dalları etkileyebilir. Arteriyel lümenin embolik obstrüksiyonu rekanalizasyon ve fibrinolizis ile temizlenmektedir. Bu oluşum sırasında damar lümeni stenotik görülebilir. Son zamanlarda kardiyak ve serebral görüntülemenin daha duyarlı olmasıyla trombüs kaynağının daha iyi tanımlaması yapılmıştır.
3. Laküner İnfarktlar (Küçük Damar Hastalığı)
Tüm inme olgularının %15 ile 30 kadarını oluşturur (16,17). Bu infarktlar tek bir damar alanında tanımlanan küçük iskemik bölgelerde oluşan lezyonlardır. Lakünün patolojik tanmlaması; ortalama 5mm çapta (3-15 mm) ufak serebral infarktlardır.
Lakünler talamus, bazal ganglia, korona radiata, sentrum semiovale, internal kapsül ve beyin sapında görülebilir.
Temel patoloji damar duvarı yıkımı, damarın fokal ekspansiyonu, trombotik tıkanma, hemorajik ekstravazasyon ve fibrinoid depolanmadır (26).
Derin penetran arterlerde stenoz, lipohyalinoz ya da mikroateromla oluşan ufak fokuslar gösterilmiştir (27). Laküner infarktlar büyük serebral arterlerin (özellikle arteria serebri media, arteria bazillaris, arteria serebri posterior, arteria serebri anterior ve arteria vertebralis) derin delici dallarının tıkanması sonucu beyinin derin bölümlerinde ve beyin sapında oluşurlar. Bu arterlerin çapları 40-500 mikron arasındadır ve tümü delici arterler olarak bilinir. Kollateral dolaşımları yoktur. Delici arterlerin kanlandırdığı alanlar değişik olduğundan farklı büyüklükte infarktlar oluşur.
Küçük damar hastalığı (lipohyalinozis) daha çok beyinin derin penetran arterlerini tutar ve arteryel hipertansiyon ile birliktedir ancak emboli kaynaklı kalp hastalığı ve büyük damar hastalıkları ile birlikte de görülebilir (26). Küçük derin infarktlara neden olabilir. Genellikle çoğuldur. Putamen, kaudat nükleus, globus pallidus, talamus, pons, internal kapsül ve periventriküler ak maddede yerleşir.
Lakünlerin gelişiminde HT, diabetes mellitus (DM), kardiyopatiler, kan basıncında ani düşmeler, polistemi, arterden artere emboliler de nedenler arasındadır (26). Küçük lakünler (2-4 mm) genelde asemptomatiktir. Kaudat nükleus ve putamende pek çok lakün asemptomatik olabilir. Nekropsi çalışmalarında lakünlerin %30'u asemptomatik
bulunmuştur. Bununla birlikte lakünler küçük olsa bile, duyusal ve motor yollarda geliştiklerinde klinik bulgular verirler. Anjiyografik incelemelerde arter tıkanmaları olağan değildir. Vakaların %20-25'inde önceden GİA görülebilir.
Lakünler semptomatik olduğunda lakünün konum ve büyüklüğüne bağlı olarak değişik klinik tablolar ortaya çıkar. Semptomatik lakünlerin altta yatan en önemli mekanizması mikroateromdur. Kronik HT'a bağlı penetran arterlerin lipohyalinozisi de önemli rol oynar. Lipohyalinozis sessiz lakünlerde de sık görülür. Ayrıca damar duvarındaki, kronik HT'a bağlı fibrinoid nekroz da önemlidir. Fibrinoid nekroz sonucu serebral otoregülasyon bozulabilir. Artmış kan basıncı ile damar duvarı kalınlaşır. Bu durum hidrostatik kapiller basıncı arttırır ve kapiller zararla vasküler nekroz küçük damar hastalığı oluşturur (29). Mikroembolizm de laküner infarkt oluşturabilir. Laküner infarktlarda hemodinamik temelde intra veya ekstrakraniyal karotis stenozu önemli rol oynar. Derin infarktlarda perfüzyon yetmezliği de önemlidir (28). Genel olarak laküner infarkt risk faktörleri geniş arter hastalığı ile aynıdır. Bilateral kapsüler lezyonlarda afoni, anartri, apraksi ve mutizm görülebilir. Multipl lakünlere bağlı frontal lob disfonksiyonu ve demans bildirilmiştir (29). Laküner infarktların tanısında bilgisayarlı beyin tomografisi/ Magnetik Rezonans Görüntüleme (BBT)/ MRG kullanılabilir. MRG tanımlamaları, BBT'ye göre daha üstündür (29,30). BBT'de 10 mm dolayındakiler kolayca tanınabilir ama 4 mm'den küçük ve beyin sapındaki lezyonları görülemeyebilir (31).
4. Diğer belirlenen etyolojiler
Daha az sıklıkla görülmekle birlikte serebral perfüzyonu azaltıp infarkt oluşturan diğer durumlar Tablo 5’de gösterilmiştir. Bu nedenler iskemik inmenin etyolojisinin yaklaşık %5’ini oluşturur (16,17).
Tablo 5: İskemik inmenin diğer etyolojileri (16,17). 1- Vazospazm ve sistemik hipotansiyon
2- Primer ya da sekonder vaskülit 3- Hiperkoagulabl durumlar
4- Hiperviskozite (polistemi, disproteinemi ya da trombositozis) 5- Arteryal disseksiyon
6- Beyin drenajını sağlayan venlerin oklüzyonu 7- Moya moya hastalığı
8- Fibromusküler Displazi
9- Tümör ile majör arterlerin ekstrinsik kompresyonu 10- Beyin drenajını sağlayan venlerin oklüzyonu
5. Sebebi belirlenemeyenler (Kriptojenik)
Tanımlanmamış infarktlar iskemik infarktların %40 kadarını oluşturur (16,17). Serebral infarkt subtiplerinin ayırt edilmesinde inme oluşumunun klinik özellikleri yardımcı olabilir.İnme etyolojisine yönelik ilk sınıflandırmalar genelikle patolojisine göre yapılmış ve tüm inmeler iskemik ve hemorajik olarak iki ana gruba ayrılmıştır. Daha sonraki çalışmalarda ileri nöroradyolojik, kardiyolojik, hematolojik ve biyokimyasal tetkiklerin kullanılması ile lezyonun patolojisi ile birlikte lezyon lokalizasyonu ve oluş mekanizması göz önüne alınarak sınıflandırmalar yapılmıştır (32). Bamford ve arkadaşları 1991 yılında klinik bulguları ön planda tutarak bir sınıflandırma yapmışlardır, bu sınıflandırmada etyolojiye yer verilmemiştir (33).
Bamford ve arkadaşlarının yaptığı Oxfordshire sınıflandırması: 1. Total anterior sirkülasyon infarktları(TACI)
2. Parsiyel anterior sirkülasyon infarktları(PACI)) 3. Laküner enfarktlar(LACI)
4.Posterior sirkülasyon infarktlarıPOCI) 2.6. İnmenin Risk Faktörleri
Akut İnme tedavisindeki önemli gelişmelere karşın, inmeye bağlı ölümler halen ölüm nedenleri arasında 3.Sıralarda yer almakta ve inmeye bağlı sakatlıklar ise büyük ekonomik kayıplara yol açmaktadır.Bu durumda inme risk faktörlerinin epidemiyolojik çalışmalarla belirlenmesi ve önlenmesi önem kazanmaktadır. Risk faktörlerinin, relatif riskinin hesaplanmasının yanı sıra, bu faktörlerin toplumdaki prevalanslarının da bilinmesi, özellikle toplum sağlığı ve ülke ekonomisi açısından önemlidir. Bireysel olarak ele alındığında ise risk faktörlerinin başta yaş olmak üzere diğer risk faktörleri ile etkileşimleri, toplum sağlığı açısından da prevalansları gözönüne alınarak değerlendirilmelidir. Bu bilgiler doğrultusunda inme risk faktörleri Tablo 6'de görüldüğü gibi sınıflandırılmıştır.
Tablo 6: İnmede risk faktörlerinin sınıflandırılması (16-18). I. Değiştirilemeyen risk faktörleri
a) Yaş b) Cins c) Irk
d) Aile öyküsü
II. Değiştirilebilen risk faktörleri a) Kesinleşmiş faktörler
1. Hipertansiyon
2. Diabetes Mellitus, hiperinsülinemi ve glikoz intoleransı 3. Kalp hastalıkları
4. Hiperlipidemi 5. Sigara
6. Asemptomatik karotis stenozu 7. Orak hücreli anemi
b) Kesinleşmemiş faktörler 1. Alkol kullanımı
2. Obezite ve Beslenme alışkanlıkları 3. Fiziksel inaktivite
4. Hiperhomosisteinemi
5. İlaç kullanımı ve bağımlılığı 6. Hormon tedavisi
i) Oral kontraseptif kullanımı ii) Hormon replasman tedavisi 8. Hiperkoagülabilite
9. Fibrinojen 10.İnflamasyon
2.6.1. Değiştirilemeyen risk faktörleri
a) Yaş: Yaş ilerledikçe inme riskinin arttığı bilinmektedir. Yaş, inme için en kuvvetli belirleyici faktördür. 55 yaşından sonraki her on yılda bu risk iki kat artmaktadır. Ancak inme gençlerde de görülebilir ve erken sakatlık nedeni olabilir (16-18).
b) Cins: inme insidansı erkeklerde kadınlara göre daha fazla görülmekle birlikte, kadınlarda inme nedenli ölüm hızı daha yüksektir (34).
c) Irk: Zencilerde, Çinlilerde ve Japonlarda inme insidansı, beyazlara göre daha yüksektir. İnme insidansındaki bu artış, bazı risk faktörlerinin o toplumda daha fazla olması ile açıklanamayacak kadar yüksek bulunmuştur (35,36).
d) Aile öyküsü: Aile öyküsünün risk faktörü oluşunda çeşitli etmenler rol oynamaktadır. Bunlar; benzer yaşam tarzları, beslenme alışkanlıkları ve bazı herediter özellikler olabilir. Monozigot ikizlerde inme riski, dizigot ikizlere göre daha yüksektir (37,38). 2.6.2. Değiştirilebilir risk faktörleri
a. Kesinleşmiş risk faktörleri:
1. Hipertansiyon: HT toplumda prevalansı en yüksek olan, hem serebral infarkt hem de intraserebral hemoraji için en önemli risk faktörüdür (39,40). İnme riski, kan basıncı artışı ile doğru orantılı olarak artmaktadır. Artmış sistolik ya da diastolik kan basıncı (ya da her ikisi), artmış inme riski ile birliktedir ve aterosklerozun progresyonu ile küçük damar hastalığı predispozisyonuna yol açmaktadır (18,41,42). Bununla beraber, antihipertansif tedavinin inme riskini belirgin şekilde azalttığı ortaya konmuştur. Bir meta-analizde, diastolik kan basıncında 5-6 mmHg azalmanın strok riskini %42 azalttığı gösterilmiştir. Ayrıca, çeşitli yaş gruplarına ait hipertansif yaşlılarda yapılan çalışmalarda antihipertansif tedavinin, bu hastalardaki inme riskinde %40 ile 45 oranında azalmaya neden olduğu bulunmuştur (43,44).
2. Diabetes mellitus, hiperinsülinemi ve glikoz intoleransı: Çeşitli çalışmalarda (45-48) diabetin, iskemik inme riskini 2-6 kat arttırdığı gösterilmiştir. İngiltere’de ve ABD’de yapılan çalışmalarda uzun süre sıkı kan şekeri kontrolü ile izlenen hastaların mikrovasküler komplikasyonlarında azalma gözlenirken, inme riskinde bir düşme görülmemiştir. Fakat, diabetli hastaların yaklaşık %40-60 'ında birlikte bulunan HT’nın tedavisi inme riskini %44 azaltmaktadır (49). Glikoz intoleransının ve serum insülin konsantrasyonunun inme riskini arttırdığına ilişkin bazı çalışmalar mevcut olmakla birlikte, bu artış muhtemelen oldukça düşüktür.
3. Kalp hastalıkları: Kalp hastalıkları, artmış iskemik inme riski ile ilişkilidir. Özellikle AF (Atrial fibrilasyon), valvüler kalp hastalığı, akut myokardiyal infarktüsü (AMI), koroner arter hastalığı, konjestif kalp yetmezliği (KKY), EKG'de sol ventrikül hipertrofisi ve mitral kapak prolapsusu risk faktörleri olarak kabul edilir (18,41,42). Kronik AF yaşla artış göstermektedir. Framingham çalışmasında AF’nin inmeyle önemli ölçüde ilişkili olduğu bulunmuştur (50). Koroner kalp hastalığı ya da kardiyak yetmezlik AF’la birleşince inme riski erkeklerde 2, kadınlarda 3 kat artmaktadır (18,41,42). Valvüler hastalık ve AF birlikteliğinde ise inme riski daha da yüksektir.
Ekokardiyografide sol ventrikül disfonksiyonu ve sol atriyal çap artışı tromboembolik riski arttıran diğer önemli bir belirleyicidir. Önceden koroner arter hastalığı varsa inme riski 2 katına, kardiyak yetmezlikli hastada 4 katına çıkmaktadır. Sol ventrikül hipertrofisi inme riskini 2.3 kat, mitral annüler kalsifikasyon inme riskini 2.1 kat arttırmaktadır. Kardiyak görüntülemenin gelişmesi ile; mitral kapak prolapsusu, patent foramen ovale, aortik ark aterosklerotik hastalığı, atriyal septal anevrizma gibi potansiyel inme risk faktörleri tanımlanmıştır (18,40,45). Yaş gruplarına göre en sık emboli nedenleri farklılık göstermektedir. Gençlerdeki en önemli emboliye neden olan kalp hastalıkları, AF ile birlikte veya yalnız olarak görülen mitral stenoz, kapak replasmanı yapılması, infektif endokardit, kardiyak tümörler, mitral yetmezlikler veya AF ile birlikte olan mitral valv prolapsusu, Libman-Sack endokarditi, dilate kardiyomyopatilerdir. Orta yaş ve üzerinde ise, en sık görülen kardioemboli sebebi myokard infarktüsüdür. İleri yaşta en önemli kardiojenik emboli riski taşıyan hastalık nonvalvüler atrial fibrilasyondur (NVAF).
4. Hiperlipidemi: Serum lipid anormallikleri (trigliserit, kolesterol, LDL, HDL, VLDL) risk faktörü olarak dikkate alınmalıdır. Bu anormallikler koroner kalp hastalıkları için de risk faktörüdür. Artmış serum kolesterol miktarları inme riski ile bağımsız ilişkilidir. Serum kolesterol düzeyinin 240-279mg/dl değerleri arasında olması, inme riskini 1,8 ve 280mg/dl üzerinde olması ise 2,6 kat artırmaktadır. ABD’de yapılan bir diğer çalışmada, kolesterol seviyesindeki artışın, hem koroner arter hastalığı hem de tromboembolik inme riskini arttırdığı gösterilmiştir. Lipoprotein-a konsantrasyonunun yine koroner arter hastalığı riskini arttırdığı gösteren çalışmaların yanısıra, diğer bazı kontrollü çalışmalarda, Lipoprotein-a ile inme riski arasında anlamlı bir ilişki bulunmamıştır. Son zamanlardaki çalışmalarda HDL inme için koruyucu etkili bulunmuştur ve statinlerle tedavi edilen kişilerde inme riskinde anlamlı azalmalar görülmüştür (18,42,51,52). 5. Sigara: Sigara içme inme için bağımsız bir risk faktörüdür. Sigara aynı zamanda karotis arter plak kalınlığının bağımsız belirleyicisidir. Sigara en çok aterosklerotik infarktla ilişkilidir (42,53). Sigara üzerinde 1980'li yıllardan beri yapılan çalışmalarda, iskemik inme için relatif riskinin 1,8-6 arasında olduğu bulunmuştur. "Framingham Heart Study" çalışmasında bu risk 1,8 olarak bulunmuş olup, bu risk, sigara bırakıldıktan 5 yıl sonra içmeyenlerin düzeyine inmekte, diğer çalışmalarda ise 1,2-1,3 arasında bulunmaktadır. Diğer tütün ürünlerine geçişin riski azaltmadığı yönünde çalışmalar mevcuttur. Sigara dumanına maruz kalanlarda yapılan çalışmalarda da bu risk en az 1,2 olarak bulunmuştur. "Honolulu Heart Study" çalışmasında ise iskemik inme yanı sıra, subaraknoid kanama riski de oldukça yüksek bulunmuştur (54).
6. Asemptomatik karotis stenozu: Asemptomatik karotis arter hastalığı, nonstenoze plak ya da karotis stenoz artmış inme riski ile ilişkili bulunmuştur. Yıllık inme riski %75'in altındaki darlıklarda %1.3, %75'in üstü stenozlarda %3.3, aynı taraflı inme riski ise %2.5'dur (55,56). Ayrıca %75 den fazla stenozlularda GİA ve inme geçirme riski her yıl için %10.5'dur (18,41,42,55-57). Asemptomatik karotis arter hastalığı olan kişilerdeki semptomların oluşması; stenoz şiddeti, kollateral sirkülasyon gelişimine, aterosklerotik plağın karakterine, stenozun tarafına ve trombüs formasyonuna bağlıdır (41,55-57). Özellikle stabil darlıklara göre hızla progresyon gösteren darlıklarda bu risk daha yüksektir.
7. Orak hücreli anemi: Otozomal dominant geçişli bir hastalık olan orak hücreli aneminin prevalansı düşük (zencilerde %0,25) olmakla birlikte relatif riski yüksektir. Bu hastalarda 20 yaşına kadar inme prevalansı ise %11'dir. Yapılan bir çalışmada sık kan transfüzyonları uygulanan orak hücreli anemi hastalarında, inme riskinin yılda %10'dan %1'e düştüğü gösterilmiştir (58).
b. Kesinleşmemiş risk faktörleri
1. Alkol kullanımı: Alkol tüketimi ile inme arasındaki ilişki kompleks bir ilişkidir ve tartışmalıdır. Günde 2 kadehe kadar alkol tüketiminin HDL kolesterol artışı, trombosit agregasyonunda azalma, fibrinojen azalması gibi mekanizmalarla iskemik inme riskini azalttığı öne sürülmektedir. Fakat daha yüksek miktarlarda kullanılan alkol, hipertansiyon, hiperkoagülabilite ve kardiyak aritmilerde artışa yol açarak inme riskini arttırmaktadır. Ayrıca çeşitli çalışmalarda, sürekli ve fazla miktarda alkol tüketen kişilerde, anevrizmal ve nonanevrizmal intraserebral kanamalarda en az 3 kat artış olduğu tespit edilmiştir (59).
2. Obezite: Beden kitle indeksinin 30 kg/m2'nin üzerinde olması ile karakterize olan ve özellikle erkeklerde sık görülen abdominal obezitenin, inme riskini 1,75-2,37 kat arttırdığı tespit edilmiştir (41) .
3. Beslenme alışkanlıkları: Diyetteki yağ miktarının, çeşidi ve balık tüketiminin koroner arter hastalıkları ile olan ilişkisi kabul edilmesine karşın, inme ile olan ilişkisi halen kesin olarak saptanabilmiş değildir. Buna karşılık bazı çalışmalarda, en fazla sebze ve meyve tüketen grupta relatif inme riski 0,69 olarak bulunmuştur. Son zamanlarda, gıdalara potasyum, kalsiyum, magnezyum eklenmesinin yararları ile ilgili çalışmalar yapılmaktadır (60).
4. Fiziksel inaktivite: Çeşitli çalışmalarda düzenli fiziksel egzersizin inme riskini azalttığına ilişkin bulgular mevcuttur. Bu azalma, diğer bilinen risk faktörlerinin (obezite, hipertansiyon, hiperglisemi vb) yanısıra, plazma fibrinojen düzeyinin azalması
ve doku tipi plazminojen aktivatörü (tPA) ve HDL kolesterol seviyesinin artışına bağlı olabilir. Koruyucu fiziksel aktivitenin sıklığı ve süresi tam olarak belirlenmemiş olmakla birlikte, hergün ortalama 30 dakikalık egzersiz önerilmektedir (61).
5. Hiperhomosisteinemi: Plazma homosistein düzeyi 16mikromol/L’ün üzerinde olmasıdır. Homosistein düzeyi yaşla da artış göstermekte olup, erkeklerde daha yüksektir. Yapılan bir çalışmada, hiperhomosisteinemisi olan hastalarda inme riskinin 2.25 kat arttığı saptanmıştır (62). Ancak bu yöndeki çalışmalarda henüz kesinleşmiş ve tekrar edilmiş bulgular yoktur.
6. İlaç kullanımı ve bağımlılığı: Amfetamin, kokain ve eroin gibi bağımlılık yapan maddelerin kullanımının, hem hemorajik hem de iskemik inmeye yol açtığı bilinmekteyse de, bu konuda geniş epidemiyolojik çalışmalar mevcut değildir. Sınırlı çalışmalarda, inme riskinin yaklaşık 7 kat arttığı bildirilmektedir. Bu maddelerin etkileri multifaktöriyel olup, ani kan basıncı yükselmesi, vaskülit ve hematolojik bozukluklara yol açmaları en önde gelen inme nedenleridir (63).
7. Hormon tedavisi:
i) Oral kontraseptif kullanımı: Oral kontraseptiflerin inme riski, içeriklerindeki estradiol miktarı ile ilişkili olup, 50 mikrogram'dan fazla estradiol içeren ilk jenerasyon ilaçlarda bu risk yüksektir. Son zamanlarda kullanılan düşük estradiollu ve kombine preparatlarla yapılan çalışmalarda ise, iskemik ve hemorajik inme riskinde hafif bir artış gözlenmiştir. Bu nedenle, özellikle 35 yaşın üzerinde olan, ailede subaraknoid kanama öyküsü bulunan, sigara içen, migren veya hipertansiyonu bulunan kadınlara diğer kontrasepsiyon yöntemleri önerilmektedir. Ayrıca, yüksek estradiol içeren preparatlarda olduğu gibi düşük estradiol'lü ilaçlarda da, özellikle trombofilili hastalarda yüksek serebral sinüs trombozu riski bulunmaktadır (64-67).
ii) Hormon replasman tedavisi: Framingham çalışmasında hormon replasman tedavisi yapılan kadınlarda aterotrombotik inme riski 2.6 olarak bulunmuş olmakla birlikte, daha sonra yapılan çalışmalarda bu doğrulanmamıştır (66).
8. Hiperkoagülabilite: Hiperkoagülabiliteye yol açan trombofililer (Protein C ve S eksikliği, aktive protein C (APC) rezistansı, antitrombin-III (ATIII) eksikliği ve protrombin 20210 mutasyonu) öncelikle venöz trombozlara yol açmakla birlikte, iskemik inmelerede neden olabilirler. Fakat diğer risk faktörleri elimine edildiğinde, gerçek risk değerleri oldukça kuşkuludur. Bir diğer hiperkoagülabilite nedeni olan antifosfolipid antikor sendromu ile yapılan çalışmalarda farklı antikor izotipleri (IgG, IgM veya IgA) göz önüne alındığından bu sendromun da prevalansı ve inme riski tartışmalıdır. Yüksek tPA, fibrin D-dimer, von Willebrand faktör ve faktör VIIIc'nin
inme risk faktörü olduğuna ilişkin bazı çalışmalar bulunmakla birlikte bu konu tam olarak anlaşılabilmiş değildir (65).
9. Fibrinojen: Bazı öncü çalışmalarda, fibrinojen yüksekliği, inme risk faktörü olarak belirlenmiş olmasına karşın, 1999'da yapılan bir diğer çalışmada bağımsız bir risk faktörü olarak bulunmamıştır (67).
2.7. Geçici İskemik Atak (GİA)
Geçici İskemik ataklarının çoğu, sadece birkaç dakika ile 2 saat arasında sürmektedir. GİA birkaç mekanizma ile oluşabilir. Şiddetli majör karotis ya da vertebrobaziller stenoz oluştuğunda, geçici bir iskemi ortaya çıkabilir ve kısa süreli GİA görülebilir (27,28,68). Bazı ataklar uzun olabilir ve sıklıkla distal dal oklüzyonu ile ilişkilidir. Bu durum ülsere plaktan embolizm kaynaklı veya daha proksimal kaynaklı olabilir. Bazı GİA'lar özellikle vertebrobaziller olanlar, hemodinamik temelde oluşabilir, geçici hipotansiyon ve kardiyak aritmi ile görülebilir (27,28). Karotis ve vertebrobaziler sistem sulama alanlarındaki GİA'lar, beynin etkilenmiş bölgelerine bağlı olarak, çeşitli belirtiler ya da farklı kombinasyonlar gösterebilir. Hastalarda herhangi bir zamanda rekürren GİA'lar görülebilir (69). Semptomlar belirsiz olduğu zaman GİA tanısı zor olabilir.
GİA ayırıcı tanısında; migren, kardiyak aritmi, nöbetler, hipoglisemi ve nörotik bozukluklar düşünülebilir (27). GİA'lı hastalar myokardiyal infarkt ve majör inme için de artmış risk taşımaktadırlar (70).
2.8. Serebral İnfarkt
Spesifik damarların iskemik sendromları, sadece oklüzyon bölgesine bağlı değildir. Önceki beyin hasarı, kollateral sirkülasyon, bölgeyi besleyen arterlerin ve Willis poligonu'nun varyasyonlarına da bağlıdır.
Bu damarların sendromları daima oklüzyon biçimi ya da tarafı ile tanımlanmamıştır (örneğin; orta serebral arter bölgesindeki infarkt sıklıkla internal karotid arterdeki oklüzyon sonucunda olmaktadır). Orta serebral arter veya dalları sıklıkla embolik olarak tıkanır (32,57,75).
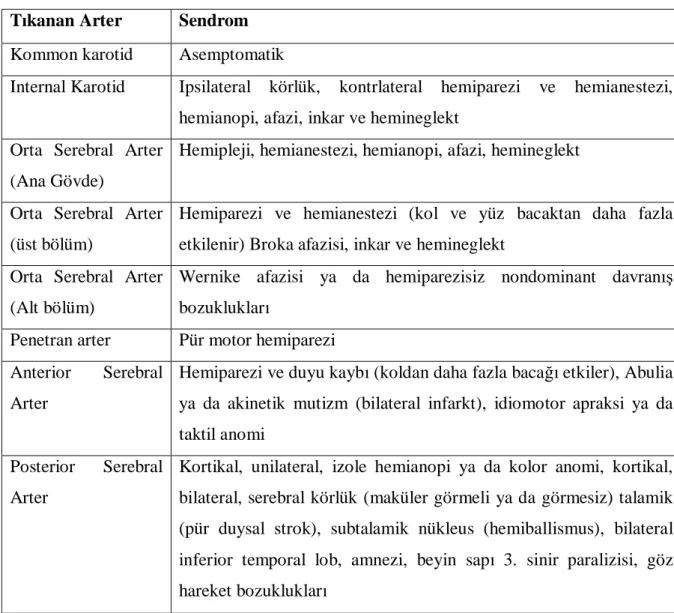
Tablo 7 : Serebral İnfarkt Sendromları. Tıkanan Arter Sendrom Kommon karotid Asemptomatik
Internal Karotid Ipsilateral körlük, kontrlateral hemiparezi ve hemianestezi, hemianopi, afazi, inkar ve hemineglekt
Orta Serebral Arter (Ana Gövde)
Hemipleji, hemianestezi, hemianopi, afazi, hemineglekt
Orta Serebral Arter (üst bölüm)
Hemiparezi ve hemianestezi (kol ve yüz bacaktan daha fazla etkilenir) Broka afazisi, inkar ve hemineglekt
Orta Serebral Arter (Alt bölüm)
Wernike afazisi ya da hemiparezisiz nondominant davranış bozuklukları
Penetran arter Pür motor hemiparezi Anterior Serebral
Arter
Hemiparezi ve duyu kaybı (koldan daha fazla bacağı etkiler), Abulia ya da akinetik mutizm (bilateral infarkt), idiomotor apraksi ya da taktil anomi
Posterior Serebral Arter
Kortikal, unilateral, izole hemianopi ya da kolor anomi, kortikal, bilateral, serebral körlük (maküler görmeli ya da görmesiz) talamik (pür duysal strok), subtalamik nükleus (hemiballismus), bilateral inferior temporal lob, amnezi, beyin sapı 3. sinir paralizisi, göz hareket bozuklukları
2.9. İNTRASEREBRAL KANAMA
Bir arteryel kaynaktan gelen kanın, ani olarak beyin dokusu içine birikmesiyle ortaya çıkan klinik tabloya intraserebral kanama denir.
2.9.1. EPİDEMİYOLOJİ
İSK’lar tüm inmelerin yaklaşık olarak %10’unu oluşturur ve iskemik inmeden daha az görülmesine rağmen daha ölümcüldürler. İSK’dan ölüm hematomun kitlesi, yaygınlığı ve lokalizasyonu ile yakından ilgili olup; ölüm oranı %25-60, sıklığı ise 12-15/100.000/yıldır.
Coğrafya ve ırklara göre de değişkenlik gösteren İSK’lar; erkeklerde kadınlara göre daha sıktır (71,72). İSK nedeniyle meydana gelen ölümlerin yaklaşık %50’si ilk 2 gün içinde olup, hastaların %6’sı hastaneye ulaşmadan kaybedilmektedir. Yaşayan hastaların %10’u ilk ayda, %20’si 6. ayın sonunda fonksiyonel yeterliliklerine kavuşabilmektedir (73).
İSK prevelansı ile ilgili olarak ülkemizdeki ilk ciddi rakamlar Türk Beyin damar hastalıkları Derneğinin Türk çok merkezli strok çalışması (Türk MST)’dan elde edilmiştir. Bu çalışmada ülkemizdeki İSK sıklığı %28,8 gibi oldukça yüksek bir rakam bulunmuştur. Aynı çalışmada ilk iki haftadaki ölüm hızı %11, tüm hemoraji olguları arasındaki ölüm hızı ise % 16.2 olarak saptanmıştır (74).
2.9.2. ETYOLOJİ
İSK oluşımına yol açan faktörler; anatomik, hemodinamik, hemostatik ve diğer faktörler olarak dört ana kategoriye ayrılır.
Anatomik Faktörler a- Amiloid anjiopati
b- Serebral Arterio Venöz Malformasyom(AVM) ve Anevrizmalar c- İntrakranyal venöz trombozlar
d- Mikroanjiomlar e- Dural AVM f- Diğer nedenler Hemodinamik Faktörler a- Arteriel hipertansiyon Hemostatik Faktörler a- Antikoagülan tedavi b- Trombolitik tedavi c- Hematolojik hastalıklar Diğer faktörler
a- İntraserebral tümörler b- Alkol kullanımı c- Sigara kullanımı d- Lipidler
e- Amfetanim kullanımı
f- Kokain ve diğer sempatomimetiklerin kullanımı g- Vaskülitler
Anatomik Faktörler
a- Amiloid anjiopati: “Primer serebral amiloidoz”, sistemik amiloidoz yokluğunda, serebral doku ve serebral meningeal damarların duvarında amiloid depolanması ile karekterize bir durumdur. Primer serebral amiloidoz ile birlikte normal beyin yaşlanması değişiklikleri; Alzheimer tipi demans, serebral infarkt, kronik vaskülitis, AVM ve normotansif kişilerde spontan İSK ile birlikte olabilir (13-15). Serebral amiloid anjiyopatinin, son yıllarda demansa ve özellikle normotansif yaşlı kişilerde, spontan İSK’lara yol açması dikkati çekmiştir. Serebral amiloid anjiopatide, amiloid; leptomeningeal kortikal arterler, arteriol-kapiller ven ve venüllerin duvarlarında depolanarak, pariyetooksipital veya frontoparyetal dominansi gösterir ve subkortikal bölge dışında ak madde tutulumu olmaz. Neokorteksteki tutulum bir topografik seçim gösterir. Bazal gangliyonlar, serebellum, beyinsapı arterleri az veya hiç tutulmazlar (17-20).
Serebral amiloid anjiyopatide beyindeki değişmeler yaşla ilgili olarak artar. Bu nedenle bir yaşlılık hastalığıdır. Kanamalar 60-70 yaşları arasında görülür ve cinsiyet ayırımı yoktur. Spontan beyin kanamalarının %2-10’unu oluşturur ve genelde yüzeyel ve/veya lober hematom tipindedir. Özellikle yaşlı kişilerde, lober yerleşimli kanamaların tekrarı ve multipl şekilde olmaları; klinik olarak serebral amiloid anjiopatiyi düşündürür. Kanama genellikle spontandır, bazende cerrahi girişim veya travma sonrası ortaya çıkabilirler (22).
b- Serebral AVM ve Anevrizmalar: İSK’lar %6.9 ile 22.1 oranında yırtılmış anevrizmalara, %18.6 oranında ise yırtılmış AVM’lere bağlıdır. Anevrizmalar SAK yapma yanında parankim içine de kanama yapabilirler. Anevrizma yırtılmalarından sonra, doku içine kanama %4-25 olarak bildirilmişitir. Mortalite daha çok; kanamanın volümüne, vazospazma ve tekrarlayan kanamalara bağlıdır (76,77).
c- İntrakranyal venöz trombozlar: İSK’ların seyrek nedenlerinden birisi olmakla beraber, ayırıcı tanıda mutlaka düşünülmelidir. Daha çok genç bayanlarda görülür ve bilateral parasagital bölgedeki kanama ile karekterizedir (74).
d- Mikroanjiomlar: 45 yaş altında sebebi açıklanamayan İSK’ların yaklaşık olarak %25’ini oluşturur. Kavernöz anjiomlar, dilate ve ince duvarlı vasküler kanallar ile kesin sınırlarla beyin dokusundan ayrılan yapılardır. Serebral dokunun herhangi bir yerinde kanama odağı yaratabilir ve ona göre semptom verirler (74).
e- Dural AVM: Çoğunlukla eksternal karotid arterin orta meningeal ve oksipital dallarından beslenen ve dural sinüslere özellikle transvers ya da sigmoid sinüse yakın dreneja sahip yapılardır. Minör ya da majör kafa travmaları, bu yapılarda kolaylıkla rüptüre ve kanamalara yol açabilir (74).
Hemodinamik Faktörler
Arteriel hipertansiyon: Spontan İSK denildiğinde ilk neden olarak HT akla gelir ve HT’la ilgili beyin kanaması, hipertansif intraserebral kanama olarak adlandırılır (23,77). Hipertansiyonun beyin kanamalarındaki rolü 19. yüzyıldan beri bilinmektedir. Ancak bu yüzyılda kan basıncı yeterince ölçülemediği için, HT’nun saptanması ve patolojik bağlantılarının bilimsel olarak çözülmesi gerektiği gibi yapılamamıştır. Yine bu yüzyıl içerisinde, HT’nun damar ve beyinde yaptığı hasarlar ve arteriosklerozis daha iyi bilinmeye başlamıştır. HT’a bağlı başlıca üç ana değişiklik tanımlanmıştır. Bunlar; fibrinoid nekroz, lipohyalinozis ve milier (Charcot-Bouchard) anevrizmalardır (23,26). Fibrinoidnekroz: Beyin, böbrek gibi organların küçük arterlerinin media tabakasında fibrinoid madde birikimi ve kas elemanlarının kaybıyla karekterize bir süreçtir. Burada kas lifleri nekrozu, intima ve media tabakalarına plazma proteinlerinin ve eritrositlerin infiltrasyonu, arter içinde ve etrafında yangısal reaksiyon ve konnektif doku elemanlarının invizyonu görülür (23,26).
Lipohyalinozis: Özellikle 200µ’dan küçük arterlerde, damar duvarlarında incelme, bağ dokusu azalması, hemosiderinden zengin makrofajlar ve damar duvarında parlak kırmızı renkli değişmeler olarak tanımlanır. Lipid birikimi, hyalinozis ve damar duvarında fibrinoid değişiklikler göze çarpar. HT’a bağlı bu değişiklikler, sonuçta iskemik lakün enfarktlara ve İSK’lara neden olur (23,26).
Miler (Charcot-Bouchard anevrizmalar): Hipertansif hastalarda yapılan patolojik çalışmalar, derin ve kortikal arter dallarının kalınlaştığını, bazal arterlerin stenoze olduğunu, anevrizmalara sık rastlandığını, 10’dan fazla anevrizması olan hastaların ise, hipertansif olduğunu göstermişir (23). Bu anevrizmaların büyük bir çoğunluğunun putamen, globus pallidus, talamus, kapsüla interna ve kortikal ak ve gri maddede