T.C.
SELÇUK ÜNİVERSİTESİ FEN BİLİMLERİ ENSTİTÜSÜ
BAZI FLORESANS BODİPY TÜREVLERİNİN SENTEZİ VE METAL HASSASİYET ÖZELLİKLERİNİN ARAŞTIRILMASI
Emine BAĞCI YÜKSEK LİSANS TEZİ
Kimya Anabilim Dalı
Temmuz-2019 KONYA Her Hakkı Saklıdır
TEZ BİLDİRİMİ
Bu tezdeki bütün bilgilerin etik davranış ve akademik kurallar çerçevesinde elde edildiğini ve tez yazım kurallarına uygun olarak hazırlanan bu çalışmada bana ait olmayan her türlü ifade ve bilginin kaynağına eksiksiz atıf yapıldığını bildiririm.
DECLARATION PAGE
I hereby declare that all information in this document has been obtained and presented in accordance with academic rules and ethical conduct. I also declare that, as required by these rules and conduct, I have fully cited and referenced all material and results that are not original to this work.
Emine BAĞCI
iv ÖZET
YÜKSEK LİSANS TEZİ
BAZI FLORESANS BODIPY TÜREVLERİNİN SENTEZİ VE METAL
HASSASİYET ÖZELLİKLERİNİN ARAŞTIRILMASI
Emine BAĞCI
Selçuk Üniversitesi Fen Bilimleri Enstitüsü Kimya Anabilim Dalı
Danışman: Prof. Dr. Ersin GÜLER 2019, 72 Sayfa
Jüri
Prof. Dr. Ersin GÜLER Doç. Dr. Nuriye KOÇAK Doç. Dr. Ahmed Nuri KURŞUNLU
Metal iyonlarının tespitinde floresans sensörlerin kullanımı, yüksek seçicilik ve kolay uygulanabilirlikleri nedeniyle tıp başta olmak üzere birçok bilim dalının gözde çalışma konusudur. Yakın-IR bölgede emisyon yapabilen moleküller, biyolojik ve tıbbi açıdan, dokuya kolaylıkla nüfuz ettiği ve dokuya daha az hasar verdiği için sensör olarak yaygın bir kullanıma sahiptir. Bu yüzden floresan özellik gösterebilen ve yakın infrared bölgede (NIR) emisyon yapabilen bileşiklerin tasarımı ile ilgili bir çok çalışma bulunmaktadır. Bu bileşikler arasında BODIPY (boron-dipirometan) boyar maddeleri, bilinen ve en geniş kullanım alanına sahip, yakın infrared (NIR) bölgede emisyon yapabilen bileşiklerden biridir. Seçimliliği artırabilmek ve kendi içerisinde enerji transferi yapabilen moleküller için anten tipi floresans bileşikler geliştirilmiştir. BODIPY bileşikleri ışık ve kimyasallara karşı dayanıklı floresans maddelerdir. Görünür bölgedeki ışınları yoğun olarak absorplarlar ve buna ilave olarak Bodipy türevleri sahip olduğu yüksek kuantum verimi, yapısal kararlılık, duyarlılık gibi üstün fotofiziksel özellikleri sayesinde birçok alanda kullanılmıştır.
Bu tezde, öncelikle organik gruplar içeren Bodipy türevleri hazırlanmıştır. Bu bileşiklerin emisyon, emilim ve uyarma özelliklerinde meydana gelen değişiklikler daha sonra bazı metal iyonlarının varlığında incelenmiştir. Böylece, bu ölçümlerde, metal
v
iyonunun seçici olması için planlanan nihai Bodipy türevlerinin olduğu tespit edilmiş olup elde edilen bileşikler, farklı metal iyonlarıyla test edilmiştir. Ancak sadece cıva metal için bir seçicilik göstermiştir. Bileşik Hg (II) iyon için bir floresan sensör olarak kullanılabilir.
vi ABSTRACT
MSc THESIS
SYNTHESIS OF SOME FLUORESCENT BODIPY DERIVATIVES AND INVESTIGATION OF METAL SENSITIVITY PROPERTIES Emine BAGCI
THE GRADUATE SCHOOL OF NATURAL AND APPLIED SCIENCE OF SELCUK UNIVERSITY
Advisor: Prof. Dr. Ersin GULER 2019, 72 Pages
Jury
Advisor Prof. Dr. Ersin GÜLER Assoc. Prof. Dr. Nuriye KOÇAK Assoc. Prof. Dr. Ahmed Nuri KURŞUNLU
The use of fluorescence sensors for the detection of metal ions is the subject of many disciplines, especially medicine, because of their high selectivity and easy applicability. The molecules capable of emission in the near-IR region have widespread use as sensors because they can easily penetrate the tissue and cause less damage to the tissue, both biologically and medically. Therefore, there are many studies on the design of compounds that can exhibit fluorescent properties and can emit near-infrared (NIR) emissions. Among these compounds, BODIPY (boron-dipyrromethene) dyes are known and capable of emitting in the near-infrared (NIR) region, which is the most widely used area. Antenna type fluorescence compounds have been developed for increasing the selectivity and the ability to transfer energy in itself. BODIPY compounds are light and chemical resistant fluorescent substances. In addition, Bodipy derivatives are used in many fields due to their superior photophysical properties such as high quantum yield, structural stability and sensitivity.
In this thesis, firstly Bodipy derivatives containing organic groups are prepared. Changes in the emission, absorption and excitation properties of these compounds were then examined in the presence of some metal ions. Thus, in these measurements, it was determined that the final Bodipy derivatives intended to be selective of metal ions were found and the compounds obtained were tested with different metal ions. However, only
vii
mercury has shown a selectivity for the metal. Compound Hg (II) can be used as a fluorescent sensor for the ion.
viii ÖNSÖZ
Tez çalışmamın yönetimini üstlenip çalışmalarımın her safhasında ilgi ve yardımlarını esirgemeyen değerli hocam Sayın Prof. Dr. Ersin GÜLER’e sonsuz saygı ve şükranlarımı sunarım.
Anorganik kimya alanındaki bilgi ve birikimi ile bu çalışmamın anorganik sentez yönünü geliştirmemde büyük desteğini gördüğüm, her konuda yönlendirici ve teşvik edici sayın hocam Doç. Dr. Ahmed Nuri KURŞUNLU ’ya sonsuz teşekkürlerimi sunarım.
Ayrıca hayatımın her bir karesinde maddi ve manevi desteğini yanımda hissettiğim anneme, babama ve kardeşlerime sevgilerimi sunar teşekkür ederim.
Emine BAĞCI KONYA-2019
ix İÇİNDEKİLER ÖZET ... iv ABSTRACT ... vi ÖNSÖZ ... viii İÇİNDEKİLER ... ix
SİMGELER VE KISALTMALAR ... xii
1. GİRİŞ ... 1
1.1. Doğadan Esinlenilmiş Yapay Fotosentez ... 3
1.1.1. Fotoelektrik Elektronik Enerji Transferi (EET) Süreci ... 3
1.1.1.1. Doğa Düzenlemeli Hafif Hasat Anten Sistemleri ... 3
1.1.1.2. Doğal ve Yapay Dizilerde EET İşleminin İncelenmesi ... 6
1.1.2. Förster Rezonans Enerji Transferi (FRET) Mekanizması ... 8
1.1.2.1. Kronik FRET ... 8
1.1.2.2. FRET Denklemindeki Parametreler ... 13
1.1.2.3. FRET'in Şartları ve Koşulları ... 14
1.1.2.4. Förster Kritik Mesafe ... 15
1.1.2.5. Oryantasyon Faktörü ... 16
1.1.2.6. Bindirme (Örtüşme) İntegrali ... 17
1.2. Enerji Transfer Kasetleri ... 17
1.2.1. Boşluk Yoluyla Enerji Transfer Kasetleri (Förster Tipi) ... 19
1.2.2. Bağ Yoluyla Enerji Transfer Kasetleri (Dexter Tipi) ... 20
1.3. Bordiflorodipirin (BODIPY) Bileşiklerinin Kimyası ... 20
1.3.1. Bodipy’lerin Özellikleri ... 22
1.3.2. İskele ... 23
1.3.3. Bor Atomunda Modifikasyon ... 24
1.3.4. Aza-Bodipy ... 25
1.3.5. Sönüm (Kuenç) ... 26
1.4. Işıkla Uyarılmış Elektron Aktarımı (PET) ... 27
1.5. Molekül İçi Yük Transferi (ICT) ... 29
2. KAYNAK ARAŞTIRMASI ... 31 3. MATERYAL VE YÖNTEM... 34 3.1. Materyal ... 34 3.1.1. Kulanılan cihazlar ... 34 3.1.1.1. Rotary evaparatör ... 34 3.1.1.2. Ultrasonik banyo ... 34 3.1.1.3. Manyetik karıştırıcılar ... 34
3.1.1.4. Erime noktası tayin cihazı ... 34
3.1.1.5. İnfrared spektroskopisi ... 35
3.1.1.6. Floresan spektroflorometresi ... 35
x
3.1.1.8. Ultraviyole-visible spektrofotometresi... 35
3.1.1.9. NMR spektrometresi ... 35
3.1.1.10. Element analiz cihazı ... 35
3.1.1.11. Kullanılan kimyasal malzemeler ... 36
3.2. Metodoloji ... 37
4. DENEYSEL BÖLÜM ... 38
4.1. 10-(4-(klorometil)fenil)-5,5-difluoro-1,3,7,9-tetrametil-5H-dipirol[1,2-c:2',1'-f][1,3,2]diazaborinin-4-ium-5-uide’ nin Sentezi ... 38
4.2. 8-(azidometil)-4,4-difloro-1,3,5,7-tetrametil-4-bora-3a,4a-diaza-s-indasen’in Sentezi ... 39
4.3. N1,N3-di(prop-2-in-1-il)izoftalamit Sentezi ... 40
4.4. Bodipy 1’in Sentezi ... 41
4.5. Bodipy 2’nin Sentezi ... 42
4.6. 1-(2-((4-(5,5-difloro-1,3,7,9-tetrametil-5H-4l4,5l4-dipirol [1,2-c:2',1'-f][1,3,2]diazaborinin-10-yl)benzil)oxy)naftalin-1-yl)-N-(2-(((2-((4-(5,5-difloro-1,3, 7,9-tetrametil -5H-4l4,5l4-dipirol [1,2-c:2',1'-f][1,3,2]diazaborinin-10-yl)benzil)oxy)naftalin-1-yl)metilen)amino)fenil) metanimin’in Sentezi ... 43
4.7. Bodipy 3’ün Sentezi ... 44
5. ARAŞTIRMA SONUÇLARI VE TARTIŞMA ... 45
5.1. Spektroskopik Uygulamalar ... 45
5.1.1. Bodipy 1 için spektroskopik uygulamalar ... 45
5.1.2. Bodipy 2 için spektroskopik uygulamalar ... 50
5.1.3. Bodipy 3 için spektroskopik uygulamalar ... 54
6. SONUÇLAR VE ÖNERİLER ... 58
6.1. Bileşiklerin Sentezi, Analizi ve Spektroskopik Uygulamalarına Dair Yorumlar 58 7. KAYNAKLAR ... 59
8. EKLER ... 62
8.1. 10-(4-(klorometil)fenil)-5,5-difluoro-1,3,7,9-tetrametil-5H-dipirol[1,2-c:2',1'-f][1,3,2]diazaborinin-4-ium-5-uide’ nin IR spektrumu ... 62
8.2. 8-(azidometil)-4,4-difloro-1,3,5,7-tetrametil-4-bora-3a,4a-diaza-s-indasen’in IR spektrumu ... 62
8.3. N1,N3-di(prop-2-in-1-il)izoftalamit’ in IR spektrumu ... 62
8.4. 1-(2-((4-(5,5-difloro -1,3,7,9-tetrametil-5H-4l4,5l4-dipirol [1,2-c:2',1'- f][1,3,2]diazaborinin-10-yl)benzil)oxy)naftalin-1-yl)-N-(2-(((2-((4-(5,5-difloro-1,3,7,9-tetrametil -5H-4l4,5l4-dipirol [1,2-c:2',1'-f][1,3,2]diazaborinin-10-yl)benzil)oxy)naftalin-1-yl)metilen)amino)fenil) metanimin’in IR spektrumu ... 62
8.5. Bodipy 2’nin IR spektrumu ... 62
8.6. 10-(4-(klorometil)fenil)-5,5-difluoro-1,3,7,9-tetrametil-5H-dipirol[1,2-c:2',1'-f][1,3,2]diazaborinin-4-ium-5-uide’ nin 1H-NMR spektrumu ... 62
8.7. 8-(azidometil)-4,4-difloro-1,3,5,7-tetrametil-4-bora-3a,4a-diaza-s-indasen’in 1H-NMR spektrumu ... 62
xi
8.8. N1,N3-di(prop-2-in-1-il)izoftalamit’ in 1H-NMR spektrumu (25 oC) ... 62
8.9. N1,N3-di(prop-2-in-1-il)izoftalamit’ in 13C-NMR spektrumu (25 oC) ... 62
8.10. Bodipy 1’in 1H-NMR spektrumu (25 oC) ... 62
8.11. Bodipy 1’in 13C-NMR spektrumu (25 oC) ... 62
8.12. Bodipy 2’nin 1H-NMR spektrumu (25 oC) ... 62
8.13. Bodipy 2’nin 13C-NMR spektrumu (25 oC) ... 62
8.14. 1-(2-((4-(5,5-difloro-1,3,7,9-tetrametil-5H-4l4,5l4-dipirol [1,2-c:2',1'- f][1,3,2]diazaborinin-10-yl)benzil)oxy)naftalin-1-yl)-N-(2-(((2-((4-(5,5-difloro-1,3,7,9-tetrametil -5H-4l4,5l4-dipirol [1,2-c:2',1'-f][1,3,2]diazaborinin-10-yl)benzil)oxy)naftalin-1-yl)metilen)amino)fenil) metanimin’in 1H-NMR spektrumu62 8.15. Bodipy 3’ün 1H-NMR spektrumu ... 62
8.16. Bodipy 3’ün 13C-NMR spektrumu ... 62
xii SİMGELER VE KISALTMALAR
Simgeler
Kısaltmalar
Bodipy : Bordipirin (Boradiazaindasen, bordipirometen) DCM : Diklorometan
MeOH : Metanol EtOAc : Etilasetat
DMSO : Dimetilsülfoksit TEA : Trietilamin
NMR : Nükleer Manyetik Rezonans IR : İnfrared spektroskopisi DMF : Dimetilformamit THF : Tetrahidrofuran BF3.Et2O : Bortriflorodietileterat
1. GİRİŞ
Çevreye ve canlılara zararlı ağır metal iyonlarının tespit ve bertarafına dair çalışmalar tıp başta olmak üzere birçok bilim dalının gözde çalışma konusudur. Bu nedenle yüksek seçicilik ve hassasiyete sahip floresans kemosensörler büyük ilgi çekmektedir. Floresans sensörler arasında biyolojik ve tıbbi olarak, dokuya kolaylıkla nüfuz edebilen ve canlı hücreye daha az hasar verdiği için Bodipy türevleri tercih sebebi olmuşlardır. Çünkü Bodipy türevleri sahip olduğu yüksek kuantum verimi, yapısal kararlılık, yüksek duyarlılık gibi üstün fotofiziksel özellikleri sayesinde birçok alanda kullanılmıştır. Öyle ki yüksek floresans şiddetleri nedeniyle çok küçük oranda kullanılmalarına rağmen tıbbi uygulamalarda yaygın olarak kullanılan porfirin gibi bileşiklere kıyasla minimum yan etkileri sahiptir. Sensör operasyonunun fotofiziksel mekanizması bağlanan grupların herbirinin yerleşimi aynı reseptör için farklı özellikler gösterebilir. Seçimliliği arttırabilmek ve kendi içerisinde enerji transferi yapabilen moleküller için anten tipi floresans bileşikler geliştirilmiştir.
Metal katyonlarının tespitinde kullanılan etkili bir floresans sensörün geliştirilmesi son yıllarda gerek kimya gerekse biyomedikal uygulamalar için önem arz etmektedir. Öyle ki ağır metal iyonları, çeşitli biyolojik sistemlerde önemli roller üstlenmelerine rağmen onların aşırı miktarı çevre için toksik etkiye sebep olabilmektedirler(Onyido ve ark., 2004). Bu nedenle metal iyonlarını algılayabilecek floresans kemosensörlerin geliştirilmesi için birçok çalışma bulunmaktadır. Sentezlenen kemosensörlerin seçici olarak iyon tanıyabilmesi ve sadece tek bir iyona hassas olması hala aşılması gereken en büyük problemlerden biridir. Eser miktarda bulunan ağır metal iyonlarının kemosensörler ve hassas floroforlar ile analizi çevre ve biyolojik uygulamalar açısından büyük önem taşımaktadır(Valeur ve Leray, 2000). Floresans sensörlerin metal iyonlarını tanıması iki temel sinyal mekanizma ile izah edilebilmektedir: foto-uyarılmış elektron transfer ve intramoleküler yük transfer (intramolecular charge transfer, ICT)(Lippert ve ark., 1961b).
Şekil 1.1. Foto-uyarılmış elektron transferi (PET) mekanizması
Intra-moleküler yük transferi (ICT) mekanizması elektron reseptör grupları ile metal iyonları etkileşime girdiği zaman, bu grupların karakteristik elektron çekici özelliğinin artması ile izah edilebilir. Bu nedenle absorpsiyon maksimumunda kırmızıya kayma ve molar absorpsiyon katsayısında artış gözlenir. Bu bileşiklerin floresans spektrumlarında da paralel kaymalar gözlenir.
Floresans görüntüleme (imaging) ve floresans tespiti (detection) gibi floresans teknolojileri özellikleri sağlık ve biyokimyasal materyal biliminde vazgeçilmez hale gelmiştir. Çok çeşitli floroforlar arasında Bodipy bileşikleri onun yüksek molar absorpsiyon katsayısı ve floresans kuantum verimi, yüksek pik şiddetli dar emisyon bandı, yüksek kimyasal kararlılık, birçok çözücüde kolay çözünürlük, nanosaniyede floresans yaşam ömrü, yakın infrared bölgeye kayan emisyon bandı gibi güzide özelliklerinden dolayı son on yılda bilim otoritelerinin ilgisini çekmeyi başarmıştır(Coskun ve Akkaya, 2006). Kolay modifiye edilebilen aktif uçları sebebiyle Bodipy bileşiklerine fonksiyonlandırma görevlisi (post-functionalization) olarak nitelendirilmiştir(Ulrich ve ark., 2008). Bu sebeple Bodipy’ler katyon hassasiyeti, elektronik anahtar, fotodinamik terapi, organik güneş hücresi, ışık yayan diyot ve organik alan elektronik transistör gibi pek çok uygulama alanında etkin bir şekilde kullanılmaktadır(ATILGAN, 2009; Mashraqui ve ark., 2010; Hu ve ark., 2012). Konjuge olarak dizayn edilmiş bir çok Bodipy türevi için absorpsiyon ve emisyon bandında kırmızıya kaymalar tespit edilmiştir(Karolin ve ark., 1994; Loudet ve Burgess, 2007).
Bodipy içeren bileşiklerin modifikasyonu için cross kapling, kondensasyon reaksiyonu flor atomlarının elektrofilik substiitasyon gibi farklı sentetik stratejileri geliştirilmiştir. Bunun için Bodipy çekirdeğinin değişik pozisyonlarına (2-6, 3-5 veya 8)
farklı fonksiyonel gruplar bağlanmıştır. Şüphesiz farklı pozisyonlara bağlanan grupların içerisinde donör atomların sayısının fazla olması sensör çalışmaları arzu edilen en önemli etkendir(Ziessel ve ark., 2007). Azot atomu içeren makro moleküllerde oluşan koordine kovalent bağ kompleks yapıların kararlılığını artırmaktadır. Bu konunun yeni orijinli ve güncel oluşu sebebiyle henüz substitue olmamış birçok Bodipy türevi mevcuttur.
Gelecekte bu metotlara alternatif olabilecek floresan özellik gösterebilen moleküler problar çok yönlü olarak çalışabildikleri, hassas oldukları ve kantitatif tayin yapabildikleri için, bu moleküllerin kullanımı gün geçtikçe yaygınlaşmaktadır.
1.1. Doğadan Esinlenilmiş Yapay Fotosentez
1.1.1. Fotoelektrik Elektronik Enerji Transferi (EET) Süreci
1.1.1.1. Doğa Düzenlemeli Hafif Hasat Anten Sistemleri
Doğanın güneş ışığını kimyasal olarak depolanmış enerjiye çevirme verimliliği, birçok bilim insanının araştırma çabalarına ilham kaynağı olmuştur. Bu araştırma alanı genellikle “yapay fotosentez” olarak adlandırılır. Fotosentez yoluyla, doğal sistemler ışık enerjisini elektrokimyasal enerjiye toplar, yoğunlaştırır ve dönüştürürler. Enerji, adenosin trifosfat ve diğer bileşiklerde depolanabilen ve karbonhidrat bazlı canlı organizmalar tarafından kullanılan kimyasal potansiyel enerjiye dönüştürülür.
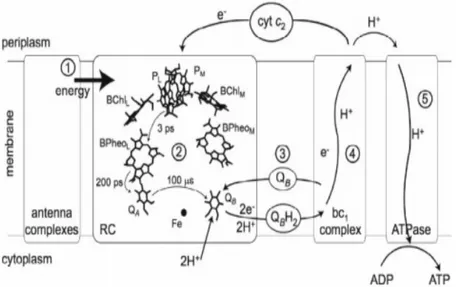
Çoğu yeşil bitki ve okyanus algleri gibi fotosentetik türler, güneş enerjisini doğrudan klorofil pigmentleri ile emilebilir. Porfirin grubu, enerji hasatı ve fotonik enerji depolama görevini tamamlamak için gerekli olan moleküllerden biridir. Enerji dönüşüm süreçlerinin yanı sıra periplazmik boşluk içindeki klorofil pigmentleri ve sitoplazmik membranın yapısı aşağıdaki şekilde gösterilmiştir.
Şekil 1.2. Periplazmik boşluk içindeki klorofil pigmentleri ve sitoplazmik membranın yapısı
Fotosentezin temel çalışması.
1: Reaksiyon merkezine uyarılmış enerji transferi 2: Reaksiyon merkezi içinde yük ayırma
3: Reaksiyon merkezinden salınan indirgenmiş hidrokinon QBH2
4: Hidrokinonun oksidasyonu ve membran boyunca bir proton gradyanının başlangıcı 5: ATPase'deki ADP'den proton gradyanı tarafından yönlendirilen ATP sentezi.
Klorofil molekülleri tarafından toplanan fotonlar rezonans enerjisi transferini başlatır ve enerji klorofil molekülü dizileri boyunca aktarılır. Enerji iletim kanalında, başlangıçta yakalanan güneş enerjisi, elektron taşınması ve fotofosforilasyon yoluyla reaksiyon merkezi protein kompleksinde depolanır. Uyarma üzerine, iki elektron fotosistem II'den kaybolur ve mobil taşıyıcı molekül plastokinon QB'ye aktarılır.
Stromadan iki proton, QB tarafından toplanır ve bu işleme, su moleküllerinin (hidrojen
iyonları gradyanı oluşturan) ve moleküler oksijenin ayrılması eşlik eder. Elektronlar daha sonra mobil taşıyıcı plastosiyanin üzerinden Fotosistem I kompleksine transfer edilir, burada elektronlar tekrar fotonlar tarafından enerjilenir ve ferredoksin-NADP-redüktaz (FNR)’e transfer edilir. Daha sonra Calvin-Benson döngüsü (karbon dioksit fiksasyonu ve indirgenmesini içeren fotosentetik karanlık reaksiyonlar) sırasında, iki elektron ve bir hidrojen iyonu NADPH üretmek için NADP + 'ya eklenir. Elektron taşıma zinciri, hidrojen iyonu gradyan, ATP sentezi ile ATP'yi oluşturmak için ADP ve Pi’ye yardımcı olmuştur. Mekanizma, mitokondride ATP sentez yoluna benzemektedir.
ATP ve NADPH, biyolojik enerji kaynağı olarak faaliyet gösteren şeker üretimi sürecinin bir parçasıdır.(Barber ve ark., 1986).
Bitkilerin ışık hasat kompleksinin kristal yapıları ve okyanusal fototropik proteobakteriler, 90’larda belirlenmiştir (Chang ve ark., 1991; Law ve ark., 2004). . Fotosentez sisteminin temel bileşenleri, ligant hasat anteni (LH2), reaksiyon merkezi (LH1-RC) ve şarj rekombinasyon bölgesidir. Aşağıdaki fotosistem II'nin (LHC-II) bitki ışık hasat pigment-protein kompleksinin şematik görüntüsüdür (Şekil 1.3).
Şekil 1.3. Mononerde hafif hasat LHC-II sisteminin çizimi (Andrews ve ark., 2011).
Enerji transfer yolu ve zaman ölçeği kıvırcık oklarda belirtilmiştir. Yeşil: enerji alıcı Chl-a molekülü
Mavi: diğer Chl-a molekülü Turuncu: Chl-b molekülü Kahverengi: bağlı çapa proteini.
Enerji aktarımı, yüksek verimlilik derecesine sahip bitişik anten komplekslerinden (LHII) reaksiyon merkezine (LH1) doğru yönlendirilir. Her transfer aşaması enerjinin yönlendirilmiş taşınmasını sağlayan ve aksi takdirde reaksiyon merkezine enerji verme oranını büyük ölçüde azaltabilecek rastgele bir yürüyüş sürecini önleyen bir enerji gradyanına tabidir. Şekil 1.4.'de okyanusal fototropik yaratık Rhodopseudomonas acidophila’da ışık toplama anteni ve reaksiyon merkezi içinde elektron transferi, rezonans enerji transferi ve enerji geçiş yolları gösterilmiştir.
Şekil 1.4. Rhodopseudomonas acidophila’ da elektronik enerji transferi ve enerji geçişi yollarının çizimi. (Choi ve ark., 2004).
Bağlı pigment proteini ile bağlanmış olan ışık toplama dizilerindeki porfirin bazlı klorofil molekülleri, fotonları toplamak için Stonehenge türünde düzenlenmiştir. Fotonlar toplandıktan sonra, bunların reaksiyon merkezine konsantre edilmeleri için bir elektronik enerji transferi (EET) işlemi gerekir. Yük ayırma reaksiyonu, kimyasal potansiyel enerjinin oluşturulduğu ve depolandığı fotosentetik membrandaki şarj rekombinasyon bölgesine nakledilen bir elektron üretir.
1.1.1.2. Doğal ve Yapay Dizilerde EET İşleminin İncelenmesi
Elektronik enerji transferinin mekanizmaları, hem doğal hem de yapay moleküler dizilerle yirmi yıldan uzun süredir araştırılmaktadır. İyi anlaşılmış mekanizma modellerinden biri, porfirin bazlı yeşil sülfür bakterisi enerji transfer kanalı, yani Fenna-Matthews-Olson (FMO) kompleksidir. FMO'nun monomerleri, protein iskelesi içine gömülmüş yedi Bakteriyoklorofili (BChl) içerir (Şekil 1.5).
Şekil 1.5. Fenna-Matthews-Olson (FMO) kompleks modelinde enerji transfer mekanizması (Deisenhofer ve ark., 1984).
Şekil 1.5. Klorofil molekülleri niteliksel olarak kaplıdır, reaksiyon merkezi 3 olarak etiketlenmiştir; Hafif hasat anteni 1, 2, 5, 6, 4, 7 olarak etiketlenmiştir. Eksito delokalizasyon modelleri renkli gölgelendirmede belirtilmiştir.
Her kromoforda, enerjilere ve geçiş anlarına karşılık gelen Hamilton ve eksitonik temel dalga fonksiyonları belirlenir. Kırmızı ve yeşil oklarla iki ana foto-eksilasyon yeniden dağıtım yolu gösterilir. Aktarım işlemi, yakın aralıklı donör-akseptör çiftleri (örn., BChl3 ve BChl7) arasında tamamen basamaklı değildir ve ara geçiş momentleri (BChl5 ve BChl6) dışarıda bırakılır.
Birçok yapay fotosentez sistemi, doğadan ilham alan tasarım ilkelerine sahiptir. Elektronik enerji transfer süreçlerinin incelenmesi, çözeltiler ve katı malzemelerde (ör., kristalli malzemeler, kuantum noktalar, metal-organik çerçeveler ve katalizörle kaplı yarı iletkenler) gerçekleştirilebilir(Benniston ve ark., 2008).Bir makalede, biyo-esinli yapay ışık-toplama anten dizilerinin ve Şekil 1.6'te temsil edilen bir güneş pili sistemi içindeki elektronik enerji transfer süreçlerinin ana bileşenleri özetlenmiştir.
Şekil 1.6. Yapay ışık hasadı anten-duyarlaştırıcı güneş pili gösterimi.
Foton hasadı ve enerji transfer verimliliği multikromofor sistemde optimize edilmiştir. Cihazın performansı, 20 mA.cm−2 ila 30 mA.cm−2 arasında kayda değer bir
ışık üreten akım yoğunluğu değeri (Jsc) ile kaydedilir. Tamamlayıcı absorpsiyon spektrumlu çoklu duyarlaştırıcılar, 400-700 nm geniş bölgesini kapsayacak bir anten etkisi yaratır (Odobel ve ark., 2013).
1.1.2. Förster Rezonans Enerji Transferi (FRET) Mekanizması
Hem doğal fotosentez sistemleri hem de yapay montajlar ile ilgili olarak, biyomühendislik ve tıbbi kimyada birçok uygulamaya sahip olan FRET- bir teori, zayıf bağlanmış kromoforlar arasındaki uyarım enerji transferinin mekanizmasını aydınlatır. FRET, uzay-içi etkileşimleri içerir ve elektron değişim etkileşimlerinin kuvvetli şekilde birleştirilmiş kromoforik diziler içinde meydana geldiği geçiş-bağı yolunu tamamlayıcıdır. Fotofiziksel ölçümler, dikkatle tasarlanmış, birbirine bağlı moleküler çift yönlü sistemler içinde, birbirlerinden bağımsız olarak incelenen ve bağlanma mekanizmaları için fırsat sağlar. Bir donör-akseptör çift moleküler sistemde enerji, elektron değişimi olmaksızın uzayda aktarılabilir. Rezonans enerji aktarımı, iki atomun veya iki moleküllü sistemin çarpışmasını gerektirmeyen ve bir fotonun emisyonu ve yeniden emilimi ile aracılık etmeyen, radyan olmayan bir işlemdir (Gilbert ve Baggot, 1991).
1.1.2.1.Kronik FRET
“Fiziğin altın çağı” ndan beri, elektronik enerji transferi (EET) ile ilgili mekanik araştırma ve pratik uygulamalar artmıştır. Rezonans enerji transferi çalışması, 20. yüzyılda başladı ve bunu yeni spektroskopik tekniklerin ortaya çıkması eşlik etti ve sonrasında ise elektromanyetik (EM) alan teorisi ve kuantum mekaniğinin (QM) araştırma geliştirme çalışmaları takip etti.
1918'de Jean Baptiste Perrin, aktivatör sensitizör sistemi içinde floresan depolarizasyon deneyleri gerçekleştirmeyi başardı. Perrin, radyasyon ve geri emilimin yanı sıra, öncelikle uyarılan molekül ve komşuları arasındaki bir enerji transferinin doğrudan bir elektrodinamik etkileşim yoluyla gerçekleşebileceğine dikkat çekmiştir. Rezonans enerji transferinin değişim bağlantı mekanizması salınımlı iki kutupludur.
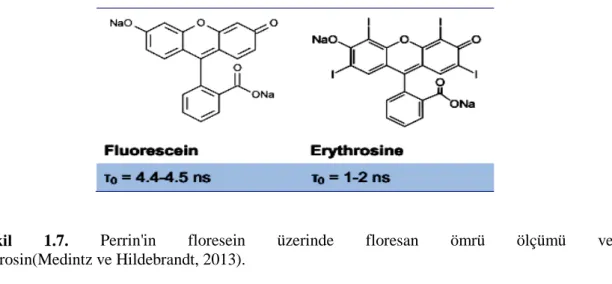
1920 yılında, floresan polarizasyon fenomeni Weigert ve Perrin (Jean Perrin'in oğlu), tarafından floresein, eritrosin, rodamin ve çözeltideki diğer boyaların ölçümü keşfedilmiştir (Şekil 1.7.). Floresan polarizasyon derecesinin yayılan türlerin hareketliliği ile ters orantılı olduğunu ve orta viskozite artışının ve sıcaklık artışının orantılı olduğunu not etmek için bir denklem çıkardılar.
Şekil 1.7. Perrin'in floresein üzerinde floresan ömrü ölçümü ve eritrosin(Medintz ve Hildebrandt, 2013).
1923 yılında floresan polarizasyonun etkisi moleküler rotasyona atfedildi ve daha sonra Vavilov ve Evshin tarafından kantitatif ölçümler yoluyla doğrulandı. Daha sonra 1926 Gaviola, faz kaymalı florometre ile H2O-gliserol içinde fluoresein ve
eritrosinin uyarılmış yaşam süresini ölçtü. Cihaz ölçek sınırı sadece bir nanosaniye doğru olmasına rağmen, sonuçlar Perrin denklemiyle uyumludur.
1925'te Franck ve 1926'da Condon, potansiyel enerji eğrileri arasında foton emilimi üzerine olası elektronik geçiş yollarını öngörmek için absorpsiyon spektrumları floresan emisyon spektrumlarını analiz etti (Şekil 1.8a). Potansiyel enerji durumları arasındaki elektronik geçiş için Franck-Condon prensibi; kuantize edilmiş nükleer titreşim modları açısından açıklanmaktadır. Uyarılmış elektronik durumun yeniden dağıtımı, foton ve elektron enerjisinin açısal dağılımına yansır.
Şekil 1.8. (a) Sol: Franck-Condon enerjisi koordinatlarının şematik gösterimi; sağ: enerji diyagramına karşılık gelen absorpsiyon ve floresan geçiş durumları. (b) Organik molekül modelinde foton absorpsiyon olayı(Adolphs, 2008).
Şekil 1.8. (b) 'ye göre, bir fotonun emilmesi üzerine, benzen 254 nm dalga boyunda ışığı emer ve bir fotonun geçmesi için gereken süre molekül aşağıdaki gibi hesaplanır:
t = 260 (nm) / 3 x 1017 (nm s-1) = 0.8 x 10-15 s
Çünkü foton absorpsiyonu femtosaniyelik zaman ölçeğinde gerçekleşir (10-15
s), ve salınım yapan elektrik alanı boyunca bir çekirdeğin titreşim hareketi içinde gerçekleştiği için, 10-13 s boyunca geçiş sırasında molekülün çekirdeğinin sabit kaldığı
düşünülebilir. Böylece elektron geçişi nükleer koordinatlara dik olarak gerçekleşir. Born-Oppenheimer yaklaşımına göre, elektronik geçişlerin olasılık ve yoğunluğu, elektronik geçiş momentinin karesel integrali ile titreşimsel örtüşmenin karesel integrali (Franck-Condon faktörü) ile orantılıdır. Büyük enerji boşluğu ayrımı ve daha iyi uyum farkı, dikey geçişler sırasında daha iyi titreşimsel örtüşme ile sonuçlanır (Şekil 1.8a).
1927 yılında Vavilov, aynı zamanda floresein spektrumundan kuantum verimini de tayin etmiştir. 1928'de dipol-dipol etkileşimi terimi Kallmann ve London tarafından yapıldı ve R0 parametresi, gaz fazındaki çeşitli atomlar arasında rezonans enerji
transferinin kuantum teorisi uygulanarak tanımlandı.
1932'de Perrin, Hallmann ve London’un teorisinden, donör floresan spektrumunun frekans ağırlıklı spektral örtüşmesinin nitel tartışması ve alıcı emilim spektrumundan esinlenerek yayınladı. Kuantum mekanik teorisi, çözelti içindeki möleküller arasındaki enerji transferinin niceliksel hesaplamasına yol açar.
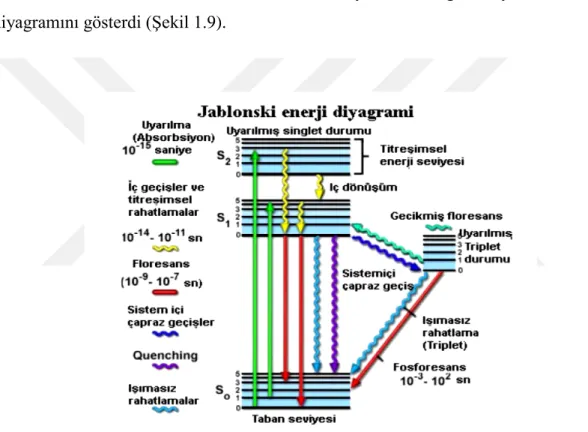
1935'te Aleksander Jablonski, olası yeniden dağıtım yollarının enerji diyagramını gösterdi (Şekil 1.9).
Şekil 1.9. Uyarma enerji yeniden dağıtım yollarının Jablonski diyagramı (Forster, 1959).
1946'da Theodor Förster, enerji transfer sürecini, esas olarak Kolombik kaplin (indüklenmiş polarizasyon) donör-alıcı içindeki dipol-dipol etkileşimlerine dayanan, indüktif rezonans transferi yoluyla, radyasyona aykırı bir işlem (elektromanyetik radyasyonla ilişkili olmayan) olduğunu belirtti.
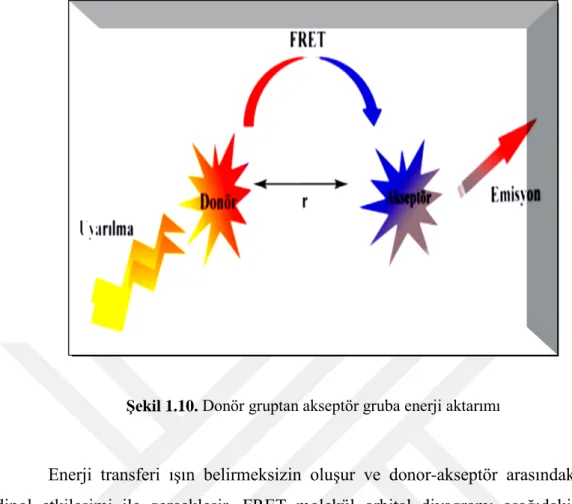
Şekil 1.10. Donör gruptan akseptör gruba enerji aktarımı
Enerji transferi ışın belirmeksizin oluşur ve donor-akseptör arasındaki dipol-dipol etkileşimi ile gerçekleşir. FRET molekül orbital diyagramı aşağıdaki şekilde verilmiştir.
Şekil 1.11. Rezonans enerji transferi için şematik molekül orbitali
İntrinsik floresan ölçümü daha sonra 1950'de yapıldı ve Kasha-Vavilov kuralını oluşturmak için fiziksel kimyager ve moleküler spektroskopist Michael Kasha
tarafından standardize edildi. Sadece ölçülen lüminesans kuantum verimi, eksitasyon dalga boyundan bağımsızdır. Ölçüm ayrıca, uyarılmış durumun yeniden dağıtılmasının foton emisyonu veya radyal olmayan süreçler yoluyla olabileceğini de açıklamıştır:
Φ=kr / ( kr+ Ʃknr ) (Denklem 1)
Floresan kuantum veriminin hesaplanması Φ üzerinden hesaplanması floresan yoluyla yayılan, fotonlara bölünen emilen fotonların denklemi ile elde edilebilir. Aynı zamanda denklemde gösterildiği gibi radyal hız sabiti (kr) ve radyal olmayan sabit hız
(knr) ile de temsil edilebilir. Uygulamada, bilinmeyen bir boyaya ait entegre emisyon
yoğunlukları, bir referans bileşik (bilinen kuantum verimine sahip kontrol floroforu) ile ilgili olarak belirlenebilir.
Uyarılmış durumun yaşam süresi, molekülün uyarılmış halde kaldığı ortalama süre ile tanımlanır. Yaşam süresi, zaman süresi ölçümlerle uyarılan durumdaki ortalama sürenin hesaplanmasıyla belirlenebilir.
90'lı yılların başında smFRET (tek moleküllü FRET) terimi, floresans mikroskobik görüntü tekniklerinin gelişmesiyle ortaya çıkmıştır (Ha ve ark., 1996).
Tek moleküllü ultra ince çözünürlükte floresans boya etiketli biyo-moleküler dinamiği izleme, biyomedikal mühendislik araştırması alanına büyük katkıda bulunur.
1.1.2.2.FRET Denklemindeki Parametreler
Förster teorisi, elektronik enerji transferi (kEET) oranı Denklem 2'de gösterildiği
gibi bir dizi parametrele ilişkili olduğunu belirtir:
(Denklem 2)
Denklem içerisinde: K2 oryantasyon faktörüdür, φD, vericinin yokluğunda
vericinin kuantum verimidir, n, çözücünün kırılma indisi, τD, vericinin yokluğunda
vericinin ömrüdir, R donördür -acceptor ayırma mesafesi (cm cinsinden) ve JF, örtüşme
integralini temsil eder (mmol-1 cm6). ΦΔ / τΔ terimi, yalnızca verici için radyasyon oranı (kRAD) olarak tanımlanır.
1.1.2.3. FRET'in Şartları ve Koşulları
Kromofor bir kuantum ışığın emisyonunu içeren elektromanyetik radyasyon kaybı yoluyla uyarılmış durumdan toprak durumuna geri dönebilir ve alıcı, ışığı yeniden emer. Radyasyon donör kısmında bir geçişli elektrik dipol momentini indüklediğinde, komşu bir alıcı kısmındakine karşılık gelen dipol momenti etkilenebilir. Ön çalışmalar, Förster tipi dipol-dipol enerji transferinin S1-S1 elektron transfer mekanizması ile
ilişkili olduğunu ortaya koymuştur (Şekil 1.12).
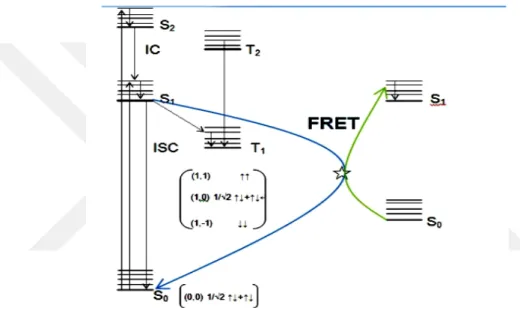
Şekil 1.12. Bir verici-alıcı arasında Förster rezonans enerji transferinin Jablonski diyagramı. Mavi çizgi, verici grubun emisyonunu bildirir, yeşil çizgi alıcı kısmın emilimini belirtir. ISC: sistem içi geçişi; IC: iç dönüşüm; S1 → S0: floresan; T1 → S0: fosforesans.
T1 → S0 veya S1 → T1 arasındaki sistemler arası geçiş (ISC) işlemine dikkat
edildiğinde elektron dönüş durumlarının değişmesini kolaylaştıran spin-yörünge kuplajı gerektirir. Bir iç dönüşüm (IC) süreci nükleer kinetik enerjiye bağlıdır (titreşimsel gevşeme). Geçiş halleri arasındaki enerji farkı genellikle: S1→ T1 <T1 → S0 <S2 → S1
<< S1 → S0; S2 → S1 arasında verimli enerji transferi fotosentezde devlet kritik öneme
1.1.2.4. Förster Kritik Mesafe
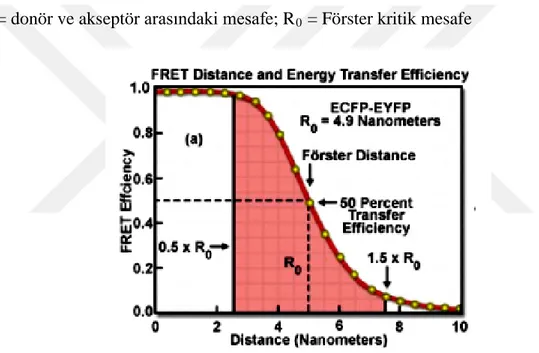
Donör- akseptör bir molekül durumunda verimli için belirli koşullar Förster tipi rezonans enerji transferinin gerçekleşmesi gerekiyor: Donör ve akseptör parçası kısa bir mesafe ile ayrılmalıdır (0.5-10 nm). Tipik durumda R0 değeri 20 ila 100 A arasında
hesaplanır. FRET teorisinde, altıncı güç (Förster) mesafesi; enerji transfer oranı tersine bağlıdır. Birçok literatür, yakın bir aralık için rapor verdi donör-akseptör, Förster mesafesi (R0) ayrılık temsil edilir oran sabit kEET = 1 / τD (τD verici ömürdür).
kEET=R60/(R6+R60)
R = donör ve akseptör arasındaki mesafe; R0 = Förster kritik mesafe
Şekil 1.13. FRET mesafesi ve enerji transfer verimliliği (Kremers ve ark., 2006).
Förster kritik mesafesi (R0) merkezden merkeze uzaklık olarak ölçüldü. Donör
ve akseptör arasında bir parametrenin donör-akseptör çifti ve enerji transferinin mesafesini temsil eder. Verimlilik maksimumun %50'sidir. Bu, çeşitli parametrelerle ilgilidir aşağıdaki Förster denkleminin alternatif versiyonunda gösterilmiştir:
(n: kırılma indeksi; ΦD: donörün flüoresansının kuantum verimi; bindirme integrali son terimlerdir; κ2
: oryantasyon faktörü)
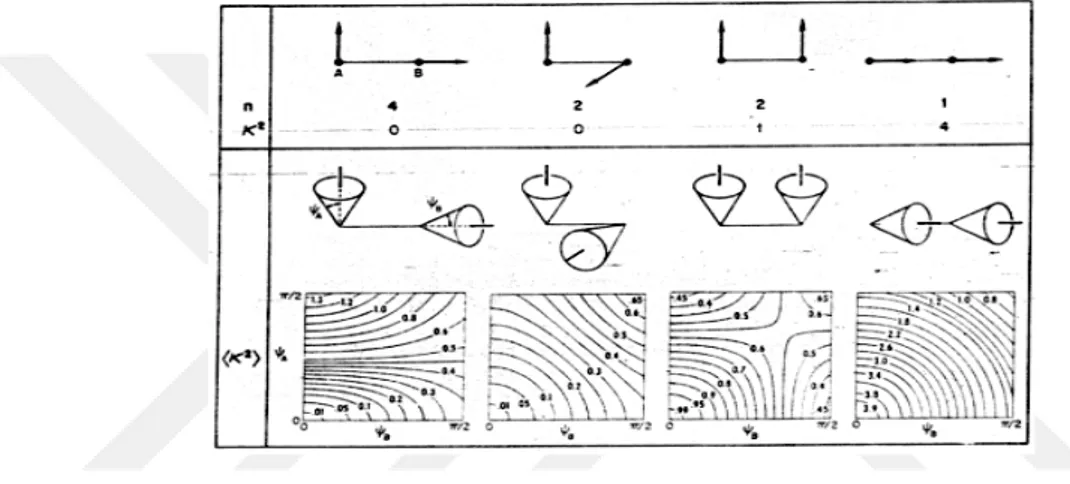
1.1.2.5.Oryantasyon Faktörü
Floresan dipollerin açısal hizalanması ve donör ve akseptör parçaların uzamsal düzenlemesi, κ2
oryantasyon faktörü ile temsil edilir. Klasik bir elektrikli yakın alan Hertzian dipol modeli aynı zamanda bir FRET geçişi dipol çiftinin kuantum mekanik türevli Hamiltoniyenini de temsil edebilir (Şekil 1.14).
Şekil 1.14. Hertzian dipol hizalamalarında oryantasyon faktörü (Eisinger ve ark., 1970).
Enerji transfer verimliliği, donör ve akseptör kısımları arasındaki geçiş momenti vektör dipollerinin göreceli molekül içi oryantasyonuna bağlıdır (Şekil 1.15).
1.1.2.6.Bindirme (Örtüşme) İntegrali
Örtüşme integrali J (λ) terimi aşağıdaki denklemle verilir:
FD (λ): donörün entegre floresan spektrumu
εA(λ): akseptörün molar decadic absorpsiyon katsayısı
Spektrumların örtüşmesi, enerji aktarımının daima ileri olmasını sağlamak için kritik öneme sahiptir. (donörden akseptöre). Bu nedenle, Stokes vardiyası tarafından oluşturulan molekül içi titreşimsel yeniden dağılım (IVR) nedeniyle geri transfer genellikle önlenir. İleri enerji aktarımı için örtüşme integrali değeri genellikle geri transfer için karşılık gelen örtüşme integralinden daha büyüktür ve akseptörün uyarıcı durumu, her zaman donörün uyarılmış durumundan daha düşük enerjidedir (Gilbert ve Baggot, 1991).
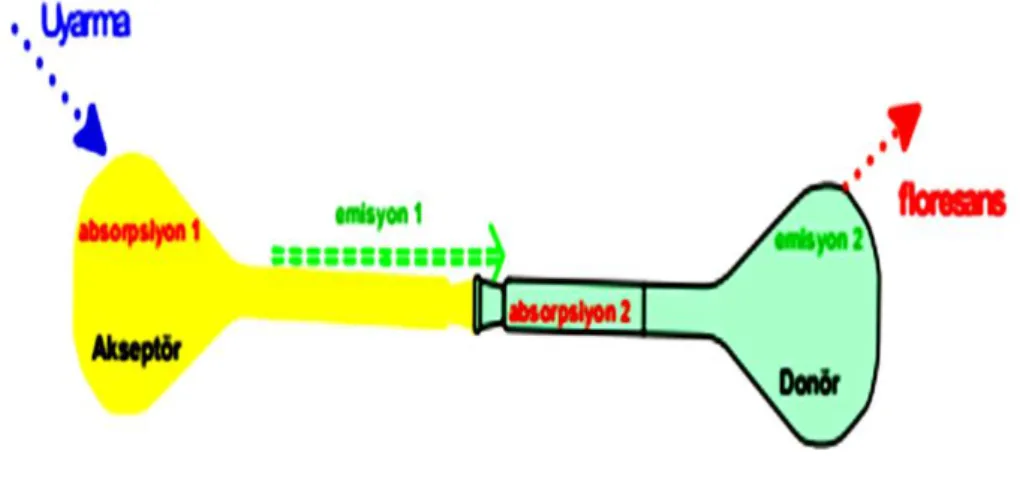
1.2.Enerji Transfer Kasetleri
Boya sistemlerinde, radyasyonsuz elektronik enerji transferin de emisyon yoğunluklarını geliştirmek üzere kullanılmıştır. Bu özellikleri gösteren sistemler, absorbe eden bir donör boyanın, enerji transferi daha uzun dalga boylarında olan floresan bir akseptöre göre daha kısadır. Bu sistemlerin, en uygun donör ve akseptör bileşenleri, enerji transfer kasetleri gibi tek bir başlık altında incelenmektedir.
Deneysel olarak, bu tür sistemlerin hazırlanmasında en uygun yöntem, donör ve alıcı bileşenlerin bir enerji transfer kasetinde tek bir birim halinde bir araya getirilmesidir(Barin ve ark., 2009).
Şekil 1.16. Enerjinin aktarımı
Bir enerji transfer kaseti iki veya ikiden fazla floresan grubun (donör ve akseptör) aynı moleküle bağlanmasıyla oluşmaktadır. Donör gelen ışığı absorplar, akseptöre doğru enerji geçişi gözlenir ve daha uzun bir dalga boyunda ışık yayılımı gözlenir. Bu enerji transferi boşluk yoluyla (Förster tip) ve bağ yoluyla (dexter tip) gerçekleşir, bu mekanizma aşağıdaki şekilde görüldüğü gibidir:
1.2.1. Boşluk Yoluyla Enerji Transfer Kasetleri (Förster Tipi)
Boşluk yoluyla enerji transferinin verimini etkileyen faktörler şunlardır: donör emisyonu ile akseptör absorbansının spektral örtüşmesi,
donör ve akseptör arasında ki mesafeye,
donör ve akseptörün arasındaki relatif yönlenmesi,
diğer relaksasyon modları (örneğin, donörün emisyonu, ışımasız prosesler vb. gibi koşullara bağlıdır).
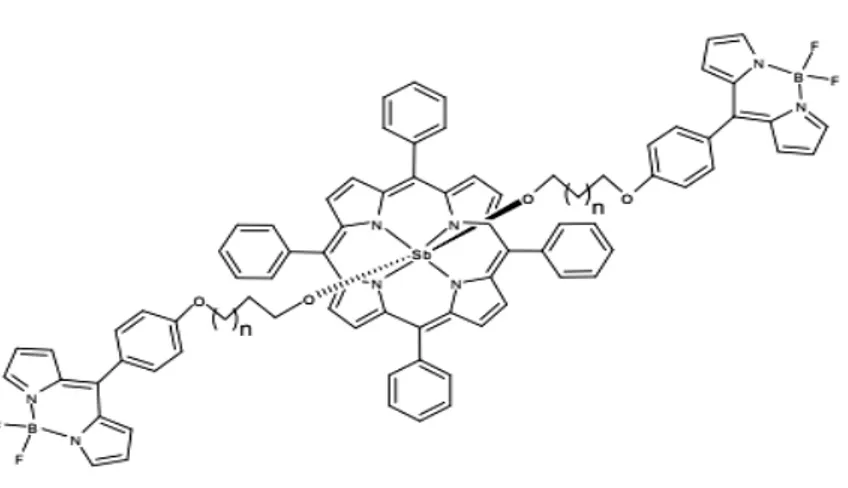
Enerji transfer kasetleri sentezlerinde BODIPY boyalarının floresan şiddetlerinin yüksek olmasından dolayı çok fazla tercih edilmektedir. Genellikle, tek bir floresans boya molekülünde çok küçük bir Stokes’ kayması vardır. Tek başına bir boyanın Stokes kayması belirli bir uygulama için yetersiz olduğu durumda, iki boya arasındaki boşluk yoluyla enerji transferi iki veya daha fazla kromoforik sistemler sık sık kullanılabilmektedir. Boşluk boyunca enerji transferinde donör florofor yerine akseptörden gelen emisyonla molekülünü yüzeysel olarak artan Stokes kayması etkilemektedir. Buna örnek olarak 8-(4-hidroksifenil)-BODIPY, boşluk yoluyla enerji transfer kaseti oluşturmak için alkil zinciri vasıtasıyla bir antimonil tetra-fenilporfirin (Sb(TPP)) ile koordine edilir. Bu madde için verim %13-40 arasında değişir. Fakat alkil zinciri uzadığında verimin azaldığı bulunmuştur. Bodipy burada donör olarak davranır ve bu sebeple Bodipy enerjisinin verilmesi ile uyarılmış halinin sönümlenmediği bulunmuştur.
1.2.2. Bağ Yoluyla Enerji Transfer Kasetleri (Dexter Tipi)
Akseptör ve donör, eğer çoklu olan bağın konjuge sistemine katılırsa bağ boyunca enerji transferi gerçekleşir. Fakat burada boşluk boyunca enerji transferinde olduğu gibi üst üste gelen spektrumlar (donör floresansı ile akseptör absorbansının üst üste gelen spektrumları) gerekmemektedir. Eğer ki akseptör ve donör çoklu bağın konjuge sistemine katılırsa bağ boyunca enerji transferi gerçekleşir.
Bağ boyunca gerçekleşen enerji transferini etkileyen temel faktörler şunlardır: HOMO-LUMO karakteristiği,
akseptör ve donör arasındaki bağın tipi, sterik etkileşim,
bağlanma yönü olabilir.
Förster mekanizmasının tersine, konjuge multi kromoforik sistemlerde ne kadar enerji transfer edildiğini tespit etmek mümkün değildir. Yine de toplam enerji transferi ölçülebilir.
1.3. Bordiflorodipirin (BODIPY) Bileşiklerinin Kimyası
Dipirometen ligandlarının bor atomu ile yaptığı bileşikler “bordipirometen” veya kısaca BODIPY (BOronDIPYrromethene) bileşikleri olarak adlandırılır.
N HN dipirometen N B N F F bordipirometan çekirdegi Şekil 1.19. Dipirometen ve Bordipirometan çekirdeği
4,4-difloro-4-bora-3a,4a-diaza-s-indasen (BODIPY) boyalarının önemi son 20 yılda önemi hızla artmıştır. Treibs ve Kreuzer (1968) ilk Bodipy boyasını rapor etmiştir. Daha sonra ise birçok farklı Bodipy boyası sentezlenmiş ve farklı uygulamada kullanılmıştır. Bu boyalar organik çözücülerdeki çözünürlükleri çok iyidir fakat suda
çözünmez veya çok az çözünen moleküllerdir. Bileşiklerin kuantum verimleri, çözücünün polaritesine ve benzen halkasına bağlanan Bodipy ünitesinin bağlanma tipine bağlı olarak değişir.
1
2
4
5
6
7
8
3
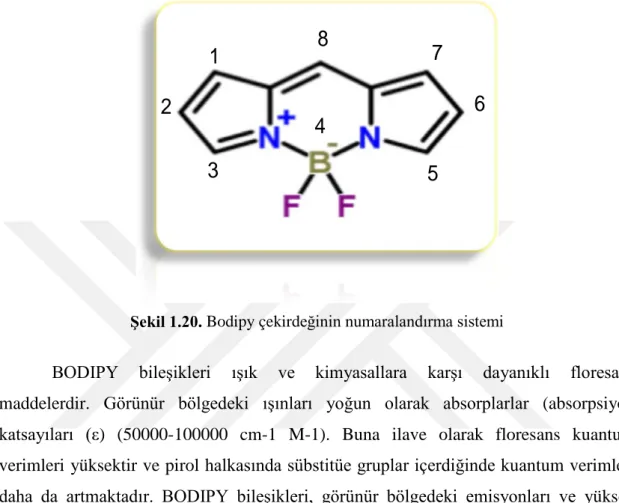
Şekil 1.20. Bodipy çekirdeğinin numaralandırma sistemi
BODIPY bileşikleri ışık ve kimyasallara karşı dayanıklı floresans maddelerdir. Görünür bölgedeki ışınları yoğun olarak absorplarlar (absorpsiyon katsayıları (ε) (50000-100000 cm-1 M-1). Buna ilave olarak floresans kuantum verimleri yüksektir ve pirol halkasında sübstitüe gruplar içerdiğinde kuantum verimleri daha da artmaktadır. BODIPY bileşikleri, görünür bölgedeki emisyonları ve yüksek kuantum verimleri nedeniyle, florofor maddeler arasında yer almaktadırlar.
Son on yılda, yeni biyomedikal ve optoelektronik teknolojilerin ortaya çıkması, ayarlanabilir lazerler, biyomoleküller ve hücre görüntüleme için floresan işaretleyiciler, ışığa duyarlı maddeler, ışık yayan cihazlar, kimyasal sensörler ve çeşitli uygulamalar gibi BODIPY tabanlı amfifilik bileşiklerin ilgisini arttırdı (Machado ve ark., 2019)
BODIPY çekirdeği, çözücü ve pH’a bağlı olarak absorpsiyon ve emisyon değerlerinde önemli değişiklikler göstermemektedir. Ancak BODIPY çekirdeğine bağlanan sübstitüe gruplar ile bu çekirdek arasında elektron aktarımı bulunması halinde, bu grubun fotofiziksel özelliklerinin değiştiği bilinmektedir. BODIPY çekirdeğine donör/akseptör özelliği bulunan fonksiyonel gruplar bağlanarak, asit-baz ve anyon/katyon indikatörleri olarak kullanılmak üzere birçok BODIPY bileşiği sentezlenmiştir. BODIPY bileşikleri akıllı devre anahtarları, ışık toplama sistemleri,
enerji transfer kasetleri, boyar madde ile duyarlaştırılmış güneş pilleri, polimerler, lazer boyaları ve OLED uygulamalarında kullanılırlar (Loudet ve ark., 2011).
Başka grupların Bodipy kromoforlarının fotofiziksel özelliklerine etkisini araştırmak için yönlendirici pirolik ünitelerinden çeşitli Bodipy’ler sentezlenmiştir. Uzun konjuge yapılar Bodipy’lerin absorpsiyonla emisyon maksimumlarını kırmızıya doğru kaydırmıştır. Elektron çekici ve verici grupların aril gruplarının farklı pozisyonlarına bağlanmasıyla fotofiziksel özellikleri büyük oranda etkilemiştir. N BOC Br (I)ArBr(OH)2,Na2CO3,Pd(PPh3)4 5:1toluen,MeOH
(II)NaOMe, MeOH, THF, r.t. NH
Ar BODIPY
Şekil 1.21. Pirol ünitesinin ön-fonksiyonlandırılışı
1.3.1. Bodipy’lerin Özellikleri
BODIPY bileşikleri, floresan özellikleri nedeniyle genellikle biyomoleküllerin hücre içinde etiketlenmesinde ve fotodinamik terapide etkin ilaç olarak kullanılma potansiyeline sahiptirler. Ftalosiyaninler ise yüksek dalga boyundaki ışığı absorplayabilmeleri (yaklaşık 700nm), yüksek triplet hal kuantum verimleri ve triplet halde uzun ömürleri, ışık kullanılmadığında toksik etki göstermemeleri ve etkin olarak singlet oksijen üretebilmeleri nedeniyle fotodinamik terapide kullanılabilecek hedef bileşiklerdir.
BODIPY boyaların en önemli özelliklerinden biri, moleküler omurgayı değiştirerek, optik özelliklerinin değiştirilebilmesidir. Bu Bodipy boyalar keskin absorbsiyon bantlarına, yüksek floresans kuantum verimlerine, iyi çözünürlüğe, çözücü içinde ya da katı durumda kimyasal ve fotokimyasal olarak dayanıklı olmaları ve enerji transferi yapabilme özelliğine sahiplerdir (Dost ve ark., 2006).
Ayrıca, çok iyi ısı ve fotokimyasal stabiliteye sahiptirler. Fiziksel koşullar da oldukça kararlı bileşikleridir, bulundukları ortamın pH ve polaritesinden pek etkilenmezler. BODIPY boyaların diğer avantajları ise basit sentez yöntemleri, organik çözücüler içinde iyi çözünebilmesi ve dar emisyon bandına sahip olmalarıdır.
BODIPY’lerin fotokimyasal özellikleri, emisyon ve uyarılma dalga boyları gibi modifikasyon yoluyla kolaylıkla ayarlanabilir (Gräf ve ark., 2013).
BODIPY ve pek çok türevi görünür bölgede absorbsiyon ve emisyon (500 - 700 nm) yapmaktadır. Temel hali singlet (S0) olan BODIPY’nin floresansının S1 halinden
kaynaklandığı düşünülmekte (ki pek çok organik kromofor için olağan durum budur) ve S1’in popüle edilmesinin de basit bir HOMO → LUMO elektron geçişi olduğu varsayılmaktadır (López Arbeloa ve ark., 2005).
1.3.2. İskele
1968'de Treibs ve Kreuzer öncüleri boradiazaindacene florofor bileşiklerini sentezlemeyi başardı(Treibs ve Kreuzer, 1968).Sentetik yöntem, 2,4-dimetilpirolün bir elektrofilik sübstitüsyonunun asetik anhidrit ile ikame edilmesi ve BF3.Et2O ile Lewis
asidi olarak katalize edilmesiyle tarif edildi ( Şekil 1.22).
N H BF3.Et2O (CH3CO)2O N H O N H NH N N N B F F Ac N N B F F Ac Ac
Şekil 1.22. Treibs ve Kreuzer tarafından geliştirilen Bodipy sentezinin elektrofilik ikame yolu.
Alternatif bir reaksiyon, bor trifluoroteheratın ara dipirometana şelatlamak ve pirol grubundaki protonu çıkarmak için trietilamin benzeri bir organik baz kullanılmaktadır. Bu yöntemi kullanarak, % 40-% 70 arası verimlerdeki bir dizi F-BODIPY boyası hazırlandı (Şekil 1.23.).
NH N R3 R1 R4 R 2 R1 N N R3 R1 Me R4 R 2 R1 Me B F F BF3Et2O Et3N
Şekil 1.23. Treibs ve Kreuzer tarafından geliştirilen Bodipy sentezinin baz katalizli yolu.
1.3.3. Bor Atomunda Modifikasyon
Çeşitlilik odaklı Bodipy modifikasyonunun yeni kapsamı, etinil-lityum reaktiflerini kullanarak iki florin atomunu değiştirmektir. Asetilen, tolil, naftil, pirenil, fluorenil ve terpiridinil kısımları gibi bu tip kimya gruplarının kullanılması bor merkezine dahil edilebilir. Bordan fazladan ekstrapolasyon ile "E-Bodipy" sistem ailesini inşa etmek mümkündür. Alkil-lityum Grignard reaktiflerinin reaksiyon durumu ılımlıdır ve Bodipy çekirdeğinin mezo pozisyonundaki fonksiyonel grupları (örneğin feniletinilpiren, piren ve 4'-terpiridin) tolere eder. B-F değiştirme ürünü çok kararlıdır, bu yüzden çoklu kromoforik sistemler yapı için ideal bir sentetik protokoldür (Harriman ve ark., 2009).
Bir enerji transfer kaseti sistemi, bir Bodipy çekirdeğinin borunu ve bağlı bir Bodipy'nin meso pozisyonunu bağlayan fonksiyonelleştirilmiş 1,4-fenilen-dietilen etilen oligomer tekrarlayan birimlerle sentezlendi; bağlı Bodipy ayrıca bor atomunda modifiye edilmiş asetilendi ve piren kalıntıları (Şekil 1.24). Bir fotofizik çalışması, konjügasyon uzunluğu bağımlılığını ve intramoleküler elektronik enerji transferi üzerindeki köprü aracılı etkisini doğruladı.
1.3.4. Aza-Bodipy
Azadipirrometen, cumen veya izopropil alkol varlığında kalkonlara nitrometan ilave edilerek hazırlanabilir ve amonyum asetat ile katalize edilir. BF2 ünitesinin
şelasyonu ve intramoleküler fenolik oksijen-flor yer değiştirmesi, bir benzo (1,3,2 )oksazaborin yoğunlaştırılmış aza-Bodipy'nin oluşması ile sonuçlanır. (Şekil 1.25). Yakın kızılötesi (NIR) bölgeyle (yani, 700-1000 nm) eşleşen ve böylece in vivo moleküler görüntüleme probları gibi yeterli B-O şelatlı aza-Bodipy bileşikleri yapan 688-782 nm civarında bir emisyon rapor edilmiştir (Loudet ve ark., 2008).
BODIPY / aza-BODIPY boyalarının işlevselliğini zenginleştirmek için yapı inovasyonu ve modifikasyonu anahtar içeriktir. Bu yüzden birçok grup, dikkatlerini BODIPY/aza-BODIPY’ lerin yeni yapılarını tasarlamaya ve sentezlemeye adamıştır(Jiang ve ark., 2017).
Şekil 1.25. B-O şelatlı aza-Bodipy sistemi örneği.
Aza-BODİPYler güçlü UV soğurma özelliklerine sahiptirler ve yüksek kuantum verimleriyle oldukça keskin floresans yapmaya meyilli moleküllerdir. Bulundukları ortamın pH ve polaritesinden çok etkilenmeyen ve fizyolojik koşullarda oldukça kararlı
bileşiklerdir. Yapılarındaki küçük değişikliklerle floresans karakteristikleri değiştirilebilir.
Aza-BODİPYlerin en önemli özelliği yakın kızıl ötesi (NIR) bölgesinde (700-1100 nm) soğurma yapabilmeleridir. Bu aralıkta soğurma yapabilen boyaların en önemli kullanım alanı görüntüleme sistemleridir.
1.3.5. Sönüm (Kuenç)
Kuenç (engelleme, söndürme) metodunun prensibi, floresans türlere ait floresans emisyonunun analit tarafından söndürülmesidir. Bunun sonucunda da analit konsantrasyonu artarken floresans şiddeti düşer (Floresans, floresent türlerin analit ile kimyasal bir reaksiyon vererek bozulmasından dolayı azalır).
Şekil 1.26. Floresent türlerin analit ile kimyasal bir reaksiyon
Çarpışmalı Sönüm (Dinamik)
Çarpışmalı sönüm olayı uyarılmış bir florofor, temel hale ışımasız geçişleri kolaylaştırabilen bir atom veya molekülle reaksiyona girdiği zaman meydana gelir. Yaygın söndürücüler: O2, I-, Cs+ ve akrilamit
Statik Sönüm (Kompleks oluşumu)
Florofor ile söndürücü yeni bir kompleks oluşturur.
1.4. Işıkla Uyarılmış Elektron Aktarımı (PET)
Işıkla uyarılmış elektron trasferi (Photoinduced electron transfer, PET) foton enerjisi ile uyarılmış elektronun BODIPY bileşiğinde bir gruptan diğer bir gruba geçişe neden olmaktadır. Bu geçiş, BODIPY çekirdeğinden sübstitüent doğru olabileceği gibi sübstitüentten BODIPY çekirdeğine doğru da olabilir.
Işıkla uyarılmış elektron transferi floresans sönümlemeden sorumludur. Bu durum genellikle doğal olaylarda gerçekleşir ki ışın-etkili yük ayrılması esasına dayanan güneş enerjisinin dönüşümü için yapay sistemlerde ve fotosentez olayında çok önemlidir.
Işıkla uyarılmış elektron transfer sönümlemenin doğası ile ilgili pek çok araştırma yapılmıştır. Florofor uyarıldığı zaman elektron akseptörü olarak davranır. Buna elektronca zengin bir bileşik olan Dimetilanilin örnek verilebilir. Burada bu bileşik polinükleer aromatik hidrokarbonlara elektron verilebilir ve elektron akseptörü olarak davranır (Kumbhakar ve ark., 2004). PET sönümleme aynı zamanda uyarılmış florofordan sönümleyiciye doğru elektron transferi ile de gerçekleşebilir.
Şekil 1.27. Oksidatif ve redüktif PET için molekül orbital diyagramları
Yükseltgen PET mekanizmasının olabilmesi için ise BODIPY çekirdeğine bağlı sübstitüentin LUMO enerji seviyesinin BODIPY çekirdeğinin HOMO ve LUMO enerji seviyelerinin arasında olması gerekmektedir. Bu durumda BODIPY çekirdeği uyarıldığı zaman uyarılan elektron temel singlet haline geçmek yerine sübstitüent’in boş LUMO enerji seviyesine geçer. Sonuçta floresansın olabilmesi için temel şart olan uyarılmış singlet durumdan temel singlet hale geçme durumu olmadığı için floresans sönümlenir. İndirgen ve yükseltgen PET mekanizmalarında BODIPY çekirdeğine bağlı sübstitüent’in elektron çekme ya da verme kabiliyeti büyük önem taşır. Mezo (8) konumunda bulunan fenil grubunda alkil ya da alkoksi grupları gibi elektron veren grupların bulunduğu durumda indirgen PET, nitro gibi elektron çekici grupların bulunduğu durumda ise yükseltgen PET mekanizmaları olur.
Şekil 1.28. İndirgen ve yükseltgen elektron aktarımı
1.5.Molekül İçi Yük Transferi (ICT)
Elektron verebilen grup içeren florofor (örneğin; amino) elektron çekici bir gruba bağlandığında ışıklı uyarma üzerine donörden akseptöre molekül içi yük transferi gerçekleşir. Dipol momentteki bu değişim bir Stokes kayması ile neticelenir ki temel olarak bu floroforun mikro çevresine bağlıdır. Elektron verici grup (ligand) ile metalin koordinasyonu floroforun fotofiziksel özelliklerini değiştirecektir. Çünkü kompleksleşen katyon molekül içi yük transferinin etkinliği değiştirmektedir.
BODIPY çekirdeğinin elektron verici olarak davrandığını belittirkten sonra eğer; elektron verici bir grubun BODIPY grubuna (donör) bağlı olduğu yapı proton (H+
) ya da geçiş metalleri gibi katyonlarla etkileşirse, elektron veren grubun donör özelliği azalır ve bu konjugasyonun azalmasına neden olur.
PET
Floresans ya çok azdır ya da yoktur. Elektron delokalizasyonuna bağlılığı azdır.
Daha çok nitel analizlerde kullanılır.
ICT
Floresans hep vardır ancak stokes kaymaları görünür. Elektron delokalizasyonu önemlidir.
2. KAYNAK ARAŞTIRMASI
Treibs ve Kreuzer tarafından Bodipy ilk olarak 1968 yılında sentezlenmiştir. Daha sonra fotodinamik terapi için ajan, ışık toplama sistemleri, enerji transfer kasetleri, boyar madde ile duyarlaştırılmış güneş pilleri, metal katyonları için kemosensör, polimerler, kemosensör alanında aktif florofor, lazer boyalar gibi pek çok alanda çalışılmıştır. Özellikle Bodipy türevleri ışık altında polar çözücülerde görünür bölge moleküller arası elektron transfer mekanizmalarında anten bileşik olarak görev alır.
Diğer yandan elektron akseptör gurupları ile hedef iyonlar etkileşime girerse, bu gurupların karakteristik elektron çekici özelliği artar. Bu yüzden absorpsiyon spektrumunda kırmızıya kayma ve molar absorpsiyon katsayısında artma gözlenir(Şekil 2.1.). Bu bileşiklerin floresan spektrumlarında da aynı yönde ve prensipler altında
kaymalar gözlenir. D A D A Kirmiziya Kayma Hedef Bilesigi Eklemeden Once Hedef Bilesigi Ekledikten Sonra
Elektron Akseptor Grupla Etkilesim
Şekil 2.1. Foto-uyarılmış yük transferlerinde gözlenen spektral kırmızıya kayma (Suzuki ve Yokoyama, 2015).
Bu gurup moleküller de gözlenen geçişler, moleküllerin sahip oldukları açısal yönelmelerine göre farklı bir grup olan Twisted intra-moleküler yük transferi (TICT) altında sınıflandırılabilirler. Twisted intra-moleküler yük transferi 1961 yılında Lippert ve arkadaşları tarafından önerilmiştir (Lippert ve ark., 1961a). Twisted intra-moleküler yük transferi bir elektron donör(D)/akseptör(A) moleküldeki yük transferleri sayesinde meydana gelir. D ve A yan gurupları, karşılıklı olarak birbirleri ile dikey durumdadırlar bu da D ve A arasında elektronik ayrılmaya (decoupling) neden olur. Daha sonra hedef iyonun kemosensör yapı içerisine katılması ve sensörün geometrisinde gözlenen
değişimler molekülün floresan özelliklerinde de değişime yol açar ve sensör aktif hale geçer. Bu değişimlerin olabilmesinde elektron transfer derecesi ve moleküler geometrideki değişim önemli bir faktördür ve bu değişimlerin olabildiği moleküllerin tasarımının zor olması bakımından bu tür sensörlere nadir olarak rastlanmaktadır (Şekil 2.2) Guclu Floresans D A D Hedef Bilesik Eklenir D A TICT Floresans gozlenmez
Şekil 2.2. Twisted intra-moleküler yük transferi şeması
Azadipyrromethene’ler kırmızı bölgede absorpsiyon yapabilen mavi kromoforlar olarak bilinirler. İlk aril sübstitüe edilmiş azadipyrromethene ligandı 1940 yılında Rogers tarafından sentezlenmiştir (Şekil 2.3. A) (McDonnell ve O'Shea, 2006). O’Shea ve ark. 2004 yıllında bu bileşiklerin sentez yöntemlerini modifiye ederek yeni azadipyrromethenes ligandları ve bu bileşiklerin BF2 kelatlı Şekil 2.3. B komplekslerini
sentezlemişlerdir. Yeniden literatürlere tanıtılan bu bileşiklerin dipyrromethane ve porfirin iskeletine olan yapısal benzerliği ve zengin fotofiziksel özellikleri birçok araştırmacının bu moleküllerle ilgili çalışma yapmasının ana sebeplerinden biri olmuştur(Gorman ve ark., 2004). NH N N N N N B F F Ph Ph Ph Ph Ph Ph Ph Ph A B
Azadipyromethan ligandı, ligandarın bor ve metal komplekslerinin X-Ray dataları incelendiğinde distal fenil kollarının sübstitüe edilen guruplara bağlı olarak açılıp kapandığı, gözlenmiştir. Serbest ligantta distil guruplarına ait fenil karbonları arasındaki uzaklık 3.885 Å iken bor komplekslerinde bu uzaklık 3.996 Å’a yükselmiş, iridyum komplekslerinde bu mesafe 3.516 Å’ a kadar düşmüştür. Distil guruplara ait bu fleksibilite sayesinde Şekil 1.31. B de bahsedilen ligandların büyük yarıçaplı civa atomu için sensör olarak davranması beklenen bir durumdur (Coskun ve ark., 2007; Maity ve ark., 2013). Önerilen proje kapsamında Tip I ligandlara bağlı hidroksil guruplarının yengeç kolları gibi davranarak distil fenil gurupları arasına metal iyonları hapsetmesi beklenmektedir. Moleküllerin iyon seçiciliklerinin bu kollar arasında bulunan boşluğa, distil kolların hareket kabiliyetine ve substitüe edilen guruplara bağlı olarak değişmesi beklenmektedir (Şekil 2.4.) (Cheng ve ark., 2014).
3. MATERYAL VE YÖNTEM
3.1.Materyal
3.1.1. Kulanılan cihazlar
Bileşiklerin sentezi, yapılarının aydınlatılması ve absorpsiyon-emisyon-eksitasyon özelliklerinin incelenmesinde kullanılan cihazlar ve kullanım amaçları aşağıda belirtilmiştir. Cihazların birçoğu Selçuk Üniversitesi Fen Fakültesi Kimya Bölümü Spektroskopi Laboratuvarları ve Anorganik Kimya Araştırma Laboratuvarından temin edilmiştir. Ayrıca bazı sentezler yurt dışında ki bir üniversite laboratuvarında gerçekleştirilmiştir. Yapılan analizlerin hangi sebeple ve nerede gerçekleştirildiği aşağıda belirtilmiştir.
3.1.1.1.Rotary evaparatör
Saf ürün kazananımı sırasında özellikle kolon kromoğrafisi uygulamalarında çözücüyü tekrar kazanmak için Heidolph marka bir rotary evaporatör kullanılmıştır.
3.1.1.2.Ultrasonik banyo
Ligand ve metal iyon çözeltilerinin hazırlanmasında Kudos 53 kHz marka bir ultrasonik banyo kullanılmıştır.
3.1.1.3.Manyetik karıştırıcılar
Ara ürünlerin ve son ürünlerin sentezinde kullanılmak üzere Velp marka manyetik karıştırıcılı ısıtıcılar kullanılmıştır.
3.1.1.4.Erime noktası tayin cihazı
Sentezlenen bazı bileşiklerin erime noktaları kapiler tüplerde Gallenkamp marka erime noktası tayin cihazı kullanılmışır.
3.1.1.5.İnfrared spektroskopisi
FT-IR spektrumları Selçuk Üniversitesi Fen Fakültesi Kimya Bölümü’nde bulunan Bruker Fourier Transform Infrared FTIR (ATR) spektrofotometresi ile kaydedilmiştir.
3.1.1.6.Floresan spektroflorometresi
Emisyon ve eksitasyon ölçümleri Selçuk Üniversitesi Fen Fakültesi Kimya Bölümü’nde bulunan Perkin Elmer LS 55 spektroflorimetre cihazı ile gerçekleştirilmiştir.
3.1.1.7.Vakum pompaları
Çözeltilerde bulunan çözücülerin uzaklaştırılması için iki farklı vakum pompası kullanılmıştır.
3.1.1.8.Ultraviyole-visible spektrofotometresi
Uv-vis spektrumları Selçuk Üniversitesi Fen Fakültesi Kimya Bölümü’nde bulunan Perkin Elmer Lambda 25 Uv-vis spektrofotometresi ile kaydedilmiştir.
3.1.1.9.NMR spektrometresi
1
H-NMR, 13C-NMR, 11B-NMR, 19F-NMR ve 1H-COSY-NMR spektrumları Selçuk Üniversitesi Fen Fakültesi Kimya Bölümü’ nde bulunan Varian 400 MHz bir spektrometresi ile gerçekleştirilmiştir.
3.1.1.10. Element analiz cihazı
Molekülde bulunan C, N ve H atomlarının element analizleri, Tübitak Marmara Araştırma Merkezi’nde bulunan Bruker marka elementel analiz cihazında yapılmıştır.
Bazı analizler ise yurtdışında yapılan çalışmalar esasında kullanılan Bruker Elemental Analyzer marka bir elementel analiz cihazı yardımıyla gerçekleştirilmiştir.
3.1.1.11. Kullanılan kimyasal malzemeler
Kullanılan bütün kimyasal maddeler; (azidometil)fenil)-5,5-difloro-1,3,7,9-tetrametil-5H-dipirol[1,2-c:2’,1'-f][1,3,2]diazaborinin-4-ium-5-uide, 10-(4-(klorometil) fenil)-5,5-difloro-1,3,7,9-tetrametil-5H-dipirol[1,2-c:2',1' f][1,3,2]diazabor inin-4-ium-5-uide, isoftaloil diklorür, 2-propin-1-amin, N1, N3-di (prop-2-in-1-il) izoftalamid, 1,4-bis (prop-2-in-1-iloksi) benzen, benzen-1,2-diamin, sodyum azid, lityum bromür, potasyum iyodür, bakır sülfat, sodyum askorbat, potasyum karbonattır. Kullanılan metaller ise; krom (Cr (III)), kobalt (Co (II)), bakır (Cu (II)), çinko (Zn (II)), civa (Hg (II)), kurşun (Pb (II)), kadminyum (Cd (II))’ dur.
Kolon kromotoğrafisi, sentez ve karakterizasyon uygulamalarında dimetilformamid, tetrahidrofuran, diklorometan, etanol, etil asetat, petrol eteri (%40- 60), n-hekzan, kloroform, metanol, toluen, aseton, dimetil sülfoksit, dötoro kloroform, dötoro dimetilsülfoksit, dötoro metanol, asetonitril, dietileter çözücüleri kullanıldı. Reaksiyon ortamı için gerekli pirol ışık ve ısıda çok çabuk bozulduğu için her defasında distillenmiş ve taze olarak kullanılmıştır. Bununla birlikte Bodipy sentezlerinde kullanılan kuru-diklorometan özel bir düzenek ve kalsiyum hidrür yardımıyla elde edilmiştir. Saf su temini ise Selçuk Üniversitesi Kimya Bölümü’nde yer alan saf su üretim cihazı ile sağlanmıştır.
3.2. Metodoloji
Bu tezde temel olarak iki aşamada gerçekleştirilmiş olup bunlar bileşiklerin sentezi ve spektroskopik uygulamalardır. Bodipy bileşikleri genel olarak pirollerin aromatik-alifatik aldehitler veya açil halojenürlerle reaksiyonundan elde edilmektedir. R X O HN R1 R2 R3 TFA, DDQ N B N R1 R2 R3 F F R R 1 R3 R2
R: Aril, Alkil gruplar X: H, Cl R1: H, Metil R2: H, Etil R3: h, Metil Bodipy BF3EtO2
Şekil 3.1. Bodipy bileşiklerinin pirollerin aromatik-alifatik aldehitler veya açil halojenürlerle reaksiyonundan elde edilişi
Bu bilgiye bağlı olarak yapılan bu tez çalışmasında; ticari veya sentez aldehit bileşikleri ve açil halojenürler pirol veya 2,4-dimetil pirol bileşikleri ile uygun şartlarda reaksiyona tabi tutulmuş ve Bodipy grupları elde edilmiştir. Amaca bağlı olarak daha sonraki sentez işlemlerinde iki farklı metodoloji kullanılmıştır. Bunlardan ilki; metal katyon hassasiyeti (kompleksleşme) gösterebileceği düşünülen uygun organik grupların çıkış-Bodipy bileşiğine bağlanmasıyla elde edilmesidir. Diğeri ise; klasik metotla hazırlanmış olan metal kompleks bileşiklerin yine çıkış-Bodipy yapısına bağlanmasını içermektedir.
Tez çalışmasının ikinci aşamasında gerçekleştirilen spektroskopik çalışmalar yapılan iki farklı sentez metoduna bağlı olarak; birinci metotla hazırlanan fonksiyonel Bodipy gruplarının metal katyon hassasiyeti çözelti ortamında Uv-vis ve florimetrik metotlarla tespit edilmiştir. İkinci metotla hazırlanan kompleks bileşikler ise benzer şekilde Uv-vis ve florimetrik değerlerdeki değişmelerin ve bunlara bağlı olarak ışımalı enerji transfer (PET) mekanizmasının yorumlanması esasına dayanmaktadır.
Spektroskopik uygulamaların sonunda hazırlanan ligandların floresan katyon sensörü veya kemosensör olarak kullanılıp kullanamayacağının değerlendirilmesi yapılmıştır.
4. DENEYSEL BÖLÜM
4.1. 10-(4-(klorometil)fenil)-5,5-difluoro-1,3,7,9-tetrametil-5H-dipirol[1,2-c:2',1'-f][1,3,2]diazaborinin-4-ium-5-uide’ nin Sentezi
N H Cl Cl O Cl N B N F F
1
Reaksiyon 1: 10-(4-(klorometil)fenil)-5,5-difloro-1,3,7,9-tetrametil-5H-4l4,5l4-dipirol[1,2-c:2',1'-f][1,3,2]diazaborinin sentezi (1 numaralı bileşik) sentezi4- (klorometil) benzoil klorür (1.5 g, 7.9 mmol), kuru diklorometan (150 mL) içinde oda sıcaklığında ve N2 altında 2,4-dimetil pirol (1.65 mL) çözeltisine damla
damla ilave edildi. Çözelti karanlık ortamda 2 saat boyunca karıştırıldı (60 °C'de). Çözeltinin soğutulmasından sonra, kalan katıya trietilamin (TEA) (10 mL) eklendi, karışım oda sıcaklığında 30 dakika N2 altında karıştırıldı ve sonra bor trifluorür dietil
eterat (7 eşdeğeri) eklenmiştir. Çözelti, 60 °C'de 2 saat karıştırıldı ve nihai tortu, kolon kromatografısiyle (petrol eteri-EtOAc; 7: 1 oranında) saflaştırıldı ve turuncu bir katı yani 1 numaralı bileşik (10-(4-(klorometil)fenil)-5,5-difloro-1,3,7,9-tetrametil-5H-4l4,5l4-dipirol[1,2-c:2',1'-f][1,3,2]diazaborinin) elde edildi (1.75 g, Verim% 41).
FT-IR değerleri: 1640 cm-1 (C=N), 1600 1450 cm-1 (C=C), 3000- 2880 cm-1 (C-H).
(1.75 g, Verim 41%). E.N.:189 oC. 1H NMR [400 MHz, CDCl3]: 7.48 (d, 2H, ArH),
7.25 (d, 2H, ArH), 6.02 (s, 2H, Pirol-H) 5.18(s, 2H, CH2), 2.53 (s, 6H CH3) 1.25 (s, 6H,
4.2. 8-(azidometil)-4,4-difloro-1,3,5,7-tetrametil-4-bora-3a,4a-diaza-s-indasen’in Sentezi Cl N B N F F N3 N B N F F NaN3 DMF LiBr
1
2
Reaksiyon 2: 10-(4-(azidometil)fenil)-5,5-difloro-1,3,7,9-tetrametil-5H-dipirol[1,2-c:2',1'-f][1,3,2]diazaborinin-4-ium-5-uide (2 numaralı bileşik) senteziDMF (30 mL) içinde 1 nolu bileşik ( 2.3 g, 6.2 mmol), NaN3 (1.2 g, 18.6 mmol )
ve LiBr ( 0.54 g, 6.2 mmol) kanşımı manyetik karıştırıcı yardımıyla 24 saat oda sıcaklığında kanştınldı. Sonra H20 (15 mL) eklendi. Sulu tabaka etilasetat ile ekstre
edildi. Birleştirilen organik katmanlar, suyla yıkandı, MgS04 ile kurutuldu, süzüldü ve
konsantre edildi. Kolon kromatografisi ile kırmızı bir katı yani 2 numaralı bileşik (10-
(4-(azidometil)fenil)-5,5-difloro-1,3,7,9-tetrametil-5H-dipirol[1,2-c:2',1'-f][1,3,2]diazaborinin-4-ium-5-uide) halinde elde edildi. Dikkat: Yüksek azid kalıntısı nedeniyle, bu bileşik özel bir dikkatle kullanılmalıdır.
FT-IR değerleri: 1642 cm-1 (C=N), 1600-1450 cm-1 (C=C), 3000- 2870 cm-1 (C-H), 3400 cm-1 (NH),
E.N.:140 oC. 1H NMR [400 MHz, CDCl3]: 7.51 (d, 2H, ArH), 7.32 (d, 2H, ArH), 5.99
4.3. N1,N3-di(prop-2-in-1-il)izoftalamit Sentezi
Reaksiyon 3: N1,N3-di(prop-2-in-1-il)izoftalamit sentezi
İzoftaloil diklorürün (167.0 mg, 1 mmol) diklorometandaki çözeltisine 0,5 mL trietilamin -5 °C’de (tuz-buz) eklendi. Daha sonra 0.4 mL propargilamin bu çözeltiye damla damla oda sıcaklığında ilave edildi ve 48 saat karıştırıldı. Karışım DCM-su karışımında ekstrakte edildi ve ham ürün organic faza çekildi. Organik faz MgSO4 ile
kurutulup çözücü vakumda uçuruldu. Ham ürün kolonda saflaştırıldı (Petrol eteri 40-60%/EtOAc; 1:1). Beyaz bir katı elde edildi.
FT-IR değerleri: 2800-3000 cm-1 (C-H), 1640 cm-1 (C=N), 1596-1448 cm-1 (C=C), 1682 cm-1 (C=O), 3370-2900 cm-1 (NH) Verim: %81. 1H-NMR [400 MHz, DMSO]: 9.07 (2H, t, J = 5.51 Hz), 8.34 (1H, t, J = 1.61 Hz), 8.02–7.95 (2H, m), 7.56 (1H, t, J = 7.75 Hz), 4.10-4.08 (4H, m), 3.15 (2H, t, J = 2.49 Hz);13C NMR [100 MHz, DMSO]:d(ppm); 165.6, 133.8, 129.9, 128.3, 126.1, 80.9, 72.6, 28.