iv T.C.
SELÇUK ÜNİVERSİTESİ FEN BİLİMLERİ ENSTİTÜSÜ
Sideritis ozturkii Aytaç&Aksoy TÜRÜNÜN SİTOTOKSİK ETKİSİNİN BELİRLENMESİ
Emine GELİNCİ YÜKSEK LİSANS BİYOLOJİ ANABİLİM DALI
YÜKSEK LİSANS/DOKTORA TEZİ
……… Anabilim Dalını
Kasım-2018 KONYA Her Hakkı Saklıdır
TEZ BİLDİRİMİ
Bu tezdeki bütün bilgilerin etik davranış ve akademik kurallar çerçevesinde elde edildiğini ve tez yazım kurallarına uygun olarak hazırlanan bu çalışmada bana ait olmayan her türlü ifade ve bilginin kaynağına eksiksiz atıf yapıldığını bildiririm.
DECLARATION PAGE
I hereby declare that all information in this document has been obtained and presented in accordance with academic rules and ethical conduct. I also declare that, as required by these rules and conduct, I have fully cited and referenced all material and result that are not original to this work.
EMİNE GELİNCİ Kasım 2018
v ÖZET
YÜKSEK LİSANS
Sideritis ozturkii Aytaç & Aksoy TÜRÜNÜN SİTOTOKSİK ETKİSİNİN BELİRLENMESİ
Emine GELİNCİ
Selçuk Üniversitesi Fen Bilimleri Enstitüsü Biyoloji Anabilim Dalı
Danışman: Dr. Öğr. Üyesi Hakkı DEMİRELMA 2018, 74
Jüri
Dr. Öğr. Üyesi Hakkı DEMİRELMA Prof. Dr. Tuna UYSAL
Doç. Dr. Hatice BAŞ
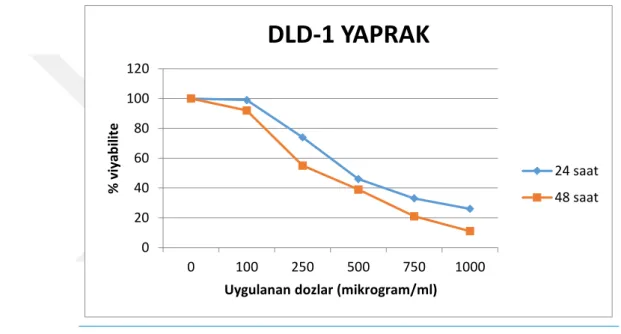
Türkiye endemiği Sideritis ozturkii Aytaç&Aksoy türünün çiçek ve yaprak kısımlarından elde edilen metanol ekstreleri RPMI-1640 besiyerin de kültüre edilen insan kolorektal kanser hücreleri, DLD-1 üzerine farklı konsantrasyon ve zamanlarda uygulanmıştır. MTT kullanılarak sitotoksite ölçümleri yapılmış ve Elisa Reader kullanılarak sitotoksite indeksleri hesaplanmıştır. Elde edilen yaprak ekstraktının HPLC ile karakterizasyonu yapılarak fenolik madde bileşimleri ortaya çıkarılmıştır.
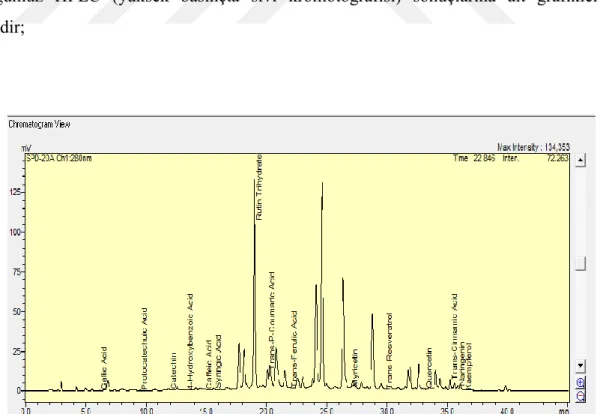
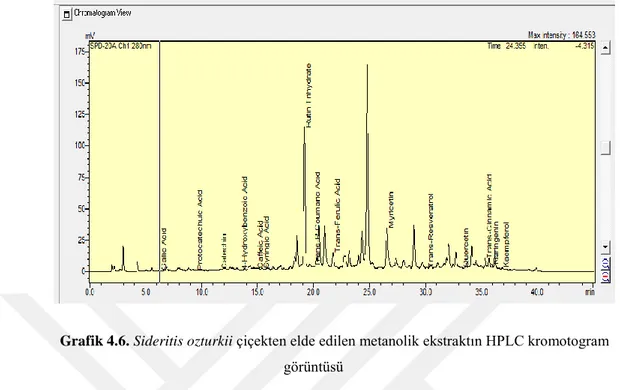
Çalışma sonucunda Sideritis ozturkii türünden elde edilen çiçek ve yaprak ekstraktlarının doz ve zamana bağlı olarak DLD-1 hücreleri üzerine sitotoksik etki gösterdiği, yaprak ekstraktının ise çiçek ekstraktından daha etkili olduğu tespit edilmiştir. Fenolik madde içeriği açısından ise yaprak ekstraktın da en fazla rutin trihidrat ve Trans-P-Coumraic Acid bulunmuştur. Sideritis ozturkii türünden elde edilen ekstraktların anti-proliferatif bir doğal ajan olarak yararlı olabileceği düşünülmektedir.
vi ABSTRACT
MS THESIS
THE DETERMINATION OF CYTOTOXIC EFFECT OF Sideritis ozturkii Aytaç&Aksoy
Emine GELINCI
THE GRADUATE SCHOOL OF NATURAL AND APPLIED SCIENCE OF SELÇUK UNIVERSITY
THE DEGREE OF MASTER OF SCIENCE IN BIOLOGY
Advisor: Asst.Prof.Dr. Hakkı DEMIRELMA
2018, 74
Jury
Asst.Prof.Dr. Hakkı DEMIRELMA Prof. Dr. Tuna UYSAL Assoc. Prof. Dr. Hatice BAŞ
The methanol extracts obtained from the flower and leaf parts of the species Sideritis ozturki Aytaç&Aksoy which is endemic in Turkey, were applied at different concentrations and for different times on DLD-1 human colorectal cancer cells cultured in RPMI-1640 medium. The cytotoxicity measurements were made through the use of MTT and the cytotoxicity indices were calculated using an Elisa Reader. The characterization of the obtained leaf extract was performed via HPLC to reveal the phenolic substance composition.
As a result of the study, it was determined that the flower and leaf extracts obtained from the species Sideritis ozturkii exhibit cytotoxic activity on DLD-1 cells in a dose- and time-dependent manner and that the leaf extract is more effective than the flower extract. As for the phenolic substance content, Rutin Trihydrate and Trans-P-Coumaric Acid were detected in the leaf extract. It is believed that the extracts obtained from the species Sideritis ozturkii could be beneficial as a natural anti-proliferative agent. Keywords: Cytotoxicity, Endemic, DLD-1, HPLC, MTT, Phenolic Substance, Sideritis ozturkii,
vii ÖNSÖZ
Selçuk Üniversitesi Fen Fakültesi Botanik Anabilim dalına bağlı moleküler bitki laboratuvarında yaptığım “Sideritis ozturkii Aytaç & Aksoy Türünün Sitotoksik Etkisinin Belirlenmesi” konulu tez çalışmamın her aşamasında bilgi ve görüşleriyle yardımlarını benden esirgemeyen değerli hocam ve danışmanım Sayın Dr. Öğr. Üy. Hakkı DEMİRELMA’ya çalışmama göstermiş oldukları ilgi ve desteklerinden dolayı değerli hocalarım Sayın Prof. Dr. Tuna UYSAL ve Prof. Dr. Hüseyin DURAL’a çalışmama başladığım ilk günden beri destek ve görüşlerini benden esirgemeyen Dr. Ela Nur ŞİMŞEK SEZER’e, Selçuk Üniversitesi Fen Fakültesi çalışanlarına, yüksek lisansa başladığım ilk günden beri benden desteklerini esirgemeyen ilgili herkese teşekkür ederim.
Ayrıca beni bu yola sevkeden ve destekleyen rahmetli babam Aziz GELİNCİ ’ye, bugünlere ulaşıncaya kadar her zaman yanımda olan, sevgi ve desteklerini bir an olsun esirgemeyen bana vermiş oldukları güven ve destekten dolayı varlıklarını her zaman hissettiğim canım annem Seher GELİNCİ ve ablam Sema GELİNCİ’ye, manevi destekleri ve sevgileri ile her zaman yanımda olan Dr. Tuğba YILMAZ, Hilal ÖNATEŞ, Nazlıcan HOŞGİT ve Sema SAYAN’a, bana inanan ve destekleyen tüm akrabalarıma, hocalarıma ve arkadaşlarıma sonsuz sevgi ve teşekkürlerimi sunuyorum.
Emine GELİNCİ Konya/2018
viii İÇİNDEKİLER ÖZET ... v ABSTRACT ... vi ÖNSÖZ ... vii İÇİNDEKİLER ... viii SİMGELER VE KISALTMALAR ... x 1. GİRİŞ ... 1 2. KAYNAK ARAŞTIRMASI ... 3 2.1. Kanser ... 3 2.1.1. Kolorektal Kanser ... 13 2.2. Sitotoksisite ... 22 2.2.1 MTT Yöntemi ... 24 2.3. Tıbbi Bitkiler ... 24 2.3.1. Endemik Bitkiler ... 33
2.3.2. Lamiaceae Familyasının Genel Özellikleri ... 33
2.3.3. Sideritis L. Cinsinin Genel Özellikleri ... 34
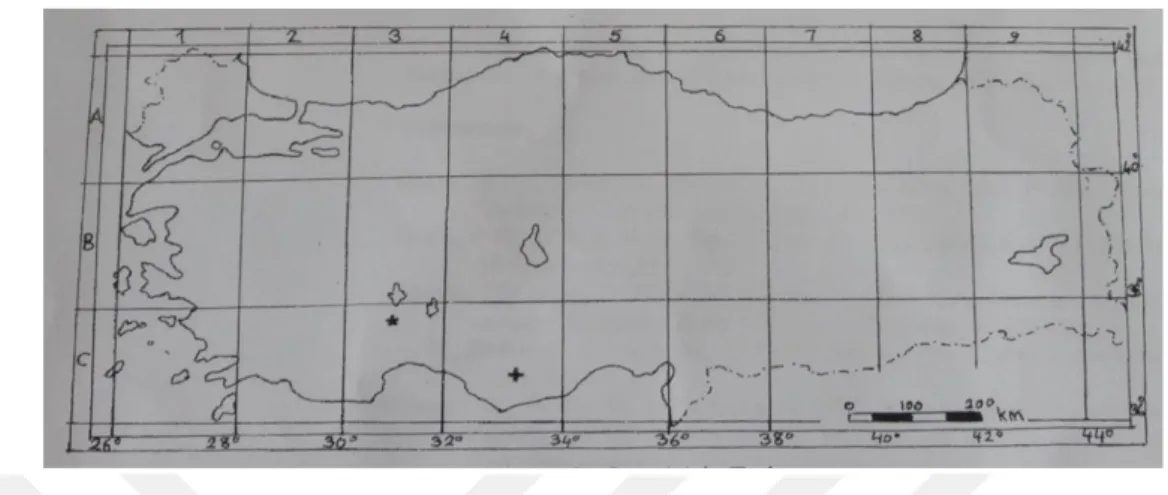
2.3.4. Sideritis ozturkii Aytaç & Aksoy Türü ... 35
2.4. Bitkisel Ekstrakt Hazırlama Yöntemleri ... 37
2.4.1. Ekstraksiyon ... 37
3. MATERYAL VE YÖNTEM ... 38
3.1. Materyal ... 38
3.1.1. Materyal eldesi ... 38
3.1.2. Kullanılan Hücre Hattı ... 38
3.1.3 Kullanılan kimyasal maddeler ... 38
3.2. Yöntem ... 38
ix
3.2.2. Hücre kültürünün hazırlanması ... 39
3.2.3. Etkin konsantrasyonların hazırlanması ... 40
3.2.4. Hücre sayımı ... 40
3.2.5. Hücrelerin testler için hazırlanması ... 41
3.2.6. MTT testi ... 41
3.2.7. Yüksek Performanslı Sıvı Kromatografisi (HPLC) ... 42
4. ARAŞTIRMA SONUÇLARI VE TARTIŞMA ... 43
4.1. Sonuçlar ... 43 4.1.1. MTT Testi Sonuçları ... 43 4.1.2. HPLC Sonuçları ... 46 4.2. Tartışma ... 49 5. SONUÇLAR VE ÖNERİLER ... 54 5.1. Sonuçlar ... 54 5.2. Öneriler ... 54 KAYNAKLAR ... 55 ÖZGEÇMİŞ ... 73
x SİMGELER VE KISALTMALAR Simgeler % : yüzde °C : santigrat derece cm2 : santimetrekare mm2 : milimetrekare µg : mikrogram mg : miligram µl : mikrolitre ml : mililitre Kısaltmalar
ABD : Amerika Birleşik Devletleri APC : Adenomatozis polipozis koli ATCC : Amerikan tipi kültür koleksiyonu BT : Bilgisayarlı tomografi
CRC : Kolorektal kanser/Colorectal cancer DLD-1 : İnsan kolorektal adenokarsinom hücre hattı
DMSO : Dimetil sülfoksit DNA : Deoksiribonükleik asit EDTA : Etilen diamin tetra asetik asit ELISA : Enzim bağlantılı bağışıklık testi
FBS : Fetal dana serumu
FDA : Gıda ve ilaç idaresi/Food and Drug Administration FOBT : Dışkıda gizli kan testi/Fecal occult blood test FOLFOX : Folinik asit, Fluorourasil ve Oksaliplatin
FOLFIRI : Kolorektal kanserin tedavisi için kemoterapi diyetidir. FOLFOXIRI : Folinik asit, 5-florourasil, oksaliplatin ve irinotekan FITC : Fluoresen-5-izotiyosiyanat
xi
HPLC : Yüksek performanslı sıvı kramotografisi/ High Performance Liquid Chromatography
HNPCC : Herediter Non-Polipozis Kolorektal Kanser HL-60 : Promyelositik lösemi hücre hattı
IARC :Uluslararası kanser araştırmaları ajansı
IUCN : Uluslararası doğa ve doğal kaynakları koruma birliği IC50 : Hücre canlılığını %50 inhibe eden konsantrasyon
M.Ö. : Milattan önce
M.S. : Milattan sonra
MRG : Manteyik rezonans görüntüleme
MTT : 3-(4,5-dimetiltiazol-2-il)-2,5-difenil tetrazolyum bromür NSAID : Non-steroidal anti-inflamatuar ilaçlar
PBMC : Periferik kan mononükleer hücreleri PET : Pozitron emisyon tomografisi
RPMI-1640 : Roswell Park Memorial Enstitüsü- 1640 sıvı besiyeri SATB2 : Özel AT bakımından zengin sekans bağlayıcı protein 2 TNM : Malign tümörlerin sınıflandırılması
UFT : Birleşik fonksiyonel test
UVB :Ultraviyole B
T4 : Tiroksin/ Tetraiyodotironin
WNT : Sinyal yolu
WHO : Dünya Sağlık Örgütü/World Health Organization WST : Hücre proliferasyonu reaktifi
1. GİRİŞ
Kanser vücudun diğer bölgelerine yayılma potansiyeline sahip hücrelerin anormal büyümeleri ile karakterize olan vücudun normal kontrol mekanizması çalışmayı durdurduğunda gelişen ve ölüme sebep olabilen bir hastalıktır. Günümüzde 100’den fazla kanser türü insanları etkilemektedir. Kanser küresel bir sağlık sorunu olup, gelişmiş ülkelerdeki ölümlerin % 9’u ve gelişmekte olan ülkelerdeki ölümlerin % 21’inin kanser kaynaklı olduğu bilinmektedir. Dünya sağlık örgütü 2050 yılı için yaptığı tahminlerde yıllık olarak yaklaşık 27 milyon yeni kanser vakasının ortaya çıkacağını ve bu vakalara bağlı olarak 17.5 milyon insanın öleceğini öngörmektedir (Hussain ve ark., 2016).
Kolon kanseri yani kolorektal kanser ise dünya da en sık rastlanan üçüncü kanser tipidir ve ölüme yol açan kanserler arasında ikinci sırada yer almaktadır. Kolon kanseri her yaşta görülebilen bir hastalık olmasına rağmen genellikle 40 yaş ve üzeri insanlarda görülme sıklığı fazladır. Tüm kanser türleri arasında görülme sıklığı kadınlarda ikinci erkeklerde ise üçüncü sıradadır (Giardiello,2014). Sağlık bakanlığı verilerine göre ise ülkemizde en sık görülen ilk beş kanser türü arasındadır. Küresel olarak her yıl bir milyondan fazla insan kolorektal kansere yakalanmaktadır. 1990 yılında yılda 490.000 kişinin ölümüne yol açtığı açıklanan kolon kanserinin 2010 yılında ise yılda 715.000 kişinin ölümüne neden olduğu açıklanmıştır. Kolorektal kanser Amerika Birleşik Devletlerin’deki erkek ve kadın ölümlerinin en büyük ikinci nedenidir. 2011 yılında Amerika’da yılda yaklaşık 141.210 vaka ve İngiltere’de ise 41.000 vaka tespit edilmiştir. Kolon kanserinin toplumda görülme sıklığında çevresel faktörlerin etmeni büyüktür. Özellikle gelişmiş ülkelerde insanların dengesiz yaşam ve yüksek yağ içeren sağlıksız beslenme alışkanlıkları kolon kanserinin görülme sıklığını artırmaktadır. Ayrıca çevresel faktörler kadar insanların genetik yatkınlıkları ve özellikleri de kolon kanserinin görülme sıklığını artırmaktadır.
Kanser vakalarının görülme sıklığındaki artış, pek çok kanser hastasının tedavisinde kullanılan kemoterapi ve radyoterapinin zamanla normal hücrelere de zarar vermesi ve hedeflenen kanser hücrelerinde direnç oluşturmasının bu tedavilerin başarı yüzdesini düşürmesi bilim insanlarını bitkilerden yeni antikanser ilaçları geliştirmeye teşvik etmiştir (Shah ve ark., 2013).
Birçok arkeolojik bulguda insanların binlerce yıldır bitkileri tedavi ve
beslenme amacı ile kullandığı görülmektedir (Koçyiğit, 2005). Bitkilerin hastalıkları tedavi etme gücüne olan inanç neredeyse insanlık tarihi kadar eskidir. İnsanlık tarihi boyunca birçok farklı formu ile bitkiler hastalıkların tedavisinde kullanılmıştır. Dünyadaki bütün kıtalarda bitkilerin tedavi amacıyla kullanıldığına dair pek çok tarihi kanıt bulunmaktadır. Bitkilerin tıbbi amaçlı kullanımını ifade eden etnobotanik alanı hakkındaki ilk yazılı bilgiler M.Ö 3000’li yıllara yani Mısır, Hitit, Grek ve Roma dönemlerine kadar dayanmaktadır (Dağcı ve ark., 2002)
M.Ö 5. yüzyılın sonlarında Hipokrates’in farklı 300-400 tıbbi bitkiden bahsettiği kitabı ve M.S 1. yüzyılda Dioskrodidas’ın ‘De Mataria Medica’ eseri modern farmakolojinin de temelini oluşturan yapıtlar olarak gösterilmektedir. Günümüzde hala bu eserlerde yer alan bitkiler ve bu bitkilerin yeni bulunan türleri geleneksel tedavide kullanılmaya devam etmektedir (Cowan, 1999).
Son yıllarda özellikle 1980’lerden sonra kimya sanayindeki hızla ilerlemeler sonucunda bitkisel ilaçların yerini sentetik (kimyasal) ilaçlar almaya başlamıştır. Ancak bu sentetik ilaçların birçok yan etkisinin ortaya çıkması ve çoğunun fiyatlarının yüksek olması nedeniyle insanlar yeniden bitkisel ilaçlarla tedavi yolunu tercih etmeye yönelmiştir (Yücel, 2010).
Anadolu’da ise tıbbi bitkilerin kullanımı ile ilgili bilgilerin kaynağı Hititler dönemine kadar dayanırken, bitkilerin tıbbi alanda şifahanelerde kullanılması Selçuklu dönemine kadar uzanmaktadır (Özbek, 2005).
Tüm dünya ülkelerinde olduğu gibi, Türkiye’de de tıbbi açıdan önemli görülen bitkiler yüzyıllardır halk arasında çay, merhem, baharat vb. şekillerde hastalıkların tedavisinde kullanılmaktadır. Günümüzde mikroorganizmaların sentetik ilaçlara karşı daha fazla direnç oluşturmaları nedeniyle doğal bitkisel ilaçlara ilgi yeniden artmıştır (Nakipoğlu ve Otan, 1992).
Bu bilgiler ışığında bu çalışma da ülkemizde de endemik olarak bulunan Sideritis L. cinsinin Konya iline endemik olan Sideritis ozturkii türünün yaprak ve çiçek kısımlarından elde edilen ekstraktların DLD-1 hücre hattı üzerindeki sitotoksik etkisinin belirlenmesi ve çağımızın hastalığı olan kanseri tedavi etme yolunda daha az yan etkisi olan ve daha etkili olabilecek ekonomik bir ilacın üretilmesine destek olmak amaçlanarak araştırma yapılmıştır.
2. KAYNAK ARAŞTIRMASI 2.1. Kanser
Kanser, hücrelerde DNA hasarı sonucu hücrelerin kontrolsüz ve anormal bir şekilde büyümesi ve çoğalmasıdır. Kanser hücreleri etraflarındaki yakın veya uzak dokulara ulaşarak kan dolaşımı, lenf sistemi, vücut boşlukları ve yüzeyleri yoluyla vücudun diğer bölgelerine yayılma özelliğine sahiptirler (Sonker ve ark, 2018).
Tütün kullanımı, kanser ölümlerinin yaklaşık % 22'sinin sebebidir (Plummer ve ark., 2016). Obezite, zayıf beslenme, fiziksel aktivite eksikliği veya aşırı alkol kullanımı da kanserden ölümlerin % 10’unu oluşturmaktadır (Plummer ve ark., 2016; Malietzis ve ark., 2016; Jayasekara ve ark., 2015). Diğer faktörler arasında belirli enfeksiyonlar, iyonlaştırıcı radyasyona maruz kalma ve çevresel kirleticiler sayılabilir (Anand ve ark., 2008). Gelişmekte olan dünyada, kanserlerin % 15'i Helicobacter pylori, hepatit B, hepatit C, insan papilloma virüsü enfeksiyonu, Epstein-Barr virüsü ve insan immün yetmezlik virüsü (HIV) gibi enfeksiyonlardan kaynaklanmaktadır (Plummer ve ark., 2016). Bu faktörler, kısmen bir hücrenin genlerini değiştirerek hareket eder (Ramagiri ve Belwal, 2018). Tipik olarak, kanser oluşmadan önce birçok genetik değişiklik gereklidir (Ramagiri ve Belwal, 2018). Kanserlerin yaklaşık % 5 ila % 10'u, bir kişinin ebeveynlerinden gelen kalıtsal genetik bozukluklara bağlıdır. Kanser belli belirti ve bulgular ya da tarama testleri ile tespit edilebilir (Plummer ve ark., 2016). Daha sonra tipik olarak tıbbi görüntüleme ile incelenir ve biyopsi ile doğrulanır (Tobin, 2012).
Pek çok kanser türü, sigara içmemek, sağlıklı bir kiloyu korumak, çok fazla alkol tüketmemek, bol miktarda sebze, meyve tüketmek, belirli bulaşıcı hastalıklara karşı aşılanmak ve çok fazla güneş ışığına maruz kalınmamak ile önlenebilir (Kushi ve ark., 2012) Tarama ile erken teşhis, servikal ve kolorektal kanser için yararlıdır (Ferlay ve ark., 2013). Meme kanserinde ise taramanın faydaları tartışmalıdır (Ferlay ve ark., 2013; Gøtzsche ve Jørgensen, 2013). Kanser genellikle radyasyon terapisi, cerrahi, kemoterapi ve hedefe yönelik tedavinin bir kombinasyonu ile tedavi edilir (Sonker ve ark., 2018). Ağrı ve semptom yönetimi tedavinin önemli bir parçasıdır (Sonker ve ark., 2018). Palyatif bakım ise kanser hastalığı ileri seviyede olan kişilerde özellikle önemlidir (Sonker ve ark., 2018). Hayatta kalma şansı, kanser türüne ve tedavinin başlangıcındaki hastalık derecesine bağlıdır (Ramagiri ve Belwal, 2018). Erken teşhiste
gelişmiş dünya ülkelerinde 15 yaşın altındaki çocuklarda beş yıllık sağ kalım
oranı ortalama % 80' dir. Amerika Birleşik Devletleri' nde kanser için, ortalama beş yıllık sağ kalım oranı ise % 66'dır (Vetter ve Stoeva, 2016).
2015 yılında yaklaşık 90.5 milyon insanda kanser hastalığı olduğu tespit edilmiştir. Yılda yaklaşık 14.1 milyon yeni vaka ortaya çıkmaktadır (Ramagiri ve Belwal, 2018) ve bunların yaklaşık 8.8 milyonu ölümle sonuçlanmaktadır (ölümlerin % 15.7'si). Erkeklerde en sık görülen kanser türleri akciğer kanseri, prostat kanseri, kolorektal kanser ve mide kanseridir (WHO, 2015). Kadınlarda en sık görülen tipler meme kanseri, kolorektal kanser, akciğer kanseri ve serviks kanseridir (Ramagiri ve Belwal, 2018). Çocuklarda akut lenfoblastik lösemi ve beyin tümörleri en yaygın olan kanser türleridir, ancak non-Hodgkin lenfoma en sık görülendir (Vetter ve Stoeva, 2016). 2012 yılında, 15 yaşın altındaki 165.000 çocuğa kanser teşhisi konmuştur (WHO, 2015). Kanser riski yaşla birlikte önemli ölçüde artmaktadır ve birçok kanser türü gelişmiş ülkelerde daha sık görülmektedir (Ramagiri ve Belwal, 2018). Gelişmekte olan dünyada daha çok insan yaşlandıkça ve yaşam tarzı değişiklikleri ortaya çıktıkça bu oranlar artmaktadır (Jemal ve ark., 2011). Kanser sonucu meydana gelen tedavi ve iş kaybı maliyetlerinin 2010 itibariyle yılda 1.16 trilyon dolar olduğu tespit edilmiştir (McGuire, 2016).
Kanser başladığında, hiçbir semptom üretmez. İşaretler ve semptomlar kitle büyüdükçe görülmeye başlanır. Sonuçta elde edilen bulgular, kitlenin türüne ve yerine göre değişir. Birkaç semptom spesifiktir. Çoğu zaman başka koşullara sahip bireylerde görülür. Kanser harika bir taklitçidir ve birçok hastalığın semptomlarını taklit etmektedir. Bu nedenle, kanser teşhisi konan kişilerin, semptomlarına neden olduğu öne sürülen diğer hastalıklar için tedavi edilmiş olması yaygındır (Kufe ve ark., 2010). Kanser teşhisi konan insanlarda endişe ve depresyon olasılığı artmaktadır ve bu belirtilerde daha sonra bir semptoma dönüşebilir. Kanserli insanlarda intihar riski normal bireylerden yaklaşık iki kat fazladır (Anguiano ve ark., 2012).
Lokal semptomlar tümörün kitleleşmesi veya ülserleşmesi nedeniyle ortaya çıkabilir. Örneğin, akciğer kanserinde oluşan kitleler bronşları bloke edebilir; özofagus kanseri, yemek borusunun daralmasına neden olarak, yutmayı zor veya ağrılı hale getirebilir; kolorektal kanser bağırsak alışkanlıklarını etkileyerek bağırsakta daralmaya veya tıkanmaya yol açabilir. Göğüsler veya testislerdeki kitleler, gözlemlenebilir
topaklar oluşturabilir. Ülserleşmeler kanamaya neden olabilir, eğer akciğer de
oluşurlarsa kanlı öksürüğe, bağırsaklarda oluşursa rektal kanamaya ve bunun sonucunda anemiye, idrar yolunda idrar yaparken kanamalara ve rahim içinde vajinal kanamaya neden olur. Gelişmiş kanser vakalarında lokalize ağrı meydana gelse de, ilk oluşan şişlikler genellikle ağrısızdır. Bazı kanserler ise göğüste veya batında sıvı birikmesine neden olabilir (Kufe ve ark., 2010).
Genel belirtiler, doğrudan veya metastatik yayılma ile ilişkili olmayan etkiler nedeniyle ortaya çıkar. Bunlar şunları içerebilir: nedensiz kilo verme, ateş, aşırı yorgunluk ve ciltte değişiklikler (O'Dell ve Stubblefield, 2009). Hodgkin hastalığı, lösemi, karaciğer veya böbrek kanserleri kalıcı ateşe neden olabilir (Kufe ve ark., 2010). Bazı kanserler, paraneoplastik sendrom olarak adlandırılan belirli sistemik semptom gruplarına neden olabilir.
Kanser vakalarının % 90-95'inden fazlası, çevresel faktörler sonucu oluşan genetik mutasyonlardan kaynaklanmaktadır (Anand ve ark., 2008). Geriye kalan % 5-10’u ise kalıtsal genetiğe bağlıdır (Anand ve ark., 2008). Kanser araştırmacıları tarafından yapılan çalışmalarda sadece kirlilik değil, yaşam tarzı, ekonomik ve davranışsal faktörler gibi genetik olarak kalıtılmayan şeylerinde kansere neden olabildiği tespit edilmiştir (Kravchenko ve ark., 2012). Kanser ölümlerine neden olan yaygın çevresel faktörler arasında tütün ürünlerinin kullanımı (% 25-30), dengesiz beslenme ve obezite (% 30-35), enfeksiyonlar (% 15-20), radyasyon (hem iyonize hem de iyonize olmayan,% 10' a kadar), stres, fiziksel aktivite azlığı ve kirlilik yer almaktadır (Anand ve ark., 2008; Islami ve ark., 2018). Belirli bir kansere neyin neden olduğunu kanıtlamak genellikle mümkün değildir, çünkü çeşitli nedenler bu belirtilere neden olabilmektedir. Örneğin, tütün kullanan bir kişi de ağır bir şekilde akciğer kanseri gelişirse, muhtemelen bunun nedeni tütün kullanımından kaynaklanmaktadır, ancak hava kirliliği ve radyasyon nedeniyle akciğer kanseri geliştirme şansı düşük olduğu için kişinin bu nedenlerle kansere yakalanmış olma ihtimalinin düşünülmesi düşük bir orandadır. Gebelikler veya ara sıra organ donörleri ile ortaya çıkan nadir bulaşma vakaları dışında, kanser genellikle bulaşıcı bir hastalık değildir (Tolar ve Neglia, 2003). Belirli maddelere maruz kalma sonucu oluşan bazı kanser türleri de vardır. Bu maddelere ise kanserojen maddeler denilmektedir. Örneğin, tütün dumanı akciğer kanserinin % 90'ına neden olur (Liao ve ark., 2014). Ayrıca, larinks, baş, boyun, mide,
mesane, böbrek, yemek borusu ve pankreasta da kansere neden olur (Kuper ve
ark., 2002a). Tütün dumanı nitrosaminler ve polisiklik aromatik hidrokarbonlar dahil olmak üzere elliden fazla bilinen kanserojen içerir (Kuper ve ark., 2002b). Tütün dünya çapında yaklaşık beş kanser ölümünden birinin sorumlusudur (Cooper, 2006). Batı Avrupa'da ise özellikle karaciğer ve sindirim sistemi kanserleri olmak üzere erkeklerde görülen kanserlerin % 10'u, kadınlarda görülen kanserlerin ise % 3'ü alkol kullanımına bağlanmaktadır.
Kanser vakalarından ölümlerin %30-35’ine ise beslenme düzensizliği, fiziksel aktivite eksikliği ve obezite neden olmaktadır (Anand ve ark., 2008; Kushi ve ark., 2006). Amerika Birleşik Devletleri'nde aşırı vücut ağırlığı (obezite) bir çok kanser türünün gelişmesi ile ilişkilidir ve kanser ölümlerinin % 14-20'sinde en etkili faktördür (Kushi ve ark., 2006). 5 milyondan fazla insanla ilgili verileri içeren bir çalışmada vücut kitle indeksinin en az 10 kanser türüyle ilişkili olduğu ve bu ülkede her yıl yaklaşık 12.000 vakadan sorumlu olduğu gösterilmiştir. Fiziksel inaktivitenin, sadece vücut ağırlığı üzerindeki etkileriyle değil, aynı zamanda bağışıklık sistemi ve endokrin sistemi üzerindeki olumsuz etkileriyle de kanser riskine katkıda bulunduğuna inanılmaktadır (Kushi ve ark., 2006).
Dünya genelinde kanser ölümlerinin yaklaşık % 18'i ise bulaşıcı hastalıklarla ilgilidir (Anand ve ark., 2008). Virüsler kansere neden olan enfeksiyöz ajanlardır. Onkovirüsler (kansere neden olabilen virüsler) insan papilloma virüsü (servikal kanser), Epstein-Barr virüsü (B-hücreli lenfoproliferatif hastalık ve nazofaringeal karsinom), Kaposi sarkom herpesvirüsünü (Kaposi sarkoması ve primer efüzyon lenfomaları), hepatit B ve hepatit C virüslerini içermektedir. Bakteriyel enfeksiyon, Helicobacter pylori ile indüklenen gastrik karsinomda da görüldüğü gibi, kanser riskini artırabilir (Pagano ve ark., 2004; Ljubojevic ve Skerlev, 2014). Kansere bağlı parazit enfeksiyonları arasında, Schistosoma haematobium (mesanenin skuamöz hücreli karsinomu) ve karaciğer parazitleri, Opisthorchis viverrini ve Clonorchis sinensis (kolanjiokarsinom) yer alır (Samaras ve ark., 2010).
İnvazif kanserlerin % 10'u, hem iyonlaştırıcı radyasyonlar hem de iyonize olmayan ultraviyole radyasyonlar dahil olmak üzere radyasyona maruz kalma ile ilgilidir (Anand ve ark., 2008). Ek olarak, invaziv olmayan kanserlerin çoğunluğu, çoğunlukla güneş ışığından kaynaklanan iyonize olmayan ultraviyole radyasyonunun
neden olduğu melanom olmayan deri kanserleridir. İyonlaştırıcı radyasyon
kaynakları, tıbbi görüntüleme ve radon gazı içerir. İyonlaştırıcı radyasyon özellikle güçlü bir mutagen değildir (Kumar ve ark., 2018). Örneğin, radon gazına maruz kalma pasif içicilik gibi benzer kanser risklerine sahiptir (Kumar ve ark., 2018). Radyasyon, radon artı tütün dumanı gibi diğer kansere neden olan maddelerle kombine edildiğinde daha güçlü bir kanser kaynağıdır (Kumar ve ark., 2018). Radyasyon vücudun birçok yerinde, tüm hayvanlarda ve her yaşta kansere neden olabilir. Çocuklar ve ergenlerde, yetişkinlere oranla radyasyona bağlı lösemi geliştirme olasılığı iki kat fazladır; Doğumdan önce radyasyona maruz kalmanın etkisi ise on kat daha fazladır (Kumar ve ark., 2018). İyonlaştırıcı radyasyonun tıbbi kullanımı radyasyon kaynaklı kanserlerin görülmesinde küçük de olsa bir etkendir. Bazı kanserleri tedavi etmek için iyonize edici radyasyon kullanılabilir, ancak bu bazı durumlarda ikinci bir kanser türünü indükleyebilir (Kumar ve ark., 2018). Güneşten ultraviyole radyasyona uzun süre maruz kalmak melanoma ve diğer deri malignitelerine yol açabilir (Brenner ve Hall, 2007). Açık kanıtlar, dünyadaki en yaygın kanser türü olan deri kanserlerinin (melanom hariç) çoğunun sebebi olarak, ultraviyole radyasyonları ve özellikle iyonize olmayan ortam dalgası UVB'yi göstermektedir (Brenner ve Hall, 2007). Cep telefonlarından, elektrik iletiminden ve diğer benzer kaynaklardan iyonize olmayan radyo frekansı radyasyonu, Dünya Sağlık Örgütü'nün Uluslararası Kanser Araştırma Ajansı tarafından olası bir kanserojen olarak tanımlanmıştır (Adekunle ve ark., 2015). Bununla birlikte, çalışmalarda cep telefonu radyasyonu ve kanser riski arasında tam olarak tutarlı bir bağlantı bulunamamıştır (Roukos, 2011).
Bazı hormonlar, hücre çoğalmasını teşvik ederek kanserin gelişmesinde rol oynarlar (Ahmad ve ark., 2009). İnsülin benzeri büyüme faktörleri ve bunların bağlanma proteinleri, kanser hücresi proliferasyonu, farklılaşması ve apoptozunda önemli bir rol oynar ve bu da karsinojenezde olası bir rol oynar (Kabel ve ark., 2014). Hormonlar, meme kanseri, prostat, yumurtalık, testis kanserleri, tiroid kanseri ve kemik kanserinde önemli ajanlardır (Ahmad ve ark., 2009). Örneğin, meme kanseri olan kadınların kızları, meme kanseri olmayan kadınların kızlarından anlamlı derecede daha yüksek östrojen ve progesteron seviyelerine sahiptir. Bu daha yüksek hormon düzeyleri, göğüs kanseri geninin yokluğunda bile, daha yüksek meme kanseri riskini açıklayabilir (Ahmad ve ark., 2009). Benzer şekilde, Afrika soyları, Avrupa soylarından daha yüksek testosteron seviyelerine sahiptir ve buna karşılık olarak daha yüksek bir prostat kanseri
düzeyine sahiptir (Ahmad ve ark., 2009). En düşük testosteron aktive edici
androstanediol glukuronid düzeyleriyle, Asya soyları, en düşük prostat kanseri seviyelerine sahiptir (Ahmad ve ark., 2009).
Kanser temel olarak doku büyüme regülasyonunun bir hastalığıdır. Normal bir hücrenin bir kanser hücresine dönüşmesi için, hücre büyümesini ve farklılaşmasını düzenleyen genler değiştirilmelidir (Axelrad ve ark., 2016). Etkilenen genler iki geniş kategoriye ayrılır. Proto-onkogenler mutasyonlar veya artmış gen ekspresyonu nedeniyle onkogene dönüşebilen, normal genlerdir. Proto-onkogenler, hücre büyümesini ve farklılaşmasını düzenleyen proteinleri kodlar. Tümör baskılayıcı genler veya tümör supresör genler normalde hücre bölünmesini engel olan genlerdir. Bu genlerin hasarı sonucunda hücre kontrolsüz büyümeye başlar. Bunun sonucunda kanser meydana gelir (Croce, 2008).
Metastaz, kanserin vücudun diğer bölgelerine yayılmasıdır. Dispersiyona uğramış tümörler metastatik tümörler olarak adlandırılırken orijinaline birincil tümör denir. Hemen hemen tüm kanserler metastaz yapabilir (Vogelstein ve ark., 2013). Kanser ölümlerinin çoğu metastaz yapmış kansere bağlıdır (Stone ve ark., 2012). Metastaz, kanserin geç evrelerinde yaygındır ve kan veya lenfatik sistem veya her ikisi yoluyla meydana gelebilir. Metastazdaki tipik adımlar lokal invazyon, kan veya lenf içine intravazasyon (kan damarı içine yabancı cisim girmesi), vücuttan dolaşım, yeni dokuya ekstravazasyon, proliferasyon ve anjiyogenezdir. Farklı tipteki kanserler, belirli organlara metastaz yapma eğilimindedirler, fakat genel olarak metastazların meydana gelmesi için en yaygın yerler akciğerler, karaciğer, beyin ve kemiklerdir (Vogelstein ve ark., 2013).
Kanserlerin birçoğu başlangıçta, belirtilerin veya semptomların ortaya çıkması veya taranması nedeniyle tanınır. Bunların hiçbiri kesin bir tanıya yol açmaz, bu da bir patolog tarafından bir doku örneğinin incelenmesini gerektirir. Şüpheli kanserli kişiler tıbbi testlerle araştırılmaktadır. Bunlar genellikle kan testleri, X-ışınları, (kontrast) BT taramaları ve endoskopi içerir. Biyopsi yapılan doku tanısı, çoğalan hücre tipini, histolojik derecesini, genetik anormallikleri ve diğer özellikleri gösterir. Bu bilgi prognozu değerlendirmek ve en iyi tedaviyi seçmek için yararlıdır. Sitogenetik ve immünohistokimya diğer doku testleridir. Bu testler, moleküler değişiklikler
(mutasyonlar, gen füzyonu ve sayısal kromozom değişiklikleri gibi) hakkında bilgi sağlar ve bu nedenle prognozu ve en iyi tedaviyi de gösterebilir.
Kanserler, tümör hücrelerinin benzediği hücre türüne göre sınıflandırılır ve dolayısıyla tümörün kaynağı olarak kabul edilir. Bu türler şunları içerir:
Karsinom : Epitelyal hücrelerden türeyen kanserlerdir. Bu grup en yaygın kanserlerin bir çoğunu içerir meme, prostat, akciğer, pankreas ve kolon kanseri gibi.
Sarkom : Bağ dokudan (yani kemik, kıkırdak, yağ, sinir) kaynaklanan ve her biri kemik iliği dışındaki mezenşimal hücrelerden kaynaklanan hücrelerden gelişen kanserlerdir. Lenfoma ve lösemi : Bu iki sınıf, kemik iliğini terk ederek sırasıyla lenf düğümleri ve kanda olgunlaşma eğilimi gösteren hematopoetik (kan oluşturucu) hücrelerden kaynaklanır (Sonker ve ark., 2018).
Germ hücre tümörü : Pluripotent hücrelerden türeyen, çoğu zaman testiste veya yumurtalıkta ortaya çıkan kanserlerdir (sırasıyla seminom ve disgerminoma).
Blastoma : Olgunlaşmamış "öncü" hücrelerden veya embriyonik dokudan türeyen kanserlerdir.
Kanseri önleme, kanser riskini azaltmak için aktif önlemler olarak tanımlanmaktadır (Varricchio, 2004). Kanser vakalarının büyük çoğunluğu çevresel risk faktörlerinden kaynaklanmaktadır. Bu çevresel faktörlerin çoğu kontrol edilebilir yaşam tarzı seçimlerinden oluşmaktadır. Bu nedenle, kanser genellikle önlenebilir bir hastalık olarak kabul edilmektedir (Dash, 2010). Kanserlerin % 70 ile % 90'ı çevresel faktörlere bağlıdır ve bu nedenle potansiyel olarak önlenebilir (Danaei ve ark., 2005). Kanserden ölümlerin % 30’ undan fazlası tütün ürünleri, aşırı kilo (obezite), zayıf beslenme, fiziksel hareketsizlik, alkol, cinsel yolla bulaşan enfeksiyonlar ve hava kirliliği gibi risk faktörlerinden kaçınmak suretiyle önlenebilir (Wu ve ark., 2016). Ancak tüm çevresel nedenler örneğin doğal olarak meydana gelen radyasyon yayılımı ve kalıtsal genetik bozukluklar gibi etkenler kontrol edilemez ve bu nedenle kişisel davranışlar yoluyla önlenebilir değildirler.
Kanser risklerini azaltmak için birçok diyet önerisi olsa da, bunları
destekleyen kanıtlar kesin değildir (Sturm, 2002; Kushi ve ark., 2012). Riski artıran birincil diyet faktörleri obezite ve alkol tüketimidir. Çalışmalar, aşırı kırmızı veya işlenmiş et tüketiminin, yüksek sıcaklıklarda pişirilen etlerdeki karsinojenlerin fazlalığından dolayı meme kanseri, kolon kanseri ve pankreatik kanser riskini arttırdığını ifade etmişlerdir (Larsson ve Alicja, 2007; Zheng ve Sang-Ah, 2009). 2015 yılında IARC, işlenmiş etin (örneğin domuz pastırması, jambon, sosisli sandviçler, sosisler) ve daha az bir dereceye kadar kırmızı etin bazı kanserler ile ilişkili olduğunu bildirmiştir (Ferguson, 2010; Wilson ve ark., 2015). Kanseri önlemek için önerilen diyetler tipik olarak sebze, meyve, tam tahıllı ürünler ve balık tüketiminin artırılması ancak işlenmiş ve kırmızı etlerden (sığır eti, domuz eti, kuzu eti), hayvansal yağlardan, salamura edilmiş gıdalardan ve rafine karbonhidratlardan kaçınılmasını içermektedir (Kushi ve ark., 2012; Sturm ve ark., 2002).
Bazı durumlarda kanseri önlemek için ilaçlar kullanılabilir (Thomsen ve Kolesar, 2008). Genel popülasyonda, NSAID' ler kolorektal kanser riskini azaltır; Aspirin' in kanserden ölüm riskini yaklaşık % 7 azalttığı bulunmuştur (Dubé ve ark., 2007). COX-2 inhibitörleri, ailesel adenomatöz polipozisli kişilerde polip oluşumu oranını azaltabilir (Rothwell ve ark., 2011). Tamoksifen veya raloksifenin günlük kullanımı, yüksek risk taşıyan kadın bireylerde meme kanseri riskini azaltmaktadır (Cooper ve ark., 2010). Vitamin takviyesi, kanseri önlemede etkili görünmemektedir (Ilic ve ark., 2006). Beta-karoten takviyesi, yüksek risk taşıyanlarda akciğer kanseri oranlarını artırır (Bjelakovic ve ark., 2014). Folik asit takviyesi kolon kanserinin önlenmesinde etkili değildir ve kolon poliplerini artırabilir (Fritz ve ark., 2011). Selenyum takviyesinin bir etkisinin olup olmadığı belirsizdir (Cole ve ark., 2007).
Bazı kanserojen virüslerin neden olduğu enfeksiyonları önlemek için ise aşılar geliştirilmiştir. İnsan papilloma virüsü aşısı (Gardasil ve Cervarix) serviks kanseri gelişme riskini azaltır. Hepatit B aşısı, hepatit B virüsü ile enfeksiyonu önler ve böylece karaciğer kanseri riskini azaltır (Vinceti ve ark., 2014).
Kemoterapinin etkinliği ise kanserin türüne ve hangi aşamada olduğuna bağlıdır. Cerrahi müdahaleler ile kombinasyon halinde kemoterapinin, meme kanseri, kolorektal kanser, pankreatik kanser, testis kanseri, yumurtalık kanseri ve bazı akciğer kanserleri gibi kanser türlerinde yararlı olduğu kanıtlanmıştır. Kemoterapinin lösemi ve bazı
kanser türleri için küratif tedavi olduğu araştırmalar ile ortaya konmuştur
(Liebert, 2008; Nastoupil ve ark., 2012). Ancak bazı beyin tümörlerinde etkisizdir (Freedman, 2012), ve çoğu cilt kanseri için ise gereksiz olduğu tespit edilmiştir (McKeith ve ark., 2005). Kemoterapinin etkinliği genellikle vücuttaki diğer dokulara olan toksisitesi ile sınırlıdır. Kemoterapi kalıcı bir tedavi sağlamazsa bile, ağrı gibi semptomları azaltmak veya ameliyatın gelecekte mümkün olabileceği ümidiyle ameliyata elverişli olmayan bir tümörün boyutunu azaltmak için yararlı olabilir.
Radyasyon terapisi, semptomları iyileştirmek amacıyla iyonlaştırıcı radyasyonun kullanılmasını içerir. Kanser dokusunun DNA'sına zarar vererek, onu öldürerek çalışır. Kemoterapide olduğu gibi, kanser çeşitlerinin radyasyon tedavisine yanıtları da değişiklik gösterir (Madan ve ark., 2010; Zachariah ve ark., 2012; Gøtzsche ve ark., 2013). Radyasyon tedavisi, vakaların yaklaşık yarısında kullanılmaktadır. Radyasyon ya dahili kaynaklardan (brakiterapi) ya da harici kaynaklardan olabilir. Radyasyon en çok cilt kanserlerini tedavi etmek için kullanılır (Janevik-Ivanovska ve ark., 2015). Radyasyon genel olarak ameliyat ve kemoterapiye ek olarak kullanılır. Ağrılı kemik metastazı için hastaların yaklaşık % 70'inde etkili olduğu bulunmuştur (Xie ve ark., 2015).
Tamamlayıcı ve alternatif kanser tedavileri, geleneksel tıbbın bir parçası olmayan çeşitli terapiler, uygulamalar ve ürünler grubudur. "Tamamlayıcı ilaç", geleneksel tıpla birlikte kullanılan yöntemlere ve maddelere atıfta bulunurken, "alternatif tıp", geleneksel tıp yerine kullanılan bileşiklere atıfta bulunur (Cassileth ve Deng, 2004). Kanser için çoğu tamamlayıcı ve alternatif ilaçlar, klinik araştırmalar gibi geleneksel teknikler kullanılarak araştırılmamış veya test edilmemiştir. Bazı alternatif tedaviler araştırılmış ve etkisiz görünmektedir, ancak hala pazarlanmaya devam etmektedir.
2008 yılında yaklaşık 12.7 milyon kanser vakası teşhis edilmiştir (melanom dışı cilt kanserleri ve diğer invazif olmayan kanserler hariç) (Jemal ve ark., 2011) ve 2010 yılında yaklaşık 7.98 milyon insan kanser nedeniyle ölmüştür (Akl ve ark., 2014). Kanserler ölümlerin yaklaşık % 13'ünü oluşturur. En yaygın olanları akciğer kanseri (1.4 milyon ölüm), mide kanseri (740.000), karaciğer kanseri (700.000), kolorektal kanser (610.000) ve meme kanseridir (460.000) (Murray ve ark., 2014). Bu veriler kanseri günümüz dünyasının önde gelen ölüm sebebi haline getirir (Jemal ve ark., 2011), 1990 yılında kanserden 5.8 milyon kişinin öldüğü rapor edilmiştir (Akl ve ark.,
2014). Ölümler, esas olarak gelişmekte olan ülkelerde daha uzun yaşam alanları
ve yaşam tarzı değişiklikleri nedeniyle artmaktadır (Jemal ve ark., 2011). Kanser gelişimi için en önemli risk faktörü yaştır (Sturm ve ark., 2002). Her ne kadar herhangi bir yaşta kansere yakalanabilse de, invaziv kanserli hastaların çoğu 65 yaşın üzerindedir (Sturm ve ark., 2002). Kanser araştırmacısı Robert A. Weinberg, "Yeterince uzun süre yaşamış olsaydık, er ya da geç hepimiz kansere yakalanırdık." demiştir.
Bazı yavaş büyüyen kanserler özellikle yaygındır, ancak genellikle ölümcül değildir. Avrupa ve Asya' da yapılan otopsi çalışmaları, insanların % 36'sının ölümleri sırasında teşhis edilmemiş ve görünüşte zararsız olan tiroid kanseri olduğunu ve erkeklerin % 80'inin 80 yaşına kadar prostat kanseri geliştirdiğini göstermiştir (De Magalhães, 2013; Baris ve ark., 2009).
Çocuklar da en sık görülen üç kanser türü lösemi (% 34), beyin tümörü (% 23) ve lenfomadır (% 12) (Kum ve ark., 2011). Amerika Birleşik Devletleri'nde kanser yaklaşık 285 çocuktan 1'ini etkilemektedir (Kaatsch, 2010). Çocukluk çağındaki kanser oranları, Amerika Birleşik Devletleri'nde 1975 ve 2002 yılları arasında yılda % 0.6 ve Avrupa'da 1978 ile 1997 yılları arasında yılda % 1.1 oranında artmıştır (Kum ve ark., 2011). Çocukluk çağında görülen kanserler nedeniyle ölümler ise, 1975'ten beri ABD'de yarı yarıya artmıştır (Kaatsch, 2010).
Birçok hastalık (kalp yetmezliği gibi) çoğu kanser vakasından daha kötü bir prognoza sahip olsa da, kanser yaygın korku ve tabular ile alakalıdır. "Uzun bir hastalıktan ve tedavi döneminden sonra" euphemizm (ölme düşüncesi) hala yaygın bir şekilde devam eder (Grange ve ark., 2002). Hatta bu nedenle Nijerya'da yerel halk, kanserden “tedavi edilemeyen hastalık” olarak bahseder (Ehrenreic, 2003).
ABD' de kanserle ilgili toplam sağlık harcamalarının 2015 yılında 80.2 milyar dolar olduğu tahmin edilmektedir (Huff ve ark., 2007). Kanserle ilgili sağlık harcamaları son yıllarda mutlak anlamda artmış olsa da, kanser tedavisine ayrılan sağlık harcamalarının payı 1960'lar ve 2004 yılları arasında % 5 civarında kalmıştır (Anonymous, 2018; Bosanquet ve Sikora , 2004). Avrupa'da ise, tüm sağlık harcamalarının yaklaşık % 6'sının kanser tedavisi için harcandığı benzer bir model gözlenmiştir (Mariotto ve ark., 2011). Tedavi harcamalarına ek olarak, kanser kayıp iş günlerine ve erken ölümlere neden olmaktadır bunun neticesin de ise üretim kayıpları
ortaya çıkmakta bu da dolaylı maliyetlere neden olmaktadır. Hatta yapılan
araştırmalar neticesinde dolaylı maliyetlerin kanserin neden olduğu sağlık giderlerini bile aştığı tahmin edilmektedir (Jönsson ve ark., 2016).
2.1.1. Kolorektal Kanser
Bağırsak kanseri ve kolon kanseri olarak da bilinen kolorektal kanser (CRC), kolon veya rektumdan (kalın bağırsağın parçaları) kanserin gelişmesidir (Lacy ve ark., 2002). Kanser, vücudun diğer bölgelerine yayılma kabiliyetine sahip hücrelerin anormal büyümesidir (Feuerstein, 2007). Belirtiler ve semptomlar dışkıda kanı, bağırsak hareketlerinde değişikliği, kilo kaybını ve her zaman yorgun hissetmeyi içerebilir (Kim, 2017).
Kolorektal kanserlerin çoğu, altta yatan genetik bozukluklara bağlı olmaktadır, az sayıda bir vaka ise yaşlılık ve yaşam tarzı faktörlerinden kaynaklanmaktadır (WHO, 2015; Hawk ve ark., 2005). Obezite, sigara ve fiziksel aktivite eksikliği risk faktörlerinden bazılarıdır (WHO, 2015; Hawk ve ark., 2005). Riski artıran diyet faktörleri arasında kırmızı ve işlenmiş etin aşırı kullanımı ile alkol bulunmaktadır (WHO, 2015; Theodoratou ve ark., 2017). Bir başka risk faktörü ise Crohn hastalığı ve ülseratif kolit içeren inflamatuar bağırsak hastalığıdır (WHO, 2015). Kolorektal kansere neden olabilen kalıtsal genetik bozuklukların bazıları ailesel adenomatöz polipoz ve kalıtsal polipsiz kolon kanseridir; ancak bunlar vakaların % 5'inden daha azını temsil etmektedir (WHO, 2015; Hawk ve ark., 2005).
Sigmoidoskopi veya kolonoskopi sırasında kolon örneğinin alınmasıyla bağırsak kanseri teşhisi konulabilir (Kim, 2017). Bu daha sonra hastalığın yayılıp yayılmadığını belirlemek için tıbbi görüntüleme ile takip edilir (Lacy ve ark., 2002). Tarama, kolorektal kanserden ölümleri önlemek ve azaltmak için etkilidir (Bibbins-Domingo ve ark., 2016). Tarama, bir dizi yöntemle, 50 ila 75 yaşından başlayarak önerilmektedir (Bibbins-Domingo ve ark., 2016). Kolonoskopi sırasında, bulunan küçük polipler çıkarılabilir (WHO, 2015). Büyük bir polip veya tümör bulunursa, kanserli olup olmadığını kontrol etmek için bir biyopsi yapılabilir. Aspirin ve diğer non-steroidal anti-inflamatuar ilaçlar riski artırır (WHO, 2015; Paleari ve ark., 2016). Bu amaçla genel kullanımları yan etkilerden dolayı önerilmez (Calonge ve ark., 2007).
Kolorektal kanser için kullanılan tedaviler, ameliyat, radyasyon terapisi,
kemoterapi ve hedefe yönelik tedavinin bazı kombinasyonlarını içerebilir (Lacy ve ark., 2002). Kolonun duvarı ile sınırlı olan kanserler ameliyatla tedavi edilebilirken, çok fazla alana yayılan kanserler genellikle tedavi edilemez ve tedavi yaşam kalitesini ve semptomları iyileştirmeye yöneliktir (Lacy ve ark., 2002). ABD'deki beş yıllık sağ kalım oranı % 65 civarındadır (Anonymous, 2016). Bireysel hayatta kalma olasılığı, kanserin ne kadar ilerlemiş olduğuna, kanserin tümünün ameliyatla çıkarılıp çıkarılmayacağına bağlıdır (Kim, 2017). Global olarak kolorektal kanser tüm vakaların yaklaşık % 10'unu oluşturan üçüncü en yaygın kanser tipidir (WHO, 2013a). 2012 yılında, 1.4 milyon yeni vaka ve hastalıktan 694.000 ölüm olmuştur (WHO, 2013a). Gelişmiş ülkelerde, vakalar % 65’den fazladır. Kadınlarda ise erkeklerden daha az görülür (WHO, 2015).
Bulgu ve semptom : Kolorektal kanserin bulgu ve semptomları, bağırsaktaki tümörün konumuna ve vücudun başka bir yerinde (metastaz) yayılıp yayılmadığına bağlıdır. Klasik uyarı işaretleri şunlardır: kötüleşen kabızlık, dışkıda kan, dışkı kalibrede azalma (kalınlık), iştah kaybı, kilo kaybı, bulantı ve kusma (Alpers ve ark., 2008). Özellikle 40 yaş ve üzerinde kilo kaybı ile diğer tanımlanmış değişikliklerin rektal kanama veya anemi ile seyretmesi kolorektal kanser ile bağlantılı olmaktadır (Astin ve ark., 2011). Nedenleri : Kolorektal kanserin % 75-95'inden fazlası, çok az veya hiç genetik riski olmayan kişilerde görülür (Watson ve Collins, 2011; Li ve ark., 2013). Risk faktörleri arasında yaşlılık, erkek cinsiyet (Li ve ark., 2013), yüksek yağ alımı, alkol kullanımı, aşırı kırmızı et ve işlenmiş et tüketimi, obezite, sigara kullanımı ve fiziksel egzersiz eksikliği bulunur (Watson ve Collins, 2011; Anonymous, 2011). Vakaların yaklaşık % 10'unda yetersiz aktivite görülmektedir (Lee ve ark., 2012). Alkol riski günde birden fazla içecekle artmaktadır (Fedirko ve ark., 2011). Günde 5 bardak su içmek kolorektal kanser ve adenomatöz poliplerin riskini azaltmaktadır. İnflamatuar bağırsak hastalığı olan kişilerde (ülseratif kolit ve Crohn hastalığı) kolon kanseri riski artmaktadır (Jawad ve ark., 2011; Ciriello ve ark., 2015). Kişinin hastalığının süresi de riski artırmakta (Xie ve Itzkowitz, 2008) daha da kötüsü inflamasyonun şiddetini artırmaktadır (Triantafillidis ve ark., 2009). Bu yüksek risk gruplarında düzenli kolonoskopiler önerilmektedir (Xie ve Itzkowitz, 2008).
İki veya daha fazla birinci derece akrabada (ebeveyn veya kardeş gibi)
hastalık öyküsü olanlar, iki ila üç kat daha fazla hastalık riskine sahiptir ve bu grup tüm vakaların yaklaşık % 20'sini oluşturur. Bir dizi genetik sendrom da yüksek oranda kolorektal kanser ile ilişkilidir. Bunların en sık görülenleri kolorektal kanserli kişilerin yaklaşık % 3'ünde bulunan kalıtsal polip dışı kolorektal kanserdir (HNPCC veya Lynch sendromu) (Li ve ark., 2013). Kolorektal kanserle güçlü bir şekilde ilişkili olan diğer sendromlar arasında Gardner sendromu (Juhn ve Khachemoune, 2010), ve ailesel adenomatöz polipoz (FAP) yer alır. Bu sendromları olan kişiler için kanser hemen hemen her zaman oluşabilir ve bunlar vakaların % 1'ini oluşturur (Half ve ark., 2009). Yüksek malignite riski nedeniyle FAP'li kişiler için önleyici bir ölçüm olarak toplam proktokolektomi önerilebilir. Kolektomi ise kolonun çıkarılmasına rağmen rektumun kalması durumunda rektal kanser riskinin yüksek olması nedeniyle önleyici bir önlem olarak yeterli olmayabilir (Möslein ve ark., 2003).
Kolorektal kanserin gelişiminde tümör baskılayıcı promotörlerin anormal DNA metilasyonu gibi epigenetik faktörler rol oynar (Schuebel ve ark., 2007). Kolorektal kanser, çoğu zaman sinyal aktivitesini artıran Wnt sinyal yolundaki mutasyonların bir sonucu olarak gastrointestinal sistemin kolonunu veya rektumunu kaplayan epitelyal hücrelerden köken alan bir hastalıktır. Mutasyonlar kalıtsal veya edinsel olabilir ve büyük olasılıkla bağırsak kript kök hücresinde meydana gelebilir (Ionov ve ark., 2004). Tüm kolorektal kanserlerde en yaygın olarak mutasyona uğramış gen, APC proteinini üreten APC genidir. APC proteini, β-katenin proteininin birikmesini önler. APC olmazsa, β-katenin yüksek seviyelerde birikir ve çekirdeğe translokasyon yapar (hareket eder), DNA'ya bağlanır ve proto-onkogenlerin transkripsiyonunu aktive eder. Bu genler normalde kök hücre yenilenmesi ve farklılaşması için önemlidir, ancak yüksek seviyelerde uygunsuz şekilde ifade edildiğinde kansere neden olabilirler. Kapsamlı, genom-ölçekli analiz, kolorektal karsinomların hipermutated ve hipermutasyona uğramayan tümör tiplerine göre sınıflandırılabileceğini ortaya koymuştur (Cancer Genome Atlas Network, 2012).
Teşhis : Kolorektal kanser tanısı, lezyonun lokasyonuna bağlı olarak, genellikle kolonoskopi veya sigmoidoskopi sırasında, muhtemel tümör gelişimi için şüpheli kolon alanlarının örneklenmesi ile gerçekleştirilir (Li ve ark., 2013). Bir doku numunesinin mikroskobik incelemesi ile doğrulanır. Hastalık derecesi genellikle göğüs, karın ve
pelvisin BT taraması ile belirlenir (Li ve ark., 2013). Bazı durumlarda PET ve
MRG gibi diğer potansiyel görüntüleme testleri kullanılabilir (Li ve ark., 2013). Bir sonraki aşamada ise radyoloji ve patoloji sonuçlarına bakılarak kanserin hangi evrede olduğu belirlenir. Tüm diğer kanser türlerinde olduğu gibi, tümör evrelemesi, başlangıçtaki tümörün ne kadar yayıldığını belirleyen TNM sistemine dayanır (Li ve ark., 2013).
Tümörün mikroskobik hücresel özellikleri bir biyopsi veya ameliyattan alınan dokunun analizinden rapor edilir. Bir patoloji raporu, tümör hücresinin sağlıklı dokulara nasıl girdiğini ve nihayetinde tümörün tamamen çıkarıldıktan sonraki mikroskopik özelliklerinin bir açıklamasını içerir. Kolon kanserinin en yaygın şekli adenokarsinomdur. Diğer, daha nadir tipler lenfoma, adenoskuam ve skuamöz hücreli karsinomdur. Bazı alt tiplerin daha agresif olduğu bulunmuştur (Bernstein ve ark., 2013).
Makroskopi : Kalın bağırsağın sağ tarafındaki kanserler (kolon ve çekum) ekzofitik olma eğilimindedir, yani, tümör bağırsak duvarındaki bir yerden dışarı doğru büyür. Bu çok nadiren dışkıda tıkanıklığa neden olur ve anemi gibi semptomlar gösterir. Sol taraflı tümörler çevresel olma eğilimindedir ve bağırsak lümenini peçete halkası gibi çok fazla tıkayabilir ve daha ince kalibreli dışkı ile sonuçlanabilir.
Mikroskopla İnceleme : Adenokarsinom, kolon ve rektumu çevreleyen yüzeysel glandüler epitelyal hücrelerden köken alan bir malign epitelyal tümördür. Muscularis mukoza tabakasına, submukoza ve daha sonra muskularis propriaya sızarak duvarı işgal eder. Tümör hücreleri düzensiz boru biçimli yapıları tanımlamaktadır, bu da pluristratifikasyonu, çoklu lümenleri, azaltılmış stromayı ("arkaya doğru") barındırır. Bazen, tümör hücreleri disseksizdir ve interstitiumun geniş mukus havuzları oluşturmasına neden olan mukus salgılar. Bu, hücrelerin zayıf bir şekilde farklılaştığı müsinöz adenokarsinomda ortaya çıkar. Mukus, tümör hücresinin içinde kalırsa, çekirdeği çevreye iter, bu da "işaret halka hücresinde" oluşur. Glandüler yapıya, hücresel pleomorfizme ve baskın paternin mukosekretisyonuna bağlı olarak, adenokarsinom üç dereceli farklılaşma gösterebilir: iyi, orta ve kötü diferansiye şeklinde (Mustafa ve ark., 2006).
İmmünokimya : Kolorektal kanserden metastazın şüphelenildiği durumlarda,
doğru tanıyı saptamak için immünohistokimya kullanılır. Daha spesifik olarak kolorektal kanserde eksprese edilen ve teşhis belirteçleri olarak kullanılabilen proteinler sitokeratin 20, CDX2, SATB2 ve CDH17'dir. Çoğu (% 50) kolorektal adenom ve (% 80–90) kolorektal kanser tümörlerinin, siklooksijenaz-2 (COX-2) enzimini ifade ettiği düşünülmektedir (Gargallo ve ark., 2014). Bu enzim, genellikle sağlıklı kolon dokusunda bulunmaz, ancak anormal hücre büyümesini tetiklediği düşünülmektedir. Önleme : Kolorektal kanser vakalarının yaklaşık yarısının yaşam tarzı faktörlerine bağlı olduğu ve tüm vakaların yaklaşık dörtte birinin önlenebilir olduğu tahmin edilmektedir (Parkin ve ark., 2010). Sürveyansı (hastalıklara ait verilerin düzenli olarak toplanması, bu verilen analiz edilerek ilgili birimlere dağıtılması işlemlerinin tümüdür.) arttırmak, fiziksel aktiviteye girmek, lifte yüksek bir diyet uygulamak, sigara ve alkol tüketimini azaltmak riski azaltır (Schottenfeld ve Fraumeni, 2006; Rennert, 2007). Kolorektal kanseri önlemek için mevcut diyet önerileri arasında tam tahıl, meyve ve sebze tüketimini arttırmak, kırmızı et ve işlenmiş etlerin alımını azaltmak bulunmaktadır (Campos ve ark., 2005). Daha yüksek fiziksel aktivite de önerilmektedir (Pérez-Cueto ve Verbeke, 2012). Fiziksel egzersiz, kolonda ılımlı bir azalma ile ilişkilidir, ancak rektal kanser riskini azaltmakla ilgili değildir (Harriss ve ark., 2009; Robsahm ve ark.,
2013). Yüksek düzeyde fiziksel aktivite kolon kanseri riskini yaklaşık % 21 oranında azaltır (Kyu ve ark., 2016). Kolon kanseri riski normal vücut ağırlığını koruyarak azaltılabilir (Lauby-Secretan ve ark., 2016). Bununla birlikte, lifli besinler, meyve ve sebze tüketiminin kanseri önleme de bir etken olduğu ancak hiçbir besinin tek başına koruyucu ve tedavi edici etkisinin olmadığı göz önüne alınmalıdır (Doyle, 2007).
Aspirin ve selekoksibinin, yüksek riskli hastalarda kolorektal kanser riskini azalttığı görülmektedir (Cooper ve ark., 2010; Emilsson ve ark., 2017). Aspirin, 50-60 yaşlarında, kanama riskinin artmadığı ve kolorektal kanseri önlemek için kardiyovasküler hastalık riski altında olanlarda önerilmektedir (Bibbins-Domingo ve ark., 2016). Ortalama risk altındakilerde önerilmemektedir (Calonge ve ark., 2007). Kalsiyum takviyesi için geçici kanıtlar vardır, ancak bir tavsiyede bulunmak için yeterli değildir (Weingarten ve ark., 2008). D vitamini alımı ve kan seviyeleri, kolon kanseri riskinin azalmasıyla ilişkilidir (Ma ve ark., 2011; Yin ve ark., 2011).
Tarama : Kolorektal kanserlerin % 80'inden fazlası adenomatöz poliplerden
kaynaklandığı için, bu kanserin taranması sadece erken teşhis için değil aynı zamanda önleme için de etkilidir (Anonymous, 2015). Kolorektal kanser vakalarının taranması ile tanısı, semptomları olan olguların tanısından 2–3 yıl önce ortaya çıkmaktadır. Saptanan herhangi bir polip, genellikle kolonoskopi veya sigmoidoskopi ile çıkarılabilir ve böylece kansere dönüşmeleri önlenir. Tarama, kolorektal kanser ölümlerini % 60 oranında azaltma potansiyeline sahiptir (He ve Efron, 2011).
Üç ana tarama testi mevcuttur kolonoskopi, fekal gizli kan testi, esnek sigmoidoskopi (Moore ve Aulet, 2017). Esnek sigmoidoskopi, ölüm riskini azaltmak için en iyi kanıtlara sahiptir (Swartz ve ark., 2017). Diğer seçenekler sanal kolonoskopi ve dışkı DNA tarama testidir. CT taraması ile yapılan sanal kolonoskopi, kanserlerin ve geniş adenomların saptanması için standart kolonoskopi kadar iyi görünmektedir, ancak radyasyona maruz kalmayla ilişkili olarak riskli ve pahalıdır ayrıca standart kolonoskopi gibi herhangi bir anormal büyümeyi ortadan kaldırmada da yetersizdir (Moore ve Aulet, 2017).
Dışkıda fekal gizli kan testi (FOBT) ise genellikle iki yılda bir önerilir ve guaiak bazlı veya immünokimyasal olabilir. Anormal FOBT sonuçları bulunursa, katılımcılar genellikle bir takip kolonoskopisi muayenesi için yönlendirilir. Her iki yılda bir FOBT taraması, kolorektal kanser ölümlerini % 16 oranında azaltır (Van Der Vlugt ve ark., 2017). İmmünokimyasal testler genellikle doğru netice verir ve testten önce diyet veya ilaç değişimlerini gerektirmez (Katsoula ve ark., 2017). Dışkı da DNA tarama testi, dışkıda değiştirilmiş DNA ve kan (hemoglobin de dahil olmak üzere) gibi prekanseröz lezyonlarla ilişkili biyobelirteçler arar. Pozitif bir sonuç görülürse bu kolonoskopi ile takip edilmelidir. Tarama 50 yaşından başlayarak her üç yılda bir tavsiye edilir.
Öneriler : Amerika Birleşik Devletleri'nde, tarama genellikle 50 ila 75 yaş arasında tavsiye edilir (Bibbins-Domingo ve ark., 2016). Amerikan Kanser Derneği 45 yaşından itibaren taramayı önerir (Wolf ve ark., 2018). 76 ve 85 yaşları arasındakiler için, karar verme bireyselleştirilmelidir (Bibbins-Domingo ve ark., 2016). Her üç yılda bir dışkı bazlı testler, her 5 yılda bir sigmoidoskopi ve her 10 yılda bir kolonoskopi dahil olmak üzere çeşitli tarama yöntemleri kullanılabilir. Yüksek risk altındakiler için taramalar genellikle 40 yaş civarında başlar (Henderson ve ark., 2018). Bu iki yöntemin hangisinin daha iyi olduğu belirsizdir (Brenner ve ark., 2014). Kolonoskopi kolonun ilk
bölümünde daha fazla kanser bulabilir, ancak daha fazla maliyet ve daha fazla
komplikasyonla ilişkilidir (Brenner ve ark., 2014). Normal sonuçlar alan yüksek kalite de bir kolonoskopi yaptırmış olan ortalama riskli kişiler için, Amerikan Gastroenteroloji Derneği kolonoskopiyi takip eden 10 yılda herhangi bir tarama türü önermemektedir (Anonymous, 2012). 75 yaşın üzerindeki kişiler veya yaşam beklentisi 10 yıldan az olanlar için, tarama önerilmemektedir. Kanada'da, normal risk altındaki 50 ila 75 yaş arasındaki bireyler için her iki yılda bir fekal immünokimyasal test veya FOBT, ya da her 10 yılda bir sigmoidoskopi önerilir (Winawer ve ark., 2003). Kolonoskopi daha az tercih edilir (Winawer ve ark., 2003). Bazı ülkelerde, genellikle 50 ila 60 yaşları arasında başlayan, belirli bir yaş grubundaki tüm yetişkinler için FOBT taraması sunan ulusal kolorektal tarama programları bulunmaktadır. Bu organizasyonun yapıldığı ülkeler arasında İngiltere (Lee ve ark., 2011), Avustralya (Ginghina ve Nitipir, 2018), ve Hollanda yer almaktadır.
Tedavi : Kolorektal kanserin tedavisi, direkt tedavi etmeye veya palyasyona yönelik olabilir. Tedavi kişinin sağlığı ve tümörün evresi de dahil olmak üzere çeşitli faktörlere bağlıdır (Stein ve ark., 2011). Kolorektal kanser erken tespit edildiğinde, cerrahi müdahale tedavi edici olabilir. Bununla birlikte, daha sonra ki aşamalarda metastazların mevcut olduğu tespit edildiğinde, cerrahi müdahale daha az olasıdır ve tedavi genellikle tümörün neden olduğu semptomları hafifletmek ve kişiyi olabildiğince rahat tutmak için palyasyona yöneliktir (Li ve ark., 2013).
Cerrahi : Kanser çok erken bir aşamada bulunursa, kolonoskopi sırasında çıkarılabilir (Lacy ve ark., 2002). Bu yöntem lokalize kanserli kişiler için tercih edilen tedavidir. Bu açık laparotomi veya bazen laparoskopik olarak yapılabilir (Li ve ark., 2013). Kolon tekrar bağlanabilir veya kişi bir kolostomiye sahip olabilir (Lacy ve ark., 2002). Karaciğer veya akciğerlerde sadece birkaç metastaz varsa bunlar da çıkarılabilir. Bazen kemoterapi, ameliyattan önce kanseri küçültmek için kullanılır. Kolorektal kanserin en sık metastaz yaptığı organlar karaciğer ve akciğerlerdir (Li ve ark.,2013).
Kemoterapi : Kolon ve rektum kanserinin her ikisinde de kemoterapi, bazı durumlarda cerrahiye ek olarak kullanılabilir. Kolon ve rektal kanserin yönetiminde kemoterapi ekleme kararı hastalığın evresine bağlıdır. Evre I kolon kanserinde kemoterapi önerilmemektedir ve cerrahi müdahale kesin tedavidir. Evre II kolon kanserinde kemoterapinin rolü tartışmalıdır ve genellikle T4 tümörü veya lenf nodu gibi yüksek
risk faktörleri olan durumlar belirlenmediği sürece önerilmez. Ayrıca
uyumsuzluk tamir genlerinin anormalliklerini taşıyan kişilerin kemoterapiden yararlanamadıkları bilinmektedir. Evre III ve Evre IV kolon kanseri için kemoterapi tedavinin ayrılmaz bir parçasıdır (Li ve ark., 2013). Kanser lenf nodlarına veya uzak organlara yayıldıysa, bu durumda evre III ve evre IV kolon kanseri söz konusu ise, kemoterapi ajanlarının eklenmesi fluorouracil, kapesitabin veya oksaliplatinin ömrünü uzatır. Lenf nodları kanser içermiyorsa, kemoterapinin yararları tartışmalıdır. Kanser yaygın olarak metastatik veya rezektabl değilse, tedavi daha sonra palyatiftir. Tipik olarak bu ortamda, bir dizi farklı kemoterapi ilacı kullanılabilir (Li ve ark., 2013). Bu durum için kemoterapi ilaçları kapesitabin, fluorouracil, irinotekan, oksaliplatin ve UFT'yi içerebilir (Modest ve ark., 2014). Kapesitabin ve fluorourasil ilaçlar birbiriyle değiştirilebilirler, kapesitabin oral bir ilaç olup, floroürasil intravenöz ilaçtır. CRC için kullanılan bazı özel rejimler FOLFOX, FOLFOXIRI ve FOLFIRI'dır (Akhtar ve ark., 2014). Bevacizumab gibi antianjiyojenik ilaçlar sıklıkla birinci basamak terapisine eklenir. İkinci basamakta kullanılan bir başka ilaç sınıfı, iki FDA onaylı olanının setuksimab ve panitumumab olduğu epidermal büyüme faktörü reseptör inhibitörleridir (Shaib ve ark., 2013).
Düşük evre rektal kansere yaklaşımdaki birincil fark, radyasyon tedavisinin dahil edilmesidir. Çoğunlukla, cerrahi yöntem rezeksiyon sağlamak için neoadjuvan tarzda kemoterapi ile birlikte kullanılır, böylece en sonunda kolostomi gerekmez. Evre IV rektum kanseri, evre IV kolon kanserine benzer şekilde tedavi edilir.
Radyasyon tedavisi : Radyasyon ve kemoterapinin bir kombinasyonu rektal kanser için yararlı olabilirken (Li ve ark., 2013), bağırsakların radyasyona duyarlılığı nedeniyle kolon kanserinde kullanımı rutin değildir (DeVita ve ark., 2010). Sadece kemoterapi için olduğu gibi, radyoterapi, rektal kanserin bazı aşamaları için neoadjuvan ve adjuvan ortamda kullanılabilir.
Palyatif bakım : Palyatif bakım, kanser gibi ciddi hastalıklardan kaynaklanan semptomların tedavisine ve yaşam kalitesinin iyileştirilmesine odaklanan tıbbi bakımdır (Goodlin, 2009). Kolonyal bakım ileri kolon kanseri olan veya belirgin semptomları olan kişiler için önerilmektedir (American Society of Clinical Oncology, 2012). Palyatif bakımın sağlanması, semptomları, kaygıları ve hastaneye kabulleri önleyerek, hem kişi hem de ailesi için yaşam kalitesini iyileştirmek için faydalı olabilir (Higginson ve
Evans, 2010). Tedavi edilemeyen kolorektal kanserli kişilerde, palyatif bakım,
kanserden kaynaklanan semptomları veya komplikasyonları hafifleten, ancak altta yatan kanseri tedavi etmeye çalışmayan ve böylece yaşam kalitesini arttıran prosedürlerden oluşabilir. Cerrahi seçenekler, bağırsakların bir kısmının atlanması veya stent yerleştirilmesi gibi bazı kanser dokularının küratif olmayan şekilde cerrahi olarak çıkarılmasını içerebilir. Bu prosedürler semptomları iyileştirmek ve tümörden kanama, abdominal ağrı ve bağırsak tıkanıklığı gibi komplikasyonları azaltmak için düşünülebilir (Wasserberg, 2007). Non-operatif semptomatik tedavi yöntemleri arasında ilaçların yanı sıra tümör büyüklüğünü azaltmak için radyasyon tedavisi yer alır (Amersi ve ark., 2004).
Takip : İzlemenin amacı, mümkün olan en erken aşamada, daha sonra gelişen, ancak orijinal kanserden (metakron lezyonlar) kaynaklanmayan metastaz veya tümörlerin teşhis edilmesidir. ABD Ulusal Kapsamlı Kanser Ağı ve Amerikan Klinik Onkoloji Derneği, kolon kanserinin takibinde rehberlik sağlar (Engstrom ve ark., 1996; Desch ve ark., 2005). Tıbbi öykü ve fiziksel muayene 2 yıl boyunca her 3 ila 6 ayda bir, daha sonra 5 yıl boyunca 6 ayda bir önerilir. Karsinoembriyonik antijen kan seviyesi ölçümleri aynı zamanlamayı takip eder, ancak sadece girişim için aday olan T2 veya daha büyük lezyonları olan kişiler için tavsiye edilir. Göğüs, karın ve pelvisin CT taraması, ilk üç yıl boyunca yüksek rekürrens riski taşıyan kişiler için (örneğin, kötü diferansiye tümörlere veya venöz veya lenfatik invazyona sahip olanlar) tedavi edici olarak düşünülebilir. Kolonoskopi 1 yıl sonra yapılabilir, ancak ilk evreleme sırasında engelleyici bir kitle nedeniyle yapılamadıysa, bu durumda 3 ila 6 ay sonra yapılmalıdır. Eğer bir villöz polip, bir polip> 1 santimetre veya yüksek dereceli displazi bulunursa, 3 yıl sonra her 5 yılda bir tekrar edilebilir. Diğer anormallikler için kolonoskopi 1 yıl sonra tekrar edilebilir. Rutin PET veya ultrason taraması, göğüs röntgeni, tam kan sayımı veya karaciğer fonksiyon testleri önerilmez (Engstrom ve ark., 1996; Desch ve ark., 2005). 2016 tarihli bir sistematik derleme daha yoğun gözetim ve yakın takiplerin metastatik olmayan kolorektal kanserlerde ek sağ kalım yararları sağlamadığı sonucuna varmıştır (Jeffery ve ark., 2016).
Epidemiyoloji : Küresel olarak her yıl 1 milyondan fazla kişi kolorektal kansere yakalanmaktadır (Li ve ark., 2013). 2012 yılı itibariyle kadınlarda en sık görülen ikinci (tanıların% 9.2'si) ve erkeklerde en sık görülen üçüncü kanser nedenidir (% 10.0).
Gelişmekte olan ülkeler de daha yaygındır (Merika ve ark., 2010). Dünya
çapında vakalar Avustralya, Yeni Zelanda, Avrupa ve ABD'de en yüksek oranlarda, Afrika ve Güney-Orta Asya'da en düşük oranlarda görülmektedir (Anonymous, 2014).
Amerika Birleşik Devletlerin de kolorektal kanser, erkek ve kadınlar için kanser oluşumunun ve ölümünün en büyük ikinci nedenidir. 2011 yılında tahmini 141.210 vaka teşhis edilmiştir (Redmond ve ark., 2012). 2007'den 2009'a kadar olan oranlara dayanarak, Amerika Birleşik Devletlerin de erkek ve kadınlarının % 4.96'sı yaşam boyu kolorektal kanser tanısı almıştır (Howlader ve ark., 2012). 2005'ten 2009'a kadar, ABD'de kolon ve rektum kanseri tanısında medyan yaşı 69'du. 20 yaşın altında yaklaşık % 0.1; 20 ila 34 arasında % 1.1; 35 ve 44 arasında % 4.0; 45 ile 54 arasında % 13.4; 55 ve 64 arasında % 20.4; 65 ile 74 arasında % 24.0; 75 ile 84 arasında % 25.0 ve 85+ yaşlarda ise % 25.0 kolon kanseri teşhis edilmiştir. Erkekler arasındaki oranlar daha yüksektir.
İngiltere'de ise yılda yaklaşık 41.000 kişi de, kolon kanseri görülmektedir ve dördüncü en yaygın kanser türü haline gelmiştir. Avustralya'da da her 19 erkek ve 28 kadından birin de, 75 yaşından önce kolorektal kanser tespit edilmektedir ve her 10 erkekten biri ile 15 kadından biri ise 85 yaşına kadar kolorektal kanser görüleceği öngörülmektedir (Wilson ve ark., 2018).
2.2. Sitotoksisite
Hücre kültürü, çok hücreli organizmalara ait hücrelerin, laboratuvar ortamında özel tasarlanmış kaplarda, ısı, nem, besin gibi ortam şartlarının kontrol edilerek kontaminasyondan uzak bir şekilde yaşatılmasıdır. İnsan da dâhil olmak üzere herhangi bir canlıdan alınan hücrelerin suni ortamda yaşatılabilmesi, herhangi bir doku ya da organdan alınan hücrelerin kullanılabilmesi ve birçok etik kaygıyı gidermesi, hücre kültürü çalışmalarının tercih sebepleri arasında yer almaktadır (Zucco ve ark., 1998). Hücre kültürünün sıkça tercih edildiği alanlar kanser, aşı çalışmaları, ilaç geliştirilmesi ve in vitro sitotoksisite çalışmalarıdır (Gilbert ve Boutros, 2016).
Sitotoksik terimi, hücre ölümüne neden olan anlamına gelmektedir. Sitotoksisite araştırmaları, bir maddenin sitotoksik potansiyelinin olup olmadığının belirlenmesi amacıyla yapılır. Hücre temelli sitotoksisite çalışmalarını, gerek uygulamadaki kolaylığı, gerekse in vivo çalışmalardan elde edilen verilerle uyum göstermesi