T.C.
EGE ÜNİVERSİTESİ TIP FAKÜLTESİ
ÇOCUK SAĞLIĞI ve HASTALIKLARI ANABİLİM DALI Prof. Dr. Savaş KANSOY
KEMİK İLİĞİ NAKLİ YAPILMIŞ
YAŞAYAN ÇOCUKLARDA SOLUNUM ve DOLAŞIM
KOMPLİKASYONLARININ ERKEN ve GEÇ DÖNEM
DEĞERLENDİRİLMESİ
UZMANLIK TEZİ
Dr. Şerife Şebnem ÖNEN
Tez Danışmanı Prof. Dr. Savaş KANSOY
II
ÖNSÖZ
Çocuk Sağlığı ve Hastalıkları eğitim süresince benden mesleki bilgi ve manevi desteğini esirgemeyen, engin bilgi ve tecrübeleriyle yetişmemde büyük katkı sağlayan ve emeği geçen tüm değerli hocalarıma, uzman ve asistan mesai arkadaşlarıma burada çalıştığım süre boyunca arkadaşlıklarıyla yanımda olan tüm hemşire ve personel ekibe,
Uzmanlık eğitimim boyunca bize düzenli bir çalışma ortamı sağlamış olan aynı zamanda mesleki bilgi ve manevi açıdan büyük desteğini gördüğüm, tez çalışmalarımda değerli fikirleriyle bana yol gösteren, bir asistanın hevesini asla kırmadan yardımları ile bu tezin yazılmasında asıl rolü oynayan tez danışmanım ve anabilim dalı başkanımız Prof. Dr. Savaş Kansoy’a ; kendi bilgi birikimlerini, tecrübelerini tüm asistanlık dönemimde benden esirgemeyen, desteklerini her zaman yanımda hissettiğim onkoloji hocalarım Prof. Dr. Nazan Çetingül, Prof. Dr. Mehmet Kantar ve Prof. Dr. Serap Aksoylar’a,
Tez çalışmamda hasta ve yakınlarıyla aramdaki bağı sağlayan Hemşire Kamile Boyacılar nezdinde tüm onkoloji poliklinik çalışanlarına teşekkür ederim.
Solunum çalışmaları için her zaman yanımda olan, desteğini hissettiğim, Prof. Dr. Esen Demir’e, solunum fonksiyon testini özveriyle, bıkmadan, sabırla tekrar tekrar yapan Gökay Çelik’e,
Kardiyovasküler çalışmalar için Doç. Dr. Zülal Ülger’e, zorlu mesai şartlarına rağmen tüm hastaların ekokardiyografisini çeken Uzm. Dr. Sibel Bozabalı, Uzm. Dr. Yasemin Özdemir Şahan’a sonsuz minnettarlığımı sunarım.
Tüm hayatım boyunca sevgilerini ve desteklerini her zaman hissettiğim ve bugünlere gelmemi sağlayan aileme sonsuz şükranlarımı sunarım.
Dr. Şerife Şebnem ÖNEN
III
ÖZET
KEMİK İLİĞİ NAKLİ YAPILMIŞ YAŞAYAN ÇOCUKLARDA SOLUNUM ve DOLAŞIM KOMPLİKASYONLARININ ERKEN ve GEÇ DÖNEM
DEĞERLENDİRİLMESİ
Hematopoietik kök hücre nakli (HKT), hastanın kendisinden ya da başka bir kişiden hastaya hematopoietik kök hücrelerin verilmesiyle kemik iliğinin yeniden yapılandırılmasıdır. HKT ile birlikte sağ kalım oranlarında artışlar sağlanmış olmakla birlikte erken dönemde hayat kalitesini bozabilecek sistemik komplikasyonlar gelişebilmektedir. Etkilenen sistemler içinde solunum ve dolaşım sistemi mortalite açısından büyük önem taşır. HKT aşamasında dolaşım ve solunum sistemindeki olumsuz yönde etkilenmeler; verilen kemoterapi, radyoterapi başta olmak üzere hastanın yaşı, nakil öncesi sağlık durumu, primer hastalığın tanısı, tanı anında solunum ya da dolaşım sistemi tutuluşu, hastanın nakil öncesi aldığı kemoterapi ya da radyoterapi gibi nedenlere bağlıdır.
Erken dönemde etkilenmeler hastanın yaşam kalitesini, yaşam süresini olumsuz yönde etkilemektedir. Bu nedenle hastalar nakil aşamasında ve nakil sonrası dönemde yakından izlenmeli ve beklenen komplikasyonlara yönelik erken sağaltım yaklaşımları planlanmalı, bireylerin kaliteli bir yaşam elde etmeleri için uğraşlar izleyen ekiplerin sorumluluğunda yürütülmelidir.
Bu çalışmada hematopoietik kök hücre nakilli çocuklarda oluşabilecek erken dönem solunum ve dolaşım komplikasyonlarını belirlemek için Ege Üniversitesi Tıp Fakültesi Çocuk Kemik İliği Transplantasyon Ünitesinde kök hücre nakli gerçekleştirilecek olan 5 yaş üzerindeki 40 olgunun nakil sonrası bir yıllık dönemde anamnez, fizik bakı, spirometri ile solunum fonksiyonları ve ekokardiyografi ile dolaşım fonksiyonları değerlendirildi. Nakil sonrası izlemde ilk bir yılda görülebilen dolaşım sistemine ait kardiyak komplikasyonların belirlenmesi, bu olgularda ilk bir yılda görülebilen solunum sistemine ait komplikasyonların belirlenmesi, bu komplikasyonların sıklığının belirlenmesi, bu komplikasyonlara neden olabilecek etkenler arasındaki ilişkinin belirlenmesi, olguların gelecekte solunum ve dolaşım komplikasyonu açısından izleminin planlanması amaçlandı.
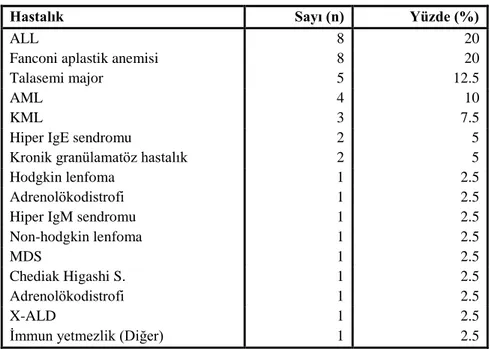
IV Çalışmada 40 olgu 1 yıl boyunca izlendi. Olguların %45’i kız, %55’i erkekti. Medyan yaş 136 ay idi. %97.5’una allojenik HKT yapıldı. Kök hücre donörlerinin %52.5’u akraba dışı, %45’i akraba idi. Hazırlama rejiminde %60 olgu myeloablatif tedavi, %40 olgu nonmyeloablatif tedavi aldı. İzlem boyunca %27.5 olguda akut GVHH, %5 olgu da kronik GVHH bulguları saptandı. Olguların primer tanıları; %47.5’u malignite, %20’si kemik iliği yetmezliği, %17.5’u immun yetmezlik, %10’u hemoglobinopati, %5’i metabolik hastalık idi. Solunum komplikasyonlarından bronşiolitis obliterans
2 olguda (%5.7) görüldü. Görülme zamanı +3 ve +6.ay idi. Bir olgu geç dönem solunum komplikasyonu nedeniyle eksitus oldu. Bronşiolitis obliteransın sağ kalıma negatif etkisi olduğu gösterildi. Olguların hiçbirinde anlamlı sistolik ve diyastolik disfonksiyon görülmedi. 1 olguda +6.ayda orta düzeyde sistolik disfonksiyon saptandı. Asemptomatik olan olgunun HKT döneminde herhangi bir risk faktörü yoktu. Bu bulgu + 1. yılda normal değerine ulaştı.
Sonuç olarak; solunum ve kardiyovasküler komplikasyonlar HKT açısından önemli bir mortalite ve morbidite sebebidir. Özellikle bu çalışmada solunum komplikasyonlarının sağ kalıma negatif etkisi gösterildi. Bu açıdan olgular sık aralıklarla izlenmelidir. Kemik iliği transplantasyon ünitelerinin bu komplikasyonlara karşı kendi izlem protokollerini oluşturması gereklilidir.
Anahtar Kelimeler: Hematopoietik kök hücre nakli, solunum, kardiyovasküler, komplikasyon
V
ABSTRACT
EVALUATION OF EARLY AND LATE RESPIRATORY/ CARDIOVASCULAR COMPLICATIONS OF BONE MARROW
TRANSPLANTATION IN LIVING CHILDREN
Hematopoietic stem cell transplantation (HSCT) is carried out(actualized) by driving multipotent hematopoietic stem cells, from bone marrow, peripheral blood or umbilical cord blood of the patient himself or another person so that the bone marrow can be reconstructed. Although in early periods survival increase is provided due to HSCT, respiratuar or cardiovascular complications depending on risk factors such as chemotherapy, radiotherapy can cause mortality or morbidity. The age, health condition or primer illnesses of the patient are the other risk factors which should be taken serious. Therefore patients should be followed closely during transplantion and post-transplantion period and early treatment approaches should be planned for the expected complications. Teams should effort to achieve a better quality of life for the patients.
In this study, it is aimed to determine the cardiovascular and respiratory complications and their incidence and risk factors.
40 patients older than 5 years who have undergone HSCT in Ege University Medicine Faculty, Pediatric Stem Cell Transplantation Unit between the years 2012 and 2013 were planned to be followed for 1 year prospectively. Demographics, HSCT characteristics, primary diagnosis, donor properties, conditioning regimen, graft versus host disease (GVHD), CMV seropositivity, cardiovascular risk factors such as hypertension, diabetes mellitus, hyperlipidemia were observed.
Results: Patients (45 % female, 55 % male) had 136 months median age. 97,5 % of cases were undergone allogenic HCST while 2,5 % were undergone autologous HSCT. The percentage of unrelated stem cell donors was 52.5, whereas 45 % of donors were relatives. Myeloablative treatment were given to 60 % of cases, myeloablative treatment was given to 40 % of cases. During follow up, acute GVHD was observed in 27,5 % of cases, chronic GVHD was observed in 5 % cases. Primary diagnosis was malignancy (47,5 %) where as bone marrow failure was (20 %), immunodeficiency was (17,5 %), hemoglobinopathies was (10 %), and metabolic disease was(5 %).
VI The incidence of Bronchiolitis obliterans, which was observed in two individuals as respiratuar complications, was % 5,7. Diagnosis time for these cases are 3 and 6 months after HSCT. One of the patients died in 12. month because of late respiratuary complications. In this study we pointed out that bronchiolits obliterans had negative effect on survival. None of the patients showed significant systolic and diastolic dysfunction. Only one patient had moderate systolic disfunction at 6. month. He had no risk factors about cardiovascular complication and also he was asymptomatic.
As a result, respiratuar and cardiyovascular complications are important causes of morbidity and mortality. In this study especially respiratory complications were shown to have a significant impact on survival. Patients should be scanned at frequent intervals with respiratuary function tests. Bone marrow transplantation units must establish their own follow-up protocols.
Keywords: Hematopoietic stem cell transplantation, respiration, cardiovascular complications
VII İÇİNDEKİLER ÖNSÖZ ... II ÖZET ... III ABSTRACT ... V TABLOLAR DİZİNİ ... IX ŞEKİLLER DİZİNİ ... XI GRAFİKLER DİZİNİ ... XII SİMGELER VE KISALTMALAR DİZİNİ ... XIII
1. GİRİŞ VE AMAÇ ... 1
2. GENEL BİLGİLER ... 3
2.1. Hematopoietik Kök Hücre Transplantasyonunun Kısa Tarihi ... 3
2.2. Hematopoietik Kök Hücre Transplantasyonu ... 4
2.2.1. Kök hücre tanımı ... 4
2.2.2. Kök hücre kaynakları ... 5
2.3. Transplantasyon Tanımlamaları ... 6
2.3.1. Verici (Donör) tanımlamaları ... 6
2.3.2. Hematopoietik kök hücre transplantasyonu kimlere yapılır? ... 6
2.4. Hazırlama rejimleri ... 9
2.5. Donör seçimi ... 9
2.6. Transplantasyon ilişkili komplikasyonlar ... 11
2.7. HKT Sonrası Görülen Erken Komplikasyonlar ... 12
2.8. HKT Sonrası Görülen Geç Komplikasyonlar ... 21
2.9. Solunum Fizyolojisi ... 23
2.9.1. Akciğer Hacimleri ... 25
2.9.2. Akciğer Kapasiteleri ... 26
2.9.3. Solunum Fonksiyon Testleri ... 27
2.10.Kök Hücre Nakli Sonrası Gelişen Solunum Komplikasyonlarının Fizyopatolojisi ... 29
2.11. Dolaşım sistemi komplikasyonları ... 30
2.11.1. Ekokardiyografi ... 31
VIII
2.11.3. Sol Ventrikül Sistolik Fonksiyonunun Değerlendirilmesi ... 34
2.11.4. Sol Ventrikül Diyastolik Fonksiyonunun Değerlendirilmesi ... 35
2.11.5. Dolaşım Fizyolojisi ... 36 3. GEREÇ ve YÖNTEM ... 40 3.1. İstatistiksel yöntem ... 42 4. BULGULAR ... 43 4.1. Hastalar ... 43 4.2. Spirometri ... 45 4.3. Ekokardiyografi ... 68 4.3.1. Sistolik fonksiyon ... 69 4.3.2. Diyastolik disfonksiyon ... 72 4.4. Sağkalım ... 72 5. TARTIŞMA ... 73 6. SONUÇ ... 78 KAYNAKLAR ... 80
IX
TABLOLAR DİZİNİ
Tablo 1. HKT endikasyonları ... 7
Tablo 2. EBMT tarafından önerilen çocuklarda HKT endikasyonları ... 8
Tablo 3. Akut GVHH’nin klinik belirtileri ... 15
Tablo 4. Akut GVHH’nın evrelendirilmesi ... 15
Tablo 5. Akut GVHH genel değerlendirilmesi ... 16
Tablo 6. Kronik GVHH’nin klinikopatolojik sınıflandırılması ... 17
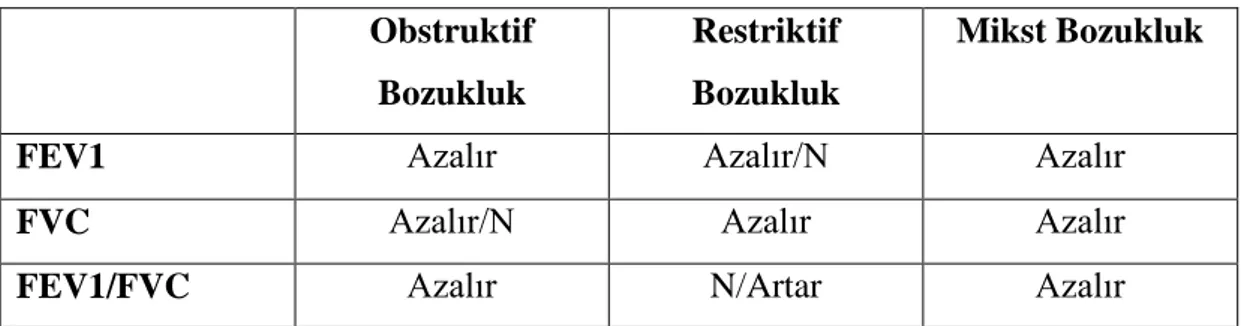
Tablo 7. Solunum fonksiyon testlerinin yorumlanması... 29
Tablo 8. Spirometrik testin değerlendirilmesi ... 40
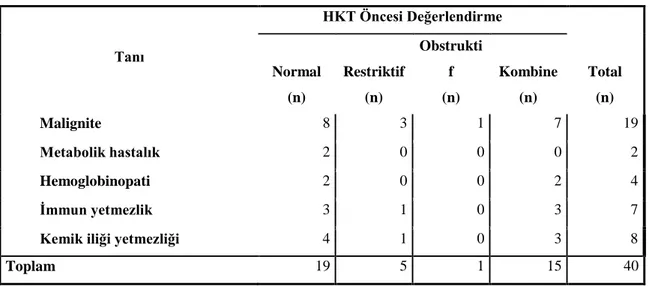
Tablo 9. Çalışmaya alınan 40 olgunun genel özellikleri ... 44
Tablo 10. Olguların primer tanıları... 45
Tablo 11. Eksitus olanların özellikleri ... 45
Tablo 12. Olguların HKT öncesi spirometrik değerlerinin kontrol grubuyla karşılaştırılması ... 46
Tablo 13. HKT öncesi spirometrik değerlere göre olguların sınıflandırılması ... 46
Tablo 14. Patoloji saptanan olguların tanılarına göre gruplandırılması ... 47
Tablo 15. Olguların 1. ay spirometri sonuçlarına göre değerlendirilmesi ... 47
Tablo 16. Olguların 1. ay sonunda ortalamalarının HKT öncesi ortalamaları ile karşılaştırılması ... 48
Tablo 17. Olguların 3. ay spirometrik sonuçlarına göre sınıflandırılması... 51
Tablo 18. Olguların HKT öncesi, 1. ay, 3.ay ortalamarının karşılaştırılması ... 52
Tablo 19. 3. aydaki FEV1/FVC değerinin akraba ve akraba dışı vericiler arasında karşılaştırılması ... 52
Tablo 20. 3. aydaki FEV1/FVC değerinin vericiler arasında karşılaştırılması ... 52
Tablo 21. Olguların 6. ayda spirometrik sonuçlara göre sınıflandırılması ... 57
Tablo 22. Olguların HKT öncesi, 1.ay, 3.ay ve 6. ay spirometrik sonuç ortalamalarının karşılaştırılması ... 57
Tablo 23. 6.ay FEV1/FVC değerinin verici özellikleri ile karşılaştırılması ... 58
Tablo 24. MEF25-75 değerinin önceden kemoterapi alanlarla karşılaştırılması ... 58
X Tablo 25. FEV1/FVC değeriyle GVHH arasındaki ilişkinin
karşılaştırılması ... 58 Tablo 26. 12. ayda olguların spirometrik ölçümlerine göre sınıflandırılması ... 63 Tablo 27. Olguların spirometrik ölçümlerinin HKT öncesi, 1. ay, 3. ay, 6.
ay ve 1. yıl ortalamalarının karşılaştırılması ... 64 Tablo 28. FEV1/ FVC değerinin GVHH ile ilişkisi ... 64 Tablo 29. Bronşiolitis obliteranslı bireylerin spirometrik değerlerinin BO
olmayanlarla karşılaştırılması ... 65 Tablo 30. Olguların EF ortalamalarının tüm dönemlere göre
karşılaştırılması ... 69 Tablo 31. Olguların FS ortalamalarının dönemlere göre karşılaştırılması ... 69 Tablo 32. Olguların EF ve FS sonuçlarına göre sistolik disfonksiyonlarının
sınıflandırılması ... 70 Tablo 33. IVSd ortalama z skorunun dönemlere göre karşılaştırılması ... 70 Tablo 34. Sol ventrikül end sistolik çap ortalama ve z skorunun dönemlere
göre karşılaştırılması ... 71 Tablo 35. Sol ventrikül end diyastolik çap ortalama ve z skorunun
dönemlere göre karşılaştırılması ... 71 Tablo 36. Aort kök çap ortalama değerlerinin dönemlere göre
karşılaştırılması ... 71 Tablo 37. Sol atrium diyastolik çap ortalama değerinin dönemlere göre
XI
ŞEKİLLER DİZİNİ
Şekil 1. Kök hücr ... e4
Şekil 2. Verici seçimi algoritması ... 11
Şekil 3. HKT sonrası görülebilen erken ve geç dönem komplikasyonlar ... 12
Şekil 4. HKT’de enfeksiyon haritası ... 18
Şekil 5. Akciğer kapasiteleri... 26
Şekil 6. Spirometrik değerlerin gösterilmesi ... 28
Şekil 7. Ventriküler relaksasyon... 36
Şekil 8. Erken dolum fazı ... 37
Şekil 9. Atrium sistolu ... 37
Şekil 10. İzovolumik kontraksiyon ... 38
XII
GRAFİKLER DİZİNİ
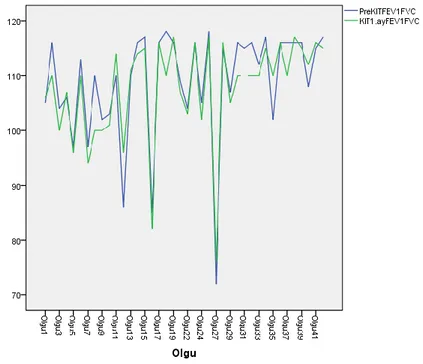
Grafik 1. FVC değerinin HKT öncesi ve 1. ay sonuçları ... 48
Grafik 2. FEV1 değerinin HKT öncesi ve 1. ay sonuçları ... 49
Grafik 3. FEV1/FVC değerinin HKT öncesi ve 1. ay sonuçları ... 50
Grafik 4. MEF25-75 değerinin HKT öncesi ve 1. ay sonuçları ... 50
Grafik 5. Olguların 1. ay FVC değerleriyle 3. ay FVC değerleri ... 53
Grafik 6. Olguların 1. ay FEV1/FVC değerleriyle 3. ay FEV1/FVC değerleri ... 54
Grafik 7. Olguların 1. ay FEV1 değerleriyle 3. ay FEV1 değerleri ... 55
Grafik 8. Olguların 1. ay MEF25-75 değerleriyle 3. ay MEF25-75 değerleri ... 56
Grafik 9. Tüm olgulara tek tek bakıldığında 3. ay FVC değerleriyle 6. ay FVC değerleri ... 59
Grafik 10. Olguların 3. aydaki FEV1 değerleriyle 6. aydaki FEV1 değerleri ... 60
Grafik 11. Olguların 3. Aydaki FEV1/FVC değerleriyle 6. Aydaki FEV1/FVC değerleri ... 61
Grafik 12. Olguların 3. ay MEF25/75 değerleriyle 6. ay MEF25-75 değerleri ... 62
Grafik 13. Olguların 6. ay FVC değerleriyle 12. ay FVC değerleri ... 65
Grafik 14. Olguların 6. ay FEV1 değerleriyle 12. ay FEV1 değerleri ... 66
Grafik 15. Olguların 6. ay ve 1. yıl FEV1/FVC değerleri ... 67
Grafik 16. Olguların 6. ay ve 1. yıl MEF 25-75 değerleri ... 68
XIII
SİMGELER VE KISALTMALAR DİZİNİ
HKT : Hematopoietik kök hücre nakli
HLA : Human lökosit antijen
HKH : Hematopoietik kök hücreler
MSD (Matched sibling donor) : Tam uyumlu kardeş donör MUD (Well matched unrelated donor) : İyi uyumlu akraba dışı donör MMUD (Mismatched unrelated donor) : Uyumlu olmayan akraba dışı donör
EBMT : Avrupa Kan ve Kemik iliği Nakli Grubu
TBI : Total vücut ışınlaması
KT : Kemoterapi
ALL : Akut Lenfoblastik Lösemi,
AML : Akut Miyeloid Lösemi
KML : Kronik Miyeloid Lösemi
HL : Hodgkin Lenfoma
NHL : Non-Hodgkin Lenfoma
MDS : Myelodisplastik Sendrom
SCID : Ağır kombine immun yetmezlik
MPS : Mukopolisakkaridoz
CR : Tam remisyon
GVHH : Graft versus Host Hastalığı
VOD : Veno okluziv hastalık
IL-1 : Interlökin 1
TNF-α : Doku nekroz faktörü
Gİ : Gastrointestinal
ATG : Anti-timosit globülin
CMV : Sitomegalovirüs
HLH : Hemofagositik lenfohistiyositoz
IPS : İdiyopatik pnömoni sendromu
DAH : Diffüz alveolar hemoraji
BAL : Bronkoalveolar lavaj
BO : Bronşiolitis obliterans
TV : Tidal Volüm
XIV
ERV : Ekspiratuvar Rezerv Volüm
RV : Rezidüel Volüm
V/Q : Ventilasyon / Perfüzyon
FRC : Fonksiyonel Rezidüel Kapasite
VC : Vital Kapasite
FVC : Zorlu Vital Kapasite
TLC : Total Akciğer Kapasitesi
FEV1 : Zorlu Ekspiratuvar Volüm 1. sn
MEF 25-75 : Maksimal Ekspirasyon Ortası Akım Hızı
GOLD : Global Initiative for Chronic Obstructive
Lung Disease
SFT : Solunum fonksiyon testi
LVEF : Sol ventrikül ejeksiyon fraksiyonu
FS : Fraksiyonel kısalma
LVDd : Sol ventrikül diyastol sonu çapı
LVDs : Sol ventrikül sistol sonu çapı
IVSd : İnterventriküler septum diyastolik çapı
IVRT : İzovolumik relaksasyon zamanı
Ao : Aort kökü diyastolik çapı
1
1. GİRİŞ VE AMAÇ
Hematopoietik kök hücre nakli (HKT), hastanın kendisinden ya da başka bir kişiden hastaya hematopoietik kök hücrelerin verilmesiyle kemik iliğinin yeniden yapılandırılmasıdır. Hematopoietik kök hücre nakli günümüzde çocuklarda hematolojik, onkolojik, immünolojik ya da genetik hastalıkların tedavisinde tercih edilmektedir. Bu hastalıklar arasında akut lösemiler, kemik iliği yetmezlikleri, hemoglobin sentez defektleri, immun yetersizlikler ve bazı metabolik hastalıklar ön planda yer almaktadır. Edinsel ya da doğumsal olabilen bu hastalıklarda HKT tek küratif tedavi seçeneğidir.
HKT ile birlikte sağ kalım oranlarında artışlar sağlanmış olmakla birlikte erken dönemde hayat kalitesini bozabilecek sistemik komplikasyonlar gelişebilmektedir. Etkilenen sistemler içinde solunum ve dolaşım sistemi mortalite açısından büyük önem taşır. HKT aşamasında dolaşım ve solunum sistemindeki olumsuz yönde etkilenmeler; verilen kemoterapi, radyoterapi başta olmak üzere hastanın yaşı, nakil öncesi sağlık durumu, primer hastalığın tanısı, tanı anında solunum ya da dolaşım sistemi tutuluşu, hastanın nakil öncesi aldığı kemoterapi ya da radyoterapi gibi nedenlere bağlıdır.
Erken dönemde etkilenmeler hastanın yaşam kalitesini, yaşam süresini olumsuz yönde etkilemektedir. Bu nedenle hastalar nakil aşamasında ve nakil sonrası dönemde yakından izlenmeli ve beklenen komplikasyonlara yönelik erken sağaltım yaklaşımları planlanmalı, bireylerin kaliteli bir yaşam elde etmeleri için uğraşlar izleyen ekiplerin sorumluluğunda yürütülmelidir.
Bu çalışmada hematopoietik kök hücre nakilli çocuklarda oluşabilecek erken dönem solunum ve dolaşım komplikasyonlarını belirlemek için Ege Üniversitesi Tıp Fakültesi Çocuk Kemik İliği Transplantasyon Ünitesinde kök hücre nakli gerçekleştirilecek olan 5 yaş üzerindeki 40 olgunun nakil sonrası bir yıllık dönemde anamnez, fizik bakı, spirometri ile solunum fonksiyonlarının ve ekokardiyografi ile dolaşım fonksiyonlarının değerlendirilmesi planlanarak bunun sonucunda;
Nakil sonrası izlemde ilk bir yılda görülebilen dolaşım sistemine ait kardiyak komplikasyonların belirlenmesi,
Bu olgularda ilk bir yılda görülebilen solunum sistemine ait komplikasyonların belirlenmesi,
2 Bu komplikasyonların sıklığının belirlenmesi,
Bu komplikasyonlara neden olabilecek etkenler arasındaki ilişkinin belirlenmesi,
Bu olguların gelecekte solunum ve dolaşım komplikasyonu açısından izleminin planlanması amaçlandı.
Bu çalışmanın sonucunda kemik iliği transplantasyon ünitelerinin bu komplikasyonlara karşı kendi izlem protokollerini oluşturması gerekliliğini göstermek hedeflendi.
3
2. GENEL BİLGİLER
2.1. Hematopoietik Kök Hücre Transplantasyonunun Kısa Tarihi
İkinci Dünya Savaşını sonlandıran Japonya’daki atom bombası patlamasından sonra birçok bilim insanı radyasyondan korunma yolları üzerine çalışmaya başladı. İlk deneyler E.D Thomas tarafından fareler ve daha sonra da köpekler üzerine yapıldı (1). 1956 yılında deneysel fare modellerinde transplante edilen dalak hücrelerinin antilösemik etki gösterdiğini gözlemlemiş olan Barnes ve Loutit kemik iliği transplantasyonunun malignitelere karşı terapötik bir etki gösterebileceği fikrini ileri sürdüler (2). E.D Thomas yüksek doz radyasyon kullanarak köpeklerde ilk transplantasyonları yaptı (3). 1959 yılında insanlardaki ilk kemik iliği transplantasyonları, lethal dozda ışın almış akut lösemili hastalarda kemik iliği infüzyonunun hematolojik yeniden yapılanma sağlayabileceği hipotezini ortaya koydu (4). E.D Thomas akut lenfoblastik lösemili iki hastaya yüksek dozlu tüm vücut ışınlaması sonrasında sinjeneik greft nakletti; hastalarda engrafman oluştu, fakat birkaç ay sonra nüks nedeniyle kaybedildiler. Mathe kaza sonucu radyasyona maruz kalmış olan bazı hastaları tedavi etmek için allojenik kemik iliği uyguladı, çoğu otolog yeniden yapılanmayla hayatta kaldı (5). 1965 yılında Mathe antilösemik etki görülen uzun süreli kardeş kemik iliği engrafmanını bildiren ilk kişi oldu (6). Transplantasyonun kendisi başarılı olmasına rağmen, hasta sonunda su çiçeği ve kronik graft versus host hastalığı nedeniyle kaybedildi. 1970 yılında M. Bortin 1958-1968 yılları arasında yapılan 203 transplantasyonla ilgili bir bildirim yaptı; rapor yayınlandığı sırada hastaların yalnızca 3 tanesi hayattaydı. Başlıca ölüm nedeni greft yetersizliği ve nükstü. Çocuklarda ilk başarılı allojenik HKT ise 1968 yılında kombine immün yetmezlikli ve Wiskott Aldrich olgularında bildirilmiştir (7). Bu hayal kırıklığı yaratan sonuçlardan sonra az sayıda merkez kaldı ve transplantasyon sayısı ciddi derecede azaldı. Başlıca ilerleme 1960’lı yıllarda J. Dausset ve J.J.Van Rood’un HLA sistemini keşfetmesiyle sağlandı. Kemik iliği vericisi olarak HLA özdeş kardeşlerin seçilmesi rejeksiyon ve graft versus host hastalığı riskinin azalmasını sağladı (8). Bu öncü niteliğindeki çalışmalardan sonra kaydedilen büyük ilerlemeler sayesinde bugün HKT dünya genelinde birçok hastanın hayatını kurtarmaktadır. Çok sayıda organizasyon aracılığıyla sağlanan uluslararası işbirliği HKT gelişmesinde anahtar rol oynamaktadır.
4 2.2. Hematopoietik Kök Hücre Transplantasyonu
Hematopoietik kök hücre nakli, kök hücrenin hastaya hazırlayıcı bir rejim sonrası genellikle intravenöz yolla verildiği ve bu yolla kemik iliğinin yeniden yapılandırılması sağlanan bir uygulama şeklidir. İlk kök hücre nakillerinde kök hücre kaynağı kemik iliği olduğundan “kemik iliği nakli” terimi günümüzde kök hücre kaynağı olarak kemik iliği dışında periferik kan ve kordon kanı kullanılmasıyla yerini “hematopoietik kök hücre nakli” terimine bırakmıştır (9).
2.2.1. Kök hücre tanımı
Kök hücre, işlevsel olarak farklılaşmamış insan vücudunda bulunan, bütün dokuları ve organları oluşturan ve her türlü vücut hücresine dönüşebilen ana hücrelerdir. Henüz farklılaşmamış olan bu hücreler sınırsız bölünebilme ve kendini yenileme, organ ve dokulara dönüşebilme yeteneğine sahiptirler (10). Bu tanım farklı fiziksel konumlarda bulunan ve temelden farklı çoğalma özelliklerine ve işlevlere sahip hücreleri kapsar. Döllenmiş bir yumurta (zigot), sonsuz bir farklılaşma potansiyeli olan totipotent bir kök hücreyi temsil eder (Şekil 1).
Şekil 1. Kök hücre
Totipotent kök hücre, fetal ve erişkin organlarının gelişmesi için gerekli bütün hücrelerin meydana gelmesini sağlama kapasitesine sahiptir. Bölünen zigotun
5 oluşturduğu blastosistin içinde bir küme oluşturan embriyonik kök hücreler çeşitli özelleşmiş hücre tiplerini oluşturma yetisine sahip pluripotent kök hücrelerdir. Totipotent hücre soyundan gelmekle birlikte farklılaşma potansiyelleri sınırlıdır, üç germ tabakasından meydana gelen neredeyse tüm hücrelere farklılaşabilirler. Daha ileri gelişimsel süreçler erişkin somatik dokularında yerleşmiş multipotent kök hücrelerin oluşmasını sağlar. Multipotent kök hücrelerin fizyolojik işlevi belirli bir doku homestazının devamlılığını sağlamak ve hasarlı dokuyu onararak strese yanıt vermektir. Hematopoietik kök hücreler multipotent erişkin doku kök hücrelerinin prototipidir (11).
2.2.2. Kök hücre kaynakları
Periferik kan HKT: Hematopoietik kök hücreler (HKH) periferik kanda az miktarda (%0.01-0.02 gibi) bulunur. Granülosit koloni uyarıcı faktörler gibi ilaçlarla kök hücrelerin kemik iliğinden periferik kana geçişleri arttırılıp periferik kandan kök hücre toplama işlemi yapılır. Periferik kandan toplanan HKH’ler ile yapılan HKT’de engrafman (nötrofili ve trombositlerin kemik iliğinde belli bir sayıya ulaşmaları) daha hızlı, erken toksisiste daha az, immun yeniden yapılanma daha üstün olmaktadır. Bu yöntemle kemik iliğine göre daha fazla T hücre verildiğinden graft versus host hastalığı daha fazla gelişmektedir. Otolog HKT’de kök hücre kaynağı olarak çoğunlukla periferik kan tercih edilmektedir. Periferik kan hücre toplanması işlemi esnasında genel anesteziye ihtiyaç yoktur, hücreler aferez cihazı ile ortalama 4 saatlik bir işlem ile toplanır.
Kemik iliği HKT: Kök hücre vericinin kemik iliğinden anestezi altında toplanır. Hemen kullanılmayacaksa dondurulup saklanır. Engrafman süresi daha uzundur. Graft versus host hastalığı periferik kan kaynaklı HKT’e göre daha azdır.
Kordon kanı HKT: Göbek kordon kanı kemik iliğine benzer şekilde %1-2 oranında HKH açısından zengindir. Miktar olarak az olduğundan erişkin ve vücut yüzey alanı büyük hastalar için yeterli sayıda HKH içermemektedir. Kordon kanı genellikle 3 yaşına kadar olan çocuklar için yeterli hücre sayısına sahiptir. Kordon kanı kordon kan bankalarından sağlanmaktadır. Verici için bir risk yaratmaz, viruslarla bulaş riski düşüktür. Doku uyumu tam olmasa bile graft versus host hastalığı riski düşüktür. Bunun yanında henüz vericide ortaya çıkmamış olası bir hastalığın alıcıya aktarılma riski vardır. Engrafman süreleri daha uzundur, bu da olası enfeksiyon riskinin artmasına neden olmaktadır.
6 2.3. Transplantasyon Tanımlamaları
Otolog HKT: Kullanılan kök hücreler hastanın kendi kemik iliği ya da periferik kanından elde edilir. Toplanan hücreler -80 veya – 194°C’de dondurularak saklanır. Olguya kemik iliğini baskılayan ve alıcıda kalan tümör hücrelerini ortadan kaldırmak amacıyla verilen yüksek dozlu hazırlama rejiminden sonra çözündürülerek kök hücreler intravenöz yoldan geri verilir.
Allojenik HKT: Kullanılan kök hücreler alıcı ile HLA açısından uyumlu bir vericinin periferik kanından, kemik iliğinden veya kordon kanından elde edilir. Olguya kemik iliğini baskılayan ve alıcıda kalan tümör hücrelerini ortadan kaldırmak amacıyla verilen hazırlama rejiminden sonra kök hücreler intravenöz yoldan verilir. Allojenik HKT’nda otolog HKT’nun aksine toplanan kök hücrelerden tümör hücre bulaş riski yoktur. Fakat graft versus host hastalığı ve bu hastalığa bağlı immünsüpresif tedaviye bağlı olarak mortalite ve morbidite otolog HKT’ye göre daha yüksektir.
2.3.1. Verici (Donör) tanımlamaları
Tam uyumlu kardeş donör (matched sibling donor- MSD): Genotipik olarak aynı olan kardeş verici
Sinjenik donör: Genotipik ve fenotipik olarak aynı olan tek yumurta ikizi verici
İyi uyumlu akraba dışı donör (well matched unrelated donor- MUD): Yüksek çözünürlük tekniği ile bakılan HLA’nın 9/10 ya da 10/10 uyumlu olduğu akraba olmayan verici
Uyumlu olmayan akraba dışı donör (mismatched unrelated donor- MMUD): Yüksek çözünürlük tekniği ile bakılan HLA’nın 6-8/10 uyumlu olduğu verici
2.3.2. Hematopoietik kök hücre transplantasyonu kimlere yapılır?
Günümüzde çocukluk yaş grubunda HKT, hematolojik maligniteler, immün yetmezlikler, hemoglobinopatiler, kemik iliği yetmezlikleri ve konjenital metabolik
7 hastalıklarda hayat kurtarıcı bir tedavi yöntemi olarak kabul edilmektedir. Çocuklarda HKT endikasyonları Tablo 1’de görülmektedir (12).
Tablo 1. HKT endikasyonları
Hematolojik malignitelerde önerilen KHT endikasyonları
Lösemi: Akut Lenfoblastik Lösemi (ALL), Akut Miyeloid Lösemi (AML), Kronik Miyeloid
Lösemi (KML), Juvenil myelomonositik lösemi (JMML), Myelodisplastik Sendrom (MDS)
Lenfoma: Nüks eden Hodgkin Lenfoma(HL) veya Non-Hodgkin Lenfoma (NHL)
Ailesel hemofagositik lenfohistiyositoz (HLH)
Solid tümörlerde önerilen KHT endikasyonları
Germ hücreli tümör
Ewing sarkom(Yüksek risk veya CR>1)
Yumuşak doku sarkomu (Yüksek risk veya CR>1)
Nöroblastom(Yüksek risk veya ≥CR1)
Wilms tümörü >CR1
Osteosarkom
Beyin tümörleri (özellikle lokal rekürrens ve kemosensitif medullablastomda)
Beniyn hastalıklarda önerilen KHT endikasyonları
Primer immün yetmezlikler: Ağır kombine immun yetmezlik (SCID), Wiskott-Aldrich
sendromu, HLA-Class II defekti, HiperIgM sendromu, Kronik granülamatöz hastalık, Lökosit adezyon defeti, Chediak-higashi sendromu, Griscelli sendromu
Hemoglobinopatiler: Orak hücreli anemi (Yüksek risk), Talasemi majör, konjenital anemiler, Fanconi anemisi, Diamond-Blackfan anemisi
Metabolik hastalıklar: Mukopolisakkaridoz –I Hurler, I Hurler-Scheie (Ağır klinik),
MPS-VI Maroteaux-Lamy, Adrenolökodistrofi, Osteopetrozis
Otoimmün hastalıklar
Edinsel: Aplastik anemi, paroksismal nokturnal hemoglobinüri, myelofibrozis
Ayrıca literatürde başarılı uygulanmış Kostmann sendromu, Aktin disfonksiyonu, Adenozin deaminaz yetersizliği, Pürin nukleosid fosforilaz eksikliği, Bare lenfosit sendromu, Disproporsiyonel büyüme gelişme geriliği ile birlikte giden immun defektler, Aspartil glukozaminüri, Gaucher tip I/III, Krabbe hastalığı,
8 Niemann-Pick tip B, Wolman hastalığı, Mukopolisakkaridoz tip I, VI, VII, Nöronal seroid lipofusinoz, Fukosidoz, Mannosidoz, Lesch-Nyhan sendromu ve Farber hastalığı olguları vardır (13).
Çocuklarda Avrupada geçerli klinik uygulamalar temelinde Avrupa Kan ve Kemik iliği Nakli Grubu (EBMT) tarafından önerilen HKT endikasyonları Tablo 2’de gösterilmiştir (12).
9 2.4. Hazırlama rejimleri
HKT hazırlığı aşamasında kullanılan protokollerin amacı, verilecek kök hücrelerin kemik iliği stromasında nişlere yerleşmesi ve engrafman oluşması için boşluk yaratmak; alıcı immün sistemin baskılanması ile birlikte greft rejeksiyon riskini azaltılma ve primer hastalığın eradikasyonudur.
Genellikle çocuklar erişkinlere oranla hazırlama rejimlerini daha iyi tolere eder. Böylece kemoterapötiklerin daha yüksek doz kullanılmasına imkan sağlar. Kullanılan total vücut ışınlaması (TBI) çocuklarda geç yan etki olarak büyüme ve puberte geriliğine yol açabilmektedir. TBI içeren hazırlık rejimlerini sadece KT içeren rejimlerle karşılaştıran birçok rapor benzer sonuçlar bildirmiştir. Bu nedenle küçük çocuklarda mümkün olduğunca TBI’dan kaçınılmalıdır; 2 yaş altında çocuklara hiç uygulanmaması gerekmektedir. ALL nedeniyle HKT uygulanacak olan 2 yaşından büyük olan çocuklarda günde iki doz TBI ile siklofosfamid ve/veya VP16 kombinasyonu yaygın olarak kullanılmaktadır. Bu çocuklar genellikle bu hastalıkta yarar sağlayan bütün ilaçları önceden kullanmış durumdadır ve TBI’ın ALL’de ek bir antilösemik etki gösterdiği düşünülmektedir (14). En sık kullanılan hazırlama rejimi busulfan ile siklofosfamid kombinasyonudur (15). Primer hastalığın özelliklerine göre bazı ilaçlar eklenebilmektedir. Klasik hazırlama rejimleri ile morbidite ve mortalitenin yüksek olması nedeniyle son yıllarda daha az toksik ve daha düşük dozlar içeren hazırlama rejimleri geliştirilmektedir. Malign olmayan hastalıklarda kusurlu hematopoezin normal donör hücreleri ile değişimi sonucu normal hematopoez sağlanması ya da alıcıda eksik enzimin kök hücre nakli ile enzim yapımının sağlanması azaltılmış yoğunlukta hazırlama rejimleri ile mümkün olabilmektedir (16). Fludarabin azaltılmış yoğunlukta hazırlama rejimlerinde en sık kullanılan kemoterapi ajanıdır. Çocuklarda malign ve malign olmayan hastalıklarda kullanılan hazırlama rejimleri ile ilgili çok sayıda çalışma olmakla birlikte uygun rejim ve uygun çocuk adaylarının belirlenmesi için çok merkezli geniş kapsamlı çalışmalara gereksinim vardır (17,18).
2.5. Donör seçimi
Allojenik HKT, malign ve malign olmayan hastalığı olan bireylerin tedavisinde kullanılmaktadır. Başlangıçta, çocuk ve genç erişkinlerde yapılan transplantasyonlarda esas HKH kaynağı HLA özdeş bir kardeşten alınan kemik iliği
10 idi. Daha sonra verici HKH kaynak seçeneklerinin artmasıyla transplantasyon endikasyonları daha fazla hastayı kapsamaya başladı. Günümüzde HKH kaynağı olarak kemik iliği, granülosit koloni uyarıcı faktör yardımıyla mobilize edilmiş periferik kan kök hücreleri ve kordon kanı seçenekleri mevcuttur. Verici, HLA özdeş bir kardeş, akraba olmayan uyumlu bir verici, haploidentik aile periferik kan kök hücresi veya kemik iliği vericisi ya da HLA uyumsuz akraba olmayan kordon kanı vericisi olabilir. Baldomero ve ark. 2009 yılında 43 ülkedeki 624 merkezde yapılan HKT’lerdeki yüm yaş gruplarına ait verici kaynaklarını yayınladı; allojenik HKT’lerde akraba olmayan vericiler (%51) HLA özdeş kardeş vericilerden (%43) daha fazla idi. Otolog HKT’lerin %99’unda allojenik HKT’lerin %71’inde kök hücre kaynağı periferik kök hücre idi. Olguların %7’sinde akraba dışı vericiden kordon kanı kullanılmıştı (18). Vericinin güvenliği önde gelen bir konu olduğundan toplama öncesindeki çalışmalar özellikle itina ile sürdürülmeli, eğitimli deneyimli bir hekim tarafından yapılmalıdır. Kişi tam olarak aydınlatıldıktan ve bütün riskler tartışıldıktan sonra aydınlatılmış onam alınır. Bazı ülkelerde bu tıbbi inceleme farklı bir ekip tarafından gerçekleştirilmektedir. Bütün tıbbi kontrendikasyonlara dikkat edilmeli, hastanın gereksinimi ne kadar fazla olursa olsun hiçbir risk alınmamalıdır. Bazı ülkelerde çocuk vericiler için özel bir prosedür uygulanır. İstenmeyen olaylara ilişkin bilgilerin toplanması ve vericilerin uzun süreli takibi için merkezi bir bildirim sisteminin yerleşmesi gereklidir.
Allojenik KHT’da ideal verici HLA genotipik olarak benzer olan kardeştir. Ancak böyle bir vericinin bulunma olasılığı çalışmalara bakıldığında yaklaşık %30-40 civarındadır (19). HLA antijenleri vücudun hemen hemen her hücresinde bulunmaktadır, bu antijenler donör T lenfositleri tarafından tanınır. Bu nedenle verici ile HLA uygunsuzluğu arttıkça ve/veya akrabalık azaldıkça GVHH, rejeksiyon riskleri artacak dolayısıyla hem kullanılan immun supresyon, hem enfeksiyon riski, hem de mortalite artacaktır. Günümüzde altta yatan hastalık, hastanın yaşı, KHT’nun aciliyeti göz önüne alınarak donör seçimi yapılmaktadır, aciliyeti olmayan nakillerde en güvenli donör aranırken hastalık riskinin fazla olduğu olgularda daha az uyumlu donörler ile KHT’nin riski göze alınabilmektedir (20). Bu durum riskli nakilleri yapan merkezlerin altyapısının özellikle mikrobiyolojik inceleme olanaklarının da daha iyi olması gerekliliğini doğurmaktadır.
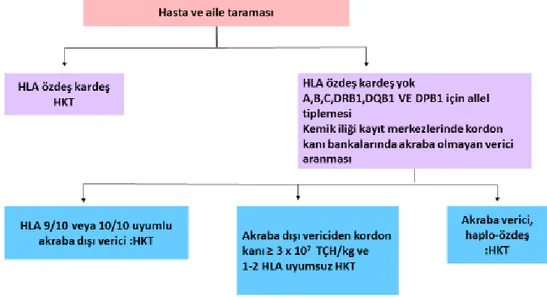
11 HLA identik kardeşin olmadığı durumlarda, HLA tam veya kısmen uygun akrabalar, dünyadaki kemik iliği verici bankalarından HLA uygun ya da kısmi uygun gönüllü vericiler bulunabilir.
Şekil 2’de Avrupa Kan ve Kemik İliği Nakli Derneği (EBMT)’nin verici seçimi algoritması görülmektedir.
Şekil 2. Verici seçimi algoritması
2.6. Transplantasyon ilişkili komplikasyonlar
Hazırlık rejimlerinde kullanılan yüksek dozlu radyoterapi ve/veya kemoterapi, alıcının bütün organlarını ve dokularını etkileyerek erken ve geç sekonder etkilere yol açar. Komplikasyon gelişmesi bireysel yatkınlık, immunsupresif tedaviler, transplant öncesi tedaviler ve nakil sırasında eşlik eden komorbid faktörlerin varlığı ile ilişkili olduğu bilinmektedir. HKT’de asıl hedef altta yatan hastalığa kür sağlamak olmasına rağmen özellikle büyümesi devam eden çocukta komplikasyonların erken tanınması, tedavisi veya önlenmesi transplant başarısını etkileyen en önemli faktörlerden biridir. HKT sonrası görülen geç ve erken komplikasyonlar şekil 3’de gösterilmiştir.
12 Şekil 3. HKT sonrası görülebilen erken ve geç dönem komplikasyonlar
2.7. HKT Sonrası Görülen Erken Komplikasyonlar
HKT sonrası erken dönemde görülen komplikasyonlar aşağıda maddelenmiştir. Graft versus host hastalığı
Enfeksiyonlar Relaps
Rejeksiyon
Karaciğerin veno-oklusiv hastalığı (VOD) Pulmoner sorunlar Kardiyak sorunlar Psikososyal Sorunlar Beslenme Sorunları Gastrointestinal Sorunları Bulantı, kusma Mukozit Diyare Kardiovasküler sorunlar Renal /Üriner sistem sorunlar Hemorajik sistit
Graft versus host hastalığı Nörolojik sorunlar
13 Enfeksiyonlar
Relaps
Sık görülen komplikasyonlara aşağıda değinilmiştir.
a. Mukozit: Yüksek dozlu tedavi ve kök hücre transplantasyonu uygulanan hastaların çoğunda ortaya çıkan önemli bir sorundur. Bu durum total parenteral nutrisyon ve opioid analjezik gereksinimde artış, hastanede yatış süresinde uzama ve enfeksiyon riskinde artış ile ilişkilendirilmiştir. TPN’nin yararlarına rağmen mukozit kendi başına önemli bir klinik sorun olarak kalmaya devam etmektedir. Mukozit hafif inflamasyondan yaygın ülserasyona kadar değişebilen, oral kavite ve sindirim sisteminin diğer bölümlerini etkileyebilen bir mukozal hasar olarak nitelenir. Oral mukozit 6 ile 12. Gün arasında zirve yapar ve engrafmanla birlikte düzelir. Mukozit mukoza bariyerinin hasarına bağlı olarak gelişen bakteriyeminin yol açtığı sistemik enfeksiyon riskinde artışla birliktedir. Mukozitin neden olduğu ağrı ve enfeksiyon önemli morbidite ve mortalite nedenidir. Tedavisi çok disiplinli bir yaklaşım gerektirir. Temel ağız bakımı ağız kökenli enfeksiyon ve enflamasyon yükünü azaltmaya yönelik olarak transplantasyon öncesinde yapılan oral muayeneyi kapsar. Hastaların çoğuna narkotik ilaçlar uygulamak gerekir. İntravenöz narkotik ilaç gereksinimi ve süresi mukozitin şiddetinin en iyi göstergelerinden biridir.
Kanama ve ağız içi enfeksiyon diğer oral komplikasyonlar arasında sayılabilir. Gingivit, periodontit derin trombositopeni sırasında kanama riskinde artışa neden olabilir. Anaerobik bakteriler, mantarlar ve virüsler gibi çok çeşitli mikroorganizmalar oral mukoza enfeksiyonlarına neden olabilir. Dental enfeksiyonlar bölgesel enfeksiyon belirtilerinin azalmış olduğu nötropeni sırasında gözden kaçabilir.
Sonuç olarak HKT öncesinde sırasında ve sonrasına ağız bakımı uygulanmalıdır. Mukozit profilaksisi ve tedavisi için çeşitli yaklaşımlar denenmiştir. Ayrı ayrı veya kombinasyon halinde kullanılabilen çok sayıda yeni ilaç klinik yarar vaat etmektedir.
b. Graft versus host hastalığı (GVHH): GVHH allojenik HKT’nin en önemli komplikasyonudur. Pediatrik olgularda erişkinlere göre risk daha düşük olmasına rağmen özellikle alternatif vericilerin kullanımının artmasıyla görülme sıklığı artmıştır. Patolojisi, verici T hücrelerinin alıcı antijenlerine karşı reaksiyon
14 geliştirmesidir. İnsanlarda geleneksel olarak akut ve kronik GVHH olmak üzere iki grupta sınıflandırılır. Akut ve kronik GVHH ayrımında genellikle başlangıç zamanı kullanılmakta ve transplant sonrası +100. günden önce gelişenler akut, +100. günden sonra başlayanlar veya devam edenler ise kronik GVHH olarak isimlendirilir.
Akut GVHH doğrudan veya dolaylı olarak allojenik HKT sonrasında kısa süreli mortalitenin başlıca sebebi olarak kalmaya devam etmektedir. Hazırlık rejiminin neden olduğu başlangıçtaki doku hasarı, daha sonra konağın antijen sunucu hücrelerinin aktivasyonu ile vericinin T hücrelerinin aktivasyonu ve çoğalması sonrasında interlökin -1 (IL-1), doku nekrozu faktörü (TNF-α) gibi sonunda doku nekrozuna neden olan faktörlerin salgılandığı üç fazlı bir sürece dayandırılmıştır. GVHH ‘nı başlatan bu patogenetik sürecin etkisi bağışıklık yanıtını engelleme yetisine sahip hücrelerin (T düzenleyici hücreler) varlığıyla kısmen yumuşatılır.
Başlıca risk faktörü HLA uyumsuzluğudur, uyumsuzluk oranı arttıkça GVHH riski artar. Yüksek çözünürlük HLA bakma yönteminin geliştirilmesi ve akraba dışı vericilerde bu yöntem ile allel düzeyinde 4 dijit 10 HLA lokusunun belirlenmesi sayesinde GVHH oranlarında belirgin düzelme sağlanmıştır (21). Graft tipi açısından her ne kadar yayınlanmış randomize kontrollü çalışma olmasa da meta-analizler periferik kök hücre nakillerinde kemik iliği nakillerine oranla akut ve kronik GVHH oranlarının daha yüksek olduğunu bildirmektedir (22). Bunun aksine pediatrik lösemi olgularının dahil edildiği geniş hasta sayısına sahip retrospektif bir kayıt çalışmasında periferik kök hücre ve kemik iliği alıcılarında akut GVHH oranları benzer bulunmuştur (23). Diğer önemli risk faktörleri ileri yaş, erkek alıcılar için kadın vericiler, vericide önceden olan alloimmunizasyon ve GVHH profilaksisidir. Yine yakın zamanda GVHH gelişiminde HLA dışı genetik faktörlerin önemi anlaşılmaya başlanmıştır. Akut GVHH’da tutulan organların ortak özelliklerinden biri de bu organların hepsinin intestinal mukoza, epidermis ve portal dolaşım üzerinden mikrobiyal patojenlere maruz kalmış olmasıdır; fareler üzerinde yapılan gastrointestinal dekontaminasyonu hedefleyen antibiyotik tedavisi alan farelerde GVHH insidansının ve şiddetinin daha az olduğu doğrulanmıştır (24). Bu tespit enfektif organizmalardan köken alan antijenlerin ve patojen tanıma reseptörlerinin etkileşimleri açısından koruyabileceği veya ona yatkınlık yaratabileceği yönünde spekülasyonlara yol açmıştır. Şu ana kadar yapılan sonuçlar çelişkilidir, bunların gerçek öneminin belirlenebilmesi için daha ileri çalışmalara ihtiyaç vardır (25). Akut GVHH ‘nın klinik belirtileri tablo 3’de özetlenmiştir. Bu sendromda hafif, kendini
15 sınırlayan bir hastalıktan, ciddi ve potansiyel olarak ölümcül hastalığa kadar değişebilen tablolar görülebilir. Allojenik transplant alıcılarının bakımı çok karmaşıktır, venookluziv hastalık, ilaç toksisitesi ve enfeksiyon gibi komplikasyonlardan ayırt edilmesi, uygun tedaviye karar verilmesi güçtür. Bu nedenle tanının bir veya daha fazla organdan biyopsi alınıp karakteristik histopatolojik özellikler doğrulanarak konması zorunludur.
Tablo 3. Akut GVHH’nin klinik belirtileri
Akut GVHH’ nin klinik belirtileri
Organ Klinik belirtiler
Deri Başlangıçta sıklıkla avuç içlerini ve ayak tabanlarını tutan eritematöz
makülopapüler döküntü
Bütün vücut yüzeyine yayılabilir Kaşıntılı ve/veya ağrılı olabilir
Ağır durumlarda, deskuamasyona yol açan büller oluşabilir
Karaciğer Belirgin sarılıkla birlikte olan veya olmayan kolestaz
Kolestaz enzimlerindeki bozukluk transaminazlardakinden daha fazladır
Gastrointestinal sistem
İştahsızlık, bulantı, kusma
İshal; tipik olarak yeşil renkli ve sulu
Ağır durumlarda dışkıda taze kan ve mukoza bulunur, buna karın ağrısı eşlik eder, bazen paralitik ileus oluşur
Bu sendromda hafif, kendini sınırlayan bir hastalıktan, ciddi ve potansiyel olarak ölümcül hastalığa kadar değişebilen tablolar görülebilir. Allojenik transplant alıcılarının bakımı çok karmaşıktır, venookluziv hastalık, ilaç toksisitesi ve enfeksiyon gibi komplikasyonlardan ayırt edilmesi, uygun tedaviye karar verilmesi güçtür. Bu nedenle tanının bir veya daha fazla organdan biyopsi alınıp karakteristik histopatolojik özellikler doğrulanarak konması zorunludur.
Tablo 4. Akut GVHH’nın evrelendirilmesi Evre Cilt Bulguları
(makülopapüler döküntüye göre)
Bilirubin düzeyi (mg/dL)
Gİ Bulguları(ishal miktarına göre)
+ Vücut yüzeyinin <%25 2-3 Diare 500-1000 mL/d
veya sürekli bulantı ++ Vücut yüzeyinin %25-50 sinde 3-6 Diare 1000-1500 mL/d
+++ Yaygın eritrodermi 6-15 Diare >1500 mL/d
++++ Yaygın eritrodermi, deskuamasyon ve büller
16 Akut GVHH sınıflaması her bir organ için 0’dan 4’e kadar evrelendirilmiş (Tablo 4) ve bu evreler birleştirilerek genel bir derece elde edilmiştir (Tablo 5).
Tablo 5. Akut GVHH genel değerlendirilmesi
Derece Evre Cilt KC Gİ Fonksiyon kaybı 0 (Yok) 0 0 0 0 I (Hafif) + - ++ 0 0 0 II (Orta) + - +++ + + + III (Ağır) ++ - +++ ++ - +++ ++ - +++ ++
IV (Hayatı tehdit edici) ++ - ++++ ++ - ++++ ++ - ++++ +++
Tedavi girişimlerine rağmen III ve IV. derece akut GVHH prognozu son derece kötüdür, oluşmasını önlemek için çaba sarf edilmektedir. Profilaksinin amacı peri ve post transplant dönemde immunsupresif ilaçlar verilmek suretiyle verici T hücre işlevinin uzun süre baskılanmasıdır. Kullanılan ajanlar; kalsinörin inhibisyonu yapan siklosporin ve takrolimus, antimetabolit olan metotreksat, DNA sentez inhibisyonu yapan mikofenolat mofetil, bir makrolid antibiyotik olan T ve B hücrelerinin aktivasyonunu önleyen sirolimustur. Profilakside alternatif yaklaşım verici T hücrelerinin poliklonal (antitimosit globülin, ATG) veya monoklonal antikorlar kullanılarak infüzyon öncesinde ex vivo veya infüzyondan önce ve/veya sonra in vivo ortadan kaldırılmasıdır. Hücresel tedaviler ile immuntolerans sağlamak mümkün olabilir ve umut verici görünmektedir. Her ne kadar yeni yaklaşımlarla olumlu sonuçlar bildiriliyorsa da hiçbirinin steroid yanıtsız olgularda genel sağ kalım üzerine belirgin düzelme sağladığı gösterilememiştir.
Kronik GVHH çocuklarda daha nadir görünmesine rağmen mortalitenin önemli nedenlerindendir. Allojenik HKT sonrasında gelişen bir bağışıklık düzenleme bozukluğu olup, otoimmunite ve bağışıklık yetmezliğinin özelliklerini paylaşır.
Vericinin bağışıklık hücreleri tarafından başlatıldığı düşünülmekle birlikte patofizyolojisi daha az anlaşılabilmiştir. Otoreaktif T lenfositlerinin anahtar rol oynadığı düşünülmesine rağmen yeni çalışmalar B hücrelerinin önemini de ortaya çıkarmıştır (26). Kronik GVHH, allojenik HKT sonrasında nükse bağlı olmayan morbidite ve mortalitenin başlıca nedenidir. Önceden akut GVHH varlığı, daha
17 yüksek HLA uyumsuzluğu derecesi, splenektomi, ileri yaş, CMV seropozitifliği, erkek alıcı için kadın donörden yararlanılması, mobilize periferik kan kök hücre grefti başlıca risk faktörleridir. Kronik GVHH’ nın klinikopatolojik sınıflandırması Tablo 6’da gösterilmiştir.
Tablo 6. Kronik GVHH’nin klinikopatolojik sınıflandırılması Sınıflandırma Kliniko-patoloji
Sınırlı Kronik GvHH'a bağlı lokal cilt tutulumu ve/veya karaciğer fonksiyon bozukluğu
Yaygın Yaygın cilt tutulumu veya lokal cilt tutulumu ve/veya karaciğer fonksiyon bozukluğu beraberinde aşağıdakilerden en az biri:
- Karaciğer biyopsisinde kronik agresif hepatit, köprüleşme nekrozu veya siroz
- Göz tutulumu (Schirmer testinde <5-mm)
- Minör tükrük bezlerinin tutulumu ya da biyopsi ile gösterilmiş oral mukoza tutulumu
- Diğer hedef organ tutulumu
c. Enfeksiyonlar: HKT yapılan hastalarda enfeksiyonlar önemli bir morbidite ve mortalite nedenidir. Son yıllarda destekleyici bakım önlemlerinde sağlanan gelişmeler, immun supresyon mekanizmalarının daha iyi anlaşılması, yoğunluğu azaltılmış hazırlık rejimlerinin, yeni antimikrobiyal ilaçların ve profilaksi uygulamalarının kullanıma girmesiyle birlikte enfeksiyonlara bağlı mortalite ve morbidite azalmıştır (27). GVHH, HKT sırasında hematolojik durum, eşlik eden hastalıklar, nötropeninin derecesi, anatomik bariyerlerin zarar görmesi, immunsupresif tedavi, B ve T hücrelerinin zarar görmesi, gecikmiş immün yeniden yapılanma, otolog nakile oranla allojenik nakil en önemli risk faktörleridir. HKT sonrasında bağışılık yetmezliği ile belirli enfeksiyonların insidansı arasında açık bir ilişki vardır. Buna göre, her birinde belirli patojenlerin ön planda olduğu üç farklı dönem söz konusudur. HKT sonrasındaki enfeksiyonların kronolojisi şekil 4 ‘de gösterilmiştir.
18 Şekil 4. HKT’de enfeksiyon haritası
Transplantasyonun her üç döneminde de enfeksiyondan korunma yöntemleri, aşılama ve farmakolojik yaklaşımların önerilen şekilde uygulanması enfeksiyöz komplikasyonların önlenmesi veya en azından azaltılması açısından önemlidir. Profilaktik antibakteriyel ajan kullanımı açısından kanıta dayalı tıp temelinde pediatrik yaş grubu için antimikrobiyal proflaksi rejimi önermek veri eksikliğinden dolayı mümkün değildir (28). Engrafman öncesi dönemde Nötropeni, ağır mukozit, santral venöz kateter varlığı invazif candidiazis riskini belirgin arttıran risk faktörleridir. Bu dönemde antibakteriyel profilaksi genel bir uygulama olmuştur. Profilaksi endojen gastrointestinal floranın eliminasyonuna ve eksojen organizmaların vücuda girişinin önlenmesine dayanır. Engrafman sonrası dönemde de kateter kullanımına devam edilir veya ağır gastrointestinal GVHH gelişir ise risk aynı oranda devam eder (29). Allojenik HKT sonrası +75.güne kadar ve GVHH varlığında immunsupresif tedavi boyunca antifungal profilaksi önerilmektedir (30). Allojenik HKT alıcılarında erken CMV replikasyonunu engellemeye yönelik yaklaşım tüm risk altındaki allojenik HKT alıcılarına engrafman sonrası posttransplant +100. Güne kadar antiviral tedavi profilaksi uygulanmasıdır (31). Çocuk hastaların sadece %25’i posttransplant dönemde viral problemlere bağlı sorun yaşamazlar (32). Geri kalan hastalarda bir veya birden çok virüsle ilişkili klinik tablo veya viremi gözlenir. Viremi çok hızlı bir şekilde çoklu organ yetersizliği yapabileceği gibi inflamatuar süreci başlatarak ve T hücrelerini aktive ederek ağır
19 GVHH tablolarına neden olabilir. Bu nedenle daha klinik bulgular ortaya çıkmadan erken dönemde pre-emptive viral tedavi günümüzde birçok nakil merkezinde rutin hale gelmiştir.
d. Karaciğerin veno-okluziv hastalığı (VOD): HKT sonrası erken dönemde hazırlık rejimi ile ilişkili karaciğer toksisitesinin sonucu olarak ortaya çıkan semptom ve bulguları ifade etmek için kullanılan terimdir. Bu sendrom HKT’den sonra ilk 35-40 gün içinde ortaya çıkan sarılık, sıvı retansiyonu ve hassasiyetin eşlik ettiği hepatomegali ile nitelenir (33). Çocuklardaki insidansı %27-40 olarak bildirilmiştir (34). Patofizolojisinde endotel hasarı, sinüzoidal fibrozis, mikrotrombüs oluşumu, fibrin depolanması rol oynar ve hepatik nekroz ile sonuçlanabilir. Deneysel modellerde toksik metabolitlerin neden olduğu endotel hasarı sonrasında meydana gelen ilk olayların sinüs endotel hücrelerinin fenestralarının kaybı, sinüs endotel hücrelerinin içinde ve arasında boşluklar oluşması, eritrositlerin Disse aralığına girip sinüsleri kaplayan hücrelerin ayrılmasına yol açmakta ve bu hücreler akım yönünde embolize olup sinüsoidleri tıkayarak hepatik venöz dışarı akımı azaltmak suretiyle postsinüzoidal hipertansiyona yol açtığı gösterilmiştir. Bu nedenle bazı yazarlar bu gözlemlere dayanarak bu komplikasyon için “sinüzoidal obtruksiyon sendromu (SOS)” teriminin kullanılmasını önermiştir (35). Gelişimi açısından tanımlanan risk faktörleri arasında hastanın 5 yaşından küçük olması, akraba dışı vericiden transplant yapılması, altta yatan hastalığın osteopetrozis veya hemofagositik lenfohistiyositoz (HLH) olması, daha önce abdominal ışınlama uygulanması, hepatik siroz varlığı, gemtuzumab kullanım hikayesi, myeloablatif rejimle ikinci transplant yapılması veya busulfan bazlı rejimlerin kullanılması sayılabilir (36). VOD tanısı klinik olarak konulmalıdır. Seattle ya da Baltimore kriterleri kullanılarak tanı konur.
Seattle kriterleri: HKT sonrası ilk 20 gün içinde şunlardan iki veya daha fazlasının bulunması: bilirubin >2 mg /dL, hepatomegali veya sağ üst kadranda ağrı, vücut ağırlığında artış (bazal ağırlığın > %2’si).
Baltimore kriterleri: HKT sonrası ilk 21 gün içinde bilirubin düzeyinin > 2mg/dL olması yanından şunlardan iki veya daha fazlasının bulunması: Ağrılı hepatomegali, asit veya vücut ağırlığında artış (bazal ağırlığın > %5’i).
20 Karaciğer ultrasonografisi, portal doppler, antitrombin III, protein C ve S düzeylerinde düşüklük, plazminojen aktivatör inhibitör düzeyinde artış, karaciğer biyopsisi tanıyı destelemek amacıyla kullanılır. VOD profilaksisi risk faktörlerinden kaçınma ve farmakolojik ajanlarla yapılır. Yalnızca çocuklarda yapılan randomize bir çalışmada defibrotide uygulanan olgularda VOD ve GVHH insidansı belirgin azalma meydana geldiği gösterilmiştir (37).
e. Pulmoner komplikasyonlar: Transplantasyon sonrası ilk 100 günde görülen erken komplikasyonlar arasında pulmoner ödem, bakteriyel, fungal ve viral enfeksiyonlar, idiyopatik pnömoni sendromu (IPS) ve diffüz alveolar hemoraji (DAH) sayılabilir.
IPS; HKT alıcılarında genellikle transplantasyonu takiben 21 gün civarı gelişir, etyolojide enfeksiyöz ajan gösterilememiş diffüz bir akciğer hasarıdır (38). Hazırlayıcı rejim toksisitesi, immünolojik hücresel hasarlanma, İnflamatuar sitokinlerin patofizyolojide rol oynadığı düşünülmektedir. Klinik bulgular arasında ateş, prodüktif olmayan öksürük, takipne, hipoksemi sayılabilir. Akciğer grafisinde diffüz alveolar veya interstisiyel infiltrasyonların görülmesi ile karakterizedir. Spesifik bir tedavisi yoktur ve sıklıkla vaka bazında düzelmeler sağlayabilen kortikosteroidler kullanılmaktadır. Anti-TNF monoklonal antikorlar ile başarılı sonuçlar bildirilmiştir.
DAH, transplantasyon sonrası ilk 30 günde görülür. Klinik bulguları dispne, takipne, prodüktif olmayan öksürük, hipoksemidir. Akciğer grafisi veya akciğer tomografisinde fokal veya yaygın infiltrasyonlar gözlenir. Bronkoalveolar lavaj (BAL) örneğinin enfeksiyon olmaksızın kanlı olması tanıyı destekler (39). Yüksek doz metilprednizolon tedavisi surviyi uzattığı gösterilmiş tek tedavi seçeneğidir. Mortalitenin yüksek olması, sitokin antagonistleri, antiinflamatuar ajanlar, rekombinant faktör VIIa gibi farklı tedavi yaklaşımlarının araştırılmasını gerekli kılmaktadır (40).
f. Kardiyak komplikasyonlar: Transplantasyon ilişkili kardiyotoksisite hem başlangıç zamanı hem de bulgular açısından çeşitlilik gösterebilir. Olguların çoğunda transplantasyon sırasında veya hemen sonrasında kardiyak işlev bozukluğu
21 gelişmekte ve bunların %50’sinde kalıcı olmaktadır. Ventrikül işlev bozukluğu, iletim bozuklukları, perikardiyal veya damarsal anormallikler gibi farklı kardiyak hasarlanmalara ait değişik klinik bulgular görülebilir (41).
2.8. HKT Sonrası Görülen Geç Komplikasyonlar
Her yıl yapılan transplantasyon sayısının artmasıyla HKT tedavisi uygulanan hastalarda uzun süreli sağkalım dönemi giderek daha fazla önem kazanmaktadır. HKT’nin temel amacı primer hastalığın tedavisidir. Uzun süreli sağkalım elde eden bireyler normal sağlık durumuna dönmeyi, yeterli fiziksel ve psikolojik işlevlere sahip olmayı beklemektedir. Allojenik HKT uygulanan hastalarda uzun süreli sağkalım olasılığı hasta özelliklerine (yaş, cinsiyet, HKT öncesinde eşlik eden hastalık), primer hastalığa, hastalığın risk kategorisine, transplantasyon öncesindeki remisyon durumuna, hazırlık rejimine, kullanılan hücre kaynağına, GVHH başlangıcına ve tedavisi için kullanılan ilaçlara bağlıdır (42). Transplantasyon sonrasındaki ilk üç aydan sonra ortaya çıkan etkiler geç etkiler olarak tanımlanırlar, uzun süreli sağkalım sırasında sağlığı kısıtlarlar. HKT sonrası görülebilen geç komplikasyonlar aşağıda özetlenmiştir:
Endokrin bozukluklar (hipotiroidi, puberte gecikmesi, gonad yetersizliği, büyüme gelişme geriliği)
İkincil maligniteler Katarakt
Böbrek yetersizliği
Obstrüktif ve restriktif akciğer hastalığı Kardiyomyopati
Aseptik nekroz, osteopeni Lökoansefalopati
İmmunolojik disfonksiyon
Post trasnsplantasyon lenfoproliferatif hastal›k Diş bozuklukları
Bu çalışmanın araştırma konusu olan HKT yapılan çocuklarda solunum komplikasyonları ayrıntılı olarak aşağıda incelenmiştir.
22 Enfeksiyona bağlı olmayan solunum yolu komplikasyonları; akciğerler üzerindeki malign olmayan geç etkiler obstruktif ve restriktif sorunları kapsar (43). Pediatrik yaş grubunda daha nadir görülmekle birlikte, transplant ilişkili mortalitenin önemli nedenlerindendir (44). HKT sonrasında hava yollarını ve akciğer parankimini etkileyen geç başlangıçlı, enfeksiyöz olmayan pulmoner komplikasyonlar sık olup, genellikle post-transplant 3 ay- 2 yıl arası dönemde ortaya çıkarlar, fakat işlevsel sonuçları yıllarca devam edebilir. En sık görülen geç pulmoner komplikasyonlar bronşiolitis obliterans, kriptojenik organize pnömoni, idiyopatik pnömoni sendromudur.
Bronşiolitis obliterans esas olarak küçük hava yollarını etkileyen ve inflamatuar olmayan bir hasarla nitelenen ağır bir obstruktif pulmoner hastalıktır. Çocuklarda genellikle akut alt solunum yolu epitelindeki hasarın ardından distal hava yollarının obstrüksiyonu ve inflamatuar değişiklikler ile tanımlanan ağır bir sekeldir. İleri evrelerde progresif peribronşiyoler fibrozis nedeniyle restriktif işlevsel değişiklikler de eklenebilir. Bronşiolitis obliterans kronik GVHH’nın başlıca pulmoner belirtisi olarak kabul edilir. Uderzo ve ark.’nın çalışmasında çocuklarda transplantasyon sonrası
5. yılda akciğer yetmezliğinin kümülatif insidansı %35 olarak bulunmuştur (45). HKT sonrası bronşiolitis obliterans insidansını belirten az sayıda çalışma vardır. Ghali ve ark.’nin yaptığı bir çalışmada HKT sonrası BO insidansı %2-6 arasında verilmiştir (46). Kriptojenik organize pnömoni, bronşiyolleri, alveolar duktusları ve alveolleri etkileyen bir klinikopatolojik sendrom olup restriktif özellikte bir solunum sistemi komplikasyonu olarak ortaya çıkar. Esas olarak post transplant 1-12 aylar arasında ortaya çıkar ve insidansı < %2’dir. Kriptojenik organize pnömoni ile GVHH arasında kuvvetli bir ilişki vardır, genellikle transplantasyon sonrasındaki ilk 120 gün içinde ortaya çıkan idiyopatik pnömoni sendromu ise TBI ve GVHH ile ilişkilidir.
Bronşiolitis obliterans klinik gelişimi genellikle sinsi olup; kuru öksürük, ilerleyici nefes darlığı ve wheezing gibi belirtilerle birliktedir. Solunum fonksiyon testlerinde FEV1 değerinin transplantasyon öncesi değere göre > %20 azalması veya öngörülen FEV1’in %80 ‘in altına inmesi alarm işareti olmalıdır. İnspirasyon ve ekspirasyon fazında alınan yüksek çözünürlüklü BT görüntülerinde karakteristik bir mozaik görünümü tespit edilir.
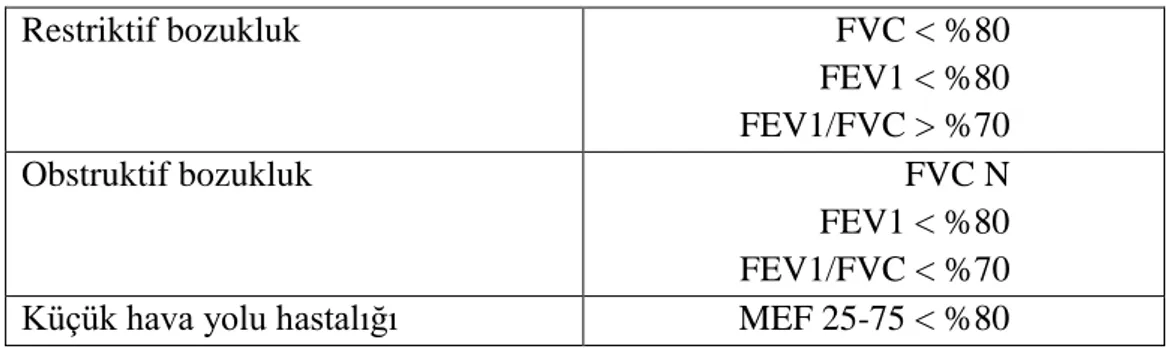
23 Restriktif tip akciğer patolojilerinde ise hazırlayıcı rejim ilişkili özellikle de TBI sonrası olup, FVC’de düşüklük (%80) ve FEV1/FVC oranında ≥ %70 oranında artış ile karakterizedir.
Tüm kılavuzlarda asemptomatik olgularda dahi pulmoner anormallikler açısından takibin yapılması önerilmekte, solunum fonksiyon testlerinin geç dönem enfeksiyon dışı pulmoner komplikasyonları belirlemede ve takipte güvenli bir yöntem olduğu vurgulanmaktadır (47).
HKT yapılan hastalarda solunum kompikasyonlarını daha iyi değerlendirmek için solunum fizyolojisi ve fizyopatolojisi tartışılmıştır.
2.9. Solunum Fizyolojisi
Solunum sisteminin dört ana fonksiyonu;
• Atmosfer ve alveoller arasında havanın giriş çıkışı anlamına gelen akciğer ventilasyonu,
• Alveoller ve kan arasında oksijen ve karbondioksitin difüzyonu,
• Kan, vücut sıvıları ve dokular arasında oksijen ve karbondioksitin taşınması, • Ventilasyonun düzenlenmesidir.
Akciğerler iki şekilde genişletilip daraltılabilir;
1. Diyafragmanın aşağı ve yukarı hareketiyle göğüs kafesi uzar ve kısalır, 2. Kostaların yükselmesi ve aşağı çekilmesi ile göğüs ön-arka çapı artar ve azalır.
Normal sakin bir solunum neredeyse tamamen diyafragmanın hareketiyle gerçekleşir. İnspirasyonda diyafragma kasılır ve akciğerlerin alt yüzünü aşağı çeker. Ekpirasyonda ise diyafragma basitçe gevşer, göğüs duvarı, abdominal yapılar ve akciğerler elastik bir şekilde geri çekilirken (recoil) akciğerlere baskı artar ve hava dışarı atılır. Göğüs kafesini yukarı kaldıran bütün kaslar inspirasyon kaslarıdır. Bunlar içinde en önemli olanları eksternal interkostal kaslardır. Ancak diğer yardımcı kaslardan, sternokleidomastoid kas sternumu, anterior serratus kaslar ise kostaların çoğunu, skalen kaslar da ilk iki kostayı yukarı kaldırarak inspirasyona yardım ederler. Ekspirasyon sırasında göğüs kafesini aşağı çeken başlıca kaslar ise, rektus abdominalis ve internal interkostal kaslardır (48). Akciğerler balon gibi sönebilecek elastik bir yapıdadır ve şişmeyi sağlayacak herhangi bir güç olmadığında trakea aracılığıyla içindeki havanın tamamını dışarı verir. Aynı zamanda, akciğerler ile
24 göğüs kafesi arasında, hiler bölge dışında, herhangi bir bağlantı yoktur. Akciğerler göğüs boşluğunda, etrafını saran plevral sıvının kayganlaştırıcı etkisiyle hareket eder ve bu boşlukta yüzer. Viseral ve paryetal plevra arasındaki fazla sıvının lenfatik kanallardan sürekli olan drenajı, düşük basınçlı bir vakum etkisi yapar. Bu sebeple, akciğerler göğüs boşluğuna yapıştırılmış gibi durur ve göğüs kafesi genişleyip daraldıkça bu kayganlaştırıcı sıvının içinde serbestçe hareket eder. Plevral basınç; akciğerler (viseral plevra) ve göğüs duvarı plevrası arasındaki boşlukta yer alan sıvının yarattığı hafif negatif bir basınçtır. İnspiryumun başında normal plevral basınç -5cm H2O’dur ve bu akciğerleri dinlenirken açık tutmak için yeterli basınçtaki
emilim gücüdür. İnspiryuma devam ederken göğüs kafesinin genişlemesi akciğerleri dışarı iter ve ortalama negatif basınç etkisi yaklaşık -7.5cm H2O’ya yükselir.
Alveolar basınç, akciğer alveollerinin içindeki havanın basıncıdır. Glottis açıldığında akciğerlere hava giriş çıkışı olmazsa, akciğer ve solunum sistemi ağacının alveollerine kadar olan basınç, atmosferik basınca eşittir ve bu da 0cm H2O’dur.
İnspiryumda alveollerin içine çekilecek şekilde hava akımı yaratmak için, alveollerdeki basınç hafifçe atmosferik basıncın altına- yaklaşık -1cm H2O’ a
düşmelidir. Bu hafif negatif basınç 2 saniyede 500 ml havayı akciğerlere çekmek için yeterlidir. Ekspiryum sırasında ise tam tersi gerçekleşir. Alveolar basınç +1cm H2O’ya yükselir ve 2-3 saniye içinde akciğerlerden 0.5 litre hava dışarı verilir.
Plevral basınç ve alveolar basınç arasındaki farka transpulmoner basınç denir. Akciğerlerin dış yüzeyindeki basınç ile alveollerin içindeki basıncın farkıdır. Kompliyans; her birim basınç artışının neden olduğu volüm artışı olarak ifade edilir. Bir başka tanımlama ile; esneyebilme kabiliyetidir. Bu, toraks ve akciğerlerde farklıdır. Çocuklarda yetişkinden farklı olan kompliyans, doğumdan itibaren değişim gösterir. Değişim elastin ve surfaktan miktarı ile ilgilidir. Kompliyans açısından akciğer ve toraksı birbirinden ayırmak güçtür. Bu durumda total akciğer kompliyansından bahsedilir. Çocukların akciğer kompliyansı yetişkinlere göre düşüktür. Çünkü farklı yapıda alveol, elastin ve surfaktan vardır. Çocuklarda alveoller küçük ve duvar kalınlığı daha fazla olduğundan alveolar yapı daha büyük bir etkiye sahiptir. Daha az elastin, daha az akciğer esnekliği ve daha fazla kollaps ihtimaline neden olur. Elastin miktarı azaldığında ekspiryum sonlanmadan önce hava yolları kollabe olur. Ayrıca kapanma hacmi, fonksiyonel rezidüel kapasiteden (FRC) daha büyük olur. Bu durum da intrapulmoner şant yaratır. Doğumda elastin yalnızca