T.C.
İNÖNÜ ÜNİVERSİTESİ FEN BİLİMLERİ ENSTİTÜSÜ
SANDVİÇ FTALOSİYANİN İÇEREN DENDRİMERLERİN SENTEZİ VE ÖZELLİKLERİNİN İNCELENMESİ
Ebru YABAŞ
YÜKSEK LİSANS TEZİ KİMYA ANABİLİM DALI
MALATYA Temmuz 2005
Fen Bilimleri Enstitüsü Müdürlüğü’ne
Bu çalışma jürimiz tarafından Kimya Anabilim Dalında Yüksek Lisans tezi olarak kabul edilmiştir.
Doç. Dr. Sinan SAYDAM
Başkan
Doç. Dr. Mustafa SÜLÜ Doç. Dr. İsmail ÖZDEMİR
Üye Üye
Onay
Yukarıdaki imzaların adı geçen öğretim üyelerine ait olduğunu onaylarım.
.../….../……....
Prof. Dr. Ali ŞAHİN
ÖZET
Yüksek Lisans Tezi
SANDVİÇ FTALOSİYANİN İÇEREN DENDRİMERLERİN SENTEZİ VE ÖZELLİKLERİNİN İNCELENMESİ
Ebru YABAŞ
İnönü Üniversitesi Fen Bilimleri Enstitüsü
Kimya Anabilim Dalı
ix + 60 sayfa
2005
Danışman: Doç.Dr.Mustafa SÜLÜ
4-(2-dimetilaminoetilsülfonil)ftalonitril in, 2-(dimetilamino)etanol de
sikliktetramerizasyonu ile simetrik tetrakis(2-dimetilaminoetilsülfonil)ftalosiyanin
hazırlandı. Trietil metantrikarboksilat ın sodyum tuzunun (NaC(CO2C2H5)3),
tris(hidroksimetil)aminometanın (tris) (H2NC(CH2OH)3) ve hekzil bromürün sırasıyla
simetrik ftalosiyanin ile reaksiyonuyla birinci, ikinci ve üçüncü jenerasyon metalsiz
dendritik ftalosiyanin hazırlandı. Simetrik ftalosiyanin lityum tuzu, dendritik
ftalosiyanin ve Lu(OAc)3.nH2O veya Eu(OAc)3.nH2O karışımının 1-oktanol da
ısıtılmasıyla dendritik sandviç ftalosiyanin bileşikleri hazırlandı. Hazırlanan bileşikler
N N N N N N NLi LiN S N(Me)2 S (Me)2N S N(Me)2 S (Me)2N O CH3 O CH3 O CH3 O O N H O CH3 NH O CH3 O O N H O S CH3 O C H3 CH3 O CH3 N(Me)2 S N(Me)2 S (Me)2N S O CH3 O CH3 O CH3 O O NH O CH3 N H O CH3 O O N H O S CH3 O CH3 CH3 O CH3 O C H3 O C H3 O C H3 O O N H O C H3 N H O C H3 O O N H O S C H3 O C H3 C H3 O C H3 O C H3 O C H3 O C H3 O O N H O C H3 NH O C H3 O O NH O S C H3 O CH3 CH3 O C H3 (Me)2N S N N N N N N N N Lu N N N N N N N N N N N N N N NH HN O CH3 O CH3 O CH3 O O N H O CH3 NH O C H3 O O N H O S C H3 O C H3 C H3 O CH3 O C H3 O C H3 O C H3 O O NH O C H3 NH O CH3 O O NH O S CH3 O CH3 CH3 O C H3 O CH3 O CH3 O CH3 O O NH O CH3 N H O CH3 O O N H O S CH3 O CH3 CH3 O CH3 O C H3 O C H3 O C H3 O O N H O C H3 NH O C H3 O O N H O S C H3 O C H3 C H3 O C H3 (Eu) 1-oktanol 200oC + Lu(OAc)3.nH2O veya Eu(OAc)3.nH2O
Anahtar Kelimeler: Ftalosiyaninler, Sandviç Ftalosiyaninler, Dendritik Ftalosiyaninler Lutesyum, Evropiyum
ABSTRACT
Master Thesis
INVESTIGATION OF PROPERTIES AND SYNTHESIS OF DENDRIMERS CONTAINS SANDWICH PHTHALOCYANINE
Ebru YABAŞ
Inönü University
Graduate School of Natural and Applied Sciences Department of Chemistry
ix + 60 sayfa
2005
Supervisor: Assoc.Prof.Dr.Mustafa SÜLÜ
Symmetric tetrakis(2-dimethylaminoethylsulphanyl)phthalocyanine was
prepared cyclotetramerization of 4-(dimethylaminoethylsulphanyl)phthalonitrile in
2-(dimethylamino)ethanol. First, second and third generation metal-free dendritic
phthalocyanine were obtained by the reaction of symmetric phthalocyanine and triethyl
methanetricarboxylate sodium salt (NaC(CO2C2H5)3),
tris(hidroksomethyl)-aminomethane (tris) (H2NC(CH2OH)3) and hexyl bromide, respectively. The dendritic
sandwich phthalocyanines were prepared by heating the mixture of Lithium salt of
symmetric phthalocyanine, dendritic phthalocyanine and Lu(OAc)3.nH2O or
Eu(OAc)3.nH2O in 1-octanol. Prepared compounds were characterized by 1H-NMR,
N N N N N N NLi LiN S N(Me)2 S (Me)2N S N(Me)2 S (Me)2N O CH3 O CH3 O CH3 O O N H O CH3 NH O CH3 O O N H O S CH3 O C H3 CH3 O CH3 N(Me)2 S N(Me)2 S (Me)2N S O CH3 O CH3 O CH3 O O NH O CH3 N H O CH3 O O N H O S CH3 O CH3 CH3 O CH3 O C H3 O C H3 O C H3 O O N H O C H3 N H O C H3 O O N H O S C H3 O C H3 C H3 O C H3 O C H3 O C H3 O C H3 O O N H O C H3 NH O C H3 O O NH O S C H3 O CH3 CH3 O C H3 (Me)2N S N N N N N N N N Lu N N N N N N N N N N N N N N NH HN O CH3 O CH3 O CH3 O O N H O CH3 NH O C H3 O O N H O S C H3 O C H3 C H3 O CH3 O C H3 O C H3 O C H3 O O NH O C H3 NH O CH3 O O NH O S CH3 O CH3 CH3 O C H3 O CH3 O CH3 O CH3 O O NH O CH3 N H O CH3 O O N H O S CH3 O CH3 CH3 O CH3 O C H3 O C H3 O C H3 O O N H O C H3 NH O C H3 O O N H O S C H3 O C H3 C H3 O C H3 (Eu) Lu(OAc)3.nH2O veya Eu(OAc)3.nH2O 1-octanol 200oC +
Key Words: Phthalocyanines, Sandwich Phthalocyanines, Dendritic Phthalocyanines, Lutetium, Europium.
TEŞEKKÜR
Bu çalışmanın seçiminde, planlanmasında ve yürütülmesinde bana yön veren, çalışmam boyunca yakın desteğini ve bilimsel yardımlarını bir an olsun eksiltmeyen, yerinde yaptığı uyarılar ile yol göstererek bana güç ve moral veren çok değerli hocam Doç.Dr.Mustafa SÜLÜ’ye;
Deneysel çalışmalarım sırasında desteğini esirgemeyen Kimya Bölümü Biyokimya Anabilim dalından Arş.Grv. Burhan ATEŞ’e;
Bu günlere gelmemde büyük emekleri olan, bana her konuda sonsuz destek veren sevgili AİLEM’e;
teşekkür ederim…
Bu çalışma İnönü Üniversitesi Bilimsel Araştırma Projeleri Birimi tarafından 2004/34 nolu proje olarak desteklenmiştir.
İÇİNDEKİLER ÖZET i ABSTRACT iii TEŞEKKÜR v İÇİNDEKİLER vi ŞEKİLLER DİZİNİ vii ÇİZELGELER DİZİNİ viii SİMGELER VE KISALTMALAR ix 1. GİRİŞ 1
1.1. Ftalosiyaninlerin Genel Sentez Yöntemleri 4
1.2. Dimer, Trimer ve Sandviç Ftalosiyaninler 5
1.3. Dendritik Ftalosiyaninler 10
1.3.1. Dendrimerlerin Tanımı 10 1.4. Ftalosiyaninlerin Saflaştırılması 15
1.5. Ftalosiyaninlerin Elektronik Spektrumları 17 1.6. Ftalosiyaninlerin Uygulama Alanları 18
2. MATERYAL VE YÖNTEM 21
2.1. Kullanılan Cihazlar 21
2.2. Kimyasal Maddeler 21
2.3. Bileşiklerin Sentezi 21
2.4. Dendritik Metalsiz Ftalosiyanin Sentezi 21
2.5. Metalli Ftalosiyanin Sentezi 26
2.6. Dendritik Sandviç Ftalosiyanin Sentezi 28
3. SONUÇ VE TARTIŞMA 31 3.1. Dendritik Metalsiz Ftalosiyaninlerin Sentezi 31
3.2. Metalli Ftalosiyanin Sentezi 46
3.3. Sandviç Metalli Ftalosiyanin Sentezi 52
4. KAYNAKLAR 57
ŞEKİLLER DİZİNİ
Şekil 1 Dendrimerlerin Sentez Yöntemi-1 11
Şekil 2 Dendrimerlerin Sentez Yöntemi-2 13
Şekil 3 Ftalosiyaninlerin UV-VIS geçişleri 17
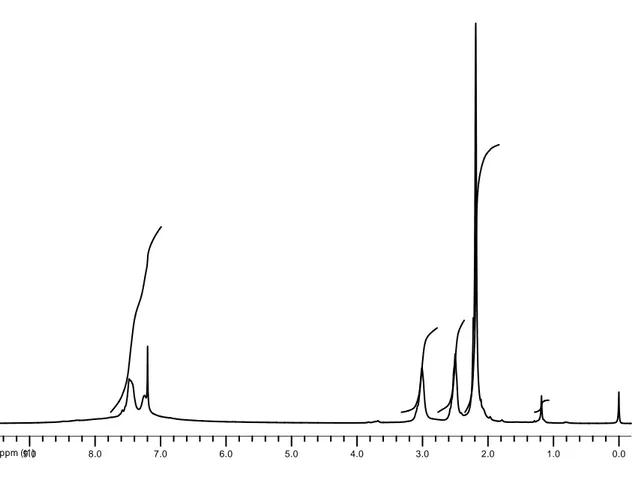
Şekil 4 2 bileşiğinin 1H-NMR spektrumu (CDCl3) 32
Şekil 5 2 bileşiğinin UV-VIS spektrumu (CHCl3) 33
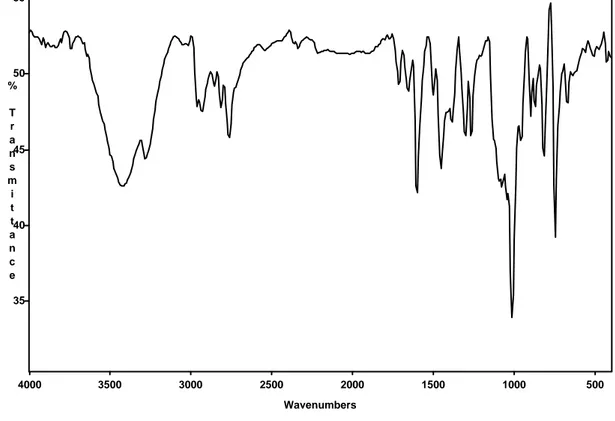
Şekil 6 2 bileşiğinin IR spektrumu 34
Şekil 7 3 bileşiğinin UV-VIS spektrumu 36
Şekil 8 4 bileşiğinin 1H-NMR spektrumu (DMSO-d6) 38
Şekil 9 4 bileşiğinin UV-VIS spektrumu (CHCl3) 39
Şekil 10 4 bileşiğinin IR spektrumu 39
Şekil 11 5 bileşiğinin 1H-NMR spektrumu (DMSO-d6) 41
Şekil 12 5 bileşiğinin UV-VIS spektrumu (CHCl3) 41
Şekil 13 5 bileşiğinin UV-VIS spektrumu (DMSO) 42
Şekil 14 5 bileşiğinin IR spektrumu 42
Şekil 15 6 bileşiğinin 1H-NMR spektrumu (CDCl3) 44
Şekil 16 6 bileşiğinin D2O yerdeğiştirme 1H-NMR spektrumu (CDCl3) 45
Şekil 17 6 bileşiğinin 1H-NMR spektrumu (DMSO-d6) 45
Şekil 18 6 bileşiğinin UV-VIS spektrumu (CHCl3) 46
Şekil 19 6 bileşiğinin IR spektrumu 47
Şekil 20 7 bileşiğinin IR spektrumu 48
Şekil 21 8 bileşiğinin 1H-NMR spektrumu (DMSO-d6) 49
Şekil 22 8 ve 10 bileşiklerinin UV-VIS spektrumu (DMSO, ---- LuPc, 8 , ___ LuPc
2, 10)
49
Şekil 23 8 bileşiğinin IR spektrumu 50
Şekil 24 9 bileşiğinin 1H-NMR spektrumu (DMSO-d6) 51
Şekil 25 9 ve 11 bileşiklerinin UV-VIS spektrumu (DMSO, ---- EuPc, 9 , ___ EuPc
2, 11)
51
Şekil 26 9 bileşiğinin IR spektrumu 52
Şekil 27 10 bileşiğinin 1H-NMR spektrumu (CDCl3) 54
Şekil 28 10 bileşiğinin IR spektrumu 55
ÇİZELGELER DİZİNİ
Çizelge 1. Bileşiklerin 1H-NMR spektrumlarının sonuçları 33 Çizelge 2. Bileşiklerin UV-VIS spektrumlarının sonuçları 34
SİMGELER VE KISALTMALAR NMR s Singlet d Dublet t Triplet m Multiplet br Geniş IR s Keskin m Orta şiddet w Zayıf br Geniş Kimyasallar Et2O Dietileter THF Tetrahidrofuran Pcs Ftalosiyaninler H2Pc Metalsiz ftalosiyanin DBU 1,8-Diazabisiklo[5.4.0]undec-7-ene
LDA Lityum diizopropil amid
DCC Disikloheksilkarbodimid HOBt 1-Hidroksibenzotriazol
1.GİRİŞ
Ftalosiyaninler (Pcs) ilk olarak tesadüfen 1907 yılında Braun ve Tcherniac adlı araştırmacılar tarafından o-siyanobenzamidin yüksek sıcaklıkta ısıtılması sonucu sentezlenmiştir [1]. 1936’da Robertson tarafından ftalosiyanin yapısı, X-ışını difraksiyonu analiziyle aydınlatılmıştır. D4h simetrisine sahip ftalosiyaninler, kararlı
π-konjuge sistemine sahiptir [2]. Ftalosiyanin ve türevleri, mavi ve yeşil renklerinden dolayı renklendirici olarak yaygın kullanılmalarının yanı sıra ilginç katalitik, elektronik ve optik özelliklerinden dolayı da çok farklı uygulama alanında görülmektedir [3, 4].
Ayrıca ftalosiyaninler, yüksek termal kararlılığa sahiptirler ve genellikle 550°C civarında erimeden süblimleşirler. Çok yönlü ve kararlı bir bileşik sınıfından olan ftalosiyaninlerin sübstitüent içermeyen türevleri su ve organik çözgenlerde son derece az çözünürler. Fakat, halkaya sübstitüentlerin (crown eter, alkil grupları, gibi) bağlanmasıyla ftalosiyaninlerin çözünürlükleri fark edilir şekilde artırılabilmektedir [1].
C32H18N8 molekül formülüne sahip ftalosiyaninlerin metalli ve metalsiz
türlerinin açık yapıları aşağıda gösterilmiştir [1].
Metalli ve metalsiz ftalosiyanin halkalarına sübstitüentler; 1,2,3,4,8,9,10,11,15,16,17,18,22,23,24,25 numaralı uçlarından bağlanabilirler.
1 2 3 4 5 6 7 8 9 1 0 1 1 1 2 1 3 1 4 1 5 N N N N N N N N 1 6 1 7 1 8 1 9 2 0 2 1 2 2 2 4 2 5 2 6 2 7 2 8 2 3 H H N N N N N N N M N C M e ta lli P c ( C3 1H1 6N8M ) M e talsiz P c ( C3 2H1 8N8) 1 2
R R R N N N N N N N M N R
Halka üzerinde bağlı olan R gruplarının konumları net olarak belli değildir. Birbirine göre simetrik olmayan uçlardan bağlı R grupları içeren ftalosiyaninler, izomer karışımları şeklinde elde edilirler. Yaygın olarak kullanılan R grupları; t-bütil, trimetilsily, n-alkil, dallanmış alkil, alkoksi, alkoksimetilen, alkilsülfonil, fenilsülfonil ve amino grupları gibi elektron sağlayıcı gruplar yada Cl, Br, NO2 gibi elektron çekici
gruplardır [1].
Ayrıca ftalosiyaninlerin birçok ana grup ve geçiş metalleriyle de türevleri hazırlanmıştır. Ağırlıklı olarak, Zn, Co, Cu, Rh, Ru gibi metallerle monomer, dimer, trimer ftalosiyaninler çalışılmıştır [5, 6].
R R R R R R N N N N N N N N N N N N N N N M N M
La, Eu, Lu, Th, U gibi Lantanid ve Aktinidlerle de double-decker ve triple-decker ftalosiyanin türleri çalışılmıştır [7-11].
N N N N N N N N R R R R N N N N N N N N M R R R R
Özellikle, monomerik, dimerik ve trimerik yapılarda ftalosiyanin halka büyüklüğüne uygun Zn, Co gibi metal merkezlerinin seçilmesiyle çok daha kararlı yapılar elde edilir [7].
N N N N N N N M N
Bunun yanında, dendrimer ftalosiyanin üzerine de ilginç çalışmalar vardır.Son zamanlarda, yeni fiziksel, elektrokimyasal, optik, fotofiziksel/fotokimyasal, biyolojik ve katalitik özelliklere sahip dendrimer ftalosiyanin türleri ortaya çıkmaya başlamıştır [2-4].
Bir veya daha fazla ftalosiyanin içeren dendrimerler çalışılmış olmasına rağmen, sandviç türü ftalosiyanin içeren dendrimerler çalışılmamıştır. Bu nedenle lantanit katyonu içeren sandviç türü ftalosiyanin merkezli dendrimerlerin hazırlanması ve özelliklerinin incelenmesi hem teknolojide hem de ftalosiyanin ve dendrimer kimyasında oldukça önemlidir.
1.1.Ftalosiyaninlerin Genel Sentez Yöntemleri
Metalsiz ftalosiyaninin ilk sentezi, o-siyanobenzamidin etanolde geri soğutucu altında kaynatılması sonucu gerçekleştirilmiştir ve verim çok düşüktür [1]. Metalsiz ftalosiyaninler, ftalonitril veya diiminoizoindol türevlerinin N,N-dimetilaminoetantiyol gibi çözücülerde siklikkondenzasyonuyla elde edilmektedir [1, 12-14].
C N C N R R R R N N N N N N N N R H H M e2N(CH2)2OH NH NH N R R H H H N N N N N N N N R R R R R R R R Me2N(CH2)2OH
Metalli ftalosiyaninler ise bu başlangıç bileşiklerinin metal tuzları ile DMF, amil alkol gibi çözgenlerde ısıtılmasıyla elde edilmektedir. Ayrıca farklı sübstitüentli dinitrillerin ve diiminoizoindollerin karışık kondenzasyonuyla asimetrik ftalosiyaninler hazırlanmaktadır [1, 12-15].
C N C N R R R R N N N N N N N M N R DM F (M )+ NH NH NH NH NH NH N N N N N N NH HN + R1 R2 R2 R1 R2 R2
1.2.Dimer, Trimer ve Sandviç Ftalosiyaninler
Monomerik türler yanında, birden fazla ftalosiyanin merkezi içeren dimerik ve trimerik yapıda birçok ftalosiyanin bileşiğide bilinmektedir. Bunlar aşağıda sınıflandırılmıştır.
1-) Köprü konumunda bir grupla birbirine bağlı metalli ftalosiyanin dimerleri;
X N N N N N N N N M N N N N N N N N M
Bu tür yapılarda kullanılabilecek bağlayıcı gruplar; O, N, C, I2, naftalin,
antrasen, taç eter, gibi gruplardır. Metal merkezi olarakta; Al, Si, Mn, Fe, Ru, Sb, Bi, Co, Cr gibi metaller kullanılabilir [7].
N N N N N N N N N N N N N N N N C o C o
2-) Direkt olarak aromatik halka üzerinden bağlanan dimerler;
R R R R R R N N N N N N N N N N N N N N N M N M M:H2, Cu, Zn, Mg, Fe
R:H, CH3, propil, tBu, 1-naftil, CH3CONH-
Bu tür dimerlerde, 1, 2, 4, 5-tetrasiyanobenzenin (yada bunun izoindol türevinin), ftalonitrilin (yada izoindolün) fazlasıyla reaksiyonundan elde edilebilir [7].
N N N N N N N N R R R R N N N N N N N N M R R R R
Bu tür yapılarda; uç grup olarak; -C10H21, -CH2OC6H13, -OC9H17 gibi gruplar
kullanılırken, metal merkezi olarak; İtriyum, Zirkonyum, Hafniyum, Kalay, İndiyum, Titanyum, Civa, Bizmut gibi yüksek koordinasyona ulaşılabilecek metaller kullanılır. Lantanid ve aktinid türevleri de ağırlıklı olarak çalışılmıştır [3, 7-11]. Bu türlerin hazırlanmasında en basit yöntem; bir metal tuzu ve ftalonitril karışımının 280-290°C’de ısıtılmasıdır.
Birçok X-ışını kristallografik çalışması; iki ftalosiyanin düzleminin çekirdekleri arasındaki uzaklığın 2.70±0.04Å olduğunu ve çoğunlukla bikonkav yapı gösteren
saucer-shaped şekli oluşturduğunu göstermiştir. Bu düzlemler, biribirlerine göre ~42°’lik bir açıyla merkez etrafında dönerler [7, 27].
İki ftalosiyanin düzlemi arasındaki bükülme açısı çoğu kez lantanid metal merkezinin büyüklüğüne bağlıdır. Bazı lantanid metalleri arasında, daha küçük olanlar daha büyük bükülme açısına sahiptir.
Ayrıca bis(ftalosiyaninato)lantanid(III) komplekslerinin, iki ftalosiyanin halkası üzerinde delokalize olmuş bir π-orbitalinde ortaklanmamış bir elektron bulunduğu için kararlı radikaller oluşturduğu bilinir. Katı fazda bu kompleksler, ortaklanmamış bu elektron yüzünden iletkenlik gösterirler. Bu ilginç özellikleri yüzünden bis(ftalosiyaninato)lantanid(III) kompleksleri, moleküler iletken teller ve molekül-based magnetlerin yapımında kullanılırlar [8].
Son çalışmalarda elektrokromik etki özelliğine sahip sandviç türü dimerik dilutesyum ftalosiyanin sentezlenmiştir [16, 17].
4-) Yine, bir grupla birbirine düzlemsel şekilde bağlı ftalosiyaninler de çalışılmıştır.
Trimer yapılar olarakta,
-Bir halka etrafında bağlanmış ftalosiyanin trimerleri çalışılmıştır [18].
N N N N N N N N N N N N N N N N N N N N N N N N M M M
O O O (CH2)6 O O O (CH2)6 O-(CH2)n M R' R' R' R' R' R' N N N N N N N M N R R R R R R N N N N N N N N Me R Me R R R R R (CH2)nO N N N N N N N M N
-Organik çözgenlerde çözünebilen trimer ftalosiyanin türüde çalışılmıştır [15].
N H NH NH N N N S S S S S S N N N N N N N N Zn S S S S S S N N N N N N N N Zn S S S S S S N N N N N N N N Zn
-Triple-decker türü ftalosiyanin trimerleri de hazırlanmıştır. Bu türler, 4:1 oranında H2Pc ve lantanid tuzlarının reflaksı sonucu elde edilebilir [20].
X-ışını sonuçları, bu yapıdaki üç halkanın ana düzlemlere tamamen paralel ve M-M aksisine tamamen dik olduğunu göstermiştir. Dıştaki ftalosiyanin halkaları, dışa doğru bükülmüştür [21].
1.3.Dendritik Ftalosiyaninler
1.3.1.Dendrimerlerin Tanımı
Dendrimerler, bir merkez içeren, tekrarlanan birimlerden oluşan ve belli bir molekül ağırlığı olan makromoleküllerdir [3, 4, 22].
On yıldan fazla bir sürede, yeni dendrimerlerin sentezi aktif araştırma alanlarından biridir ve farklı fonksiyonel merkez içeren türleri, ilgi çekmektedir, örneğin; porfirin, ftalosiyanin gibi merkez içeren dendrimerler. Bu ilginin artmasının nedeni ftalosiyanin çekirdeğine uygun sübstitüentlerin takılmasıyla yapının kontrol edilebilmesidir. Bu kontrol, ftalosiyanin halkasının optik ve elektronik özelliklerinin takip edilmesine yardımcı olur. Ftalosiyanin içeren dendrimerler, şeffaf, sağlam ve camsı katılar oluşturma kabiliyetine de sahiptirler. Katı fazdaki moleküler dizilim, ftalosiyanin halkasına bağlı dendritik uçların büyüklüğü, sayısı ve pozisyonuyla kontrol edilir [3, 23].
Ftalosiyanin dendrimerleri başlıca iki farklı yöntemle sentezlenir,
I-) Dendrimer sentezi merkezden başlayarak dışarı doğru kademe kademe büyütülür. Bu yöntem kullanılarak ilk sentezlenen dendritik ftalosiyanin türü, Şekil 1'de
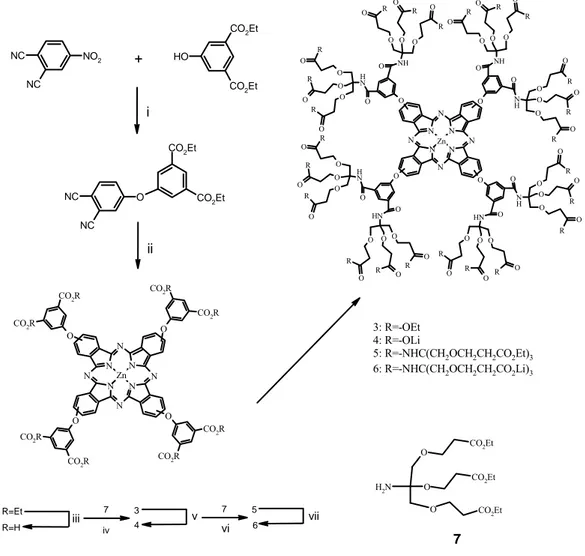
Burada (Şekil 1) dendrimerlerin (3,6) sentezi için başlangıç noktasında, esterden (1) oktakarboksilik asit içeren ftalosiyanin türevi (2) hazırlanmıştır. Ardından, asidin (2) THF'de 5oC'de, amin(7), disikloheksilkarbodimid (DCC) ve 1-hidroksibenzotriazol (HOBt) ile reaksiyonundan %75 verimle ilk jenerasyon (3) dendrimer ftalosiyanin hazırlanmıştır. Elde edilen bu ürün, gel permeation kromatografisiyle saflaştırılmıştır. 3 numaralı dendrimer ftalosiyaninin MeOH-H2O içinde LiOH ile hidrolizi 24 karboksilik
asit grubu içeren ilk jenerasyon dendrimer ftalosiyanini (4) vermektedir. Bu reaksiyonun tekrarı, ikinci jenerasyon dendrimer ftalosiyaninleri (5-6) vermektedir [24].
NO2 NC NC HO CO2Et CO2Et O NC NC CO2Et CO2Et N N N N N N N N O CO2R CO2R O CO2R CO2R O CO2R CO2R O CO2R CO2R N N N N N N N N R O O R O O N H O O R O R O O R O O N H O O R O O R O O R O O NH O O R O R O O R O O N H O O R O O R O O R O O N H O O R O R O O R O O N H O O R O O R O O R O O NH O O R O R O O R O O NH O O R O O O O O N H2 CO2Et CO2Et CO2Et + i ii Zn Zn 3: R=-OEt 4: R=-OLi 5: R=-NHC(CH2OCH2CH2CO2Et)3 6: R=-NHC(CH2OCH2CH2CO2Li)3 7 1 R=Et 2 R=H iii 7 iv 3 4 v 7 vi 5 6 vii
Şekil 1. Dendrimerler’in (3-6) sentezi. Maddeler ve koşullar: i) K2CO3, DMF,
oda sıcaklığı, 72%; ii) DBU, ZnCl2, n-pentanol, Reflaks, 24h, 42%; iii) NaOH, H2
O-THF, 48h, 96%; iv) DCC, HOBt, O-THF, 5oC, 72h, 75%; v) LiOH, MeOH-H2O, (1:1),
20oC, 48h, 96%; vi) DCC, HOBt, THF, 5oC, 72h, 70%; vii) LiOH, MeOH-H2O, 48h,
Elde edilen bu bileşiklerin yapıları, 1H, 13C-NMR, UV-VIS ve Kütle spektroskopileriyle aydınlatılmıştır [24].
Bir jenerasyonlu türler, sulu ortamda hidrofobik etki gösterirler. Jenerasyonun artmasıyla, dendrimerler’in koruyucu kalkan etkisinin ve moleküler kafesin büyüklüğünün artması nedeniyle, hidrofobik etki artmaktadır [2].
II-) a) Bu yöntemde ise, ilk önce dendron uçları sentezlenir,
b) Daha sonra bu dendronlar, ftalonitril veya izoindol bileşiklerinin uçlarına bağlanır. Ftalonitril veya izoindol gruplarının tetramerizasyonuyla dendritik ftalosiyaninler elde edilir. Yada hazırlanan dendron uçlarının metalli ftalosiyanin türlerinin aksiyel konumlarına koordine olmasıyla farklı türde dendritik ftalosiyaninler elde edilebilir.
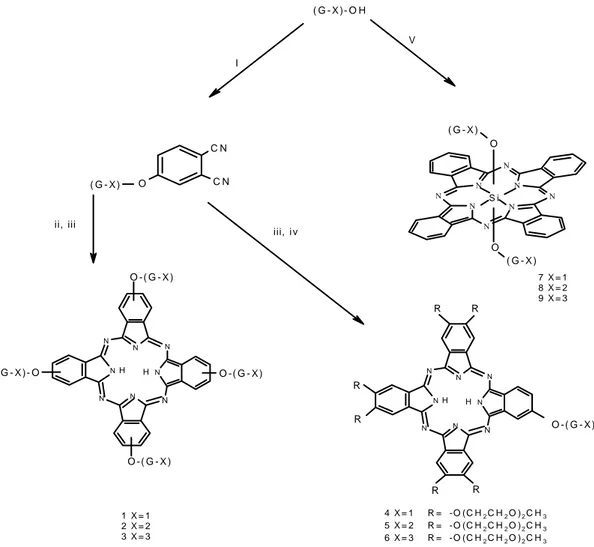
Bu yöntemle elde edilen farklı türdeki dendrimer ftalosiyaninler'in oluşum mekanizmaları Şekil 2'de gösterilmiştir [3, 4]. Dendritik ftalosiyanin oluşumunda başlangıç maddesi olarak, merkez noktasında benzilalkol gruplarını içeren birinci ([G-1]-OH), ikinci ([G-2]-OH) ve üçüncü ([G-3]-OH) jenerasyon dendronları hazırlanır [4, 25]. O O O O O O O O O O O O O O O O O O O O O O
Hazırlanan [G-X]-OH dendronları (X=jenerasyonu göstermek üzere) ve 4-nitroftalonitril arasındaki aromatik nükleofilik reaksiyonla, yüksek verimle hazırlanan dendron sübstitüentli ftalonitrilin siklotetramerizasyonuyla bir izomer karışımı olan (1-3) metalsiz ftalosiyanin merkezli dendrimerler elde edilir. Bu dendrimerler (1-(1-3), Et2O
ve heksan hariç, THF, toluen ve kloroform gibi aprotik çözgenlerin hepsinde çözünebilmektedir [3].
( G - X )- O H O C N C N ( G - X ) I V N N N N N N N N S i O O ( G - X ) ( G - X ) H H O - ( G - X ) N N N N N N N N R R R R R R N N N N N N NH H N ( G - X ) - O O - ( G - X ) O - ( G - X ) O - ( G - X ) ii, iii iii, i v 7 X = 1 8 X = 2 9 X = 3 1 X = 1 2 X = 2 3 X = 3 4 X = 1 R = -O (C H2C H2O )2C H3 5 X = 2 R = -O (C H2C H2O )2C H3 6 X = 3 R = -O (C H2C H2O )2C H3
Şekil 2. Maddeler ve koşullar: i) 4-nitroftalonitril, kuru K2CO3, DMF, 50oC; ii)
C5H11OLi, C5H11OH, 135oC; iii) asetik asit; iv) 4,5-di(1,4,7-trioksaoktil)ftalonitril,
C5H11OLi, C5H11OH, 135oC; v) dikloro(ftalosiyaninato)silikon, piridin, 80oC.
2 ve 3 türü dendritik ftalosiyaninlerin agregasyon eğilimi, dendritik uçların sterik hacmi çok daha büyük olmasına rağmen, çoğu sübstitüentli ftalosiyaninlerden (örneğin; tetra-tersiyerbütil Pc) daha güçlüdür.
Tetra-dendron sübstitüentli ftalosiyanin dendrimerleri, geniş bir sıcaklık aralığında sütunlar halinde bir mezofaz oluştururlar. Bu mezofaz özelliğine, dendritik uçların büyüklüğü önemli ölçüde etkilidir. Ancak, tek bir uç dendronun, ftalosiyanin halkasına sübstitüsyonu bu mezofaz oluşumunu önlemektedir. Bu nedenle, asimetrik ftalosiyanin dendimerleri (4-6) üzerinde çalışmalar yapılmıştır. Bu türler, uygun miktarda dendron sübstitüentli ftalonitril ve 4,5-bis(1,4,7-trioksooktil)ftalonitrilin fazlasıyla arasındaki karışık siklotetramerizasyon reaksyonuyla hazırlanmaktadır. Bu
ürün, kolon kromatografisi kullanılarak oluşabilecek diğer yan ürünlerinden izole edilebilir [3].
Bir başka dendritik yapıda Silikon(IV)Pc üzerine poly(arileter) uçlarının aksiyel konumda sübstitüye olduğu ftalosiyanin dendrimeridir. Bu bileşik, [G-X]-OH ve dikloro(ftalosiyaninato)silikon arasındaki reaksiyonla kolayca %10-40 verimle elde edilir (7-9). Bu ürün, THF, toluen ve kloroform gibi aprotik çözgenlerde çözünebilir. Bu bileşik üzerinde yapılan X-ışını analizi sonucunda; O-Si-O arasındaki bağ açısının 179° olduğu, ftalosiyanin çekirdeğinin düzlemsel yapıda bulunduğu ve silikon atomuna direkt bağlı benzil grubunun ftalosiyanin çekirdeğine 15.64°’lik bir açı oluşturduğu görülmüştür [23, 25].
Bir başka dendritik ftalosiyanin türüde, SiPc’lerin dendrimer iskeletinin bir parçası olarak kullanıldığı dendrimerlerdir. Burada ftalosiyanin birimleri merkezin etrafına yerleşmiştir. Bu bileşiği hazırlamak için ilk olarak, aksiyel konumda bir fenil grubu ve hidroksi grubu içeren SiPc hazırlanır. Daha sonra, monoalkillenmiş diftalosiyaninil syanülik bileşiği hazırlanır. En son, bu syanülik bileşiği bir katalizör varlığında benzen trikarboksilik asit ile reaksiyona sokulur [2].
Si O O N N N Si O O O O O O Si O O N N N Si Si O O N N N Si N N N N N N N N Si O O Si
Diğer taraftan CO2 sensör özelliği gösteren üç ftalosiyanin merkezi içeren
N N N N N N N N O H O H O H N H OH OH O H NH OH OH OH N H O O O S O H O H O H N H O H O H O H NH OH OH O H NH O O O S OH OH OH N H O H OH O H NH OH OH O H N H O O S O N N N N N N N N O H O H OH NH O H HO O H N H O H O H O H N H O O O S OH OH OH NH O H O H OH NH O H O H O H N H O O O S O H O H OH N H O H OH O H NH O H O H O H N H O O S O N N N N N N N N O H O H OH NH OH OH OH NH OH OH OH N H O O O S OH OH OH N H OH OH OH N H OH OH O H N H O O O S O H O H OH N H OH OH OH N H OH OH OH N H O O S O NH N H N H N N N M = 2H M = Zn M = Co M M M 1.4.Ftalosiyaninlerin Saflaştırılması
Sübstitüye olmayan ftalosiyaninler ve bunların metalli türevleri;
1-) Çözünürlükleri çok az olduğundan ve ~550˚C gibi yüksek bir sıcaklığa son derece dayanıklı olduklarından dolayı süblimasyon yöntemiyle,
2-) Güçlü asitlere karşı son derece dayanıklı olduklarından dolayı da der.H2SO4 içinde
çözme ve daha sonra soğuk su yada buzda çöktürme yapılarak kolayca saflaştırılmaktadır [1].
Sübstitüye ftalosiyaninlerde, sübstitüye gruplar arasındaki mümkün olabilecek dipol etkileşimler ve molekül ağırlığındaki artış nedeniyle saflaştırma için süblimasyon yöntemi pek uygulanmaz. Bu türler, çözeltide agregasyona güçlü bir eğilim gösterseler bile, su ve organik çözgenlerde daha fazla çözünürler. Böylece, sübstitüentlerin bağlanması sonucu artan çözünürlüklere bağlı olarak su veya organik çözgenlerdeki çözünürlük farkından saflaştırma yapılması mümkündür.
Sübstitüye ftalosiyaninlerin saflaştırılmasında kullanılan metodlar aşağıdaki gibi sıralanmıştır [1];
1-) Çözünürlüğü az olan ftalosiyaninleri çeşitli çözgenlerle yıkayarak çözünen safsızlıkları uzaklaştırmak,
2-) Çözünmeyen safsızlıkları uzaklaştırmak için, çözünen sübstitüye ftalosiyaninlerin ekstraksiyonu ve daha sonra çözücünün buharlaştırılması yada yeniden kristallendirme,
3-) Amino sübstitüye ftalosiyaninler için, der.HCl içinde çözme ve daha sonra sulu bazik ortamda çöktürme,
4-) Özellikle asimetrik ftalosiyaninlerin saflaştırılmasında, Alumina ve Silikajel gibi dolgu maddeleri üzerinde normal, flaş veya vakum yöntemleri kullanılarak kolon kromatografisi uygulamak,
5-) Gel permeation kromatografisi,
6-) der.H2SO4 içinde çözme ve daha sonra soğuk su yada buzda çöktürme,
7-) Süblimasyon metodları,
8-) İnce Tabaka Kromatografisi (TLC), yüksek performance sıvı kromatografisi (HPLC), işlemleri uygulanır.
Özellikle, tetra- ve okta-sübstitüye ftalosiyanin oluşumunda her zaman sübstitüye grupların birbirine göre simetrik konumlarda bağlanması beklenemez. Sonuçta, bir izomer karışımı olan sübstitüye ftalosiyaninler oluşur. Oluşan bu izomer karışımı, mevcut bulunan saflaştırma yöntemlerinden hiçbiriyle birbirinden ayrılamaz. Ürün, izomer karışımları şeklinde elde edilir.
9-) Dimer, trimer ve dendritik ftalosiyaninler, yukarıda açıklanan ftalosiyanin saflaştırma yöntemleri kullanılarak saflaştırılabilmektedir. Bu tekniklerden ürün saflaştırılması çoğunlukla kolon kromatografisi yöntemi ve farklı çözgenlerdeki
Ayrıca elde edilen dimer, trimer ve dendritik ftalosiyaninler de, herbir tepkime basamağının saflığı, Elementel analiz ve TLC yöntemleriyle kontrol edilebilmektedir.
1.5.Ftalosiyaninlerin Elektronik Spektrumları
Ftalosiyaninler de UV absorpsiyonunda π-π∗ ve yük transfer (CT) geçişleri olmak üzere iki geçiş vardır [1].
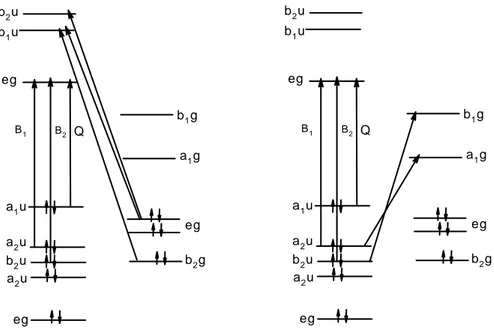
Ftalosiyaninler, Şekil 3’de de görüldüğü gibi UV bölgesinde yaklaşık 300-400 nm’de (B-bandı) ve görünür bölgede 600-700 nm’de (Q-bandı) olmak üzere tipik iki elektronik spektruma sahiptirler.
Ftalosiyaninler de, ~600-700 nm civarında ortaya çıkan Q-bandı; Pc-2 halkasının, en yüksek enerjili dolu molekül orbital’inden (HOMO) en düşük enerjili boş molekül orbitaline (LUMO) gerçekleşen π-π∗ geçişine aittir. Bütün ftalosiyaninler için deeper π-levels→LUMO geçişlerinden kaynaklanan B-bandları, 300-400 nm civarında UV bölgesinde gözlenir [15].
D2h simetrisine sahip metalsiz monomerik türler, 600-700 nm civarında iki
şiddetli absorpsiyon gösterirken, D4h simetrisine sahip metalli monomerik türler, bu
bölgede yalnızca tek bir band verirler [1].
Şekil 3. Ftalosiyaninler’in UV-VIS geçişleri
eg a2u b2u a2u a1u b1u b2u b2g eg a1g b1g eg Q B2 B1 eg a2u b2u a2u a1u b1u b2u b2g eg a1g b1g eg Q B2 B1
Yük transfer geçişleri, d0 ve d10 dizilimine sahip metalleri içeren ftalosiyanin türlerinde gözlenir. Yük transfer geçişleri, ftalosiyanin π-halka orbitalleri ve metal orbitalleri arasındaki ligandtan metale yük transfer geçişleri (LMCT) ve metalden liganda yük transfer geçişlerinden (MLCT) kaynaklanan uyarılmalarla olur. CT bandlarının yönleri ve enerjileri, metal merkezinin hem spinine hemde oksidasyon basamağına bağlıdır. Bu bandlar, 450 ve 600 nm arasında görünür bölgede gözlenebilir. Ayrıca, 700 ve 1500 nm arasında Q-bandının yanında da ortaya çıkabilir.
Ftalosiyaninlerin absopsiyon spektrumlarında; farklı çözgen türlerine, ftalosiyaninlerin içerdiği çeşitli metallere, metalli ftalosiyaninlerde aksiyel konumlara koordine olabilen çözgenlere, bağlı olarak spektrumlarda birtakım kaymalar meydana gelebilir [1].
1.6.Ftalosiyaninlerin Uygulama Alanları
Ftalosiyaninler, mürekkeplerde (özellikle tükenmez kalemlerde), plastik ve metal yüzeylerini renklendirmede, elbise ve kumaş türleri için boya maddeleri olarak kullanılan önemli endüstriyel maddelerdir [1, 27-29].
Çoğu tür ftalosiyanin boyaları, toksik özelliğe sahip değildir. Örneğin; CuPc türü, Almanya’da gıda boyası olarak kullanılmaktadır. Yine, bu türler Amerika’da kontak lenslerin boyanmasında da kullanılır. Aynı zamanda, yiyeceklerin paketlenmesi ve hazırlanmasında kullanılan, polimerik kaplama maddeleri için renklendirici olarak da kullanılabilirler [1, 27-29].
Ftalosiyaninlerin fotokopi makinalarında fotoiletken madde olarak kullanılmaları bu türler üzerindeki ilginin artmasına neden olmuştur.
Ftalosiyaninler üzerine çalışmaların devam etmesiyle çeşitli alanlarda gelişim ve ilerlemeler kaydedilmiştir.
Ftalosiyaninlerin yaygın olarak kullanım alanları [1, 27-29];
1-) CuPc, CoPc ve fotodinamik aktiviteye sahip ZnPc, gibi türler kimyasal sensörlerde duyarlı algılayıcı elementler olarak, MgPc ince filmleri yüksek duyarlıklı gaz
2-) Elektrokromik görüntüleme aygıtları olarak,
3-) Kanser tedavisi ve diğer tıbbi uygulamalar için fotodinamik maddeler (ışığa karşı duyarlı) olarak, aşağıda gösterilen ftalosiyanin türevleri kullanılmaktadır [30].
O N+ N N N N N N N N Zn Cl O N+ Cl N+ O Cl N+ O Cl O N+ CD3 N N N N N N N N Zn Cl O N+ CD3 Cl N+ CD3 O Cl N+ CD3 O Cl RLP068/Cl RLP068-D12/Cl
Tetrakatyonik Zn(II)Pc fotoduyarlı RLP068/Cl ve Dötörolu iç standart RLP068D12/Cl 4-) Optik bilgisayar okuma-yazma disklerin uygulamalarında,
5-) Sülfür atıklarının kontrolü için katalizör olarak, sülfür heterohalkalarının degradasyonu için kullanılan katı fotokatalizörler olarak silika üzerine destekli yada Y zeolit içine hapsedilmiş demir ftalosiyanin aşağıda gösterilmiştir [31].
N N N N N N N N Fe F eP c@ N a Y
6-) Fuel-cell (H2 ve O2 ile çalışan elektrik akımı veren cihaz) uygulamaları için
7-) Enerji üretimi için fotovoltaik hücre elementleri olarak, bu amaç için fotoelektrokimyasal özelliklere sahip Zn(II)Pc türleri kullanılmaktadır.
8-) Moleküler metallerde ve iletken polimerlerde,
9-) Sıvı kristalleri ve langmuir filmleri hazırlanmasında [32],
CH3 C H3 C H3 CH3 CH3 CH3 CH3 CH3 CH3 S O O NaO N N N N N N N N Zn
Özellikle, yukarıda gösterilen “Çinko tri(tersiyer-bütil)-4-sülfoftalosiyanin” Langmuir-Blodgett filmlerinde kullanılır.
10-) Yarı iletken malzemelerin hazırlanmasında, kullanılmaktadır.
Bu amaçlar için, yılda 500.000 tondan fazla monomerik ftalosiyaninler kullanılmaktadır.
Bu uygulamalarda ftalosiyaninlerin üstünlükleri ; -termal ve kimyasal kararlılıklarına, -yoğun renklerine,
-redoks özelliklerine,
-katalitik, elektronik ve optik özelliklerine, ve -toksik olmamalarına, bağlıdır.
Yine son yıllarda, ftalosiyanin kimyasının temel akademik araştırmalarının sayısı artmaktadır.
Bu çalışmalar;
-Yeni çözünebilir türlerin sentezi, -Asimetrik ftalosiyaninler,
-Polinükleer, köprülü, polimerik ve dendritik türlerin sentezi üzerine yeni yaklaşımların geliştirilmesi,
2.MATERYAL VE YÖNTEM
2.1.Kullanılan Cihazlar
1H-NMR spektrumları, Bruker 300 MHz ve Varian EM360 L 60 MHz
spektrometrelerinde oda sıcaklığında alındı. Kimyasal kaymalar ppm olarak verildi. Infrared spektrumları, ATl Unicam-Mattson 1000 spektrometresinde KBr pelet yapılarak 4000-400 cm-1 aralığında alındı. UV/VIS spektrumları, SHIMADZU UV/VIS spektrometresinde CHCl3
ve DMSO çözücüleri kullanılarak alındı.
2.2.Kimyasal Maddeler
4-(2-dimetilaminoetilsülfonil)ftalonitril, [12], Tetrakis(2-dimetilaminoetilsülfo nil)ftalosiyanin, [12], Tetrakis[(2-trimetilaminoetilsülfonil)ftalosiyanin]tetraiyodür, [12], bileşikleri ilgili literatürdeki yöntemlerle sentezlendi.
2.3.Bileşiklerin Sentezi
Tüm reaksiyonlar argon atmosferi altında yapıldı. Reaksiyonlar belirtilmedikçe, vidalı kapaklı, teflon musluklu, basınca dayanıklı şilenk kullanılarak gerçekleştirildi. Çözücüler moleküler elekle ve literatürdeki uygun yöntemle kurutulup oksijeni uzaklaştırıldıktan sonra kullanıldı.
2.4.Dendritik Metalsiz Ftalosiyanin Sentezi
4-(2-dimetilaminoetilsülfonil)ftalonitril Sentezi, 1, [12]
4-nitroftalonitrilin (12.0 g, 0.069 mol) susuz DMSO (100 cm3) içindeki çözeltisine 2-dimetilaminoetantiyol hidroklorür (10.8 g, 0.076 mol) eklendi. 10 dakika karıştırıldıktan sonra ortama susuz K2CO3 (14.3 g, 0.104 mol) 2 saat süresince azar azar ilave edilerek karıştırıldı.
Reaksiyon karışımı oda sıcaklığında 72 saat boyunca karıştırıldıktan sonra çözücüsü kuruluğa kadar vakum distilasyonuyla uzaklaştırıldı. Kalıntının üzerine H2O (150 cm3) ilave edildi ve
çözücü döner buharlaştırıcıda kuruluğa kadar uzaklaştırıldı. Kalıntı EtOH de (150 cm3) tekrar kristallendirilerek saf ürün elde edildi. Elde edilen kahverenkli ürün, CHCl3, Aseton, CH2Cl2,
THF, DMF ve DMSO da çözünüyor. Verim: 11.6 g (%72)
Karakterizasyon C12H13N3S (231,32 gmol-1) 1H-NMR: (60 MHz, CDCl 3, 25oC, δ ppm) δ 7.72-7.27 m (3H, Ar-H), 3.09 t (2H, S-CH2), 2.70 t (2H, C-CH2), 2.30 s (6H, N-CH3) Tetrakis(2-dimetilaminoetilsülfonil)ftalosiyanin Sentezi, 2, [12]
1’in (2.3 g, 0.01 mol) 2-(dimetilamino)etanol (6 cm3) içindeki çözeltisi 15 saat süresince argon gazı altında 140oC de ısıtıldı. Reaksiyon tamamlandıktan sonra çözücünün miktarı yaklaşık ¼ oranına kadar vakumda uzaklaştırıldı. Koyu yeşil karışımın üzerine 3 cm3 EtOH eklendi. Bu çözelti aseton (100 cm3) üzerine karıştırılarak damla damla ilave edildi. Oluşan yağımsı katının çözücüsü dekante edilerek uzaklaştırıldı. Kalıntıya tekrar aseton (30 cm3) eklendi ve 15 dakika karıştırıldı, oluşan katı süzüldü, eterle yıkandı ve vakumda kurutuldu. Elde edilen koyu yeşil renkli ürün, CHCl3, THF, DMF ve DMSO da çözünüyor.
Verim: 1.02 g (%44) Karakterizasyon C48H54N12S4 (927,32 gmol-1) 1H-NMR: (300.13 MHz, CDCl 3, 25oC, δ ppm) δ 7.71-6.65 m (12H, Ar-H), 3.14 s (8H, S-CH2), 2.75 s (8H, C-CH2), 2.33 s (24H, N-CH3), -6.3 br s (2H, -NH) IR: (KBr pelet, ν cm-1)
UV-VIS: (CHCl3, λMax / nm)
714.0, 680.0, 651.5, 416.0, 343.5, 301.5
Tetrakis[(2-trimetilaminoetilsülfonil)ftalosiyanin]tetraiyodür Sentezi, 3,[12]
2 (950 mg, 0.6 mmol), mutlak EtOH de (4 cm3) çözüldü ve MeI (582 mg, 0.4 mmol, 0.26 cm3) eklendi. Reaksiyon karışımı argon atmosferinde 4 saat 90oC de ısıtıldı. Reaksiyon tamamlandıktan sonra reaksiyon oda sıcaklığına soğutuldu ve yeşil renkli katı süzüldü, EtOH ve Et2O ile yıkanıp vakumda kurutuldu. Ürün, H2O ve DMSO da çözünüyor. Verim: 1.35 g
(%88)
Karakterizasyon
C52H66N12S4I4 (1495,08 gmol-1)
IR: (KBr pelet, ν cm-1)
3276 m (NH), 3004-2958 m (Alifatik–CH), 1606 m (Aromatik-C=C), 750 s (sübstitüye benzen)
UV-VIS: (DMSO, λMax / nm)
711.5, 685.0, 624.5, 349.5, 297.5
Trietil metantrikarboksilat ile birinci jenerasyon dendritik ftalosiyanin hazırlanması, 4,
Mutlak EtOH (15 cm3) içinde Na metali (0.80 g) ile trietil metantrikarboksilatın (1.50 cm3) reaksiyonu ile trietil metantrikarboksilatın sodyum tuzu hazırlandı. Hazırlanan tuz çözeltisine 3 (1.30 g, 0.870 mmol) eklendi ve çözeltiden sürekli olarak argon gazı geçirilerek 90 dakika reflaks yapıldı. Reaksiyon süresince trimetilamin çıkışı gözlendi. Reaksiyon karışımı oda sıcaklığına soğutuldu ve ortama %40'lık NaOH çözeltisi (6 cm3) eklendi. Baz eklenir eklenmez trimetilamin çıkışında artış gözlendi. Koyu yeşil çözelti 10 dakika oda
(10 cm3) ilave edildi ve 150 dakika tekrar reflaks yapıldı. Reaksiyon tamamlandıktan sonra ortamdaki EtOH vakumda uzaklaştırıldı ve oluşan süspansiyona H2O (10 cm3) ilave edildi.
Bu karışım eterle ekstrakte edildikten sonra ürünün tamamen çöktürülebilmesi için ortam der.HCl ile asitlendirildi. Oluşan yeşil katı süzüldü, H2O (3x25 cm3), aseton ve Et2O ile
yıkandı. Vakumda kurutuldu. Ürün, CHCl3 da az, DMF ve DMSO da kolayca çözünüyor.
Verim: 0.510 g (%35) Karakterizasyon C80H90N8S4O24 (1675,92 gmol-1) 1H-NMR: (300.13 MHz, DMSO-d 6, 25oC, δ ppm) δ 7.90-6.80 m (12H, Ar-H), 3.34 br s (8H, S-CH2, 24H, O-CH2), 2.37 br s (8H, C-CH2, 36H, O-CH2CH3) IR: (KBr pelet, ν cm-1)
3289 m (NH), 2921-2851 w (Alifatik–CH), 1753 w (ester C=O), 1588 m (Aromatik-C=C), 748 s (sübstitüye benzen)
UV-VIS: (CHCl3, λMax / nm)
711.5, 678.0, 647.5, 418.0, 340.5, 300.5
Tris ile ikinci jenerasyon dendritik ftalosiyanin hazırlanması, 5,
DMSO (3 cm3) de 4 (470 mg, 0.280 mmol), Tris (tris(hidroksimetil)-aminometan) (480 mg, 3.9 mmol) ve K2CO3 (1.60 g, 0.011 mol) karışımı 24 saat 100oC de ısıtıldı.
Reaksiyon tamamlandıktan sonra çözücü (DMSO) vakum distilasyonuyla uzaklaştırıldı. Yağımsı kalıntı Et2O ile yıkandı ve kurutuldu. Oluşan katı su (3x5 cm3) ile yıkandı (suda çok
az çözünüyor). Ardından sırasıyla aseton, etanol ve Et2O ile yıkandı ve vakumda kurutuldu.
Elde edilen yeşil renkli ürün, CHCl3 da az, DMF ve DMSO da kolayca çözünüyor. Verim:
C104H150N20S4O48 (2576,73 gmol-1)
1H-NMR: (300.13 MHz, DMSO-d
6, 25oC, δ ppm)
δ 9.3 br s (12H, OHCH2C-NH), 8.03-7.09 m (12H, Ar-H), 3.26 br s (108H, OH, 8H, S-CH2,
72H, OH-CH2), 2.36 br s (8H, C-CH2)
IR: (KBr pelet, ν cm-1)
3428 br (OH), 3291 m (NH), 2928-2964 w (Alifatik–CH), 1759 w (ester C=O), 1627 m (Aromatik-C=C), 744 s (sübstitüye benzen)
UV-VIS: (CHCl3, λMax / nm)
711.5, 678.0, 648.5, 418.5, 341.0, 300.5
Hekzil ile üçüncü jenerasyon dendritik ftalosiyanin hazırlanması, 6,
DMF de (2 cm3) 5 (300 mg, 0.12 mmol), C6H13Br (780 mg, 4.7 mmol, 0.66 cm3) ve
K2CO3 (810 mg, 5.8 mmol) karışımı 24 saat süresince 100°C de ısıtıldı. Reaksiyon
tamamlandıktan sonra ortamdaki DMF vakum distilasyonuyla uzaklaştırıldı. Elde edilen yağımsı kalıntı CHCl3 da çözüldü ve oluşan koyu yeşil karışım süzüldü. CHCl3 çözeltisi 1-2
cm3 kalıncaya kadar vakumda deriştirildi. Üzerine Et2O ilave edildi ve oluşan yağımsı
kalıntının çözücüsü dekante edilerek uzaklaştırıldı. Kalıntı Et2O ile yıkandı ve vakumda
kurutuldu.Viskoz yağımsı koyu yeşil ürün CHCl3 da çözünüyor.
Verim: 0.180 g (%28) Karakterizasyon C320H582N20S4O48 (5606,57 gmol-1) 1H-NMR: (300.13 MHz, CDCl 3, 25oC, δ ppm)
δ 8.75 br s (12H, OHCH2C-NH), 7.84-6.76 m (12H, Ar-H), 3.26 (8H, S-CH2),2.97 s (72H,
CH2O-CH2),1.49 s (8H, C-CH2), 1.18 (288H, OCH2(CH2)4), 0.81 (108H, (CH2)4CH3), -9.6 br s(2H, Ar-NH)
IR: (KBr pelet, ν cm-1)
3287 m (NH), 2951-2851 s (Alifatik–CH), 1756w (ester C=O), 1605 m (Aromatik-C=C), 744 s (sübstitüye benzen)
UV-VIS: (CHCl3, λMax / nm)
711.5, 678.0, 649.0, 418.0, 341.5, 300.0
2.5.Metalli Ftalosiyanin Sentezi
İzoindol Sentezi, 7,
MeOH (70 cm3) içerisine Na metali (0.7 g) ilave edilerek sodyum metoksit hazırlandı. Ardından ortama 1 (10.0 g, 0.043 mol) ilave edilerek oda sıcaklığında 2 saat süresince çözeltiden NH3 gazı geçirildi. Çözeltinin rengi kahverengiden koyu kırmızıya dönüştü.
Kırmızı çözeltiden sürekli NH3(g) geçirilerek 34 saat süresince reflaks yapıldı. Reflaks işlemi
sırasında çözeltinin rengi koyu kırmızıdan yeşile döndü. Reaksiyon tamamlandıktan sonra ortamdaki MeOH döner buharlaştırıcıda kuruluğa kadar çekildi. Kalıntı asetonda (50 cm3) çözüldü ve oluşan süspansiyon süzüldü. Katı tekrar asetonla yıkandı ve süzüntüler birleştirildi. Çözeltinin hacmi 10 cm3 e deriştirildi ve Et2O ile (25 cm3) çöktürüldü. Oluşan
katı süzüldü, Et2O ile yıkandı ve vakumda kurutuldu. Elde edilen sarı renkli ürün, H2O, THF,
CHCl3, DMF ve DMSO da çözünüyor.
Verim: 4.30 g (%40)
Karakterizasyon
C12H16N4S (248,36 gmol-1)
δ 7.76-6.99 m (3H, Ar-H), 3.04 s (2H, S-CH2), 2.56 s (2H, C-CH2), 2.09 s (6H, N-CH3), 3.04
s (3H, -NH)
IR: (KBr pelet, ν cm-1)
3262-3142 (NH), 2966-2776 br (Alifatik C-H), 1637 (Aromatik-C=C), 872 s (sübstitüye benzen)
Lutesyum(III)ftalosiyanin Sentezi, 8,
7 (800 mg, 3.2 mmol) ve Lu(OAc)3.nH2O (280 mg, 0.81 mmol) karışımı amil alkol (2
cm3) içerisinde 6 saat süresince 150oC de ısıtıldı. Reaksiyon sonunda çözücü vakumda 1-2 cm3 kalıncaya kadar uzaklaştırıldı. Koyu yeşil kalıntı CHCl3 (15 cm3) da çözüldü ve süzüldü.
Süzüntünün çözücüsü tekrar kuruluğa kadar uzaklaştırıldı ve yağımsı katı asetonda (75 cm3) çözüldü. Oluşan süspansiyon süzüldü ve katı süzüntüsü renksiz olana kadar asetonla yıkandı. Sonra Et2O ile yıkanarak vakumda kurutuldu. Elde edilen yeşil renkli ürün CHCl3 de çok az,
DMSO da kolayca çözünüyor. Verim: 0.230 g (%23) Karakterizasyon C50H55N12S4O2Lu (1159,32 gmol-1) 1H-NMR: (300.13 MHz, DMSO-d 6, 25oC, δ ppm) δ 7.96-6.77 m (12H, Ar-H), 3.38 s (8H, S-CH2, 6H, OOCCH3), 2.44 s (8H, C-CH2), 2.04 s (24H, N-CH3) IR: (KBr pelet, ν cm-1)
2939-2775 m (Alifatik–CH), 1754 (Asetat-C=O), 1665 m (Aromatik-C=C), 752 s (sübstitüye benzen)
UV-VIS: (CHCl3, λMax / nm)
Evropiyum(III)ftalosiyanin Sentezi, 9,
7 (750 mg, 3.02 mmol) ve Eu(OAc)3.nH2O (248 mg, 0.75 mmol) kullanılarak bileşik 8
deki yöntemle sentezlendi. Verim: 200 mg (%22)
Karakterizasyon C50H55N12S4O2Eu (1136,30 gmol-1) 1H-NMR: (300.13 MHz, DMSO-d 6, 25oC, δ ppm) δ 8.02-6.97 m (12H, Ar-H), 3.40 br.s (8H, S-CH2, 6H, COOCH3), 2.58 s (8H, C-CH2), 2.02 s (24H, N-CH3) IR: (KBr pelet, ν cm-1)
2930-2769 m (Alifatik C-H), 1724 m (Asetat-C=O), 1601 m (Aromatik-C=C), 748 s (sübstitüye benzen)
UV-VIS: (DMSO, λMax / nm)
685.5, 354.5, 277.0
2.6.Dendritik Sandviç Ftalosiyanin Sentezi
LuPcPc’ Sentezi, 10, a)LuPc(OAc) ile
6 nın (40 mg, 0.0071 mmol) kuru amil alkol içerisindeki çözeltisine Li metali (1.5.10-4 mg, 2.2.10-5 mmol) eklendi. Bu karışım 3 saat reflaks yapıldı. Reaksiyon karışımı oda sıcaklığına soğutulduktan sonra 8 (8.7 mg, 7.1.10-3 mmol) eklendi ve kapaklı şlenkte 15 saat 150oC de ısıtıldı. Reaksiyon tamamlandıktan sonra amil alkol vakumda kuruluğa kadar çekildi. Kalıntı aseton ve Et2O ile yıkandı ve vakumda kurutuldu.
(6704,83 gmol-1)
Ürün karakterize edilemedi.
b) Lu(OAc)3.nH2O ile
i) Li2Pc Sentezi
Argon gazı altında 2 nin (100 mg, 0.1 mmol) THF (5.0 cm3) içerisindeki çözeltisine LDA (21.4 mg, 0.2 mmol, 0.1 cm3) eklendi. Bu karışım 3 saat reflaks yapıldı. Reaksiyon tamamlandıktan sonra karışım oda sıcaklığına soğutuldu. Ortamdaki THF vakumda uzaklaştırıldı. Kalıntı kuru Et2O ile (2x5 cm3) yıkandı ve vakumda kurutuldu. Verim: 100 mg,
(%99)
Karakterizasyon
C48H52N12S4Li2 (939.15 gmol-1)
IR: (KBr pelet, ν cm-1)
2959-2824 m (Alifatik–CH), 1603 s (Aromatik-C=C), 756 s (sübstitüye benzen)
ii) LuPcPc’ Sentezi, 10,
Argon gazı altında Li2Pc (8.4 mg, 0.009 mmol), 6 (50 mg, 0.009 mmol) ve
Lu(OAc)3.nH2O (3.2 mg, 0.009 mmol) karışımının 1-oktanol (5 cm3) içerisindeki çözeltisine
24 saat reflaks yapıldı. Reaksiyon tamamlandıktan sonra 1-oktanol vakum distilasyonuyla uzaklaştırıldı. Yağımsı kalıntı, Et2O/n-hekzan ile çöktürüldü, süzüldü ve vakumda kurutuldu.
Ardından ürün CHCl3 da çözüldü ve süzüldü. CHCl3 fazının çözücüsü vakumda uzaklaştırıldı.
Yağımsı kalıntı Et2O ile yıkandı ve vakumda kurutuldu. Verim: 20 mg,(%34)
Karakterizasyon C368H632N32S8O48Lu
1H-NMR: (300.13 MHz, CDCl
3, 25oC, δ ppm)
δ 8.08-7.21 m (24H, Ar-H), 2.50 br s (16H, S-CH2,72H, CH2O-CH2), 1.50-0.59 m (16H, C-CH2, 484H, CH2O-CH2, OCH2-(CH2)4CH3)
IR: (KBr pelet, ν cm-1)
2293-2775 m (Alifatik–CH), 1638 m (Aromatik-C=C), 752 s (sübstitüye benzen)
UV-VIS: (CHCl3, λMax / nm)
685.5, 633.2, 492.5, 355.7, 329.5, 295.5
EuPcPc’ Sentezi, 11,
Li2Pc (8.4 mg, 0.009 mmol), 6 (50 mg, 0.009 mmol) ve Eu(OAc)3.nH2O (2.9 mg,
0.009 mmol) kullanılarak bileşik 10 daki yöntemle sentezlendi. Verim: 20 mg (%35) Karakterizasyon C368H632N32S8O48Eu (6681.82 gmol-1) 1H-NMR: (300.13 MHz, CDCl 3, 25oC, δ ppm) δ 8.13-7.22 m (24H, Ar-H), 3.56 br s (16H, S-CH2, O-CH2), 2.6-0.43 m (16H, C-CH2, 484H, CH2O-CH2, OCH2-(CH2)4CH3) IR: (KBr pelet, ν cm-1)
2919-2847 m (Alifatik C-H), 1630 m (Aromatik-C=C), 750 s (sübstitüye benzen)
UV-VIS: (DMSO, λMax / nm)
3.SONUÇ VE TARTIŞMA
3.1.Dendritik Metalsiz Ftalosiyaninlerin Sentezi
İlgili literatüre göre, 4-(2-dimetilaminoetilsülfonil)ftalonitril, 1, argon atmosferi altında 4-nitroftalonitrilin 2-dimetilaminoetantiyol hidroklorür ile K2CO3 varlığında DMSO
içinde etkileştirilmesi sonucu elde edildi [12].
N(Me)2 S NC NC NO2 NC NC HS N(Me)2HCl + + K2CO3 RT DMSO 1
Çizelge 1 de görüldüğü gibi bu bileşiğin oda sıcaklığında CDCl3 da alınan 1H-NMR
spektrumunda, 7.72-7.27 ppm de Ar-H, 3.09 ppm de S-CH2, 2.70 ppm de C-CH2 ve 2.30 ppm
de N-CH3 pikleri gözlenmiştir. Bu değerler ilgili literatür değerleri ile aynıdır [12].
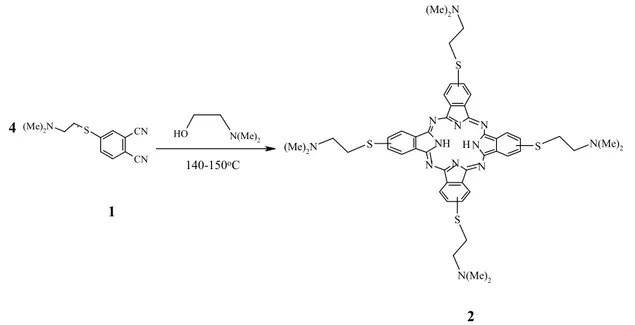
Tetrakis(2-dimetilaminoetilsülfonil)ftalosiyanin, 2, argon atmosferi altında 4-(2-dimetilaminoetilsülfonil)ftalonitrilin, 1, 2-(dimetilamino)etanol de sikliktetramerizasyon reaksiyonu sonucu %45 verimle elde edildi. Koyu yeşil renkli ürün literatürdeki gibi asetonla yıkanarak saflaştırıldı [12]. N N N N N N NH HN S N(Me)2 S (Me)2N S N(Me)2 S (Me)2N (Me)2N S CN CN N(Me)2 O H 4 2 1 140-150oC
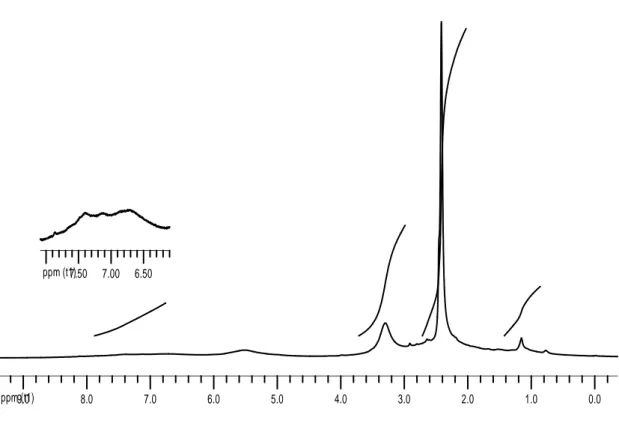
2 bileşiğinin oda sıcaklığında CDCl3 de ölçülen 1H-NMR spektrumunda (Şekil 4),
7.71-6.65 ppm de geniş bir multiplet Aromatik protonlar, 3.14 ppm de S-CH2, 2.75 ppm de
C-CH2, 2.33 ppm de N-CH3, -6.3 ppm de ftalosiyanin halkasının merkezindeki N-H pikleri
gözlendi (Çizelge 1). Literatürde de belirtildiği gibi aromatik halka proton pikleri oldukça yayvan çıkmaktadır [12].
ppm (t1)9.0 8.0 7.0 6.0 5.0 4.0 3.0 2.0 1.0 0.0
Şekil 4. 2 bileşiğinin 1H-NMR spektrumu (CDCl3)
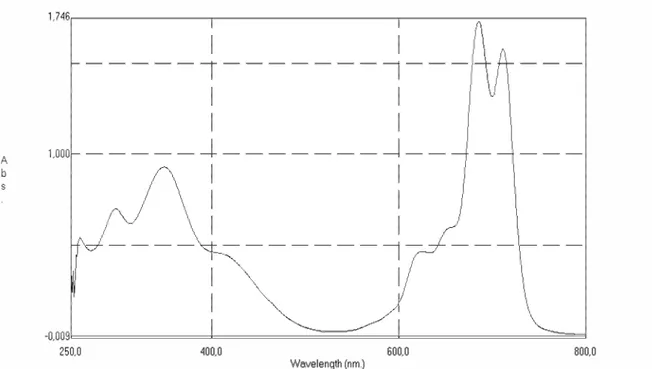
2 bileşiğinin CHCl3 de ölçülen UV spektrumunda (Şekil 5), 714-680 nm de Q-bandı,
343.5 nm de ise B-bandına ait maksimumlar gözlenmektedir. Metalsiz ftalosiyaninler Q-bandı literatürde tanımlandığı gibi de ikiye bölünmüştür [12].
2 bileşiğinin IR spektrumunda (Şekil 6), 3281 cm-1 de NH, 2933-2764 cm-1 de alkil pikleri gözlenmiştir. Tüm spektroskopik sonuçlar ilgili literatür değerleri ile örtüşmektedir (Çizelge 1, 2, 3) [12].
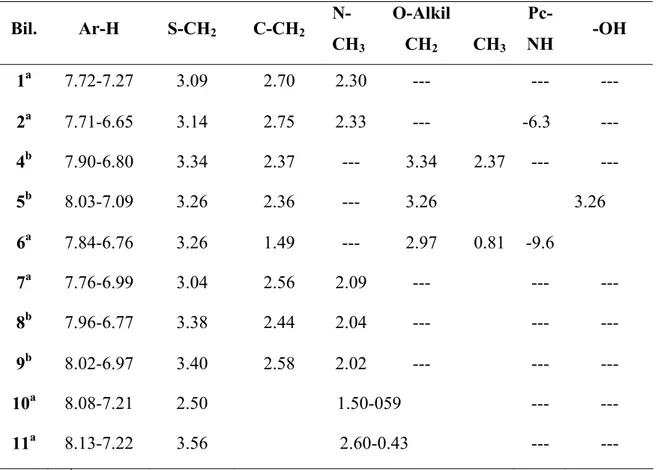
Çizelge 1. Bileşiklerin 1H-NMR spektrum sonuçları, (δ ppm) Bil. Ar-H S-CH2 C-CH2 N-CH3 O-Alkil CH2 CH3 Pc-NH -OH 1a 7.72-7.27 3.09 2.70 2.30 --- --- --- 2a 7.71-6.65 3.14 2.75 2.33 --- -6.3 --- 4b 7.90-6.80 3.34 2.37 --- 3.34 2.37 --- --- 5b 8.03-7.09 3.26 2.36 --- 3.26 3.26 6a 7.84-6.76 3.26 1.49 --- 2.97 0.81 -9.6 7a 7.76-6.99 3.04 2.56 2.09 --- --- --- 8b 7.96-6.77 3.38 2.44 2.04 --- --- --- 9b 8.02-6.97 3.40 2.58 2.02 --- --- --- 10a 8.08-7.21 2.50 1.50-059 --- --- 11a 8.13-7.22 3.56 2.60-0.43 --- --- aCDCl 3, bDMSO-d6
Çizelge 2. Bileşiklerin elektronik spektrum sonuçları Bileşik λnm 2a 714.0, 680.0, 651.5, 416.0,343.5, 301.5 3b 711.5, 685.0, 624.5, 349.5, 297.5 4a 711.5, 678.0, 647.5, 418.0, 340.5, 300.5 5a 711.5, 678.0, 648.5, 418.5, 341.0, 300.5 6a 711.5, 678.0, 649.0, 418.0, 341.5, 300.0 8a 695.5, 629.5, 357.0, 286.0 9b 685.5, 354.5, 277.0 10a 685.5, 633.1, 492.5, 355.7, 329.5, 295.5 11b 681.5, 619.0, 490.0, 362.0, 291.0, 262.0, 253.0 aCHCl 3, bDMSO 500 1000 1500 2000 2500 3000 3500 4000 35 40 45 50 55 Wavenumbers % T r a n s m i t t a n c e
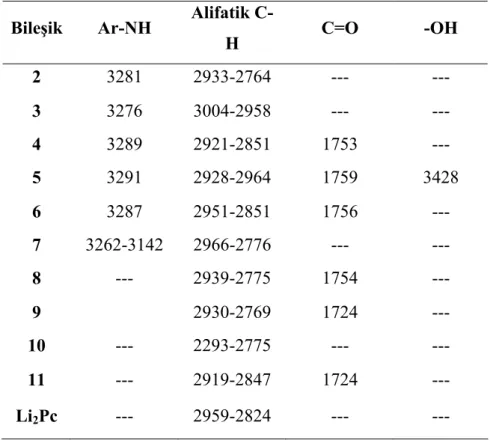
Çizelge 3. Bileşiklerin karakteristik IR sonuçları (ν cm-1, KBr pelet)
Bileşik Ar-NH Alifatik
C-H C=O -OH 2 3281 2933-2764 --- --- 3 3276 3004-2958 --- --- 4 3289 2921-2851 1753 --- 5 3291 2928-2964 1759 3428 6 3287 2951-2851 1756 --- 7 3262-3142 2966-2776 --- --- 8 --- 2939-2775 1754 --- 9 2930-2769 1724 --- 10 --- 2293-2775 --- --- 11 --- 2919-2847 1724 --- Li2Pc --- 2959-2824 --- ---
2 bileşiğinin argon atmosferi altında MeI ile etkileştirilmesi sonucu kuartenize tetrakis[(2-trimetilaminoetilsülfonil)ftalosiyanin]tetraiyodür, 3, elde edildi [12].
N N N N N N NH HN S N(Me)3I S I(Me)3N S N(Me)3I S I(Me)3N + 4 MeI EtOH 3 2 80-90oC
3 bileşiğinin 1H-NMR, UV-VIS ve IR spektrumlarında gözlenen değerler 2 bileşiğinin ve ilgili literatürdeki değerler ile aynıdır (Çizelge 1, 2, 3) [12].
Şekil 7. 3 bileşiğinin UV-VIS spektrumu
Mutlak EtOH de sodyum metali ile trietil metantrikarboksilatın etkileşmesi sonucu hazırlanan sodyum trietil metantrikarboksilat tuzunun kuartenize ftalosiyanin 3 ile
etkileştirilmesi sonucu birinci jenerasyon dendritik ftalosiyanin hazırlandı. Oluşan ürün sırasıyla H2O, aseton ve Et2O ile yıkandı. Koyu yeşil renkli 4 bileşiği CHCl3 de çok az, DMF
N N N N N N NH HN O O O S O O O CH3 CH3 CH3 O O O S O O O CH3 CH3 C H3 O O O S O O O C H3 C H3 C H3 O O O S O O O C H3 H3C CH3 + 4 Na + 8 CH(CO2C2H5)3 4 3 1. EtOH 2.%40 NaOH + Su Reflaks
4 ün DMSO-d6 da ölçülen 1H-NMR spektrumunda (Şekil 8), 7.90-6.80 ppm de çok
yayvan olarak aromatik protonlar, 3.34 ppm de S-CH2, ester grubunun O-CH2, 2.37ppm de
C-CH2, OCH2CH3 protonları geniş singlet olarak gözlenmektedir. 4 bileşiğinin ftalosiyanin merkezindeki NH protonları gözlenmemiştir. Bunun nedeni DMSO-d6 ile NH protonları
arasındaki etkileşim sonucu, muhtemelen NH proton pikleri alifatik proton pikleri ile çakışmaktadır [26, 33].
ppm (t1)9.0 8.0 7.0 6.0 5.0 4.0 3.0 2.0 1.0 0.0 ppm (t1)7.50 7.00 6.50
Şekil 8. 4 bileşiğinin 1H-NMR spektrumu (DMSO-d6)
Birinci jenerasyon dendritik ftalosiyanin 4’ün CHCl3 de ölçülen elektronik
spektrumunda (Şekil 9), ftalosiyaninler için karakteristik olan 711.5 ve 678.0 nm de Q ve 340.5 nm de B-bandları gözlenmiştir. Q-bandı metalsiz ftalosiyaninlerin D2h simetrisinden
dolayı ikiye bölünmektedir.
4 bileşiğinin IR spektrumunda (Şekil 10), 3289cm-1 de NH titreşim bandı, 2921-2851 cm-1 de alifatik C-H bandı, 1753 cm-1 de trietil metantrikarboksilat grubundaki C=O bandı, 1588 cm-1 de Aromatik-C=C bandı pikleri gözlenmiştir. 4 bileşiğinin 1H-NMR, UV-VIS, IR spektrumları (Çizelge 1, 2, 3), birbirlerini desteklemekte ve 4 bileşiğinin yapısını
doğrulamaktadır. Ayrıca karakterizasyon verileri ilgili literatürdeki sonuçlarla uyumludur [26, 33].
Şekil 9. 4 bileşiğinin UV-VIS spektrumu (CHCl3) 500 1000 1500 2000 2500 3000 3500 4000 40 60 80 100 Wavenumbers % T r a n s m i t t a n c e
DMSO içinde 4 bileşiğinin K2CO3 varlığında tris(hidroksimetil)aminometan (tris) ile
90oC de reaksiyonuyla ikinci jenerasyon dendritik ftalosiyanin, 5, elde edildi. Reaksiyon karışımının çözücüsü uzaklaştırıldıktan sonra kalıntı sırayla H2O, aseton, CHCl3 ve Et2O ile
yıkanarak saflaştırıldı. Koyu yeşil ürün suda çok az, CHCl3 de az, DMF ve DMSO da ise
kolayca çözünmektedir. N H2 OH OH OH N H OH OH OH O N H OHOH OH O N H OH OH OH O S N H O H O H O H O N H O H O H O H O N H O H O H O H O S NH O H O H OH O NH OH OH O H O NH OH OH OH O S NH OH OH OH O N H O H HO OH O NH O H HO OH O S N N N N N N NH HN + 40 K2CO3 14 DMSO 80oC 4 + 5
5 bileşiğinin DMSO-d6 da ölçülen 1H-NMR spektrumunda (Şekil 11), 8.03-7.09 ppm
de aromatik protonlar, 3.26 ppm de S-CH2, O-CH2, CH2-OH, 2.36.ppm de C-CH2 pikleri
ppm (t1)9.0 8.0 7.0 6.0 5.0 4.0 3.0 2.0 1.0 0.0 ppm (t1)8.00 7.50 7.00 6.50
Şekil 11. 5 bileşiğinin 1H-NMR spektrumu (DMSO-d6)
İkinci jenerasyon dendritik ftalosiyanin 5’in CHCl3 da ölçülen elektronik
spektrumunda (Şekil 12), 4 bileşiğinin spektrumunda olduğu gibi 711.5 ve 678.0 nm de Q-bandı, 341.0 nm de B-bandı görülmektedir. Çözücü polaritesine oldukça bağımlı olan Q-bandı DMSO içinde etkin agregasyon yapmaktadır (Şekil 13).
Şekil 13. 5 bileşiğinin UV-VIS spektrumu (DMSO)
5 bileşiğinin IR spektrumunda (Şekil 14), 4 bileşiğinin IR spektrumundan farklı olarak 3428cm-1 de OH titreşim bandı gözlenmiştir.
500 1000 1500 2000 2500 3000 3500 4000 40 50 60 70 80 90 100 Wavenumbers % T r a n s m i t t a n c e
Üçüncü jenerasyon dendritik ftalosiyanin, 6, K2CO3 varlığında hekzil bromür ile 5 in
DMF içinde 100oC de reaksiyonu sonucu elde edildi. Reaksiyon karışımının çözücüsü vakumda uzaklaştırıldıktan sonra kalıntı, CHCl3 de çözülerek süzüldü ve inorganik türler
uzaklaştırıldı. CHCl3 fazı deriştirildikten sonra kalıntı Et2O ile çöktürüldü. Yağımsı kalıntı
Et2O ile yıkanarak saflaştırıldı. Elde edilen koyu yeşil, viskoz, yağımsı ürün CHCl3 da
kolayca çözünmekte, Et2O de çok az çözünmektedir.
N N N N N N NH HN O CH3 O CH3 O CH3 O O N H O CH3 NH O C H3 O O N H O S C H3 O C H3 C H3 O CH3 O C H3 O C H3 O C H3 O O NH O C H3 NH O CH3 O O NH O S CH3 O CH3 CH3 O C H3 O CH3 O CH3 O CH3 O O NH O CH3 N H O CH3 O O N H O S CH3 O CH3 CH3 O CH3 O C H3 O C H3 O C H3 O O N H O C H3 N H O C H3 O O NHO S C H3 O C H3 C H3 O C H3 + 40 C6H13Br + 50 K2CO3 DMF 100 oC 5 6
6 bileşiğinin CDCl3 de ölçülen 1H-NMR spektrumunda (Şekil 15), 7.84-6.76 ppm de
aromatik, 3,26 ppm de S-CH2, 2.97 ppm de O-CH2, 1.49 ppm de C-CH2 1.18 ppm de heksil
CH2, 0.81 ppm de heksil CH3 pikleri gözlendi. Ftalosiyanin molekülündeki NH pikleri -9.6
ppm de gözlenirken, -OH grubundaki -NH pikleri 8.75 ppm de geniş singlet olarak gözlenmiştir. Her iki NH pikide D2O ile yer değişimi sonucu yok olmaktadır (Şekil 16). 6
bileşiğinin DMSO-d6 da alınan 1H-NMR spektrumu, 4 ve 5 bileşiklerinde olduğu gibi NH
pikleri gözlenememiş ve aromatik pikler daha da genişlemiş, alifatik pikler ise çözücü ve su pikleri ile çakışmaktadır (Şekil 17).
ppm (t1) 10.0 5.0 0.0 -5.0 -10.0
ppm (t1)-6.0 -7.0 -8.0 -9.0-10.0-11.0 ppm (t1)9.008.508.007.507.00
Şekil 15. 6 bileşiğinin 1H-NMR spektrumu (CDCl3)
6 bileşiğinin CHCl3 de alınan elektronik spektrumunda, 4 ve 5 (Şekil 18),
ppm (t1)10.0 5.0 0.0 -5.0 -10.0 ppm (t1)-7.0 -8.0 -9.0 -10.0 ppm (t1)9.509.008.508.007.507.00
Şekil 16. 6 bileşiğinin D2O yerdeğiştirme 1H-NMR spektrumu (CDCl3)
ppm (t1) 10.0 5.0 0.0 -5.0 -10.0
ppm (t1)-7.0 -8.0 -9.0 -10.0 ppm (t1)8.50 8.00 7.50 7.00 6.50
Şekil 18. 6 bileşiğinin UV-VIS spektrumu (CHCl3)
Üçüncü jenerasyon dendritik ftalosiyanin 6 nın IR spektrumunda (Şekil 19), 4 den farklı olarak 2951 ve 2851 cm-1de alifatik-CH titreşim bandı gözlenmiştir.
3.2.Metalli Ftalosiyanin Sentezi
7 bileşiği, MeOH de 4-(2-dimetilaminoetilsülfonil)ftalonitril, 1, ve sodyum metoksit karışımından susuz amonyak geçirilerek reflaks yapılmasıyla hazırlandı. Reaksiyon sonucu çözücü kuruluğa kadar uzaklaştırıldı. Kalıntı asetonda çözülerek süzüldü ve süzüntüdeki ürün Et2O ile çöktürüldü. (Me)2N S CN CN (Me)2N S NH NH NH 1. MeOH 2. NH3(g) Reflaks 7
500 1000 1500 2000 2500 3000 3500 4000 60 70 80 90 100 Wavenumbers % T r a n s m i t t a n c e
Şekil 19. 6 bileşiğinin IR spektrumu
7 bileşiğinin CDCl3 de alınan 1H-NMR spektrumunda 7.76-6.99 ppm de aromatik,
3.04 ppm de S-CH2, 2.56 ppm de C-CH2 ve 2.09 ppm de ise N-CH3, 3.04 ppm de NH
protonlarının pikleri gözlendi (Çizelge 1). Bu değerler.ilgili literatürdeki sonuçlarla uyum içerisindedir [10, 16, 17].
7 bileşiğinin IR spektrumunda (Şekil 20), 3262 ve 3142 cm-1 de NH pikleri , 2966-2776 cm-1 de ise alifatik CH pikleri gözlenmektedir.
Diiminoizoindol, 7, ile Lu(OAc)3.nH2O ın amil alkolde 6 saat 150oC de ısıtılması
sonucunda yalnızca monomerik Lutesyum ftalosiyanin türevi, 8, hazırlandı. Reaksiyon karışımı deriştirildikten sonra ürüne CHCl3 ilave edilerek süzüldü. Süzüntünün çözücüsü
kuruluğa kadar vakumda uzaklaştırıldı. Kalıntı asetonla yıkanarak saflaştırıldı. Koyu yeşil ürün CHCl3 de az, DMF ve DMSO da kolayca çözünmektedir.
N N N N N N N N S (Me)2N S (Me)2N S N(Me)2 S N(Me)2 NH NH NH (Me)2N +Lu(OAc)3.nH2O M=LuCH3COO Amil alkol 4 M 8 140-150oC
8 bileşiğinin DMSO da ölçülen 1H-NMR spektrumunda, 7.96-6.77 ppm de aromatik, 3.38 ppm de S-CH2, -OOCH3, 2.44 ppm de C-CH2 ve 2.04 ppm de N-CH3 pikleri
gözlenmektedir (Şekil 21). Bu sonuçlar, 2 ve literatürdeki analoğu bileşiklerinin sonuçları ile uyum içindedir [16, 17]. 500 1000 1500 2000 2500 3000 3500 4000 0 20 40 60 80 Wavenumbers % T r a n s m i t t a n c e
ppm (t1)9.0 8.0 7.0 6.0 5.0 4.0 3.0 2.0 1.0 0.0 ppm (t1)8.00 7.507.00 6.506.00
Şekil 21. 8 bileşiğinin 1H-NMR spektrumu (DMSO-d6
8 bileşiğinin DMSO da ölçülen elektronik spektrumunda (Şekil 22), 695.5 ppm de Q-bandı singlet olarak gözlenmektedir. Bu karakteristik band konjuge 18 elektron
sistemlerindeki π-π* geçişine aittir. B-bandı ise 357 nm de gözlenmiştir [16, 17].
Şekil 22. 8 ve 10 bileşiklerinin UV-VIS spektrumu (DMSO, ---- LuPc, 8 , ___ LuPc2,
8 bileşiğinin IR spektrumunda (Şekil 23), metalsiz ftalosiyaninlerde gözlenen NH piki gözlenmemiş, 1754 cm-1 de Lu(OAc) grubu C=O titreşim bandı orta şiddette gözlenmiştir. Diğer gruplara ait titreşim bandlarının metalsiz ftalosiyanin türevleri ile küçük kaymalar dışında aynı olduğu gözlenmektedir.
500 1000 1500 2000 2500 3000 3500 4000 50 60 70 80 90 Wavenumbers % T r a n s m i t t a n c e
Şekil 23. 8 bileşiğinin IR spektrumu
Monomerik Evropiyum ftalosiyanin, 9, 8 bileşiği gibi sentezlendi ve 1H-NMR, (Şekil 24), UV-VIS (Şekil 25) ve IR (Şekil 26) spektroskopileri ile karakterize edildi.
Karakterizasyon sonuçları monomerik LuPc, 8, ile küçük kaymalar dışında aynı olduğu gözlendi (Çizelge 1, 2, 3).
8 bileşiği, 4-(2-dimetilaminoetilsülfonil)ftalonitrilin Lutesyum(III)asetat ile DMF, 1-oktanol, amil alkol gibi farklı çözgenlerde reflaksı ile sentezlenmeye çalışıldı. Fakat
ppm (t1) 8.0 7.0 6.0 5.0 4.0 3.0 2.0 1.0 0.0
Şekil 24. 9 bileşiğinin 1H-NMR spektrumu (DMSO-d6)
Şekil 25. 9 ve 11 bileşiklerinin UV-VIS spektrumu (DMSO, ---- EuPc, 9 , ___ EuPc2,
500 1000 1500 2000 2500 3000 3500 4000 40 50 60 70 80 90 Wavenumbers % T r a n s m i t t a n c e
Şekil 26. 9 bileşiğinin IR spektrumu
3.3.Sandviç Metalli Ftalosiyanin Sentezi
Sandviç Metalli ftalosiyaninler iki farklı yolla sentezlenmeye çalışıldı.
Birinci olarak dendritik alkil ftalosiyanin, 6, bileşiğinin Li metali ile amil alkol de reflaksı yapılarak 6 bileşiğinin lityum tuzu hazırlandı. Hazırlanan tuz çözeltisine ekivalent miktarda monomerik Lutesyum ftalosiyanin, 8, eklenerek tekrar reflaksa devam edildi. Reaksiyon sonunda çözücü vakum distilasyonuyla uzaklaştırıldıktan sonra kalıntı aseton ve eterle yıkandı. Koyu yeşil ürün DMSO ve DMF de çözünmektedir. Bu katının DMSO-d6 da alınan 1H-NMR ve DMSO da ölçülen elektronik spektrumlarında beklenen sandviç lutesyum
ftalosiyanin, 10, olmadığı, muhtemelen monomerik lutesyum ftalosiyanin, olduğu gözlenmiştir.
İkinci yol olarak simetrik ftalosiyanin 2 ile Lityum diizopropilamid (LDA) nın THF de etkileştirilmesi sonucu 2 bileşiğinin lityum tuzu hazırlandı. Hazırlanan tuz izole edilerek IR spektrumu alındı. Lityum tuzunun IR spektrumunda (Çizelge 3), simetrik ftalosiyaninde
bileşiği, 10, ekivalent miktardaki Li2Pc, dendritik alkil ftalosiyanin, 6, ve Lu(OAc)3.nH2O
karışımının 1-oktanol de 200oC de kapalı şilenkte ısıtılmasıyla elde edildi. Reaksiyon karışımının çözücüsü vakum distilasyonuyla uzaklaştırıldıktan sonra yağımsı kalıntı CHCl3
ile çözülerek süzüldü. Koyu yeşil renkli süzüntünün çözücüsü kuruluğa kadar uzaklaştırıldı ve kalıntı Et2O ile yıkandı.
O CH3 O CH3 O CH3 O O N H O CH3 NH O CH3 O O N H O S CH3 O C H3 CH3 O CH3 N(Me)2 S (Me)2N S (Me)2N S O CH3 O CH3 O CH3 O O NH O CH3 N H O CH3 O O N H O S CH3 O CH3 CH3 O CH3 O C H3 O C H3 O C H3 O O N H O C H3 N H O C H3 O O N H O S C H3 O C H3 C H3 O C H3 O C H3 O C H3 O C H3 O O N H O C H3 NH O C H3 O O NH O S C H3 O CH3 CH3 O C H3 (Me)2N S N N N N N N N N Lu N N N N N N N N Li2Pc + 6 + Lu(OAc)3 nH2O 1-oktanol 200oC 10