T.C.
DİCLE ÜNİVERSİTESİ TIP FAKÜLTESİ
AİLE HEKİMLİĞİ ANABİLİM DALI
DİCLE ÜNİVERSİTESİ TIP FAKÜLTESİ AİLE HEKİMLİĞİ POLİKLİNİĞİNE BAŞVURAN POSTMENOPOZAL KADINLARDA OSTEOPOROZ VE HASTA
ÖZELLİKLERİNİN İNCELENMESİ
Dr. Karanfil SITMAPINAR TIPTA UZMANLIK TEZİ
Tez Danışmanı
Doç. Dr. İsmail Hamdi KARA
DİYARBAKIR 2007
İçindekiler I Teşekkür II Kısaltmalar III 1. Giriş 1 2. Genel Bilgiler 3 3. Materyal ve Metot 40 4. Bulgular 42 5. Tartışma 53 6. Sonuç ve Öneriler 59 7. Özet 60 8. Abstract 61 9. Kaynaklar 62 10. Ek 72
TEŞEKKÜR
Aile Hekimliği Anabilim Dalı’nın kurulmasında ve hizmet verilmesindeki desteklerinden ötürü Sayın Rektör Prof. Dr. Fikri CANORUÇ,
Sayın Dekan Prof. Dr. Ramazan ÇİÇEK’e,
Asistanlığım ve tez çalışmalarım süresince her konuda yardım ve desteğini esirgemeyen Aile hekimliği Anabilim Dalı Başkanı Sayın Doç. Dr. İsmail Hamdi KARA’ya,
Rotasyon eğitimleri süresince, bilgi ve deneyimlerinden faydalandığım başta Dahiliye, Pediatri, Kadın Hastalıkları ve Doğum, Acil ve İlk Yardım ve Psikiyatri Anabilim Dalları olmak üzere, burada isimlerini tek tek yazamadığım, Dicle Üniversitesi Tıp Fakültesi’nin değerli öğretim üyeleri ve elemanlarına,
“Tıp Doktoru” olarak yetişmemde emeği geçen İstanbul Üniversitesi Cerrahpaşa Tıp Fakültesi’nin değerli öğretim üyeleri ve elemanlarına,
Uz. Dr. Özcan ÖZDEMİR, Uzm. Dr. Zühre ALPUA, Anabilim Dalı çalışanlarımız, mesai arkadaşlarım, Dr. Nilüfer MATUR, Dr. İlknur DEVRAN SENCAR, Dr. Özgür ERDEM, Dr. Doğan DEMİR, Hemşire Gülfer TOPÇU SAYIN, personellerimiz Suzan İYİ, Veli ADIYAMAN’a ve arkadaşım Bahar DEPREM’ e,
Ayrıca bu günlere gelmemde en büyük paya sahip olan, destek, ilgi ve sevgilerini benden esirgemeyen ve hiçbir fedakarlıktan kaçınmayan çok sevdiğim teyzeme ve anneanneme;
Sonsuz saygı ve teşekkürlerimi sunarım
Dr. Karanfil SITMAPINAR Diyarbakır, 2007
KISALTMALAR
BKI= Beden Kitle İndeksi
KMI (BMC)= Kemik Mineral İçeriği KMY (BMD)= Kemik Mineral Yoğunluğu DSÖ (WHO)= Dünya Sağlık Örgütü DHEAS= Dehidroepiandrosteron sülfat DHEA= Dehidroepiandrosteron
HDL= Yüksek Dansiteli Lipoprotein LDL= Düşük Dansiteli Lipoprotein PTH= Paratiroid Hormonu
OP= Osteoporoz HT= Hormon Tedavisi
GİRİŞ
Menopoz Yunanca' da ay (men) ve sonlanma (pause) kelimelerinden türemiş olup, sözlük anlamı son adettir. Adet kanamalarının kesin olarak bitmesi anlamına gelmektedir (1,2).
Menopoz; kadın yaşam döngüsünde üreme yeteneğinin sona ermesiyle karakterize bir dönemdir. Ovaryan folliküler fonksiyonun kaybıyla birlikte menstruasyonun kalıcı olarak sona ermesidir. Kadın sağlığını biyolojik, psikolojik ve sosyal yönden etkiler (3).
Klimakterium ise Yunanca kritik periyod ve merdiven basamağı anlamına gelen "klimakter" kelimesinden türemiştir. Klimakterium, kadının doğurganlık devresinden, doğurgan olmadığı döneme geçişi içeren tüm evreye verilen addır. Premenopozal, menopozal ve postmenopozal dönemleri içine alır. Bu sürede ortaya çıkan hormonal ve biyokimyasal farklılaşmalar kadın vücudunda çeşitli semptomlara ve biyokimyasal değişikliklere yol açar (3).
Menopozla birlikte overlerde östrojen hormon yapımının azalmasına bağlı olarak sadece genital organlarda değil, tüm vücutta önemli değişiklikler olmaktadır. Menopozda yaşanan ateş basması, terlemeler, baş ağrıları, uyku ve ruh durum bozuklukları gibi belirtiler kişinin yaşam kalitesini ciddi şekilde bozmaktadır. Menopoz yaşı; ırk, sosyo-ekonomik durum, gebelik sayısı, oral kontraseptif kullanımı, eğitim, fiziksel özellikler, alkol tüketimi, menarş yaşı veya son gebeliğin tarihinden etkilenmemektedir. Sadece sigara içiminin kesin biçimde follikül tükenmesini hızlandırdığı saptanmıştır (4).
Klimakterik dönemde iki nedene bağlı organ ve sistem değişiklikleri olmaktadır. Yaşlanmaya bağlı oluşan morfolojik değişiklikler ve overlerdeki östrojen eksikliğine bağlı oluşan genital ve ekstragenital değişiklikler. Kardiovasküler ve kemik dokuda oluşan değişiklikler postmenopozal dönemde kadın hayatını etkileyen önemli değişikliklerdir. Bugün menopozla çağdaş bir şekilde uğraşmaya çalışan araştırıcılar ve tedavisini yönlendiren klinisyenler osteoporoz, kalp damar hastalıkları, beyin fonksiyonları gibi su altında kalmış ciddi sağlık sorunlarıyla ilgilenmektedirler. Tüm bu yaklaşımların amacı 40- 50 yaşlarında menopoza girecek kadınlarımızı 70’li yaşlarına sağlık içinde hazırlamaktır (5).
Günümüzde kadınların menopoz sonrası geçirdiği yıllar uzadıkça yaşam kalitesinin iyileştirilmesine yönelik çalışmalar hız kazanmıştır.
Osteoporoz tüm dünyada önemli bir toplum sağlığı sorunudur (6). Osteoporoz, kemik kırılganlığı ve kırık olasılığının artışı, düşük kemik mineral yoğunluğu (KMY) ve kemik mikroçevresinin bozulması ile karakterize, ilerleyici bir iskelet hastalığıdır (7).
Dünya Sağlık Örgütü (DSÖ) osteoporoz ile ilgili 4 tanı kriteri kabul etmiştir (7): 1- Normal kemik yoğunluğu: KMY veya kemik mineral içeriği (KMI) genç erişkin ortalama değerlerine göre 1 standart sapmadan (SD) daha az sapma gösterenler. 2- Düşük kemik kitlesi (Osteopeni): KMY’nun genç erişkin ortalama değerlerine göre – 1SD ile – 2.5 SD arasında olduğu değerler.
3- Osteoporoz : KMY’nun genç erişkinlerin ortalama değerlerine göre -2.5 SD ve daha düşük olduğu değerler.
4- Yerleşmiş osteoporoz: KMY genç erişkin ortalama değerlerine
göre -2.5 SD veya daha fazla düşük olduğu değerler ve beraberinde bir veya daha çok kırığın eşlik etmesi.
Osteoporoz için birçok farklı sınıflama yapmak mümkündür. Genel olarak postmenopozal (tip 1) ve senil osteoporoz (tip 2) olmak üzere tanımlanabilir. Postmenopozal osteoporoz 50-70 yaşları arasında ortaya çıkan, östrojen yetersizliği ile ilişkisi olan, kemik kaybının hızlı olduğu ve ağırlıklı olarak trabeküler kemikleri tutan bir tablodur. Senil osteoporozda ise kortikal ve trabeküler kemik birlikte tutulmakta, kemik kaybı hızlı olmamakta ve kalsiyum emilimindeki azalmayla oluşan metabolik olaylarla karşımıza çıkmaktadır (8-10).
Osteoporozu olan hastaların çoğunda kemik kaybı yavaş yavaş olmakta ve hastalık ilerleyinceye kadar belirti vermemektedir. İlerlemiş osteoporoz klinikte ekstremite kırıkları, vertebra deformiteleri, akut ve kronik ağrı ile karşımıza çıkmaktadır. Bir kez osteoporotik kırık oluştuktan sonra, kişinin tekrar tam sağlığına kavuşması mümkün olmamakta ve yaşam kalitesi belirgin düzeyde azalmaktadır. Oysa ki erken tanı konulursa osteoporozun durdurulması hatta basit bazı girişimlerle kaybın yerine konulması mümkün olabilmektedir. Osteoporotik kırıklar ve bunların neden olduğu özürlülük özellikle yaşlı nüfusta çok önemli sağlık sorunları yaratmakta, hastaneye yatış gerektirmekte, rehabilitasyon ve bakım ünitelerine yoğun gereksinim doğurmaktadır (11).
Önümüzdeki yıllarda, dünyanın pek çok bölgesinde olduğu gibi ülkemizde de beklenen yaşam süresi uzayacak, bunun sonucunda da osteoporotik kırıklara maruz kalan kişi sayısında dramatik bir artış gözlenecektir. Ortaya çıkacak büyük ekonomik yük ise açıktır. Osteoporozun nedenlerinin anlaşılması, osteoporozlu hastanın değerlendirilmesi, tanı yöntemleri ve tedavi konularında son yıllarda çok önemli bilgi birikimi oluşmasına rağmen hala pek çok hastaya tanı konulmamış ve uygun tedavilerine başlanamamış durumdadır (11).
Osteoporozdan korunmak için alınacak önlemler önceliklidir. Kemik sağlığına doğum öncesinden itibaren dikkat edilmelidir. Ana çocuk sağlığı birimleri de dahil olmak üzere bu konuda eğitimlere ağırlık verilmeli ve özellikle beslenme ve fiziksel aktivitenin önemi vurgulanmalıdır. Toplumumuzda yetersiz olan egzersiz alışkanlıkları küçük yaşlardan itibaren verilmeye çalışılmalıdır (11).
Bu çalışmada Dicle Üniversitesi Tıp Fakültesi Aile Hekimliği polikliniğine başvuran postmenopozal kadınların osteoporoz prevalansı ile sigara içme, beden kitle indeksi (BKI), hormon tedavisi (HT), çay tüketimi, süt ve protein tüketimi ile sosyodemografik özelliklerinin osteoporoz ile ilişkisinin incelenmesi amaçlanmıştır. Araştırma kapsamına 1 Ocak 2006-31 Aralık 2006 tarihleri arasında aile hekimliği polikliniğine başvuran hastalardan menopoza girmiş kadınlar alındı.
GENEL BİLGİLER
MENOPOZ DA FİZYOPATOLOJİK VE ENDOKRİN DEĞİŞİKLİKLER OVERLER VE MENOPOZ
Menopozu her yönü ile tanımlayabilen tek bir teori yoktur. Gebeliğin 42. gününe kadar farklılaşmamış gonadlarda bulunan 300-1300 kadar primordial germ hücresi, oogonia yada spermatozoa olur. Dişilerde, bunlar mitoz sonrası oogoniayı yapar. Oogonialar çoğalır ve gebeliğin sekizinci haftasında yaklaşık 600.000, gebeliğin 20. haftasında ise yaklaşık 6-7 milyonu bulur. Tahminlere göre, bunlardan sadece 700.000-2 milyonu primordial follikülleri oluşturur. Yani, değişken fakat sınırlı sayıda primordial follikül bulunmaktadır. Menarş da overlerde ortalama 380.000 oosit mevcuttur. Belli bir primordial follikülün ovulasyon veya atreziye gitmesini saptayan faktörler bilinmemektedir. Pubertedeki toplam oosit sayısı ve atretik sürecin verimliliği, menopoz yaşını belirler. Doğumda overlerde var olan primordial folliküller,
ovulasyon veya folliküler atrezi sonucunda tükenir. 45 yaşına ulaşan kadında, ortalama 5000-20.000 kadar oosit kalır. Zamanla folliküller azaldıkça, overden salgılanan steroid hormonlar da azalır. Primordial folliküllerin sayısının azalması yanında gonadotropinlere olan duyarlılıkları da azalır (12).
Menopoz, kadınlarda iki sürece bağlı gelişir: gonadotropinlere duyarlı oositler overde tükenirken, geride kalan az sayıdaki oositler de gonadotropinlere yanıt vermezler. Yapılan histolojik gözlemlerde, postmenopozal dönemdeki kadınların ovaryumlarında da bazen primordial folliküller bulunmuştur. Bu, fonksiyonel olarak normal olan folliküllerin daha önce tüketildiğini düşündürür. Bunun sonucunda, kadın yaşlandıkça, gonadotropine direnci artmış ve hormonal aktivitesi azalmış folliküllere sahip olur (13,14).
KLİMAKTERİK DÖNEMDEKİ KADINDA REPRODUKTİF ENDOKRİN SİSTEMDEKİ DEĞİŞİKLİKLER
Her menstruel siklusta oositlerin bir kısmı gelişmek üzere stimüle edilir. Dominant olan dışında diğerleri atreziye uğrar. Bu şekilde follikül sayısında azalma olur ve bunlar over stromasında saklanır. 35 yaş üstünde over gerilemeye, atrezik ve dejenere follikül içermeye başlar. Bu oosit ve follikül kaybı en sonunda östrojen ve inhibinde azalma ile sonuçlanır. Hipotalamus-hipofîz-gonad ekseninde meydana gelen değişiklikler, perimenopoza ait menstruel düzensizliklerden sorumludur. Östrojen seviyesi preovulatuar düzeyine ulaşamadığından, anovulatuar sikluslar oluşur (4,15).
Menopozda inhibin azalması, FSH' ın yükselmesine yol açmaktadır. Artmış FSH, hızlı folliküler gelişime neden olmakta ve bunu izleyen siklusun kısalması perimenopozun ilk belirtisi olmaktadır. Folliküllerin sayısının daha da azalması ile östrojen yapımı düşmeye başlar ve ani LH artışı olur. LH indüksiyona uygun olmayan düzeye ulaştığından, ovulasyon durabilir veya daha sık olarak düzensizleşir. Bu hormonal tablo, klinik yönden düzensiz sikluslar ve kısalmış luteal dönemle veya karşılanmamış östrojen uyarısının eşlik ettiği anovulatuar sikluslar ve endometrial hiperplazi ile beraberdir. Ovulasyon tamamen durduğunda LH yükselmeye başlar ve adetlerin kesilmesi ile menopoz oluşur. Yine de overlerde cevap verecek follikül kaldığından, ilk bir iki yılda klinik bulgu ve semptomların yanında laboratuar bulgularının da tersine dönebileceği akılda tutulmalıdır.
Postmenopozal overler normalde östrojen ve progesteron salgılayan folliküllerden yoksun olmasına karşın, birçok postmenopozal kadın tamamen östrojensiz değildir. Perimenopozda, 40 mIU/ml veya üstünde FSH değerlerine sıklıkla rastlanır. 100 mlU/ml'nin üstündeki değerler hemen daima folliküler tükenmeyi gösterir. FSH, puberteden beri ilk kez LH düzeylerini aşmıştır. LH ve FSH' da ki maksimum artış, menopozdan sonraki ilk 2-3 yıl içinde saptanır. FSH ve LH, kastrasyon düzeyine (40 mlU/ml) çıkar, serum östradiol konsantrasyonu ise 20 pikogram/ml'nin altına düşer (4,16).
Premenopozdaki kadınların dolaşımındaki başlıca östrojen, 17-β östradiol'dür. 17-β östradiol' ün serum konsantrasyonları, over follikülünün ve corpus luteumun olgunlaşması ve involüsyonuna bağlıdır. Premenopozdaki kadınlarda uygulanan ooforektomi, dolaşımdaki östrojen yoğunluklarını, ortalama 120 pg/ml'den 18 pg/ml'ye düşürür. Buna göre, dolaşımdaki östradiolün %95'i over kökenlidir. Folliküller tükendikçe östradiol konsantrasyonları giderek düşer. Zaman geçtikçe daha az follikül kalır ve östradiol yoğunlukları, premenopozda ooforektomi geçirmiş kadınların östradiol düzeyine yaklaşır (4).
Postmenopozdaki baskın östrojen ise, östron' dur. Over veya adrenal, hemen hemen hiç östron üretmez. Postmenopozda yapılan ooferektomi, dolaşımdaki östron veya östradiol düzeylerinde anlamlı değişime yol açmaz. Östronun çoğu, androstenedionun ekstraglandüler aromataz tarafından periferik dönüşümünün ürünüdür. Aromataz karaciğer, yağ dokusu ve bazı hipotalamik nukleuslarda bulunmuştur. Ekstraglandüler aromatazın aktivitesi, yaşa ve vücut ağırlığına bağlıdır. Postmenopozdaki kadınlarda östradiolün hepsi, östrondan östradiole dönüşümün ürünüdür. Postmenopozda, testosteron yapımı sabit kaldığı halde, testosteronun sadece yaklaşık %0.1' i östradiole dönüşür. Menopozdan sonra, östron miktarı östradiolün dört katına çıkmaktadır (4).
Klimakteriumda kısmen overden salınan androjenlerin düzeyleri de düşmektedir. Postmenopozdaki kadınlarda, dehidroepiandrosteron sülfat (DHEAS) ve dehidroepiandrosteron (DHEA) düzeyleri sırası ile %20 ve %40 düşüş göstermektedir. Östrojen takviyesi, DHEAS değerlerinde iki kat artışa yol açmaktadır. Bu nedenle, bu iki androjenin azalma sebebi herhalde östrojen yetmezliğidir. Serum kortizol düzeyleri ise östrojen tedavisinden etkilenmemektedir. İn vitro verilere göre, östrojen, 3β- hidroksisteroid dehidrogenazın bir nonkompetitif inhibitörüdür. Bu bölgedeki kısmi blok, DHEA ve DHEAS yapımını arttıracaktır (4).
Doğurganlık çağındaki kadında en fazla üretilen androjen olan androstenedion klimakteriumda azalır. Postmenopozal kadında, androstenedion yapımı 1500 pg/ml' den 800 pg/ml' ye düşer. Postmenopozdaki over, dolaşımdaki androstenedionun ancak % 20' sini sağlar. Postmenopozda testosteron düzeyleri azalır, fakat bu azalış östrojeninkine eşdeğer değildir. Premenopozda, dolaşımdaki testosteron kaynakları; overler (%25), adrenal bez (%25) ve androstenedionun ekstraglandüler dönüşümü (%50)' dür. Postmenopozdaki overler, premenopozdakinden daha fazla testosteron yapar ve dolaşımdaki yoğunlukların yaklaşık % 50'sini oluşturur (4). Postmenopozal kadınlarda ovaryan venlerdeki testosteron seviyelerinde büyük artışlar bulunmuştur. Bu artışlar, postmenopozal overin premenopozal overe göre daha fazla testosteron salgıladığı hipotezini desteklemektedir (13) .
Menopoz Yaşı
Menopoz yaşıyla ilgili çeşitli kültür ve toplumlarda farklılıklar görülmektedir. Menopoz yaşı heredite, sosyal faktörler, beslenme ve çevresel faktörlere göre değişir. Menopoz yaşı 45-55 yaş arasında ve ortalama 51.4 olarak bildirilmektedir (14,17). ABD' de 2570 kadından alınan bilgilerle gerçekleştirilen Massachusetts Kadın Sağlığı çalışmasında ortalama menopoz yaşı 51.3 olarak bulunmuştur (18). ABD'de kadın ömrünün yaklaşık %34'ü postmenopozal dönemde geçmektedir. Türkiye Menopoz Derneği tarafından 2002 yılında ülkemiz genelindeki merkezler tarafından elde edilen verilere göre, menopoz yaşının 46,7 olduğu anlaşılmaktadır. Türkiye’de ortalama yaşam süresi 72,3 ve postmenopozal kadın oranı 1/5’dir (17).
Yapılan çalışmalarda menarş ve menopoz yaşları arasında ilişki bulunamamıştır. Ev kadınları ve kırsal kesim kadınlarının işçi ve diğer meslek grubu kadınlara göre menopoza bir yıl daha geç girdiği, bekar kadınlarda menopozun evli kadınlara göre daha erken başladığı, sigara bağımlılarının 1.5 yıl kadar daha önce menopoza girdiği, son gebelik yaşının menopoz yaşının yüksekliği ile bağlantılı olduğu, kötü beslenme ile erken menopoz arasında bir ilişki olabileceği ileri sürülmüş, alkol tüketimi ve obesitenin geç menopoza neden olabileceği belirtilmiştir (14,20,21,22). Yağ dokusunun östrojen üretme etkisinden dolayı şişman kadınlarda menopoz daha geç oluşur (2,14,23). Erken menopoza yüksek rakımlı yerlerde yaşayanlarda ve sigara içenlerde daha sık rastlanır. Over kanlanması
bozulduğundan histerektomi geçirmiş kadınlarda da erken menopoza rastlanır (18,24).
Menopozda Klinik Bulgu Ve Semptomlar
Klimakterik dönemde ani östrojen eksikliğine bağlı olarak özellikle östrojen reseptörü içeren pelvik ve ekstrapelvik dokularda fonksiyonel, metabolik veya organik değişimler meydana gelir (2).
Klimakteriyumda yaşanan problemler özetlenecek olursa:
1- Menstrüel kanama paterninin bozulması (hipomenore, hipermenore, anovulasyon ve fertilitede azalma, menstruasyon aralıklarının bozulması ve amenore).
2- Vazomotor semptomların görülmesi (sıcak basması, terleme, sıkıntı).
3- Psikolojik semptomların görülmesi (anksiyete, gerginlik, depresyon ve irritabilite). 4- Atrofik değişiklikler (vulva, introitus ve vajinadaki atrofilere bağlı kaşıntı, disparoni gibi şikayetler, alt üriner sistem atrofisi ve buna bağlı olarak ortaya çıkan sık idrara çıkma, idrar inkontinansı, aseptik üretrit ve sistit).
5- Uzun süreli östrojen eksikliğine bağlı geç dönemlerde ortaya çıkan ve hayatı tehdit edebilen kalıcı sistem değişimleri (kardiyovasküler sistem ve kemik dokusuna ait değişimler)
6- Nörolojik sistem değişiklikleri (Alzheimer, Demans)(14).
Vazomotor Semptomlar
Perimenopoz ve postmenopoz kadınların %75-85’i ateş basması ve terleme şikayetinden yakınır. Östrojen yetersizliğinin klasik semptomu sıcak basmasıdır (25). Bu semptom sıklıkla çarpıntı ve korku hissi ile beraber ve bazen titremeyle devam eden tekrarlayan, geçici kızarma, terleme ve sıcak hissetme periyotlarıdır (26). Bütün epizod genellikle bir-üç dakikadan fazla sürmez ve günde 30 defaya kadar tekrarlayabilirse de günde beş-on defa görülmesi daha sıktır (27).
Ateş basmaları geceleri ve stres zamanlarında daha sık ve daha şiddetlidir. Doğal menopozlu hastaların en az yarısında, cerrahi menopozlu kadınların daha fazlasında hissedilir (23,27). Ateş basması premenopozda da görülmekle birlikte asıl postmenopozal döneme ait bir semptomdur. Çoğu kadın tarafından bir-iki yıl
boyunca hissedilirken, %25-50’sinde beş yıldan uzun süreli olarak görülür (14). Fizyolojisi tam olarak anlaşılmamakla birlikte hipotalamus orijinli olup östrojen eksikliğinin sonucu olduğu düşünülmektedir (28).
Vazomotor semptomlu hastalarda, bu semptomun bulunmadığı hastalara kıyasla, LH/FSH oranında veya LH/total östrojen oranında bir fark olmadığını saptamışlardır. Ayrıca, ateş basmalarının bildirildiği zamanlarda östron veya östradiol düzeylerinde belirgin bir değişiklik saptamamışlardır. Her ateş basması ile LH piki arasında önemli bir ilişki gözlemlenmiştir. Buna göre, gonad yetmezliği vakalarında ya bizzat LH ya da LH salgısını başlatan faktörler ateş basmalarından sorumlu tutulmuştur (29). Ateş basmaları postmenopozal dönemde görülen en sık semptom olmakla birlikte, fizyolojik birçok parametreyle birliktedir. Psikolojik değişikliklerin önemli bir göstergesi olmasına rağmen ciddi bir sağlık problemi değildir (14).
Psikolojik ve Cinsel Fonksiyonlara ait değişimler
Östrojen uykuya geçişi kolaylaştıran ve uykunun “Rapid eye moment” fazını hem sayı hem de süre olarak arttıran bir hormondur. Premenopozal dönemde duygusal denge zayıf uyku paterniyle bozulabilir. Ateş basması uykunun kalitesini etkileyebilir ve gelecek günün problem ve stresleriyle baş edebilme yeteneği azalır (30). Asemptomatik olduğu rapor edilen postmenopozal kadınlarda bile östrojen tedavisiyle insomnia da iyileşme elde edilebilir (14).
Östrojenin mental fonksiyonlar üzerine direk etkisi olduğu görülmektedir ve hormon tedavisinin postmenopozal kadında hem kısa hem de uzun vadeli hafızayı arttırdığı gösterilmiştir (31,32). Alzheimer hastalığı gelişme riskinin östrojen tedavisi ile düştüğü bildirilmiştir (33). Ayrıca östrojen tedavisinin kadının iyilik hali üzerinde, ateş basmaları gibi semptomların giderilmesinin ötesinde, daha güçlü bir etki yaptığı rapor edilmiştir (14). Postmenopozal kadınlarda yaşlanma ve çocuk doğurma yeteneklerinin kaybolması psikolojisinin yanısıra, cinsel yönden dişilik görevinin azalacağı veya kaybolacağı endişesi yerleşebilir. Bu duyguları kompanse etmek amacı ile psikolojik ve sosyal yapılarına göre bazı klimakterik kadınların cinsel isteklerinde ve koitus frekanslarında artışlar gözlenebilir (2).
Menopoza ilişkin psikolojik belirtiler şunlardır : • Depresif ruh hali
• Sinirlilik
• Karar vermede zorluk çekme • Kaygı (endişe)
• Unutkanlık
• Dikkat toplamada güçlük çekme • Kendini değersiz hissetme • Uykusuzluk
• Yorgunluk hissi
• Baş dönmesi nöbetleri • Cinsel istekte azalma (2)
Yapılan bir çalışmada klimakteryum döneminde irritabilite-sinirlilik %10-91, depresyon %13-86, konsantrasyon kaybı %82, kişilik değişikliği %81, uyku bozukluğu %9- 77, motivasyon yokluğu %77, hafıza kusuru %75, sıcak basması %37, baş ağrısı %19 ve aşırı terlemenin %18 oranında olduğu belirtilmiştir (34).
Psikologlar tarafından yapılan araştırmalar, menopozun yaş ilerlemesine bağlı ortaya çıkan gelişimsel bir değişim dönemi olduğunu ve kadınların bu döneme ilişkin yaşadıkları sıkıntıların adet kanamasının sona ermesinden çok sağlık, yaşlanma, psikolojik ve sosyal yaşamdaki değişiklikler gibi psikososyal etkenlere bağlanabileceğini göstermişlerdir. Jinekologlar tarafından yapılan çalışmalarda ise menopoza bağlı ortaya çıkan belirtiler hormon düzeyindeki değişimlere bağlanmıştır. Bu iki farklı bakış açısı psikososyal görüş ve biyolojik görüş adı altında ifade edilmektedir. Tam olarak kanıtlanmış olmasa da menopoz döneminde meydana gelen psikososyal ve biyolojik değişiklikler psikolojik problemler için tetikleyici olmaktadır ve mevcut psikolojik sıkıntının kaynağı çok yönlüdür (34).
Menopoz dönemindeki pek çok kadının duygusal rahatsızlık yaşadığı, ancak bu rahatsızlıkların menopoz öncesi dönemden başlayarak menopoz dönemine mi taşındığı, yoksa doğrudan menopoz döneminde mi başladığı ayırtedilememektedir. Menopoz döneminde her kadında duygu durumunda dalgalanmalar ve davranış bozukluklarının ortaya çıkmadığını ve menopoz ile doğrudan ilişkili duygusal bir sendromun bulunmadığını gösteren çalışma bulguları mevcuttur (34).
Atrofik değişiklikler
Postmenopozal kadınlarda, vajina epitelinde farklı derecelerde atrofîk değişiklikler oluşur. Vagina zamanla kısalır ve daralır. Vagina cildi incelmiş, rugalar düzleşmiştir. Epitel inceldikçe, kapiller yatak yaygın ve yama tarzında parlar. Yüzey
kapillerlerinin yırtılması düzensiz olarak dağılmış peteşi ve kahverengine çalan akıntıya sebep olabilir. Vajinal duş veya koitusa bağlı minimal travma, hafif vajinal kanamaya sebep olabilir. Östrojen yetersizliği sonucu, vajina epiteli hücrelerinde yeterli glikojen depolanamaz. Döderlein basilleri için yeterli gıda ortamı kaybolduğundan bu bakterilerin yerine çeşitli bakterilerden oluşan bir flora oluşur. Vajinanın asit reaksiyonu geriler. Bu nedenlerden dolayı, vajinal atrofî ve lokal bakteriyel yayılım, vajinal akıntı ve kaşıntıyı erken dönemde başlatabilir. Vajinal epitelin ileri derece atrofisi ile kapiller yataklar giderek seyrekleşir; hiperemik görünümün yerini, düz, parlak ve soluk renkli görünüm alır (12,13) .
Serviks uterinin rengi de, vajina gibi soluklaşır. Östrojenlerin azalmasına paralel olarak servikal kanalı döşeyen silindirik epitelin yerini yassı epitel alır (12). Genellikle serviks küçülür ve servikal mukus salgısında azalma olur. Bu durum disparoni şikayetine neden olabilecek vajinal kuruluğu arttırır (13). Klimakterik kadında, uterusun aşağı inmesi, sistosel ve rektosel insidensi artabilir. Bu durum muhtemelen östrojen kaybı ile birlikte, yaşa bağlı hücre bölünmesi yavaşlaması ve doku esnekliğinin azalması ile de ilişkilidir (4).
Östrojen, mesane ve üretra epitelinin devamlılığında önemli bir rol oynar. Belirgin östrojen eksikliği, bu organlarda atrofîye neden olabilir. Bu durum üriner urgency, inkontinans, piyüri veya dizüri olmadan pollaküri ile karakterize atrofîk sistite yol açabilir. Meatusun sarkması ve epitelin incelmesi ile üretral tonusun kaybı dizüri, üretral meatusda hassasiyet ve bazen hematüriye neden olan üretral karünkül oluşumunu kolaylaştırır (13).
Hem endometrium hem de myometriumun küçülmesiyle birlikte, uterus atrofîye uğrar. Bu küçülme, küçük ve orta boy uterus myomu olan kadınlar için faydalıdır. Myomun boyutlarındaki küçülme ve semptomların kaybolması, sık olarak cerrahi tedavi gerekliliğini ortadan kaldırabilir. Folliküler aktivitenin durmasıyla, endometriumun uyarımı da son bulur. Bu doku yalnız uterus içinde değil, ektopik yerleşimde de inaktif olur. Böylece, endometriozisin semptomatik alanları giderek küçülür ve daha az rahatsızlık verir. Ayrıca tubalar ve overler de küçülür (13).
Kardiyovasküler sisteme ait değişiklikler
Reprodüktif dönemdeki kadınlar, aynı yaştaki erkeklere oranla 2,5-4,5 kat daha az kardiyovasküler hastalık riskine sahipken, 55 yaşını aşmış bir kadında
koroner damar hastalığı görülme sıklığı, 35-54 yaş grubuna göre 10 kat artış gösterir. Böylelikle 50 yaşından itibaren bir kadının yaşamı boyunca koroner kalp hastalığına yakalanma ihtimali %46, bu hastalıktan ölüm ihtimali %31'e ulaşır. Yapılan çalışmalar reproduktif dönemde östrojenin kardiyoprotektif etkisini ortaya koymaktadır. Nitekim genç erişkinlik dönemindeki erkeklerle kadınlar arasındaki farklılık, menopozu takiben yavaş yavaş ortadan kalkmaktadır. Yaklaşık 10 yıl sonra eşit düzeylere ulaşmaktadır. Böylece kalp ve damar hastalıklarına bağlı ölümler, postmenopozal kadınlarda ilk sıraya yerleşmektedir (2,35).
Klimakteryumda meydana gelen östrojen eksikliği sonucunda kan lipid tablosundaki değişiklikler vasküler hastalık riskinde artışa neden olabilir. Bu değişikliklerin doğrultusunda oluşabilecek enfarktüs benzeri ciddi komplikasyonlar, klimakteryumun sonlarına doğru ya da yaşlılık döneminde ortaya çıkar. Menopoz öncesi dönemde, kadınlar aynı yaştaki erkeklere göre çok daha düşük kardiyovasküler hastalık riskine sahiptirler. Menopoz sonrası dönemde ise, kadınların risk oranı hızla artarak erkeklerin risk oranına yaklaşmaktadır. Bu bulgular, östrojenin kardiovasküler hastalık riskine karşı koruyucu bir özelliğe sahip olduğuna işaret etmektedir. Epidemiyolojik araştırmalar, kardiovasküler hastalık riskinin östrojen alan postmenopozal kadınlarda, hormon tedavisi görmeyen, aynı yaş grubuna mensup kadınlara nazaran %50 oranda daha düşük olduğunu ortaya koymuştur. Büyük ölçüde, östrojenin kan lipid profiline olan olumlu etkisine bağlanan bu risk azalmasının, kısmen östrojenin doğrudan damar sistemi üzerine olan etkisinden de kaynaklandığı düşünülmektedir. Östrojenin periferik damar direncini düşürdüğünü, damar dilatasyonuna neden olduğunu ve kapiller kan dolaşımını artırdığını ortaya koyan araştırmalar mevcuttur (36-38).
Menopozdan önce kadınların koroner kalp hastalığına erkeklerden daha az yakalanması, östrojenlerin lipoprotein risk faktörleri üzerindeki koruyucu etkisine bağlanmıştır (14,23,35,36). Östrojenin ateroskleroz gelişimini, lipid ve lipoprotein metabolizması üzerindeki etkilerinden bağımsız olarak farklı vasküler mekanizmalarla da inhibe ettiği gösterilmiştir. İnsan arterlerinin endotelyumunda ve düz kaslarında belirgin derecede östrojen ve progesteron reseptörlerinin bulunduğunun belirlenmesi de bu çalışmaları desteklenmektedir. Pek çok çalışma bu reseptörlerin, kolesterol değişimi, trombosit agregasyonu, düz kas proliferasyonu ile prostaglandin sistemindeki değişimleri etkilediğini yani fizyolojik olarak aktif olduğunu göstermektedir (14,37).
Östrojenin kardiyo-vasküler sistem üzerine etkisini gruplandırırsak;
1-Östrojen lipid profiline etki eder. Östrojen eksikliğinde HDL düzeyleri düşerken LDL düzeyleri artar.
2-Östrojenin arter üzerine doğrudan aterosklerozu önleyici etkisi vardır.
3-Östrojen, nitrik oksit, prostasiklin gibi vazodilatatör ve antiagregan faktörlerin etkisini arttırır.
4- Kalp üzerine doğrudan inotropik etkisi vardır.
5-İnsülin düzeylerini düşürerek kardiyo-vasküler hastalıklar için risk faktörü olan bozulmuş glukoz toleransını düzeltici rol oynar.
6- Lipoprotein oksidasyonunu inhibe eder. Postmenopozal dönemde total kolesterol ve LDL kolesterol düzeylerinde belirgin artış görülürken, HDL kolesterol düzeylerinde düşüş olmaktadır (Trigliserid ve lipoprotein artar) (39).
Yakın zamandaki Women’s Health Initiative (WHI) ve Heart and Estragen/Progestin Replacement Study I ve II çalışmalarının sonuçları ortaya çıkana kadar östrojen veya Östrojen + Progesteron kombine tedavisi kardiyovasküler hastalıktan primer ve sekonder korunma amacıyla dünyada yaygın olarak kullanılmaktaydı. Bu çalışmalarda hormon tedavisinin kardiyovasküler hastalık riskini azaltmadığı saptandı (40-42). Bütün bu çalışmaların ışığında Ocak 2003 tarihinde “Food and Drug Administration (FDA)” Östrojen ve Östrojen + Progesteron kombine tedavisinin konumunu değiştirdi ve kardiyovasküler hastalıktan korunma amacıyla kullanılamayacağı kararına vardı (43).
OSTEOPOROZ
Osteoporozun ilk defa kesin tarifi 1829 yılında histolojik olarak gözeli kemik anlamına gelen "porous bone" başlığı altında Strasbourg'lu patolog Jean Georges Lobstein tarafından yapılmıştır. 19. yüzyıldaki Fransız ve Alman hekimleri osteoporozdan bahsedip; normal mineralize olmuş fakat miktarı azalmış kemik dokusu olarak tarif etmiştir. Takiben hastalığın balık yağı ile tedavisi 1824'te, güneşle olan ilişkisi ise 1919 yılında ortaya konmuştur. İngiliz bilim adamlarınca 1922 yılında kemiğin mineralizasyonunda D vitaminin rolü ortaya konmuştur. Hastalığın östrojen yetmezliğine bağlı olduğunu ilk ifade eden 1940 yıllında Fuller Albright ve arkadaşları olmuştur. Kırıkdan korunma 1973'de, cerrahi menopozdan sonra hormon kullanımı 1976'da, postmenopozal ve senil osteoporoz ayrımı ancak 1983 yılında
yapılabilmiştir. Son olarak osteoporoz daha önce de belirtildiği gibi 2000 yılında National Institutes of Health tarafından tanımlanmış ve düşük kemik kütlesi, kemiğin mikromimarisinde değişikler ve bunun sonucunda kemik kırılganlığında artışla karakterize sistemik bir hastalık olarak ifade edilmiştir (8) .
Sınıflandırma: ♦Yaşa göre : • juvenil osteoporoz • erişkin osteoporoz • senil osteoporoz ♦Lokalizasyona göre : • genel osteoporoz • bölgesel osteoporoz ♦Tutulan kemik dokuya göre:
• trabeküler osteoporoz • kortikal osteoporoz ♦Etyolojiye göre :
• primer osteoporoz • sekonder osteoporoz ♦Histolojik görünüme göre:
• hızlı döngülü osteooporoz • yavaş döngülü osteoporoz
Günümüzde yaygın olarak etyolojiye göre yapılan sınıflandırma kullanılmaktadır. Etyolojik yönden primer ve sekonder olmak üzere iki grupta gözden geçirilebilir. Vakaların büyük çoğunluğu (%80) primer osteoporoz olarak karşımıza çıkarken sadece %20’si diğer hastalıklara sekonder olarak oluşmaktadır (7-9).
Primer osteoporoz:
A-İdyopatik Juvenil Osteoporoz: Puberte öncesi kız ve erkek çocuklarda görülür. 2-4 yıl süren akut bir klinik seyir takip eder ve kemik büyümesi devam ederken spontan bir remisyon olur.
B-İdyopatik osteoporoz: (nedeni tam aydınlatılamayan premenopozal kadın, gebelik, genç ve orta yaşlı erkek) Genç erişkinlerde her iki cinste de görülen etyolojisi kesin bilinmeyen, omurga, kaburgalar ve iskeletin uzun kemiklerinde
kırıklarla seyreden tipidir. Klinik gidiş hafif veya ağır olabilir ancak genelde ilerleyici ve tedaviye dirençlidir.
C-İnvolusyonel osteoporoz: En sık görülen şekildir. Orta yaşlarda başlayarak, yaşla birlikte artar. Bu tip osteoporoz iki gruba ayrılır. Menopoz sonrası oluşana Tip I, yaşlandıkça oluşana ise Tip II.
Tip I Postmenopozal Osteoporoz: Trabeküler kemik kaybı normalden oldukça fazla, kortikal kemik kaybı ise normalden hafif yüksektir. Omurgadaki kırıklar genellikle "crush" tipi olup ağır ve deformasyonla birliktedir. Kemik kaybının hızlandığı bu dönemde trabeküler yapılar zayıflar ve omurgada akut çökmeler gözlenir. Bu dönemde östrojen kaybına bağlı olarak kemik kaybı hızlanır, parathormon (PTH) sekresyonu azalır, kalsitonin sekresyonu artar, 1 alfa-25(OH)² vitamin D yapımındaki azalma ile birlikte barsaktan kalsiyum absorpsiyonu azalır, bu da kemik kaybını hızlandırır.
Tip II Senil (yaşlılığa bağlı) Osteoporoz: 70 yaşın üzerindeki kadın ve erkeklerde etkilendiği yavaş kemik kaybı mevcuttur. Omurga kırıkları kama tipi kırıklardır ve hastada "yaşlı kadın kamburu" diye tarif edilen dorsal kifoza neden olur. Kemik yoğunluğu değerleri gerek trabeküler gerekse kortikal kemikte düşüktür. Senil osteoporozlu hastalarda kemik kaybından sorumlu iki mekanizma; barsaktan kalsiyum absorpsiyonunun azalması sonucu sekonder gelişen hiperparatiroidizm ve kemik formasyonunun bozulmasıdır (8-10).
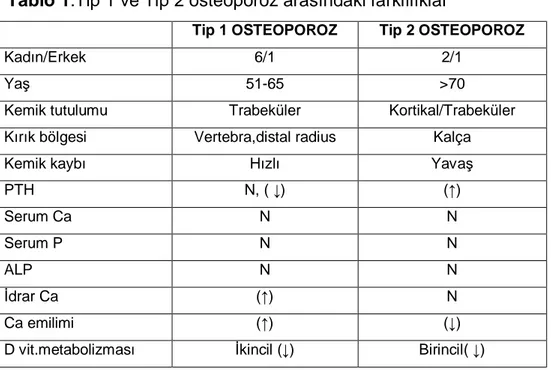
Tablo 1.Tip 1 ve Tip 2 osteoporoz arasındaki farklılıklar
Tip 1 OSTEOPOROZ Tip 2 OSTEOPOROZ
Kadın/Erkek 6/1 2/1
Yaş 51-65 >70
Kemik tutulumu Trabeküler Kortikal/Trabeküler Kırık bölgesi Vertebra,distal radius Kalça
Kemik kaybı Hızlı Yavaş
PTH N, ( ↓) (↑) Serum Ca N N Serum P N N ALP N N İdrar Ca (↑) N Ca emilimi (↑) (↓)
Sonuç olarak postmenopozal dönemde kemik rezorpsiyonunun hızlı, formasyonun yavaş olduğu şekille (hızlı kemik kaybeden, hızlı turnoverlı tip) karakterize kemik kaybı hakimken, senil osteoporozda kemik rezorpsiyonunun artmayıp, formasyonun azaldığı bir kayıp mevcuttur (yavaş kemik kaybeden, yavaş turnoverlı tip) (Tablo-1).
Sekonder osteoporoz
a- Endokrin nedenler: Hipogonadizm, over agenezisi, hipertirodi, hiperparatirodi, Cushing hastalığı, Diyabetes Mellitus
b- Malign nedenler: Multiple myelom, lösemi, lenfoma, mastositosis
c- İlaçlar: Heparin, etanol, tiroid hormonu, antikonvülzanlar, kemoterapötikler, steroidler
d- Kollajen sentez bozuklukları: Homosistinüri, Ehler-Danlos sendromu, osteogenesis imperfekta, Marfan sendromu
e- Hepatik ve gastrointestinal nedenler: Primer bilier siroz, subtotal gastrektomi, hemokromatozis, malabsorbsiyon
f- Beslenme: Diyette kalsiyum azlığı, proteinden zengin diyet g- İmmobilizasyon
h- Diğer: albinizm, sigara (8-10).
Epidemiyoloji
Osteoporozun en sık görülen formu olan primer osteoporoz, genellikle 45 yaştan sonra başlar ve yaş ilerledikçe görülme insidansı artar. 50 – 60 yaş arasında kadınlarda prevalans %40–55, 60 – 70 yaş arasında %75, 70 yaş üzerinde ise %85-90 olarak bildirilmektedir (44). Osteoporozun kırıkla olan bağlantısı özellikle yaşlı popülasyon için önemli bir toplum sağlığı sorunudur. KMY azaldıkça kırık riski artar. KMY’nun 1 SD azalması kırık riskini 3 kat artırır. 50 yaşında, beyaz (Caucasian) bir kadında osteoporoza bağlı kırık riski tüm yaşam boyu % 40 iken bu oran erkeklerde %13’tür (44,45).
İngiltere’de her yıl 60.000 kalça kırığı, 50.000 radius kırığı ve 40.000 klinik olarak tanı konmuş vertebra kırığı görülmektedir. Bu rakamlar ABD için sırasıyla 300.000, 500.000, 200.000’dir. Bunlara ek olarak, özellikle osteoporoza bağlı pelvis ve humerus kırığı gibi yaşlılarda önemli bir morbidite sebebi olan kırıkların toplamı İngiltere’de 250.000, ABD’de ise 1.500.000 dolayındadı (45). Osteoporoza bağlı kırık
insidansında bölgesel farklılıklar önemli rol oynar. Bunun nedeni özellikle ırklar arasındaki iskelet boyutlarının farklı olması ile açıklanabilir. Asyalı ve beyaz kadınlarda osteoporoz yaygın iken, Afrika kökenli Amerikalı siyah kadınlarda nadir olarak izlenmektedir (45).
Osteoporoz Patogenezi
Kemik Yapısı
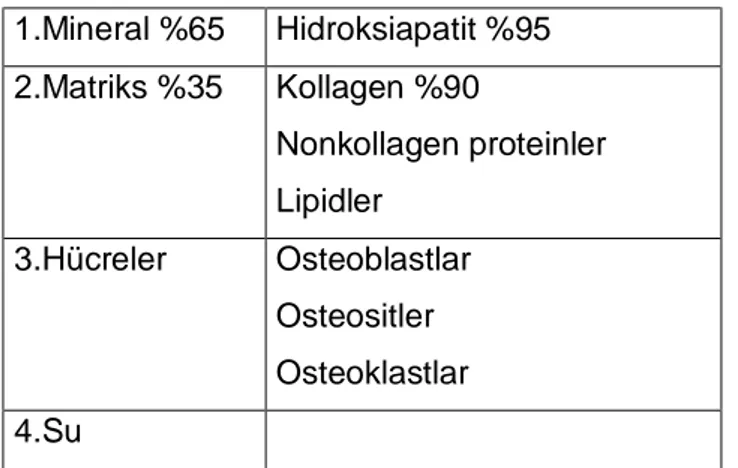
Kemik insan vücudunda önemli fonksiyonları olan özellişmiş bir bağ dokusudur. Hayati organları korumak, kan hücrelerinin kaynağı olan kemik iliğinin çatısını oluşturmak, kalsiyum ve fosfat gibi birçok iyonun kaynağı ve depo yeri olmak, normal postürün ve bedensel hareketlerin sağlanması gibi birçok önemli görevi vardır. Kemikte mineralize bir kollajen çatısı bulunmaktadır. Kollajen; matriks kollajen, proteoglikan, nonkollajen proteinlerden oluşur (Tablo-2).
Tablo 2. Kemiği oluşturan matriks ve mineral elemanların oranı 1.Mineral %65 Hidroksiapatit %95 2.Matriks %35 Kollagen %90 Nonkollagen proteinler Lipidler 3.Hücreler Osteoblastlar Osteositler Osteoklastlar 4.Su
Kemik kortikal (kompakt) ve trabeküler (spongiyoz) bölümlerden oluşur. Kompakt kemik uzun kemiklerin diafizinde ve yassı kemiklerin yüzeyinde bulunur. Ortasındaki Haversian kanalın içinde damar sistemi, sinirler ve etrafında düzgün dizilimli tabakalardan oluşur. Trabeküler kemik ise, uzun kemiklerin uçlarında (femur boynu gibi) ve yassı kemiklerin yapısında bulunan kemiktir. İçinde kemik iliği içeren boşluklar ve bağlantılı plaklar bulunduran oluşan gevşek bir sistemdir.
Kemiğin 3 ana hücresi bulunur:
- Osteoklast (kemik yıkımından sorumlu) - Osteoblast (kemik yapımından sorumlu) - Osteosit (olgunlaşmış osteoblast)
Osteoklastlar hematopoetik sistemin ana hücrelerinden köken aldığı düşünülen büyük ve multinükleer hücrelerdir. Kemik yıkımı sırasında bir proton pompası yardımıyla hidrojen iyonlarını ortama salarak kemik mineralinin eritilmesini sağlarlar. Bu asidik ortama lizozomal enzimlerin salınması ile kemik matriks parçalanır. Bu işlem sırasında osteoklastların kemik matrikse yapışması ise integrin denilen yüzey proteinleri tarafından sağlanır. Integrinlerin yokluğunda osteoklast işlev göremez. Osteoblastlar kemik iliğinden köken alan, kemik matriksin yapımından ve mineralizasyonundan sorumlu hücrelerdir. Çeşitli büyüme faktörlerini sentezlerler. Ayrıca osteoklastların farklılaşmasında ve fonksiyonunda önemli görevleri vardır. Osteoblast giderek kendi yaptığı mineralize kemik içinde hapsolur ve osteosit haline dönüşür. Osteoblastların bir kısmı ise kemik yüzey hücresi olarak kalır. Osteositlerin fonksiyonunun ise, mekanik uyarıları algılayarak kemik cevaplarını oluşturmak yönünde olduğu düşünülmektedir. Kemiğe binen fiziksel uyarının osteosit tarafından üretilen kimyasal haberciler yoluyla kemikte yeniden yapılanmaya neden olduğu ileri sürülmektedir. Bu kimyasal habercilere örnek olarak glukoz 6-fosfat dehidrojenaz, nitrik oksit, prostaglandinler ve insülin benzeri büyüme faktörü verilebilir (46).
Kemik Yeniden Yapılanması (Remodeling)
Yeniden yapılanma hem kortikal hem de trabeküler kemikte eski kemiğin yerini yeni kemiğin alması ile sonuçlanan ve hayat boyunca devam eden bir süreçtir. Kemik yüzeyde önce aktivasyon ve osteoklastik bir yıkımla başlar. 3 hafta kadar süren bu işlemi takipen osteoid oluşumu ile mineralizasyon tamamlanır. Bu olaylar, ortalama 2-6 ay sürede oluşur ve lokal büyüme faktörlerinin etkisi altında gelişir. Yapılan kemik yıkılan kemiğe eşit olduğu zaman bir denge (homeostazis) söz konusudur. Osteoklastik yıkım arttığı zaman yeniden yapılanma yüzeyinde lakünaların sıklığı ve derinliği artar. Bu dönemde trabeküller giderek incelir ve yer yer kırılarak ortadan kalkabilir. Kemik yeniden yapılanması oldukça karmaşık bir mekanizma tarafından düzenlenir. Mekanik stres, sistemik hormonlar (Paratiroid hormon, 1-25 (OH)2 vitamin D3, seks steroidleri, tiroid hormonları, glukokortikoidler,
Kemik Kütlesinin Hayat Boyunca Gösterdiği Değişiklikler
Çocukluk ve ergenlik döneminde hızlı bir iskelet büyümesi gerçekleşir ve 3. dekadın ortalarında doruk kemik kütlesine ulaşılır. Dördüncü dekaddan sonra her iki cinste ve sağlıklı bireylerde yaşa bağlı kemik kaybı oluşmaya başlar. Kadınlarda menopoz yıllarında hızlı kemik kaybı dönemi vardır ve 5-10 yıl kadar sürer. Kayıp hızı trabeküler kemikte daha fazladır. Bunun nedeni metabolik aktivitenin trabeküler kemikte kortikal kemiğe göre daha yüksek olmasıdır. Trabeküler kemikte yüzeyin hacme oranı fazladır ve bu nedenle daha fazla remodeling ünitesi çalışmaktadır. Hayat boyunca trabeküler kemiğin %50' sinin, kortikal kemiğin ise %35' inin kaybolduğu hesaplanmaktadır.
Postmenopozal kemik kaybının başlıca nedenleri; Serum 1,25 (OH)2 vit D3 düzeyi azalır
Kalsiyumun barsaktan emilimi azalır. IL-1 ve IL-6 düzeyi artar
TNF düzeyi artar
İdrarda kalsiyum atılımı artar
Sekonder hiperparatiroidemi gelişir (46-48).
Doruk kemik kütlesi
Doruk kemik kütlesi, normal büyüme sırasında kazanılan en yüksek kemik kütlesi düzeyidir. Bir başka deyişle kişinin yaşlanmasıyla artan kemik kaybı süreci başlamadan önce kişinin kazandığı maksimum kemik miktarıdır. Doruk kemik kütlesi, ileri yaşlardaki kemik kütlesini anlamada ve kırık riskine hassasiyeti ve direnci ortaya koymada önemli bir faktördür. Adolesan dönemde, doruk kemik kütlesinin yaklaşık yarısına yakını hızlı bir kemik büyümesiyle oluşmaktadır. Bu dönem, doruk kemik kütlesini arttırmak ve hayatın ileriki dönemlerinde osteoporoz riskini azaltmak için önemli bir fırsattır. Doruk kemik kütlesine erişme yaşı en erken 17-18, en geç 35 yaş olarak bilinmektedir. Hidroksiapatit, kemiğin en önemli mineralidir. Ağırlığının yaklaşık %40’ını kalsiyum oluşturmaktadır. Kişinin kemik mineral düzeyi diyet ve egzersiz ile değiştirilebilir. Kalçada kemik yoğunluğu 18 yaş civarında doruğa ulaşır ve bundan sonra yaşam boyunca yavaş yavaş düşer. Omurgadaki hızlı büyüme fazı 18 yaşına kadar tamamlanır, ama total omurga kütlesi menopoz sonuna kadar yavaşça artar. Bazı bölgelerde, özellikle fazla kilolu kadınlarda bu artış daha hızlı olmaktadır. Önkol ve el kemikleri, büyümenin
durmasından sonra, çok az bir periosteal genişleme gösterdiğinden kütle ve yoğunluğu, paralel olarak değişir. Radial shaftta kemik kütlesi menopoza kadar yavaş bir artış gösterir.
İskelet boyutunu ve yoğunluğunu etkileyen ana etkenler şunlardır: 1- Genetik faktörler
2- Çevresel faktörler
a- Hormonal faktörler, b- Beslenme,
c- Fiziksel aktivite.
Doruk kemik kütlesi üzerinde etkili olan bu faktörlerden genetik kodu değiştirmek henüz mümkün olmadığı için çevresel faktörlerin tanınması ve değiştirilmesi osteoporozun önlenmesinde ilk basamağı oluşturmalıdır. Dolayısıyla hormonal faktörler, beslenme ve fiziksel aktivitenin kontrolü önem kazanmaktadır (49,50).
Genetik Faktörler :
Doruk kemik kütlesinin oluşumunda yüksek oranda genetik faktörlerin rol oynamaktadır. Genç yaşlarda genetik faktörlerin doruk kemik kütlesinin belirlenmesinde çevresel faktörlerden daha etkindir. Çevresel faktörler daha ileri yaşlarda önem kazanmaktadır. Ancak doğum öncesi dönemde plasental beslenme düzeyini etkileyen çeşitli faktörler gibi çevresel etkenler doruk kemik kütlesi belirlenmesinde genetik faktörlerin önüne geçmektedir. Özellikle son yıllarda maternal sigara kullanımı, beslenme ve fiziksel aktivite gibi anneye ait bazı faktörlerin de doruk kemik kütlesi üzerinde etkili olduğu gösterilmiştir. Kırık riskinin intrauterin hayat sırasında programlandığı düşünülmektedir. Düşük doğum ağırlığı ve infantil dönemdeki vücut ağırlığı ile yetişkin kemik kütlesi arasında bir bağlantının olduğu savunulmaktadır. En çok araştırılan gen Vitamin D reseptör (VDR) genidir. Çelişkili bilgiler verilmekle birlikte VDR genindeki polimorfizmin KMY’nun genetik değişkenliğinin %15-75'inden sorumlu olduğu düşünülmektedir (47,48) Kollajen IA1, östrojen reseptörü, interlökin-6 ve tümör büyüme faktörü-b (TGF-b) genleride etkili olabilecek diğer genlerdir (49,50).
Çevresel faktörler :
A-Hormonal Faktörler: Doruk kemik kütlesini etkileyen faktörler, iskelet büyümesini düzenleyen insulin benzeri büyüme faktörü-1 ve epifizyel olgunlaşmayı uyaran gonadotropik hormonlardır (51). Östrojen eksikliği ve amenore kemik kemik kütlesini azaltıcı etkiye sahiptir (52). Hipotalamo-pitüiterover aksının disfonksiyonu adolesan kız çocuklarına oligomenore yada sekonder amenoreye neden olarak doruk kemik kütlesinde azalmaya neden olur. Bu nedenle kız çocuklarında menstruel siklusun gözlenmesi ileriki yaşlardaki osteoporozun önlenmesi bakımından da önemlidir. Çocukluk çağındaki büyüme hormonu kemik kütlesi oluşumu için major belirleyici iken, yetişkinlerde kemik yeniden yapılanmasını etkileyerek KMY’nun sürdürülmesini sağlar (53).
B-Beslenme ve Kalsiyum: Kemik dokusu protein ve mineralden oluşur. Enerji, protein, vitamin ve mineral gibi beslenme faktörleri kemiğin kompozisyonuna etki eder. Bunların herhangi birindeki eksiklik, kemiğin boyutunu veya yoğunluğunu, bazen de her ikisini birden etkiler (54). Doğumda insan vücudunda yaklaşık 25 gr kalsiyum bulunurken, erişkin kadınlarda bu değer 1000 gr kadardır. Bu farklılık diyetle oluşmuştur. Diğer yapısal besinlerden (protein gibi) farklı olarak tutulan kalsiyum miktarı her zaman alınandan daha azdır. Yetersiz kalsiyum alımı, kemiğin enine ve boyuna büyümesini kısıtlamaz. Ancak kalsiyumun yetersiz olması, daha ince korteks ve daha ince trabeküller ile sonuçlanır. Düşük kütleli iskelet oluşumu gerçekleşir. Şekli ve boyutu normaldir. Sigara kullanımı kemik üzerine toksik etkilidir. Sigara içenlerde barsaklardan kalsiyum absorbsiyonu azalmakta, sekonder hiperparatiroidi gelişmekte ve kemik rezorbsiyonu artmaktadır. Alkol tüketimi de kırık riskini arttırmaktadır. Aşırı alkol tüketimi ile kalsiyum emilimi azalır, atılımı ise artar. Alkol ile beslenme alışkanlığı da bozulmaktadır. Protein ve sodyum alımı azalır, protein kaybı artar. Ayrıca alkole bağlı endokrin değişiklikler sonucu testosteron azalması ve kortikosteroid artışı osteoporoz gelişimini kolaylaştırır (50).
C -Fiziksel aktivite: Egzersiz, erişkinlerde doruk kemik kütlesini mekanik yüklenme ile arttıran major etkendir. Büyüme sırasında yapılan farklı seviyedeki egzersizler, kemik gücündeki artıştan ziyade, uzun kemiklerin çaplarında ve kortikal kalınlıklarında farklılıklara yol açar. Egzersiz ile kortikal kalınlıkta %25 ile %30 oranında bir artış sağlanır, bu da azımsanmayacak bir değerdir. Kemikte yüklenme ne kadar çoksa, kemik birikimi de o kadar çok olur (50).
RiSK FAKTÖRLERİ
Bugüne kadar epidemiyolojik çalışmalarda osteporoz oluşumu için bilinen risk faktörleri listeler halinde bildirilmişse de bunların ne oranda osteoporoz yaptığına dair kesin ölçümler ve sonuçlar yoktur. Az çok hepsi deneyler sonucu bazı varsayımlara bağlıdır. Osteoporoz oluşumu için bilinen risk faktörlerini iki grupta toplamak mümkündür.
1-Genetik ,hayat tarzı ,beslenme 2-Hastalıklar ve ilaç kullanımı
Genetik-Hayat tarzı-Beslenme: (Tablo 3). Birçok araştırma genetiğin (47,50), etnik varyasyonların osteoporozdaki etkisini göstermektedir (55).
Düşük ağırlıklılar osteoporoz açısından belirgin bir risk taşımaktadırlar. Beslenmeyle ilgili faktörlerde osteoporozda önemli yer tutar. Günlük kalsiyum alınımı ortalama 1200 ile 1400 mg civarında olmalıdır. Postmenopozal dönemde alım 1500 mg/gün olmalıdır (56).
Yetersiz kalsiyum alınımı ile birlikte, kafein, protein, sodyum ve fosfat alınımı da çok önemlidir. Protein sentezi kemik formasyonu için gereklidir. Yüksek proteinle beslenenlerde idrarla kalsiyum atılımında artış görülür. Yüksek protein alımında böbrek fonksiyonları, kalsiyum absorpsiyonu, kemik mineralizasyonu, asit-baz dengesi ve insülin salgılanması değişiklikler gösterir. Sülfür içeren aminoasitli proteinler idrardan kalsiyum atılımını arttırır. Proteinler, renal tübüler kalsiyumun geri emilimini azaltıcı, glomerüler filtrasyonu arttırıcı etkileri ile birlikte asit tamponlanmasında iskelet kalsiyumunu kullanarak osteoporozu kolaylaştırıcı rol oynarlar (54).
Tablo 3. Osteoporoz için bilinen risk faktörleri
Genetik Hayat tarzı Beslenme
Beyaz ve Asyalı olmak Aile hikayesi
Düşük ağırlık
Sigara
İnaktivite, kronik immobilizasyon Nulliparite
Aşırı egzersiz (amenore) Erken menopoz
Geç menarş, puberte
Düşük kalsiyum alınımı Vejetaryan diyet
Aşırı alkol alımı
Fazla sodyum alımı idrarla kalsiyumun atılmına neden olur. Ayrıca mineralize dokunun kalitesini de etkiler. Aluminyum içeren antiasitler barsakta fosfatı bağlayarak idrarla kalsiyum kaybettirirler. Kafein de aynı şekilde etki gösterir. Sodyum, antiasitler ve kafein idrardan kalsiyum atılımını arttırarak negatif kalsiyum dengesine neden olurlar. Diğer minerallerin (çinko, bakır, manganez, magnezyum) eksikliğinde de kemik formasyonu bozulur. Günde 150 mg kafein (1 büyük bardak kahve) alınınca idrada 5 mg. kalsiyum atılmaktadır. Bu etkinin prostaglandin sentezini etkileyerek olduğu düşünülmektedir. Buna karşın çay içilince kemik kaybı olmadığı, aksine teofilin'in koruyucu etki göstermektedir. Sigara içince östrojen düzeyinin düştüğü, buna bağlı olarak menopoz yaşının öne geldiği, sigara içenlerin daha zayıf oluşları nedeniyle yağ dokularından östrojen yapımının daha az olduğu ve bütün bu nedenlerin kemik kütlesini azalttığı bilinmektedir. Sigara içenlerin yaşam süresi sigara içmeyenıerden daha az olduğuna göre yaşam boyu kırık oluşma ihtimali her iki grupta pek farklı olmayacağı düşünülebilirse de, 5 yıl yaşam süresi kısalsa dahi yaşa bağlı kırık riskinde 2 kat artma olmaktadır (57). Yine alkolde benzer şekilde kırık riskini artırmaktadır. Alkol osteoblastlar için oldukça toksik etki gösterir (58). Bununla birlikte hormonal düzeyde yaratığı değişiklikler (hipogo-nadizm), kalsiyum emiliminde azalma, atılımındaki artma, D vitamini metabolizma-sında bozulma, protein ve sodyum alımında azalma bilinen diğer etkilerindendir. Alkol kullanan kişilerde bilindiği üzere düşme riskide oldukça artmıştır (Tablo 4).
Tablo 4. Bazı Hastalıklar ve ilaç kullanımı
Hastalıklar Anoreksia Nervosa, Çölyak Hast., Tirotoksikosis, Hiperparatiroidism, Cushing’s Send., Tip I Diyabet, Osteogenesis imperfekta, Romatoid Artrit, Hemolitik Anemi send., Fenilketonuri, Endometriosis, Sarkoidoz, Hiperprolaktinemi, Akromegali, Turner Send.
İlaç kullanımı Tiroid Repl. Tedavisi, Glukokortikoidler, Lityum, Kemoterapi, GnRH agonistleri, Siklosporin, Heparin, Kumadin, Antikonvulsanlar.
Bilindiği üzere birçok hastalık ve uzun süreli ilaç kullanımı kadınlarda postmenopozal dönemdeki kırık riskini arttırmaktadır. Hipertiroidizm kalsiyum emilimini azaltan, atılımını arttıran ve kırık riskini bu yönleriyle arttırabilen bir
hastalıktır (59,60). Hipertiroidizm gibi hiperparatiroidizm’de kırık riskini artıran diğer bir hastalıktır (61). Tip I diyabette hastalığın çoçukluk döneminden beri süre gelmesi hastalığın kemik kütlesini uzun yıllar etkisi altında tutmasına neden olur. Bunların dışında anoreksia nervosa, çölyak hastalığı, kortikosteroid kullanımıda diğer önemli risk faktörlerindendir (62,63).
Osteoporozda Tanı Yöntemleri
Osteoporoz bir çok vakada sessiz bir hastalık olarak kalır. Hafif bir ağırlık kaldırma gibi günlük aktiviteler sırasında vertebra kırığı oluşunca veya düşme sonucu kalça kırığı gelişene kadar osteoporoz tanısı konulmayabilir. Osteoporozlu hastaların tanısı, tedavisi ve takibinde öykü ve fizik muayenin yanında kullanılan tanı yöntemleri şunlardır: A-Görüntüleme yöntemleri a-Radyografik incelemeler b-KMY ölçümleri c-Kemik sintigrafisi B-Laboratuar testleri C-Kemik biyopsisi A-Görüntüleme Yöntemleri:
a- Radyografik İncelemeler: Konvansiyonel radyografiler sık kullanılan ucuz yöntemlerdir. Torakal ve lumbosakral bölgelerin ön-arka ve yan, pelvisin ise ön-arka grafilerinin alınması gerekir. Radyografilerde osteoporoz tanısı için kullanılan kriterler; radyolusens (ışık geçirgenliği) artışı, trabeküler yapıdaki değişiklikler, kemik korteksinin incelmesi, vertebra korpusu, radius distali ve femur boynu kırıklarıdır. Ancak yumuşak doku görüntülerinin süperpozisyonu, ışığın sertliği ve film özelliklerinin değişkenliği gibi nedenler ile kemik yoğunluğunun değerlendirilmesinde hassasiyeti düşüktür (64).
b -KMY Ölçümleri : Kemik kaybı en az %30 oranına ulaşmadan radyolojik olarak osteoporoz tanısı koymak mümkün değildir. Kemik kaybının kırık riski olmadan önce saptanması önemlidir. Bu amaçla son 10 – 15 yılda KMY ölçüm yöntemleri geliştirilmiştir. Bu yöntemler ile kemik kütlesi, kemik kayıp hızı ve gelecekteki kırık riski tahmin edilebilmektedir (64).
KMY ölçümü için endikasyonlar:
- Premenopozal dönemde yüksek risk grubundaki kadınlar o Amenore veya hipermenore (yoğun spor aktiviteleri) o Anoreksia nevroza
- Postmenopozal dönemde aşağıdaki risk faktörlerinden iki veya daha fazlasına sahip olan kadınlar:
o Ailede osteoporoz tanısı
o Kısa boy, minyon tip (genelde 1,60 cm’den kısa, 50 kg altında) o 65 yaş üzerinde olmak
o Boyda 2,5 cm’den fazla kısalma
o Yaşam boyunca kalsiyumdan fakir besinler ile beslenmek o Minör travmalar ile çok sayıda kırık öyküsü
o Radyografilerde osteopeni saptanması
o Östrojen tedavisine intolerans veya kontraendikasyon o Aşırı derecede alkol, sigara ve kahve tüketimi
- Cerrahi menopoz
- Osteoporoz tedavisinin izlenmesinde (HT, kalsitonin, bifosfonat, anabolik steroid, D vitamini tedavilerinde)
- Dört haftanın üzerinde immobilizasyon
- Romatoid artrit veya ankilozan spondilit tanısıyla beş yıldan fazla süredir izlenen hastalar
- Kortikosteroid veya metotreksat tedavisi uygulanan hastalar - Beş yıldan fazla antikonvülzan kullanımı
- Osteomalazi
- Nefropatiler ve tubulopatiler - Hiperparatiroidi
- Tiroid replasman tedavisi on yıldan uzun süren hastalar
- Kemik kaybına neden olduğu bilinen diğer ilaçların kronik kullanımı (antiasit, heparin, lityum vs.)
- Kalsiyum eksikliği olduğu düşünülen bireyler o Renal taş veya kalsiüri
KMY Ölçüm Yöntemleri:
Tek Foton Absorpsiyometri (SPA) (Single Photon Absorptiometry) Çift Foton Absorpsiyometri (DPA) (Dual Photon Absorptiometry )
Tek Enerji X-ışını Absorpsiyometri (SEXA) (Single Energy X-ray Absorptiometry ) Çift Enerji X-ışını Absorpsiyometri (DEXA) (Dual Energy X-ray Absorptiometry) Kantitatif Bilgisayarlı Tomografi (QCT) (Quantitative Computed Tomography) Kantitatif Ultrasonografi (QUS) (Quantitative Ultrasonography)
Manyetik Rezonans (MRI) (Magnetic Resonance Imaging)
Tek Foton Absorpsiyometri (SPA) (Single Photon Absorptiometry): Foton olarak
izotop radyoaktif madde (örneğin İyot 125) kullanılır.Yalnız etrafındaki yumuşak dokusu az olan kemiklerin mineral içeriğini ölçmekte kullanıldığı için femur ve vertebrada doğru ölçüm yapamaması gibi dezavantajları vardır (65)
Çift Foton Absorpsiyometri (DPA) (Dual Photon Absorptiometry): SPA’dan farklı
olarak etrafında yumuşak dokusu olan kemiklerin yoğunluğunu da ölçer. Kortikal ve trabeküler kemik ayrımı yapılamaz (14,64)
Tek Enerji X-ışını Absorpsiyometri (SEXA) (Single Energy X-ray Absorptiometry):
Sadece apendiküler sistem, özellikle radius ve topuk kemik yoğunluğunun ölçülmesi için kullanılır. (45).
Çift Enerji X-ışını Absorpsiyometri (DEXA) (Dual Energy X-ray Absorptiometry):
Ölçüm için radyoizotop madde yerine X-ışınları kullanılır. Lomber vertebraları, kalça, ön kol ve tüm vücut değerlendirilebilir. Her vertebra tek tek incelenebilir. Genellikle L1-4 vertebralar seçilmektedir. Alınan radyasyon miktarı 2 mrad’ın altındadır. Süre çekilen bölgeye göre 5 – 15 dk arasında değişmektedir. Hata payı düşük, duyarlılık oranı yüksektir. Ölçümler gr/cm² olarak hesaplanır. DEXA ile kortikal ve trabeküler kemik ayrımı ve ölçümü yapılabilir.1993’de Hong Kong’da yapılan osteoporoz sempozyumunda alınan ortak bir karara göre DEXA KMY’nu belirlemede en iyi yöntem olarak kabul edilmiştir. KMY ölçümleri için T ve Z-skorları kullanılmıştır (14,64).
T-skoru: Hasta ve genç erişkin ortalama kemik yoğunluğu arasındaki standart sapma
Z-skoru: Hasta ve aynı yaş ve ağırlıktaki grupta kemik yoğunluğu arasındaki standart sapma
Kantitatif Bilgisayarlı Tomografi (QCT) (Quantitative Computed Tomography): Hem
aksiyal hemde apendiküler iskelette ölçüm yapabilir. Bu teknikte X-ışınları kullanılır. Trabeküler kemik, kortikal kemikten ayırt edilir. Vertebra cismindeki mineral içeriği spinal çıkıntılardan, osteofitlerden ve vertebra dışındaki kalsifikasyonlardan ayrı olarak saptanabilir. Radyasyon dozu DEXA’dan belirgin olarak daha fazladır (45,64).
Kantitatif Ultrasonografi (QUS) (Quantitative Ultrasonography): Radyasyonsuz bir
yöntemdir. Kemik yoğunluğunu göstermez fakat kemik yapısı hakkında bilgi verir (45,64).
Manyetik Rezonans (MRI) (Magnetic Resonance Imaging): Kemiklerin trabeküler
yapısını incelemede kullanılan, radyasyonsuz, fakat pahalı bir yöntemdir.
c-Kemik Sintigrafisi: Özellikle osteoporozun, kemik metastazları, osteomalazi gibi hastalıklardan ayırt edilmesinde kullanılır. Önceden oluşmuş krıkların gösterilmesinde de yeri vardır. Osteoporoz tanısında fazla spesifitesi olmayan bir yöntemdir.
B-Laboratuar Testleri:
Osteoporoz tanısı, tedavisi ve takibinde biyokimyasal testlerin önemli bir yeri vardır. Primer osteoporoz tanısını kesinleştirip sekonder osteoporoz olasılığını ekarte etmek için yapılması gereken laboratuar testleri aşağıdadır:
Rutin olarak yapılanlar: - Tam kan sayımı
- Eritrosit sedimentasyon hızı - Serum kalsiyum , fosfor.. - Total alkalen fosfataz - Karaciğer fonksiyon testleri - Tam idrar tetkiki
- Serum albumin, total protein Gerekli görüldüğünde yapılanlar:
- 24 saatlik idrarda kalsiyum ve sodyum düzeyi - Serum ve/veya idrar elektroforezi
- PTH, 1,25(OH) D vitamini - TSH, FT3, FT4
- LH, FSH, Prolaktin
- Plazma testesteron ve östradiol düzeyi - Serum kortizol düzeyi
- Bence-Jones proteini
- Kemik döngüsünün biyokimyasal belirteçleri (66): • Kemik yapımı göstergeleri serumda:
Total ve kemiğe spesifik alkalen fosfataz (TAP, BAP) Osteokalsin
Prokollajen Tip 1 karboksi terminal propeptidi (PICP) Prokollajen tip 1 aminoterminal propeptidi (PINP) • Kemik yıkımı göstergeleri:
• serumda:
Tartarat rezistan asit fosfataz (TRAP) Tip 1 kollajen telopeptid (ICTP) • İdrarda:
Hidroksiprolin
Pridinolin ve deoksipridinolin (PYD, DPD) Tip 1 kollajen telopeptid (INTP, NTX-1, CTX-1) Hidroksilizin glikozidleri
C-Kemik Biyopsisi:
Kemik biyopsisi metabolik kemik hastalıklarının tanısı ve araştırılması için önemli bir yöntemdir. Doku veya hücre düzeyinde incelemeye imkan tanıyan tek yöntemdir. Kemik biyopsisi ve histometrisinin klinik kullanımı şüpheli osteomalazi, sistemik mast hücresi hastalığı (mastositoz), renal osteodistrofi, tanısı koyulamamış osteoporoz, östrojen yetersizliği olmayan kadınlarda osteoporoz, klasik tedaviye yanıtsız osteoporoz ve tanısı konulamamış çocukluk çağı kemik hastalıkları ile sınırlıdır (64).
OSTEOPOROZ TEDAVİSİ
Osteoporoz tedavisinin amacı hastanın yakınmalarını gidermek ve yaşam kalitesini artırmak, kaybolan kemik kütlesini yerine koymaya çalışmak, komplikasyonları önlemek, geciktirmek ve oluşmuş komplikasyonları tedavi etmektir. Osteoporoz oluşumunda kemik yapım-yıkım dengesi bozulmuştur. Yıkım, yapımın önüne geçmiştir. Bu nedenle osteoporoz tedavisinde rezorpsiyonun önlenmesi daha öncelikli görünmektedir. National Osteoporosis Foundation (NOF); T-skoru -2 ve altında olan hastalara ve T-skoru -1,5 ile -2 arasında olup bir veya daha fazla risk
faktörü olan tüm kadınlara tedavi verilmesini tavsiye etmektedir (67,68). Kemik rezorpsiyonunu azaltan ilaçlar:
- Kalsiyum - Vitamin D metabolitleri - Östrojenler - Kalsitonin - Bifosfonatlar - Anabolik steroidler - Tibolon - İpiriflavon
- Selektif östrojen reseptör modülatörleri Kemik formasyonunu artıran ilaçlar. - Parathormon
- Anabolik steroidler - Floridler
Hormon Tedavisi (HT) :
Östrojenlerin kemik dokusuna olan etkileri tam olarak bilinmesede, osteoblastlar üzerinde etkili olabilecekleri ya da osteoblast oluşumunda etkili olan ve düzenleyici etkilere sahip IL-1 veya TNF-alfa gibi sitokinlere etki edebilecekleri düşünülmektedir (69). Östrojenlerin kalsitonin salgılanmasını artırarak veya lokal faktörleri etkileyerekte bu görevi yerine getirmesi mümkün gibi gözüküyor. HT halen osteoporoz’un önlem ve tedavisinde önemli bir yöntemdir. Yıllardan beri HT’nin kalça kırıklarının önlenmesindeki etkinliğine ait bir çok delil mevcuttur (70,71). 3140 perimenopozal ve postmenopozal kadının ortalama 2,5 yıl izlendiği bir çalışmada, hormon replasman tedavisinin uygulandığı kadınlarda, tedavinin uygulanmadığı kadınlara göre düzeltilmiş nispi kırık riskinin 0.75 olduğu hesaplanmıştır (72). Yine benzer şekilde omurga kırıklarında da etkili olduğuna dair araştırmalar mevcuttur (73).
Deri altına yerleştirilen östradiol implantları, kemik dokusu kaybını önleyebilmektedir. McKay Hart ve ark. (74), her 6 ayda bir 50 mg'lık östradiol implantı yerleştirilen, ooforektomi geçirmiş 19 kadını, 2 yıl boyunca izlemişlerdir. Bu uygulamayla lomber omurgada kemik mineral dansitesi, her yıl %4.3 oranında artmıştır. 3 yıl süreyle uygulanan aynı tedavinin, bilgisayarlı tomografiyle ölçülen
trabeküler kemik yoğunluğunu her yıl %3.3 oranında artırdığı da bildirilmiştir (75). İmplant tedavisiyle kemik dansitesinde sağlanan en fazla artış, tedavi sırasındaki östradiol düzeyleri en yüksek olan kadınlarda elde edilmektedir (76). Transdermal östrojen tedavisi de oral östrojen tedavisine benzer etkilere sahip gözükmektedir.
Riis ve ark (77) perkütan östrojen ve oral progesteron ile tedavi edilen postmenopozal kadınlardaki kemik mineral yoğunluğunun arttığını kanıtlamışlardır. Kardiyovasküler problemler halen postmenopozal dönemdeki kadınlarda en sık karşılaşılan hastalıklardan birisidir (78). Bu konu ile ilgili ilk çalışmalar HT’in kardiak fonksiyon üzerine pozitif etkilerini göstermiştir. Pines ve ark. (79) 12 aylık HT kullanımını takiben aortik akım parametrelerinde artışlar göstermiştir. Benzer sonuçlar transdermal östradiol ile de gösterilmiştir (80,81).
Yine, 4 ve 6 aylık HT tedavilerinin araştırılması sonucunda, HT’nin sol ventrikül fonksiyonunu düzeltiği dair kanıtlar bulunmuştur (82,83). Hipertansif hastalarda da benzer etki tespit edilmiştir (79,84). Light ve ark.’da (85) bu etkiyi randomize plasebo-kontrollü bir çalışmada göstermiştir. HT’nin HDL (yüksek-dansiteli lipoprotein), total kolesterol, trigliserit üzerine artırıcı, LDL (düşük-densiteli lipoprotein) üzerine düşürücü etkisi de bu bulguları destekler türdendir (86). Ancak ne var ki hormon replasmanının kardiyak fonksiyona hiçbir faydasının olmadığı sonucuna varan çalışmalar bu konudaki fikirlerimizde büyük bir şüphe uyandırmıştır. Transdermal ve oral östrojenin kullanıldığı 3 kısa çalışmada, kardiyak fonksiyona etki ile ilgili herhangi bir kanıt bulunamamıştır (79, 87).
Randomize, kontrollü bir çalışmada, Kessel ve ark. (88) postmenopozal sağlıklı kadınlarda 12 aylık düşük doz HT kullanımı sonrası herhangi bir kardiyak fonksiyon değişikliği tespit etmemiştir. HERS (Heart and Estrogen/Progestin Replacement Study) çalışmasının sonuçları da benzer bir şekilde HT’nin kardiyak fonksiyonlardaki etkisizliğini göstermiştir (40).
Tatjana ve ark.’da (89), 157 postmenopozal sağlıklı kadın üzerinde yaptıkları randomize çift-kör plasebo-kontrollü bir çalışmada konjuge östrojen’in sol ventriküler sistolik fonksiyonu üzerindeki etkilerini ortaya çıkarmışlardır. Sonuçta 2 yıllık kullanım sonrası dahi hiçbir grupta sol ventriküler sistolik fonksiyonu üzerine pozitif bir etki tespit edilmemiştir. Son olarak 16.608 postmenopozal kadında da bu etki gösterilmiştir. Konjuge östrojen (0.625 mg/g) ve beraberinde (2.5 mg/g) medroksi-progesteron asetat (MPA) kullanan grupta araştırma 8,5 yıl devam etmesi tasarlanırken 5. yılda ortaya çıkan yan etkiler nedeniyle durdurulmuştur. Halen