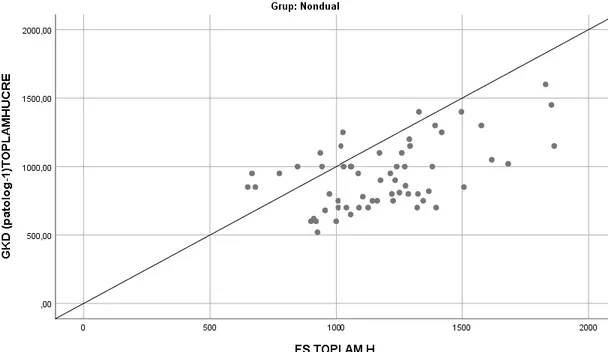
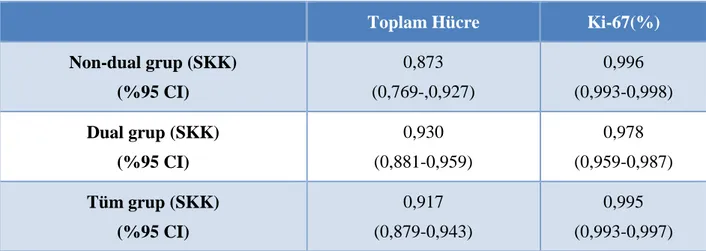
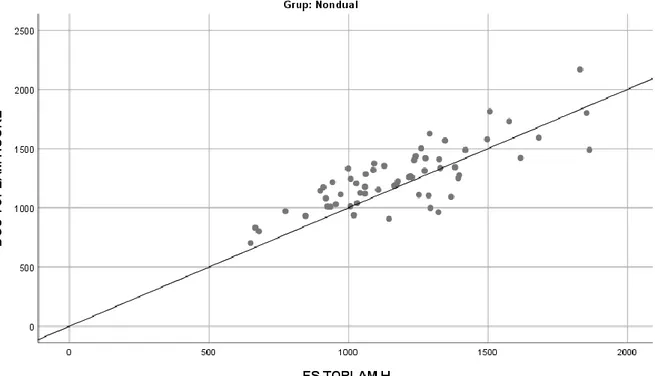
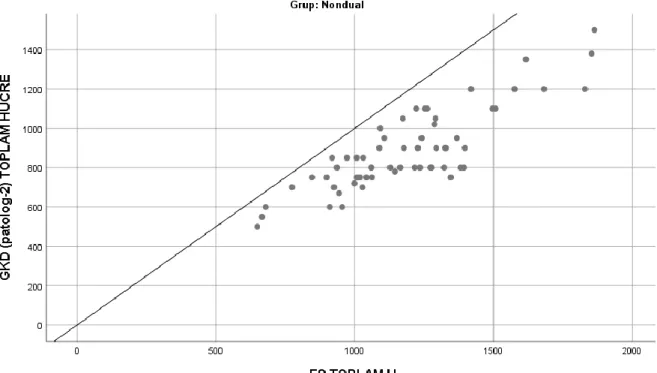
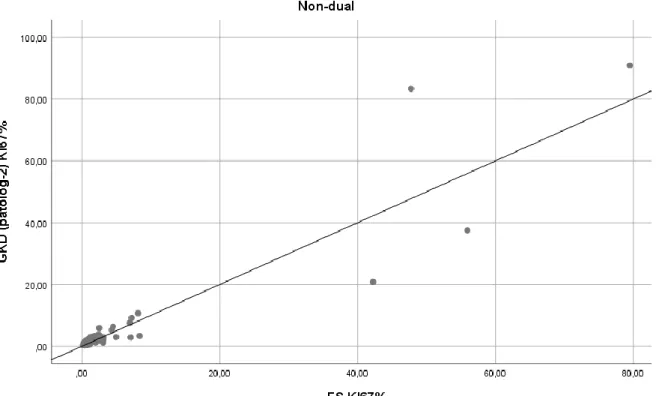
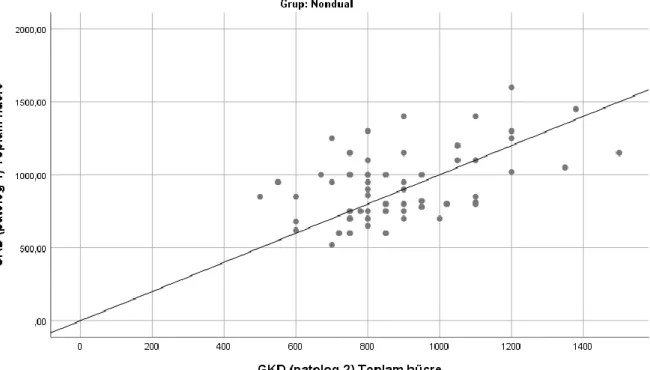
Gastrointestinal traktus nöroendokrin neoplazilerinde Ki-67 proliferasyon indeksinin hesaplanmasının optimizasyonu
Tam metin
Şekil
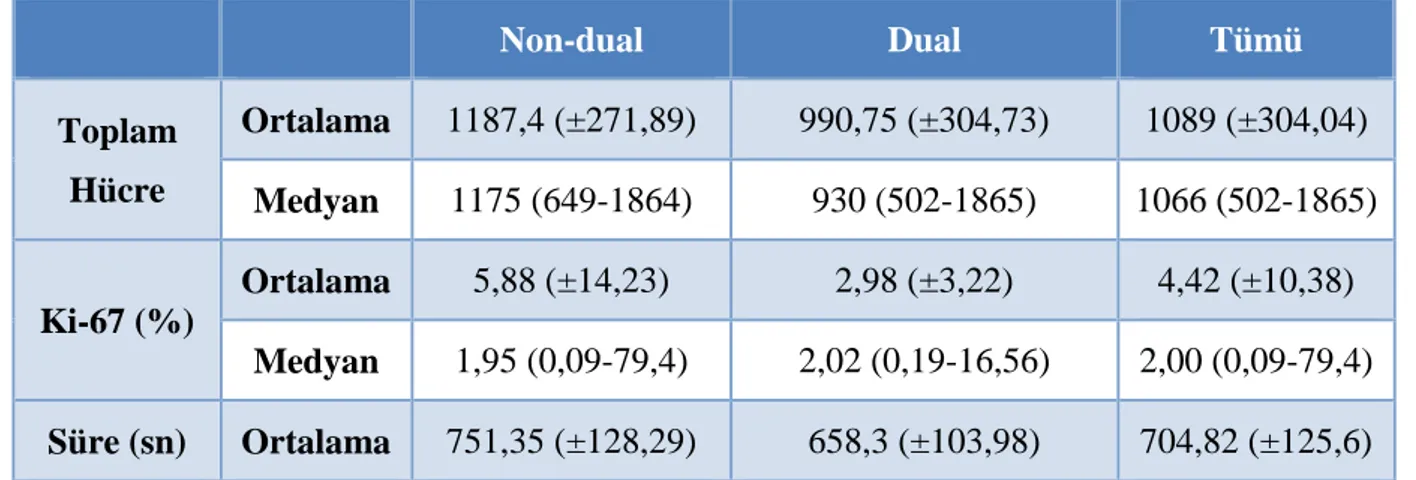
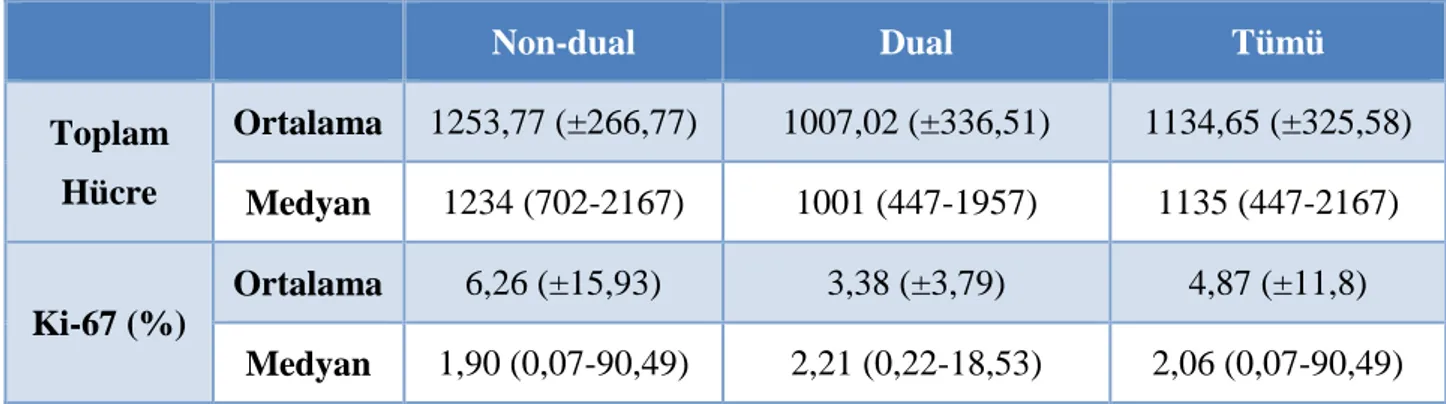
Benzer Belgeler
be 1.65 eV for the calix[4]acid/amine alternate layer LB film and a comparison of electrical properties of this LB film compared to LB films of other materials is given in Table
Ancak hüc- relerin, ›fl›klar söndürüldükten sonra bile bu ifllevlerini yerine getirebilmesi, akla baflka fleyler getiriyor: bafl-yönü hücreleri gibi, yer
Bu temel için, simpleks tabloda tüm temel dışı değişkenlere ilişkin tüm Z c 0 ise, problem için en iyilik koşulları (dual uygunluk) sağlanmıştır..
Altıncı bölümde, D , 3-boyutlu dual Lorentz uzayında aynı merkezli ve birbirine 1 3 göre hareket eden dual küre yüzeylerinin bir parametreli hareketi, kanonik
[9] birinci-mertebe kayma deformasyonlu sonlu eleman geliştirerek, bu elemanı simetrik ve asimetrik dizilişe sahip çapraz-tabakalı kompozit kirişlerde serbest titreşim ve
As easily seen, a bent function obtained by the construction described in Proposi- tion 1 is weakly regular if and only if all near-bent functions used as building blocks are
Later in this chapter, the duality between statics and kinematics especially for robotic manipulators will be discussed; while fundamentals of screw theory
Throughout the history of English language teaching, various approaches or methods adopted different views concerning the role of pronunciation in language instruction,