I
EGE ÜNİVERSİTESİ BİLİMSEL ARAŞTIRMA PROJE KESİN RAPORU
EGE UNVERSITY SCIENTIFIC RESEARCH PROJECT REPORT
PROJE NO: 2013-TIP-081
POLİKİSTİK OVER SENDROMU TANILI
HASTALARDA BETA-3 ADRENORESEPTÖR GENİNDE Trp64Arg GEN POLİMORFİZMİNİN ARAŞTIRILMASI
PROJE YÖNETİCİSİ PROF. DR. NİYAZİ AŞKAR
ARAŞTIRMACI DR. ŞAHLA VELiZADE
PROF.DR.HİKMET HAKAN AYDIN DOÇ.DR.HANDAN ÇELİK
YRD.DOÇ.DR.AHMET METE ERGENOĞLU YRD. DOÇ.DR.AHMET ÖZGÜR YENİEL
OP.DR.ALİ AKDEMİR
UZMANLIK TEZİ T.C.
EGE ÜNİVERSİTESİ TIP FAKÜLTESİ
KADIN HASTALIKLARI ve DOĞUM ANABİLİM DALI Faculty of Medicine
Department of Obstetrics and Gynecology
II
Ege Üniversitesi Rektörlüğü Bilimsel Araştırma Projeleri Komisyonuna ve Ege Üniversitesi Tıp Fakültesi Bilimsel Araştırma Projeleri Alt Komisyonuna projemize verdikleri destek nedeniyle teşekkür ederiz.
III İÇİNDEKİLER
TABLOLAR VE ŞEKİLLER LİSTESİ………..IV KISALTMALAR...………...VI ÖZET……….VIII GİRİŞ ... 1 1. GENEL BİLGİLER ... 1 1.1 TANIM ... 1 1.2 TARIHCE ... 1 1.3 ETYOPATOGENEZ ... 5 1.4 KLİNİK BULGULAR ... 9 1.5 LABORATUVAR BULGULARI ... 18
1.6 PKOS VE UZUN DÖNEM ETKİLERİ ... 19
1.7 PKOS’UN TANISI ... 23 1.8 PKOS’ UN TEDAVİSİ ... 26 1.9 β3-AR’ler ... 29 2. MATERYAL VE METOD ... 34 3. BULGULAR ... 40 4. TARTIŞMA ... 43 5. SONUÇ ... 46 6. KAYNAKLAR ... 47
IV TABLOLAR VE ŞEKİLLER LİSTESİ
TABLOLAR
Tablo 1: Polikistik over sendromu tanı kriterleri ... 2
Tablo 2: 2003 Rotterdam tanı kriterleri ... 3
Tablo 3: PKOS ile ayırıcı tanıya giren hastalıklar ... 4
Tablo 4: TaqMan® SNP Genotyping Assays listesi ... 35
Tablo 5: TaqMan® SNP assay PCR reaksiyon karışımının hazırlanması ... 37
Tablo 6: Real-Time PCR için uygulanan termal döngü protokolü ... 38
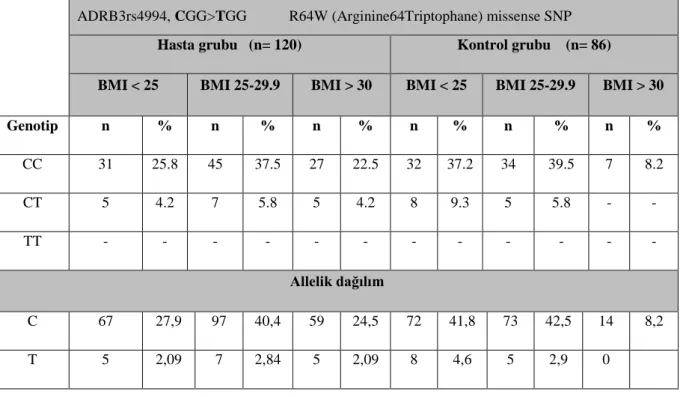
Tablo 7: ADRB3C>T (rs4994) polimorfizmi allel ve genotiplerinin control grubu ve hasta grubundakı dağılımı ... 40
Tablo 8: ADRB3C>T (rs4994) polimorfizmi allel ve genotiplerinin kontrol grubu ve hasta grubunda BMI ne göre dağılımı ... 41
V ŞEKİLLER
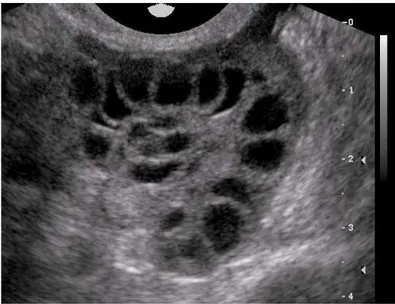
Şekil 1: Polikistik over ultrasound görüntüsü ... 3
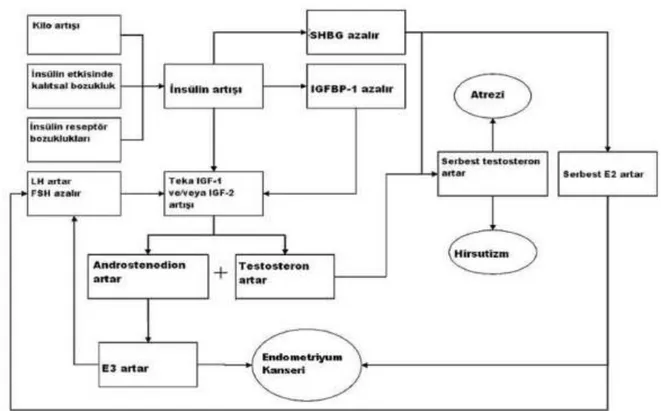
Şekil 2: PKO’da insülin/IGF1-2 etkisi ... 8
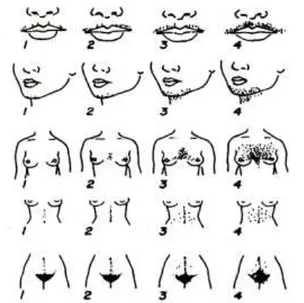
Şekil 3:Ferriman-Gallwey skorlama skalası ... 11
Şekil 4: Beta adrenoreseptörlerin şematik görüntüsü ... 30
Şekil 5: 5’Nuclease assay süreci ... 35
Şekil 6: TaqMan SNP Genotyping Assays prosedürünün kısa özeti. ... 36
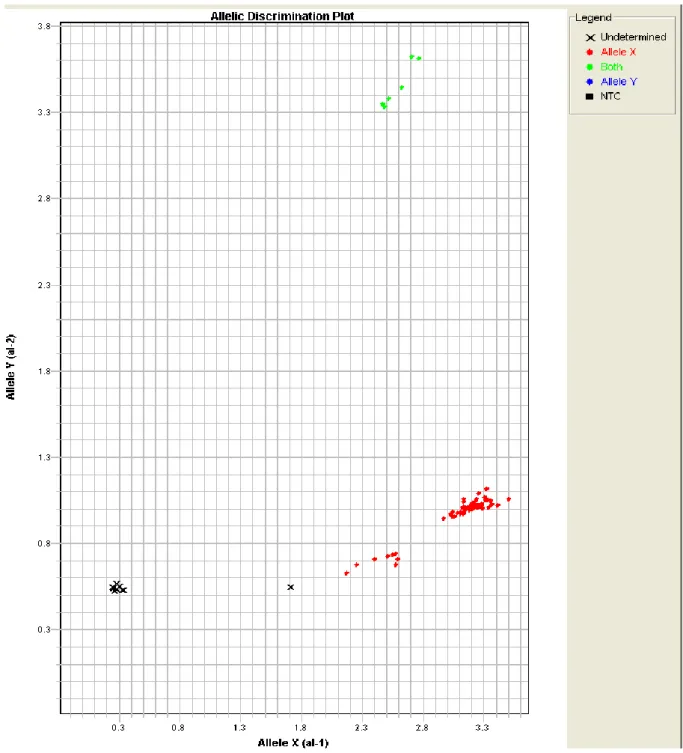
Şekil 7: Allelik diskriminasyon haritası ... 39
Şekil 8:Hasta ve konrol grububndaki genotipik dağılım oranları ... 41
Şekil 9: ADRB3C>T (rs4994) polimorfizmi allel ve genotiplerinin kontrol grubu ve hasta grubunda BMI ne göre dağılımının grafik görünümü. ... 42
VI KISALTMALAR
ACTH : Adrenokortikotropik hormon ADA : Amerikan Develt Enstitüsü ADRB3 : Beta 3 Adrenoreseptor AF : Antra folikül
AMH : Antimülleryan hormon Arg : Arginin
BGT : Bozulmuş glukoz toleransı CRH : Kortikotropin salgılatıcı hormon DHEA : Dihidroepiandrostenedion DHEAS : Dihidroepiandrostenedion sülfat DHT : Dihidrotestosteron
DM : Diabetes mellitus E2 : Östradiol
E3 : Östron
FGIR : Açlık glukoz/insulin oranı FGS : Ferriman-Gallwey skorlaması FSH : Folikül stimüle edici hormon GnRH : Gonodotropin salgılatıcı hormon
HAIR-AN : Hiperandrojenizm - insülin rezistansı - akantozis nigrikans HDL : Yüksek dansiteli lipoprotein
HT : Hipertansiyon İD : İsnülin direnci
VII
IGFBP-1 : İnsülin benzeri büyüme faktörü bağlayıcı protein-1 KAH : Konjenital adrenal hiperplazi
LDL : Düşük dansiteli lipoprotein LH : Luteinize hormon
NIDDM : İnsüline bağımlı olmayan diabetes mellitus PAI-1 : Plazminojen aktivatör inhibitörü-1
PKO : Polikistik over
PKOS : Polikistik over sendromu PRL : Prolaktin
SHBG : Seks hormon bağlayıcı globulin Trp : Triptofan
TSH : Tiroid uyarıcı hormon USG : Ultrasonografi
VIII
Polikistik over sendromu tanili hastalarda beta-3 adrenoreseptör
geninde Trp64Arg gen polimorfizminin araştırılması
ÖZET.
Amaç: Polikistik over sendromlu hastalarda beta-3 adrenoreseptörlerde Trp64Arg gen polimorfizmi ile ilişkinin saptanması.
Yöntem: Klinik, ultrasonografik ve laboratuvar değerlere bakılarak Rotterdam kriterlerine uygun polikistik over sendromu tanısı konulan 120 hastadan ve poliklinik müraacatı olan 87 sağlıklı bayandan alınan kan örneklerinde TaqMan® SNP Yöntemi İle ADRB3 rs4994 Polimorfizmi tespit edildi.
Bulgular:Yaptığımız arastırma sonucunda, PCOS olgularında ADRB3 Trp64Arg polimorfizmi taşıyıcılarının yaygınlığı PCOS’da %14,2 ve kontrol grubunda % 15,2 tespit edimiştir.
Hasta ve sağlıklı kontrollerde C ve T allellerinin dağılımı ve genotipik dağılım çıkarıldıktan sonra gruplar arası farklılık olup olmadığı χ2 testi ile analiz edilerek Odd ratio ve güvenilirlik aralıkları hesaplanmıştır. Anlamlılık için p < 0.05 kabul edilmiştir.
PCOS hastalarına göz attığımızda bu hastaların % 26.6’sı BMI’si 30 kg/m2’ den yüksek hastalar oluştururken, % 43.3’ı 25-30 kg/m2
arasında saptanmıştır. Polimorfizmin normal kilolu hastalarda %4,2, fazla kilolu hastalarda %5,8 ve obez PCOS’lu hastalarda ise %4,2 tespit edilmiştir.
Yapılan istatistiksel değerlendirmelerde; Hasta grubu ile kontrol grubu arasında ADRB3 Trp64Arg polimorfizmi sıklığı açısından istatistiksel olarak anlamlı bir fark bulunmamıştır. Tartışma ve sonuç: ADRB3C>T (rs4994) polimorfizmi allel ve genotiplerinin control grubu ve hasta grubundaki dağılımına dikkat ettiğimizde hasta grubu ile kontrol grubu arasında ADRB3 Trp64Arg polimorfizmi sıklığı açısından istatistiksel olarak anlamlı bir fark bulunmamıştır.
Ayrıca, hasta ve kontrol grubundan olan hastalar arasında ADRB3 gen polimorfizminin BMI’ne göre dağılımı da değerlendirildi. ADRB3C>T (rs4994) polimorfizmi allel ve genotiplerinin hasta grubunda BMI’ne göre dağılımı degerlendirildiğinde, normal kilolu, fazla kilolu ve obez hasta grupları açısından anlamlı bir fark olmadığı ortaya konulmuştur (sırasıyla %4,2, %5,8 ve %4,2).
Elde edilen sonuçlarla, ADRB3C>T (rs4994) polimorfizminin PCOS olgularının etiyolojisinde genetik belirteç olmadığı kanaatine varılmıştır.
Anahtar sözcükler: PCOS, ADRB3 Trp64Arg polimorfizmi (ADRB3C>T (rs4994) polimorfizmi).
IX
Trp64Arg polymorphism of the 3 adrenergic receptor (ADRB3) in women
with polycystic ovary syndrome (PCOS).
SUMMARY.
Objective: To establish the frequency of the Trp64Arg polymorphism of the 3 adrenergic
receptor (ADRB3) in women with polycystic ovary syndrome (PCOS).
Material and method: In a case–control design study, a total of 120 women with clinical and hormonal evidence of PCOS and 87 healthy women , attending the Depatment of Obstetrics and Gynecology , Ege University were evaluated. Diagnosis of PCOS was made according to the Rotterdam criteria for PCOS. The ADRB3 rs4994 Polimorfism was determined by TaqMan® SNP method.
Results: The frequency of the heterozygous condition was similar between PCOS and Healthy Women (14,2% vs. 15,2%).
After the detecting distribution of C and T allele and genotype distribution, the differences between PCOS and healthy control groups were analyzed by χ2 test. Odds ratio and confidence intervals were calculated.The significance level was set at p < 0.05.
There were 26,6% obese and 43,3 % overweight subjects In PCOS group.When data were stratified by BMI categories, the statistical test for interaction between Trp64Arg carrier status and obesity was not significant between normal weight, overweight and obese subjects (4,2 %, 5,8 % and 4,2%, respectively)
The frequency of the Trp64Arg polymorphism was similar in healthy women and PCOS women, and a possible interaction between the effect of this variant and obesity in PCOS could not be demonstrated.
Conclusion: We found a similar frequency of this polymorphism in healthy and PCOS women, and a possible interaction between the effect of this variant and obesity in PCOS could not be demonstrated. In the HW group, no differences were observed in BMI between Trp64Arg carriers and noncarriers . The same tendency was observed in the PCOS group. With obtained results, ADRB3C> T (rs4994) polymorphism cannot be used as genetic marker in the etiology of PCOS patients.
1 GİRİŞ
1. GENEL BİLGİLER
1.1 TANIM
PKOS, değişik derecelerde adet düzensizliği (oligomenore, amenore), hirsutizm, akne ve obezite ile seyreden, ilk belirtileri erken ergenlik çağında ortaya çıkan bir sendrom’dur. Polikistik over sendromu kısaca santral sinir sistemi, hipofiz, overler, adrenal bezler ve ekstraglanduler dokular arasındaki ilişkinin bozulmasıyla; üreme çağının herhangi bir döneminde ortaya çıkan, kronik seyirli ve yaşam kalitesini olumsuz etkileyebilen kompleks bir hastalık olarak tanımlanabilir (1).
1.2 TARIHCE
PKOS; üreme çağındaki kadınlarda en sık görülen endokrin bozukluktur. Prevalansı baz alınan tanı kriterlerine göre değişir fakat, genel olarak %6-8 civarındadır. Bu hastaların %50- 65'inde obezite, %35-45'inde insülin direnci ve %7-10'unda insülinden bağımsız diabetes mellitus saptanır.
İlk kez 1935 te Irving F. Stein ve Michael Leventhal kadınlarda anovulasyon ile ilişkili bir sendrom olarak tanımlamışlardır. Bu sendrom; dördü obez, amenoreik, hirsutik ve büyük polikistik görünümde overleri olan yedi kadın üzerinde tanımlanmıştır. Hastalarda overler normalden büyük ve tunika tabakasının daha kalın olduğu gözlemlenmiş ve bu tablo Stein-Leventhal Sendromu adlandırılmıştır. Over dokularının ½ - ¾’ü kadarlık kısmına kama rezeksiyon yapıldıktan sonra, tümünde menstruel siklusun normale döndüğünü ve hastaların ikisinde de gebelik sağlandığını belirtmişlerdir (2). 1958’de McArthur, Ingersoll ve Worchester bu tanımlanan hasta grubunda idrar LH düzeyinin normalden yüksek olduğunu saptamışlar. Yen; 1980’de polikistik over (PKO) olan hastalarda serum LH/FSH oranının LH
2
lehine bozulması ilk kez 1980’li yıllarda tanıda yer almıştır. USG’de ‘polikistik over görünümü’ ilk kez 1981’de Saurberi ve Cooperberg tarafından tariflenmiştir.(3). Günümüzde Ultrasonografide (USG) polikistik over görünümünün olması tanı koymak için yeterli değildir. Bugün PKOS’un iki tanımı genel kabul görmektedir. Polikistik over sendromu tanı kriterleri Tablo 1’de verilmiştir.
Tablo 1: Polikistik over sendromu tanı kriterleri
İlki 1990 yılında U.S National Institues of Health (NIH)’e bağlı National Institues of Child Health Human Disease (NICHD) konsensusunda kararlaştırılmıştır. Diğer tanım ise 2003 yılında Roterdam kentinde toplanan Europan Society for Human Reproduction and Embryology (ESHRE) ve American Society for Reproductive Medicine (ASRM) tarafından yapılmıştır. 2003 Rotterdam yeniden gözden geçirilmiş tanı kriterleri Tablo 2’de gösterilmiştir.
3 Tablo 2: 2003 Rotterdam tanı kriterleri
2003 Rotterdam yeniden gözden geçirilmiş tanı kriterleri* 1. Oligo-anovülasyon
2. Klinik ve/veya biyokimyasal hiperandrojenizm bulguları 3. Polikistik overler ve diğer etyolojik nedenlerin ekarte edilmesi *Tanı için üç kriterden ikisinin bulunması gerekmektedir.(4)
Son olarak 2006 yılında Androgen Excess Society tarafından yeni bir düzenleme önerilmiş ve hiperandrojenizm olmadan polikistik over görünümünün olması ile oligo-amenore varlığı tanısal kabul edilmemiştir.
Androgen Excess Society tanı kriterleri
1. Hiperandrojenizm (hirsutizm ve/veya hiperandrojenemi)
2. Over disfonksiyonu (oligo-anovulasyon ve/veya polikistik over) (5)
USG ile stroma dokusunun artması nedeniyle büyümüş overler ve inci kolye tarzında periferik yerlesimli 2-8 mm boyutlarında 10’un üzerinde folikül görünümünü PCO olarak ifade edilmektedir (4). Polikistik over ultrasound görüntüsü Şekil 1’de gösterilmiştir.
4
PKOS' un tanısını koymak için USG bulguları ile birlikte bazı klinik (Oligomenore/amenore, obezite, hiperandrojenizm, akne, hirsutizm, alopesi) ve biyokimyasal belirteçlerinde (Serum total testosteron veya serbest testosteron, LH, insülin düzeylerinin artması gibi) de bulunması gereklidir (4).
Anovulatuar kadınlarda PKO sıklığı %75’tir. Normal kadınların da %8-25’inde PKO görüntüsüne rastlanabilmektedir (6).
PKOS tanısı koyabilmek için benzer kliniğe neden olabilecek hastalıkların ekarte edilmesi gerekir. Tablo 3’de PKOS ile ayırıcı tanıya giren hastalıklar gösterilmiştir.
Tablo 3: PKOS ile ayırıcı tanıya giren hastalıklar
-Androjen salgılayan tümörler -Ekzojen androjen alımı -Cushing Sendromu
-Nonklasik konjenital adrenal hiperplazi -Akromegali
-Primer hipotalamik amenore -Primer ovaryen yetmezlik -Tiroid patolojileri
-Hiperprolaktinemi durumları -Hipertekozis
Polikistik over sendrom ayırıcı tanısı yapılırken; androjen yüksekliği ve anovulasyon ile birlikte olan klinik durumlar, androjen salgılayan tümörler, Cushing sendromu, konjenital adrenal hiperplazi, hiperprolaktinemi mutlaka göz önünde bulundurulmalıdır.
5
Dehidroepiandrostenodion sülfat ve DHEA düzeyleri androjen salgılayan tümörlerde birhayli yükselmektedir. Konjenital adrenal hiperplazi ile ayırıcı tanı periferik kanda 17- hidroksi progesteron (17-OHP) düzeylerinin yüksekliğinin gösterilmesiyle yapılabilir.
Hiperprolaktinemi, GnRH pulsasyonlarını değiştirerek gonadotropin salınımını etkiler. Östrojenin LH üzerine olan pozitif "feedback" etkisini engeller, adrenal kaynaklı androjenlerin salınmasını tetikler. PCOS ile ayırıcı tanıda PRL düzeyleri de önemlidir. PCOS’da %3-12 oranında orta düzeyde PRL yüksekliği görülür. Cushing sendromu, devamlı olarak kortizol sekresyonu fazlalığıdır. Tanıda bazal şartlarda en faydalı ölçümler 24 saatlik idrarda kortizol miktarı (10-90 μg/24 saat) ve gece plazma kortizol düzeyidir (< 15 μg/dL) (7)
1.3 ETYOPATOGENEZ
Menstrüasyondan hemen önce ve menstrüasyon sırasında östrojen, progesteron ve inhibin’in negatif "feedback" etkisi ortadan kalkar ve böylece hipofizden FSH sekresyonu artar. Bu artış folliküler gelişim ve steroidogenez için gereklidir. Follikülün gelişmesi ile follikül içerisinde oluşan otokrin-parakrin faktörler FSH’ya olan folliküler duyarlılığı devam ettirir. Bu da folliküler mikroçevredeki androjenik üstünlüğün östrojenik üstünlüğe dönüştürülmesini sağlar. FSH ve aktivinin birlikte etki göstermesi, ovulasyon ve luteinizasyon için gerekli olan, granuloza hücreleri üzerinde LH reseptörlerinin ortaya çıkmasını sağlar. Dolaşımdaki östradiol (E2) seviyesinin ani artışı ovulasyonu tetikler. Hipofiz ön lobu ve muhtemelen de hipotalamus üzerinde oluşturulan bir pozitif "feedback" etki ile de, siklus ortasında LH salınımı, yumurtanın ekspulsiyonu ve korpus luteumun oluşması sağlanır. Ovulasyonla birlikte E2 düzeylerinde ikinci bir artış ve progesteron artışı ile beraber düşük LH ve FSH düzeyleri ile karakterize olan 14 günlük luteal faz oluşturulur. Korpus luteumun fonksiyonunu kaybetmesi ile hormon düzeyleri düşer, FSH yükselmeye başlar ve yeni bir siklus oluşur (7).
6
PKOS’ ta etyoloji kesin olarak bilinmemekle birlikte sendrom genetik ve çevresel faktörlerin etkileşimiyle ortaya çıkmış sık görülen ve kompleks bir problem olarak değerlendirilebilir. Sendromun fizyopatalojisinde gonadotropin dinamiğinde değisiklikler, steroidogenez defektleri, insülin salınım ve etki bozuklukları beraberinde genetik faktörler ön plana çıkmaktadır.
a.Gonadotropin sekresyon defektleri: PKOS’”ta hipotalamus-hipofiz-over aksının
fonksiyonunda bozukluklar tanımlanmıştır. Gonadotropin Releasing Hormon(GnRH) puls sıklığının artışı, GnRH’ya yanıt artışı ve yüksek östrojen düzeylerinin neden olduğu serum LH konsantrasyonu artışı izlenmektedir.(8). LH’nın aksine hipofizer FSH sekresyonu erken foliküler fazda belirgin düşük olarak tesbit edilmektedir(9). Düsük FSH düzeyinin nedeni tam olarak anlaşılamamakla beraber kronik karşılanmamış östrojenin negatif geri-denetim etkisi ile, artmış GnRH pulsatilitesinin LH β gen ekspresyonunu FSH β gen ekspresyonuna göre daha fazla arttırması patogenezde rol aldığı düşünülen iki mekanizmadır (10).
b.Steroidogenez değisiklikleri: Yükselmiş LH düzeyi overlerde siklik adenozin monofosfat
(cAMP) artışı ile steroidogenezi androjenlerin üretimi yönünde etkiler ki bu da folikül gelişiminde duraklama ile sonuçlanmaktadır (11). Artmış LH düzeylerine cevap olarak androjen salgısı hızlanmaktadır. Yükselmiş androjen düzeyleri, ekstraglandüler olarak androjen-östrojen dönüşümünü arttırırken, seks hormon bağlayıcı globulin (SHBG) sentezini baskılamakta, sonuçta östrojen düzeylerinde yükselmeye neden olmaktadır. Buna ilaveten SHBG’deki azalma, serbest testosteron miktarında iki katlık bir artışa neden olmaktadır.
Artmış androjenler, over içerisinde normal follikül gelişmesinin engellenmesine katkıda bulunmakta ve prematür atreziyi uyarmaktadır. Lokal androjen bloğu, sürekli anovulasyonun devam etmesinin ana nedenlerinden biridir. Overdeki androjen
7
konsantrasyonları yüksek olduğunda bunlar, aromataz aktivitesini ve östrojen sentezini inhibe eden 5-alfa metabolitlerine dönüşmektedir.
Normalde oluşan, bir siklusun bitmesinden sonra yeni bir siklusun başlaması olayını oluşmaması sonucunda sabit bir hormonal durum ortaya çıkmakta, bu da artmış androjen sentezine bağlanabilecek sürekli bir anovulasyona neden olmaktadır (7).
c. Genetik faktörler: PKOS hastalarında genetik özellikler de araştırılmıştır (24). PKOS’lu
kızların annelerinde ve kız kardeslerinde hiperandrojenizm ve menstrüel disfonksiyonun artmakla birlikte, baba ve erkek kardeşlerde de serum androjen düzeyleri artmış gibi görünmektedir (25). Bu hastaların birinci derece yakınlarda insülin direnci ve değişik derecelerde glukoz hemostaz bozukluklarının görülme riski, yaş ve vücut kitle indeksi (VKİ) artmıştır (25). PKOS gelisiminde rol oynayabilecek olası genetik defektlerin incelendiği değisik çalısmalar sendromun kompleks, poligenik bir bozukluk olduğunu göstermektedir.
d.İnsülin salınım bozuklukları: İnsülin anabolik etkili bir hormon olup başlıca etkileri
hücreye glukoz ve aminoasit girişini, lipojenez ve mitojenezi arttırmaktır. İnsülin etkilerini insülin reseptörleri aracılığıyla yapar. İnsülin benzeri büyüme faktörü (IGF-1) büyüme hormonu etkilerinde bir ara madde olarak keşfedilmiştir. Bu gün için büyüme hormonun birçok dokuda etkilerini IGF-1 aracılığı ile yaptığı kabul edilmektedir. IGF-1 karaciğerde üretilen ve 12. kromozom tarafından kodlanan 70 aminoasitli bir polipeptiddir. Kanda insülin benzeri büyüme faktörü bağlayan protein-1 (IGFBP-1) ile taşınır. IGF-1 ve IGF-2’nin reseptörleri farklıdır. IGF-1 resptörleri insülin reseptörleri ile benzerlik gösterir. Pek çok hücrede DNA sentezini arttırarak mitojenik etki yapar. IGF-2 ise embriyonik ve fetal gelişim üzerine etkilidir (15, 16) Erken folliküler dönem gonadotropinlerden bağımsızdır ve bu dönemde lokal büyüme faktörleri gereklidir. Özellikle IGF-1’in bu dönemde etkili olduğuna
8
dair pek çok çalışma vardır. IGF-1’in inaktivasyonu ile follikül gelişiminin preantral dönemde durduğu gösterilmiştir(17). PCOS’ da birçok alanda IGF-1 artmıştır. Bu artış LH ve FSH’ya over cevabını arttırır. Buna bağlı olarakta gelişen follikül sayısı artar, fakat bunu atrezi izler.
PCOS’da IGFBP-1’in azalması da IGF-1’in etkilerini arttırır. IGF-1 ve insülin androjen üretimini arttırır. IGF-1’in insülin ile benzer etkisi granüloza hücrelerinde aromataz aktivitesini arttırır (18). Şekil 2’de PKO’da insülin/IGF1-2 etkisi gösterilmiştir.
Şekil 2: PKO’da insülin/IGF1-2 etkisi
İnsülin direnci (İD), belli bir glukoz düzeyi için gereken insülin yanıtının olmamasıdır. PCOS’lu vakaların yaklaşık %10’unda ID saptanmıştır. Bu hastalarda İD’nin patofizyolojisi henüz tam olarak bilinmemektedir (19).
Hem zayıf hem de obez PKOS hastalarında İnsülin direnci ve kompanzatuar hiperinsülinemi sık görülen bir bulgudur (20). İlk kez 1980 yılında Burghen ve ark. (21) tarafından obez PKOS’lu hastalarda hiperandrojenizm ve hiperinsülineminin pozitif lineer korelasyonu bulunmuştur. Sendromda insülin etki anormalliklerinin mekanizması net olarak
9
bilinmemektedir. Ne obezite ne de tek basına androjen fazlalığı PKOS’ da görülen insülin etki bozukluğunu açıklamamaktadır (22).
İD ölçümü PKOS tanı kriteleri arasında yer almaz (23).
Sonuç olarak patofizyolojiyi anlamamızı kolaylastıran bu alt gruplar aslında birbiriyle iç içedir. Bazı olgularda ailesel bir yatkınlık genetik bağlantıyı düsündürmekle beraber aday genler hala bulunamamıştır.
1.4 KLİNİK BULGULAR
PKOS ile ilgili pek çok farklı görüş vardır. Klinisyenlerin çoğu PKOS’u gördüklerinde kesin olarak tanımlayabildikleri konusunda hemfikirdirler. Semptomlar menarşla başlamaktadır, ancak hastalığın klinik gidişi birçok farklı faktörlerden etkilenmektedir. Erken yaşlarda daha çok mestrüel düzensizlikler görülmekte iken, daha ileri yaşlarda ise hirsutizm ve infertilite ön plana çıkmaktadır.
Orta ve ileri derecede PKO’leri olan bazı vakalarda ovaryan disfonksiyona sebep olacak kadar adipoz doku birikinceye kadar semptom görülmeyebilir (26). PKOS’li olguların %20’de adetlerin düzenli olabileceği de bildirilmiştir (27). Kronik oligo-amenore kriteri olarak menseslerin arasında 45 günden fazla olması veya yılda sekiz veya daha az menses görme, hiperandrojenizm kriteri olarak ise klinik hirsutizm varlığı (akne, hirsutizm, androgenik alopesi, akanthosis nigricans) veya laboratuvar bulgusu olarak androgenlerin yüksekliği (serum total ve serbest testosteron düzeylerinde artış) kullanılmaktadır (28).
PKOS’de anahtar bulgu, anovulasyon olup, olguların % 50‘sinde amenore , % 30’unda ise düzensiz siddetli kanama seklinde kendini göstermektedir. Anovulatuar hastaların %70‘inde hirsutizm mevcuttur. Gerçek virilizasyon nadir görülür. Olgularda obezite varlığının çok değiskenlik gösterir ve tanısal değeri bulunmamıştır. Bununla birlikte VKİ arttıkça, T düzeyi de arttığından asırı kilolu anovulatuar kadınlarda hirsutizm daha sıktır. Alopesi ve akneye de hiperandrojenizm neden olmaktadır.
10 1.4.1. Kronik Anovulasyon
Kronik anovulasyonun klinik görüntüsü, irregüler menstrüel siklus, oligomenore ve ya amenore şeklindedir. PKOS’da menstrual disfonksiyon genellikle menars ile baslar. Şiddetli oligomenore durumlarında endometrial hiperplazi ve ardından gelişebilecek neoplastik değişiklik riski mevcuttur. Ultrasonografi ile endometrial kalınlık ölçülerek takip takip edilebilse de bu yöntem malign değisim için risk altındaki kadınların belirlenmesinde hassas etkili olup olmadığı tartışmalıdır. PCOS’lu ve şiddetli oligomenoresi olan kadınlarda, düzenli bir çekilme kanaması sağlamak gerekir. Kronik anovulasyonlu PCOS’da anormal follikülogenezis söz konusudur. Bu hastalarda infertilite şikâyeti mevcuttur. Nadiren, spontan gebelik ve ovulasyon olabilmektedir. Ancak oluşan gebeliklerde spontan abortus, gestasyonel DM ve gebelikte hipertansif durumlara yatkınlık artmıştır (7, 29).
Kronik anovulasyonun klinik sonuçları olarak infertilite, amenoreden disfonksiyonel kanamaya kadar değisen menstrüel kanama problemleri, hirsutizm, akne, endometrial kanser ve muhtemelen meme kanseri riskinde artış, kardiovasküler sistem hastalıklarında artış şeklinde olabilmektedir.
1.4.2. Hiperandrojenizm ve hirsutizm
PKOS, androjen fazlalığının ve hirsutizmin en sık rastlanan nedenidir. Hirsutizmli hastaların %65-85i PCOS’lu olgulardır (30, 31). Hiperandrojenemi hastaların yaklaşık yarısında mevcuttur. LH; overin teka hücrelerinden androjen sentezini uyarır, SHBG’nin azalması da serbest androjen formlarını arttırır. Dolaşımdaki major androjen testosteron olmakla birlikte, DHT; kıl follikülleri ve derideki pilosebase birim gibi, birçok duyarlı dokuda major androjendir. Hirsutizmde, total ve serbest testosteron yüksekliği, ovaryan hiperandrojenemi bulgusudur. Androstenedion düzeyleri de genelde artar ve ovaryan orjinlidir. DHEA ve DHEAS adrenal kökenlidir, yükselebilir. Periferde Testosteron ve DHT’a dönüsür. Androjenler periferde östrona (E3) dönüşür. LH/FSH yüksekliği %75
11
saptanır. Hirsutizmin esas nedeni; anovulasyon ve overlerden aşırı androjen üretimidir (32). Hirsutizm; kadınlarda kıllanmanın normalde hiç olmadığı ve ya çok hafif olduğu androjene duyarlı alanlarında, tipik koyu ve kalın telli kılların fazlalığı olarak tanımlanır. Hastaların %70‘i hirsutizm sergilerken, daha azı ise aknelidir. Kıl büyümesindeki artışın derecesinin belirlenmesinde Ferriman-Gallwey yöntemi kullanılır (33). Burada vücudun 9 farklı bölgesi objektif olarak değerlendirilir.
Bu bölgeler yüz (özellikle bıyık ve sakal bölgesi), göğüs, meme areolası, sırtın üst kısımları, sırtın asağı kısımları, linea alba, kalçalar, uyluk iç kısımları ve dıs genital bölgelerdir. Her bölge için 1 ile 4 arasında puan verilir. Toplam 8’in üzerindeki değerler hirsutizm olarak değerlendirilir. Hirsutizm hafif, orta, siddetli olarak 3 gruba ayrılır. Hafif hirsut kadınlarda tek alan skoru 0-2 olup tipik olarak, yüzde, göğüs ve alt abdomende, ince, renkli kıllar bulunur. Orta derecede hirsutizmde, tek alanda 1-3 skorlarına rastlanır. Bu grupta kol-bacakta, yüzde göğüste, abdomende ve perinede kaba, renkli, uzayabilen kıllar vardır. Siddetli hirsutizmde ise skor 3-4 ve üstü olup tüm sakal bölgesinde ve geri kalan androjene duyarlı alanlarda kalın ve renkli kıllar mevcuttur (Şekil 3).
12 1.4.3. Obezite
Obezite; PKOS’lu kadınlarda sık görülür ve genetik faktörler, fiziksel aktivite ve diyetle bağlantılı olabilir. Obezite, normal ovulasyonu bozan üç değişiklik yapmakta olup, zayıflama ile bu değisiklikler düzelebilmektedir. Bu değişiklikler şunlardır: periferde androjenlerin östrojenlere aromatizasyonu, serbest E2 ve testosterone düzeylerinin artmasına neden olan, SHBG düzeylerinde azalma ve overin stroma dokusunda androjen sentezini uyaran insülin düzeyinde artış. PKOS olan kadınlarda vücut kütle indeksi normal kabul edilen sınırın genelde üzerindedir. Şişmanlık genelde santral obezite şeklindedir. Santral obezitede bel/kalça oranı fazladır (>0.85). VKİ obesitenin en yaygın kullanılan indeksidir. VKİ; ağırlığın boyun karesine bölünmesiyle hesaplanır (kg/m2
).VKİ aralıkları genellikle şu sekilde tanımlanmıstır; normal ağırlıkta (19.1-24.9 kg/m2), yüksek kilolu (25-29.9kg/m2) ve obez (>30kg/m2). Bel ölçüsü olarak göğüs kafesi ile krista iliakalar arasındaki en küçük çevre ölçülürken, kalça ölçüsü olarak bel ve uyluklar arasındaki en geniş çevre ölçülmektedir. Kadınlarda 0.85 ve altındaki değerler normal kabul edilir. WHR 0.85’ten fazla olduğunda, android tipte yağ dağılımı söz konusudur. Obez ve santral yağ dağılımlı kadınlar daha yüksek LH, androstenedion, E3, insülin, trigliserid, LDL, apolipoprotein-B seviyelerine sahiptir. HDL ise düşüktür(36). Yüksek bel/kalça oranının, daha fazla menstrual anormallik ve daha yüksek infertilite prevalansıyla birlikte olduğu gösterilmiştir. Obezite ve PKOS’u olan hastaların, sıkı kalori kısıtlaması sonucu %5 veya daha fazla kilo kaybı durumunda insülin, IGF-1, SHBG ve menstrüasyonda değişiklikler gözlemlenmiştir. Menstrüel düzen sağlanmış, hirsutizm düzelmiştir. Bazı spontan gebelikler de görülmüştür (34).
PCOS gibi hiperandrojenik obezitede, androjenlerin artmıs üretimi menstrüel düzensizlikle birliktedir. Estrona çevrilen androstenedion miktarı total vücud ağırlığına bağlı olarak değisiklik gösterir (34). Obezite ve asırı kilonun menstrüel disfonksiyona anlamlı bir katkıda bulunduğu görülmektedir. Yayınlarda; VKİ ve infertilite’nin artmıs insidansı arasında
13
bir bağ olduğu görülmektedir (35). Kilo fazlalığı, artmıs abortus riski ile de birliktedir. Genel olarak PKOS‘lu kadınların, PKOS olmayanlara göre daha yüksek oranda abortus riskine sahip olduğu gösterilmistir. Bu sonuç kısmende olsa, PKOS’daki yüksek LH konsatrasyonu sonucunda bozulmus oosit ve embriyo kalitesi ile ilişkilendirilir. Artmıs VKİ ile DM arasındaki iliski konusunda çok miktarda yayın vardır. PCOS olan olgularda önemli bir glukoz intoleransı riski vardır. Yapılan bir çalısmada VKİ’i 30 kg/m2
‘nin üzerindeki 20-30 yas arasındaki tüm kadınların %18’inde glukoz metabolizmasında bozukluk saptanmıstır. PKOS’u olan kadınların %15’inde başlangıç çalısmasında glukoz toleransı normalken, 5-7 yıl sonra bozulmus glukoz toleransına veya asikar diabete dönüs görülmektedir (37). Bu değisimin hemen hepsinin artan obezite ile bağlantılı olabileceği ve kilo alımının önlenmesinin anormal glukoz toleransının azaltılmasında yararlı olabileceği düşünülmektedir. PKOS’lu kadınlar gebeyken gestasyonel diabet olmaya daha eğilimlidir ve gebelikte glukoz intoleransı olan pek çok kadın PCOS özelliklerine sahiptir. Obezite ve PKOS’u olan hastaların kalori kısıtlaması sonucu %5 veya daha fazla kilo kaybı durumunda insülin, insülin-like growth faktör, SHBG düzeylerinde değisiklikler gözlemlenmistir. Menstrüel düzen sağlanmış, hirsutizm düzelmistir. Bazı hastalarda spontan gebelikler de görülmüştür (38).
1.4.4. İnfertilite
PKOS’da infertilitenin primer sebebi anovulasyondur. Anovulasyon’a neden olan LH hipersekresyonu ile infertilite arasındaki iliski sanıldığından daha komplekstir. LH ayrıca bilinmeyen bir mekanizma ile fertilizasyon ve erken gebelik kayıpları ile de iliskili olabilir (34, 39). Ovulasyon indüksiyonundaki ve yardımcı üreme tekniklerindeki gelismelere rağmen PKOS’lu infertil hastalar anlamlı bir başarıya ulaşılamamaktadır. Kilo vermeye direnç gösteren hastalarda ovulasyon indüksiyonu esnasında hiperinsülinemiyi azaltıcı akut bir diyet kısıtlaması tedavinin etkinliğini artıracaktır (39, 40).
14 1.4.5. Hiperinsülinemi ve Insülin Direnci
İlk kez 1980 yılında PCOS ile hiperinsülineminin ilişkili olduğunu tesbit edilmiştir Daha sonra 1980’li yılların ortalarında ise PCOS’lu hastalara oral glukoz tolerans testi (OGTT) bir tarama testi olarak önerilmiştir (41). Günümüzde PCOS ile insülin direnci arasındaki ilişki artık daha iyi bilinmektedir.
PKOS endokrin ve metabolik bir hastalıktır. İD; endojen ve eksojen insüline normal biyolojik cevabın verilememesi diye tanımlanır. PKOS’lu vakaların %43-76’sında İD tespit edilmistir. Bu vakalarda Tip 2 DM gelişme ihtimalinin normal popülasyonuna nazaran daha fazla olduğu yapılan birçok çalısmada bildirilmektedir (42, 43, 44). Çoğu çalışma, obez ve nonobez PKOS’lu kadınların, aynı yas ve kilolu normal kadınlara göre daha fazla İD ve hiperinsülinemi gösterdiğini ortaya koymustur. Azalmıs insülin sensitivitesinin yanısıra, PKOS’lu obez kadınlarda rölatif olarak insülin sekresyon defekti mevcuttur. PKOS’lu kadınların kilo vermesi insülin rezistansını önemli derecede iyilestirmesine rağmen, beta hücre defektini düzeltememektedir. Bu durum beta hücre defektinin PKOS’da primer anormallik olabileceğini göstermektedir (21, 22).
PKOS’lu kadınlardaki çalısmalar, insülin reseptörlerinin normal olduğunu göstermistir. İnsülin stimülasyonuna cevap olarak, adipozitlerde insülin bağlanması da normaldir. Glukoz tasıyıcı proteinlerin aktivasyonu ve glukozun hücre içine alınması gibi gelişen olaylarda azalma saptanması defektin postreseptör seviyede olduğunu göstermektedir (21, 22, 45). PKOS’lu obez kadınların yaklasık yarısında insülin reseptörü otofosforilasyonunda defekt olduğu görülmüstür. Bu kadınlarda uyarılmamış insülin reseptöründe zaten önemli derecede fosforilasyon vardır.
Son yıllarda serin fosforilizasyonunun androjen yapımında anahtar rol oynayan P450c17alfa enzim kompleksinin çalısmasını düzenlediği saptanmış olup PKOS’lu hastalarda tek bir bozukluğun hem insülin direnci hem de hiperandrojenemiye neden olabileceği
15
düsünülse de PKOS’lu vakaların yarısında tirozin otofosforilasyonunun normal olması bu kadınlarda insülin direncinin mekanizmasının multifaktoriyel olabileceğini düşündürmektedir (48). Hiperinsülineminin oranı ve hiperandrojenizm arasında anlamlı bir korelasyon bulunmaktadır. Hiperinsülineminin hiperandrojenemiye yol açışını açıklayan iki mekanizma daha mevcuttur.
1. Hepatik seks hormonu bağlayıcı globulin (SHBG) sentezinin inhibisyonu.
2. İnsülin benzeri büyüme hormonu bağlayıcı protein -1’in (ĐGFBP-1) sentezinin inhibisyonu.
İnsülinin IGFBP-1‘in intrafolliküler seviyesini azaltarak indirekt etki ile serbest IGF- 1’in intrafolliküler konsatrasyonunu arttırdığı ileri sürülmüstür. IGF-1 ovaryan intertsisyel hücrelerince LH’ın indüklediği androjen sentezinin potent stimulatörüdür. (49).
1.4.6. İnsülin Sensitivitesinin değerlendirilmesi
İnsülin direncinin veya duyarlılığının gösterilmesi için birçok test gelistirilmistir. Bunlardan bazıları; bazal insülin düzeyi, hiperglisemik glukoz klemp tekniği, öglisemik hiperinsülinemik klemp tekniği, intravenöz insülin tolerans testi, oral glukoz tolerans testi ve homeostasis model assessment (HOMA)’ dır. Ancak pratikte en sık kullanılan, açlık insülin düzeyi, açlık glukoz/ insülin oranı ve oral glukoz tolerans testi (OGTT) ile HOMA’dır.
A-Bazal insülin düzeyi: Đnsülin direncinin belirlenmesinde çok daha basit bir yöntem olarak
açlık insülin düzeylerinin de insülin direncinin bir kriteri olabileceği gösterilmistir. Bazal insülin düzeyi, her toplum için farklılıklar gösterir. Standardize edilmis bir esik değer bulunmamaktadır. Ancak bazı çalısmalarda 8 IU/ml üzeri, bazı çalısmalarda ise 15 IU/ml üzeri insülin direnci olarak kabul edilmistir. Bazal insülin düzeyleri de öglisemik klemp tekniği ile korelasyon göstermektedir.
16
B- Açlık glukoz/ insülin oranı (FGIR): Pratikte sık kullanılır. Açlık sonrasında alınan glukoz
ve insülin seviyelerinin oranıdır. Her toplum için farklılık arzeder. Oranının düsük olması, insülin direnci varlığını gösterir. . Pek çok çalışmada 4.5’in altındaki değerlerin PCOS’lu hastalarda ID’nin tanısını koymak açısından %95 sensitivite ve %84 spesifite gösterdiği bildirilmiştir. Glukoz mmol/L olarak alındığında 0.33’ün altındaki değerler ID’yi göstermektedir. Hiperglisemik hastalarda sensitivitesi düşer (37).
C- Hiperglisemik glukoz klemp tekniği: Metabolize edilen glukozun insüline oranı ile insülin
duyarlılığı hesaplanır.(metabolize glukoz/ insülin) (50).
D- Öglisemik hiperinsülinemik klemp tekniği: İnsülin infüzyon sistemine iv olarak glukoz
infüzyonu verilmesinde hastanın öglisemik sınırlarda tutulması prensibine dayanır. İD’ni belirlemede gold standarttır. Kullanılan diğer testlerin sensitivite ve spesifitesini belirlemek için, yapılan çalışmalarda bazal yöntem olarak da kullanılan bu yöntem zor uygulanması, invaziv olması, tecrübe ve zaman gerektirmesi nedeniyle pratikte uygulanabilir olmayıp, tercih edilmemektedir (50).
E- İntravenöz insülin tolerans testi: Sonuç ne kadar yüksekse insülin direnci o kadar azdır. F- Oral glukoz tolerans testi ve Homeostazis Model Assesment: OGTT karbonhidrat
metabolizmasını değerlendirmek için yaygın olarak kullanılan testtir. 75 veya 100 gr glukoz oral yoldan verildikten sonra 2–4 saat içinde değişik aralıklarda glukoz veya glukozla beraber insülin değeri bakılır. Bu testte; 0, 30, 60 ve 90’ıncı dakikadaki glukoz değerleri kriter olarak alınabildiği gibi, glukoz/insülin oranı bakılabilir veya belli bir denkleme dayanarak 0 ve 120’nci dakikadaki insülin ve glukoz değerleri kullanarak insülin sensitivite indeksi (ISI 0,120) çıkartılabilir (51).
120 dakika sonraki glukoz cevabının değerlendirilmesi: Normal <140 mg/dL
17 İnsüline bağımlı olmayan diabet >200 mg/dL
120 dakika sonraki insülin cevabının değerlendirilmesi: IR olabilir 100-150 MU/mL
IR 151-300 MU/mL Aşırı IR >300 MU/mL
HOMA beta hücre fonsiyonu ve İD hakkında bilgi veren bir yöntemdir. Açlık glukozu ve insülin konsantrasyonunun aritmetik örneklemesinden faydalanılarak insülin duyarlılığı belirlenir.(açlık insülin x açlık glukoz) / 22.5 formülüyle hesaplanır. HOMA indeksinin değeri ID ile doğru orantılı olup, indeks değeri ne kadar fazla ise ID’de o kadar fazladır. HOMA indeksinin hiperglisemik hastalarda da anlamlı ve doğru sonuç vermesi, açlık kan şekeri/insülin değerine göre önemli bir üstünlüktür. HOMA skorunun bazı yayınlarda 2,5 ve bazı yayınlarda ise 2,8’ in üzerinde olması İD ile iliskilendirilmistir (42). Normal kisilerde bu oran 2’nin altındadır. HOMA ile İD tesbit edilen kisilerde OGTT ile normal glukoz toleransı saptansa bile hayatlarının ilerleyen zamanlarında Tip 2 DM gelisimi açısından risk tasıdıkları söylenebilir (52).
1.4.7. Hiperprolaktinemi
Prolaktin gen ekspresyonu ön hipofiz laktotrop hücrelerinde, desidualize endometriyumda ve myometriyumda meydana gelir. İnsanlarda ana fonksiyonu laktasyonu başlatmak ve devam ettirmektir. 1985’den bugüne, PKO’li hastalarda hiperprolaktinemi sıklığı %3,2 ile %12,5 arasında değişiklik göstermiştir. PKO olan ve olmayan kadınlarda, intravenöz dopamin uygulanması ile her iki grupta da serum LH ve prolaktin seviyelerinde düşme görülür, bu da gösteriyor ki; PKOS’lu tüm olgularda anormal LH sekresyonu ile ilişkili hipotalamik dopamin varlığında sonuç hiperprolaktinemidir. Gerçekte, PKOS’lu tüm hastalarda LH puls sıklığı ve amplitüdünde artış görülür, fakat sadece birkaç hastada prolaktin artışı görülmektedir.
18
1.5 LABORATUVAR BULGULARI
Laboratuar bulgularında özellikle androjen düzeylerinin tanıda önemi vardır. Normal bir kadında günde 0.2-0.3 mg Testesteron (T) üretilir ki, bunun da %50’si Androstenedionun(A) periferik dönüşümünden, geri kalanı eşit miktarlarda (% 25) over ve adrenalden salgılanır. DHEAS’ın neredeyse tamamı, DHEA’ın ise % 90’ı adrenal kaynaklıdır. Dolasımdaki testesteronun % 80’i beta globulin olan SHBG, % 19’u albumine bağlı , % 1’i ise serbest durumdadır. Androjen etkisi bu serbest kısım ve bir miktarda albumine bağlı kısıma bağlıdır. DHEA, DHEAS ve A ise belirgin sekilde proteine bağlı değildir ve rutin immunassay testler biyolojik aktif düzeylerini yansıtır. T için durum farklıdır, rutin testler bağlı olan ve olmayan total T düzeyini ölçer. SHBG düzeyleri, artmış androjen ve hiperinsulinemi varlığında düşer. Östrojen ve tiroid hormonu ise SHBG düzeylerini arttırır. Hirsutizmi olan kadınlarda artmış T ve A’ un kaynağının over olduğu gösterilmiştir.
Hiperandrojenemiyi değerlendiren en sensitif ölçümler serum serbest T düzeyi ve serbest androjen indeksidir (SAi = total testosteron mol / L) / SHBG (nmol / L )x100). PKOS’lu kadınların yaklaşık % 60-80’ inde artmış androjen düzeyleri ölçülür. Genelde serbest T düzeyleri yükselmiştir. Total T ölçümünün katkısı azdır. A ölçümü hiperandrojenemik olarak tanımlananların sayısını %10 kadar arttırır. DHEAS, PKOS’lu kadınların %25’inde normal değerlerin üzerinde ölçülür (13). DHEA ölçümünün tanı değeri kısıtlıdır. Androgen Excess Society 2006 raporunda (13) serbest T dahil androjenlerin kan seviyelerinin hiperandrojenemi tanısı için sadece yardımcı olduğunu, tanı için tek kriter olmadığını ve klinik değerlendirmenin yerini tutmadığını belirtmiştir. Total T düzeylerinin 200 ng/dL nin üzerinde olması over ve adrenal tümör araştırılmasını, DHEAS düzeylerinin normalin iki katından yüksek olması adrenal tümör araştırılmasını gerektirir.
Luteal fazın ortasında ölçülen progesteron düzeyleri ile ovulasyon objektif olarak gösterilebilir. Bazal foliküler faz 17-(OH)-P ölçümü ise PKOS’un geç başlangıçlı konjenital
19
adrenal hiperplaziden ayırımı için gereklidir. Geç baslangıçlı konjenital adrenal hiperplazide 17-(OH)-P düzeyinin erken foliküler fazda < 3ng/ ml olması ile ekarte edilebilmektedir. Bu değerin üzerindeki olgularda ACTH uyarısı ile ölçülen 17(OH)Progesteron seviyesinin > 10 ng/ml olması 21-hidroksilaz eksikliğinin tanısını koydurur. Cushing Sendromunu düsündüren klinik bulguların varlığında, Deksametazon supresyon testi ve 24 saatlik idrarda serbest kortizol düzeyinin ölçülmesi tarama için kullanılabilir. Prolaktin(PRL) ile ilgili bozukluklar ve tiroid hastalıkları da ayırıcı tanıda düsünülmesi gereken durumlardır. PKOS’ da %30 ‘a varan oranlarda hafif-orta düzeylerde PRL yüksekliği görülebilir. Tiroid hastalıklarında menstürel düzensizlikler görülebilir ancak çoğu zaman hastalıkla iliskili diğer semptom ve bulgular tanıya olanak sağlar.
1.6 PKOS VE UZUN DÖNEM ETKİLERİ
Kadın sağlığıyla iliskili bu metabolik ve endokrin bozukluğun uzun dönem etkilerinin ortaya çıkması ve sağlığı tehdit edici boyutlara ulasması nedeniyle PKOS’lu hastaların uzun süreli takipleri çok önem kazanmıstır.
1.6.1. Abdominal Obesite Ve Dislipidemi
PKOS’da ortaya çıkan obezitenin nedeni hala bilinmemekle beraber farklı serilerde %10 ile %75 arasında değişebilen oranlarda obezite varlığı bildirilmektedir. Obez olan hastaların daha düşük LH, SHBG, DHEAS, dihidrotestosteron, IGF-1 ve yüksek dansiteli lipoprotein (HDL) düzeylerine, buna karşılık daha yüksek LDL (düşük dansiteli lipoprotein) düzeylerine sahip oldukları gösterilmiştir.(55)
PKOS’lu kadınların obesiteye vücut yağının abdominal depolanmasına ve insülin rezistansına eğilimi olduklarından, sendrom X olarak adlandırılan durumun diğer metabolik özelliklerinede sahip olabilecekleri öne sürülmektedir.
20
PKOS’lu kadınların karakteristik bir dislipidemiye sahip olup olmadıkları tartışmalı bir konu olmakla beraber, yapılan çalışmalarda genellikle bu grup kadınların düşük HDL kolesterol ve yüksek trigliserid düzeylerine sahip oldukları bildirilmektedir (56). Kardiyometabolik sendromda ortaya çıkan yüksek TG ve düşük HDL düzeyleri, insülinin kolesterol ester transfer proteini üzerindeki etkileri sonucu ortaya çıkmaktadır. Bu protein kolesterolün HDL’den VLDL’ye transferini ortaya çıkarmakta ve sonuçta Apolipoprotein A katabolizması gelişmektedir (58, 59).
1.6.2. Kemik Metabolizması
Hipotalamik orjinli amenorelerde osteopeni sık bir bulgudur. PKOS’lu kadınlarda normal yada supernormal iskelet mineralizasyonu ve androjen seviyeleri arasında pozitif bir iliski olduğu gösterilmistir. PKOS’lu kadınlarda düsük öströdiol seviyelerine rağmen hiperandrojenemi ve ilgili metabolik prosesler kemik kütlesini korur. PCOS’lu kadınlarda kilo fazlalığı eğilimi vardır ve vücut ağırlığı kemik kütlesinin güçlü bir belirtecidir.
En yüksek kemik dansitesi PKOS ve hirsutizmi olan normal adet gören kadınlarda gözlenmistir. Yeterli östrojen varlığında androjenler kemik üzerine pozitif bir etki yaparlar. Östrojen seviyelerinin düsük olduğu bazı oligomenoreik ve amenoreik PKOS’lu kadınlar osteopeni riski altında olabilir. Hiperandrojenik kadınlarda görülen yüksek kemik dansitesi androjenlerin bir sonucudur demek için henüz erkendir.
1.6.3. Kanser Riskleri
Çalısmaların birçoğunun kontrollü çalısma olmaması ve sendromu tanımlamak için kullanılan tanı kriterlerinin farklılıklar içermesi nedeni ile şuana kadar PKOS ile kanser ilişkisini destekleyen güçlü kanıtlara rastlanmamıstır. Ancak mevcut veriler ışığında özellikle basta endometrial kanser olmak üzere PKOS ile jinekolojik kanserlerin ilişkisini göz ardı etmek mümkün değildir.
21
Obezite, uzun süreli anovulasyon nedeni ile karşılanmamış östrojen maruziyeti, nulliparite, infertilite endometrium kanseri riskini arttıran faktörlerden bazılarıdır. DM ve HT hastalarında endometrium kanseri daha fazla görülmektedir. Bu yüzden amenoresi olan hastalara en az üç ayda bir endometrial dökülmenin sağlanması önerilmiştir (62).
PKOS’lu kadınlarda artmıs endometrium kanseri riskinden sorumlu olduğu düşünülen mekanizma uzamıs anovulasyon ve takibinde progestron ile karsılanmayan, devam eden östrojen sekresyonudur. Karsılanmamıs östrojene maruziyet endometrial hücrelerde mitotik aktivitenin artmasına, DNA replikasyon hatalarının artmasına ve sonucunda malign fenotip ortaya çıkmasına neden olmaktadır (62).
PKOS’un bir özelliği olan LH hipersekresyonunun endometrium kanseri gelişiminde etkili olabileceği bildirilmistir. Endometrium adenokarsinomlarında LH ve hCG reseptörleri asırı eksprese edilirler (63).Konishi ve ark. yaptığı çalısmada LH ve hCG reseptörlerinin asırı ekspresyonunun genç anovulator kadınlarda gelisen endometrial hiperplazi ve kanser ile iliskili olduğu sonucuna varmışlardır (64).
PKOS ile over kanserleri arasındaki doğrudan iliskiyi ortaya koymaya yönelik çok az sayıda çalısma vardır. Over kanseri gelismis 31 kadın, yas ve menopozal durum olarak eslestirilmis 62 kontrol vakası ile karsılastırıldığında tanı öncesi androstenodion ve dehidroepiandrosteron seviyelerinin belirgin olarak yüksek saptanması androjenlerin ovaryan karsinogenezde rol oynadığını desteklemektedir (67). Obezite ve epitelyal over kanseri arasındaki iliskiyi açıklamaya çalısan çalısmaların sonucu çeliskili olup bazı çalısmalarda pozitif bir korelasyon saptanmısken diğer bazı çalışmalarda saptanmamıstır.
1.6.4. Kardiyovasküler Hastalık Ve Metabolik Sendrom
PKOS, insulin direnci, obezite, aterojenik dislipidemi ve hipertansiyon ile karakterizedir. Metabolik sendrom, artmış kardiyovasküler hastalık (KVH) ve tip 2 DM riski ile ilişkilidir (69). Metabolik sendrom prevelansı, PKOS olan kadınlarda %45, yaş olarak
22
eşleştirilmiş kontrol grubundaki kadınlarda ise %4 olarak bildirilmiştir (70). PKOS’lu kadınlarda artmış KVH sıklığı için kesin kanıtlar olmasa da, PKOS, metabolik sendrom için çeşitli endokrin özellikleri paylaşır (71, 72). Ancak, Dahlgen ve arkadaşları (1992) PKOS olan kadınlardan oluşan küçük bir grupta, miyokard infarktüsü için relatif riski 7.4 saptamışlardı (73). Başka bir 10 yıllık izlem çalışması, aşırı kilolu PKOS olan beyaz ırkta kadınlarda KVH için relatif riski 5,91 olarak göstermişlerdir (74).
Kadınlarda metabolik sendromun tanı kriterleri: Bel çevresi >88 cm
Trigliserid düzeyi > 150 mg/dl HDL kolesterol < 50 mg/dl
Açlık glukoz düzeyi : 110-126 mg/dl HT > 130/85 mmHg
Metabolik sendrom parametrelerine ek olarak, diğer bazı subklinik hastalık belirteçleri de PKOS ve KVH arasında bağlantının olduğunu gösterir. PKOS’lu kadınların sol ventrikül diyastolik disfonksiyonu için artmış sıklığa ve artmış internal ve eksternal karotid arter sertliğine sahip oldukları tespit edilmiştir (78). Ayrıca birçok çalışma ateroskleroz gelişiminde erken olay olarak tanımlanan endotel disfonksiyonun, etkilenmiş kadınlarda daha fazla olduğunu göstermiştir (79, 80).
PKOS ‘lu kadınlarda yapılan çalısmalar bu kadınlarda makrovasküler hastalık ve Tromboza daha fazla yatkınlık olduğu gösterilmiştir (81). Bu hastalarda yüksek Plazminojen aktivatör inhibitör tip 1 (PAI-1) düzeyleri bildirilmiştir (82)
PKOS’ da aterosklerozun ilk bulgularından olan endotel hasarın gelisiminde İD anahtar rol oynar. Bunun sonucu olarak PKOS’ lu kadınlar ileri yaşlarda hipertansiyon, artmıs kardiyovasküler risklerle PKOS’ lu olmayan kadınlara göre daha sık karşı karşıyadırlar (85).
23
1.6.5. PKOS’da
Kardiyovasküler
risk
ve
hiperinsülinizmi
değerlendirmek için biyolojik markerlar
a. Açlık hiperinsülinemisi
b. OGTT esnasında artmıs insülinemi c. Düsük glukoz/insülin oranı
d. Azalmıs serum HDL –kolesterol seviyesi ve lipid profili, artmıs TG e. Serum SHBG seviyesinde azalma
Artmıs oksidatif stresin PKOS’lu kadınlarda kardiyovasküler hastalık riskini artırabileceği bildirilmistir. Oksidatif stresin doku hasarına yol açma mekanizmalarından biri de lipid peroksidasyonudur.Lipid peroksidasyonunu yansıtan malondialdehid(MDA),hücrenin yapı ve fonksiyonunu bozabilir. Paraoksinaz 1 (PON1),okside lipoproteinler üzerindeki lipid peroksidleri hidrolize edip HDL ve LDL’i oksidatif stresin etkilerinden koruyan ve HDL’nin antioksidan etkilerinden kısmen sorumlu bir enzimdir.
1.7 PKOS’UN TANISI
1.7.1. Görüntüleme Yöntemleri
Transvajinal ultrasonografideki gelişmeler overlerin boyut ve şekli ile birlikte follikül ve stromanın da görüntülenmesine olanak sağlamıştır. PCO; ultrasonografi ile stroma dokusunun artması nedeniyle büyümüş overler ve inci kolye tarzında periferik yerleşimli 2-8 mm boyutlarında 10’un üzerinde follikül görümünü olarak tanımlanmıştır. Üreme çağındaki kadınlarda ultrasonografik olarak PCO görünümünün sıklığı ile ilgili bazı çalışmalarda bu oran %17-23 oranında bildirilmiştir. Bu kadınların %10’unda PCOS tanısı koyduracak diğer semptomlar vardır (7). PCO’da oluşan histolojik değişiklikler şunlardır (87):
● Yüzey alanı iki kat artmıştır. ● Over hacmi 2-8 kat artmıştır.
24
● Aynı sayıda primordial follikül vardır. Ancak büyümekte olan ve atreziye uğramış follikül sayısı normalin yaklaşık 2 katıdır.
● Kortikal stromada 1/3 kat, subkortikal stromada 5 kat artış vardır. ● Over hilus hücre hiperplazisi normalden 4 kat fazladır.
Multifolliküler overler PCO ile karıştırılmamalıdır. PCO, normal overler ve multifolliküler overlerden daha büyük olması, daha fazla follikül içermesi ve hipertrofik stroması ile ayrılmaktadır. Stromal hipertrofi ve hiperekojenite PCO ve multifolliküler overleri ayırmada en güvenilir ultrasonografik belirti olarak kabul edilmektedir (88).
Tanıda kullanılan ultrasonografik kriterler eksternal ve internal olmak üzere ikiye ayrılır. Eksternal morfolojik bulgular: ovarian alan ve volümün artması, yuvarlak indeks (ovarian genişlik/uzunluk) artışı, uterin genişlik/ovarian uzunluk oranının azalmasıdır.
İnternal morfolojik bulgular ise, çok sayıda periferal dağılımlı mikrokist (<10 mm), ovarian stromanın artmış ekojenitesi ve ovarian stromanın yüzeyinin artmasıdır (26).
Renkli Doppler ultrasonografisi, over stromasındaki vaskularizasyon ağının tespitini sağlamaktadır. Kan akımı, erken folliküler fazda PCOS’lu hastalarda (%88) normal hastalara (%50) göre daha sık olarak görüntülenir ve artmış gibi görünmektedir. PCOS’de artmış stroma komponenti, artmış sistolik hız ve azalmış pulsatilite indeksi ile beraberdir. Şimdiye kadar PCOS’da Doppler ultrasonografinin tanısal faydasını gösteren bir veri elde edilememiştir. Ama son veriler, gonadotropin tedavisinde ovarian hiperstimulasyonu tahmin etmede yararlı olabileceği yönündedir (90).
1.7.2. Hormon Analizleri
Androjenik hormonlar: Terminal kılların büyümesini stimüle eden, ses ve kas yapısında değişikliklere, klitoral büyümeye ve meme hacminde küçülmeye neden olan hormonlardır. En iyi bilinenleri testosteron ve androstenedion’dur. DHEA-S ise önemli bir androjen prekürsörüdür.
25
1. Testosteron: Kadınlarda adrenal bez ve overler tarafından eşit olarak üretilir. Bu iki yerdeki üretim dolaşımdaki testosteronun %50’sini oluşturur. Geriye kalan testosteron over ve adrenal bezden salgılanan androstenedionun periferde testosterona dönüşümü ile oluşur. Kadında normal testosteron konsantrasyonu 20 ila 75 ng/dL arasındadır. Testosteron düzeyleri ile hirsutizmin şiddeti arasında yüksek bir bağıntı yoktur. Çünkü hirsutizme neden olan testosteron değil onun daha güçlü bir metaboliti olan DHT’dir. Yüksek serbest testosteron düzeyleri (>80 ng/dL) anovulasyonlu ve hirsutizmli kadınlarda bulunur. Total testosteron düzeyinin >200 ng/dL olduğu olgularda tümör araştırması yapılması önerilmektedir (91). 2. Androstenedion: Adrenal bez ve overler tarafından eşit olarak üretilir. Testosterondan daha az potenttir. Ancak aşırı konsantrasyonlarda androjenlerin biyolojik etkinliğini gösterir. 3. Dehidroepiandrosteron: DHEA ve sülfat formunun hemen tamamı adrenal bez tarafından üretilir. DHEA hızla metabolize olur ve bu nedenle düzeyinin ölçülmesi tam olarak adrenal bez aktivitesini göstermez. DHEA-S ise bunun tersine daha uzun yarılanma ömrüne sahiptir ve adrenal bez aktivitesini gösterir. DHEA’nın normal değerleri 38 ile 338 mg/dL arasındadır. Luteinizan Hormon: PCOS’lu kadınlarda, sıklıkla serum LH düzeyleri yükselmiş, FSH düzeyleri baskılanmıştır. Böylece LH/FSH oranı artar. Geç başlayan konjenital adrenal hiperplazili kadınlar genellikle normal bir LH/FSH oranına sahiptir.
Prolaktin: PCOS’lu vakaların %10-30’unda prolaktin (PRL) yükselmiş olabilir (>30ng/mL). Bu bilgiler ışığında PCOS’da;
1. Androstenedion ve testosteron gibi primer olarak over tarafından salgılanan biyolojik olarak en aktif androjenlerin dolaşımdaki düzeyleri artmıştır.
2. Vakaların yaklaşık %50’sinde DHEA ve DHEA-S gibi adrenal androjenler artmıştır. 3. Östron (E1) seviyesi E2 düzeyinden daha yüksektir, normal E1/E2 oranı tersine dönmüştür. 4. Olguların yaklaşık 2/3’ünde LH artmıştır, hemen tamamında FSH baskılanmıştır.
26 6. Serum insülin düzeyinde belirgin artış vardır.
7. Olguların %25’inde prolaktin düzeyinde artma olduğu saptanmıştır.
1.8 PKOS’ UN TEDAVİSİ
PKOS’ lu hastalarda tedavi amaçları: androjen seviyelerini düşürmek, endometriumu korumak, normal vücut kilosuna erismeyi sağlamak, uzun dönemde kardiyovasküler riskleri azaltmak, hirsutizm ve insülin direncini düzeltmek, ovulasyonu indüklemektir. Tedaviyi yönlendirmede, fertilite isteğine göre tedavi seçenekleri hastayla birlikte değerlendirilip karar verilmelidir. Bu hedeflere ulaşmak için öncelikle yaşam tarzı modifikasyonunu sağlamak önerilmektedir. Bu hastalarda bilinen en etkin tedavi kilo vermektir. Kilo kaybı ve düzelmiş endokrin profil ile ovulasyon ve sağlıklı bir gebelik ihtimali yükselecektir. Mevcut kilonun %10 kadarı verilmelidir. Kilo kaybı ile periferde androjenlerin östrojene dönüşme oranı azalır, SHBG düzeyleri artar. İnsülin düzeylerinde azalma olur (92).
PCOS tedavisinde aşağıdaki grup ilaçlar kullanılır:
1.8.1. Antiandrojenler
Spiranolakton: Aldesteron antagonisti, potasyum tutucu diüretik olup hirsutizm tedavisinde de kullanılır (94). Androjenlerin periferik androjen reseptörlerine bağlanmalarını bloke eder. En sık görülen yan etkileri: menstruel düzensizlik, hiperkalemi, geçici poliüri, bas dönmesi ve bulantıdır.
Siproteran asetat: T ve DHT’ un etkisini hücre içi reseptörlere bağlanarak bloke eden güçlü bir progesterondur. LH salınımını inhibe ederek, ovaryan T sekresyonunu azaltır, androjenlerin klirensini arttırır, periferal düzeyde androjen etkisini antagonize eder. Akne ve hirsutizm tedavisinde sık kullanılır (94). Yan etkileri: hepatotoksisite, kilo artısı, ödem, kisilik değisiklikleri, açlık insülin ve lipid düzeylerinde hafif artıstır.
27
Flutamid: Esas olarak prostat hipertrofisi ve prostat kanserinde kullanılan saf antiandrojendir. T ve DHT’ nin reseptörlere bağlanmasını yarısmalı olarak inhibe eder. En önemli yan etkisi hepatotoksisitedir. Tedavi süresince karaciğer fonksiyon testleri yakın izlenmelidir. Ancak düsük dozlarda bu yan etkinin az olduğu ve hirsutizmde etkili olduğu gösterilmiştir (94). Bikalutamid: Yapısı testesterona benzeyen antiandrojen bir ilaçtır. Testesteronun reseptör bağlanmasını bloke eder. İlk olarak prostat kanserinde kullanılmıstır. Literatürde yapılan tek çalısmada bikalutamid hirsutism tedavisinde etkili bulunmuştur (95).
Finasterid: Kıl folikülleri üzerine en güçlü androjen aktiviteye sahip olan DHT’ un T’dan dönüsümünü sağlayan 5α-redüktaz enziminin inhibitörüdür. Hirsutizm ve PKOS’daetkili olduğunu gösteren çalısmalar vardır(96, 97). Yan etkileri; hafif gastointestinal bozukluklar, baş ağrısı, kuru cilt ve libidoda azalma yapmasıdır. Ketokonazol: 400 mg/gün dozunda 6 hafta içinde hirsutizmde tedavi edici etkiye sahiptir. Adrenal ve gonadal steroidogenezisi bloke eder (26).
1.8.2. İnsülin duyarlılığını arttıran ilaçlar
PKOS’ nun insülin direnci ile iliskili olması, Tip 2 DM ve kardiyovasküler hastalıklar açısından atmıs riske sahip olması önemli klinik bulgulardır. Bu durum gösteriyor ki; PKOS sadece infertilite ya da kozmetik bir problem değil, daha çok önemli bir genel sağlık problemidir. Bu nedenle PKOS’ a yönelik herhangi bir tedavi sadece ovulatuar disfonksiyon ve hiperandrojenizmi hedef almamalı aynı zamanda metabolik sendrom ile iliskili komorbiditeleri de hedef almalıdır. Bundan dolayı PKOS’ da İD’ nin önemi fark edildikten sonra insülin duyarlılığını arttıaran ilaçların kullanımı da giderek yaygınlaşmaktadır.
Bu amaçla kullanılan ilaçlar metformin ve tiazolidinedionlardır. Metformin: En eski ve dünyada hala en çok kullanılan insülin hassasalastıcı, biguanidler sınıfından oral antidiyabetik ajandır. Direkt etkisi karaciğerde glukoneogenezi azaltıp, glikojenolizisi artırarak glukoz üretimini azaltmak, kas ve yağ dokusunda glukoz alımını arttırmak, intestinal
28
glukoz emilimini azaltmaktır(98). Hiperandrojenizm üzerine olan etkisini; karaciğer tarafından üretilen SHBG yapımını arttırıp, bunun sonucunda serbest T düzeylerini azaltarak sağlar. PKOS’ da kullanım dozu 1000-2000 mg/gündür. En sık görülen yan etkiler; bulantı, kusma ishal, siskinlik gibi gastrointestinal sistem semptomlarıdır.
Tiazolidinedionlar (TZD): Glitazonlar olarak da adlandırılan bu grup, insülin hassaslastırıcı oral antidiyabetiklerdendir. Bir nükleer reseptör olan, peroksizom proliferatör aktive edici reseptör gamaya (PPAR-γ) bağlanan sentetik ligandlardır. TZD’ların PPAR-γ’ yı aktive etmesi sonucunda özellikle kas ve yağ dokusunda insülin duyarlılığı artar, yağ hücrelerinin diferansiyasyonu stimüle olur (98).Troglitazon bu grubun ilk ilacıdır ancak idiosenkrotik hepatotoksisite nedeniyle Mart 2000’ de piyasadan kaldırılmıstır. Troglitazon ile PKOS’ lu hastalarda serum insülin, LH ve androjen seviyelerinde düsme, ovulasyon oranlarında artıs tesbit edilmiştir (100).
1.8.3. Oral kontraseptifler
Polikistik over sendromunda uzun dönem kontrol için kullanılır. Hirsutizm tedavisinde halen en popüler tedavi aracıdırlar. Oral kontraseptifler dolaşımdaki LH ve FSH düzeyini baskılayarak overde androjen yapımını azaltırlar (106). Henüz tam olarak anlaşılamamış bir mekanizmayla adrenal androjen üretimini de azaltmaktadırlar. Oral kontraseptiflerdeki progesteronlar derideki 5 α redüktaz aktivitesini de inhibe eder.
1.8.4. GnRH agonistleri
Ovaryan androjen sentezi LH etkisi ile olduğundan GnRH agonistleri tedavisi ile hipofiz supresyonu hirsutizmin gerilemesini sağlar. PCOS’lularda 4 hafta süreyle günlük kısa etkili GnRH agonisti kullanan kadınlarda ovaryan steroidogeneziste belirgin baskılanma olur. Ovaryan androjen üretiminin baskılanması, hirsutizmde belirgin düzelmeye yol açar.
29 1.8.5. Cerrahi Tedavi
Cerrahi tedavide ya "wedge" rezeksiyon ya da "drilling" kullanılabilir. "Wedge" rezeksiyonda overin en kalın kısmından yarısını medulla dokusunun oluşturduğu over dokusu çıkarılır. "Drilling" ise over stromasında laser yada koter ile termal hasar oluşturulmasıdır. Her iki işlem sonrasında normal menstrüel sikluslar, gebelik, hormon değerlerinde düzelme gibi olumlu sonuçlar elde edilebilmektedir (29,107). Laparoskopik ovaryan drilling işlemi ile 3-6 ay arasında gonadotropinler ile ovulasyon indüksiyonu yapılan hastalar karşılaştırıldığında sonuçları benzerdir (107).
1.8.6. İnfertilite Tedavisi
Polikistik over sendromlu hastalarda ovülasyon indüksiyonunda ilk seçenek klomifen sitrattır. Bu ajanla hastaların %80’inde ovülasyon, %40’ında gebelik sağlanır. Klomifen sitrata yanıtsız hastalarda ikinci basamak ekzojen gonadotropinler kullanılabilir.
1.9 β3-AR’ler
Emorine ve arkadaşları, 1989 yılında insan β3-AR’yi klonlamışlardır (117). Ancak β3-AR agonistlerinin keşfi, obesite tedavisi çalışmalarında denendikleri daha önceki tarihlere dayanmaktadır. Bu tarihlerde, yeni geliştirilen β-AR agonistlerinin sıçanda beyaz veya kahverengi adipozitlerde lipolizi uyardıkları, bu lipolitik etkinin standart β1- ve β2-AR antagonistleri ile blokaja dirençli olduğu keşfedilmiştir (119). Barbe ve arkadaşları (1996), β3-AR’lerin, insan beyaz yağ dokusunda lipolizin düzenlenmesinde kemirgenlerdekinden daha az önemli olduğunu göstermişlerse de daha sonra bu reseptörlerin insanlarda enerji dengesinin düzenlenmesinde önemli bir rol oynadığı belirtilmiştir (120). Önceki çalışmalarda β3-AR’lerin en çok beyaz ve kahverengi adipozitlerin yüzeyinde bulunduğu belirlenmiş, daha yeni çalışmalar β3-AR’lerin insanda kalp, kolon, mesane detrüsörü, miyometrium dokularında da eksprese edildiğini göstermiştir (121).
30 1.9.1. β3-AR’lerin Yapısı ve Özellikleri
β3-AR geni, insanlarda, sıçanlarda ve diğer bazı türlerde klonlanmıştır (117). Bu gen insanda 8. kromozomda bulunur. β1-AR ve β2-AR’leri kodlayan genlerden farklı olarak, β3-AR geni bir veya daha fazla intron içerir. Birkaç ekzon varlığı, alternatif splicing olasılığını ve böylece ayrı farmakolojik özellikleri olan farklı reseptör izoformlarının meydana gelme olasılığını artırır. Farklı türler arasında, C terminal kuyruğunun dizisinin aminoasit içeriğinde ve uzunluğunda varyasyonlar bildirilmiştir. İnsan β3-AR geninin yapısı hakkında iki görüş ileri sürülmüştür. İlk görüşe göre, β3-AR geni 2 ekzon ve 1 intron içerir. İlk ekzon, reseptörün ilk 402 aminoasitini kodlarken, diğer ekzon C terminal kuyruğunun son 6 aminoasitini kodlar (118). Bu yüzden, C terminal kuyruğunun çeşidine göre β3-AR’nin, izoform A (402 aminoasitlik) ve izoform C (6 ek aminoasit ile) diye iki varsayımsal formu vardır. Diğer görüşe göre, β3-AR geni 3 ekzon ve 2 intron içeren bir yapıdadır. Sıçan ve farede de β3-AR’yi kodlayan gen 3 ekzon ve 2 intron içerir (122). Şekil 4’de Beta adrenoreseptörlerin şematik görüntüsü gösterilmiştir.
Şekil 4: Beta adrenoreseptörlerin şematik görüntüsü
Yoshida ve arkadaşları (1994), kemirgen beyaz ve kahverengi yağ dokusunda baskın olan alt-tipin β3-AR olduğunu, obez farelere β3-AR agonisti uygulanmasının, yem tüketiminde azalma olmadan ağırlık kaybına yol açtığını göstermişlerdir. Ayrıca, β3-AR
31
agonistleri yağ oksidasyonunu artırırlar ve beyaz yağ dokusunda lipolizi uyarırlar. β3-AR stimülasyonunun beyaz yağ dokusu depolarından yağ serbestleşmesine yol açtığı ve bunun kahverengi yağ dokusunda okside edildiği ileri sürülmüştür. Kemirgenlerde β3-AR agonistlerinin anti-obezite etkileri, beyaz yağ dokusu depolarında lipoliz, yağ oksidasyonunun artması, kahverengi yağ dokusu aracılı termogenezin artması şeklinde özetlenebilir. Sonuçta, yiyecek tüketimi azalmadan vücut yağındaki seçici azalma ağırlık kaybına yol açar ve yağsız kitle korunur (123).
İnsan β3-AR geninde 64. kodonda, reseptörün ilk intraselüler kangalında arjininle triptofanın yer değiştirmesine yol açan bir mutasyon tanımlanmıştır. Klinik açıdan önemi henüz bilinmese de bu polimorfizmin, Avrupa ve Kuzey Amerika’nın % 8-10’unda görüldüğü bildirilmiştir.
1995 yılında, Walston ve ark. (108, 109, 110) Pima Kizilderililerinde B3-adrenerjik reseptörde yanlış anlamlı bir mutasyon tespit etmisler. İnsanlarda, ADRB3 esas olarak visseral adipoz dokuda ekspresse oluyor ve bunlarin enerji tüketimi ve vücut yağ dagilimi, lipoliz ve serbest yağ asitlerinin portal vene taşinmasında katkıda bulunduğu düşünülmektedir.
Missense mutasyon protein duzeyinde ADRB3’de 64. aminoasit olan triptofan yerine, Arginin gecmesine (Trp64Arg mutasyon) neden olur. Japon denekleri bir çalışma raporunda bu mutasyonun dinlenme metabolik hizinda 200 kcal / gün düşüşe neden oldugu gösterilmiştir.(111). Ayrıca, bu mutasyon olduğu bildirilmiştir calorigenik fonksiyon anormallileri, obezite, sendrom X özellikleri (abdominal obezite, yüksek kan şekeri, insülin direnci ve kan basıncı yükselmesi), yaşla birlikte kilo aliminda artis, ve erken başlangıçlı diabetes mellitus ile iliskili oldugu gosterilmistir (108).