DİCLE ÜNİVERSİTESİ
TIP FAKÜLTESİ
İÇ HASTALIKLARI ANABİLİM DALI
NEFROTİK SENDROMLU HASTALARDA CRP
YÜKSEKLİĞİNİN LİPİD PARAMETRELERİ, PROTEİNÜRİ,
EKOKARDİOGRAFİ GÖSTERGELERİ VE KLİNİK GİDİŞ
ÜZERİNE ETKİSİNİN DEĞERLENDİRİLMESİ
UZMANLIK TEZİ
Dr.
İdris YILDIRIM
TEZ DANIŞMANI
Prof. Dr. M. Emin YILMAZ
İÇİNDEKİLER
TEŞEKKÜR………..…3 ÖZET……….4 İNGİLİZCE ÖZET(ABSTRACT)……….………...5 TABLOLAR VE ŞEKİLLER………...6 KISALTMALAR………..7 1.GİRİŞ VE AMAÇ………..9 2.GENEL BİLGİLER………...10 2.1.Nefrotik Sendrom………...102.1.1.Tanım, Tarihçe, İnsidans………10
2.1.2.Patoloji………....11
2.1.2.1.Minimal Değişiklik Hastalığı (MDH) ve Fokal Segmental Glomerüloskleroz (FSGS)………..12
2.1.2.2.Membranöz Nefropati(MN)………14
2.1.2.3.Membranoproliferatif Glomerülonefrit(MPGN)………15
2.1.2.4.IgA Nefropatisi……….……...17
2.1.3.Sekonder Nefrotik Sendrom Nedenleri……….19
2.1.3.1.Diyabetik Nefropati………....19
2.1.3.2.Renal Amiloidoz………...21
2.1.3.3.SLE Nefriti………..24
2.1.4.Nefrotik Sendrom Patogenezi………...29
2.1.5.Klinik ve Tanı………....31
2.1.5.1.Klinik Tanı Kriterleri………..31
2.1.5.2.Laboratuar Bulguları………..31 2.1.6.Tedavi………...32 2.2.AKUT FAZ REAKSİYONU……….34 2.2.1.C-reaktif Protein(CRP)………..34 3.GEREÇ VE YÖNTEMLER……….38 4.İSTATİSTİKSEL YÖNTEM………...38 5.BULGULAR………...…….39 6.TARTIŞMA VE SONUÇ………...43 7.KAYNAKLAR……….48
T
EŞEKKÜR
Bilimsel düşünme ve çalışmayı bizlere öğreten, engin bilgi ve birikimlerini bizimle paylaşan, bugünlere gelmemizde büyük emeği olan, hekimliği bizlere öğreten değerli hocamız Prof. Dr. Ekrem MÜFTÜOĞLU’ na başta olmak üzere, İç Hastalıkları A.B.D. Başkanımız Prof. Dr. M. Emin YILMAZ’a yetişmemde büyük emekleri olan bütün değerli öğretim üyeleri; Prof. Dr. Vedat GÖRAL, Prof. Dr. Orhan AYYILDIZ, Prof. Dr. Abdurrahman IŞIKDOĞAN, Prof. Dr. Kendal YALÇIN, Prof. Dr. Alpaslan TUZCU, Doç.Dr. Muhsin KAYA, Yrd. Doç. Dr. Deniz GÖKALP, Yrd. Doç. Dr. Hasan KAYABAŞI, Yrd. Doç. Dr. M.Ali KAPLAN, Uzman Dr. Yaşar YILDIRIM, Uzman Dr. Remzi BEŞTAŞ, Uzman Dr. Feyzullah UÇMAK, Uzman Dr. Coşkun BEYAZ, Uzman Dr. Mehmet KÜÇÜKÖNER’e teşşekürlerimi sunuyorum.
Tezimin her aşamasında büyük emeği olan, yardımlarını esirgemeyen sayın Doç. Dr. Ali Kemal KADİROĞLUNA,
Rotasyon eğitimim sırasında bilgilerini benden esirgemeyen Kardiyoloji A.B.D. , Enfeksiyon Hastalıkları ve Mikrobiyoloji A.B.D. , Göğüs Hastalıkları ve Tüberküloz A.B.D. ve Biyokimya A.B.D. başkanlarına ve değerli öğretim üyelerine,
Birlikte çalışmaktan her zaman büyük mutluluk ve onur duyduğum tüm asistan arkadaşlarıma ve İç Hastalıkları A.B.D. çalışanlarına teşşekürlerimi sunuyorum.
Güçlerini her zaman arkamda hissettiğim sevgili annem, babam ve kardeşlerim’e sonsuz teşşekürler.
ÖZET
GİRİŞ: CRP, inflamasyonun özgün olmayan bir göstergesi olmakla birlikte, birçok klinik durumda
büyük bir tanı değerine sahiptir ve birçok çalışmada çeşitli hastalıkların aktivite göstergesi ve klinik gidiş belirleyicisi olarak kullanılmıştır.
Biz bu çalışmada; CRP düzeyinin nefrotik sendromlu hastalarda proteinüri, lipid parametreleri, EKO göstergeleri ve klinik gidiş üzerine etkisini değerlendirmeyi amaçladık.
MATERYAL VE METOD: Bu çalışmada, 2000-2010 yılları arasında Dicle Üniversitesi Tıp
Fakültesi Nefroloji Kliniğinde nefrotik sendrom tanısı ile yatırılarak takip ve tedavi edilen tüm hastaların dosyaları (1440 hasta) tarandı ve içlerinden verileri yeterli olan 49’u (% 37.5) erkek, 55’i (% 62.5) kadın 104 hastanın dosyası retrospektif olarak incelendi. Çalışma parametreleri olarak, hastaların demografik bilgileri, histopatolojik tanıları, kliniğe yatışı esnasında bakılan kan basıncı, aldığı-çıkardığı sıvı miktarı, hemoglobin, hematokrit, beyaz küre, trombosit, glukoz, üre, kreatininin, sodyum, potasyum, klor, kalsiyum, fosfor, magnezyum, ürik asit, AST, ALT, LDH, ALP, GGT, kolesterol, trigliserid, HDL, LDL, albumin, total protein, fibrinojen, IgG, IgA, IgM, C3, C4, sedim, CRP, esbach, idrar dansitesi, idrar lökosit, eritrosit, protein, EKO’da sol atrium kalınlığı, sol ventrikül arka duvar kalınlığı, interventriküler septum kalınlığı, ejeksiyon fraksiyonu değerleri ve yatış süreleri incelendi. Hastalar CRP değerine göre ( CRP referans aralığı 0-5 mg/l ) iki gruba ayrıldı, Grup 1’e CRP düzeyi > 5mg/l, Grup 2’ye CRP düzeyi ≤ 5mg/l olan vakalar alındı. Grupların karşılaştırılma sından başka her grup kendi içinde olmak üzere hastaların kliniğe yatırıldıkları ve taburcu edildikleri dönemde CRP ve diğer çalışma parametrelerine bakılarak değerlendirildi ve aralarındaki ilişki karşılaştırıldı.
BULGULAR: CRP değerlerine göre yapılan gruplandırma sonrası ;
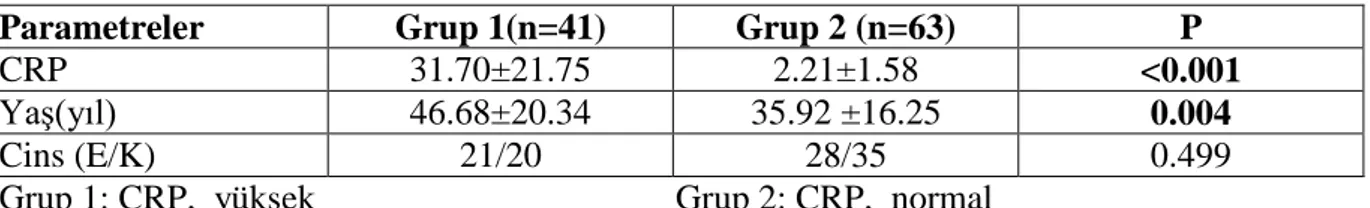
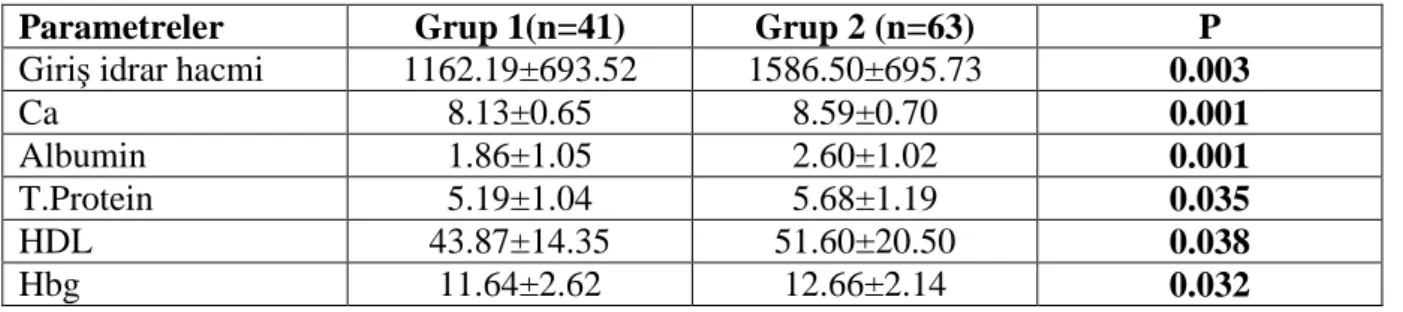
1- Hastaların yaş ortalaması; grup 1’de 46.68±20.34 yıl, grup 2’de 35.92±16.25 yıl (p=0.004) idi. 2- Grup 1’de grup 2’ye göre, kliniğe yatarken bakılan 24 saatlik idrar miktarı (p=0.003) ve kalsiyum(p=0.001), albumin(p=0.001), total protein(p=0.035), HDL(p=0.038), hemoglobin (p=0.032) düzeylerinin istatistiksel olarak anlamlı bir şekilde daha düşük olduğu saptandı.
3- Grup 1’de grup 2’ye göre yaş(p=0.004), klinikte yatış süreleri(p=0.030), kreatinin(p=0.009), LDH(0.006), trombosit(0.005), sedim(p<0.001), C4(p<0.001), spot idrar protein(p=0.038) ve esbach(p<0.001) düzeylerinde istatistiksel olarak anlam taşıyan yükseklik saptandı. Ancak Grup 1’de grup 2’ye göre LDL(p=0.051) düzeyleri daha yüksek olmasına rağmen istatistiksel olarak anlamlı değildi.
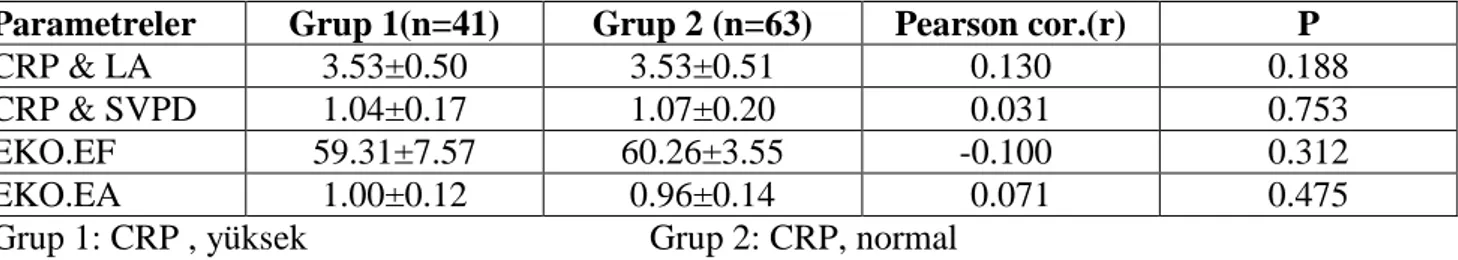
4- Çalışmamızda CRP değeri ile Ekokardiografide ölçülen kardiak parametreler (LAD, EA, SVPDK, EF) arasında anlamlı bir ilişki saptanmadı (p>0.005).
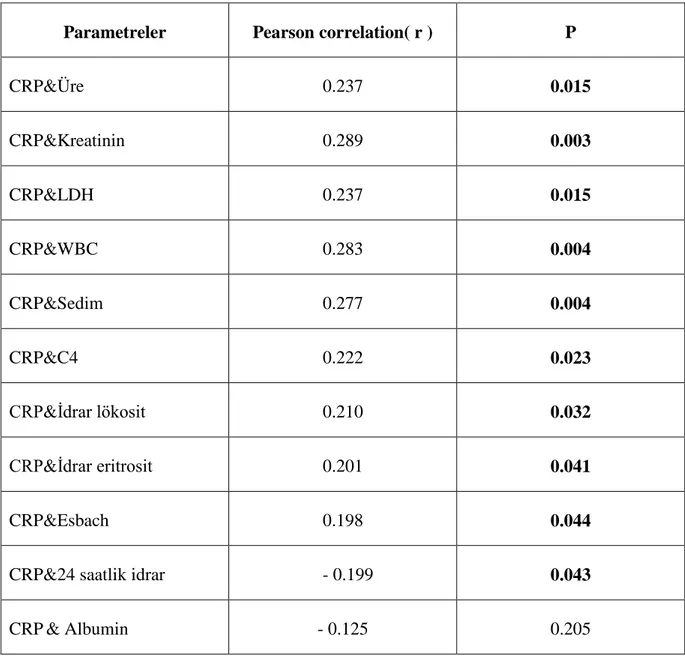
5- CRP düzeyinin, diğer çalışma parametreleri ile yapılan korelasyon değerlendirmesinde ise CRP yüksekliği ile üre(p=0.015), kreatinin(p=0.003), LDH(p=0.015), WBC(p=0.004), sedim(p=0.004), C4(p=0.023), idrar lökosit(p=0.032), idrar eritrosit (p=0.041), 24 saatlik idrar protein(p=0.044) düzeyleri arasında pozitif, CRP yüksekliği ile 24 saatlik idrar miktarı (p=0.043) arasında negatif korelasyon olduğu saptandı.
SONUÇ: Nefrotik Sendromlu hastalar arasında proteinüri miktarında artış, böbrek fonksiyonlarında
kötüleşme, hastanede kalış süresinde uzama, günlük idrar miktarında ve serum albumin değerinde azalma CRP değeri normal olan gruba göre CRP değeri yüksek olan grupta daha fazla idi.
CRP ile üre, kreatinin, lökosit, sedimentasyon, kompleman ve esbach arasında pozitif korelasyon, albumin ve günlük idrar miktarı arasında negatif korelasyon saptadık.
Erişkin nefrotik sendromlu hastalarda CRP ile proteinüri, hastalık aktivitesi, lipid parametreleri, ekokardiyografik parametreler ve klinik gidiş arasındaki ilişkiyi inceleyecek büyük ölçekli çalışmalara gereksinim vardır.
ABSTRACT
OBJECTIVE: Although CRP is not a unique marker of inflammation, it has a diagnostic value in
many clinical situations and it has been used as an indicator of activity and clinical outcome in many studies.
We aimed to assess the impact of CRP levels on proteinuria, lipid parameters, EKO parameters and clinical outcome at patients with nephrotic syndrome in this study.
MATERIALS AND METHODS: The files of patients which hospitalized and treated with
diagnosis of nephrotic syndrome (1440 patients) in Nephrology Clinic of Dicle Universty Medical Faculty between years 2000 to 2010 were scanned in this study. The files of 104 patients (49 of them (37.5%) were male, and 55 (62.5%) women) with sufficent data were analyzed retrospectively. Demographic data of the patients, histological diagnosis, blood pressure examination during clinical admission, taken-off the fluid volume, hemoglobin, hematocrit, white blood cell, platelets, glucose, urea, creatinine, sodium, potassium, chloride, calcium, phosphorus, magnesium, uric acid, AST, ALT, LDH, ALP, GGT, cholesterol, triglycerid, HDL, LDL, albumin, total protein, fibrinogen, Ig G, Ig A, Ig M, C3, C4, ESR, CRP, esbach, urine density , urine leukocytes, urine erythrocytes, urine protein, thickness of left atrium, thickness of left ventricular posterior wall, thickness of interventricular septum and values of ejection fraction in EKO and the length of stay at hospital were examined as operating parameters. Patients were divided into two groups according to CRP levels (CRP reference range 0-5 mg / l) . Group 1, CRP level> 5mg / l, Group 2 CRP level ≤ 5mg / l from the cases. The data obtained were compared between the two groups. Moreover, patients were evaluated by looking at the CRP and other parameters and compared the relationships between them when they were admitted to the clinic and discharged.
RESULTS: After grouping according to the CRP values;
1 - The average age of patients, was 46.68 ± 20.34 years in the group 1, was 35.92 ± 16.25 years in the group 2 (p = 0.004).
2- The 24-hour urine volume which examinated when hospitalization (p = 0.003) and levels of calcium (p = 0.001), albumin (p = 0.001), total protein (p = 0.035), HDL (p = 0.038) and hemoglobin (p = 0.032) were significantly lower in group 1 according to group 2.
3 - There were high levels of statistical significance between age (p = 0.004), length of stay at the clinic (p = 0.030), creatinine (p = 0.009), LDH (0.006), platelet (0.005), ESR (p <0.001) , C4 (p <0.001), urinary protein (p = 0.038) and esbach (p <0.001) in group 1 according to group 2 . Although LDL(p = 0.051) was higher levels in group 1 according to group 2 but there was not statistically significant.
4 -There were not significant correlation between CRP levels and cardiac parameters measured with EKO (LAD, EA, SVPDK, EF)(p> 0.005).
5-We detected a positive correlation between CRP elevation and levels of urea (p = 0.015), creatinine (p = 0.003), LDH (p = 0.015), WBC (p = 0.004), ESR (p = 0.004), C4 (p = 0.023), urine leukocyte (p = 0.032), urine red blood cells (p = 0.041), 24-hour urine protein (p = 0.044) levels and negative correlation between CRP elevation and amount of 24-hour urine (p = 0.043) with correlation of CRP and other parameters.
CONCLUSION: The increase in the amount of proteinuria, worsening renal function, prolonged hospitalization, decrease in the value of serum albumin and daily urine volume between patients with nephrotic syndrome was higher in the group with high CRP values according to the group with normal CRPvalue.
We found a positive correlation between CRP and urea, creatinine, leukocytes, sedimentation rate, complement and esbach, a negative correlation between albumin and the amount of daily urine. Large-scale studies are needed to examine the relationship between CRP and proteinuria, disease activity, lipid parameters, echocardiographic parameters and clinical course in nephrotic syndrome in adult patients
TABLOLAR
Tablo 1: Yetişkinlerde nefrotik sendrom olarak ortaya çıkan ve sık rastlanan glomerüler hastalıklar
Tablo 2: WHO Lupus Nefriti Sınıflandırması
Tablo 3: Lupus Nefriti İçin Aktivite-Kronisite İndeksi Tablo 4: Gözden geçirilmiş SLE tanı kriterleri 1997
Tablo 5: SLE düşünülen bir hastada yapılması gereken rutin testler
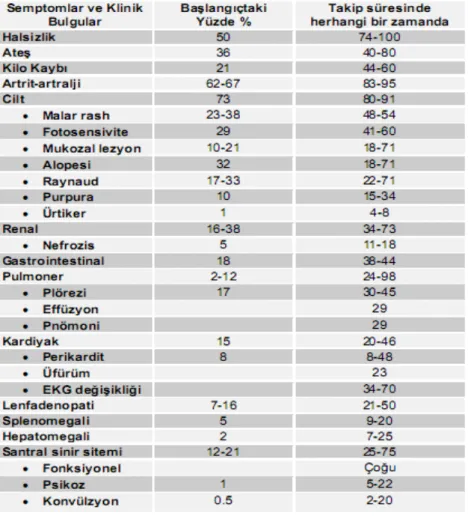
Tablo 6: SLE tanı kriterleri içinde yer alan klinik ve laboratuvar bulgularının hastalığın başlangıcı, tanısı ve takibindeki görülme yüzdeleri
Tablo 7: CRP’nin tanıda ve klinik izlemde faydalı olduğu durumlar Tablo 8: Grupların yaş ve cinse göre dağılımı
Tablo 9: Çalışma hastalarımızın nefrotik sendrom alt tiplerine göre dağılımı Tablo 10: Grup 1 de grup 2’ ye göre düşük saptanan parametreler
Tablo 11: Grup 1 de grup 2’ye göre yüksek saptanan parametreler
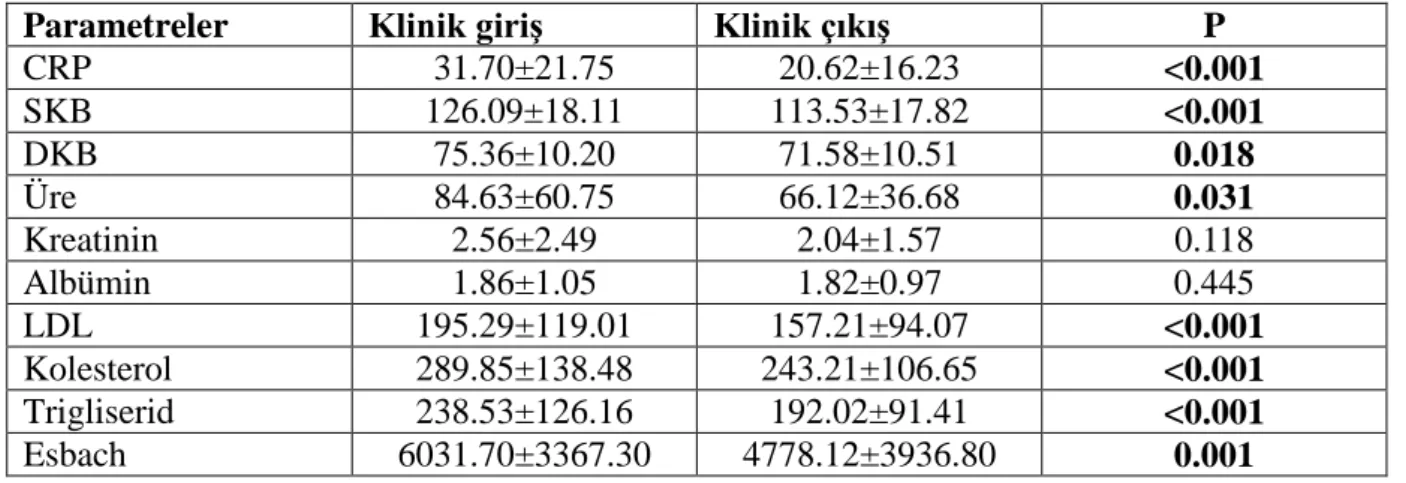
Tablo 12: Grup 1’in çalışma öncesi ve sonrası verilerinin karşılaştırılması Tablo 13: Grup 2’ nin çalışma öncesi ve sonrası verilerinin karşılaştırılması Tablo 14: CRP ile bağımlı ve bağımsız değişkenler arasındaki ilişki
Tablo 15: Gruplar arası EKO bulguları
ŞEKİLLER
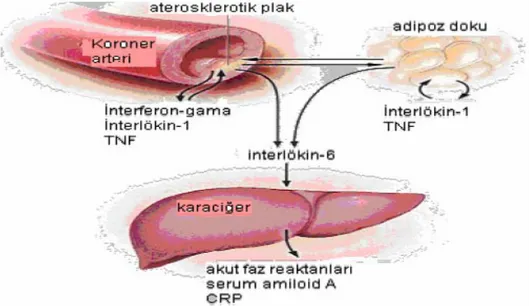
Şekil 1: Diyabetik nefropatinin patogenezi Şekil 2: Nefrotik sendrom patogenezi Şekil 3: CRP oluşumunda etkenler
KISALTMALAR
NS: Nefrotik sendrom CRP: C reaktif protein
AST: Aspartat aminotransferaz ALT: Alanin aminotransferaz ALP: Alkalen fosfataz
GGT: Gama glutamil transferaz LDH: Laktat dehidrogenaz Ig: İmmünglobulin C3: Kompleman 3 C4: Kompleman 4 C1q: Kompleman 1q TG: Trigliserit LDL: Düşük dansiteli lipoprotein HDL: Yüksek dansiteli lipoprotein VLDL: Çok düşük dansiteli lipoprotein SLE: Sistemik lupus eritematozus DM: Diyabetes mellitus
MDH: Minimal değişim hastalığı
MPGN: Mezengioproliferatif glomerulonefrit FSGS: Fokal segmental glomerüloskleroz MN: Membranöz nefropati
YBH: Yoğun birikim hastalığı IgAN: IgA nefropatisi
RPGN: Rapidly progressif glomerülonefrit KBY: Kronik böbrek yetmezliği
WHO: Dünya sağlık örgütü DNp: Diyabetik nefropati GFR: Glomeruler filtrasyon hızı SDBY: Son dönem böbrek yetmezliği HT: Hipertansiyon
TGF-β 1: Transforming growth factor-β 1 VEGF: Vascular endothelial growth factor GBM: Glomeruler bazal membran
ECM: Ekstrasellüler matriks AGE: Glikozillenmiş son ürün Ang-II: Anjiotensin 2
ET-I: Endotelin 1 IM: Işık mikroskobu EM: Elektron mikroskobu IF: İmmünfloresan
IL: İnterlökin
Th1: Yardımcı T lenfosit
TNF-α: Tümör nekrozis faktör α
ACEİ: Anjiotensin dönüştürücü enzim inhibitörleri ARB: Anjiotensin reseptör blokerleri
NSAII: Steroid olmayan antiinflamatuar ilaçlar AFR: Akut faz reaksiyonu
PAF: Platelet aktive edici faktör SKB: Sistolik kan basıncı DKB: Diyastolik kan basıncı LAD: Sol atrium çapı
SVPDK: Sol ventrikül arka duvar kalınlığı EF: Ejeksiyon faraksiyonu
MBL: Mannoz bağlayıcı lectin
TNFR-2: Tümör nekrozis faktör reseptör 2 ICAM-1: İntrasellüler cell adezyon molekülü 1
1.
GİRİŞ VE AMAÇ
Nefrotik Sendrom (NS) masif proteinüri, hipoalbuminemi, ödem ve hiperlipidemi ile karakterize bir tablodur. Amerika Birleşik Devletleri’nde çocuklardaki yıllık NS insidansının 2-2.7/100000, kümülatif prevalansının ise 16/100000 olduğu tahmin edilmektedir. Asyalı çocuklarda Avrupalı çocuklardan 6 kat daha fazla olduğu bildirilmektedir(1-4). NS primer (idiopatik) veya sekonder olarak sınıflandırılabilir ve her yaşta oluşabilir. Çocuklarda, NS’un primer şekilleri genellikle iyi prognozu olan minimal değişim hastalığı(MDH) ile beraber görülür. Bununla beraber, mezengioproliferatif glomerulonefrit(MPGN) ve fokal segmental glomerüloskleroz(FSGS) gibi diğer patolojik durumlarda kliniğe primer NS olarak yansıyabilirler(5). Membranöz nefropati(MN) beyaz ırkta en sık primer(idiopatik) nefrotik sendrom nedeni iken, FSGS siyah ırkta en sık primer nefrotik sendrom nedenidir(% 50-57) (6). FSGS son evre böbrek hastalığının belirgin bir sebebidir ve erişkinlerde %5, çocuklarda %15-20 son evre böbrek hastalığı nedenidir(5, 7). Amerika Birleşik Devletleri’nde DM en yaygın NS nedenidir. Tüm DM hastalarının yaklaşık üçte birinde 25 yıl içinde NS gelişir. Nefrotik sendroma neden olan diğer sistemik hastalıklar SLE, amiloidoz ve lösemidir(8,9).
NS genel olarak sporadik hastalık olarak düşünülmesine rağmen, bazı çalışmalarda genetik faktörleri de içeren değişik faktörlerle ilişkisi belirtilmiştir. NS’da otosomal dominant ve resesif kalıtım bildirilmiştir. Ailesel vakalar proteinürinin genetiği ve patobiyolojisini anlamamıza yardımcı olmuştur. FSGS’nin son zamanlarda bazı genler ile NS ilişkisi ve bazı kromozomal bölgelere bağlantı analizleri bildirilmiştir(10).
CRP insanlarda enfeksiyon ve doku zedelenmesine yanıt olarak akut ve hızlı yükselen majör bir akut faz reaktanıdır. CRP nonspesifik bir laboratuar bulgusudur ve enfeksiyon, doku hasarı ve inflamasyonun çeşitli şekillerinde hepatik yapımı tetiklenir. CRP düzeyi normal kişilerin çoğunda 2mg/l veya daha düşüktür. Standart yöntemlerle CRP’nin 3-8 mg/l düzeyleri tespit edilebilmektedir. Yeni “high sensitivity” (hs-CRP) yöntemleri ile CRP’nin bu değerlerden düşük düzeyleri de saptanabilmekte ve bugün risk belirlenmesinde hs-CRP ölçümleri kullanılmaktadır. CRP infalamasyonun özgün olmayan bir göstergesi olmakla birlikte, birçok klinik durumda büyük bir tanı değerine sahiptir (11). Bugün kabul edilen değerlere göre; düşük risk CRP < 1 mg/l, orta risk CRP= 1-3 mg/l, yüksek risk CRP> 3 mg/l dir (12,13,14). CRP birçok çalışmada çeşitli hastalıkların aktivite göstergesi ve klinik gidiş belirleyicisi olarak kullanılmıştır.
Biz bu çalışmada CRP düzeyinin nefrotik sendromlu hastalarda proteinüri, lipid parametreleri, EKO göstergeleri ve klinik gidiş üzerine etkisini değerlendirmeyi amaçladık.
2. GENEL BİLGİLER
2.1. NEFROTİK SENDROM
2.1.1. TANIM, TARİHÇE, İNSİDANS
Nefrozis veya NS terimi 20. yüzyılın başlarında kullanılmaya başlanmış ve öncelikle glomerüllerdeki hücresel proliferasyon ile ilişkili olarak hematüri ve proteinüri ile klinik bulgu veren nefrit ile ayırım için kullanılmıştır. Bu dönemde klinisyenler nefritik sendromun inflamatuar başlangıçlı, NS’nin ise dejeneratif süreçler sonrasında oluştuğunu öne sürerek bir ayırıma gitmişlerdir. Günümüzde NS, idrarda görülen protein seviyesinin bir günde her 1.73m2 vücut alanı için 3,5 gramı aştığı durum olarak tarif edilir (6).
NS kliniğine, ağır proteinüriyi takiben ortaya çıkan hipoalbuminemi ve ödem hakimdir. Bununla beraber hiperlipidemi, hiperkolesterolemi ve artmış lipidüri görülebilir. Hipertansiyon, hematüri ve azotemi NS’nin bir parçası olmasa da beraberinde eşlik edebilir. Bu durumda mikst nefrotik sendromdan bahsedilir. (4,6,8)
NS genel olarak bir glomerüler sebepten oluşur. Primer ve sekonder NS olarak iki alt grupta incelenebilir. Primer NS, bazı durumlarda eski bir terim olan idiopatik NS terimi ile yer değiştirmesine rağmen, her iki terim de nedene dair aynı belirsizliği gösterir. Her iki terim de birçok farklı klinik ve patolojik durumu ihtiva eder. Sekonder NS terimi ise klinik olarak daha kesin tarif edilmiş anaflaktoid purpura, sistemik lupus eritematozus, diabetes mellitus, orak hücre hastalığı, amiloidoz ve sifiliz gibi hastalık durumları ile ilişkili olduğunda kullanılır.
Genel olarak çocukluk çağı NS’nin prevalansı 100.000 çocukta 2–5 vakadır. Toplam prevalans oranı yaklaşık olarak 15.5/100.000 dir. On sekiz yaşından genç sağlıklı çocuklarda tahmin edilen yıllık insidans ise 100.000 çocukta 2–7 yeni vakadır. Hastalığın başlangıcının en sık olduğu yaş aralığı, nadir görülen konjenital NS’lar haricinde, 2 ile 3 yaş aralığıdır. Yaklaşık olarak etkilenmiş olan çocukların %50’si 1–4 yaş aralığındadır; %75’i ise 10 yaşından küçüktür (15). Minimal değişiklik hastalığı(MDH) çocukluk çağında en sık görülen alt grup olup, prevalansı başlangıç yaşı ile ters orantılıdır. Fokal segmental glomerüloskleroz(FSGS), erişkin idiopatik nefrotik sendromun en sık nedeni ve önemli bir
son dönem böbrek yetmezliği nedenidir. Amerika Birleşik Devletleri’nde diabetes mellitus(DM) en yaygın NS nedenidir. Tüm DM hastalarının yaklaşık üçte birinde 25 yıl içinde NS gelişir. Nefrotik sendroma neden olan diğer sistemik hastalıklar sistemik lupus eritematosus(SLE), amiloidoz ve lösemidir.(16,9)
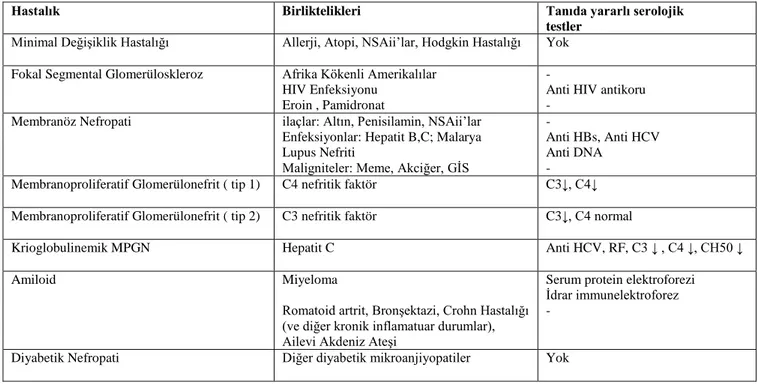
Tablo 1: Yetişkinlerde nefrotik sendrom olarak ortaya çıkan ve sık rastlanan glomerüler hastalıklar (18)
2.1.2. PATOLOJİ
Minimal değişiklik hastalığı (MDH), fokal segmental glomerüloskleroz (FSGS), membranöz nefropati(MN), membranoproliferatif glomerülonefrit (MPGN), diabetik nefropati, sistemik lupus eritematozus (SLE) ve amiloidoz erişkinlerdeki NS vakalarının >%90’ını oluşturur. Renal biyopsi erişkinlerde NS’ye yol açan hastalığın tanısını koymak, tedaviyi yönlendirmek ve prognozu değerlendirebilmek için önemli bir yöntemdir. Fakat çocukluk çağı NS vakalarının çoğundan MDH sorumlu olduğundan biyopsi öncelikle gerekli değildir.
Hastalık Birliktelikleri Tanıda yararlı serolojik
testler
Minimal Değişiklik Hastalığı Allerji, Atopi, NSAii’lar, Hodgkin Hastalığı Yok Fokal Segmental Glomerüloskleroz Afrika Kökenli Amerikalılar
HIV Enfeksiyonu Eroin , Pamidronat
-
Anti HIV antikoru -
Membranöz Nefropati ilaçlar: Altın, Penisilamin, NSAii’lar Enfeksiyonlar: Hepatit B,C; Malarya Lupus Nefriti
Maligniteler: Meme, Akciğer, GİS
-
Anti HBs, Anti HCV Anti DNA
- Membranoproliferatif Glomerülonefrit ( tip 1) C4 nefritik faktör C3↓, C4↓ Membranoproliferatif Glomerülonefrit ( tip 2) C3 nefritik faktör C3↓, C4 normal
Krioglobulinemik MPGN Hepatit C Anti HCV, RF, C3 ↓ , C4 ↓, CH50 ↓
Amiloid Miyeloma
Romatoid artrit, Bronşektazi, Crohn Hastalığı (ve diğer kronik inflamatuar durumlar), Ailevi Akdeniz Ateşi
Serum protein elektroforezi İdrar immunelektroforez -
2.1.2.1. Minimal Değişiklik Hastalığı(MDH) ve Fokal Segmental Glomerüloskleroz(FSGS):
Minimal değişiklik hastalığı ve FSGS tipik olarak NS ile kliniğe yansırlar ve sadece klinik bulgulara dayanılarak ayrılamazlar. Çocukluk çağında, NS’nin sıklıkla MDH’dan oluştuğu düşünülür ve bundan dolayı biyopsi sadece steroide cevapsız veya diğer NS’a yol açan hastalıkları düşündüren bulgular olduğu zaman yapılır. Erişkinlerde MDH, NS’ye sebep olan hastalıkların sadece %20’sini oluşturur. FSGS’nin insidansı giderek artmaktadır. MDH ve FSGS’de serolojik testler genelde normal sınırlardadır. Erişkinlerde ve steroide yanıt vermeyen çocuklarda NS’nin nedenini anlamak için biyopsi yapmak gereklidir.
MDH, isminden de anlaşılacağı gibi, ışık mikroskobik incelemelerde yapısal olarak normal görülen glomerüller ile karakterizedir. Spesifik damarsal veya tübülointersitisyel lezyon yoktur. Bununla beraber MDH, özellikli olmayan fokal tübülointersitisyel fibrozis ve hafif damar lezyonları (ateroskleroz, hipertansiyonla ilişkili arterioler hiyalinozis) olan orta yaşlı veya yaşlı erişkinlerde de görülebilir. Global glomerulosklerozun, segmental lezyonun tersine, MDH ile FSGS’nin ayırımında belirgin tanısal önemi yoktur. Global olarak skleroze olmuş glomerüller her yaşta normal olarak görülebilir ve bununda normal bir “kullanma ve eskime” sürecinin sonucu olduğu, dolayısı ile çoğu vakada özel bir oluşum mekanizmasının olmadığı düşünülür. Kırk yaşından genç insanlarda, tüm glomerüllerin yaklaşık %10’u tamamen skleroze olmuş olabilir. Yaşlanma ile beraber global skleroza giden glomerül oranı artar ve 80 yaşındaki insanlarda %30’a kadar varabilir.
MDH’de immunofloresan çalışmaları tipik olarak negatif sonuç verir. Bazı MDH biyopsilerinde görülen IgM boyanması tartışma konusudur ve bazı yazarlar bunu “IgM nefropatisi” olarak adlandırmaktadır.
MDH’de elektron mikroskopisindeki bulgular, podositlerdeki ayaksı uzantıların kaybolması, vakuolizasyon ve epitel hücrelerindeki mikrovillüs dönüşümüdür.
FSGS’de genellikle skleroz, glomerüllerin bir kısmında (fokal) ve etkilenen glomerüllerin de bazı bölgelerinde (segmental) görülür. FSGS’nin morfolojik tanısı bu görünümün ışık mikroskobundaki tarifidir. MDH ile FSGS’yi tanısal yönden ayırmak yeterli büyüklükteki örneğin incelenmesi sonucu ortaya konur. Tek bir segmental skleroze glomerül görülmesi FSGS tanısı koymaya yönlendirebilir. Bundan dolayı biyopsi yaparken alınacak küçük örnekler FSGS ile MDH’nin ayırımını zorlaştırabilir. Skleroz genellikle jukstameduller glomerüllerde başladığından örneğin içinde bu bölge mutlaka olmalıdır. Hastalık kliniği tam
oturduğunda dahi yapılan biyopsilerde skleroze olmamış glomerüller görülmüştür. Bu da hastalığın fokal doğasını göstermektedir.
Sklerotik lezyonların görülebilmesi güç olduğundan, skleroza götüren süreçlerin görülmediği glomerüllerdeki diğer tanısal özellikler, skleroze olamamış glomerüllerde dahi FSGS tanısını düşündürebilir. Anormal glomerüler genişleme, skleroz gelişmeden önce, sklerotik ilerleyişin erken belirtisi olabilir. Belirgin MDH yok ise, belirgin glomerüler genişleme FSGS’nin erken bir safhası olarak kabul edilebilir. Yaygın mezengial hipersellülarite, IgM birikimi olsun veya olmasın, tariflenmiş prognostik faktör olmamasına rağmen, MDH ve FSGS’de varolan değişikliklerin üzerine eklenmiş morfolojik bir özellik olabilir.
Segmental sklerotik glomerüldeki PAS pozitif asellüler maddenin mahiyeti, altta yatan farklı patofizyolojik mekanizmalara göre değişkenlik gösterebilir. Skleroza gidiş matriks artışı ile beraber giden glomerüllerdeki kapillerlerin kollapsı olarak tarif edilir ve erken küçük lezyonlardan tama yakın global skleroza varan değişimler gösterir. Segmental skleroz lezyonları ayrı ayrı yerleşmiş olup, glomerülün perihiler ve/veya periferal bölgelerinde yerleşim gösterebilirler. Buna eşlik eden, fakat tanısal değeri olmayan global glomerüler skleroz bulunabilir. Etkilenmemiş glomerüllerde ışık mikroskobu ile yapılan incelemede lezyon görülmez, fakat bu glomerüller genişlemiş olabilir ve bu glomerüllerin segmental sklerozun erken safhasında olduğu düşünülür. Glomerulosklerozun beraberinde, plazma proteinlerinin birikimi sonucunda oluşan düz ve camsı görünüm gösteren hyalinozis bulunabilir. Bu genellikle aksiyal, damarsal bölgede görülür. Arterioler hyalinozis hipertansif hasar sonrasında da oluşabileceğinden tek başına sklerotik lezyon kanıtı olarak düşünülmemelidir. FSGS’nin ilerleyişinin geç dönemlerinde damarsal kalınlaşma belirginleşebilir. Podositlerin bowman kapsülüne adhezyonları (sineşi) sklerozun erken belirtisi olabilir. Glomerüldeki etkilenmenin derecesi ile orantılı olarak, glomeruloskleroza tubuler atrofi ve interstisyel lenfositozlu intersitisyel fibrozis eşlik edebilir.
İmmunofloresan değerlendirmelerde, mezengial matriksin arttığı alanlarda veya sklerotik alanlarda özellikli olmayan IgM ve C3 tutulumu görülebilir. Elektron mikroskopisinde podositlerin ayaksı çıkıntılarında silinme FSGS’de tam değildir. Fakat bu silinmenin derecesi FSGS ile MDH arasında kesin ayırım yapmaya yardımcı olmaz. Ayaksı çıkıntıların olmaması FSGS tanısını düşündürebilir.
2.1.2.2. Membranöz Nefropati (MN)
Membranöz nefropati yaygın, global subepitelyal birikimlerden dolayı oluşur. Hastalığın erken zamanlarında damarlara daha sert bir görünüm veren bu özellik ışık mikroskobunda görülen tek belirti olabilir. Bazı kesitlerde Jone gümüş boyaması ile küçük berrak alanlar görülebilir. Bu da birikimlerin gümüş ile boyanmadığını gösterir. Bu berrak alanlar “Delikler” olarak adlandırılır ve MN’nin ışık mikroskobunda görülen en erken belirtisidir. Birikim varolduğu sürece, glomerüler bazal membran matriks reaksiyonu gümüş boya ile görünür hale gelen sivri çıkıntılar oluşturur. İlerleyen bazal membran reaksiyonu sonucunda, matriks, varolan birikimleri çevreler ve glomerül bazal membranda gümüş boya sonrası merdiven benzeri görünüm oluşur. Subepitelyal birikimlerle ilişkili morfolojik bulgular safhalara ayrılır.
Hilal görünümü oluşumundan skleroza varan farklı ek lezyonlar da olabilir. Segmental skleroz, intersitisyel fibrozis ve tubuler atrofi kötü prognozla ilişkilidir. Hilal görüntüsü membranöz glomerülopatide nadir olup, genelde lupusla ilişkili lezyonlarda görülür.
İmmunofloresan mikroskobunda subepitelyal birikimler kapiller duvar boyunca yaygın, global granüler pozitivite olarak görülür. İmmunofloresan mikroskopi, birikimlerin ortaya konmasında ışık mikroskobundan ve elektron mikroskobundan daha duyarlıdır. Evre 1’de bu birikimler ince granüler haldeyken, ilerleyen safhalarda kaba granüler halde gözükürler. IgG tipik olarak en baskın immunoglobulindir. C3 sıklıkla vardır. Ek olarak, mezengial birikimler idiopatik MN’de bulunmamasına rağmen, sekonder glomerulopatide tipik olarak vardır. IgA, IgM ve C1q varlığında sistemik lupus eritematozusa sekonder membranöz glomerulopati düşünülmelidir.
Elekton mikroskopisinde, MN’nin bulunduğu safhaya tekabul eden birikimler ile beraber farklı derecelerde glomerüler bazal membran reaksiyonu, birlikte görüntülenir. MN’de evre 1’in erken safhalarında, birikimler çok küçüktür ve gözle fark edilemeyebilirler. Birikimlerin etrafında glomerüler bazal membran reaksiyonu yoktur ve dolayısı ile sivri çıkıntılar ışık mikroskopisinde görülmezler. Evre 2’de belirgin oluşmuş sivri çıkıntılar mevcuttur. Evre 3’de birikimler glomerüler bazal membran reaksiyonu ile çevrelenmişlerdir. Evre 4’de birikimler absorbe edilmiş ve yerlerinde şeffaf alanlar bırakmışlardır. Visseral epitel hücrelerde ayaksı çıkıntılar silinip mezengial birikimler göründüğünde, membranöz glomerülopatinin sekonder nedenleri düşünülmelidir. Eğer endotel hücrelerinin sitoplazmalarında retiküler kümeler varsa, lupusla ilişkili glomerulopati düşünülmelidir.
2.1.2.3 Membranoproliferatif Glomerülonefrit(MPGN) A) MPGN Tip I (Mezengiokapiller)
MPGN tip I tipik olarak hipokomplementemi ile beraber nefritik ve NS’lerin karışımı olarak ortaya çıkar. Çoğunlukla çocuk ve genç erişkinde görülür. Erişkinlerde kronik bir inflamatuar duruma sekonder olarak gelişir. MPGN tip I’in insidansı çocuklarda son zamanlarda düşüş göstermektedir. MPGN Tip I hastalığı olan çocuklar bu hastalığa MPGN Tip II’li çocuklardan daha geç yaşta tutulmaktadır. C3 nefritik faktör varlığı ve aynı zamanda oluşan parsiyel lipodistrofi MPGN TipI’de Tip II’ye kıyasla çok nadirdir. Hastalarda tipik progresif böbrek hastalığı vardır. Hipertansiyon, azalmış böbrek fonksiyonları ve NS klinik açıdan kötü prognoz göstergeleridir. Tip I MPGN transplant hastalarının 1/3’ünde tekrarlar ve özellikle hilal oluşum bulgusu varsa allograft kaybedilir. MPGN’li trasplantta hepatit C infeksiyonu ve krioglobulinemi de de novo olarak gelişebilir.
Membranoproliferatif glomerulonefrit terimi, endokapiller proliferasyondan dolayı oluşan yaygın mezengial genişleme ve artmış mezengial matriks ve sıklıkla tramvay yolu görünümü veren kapiller duvarlardaki kalınlaşma ile karakterize hasarın ışık mikroskopideki görünümüdür. MPGN terimi, tercihen bu görüntü immun kompleks glomerulonefritleri sonucu oluşmuşsa kullanılır. Bazal membran ayrılması trombotik mikroanjiopatinin organize fazında, radyasyon nefritinde, kronik transplant glomerulopatide ve orak hücre hastalığında da görülebilir. Bu hastalıklarda ışık mikroskopi bulguları, her ne kadar MPGN’ye benzese de, immunofloresan bulguları ve elektron mikroskopi bulguları MPGN’deki immun kompleksleri ortaya koyar.
Membranoproliferatif glomerulonefrit, ışık mikroskop bulguları benzer olan 3 alt grupta incelenir. Mezengiokapiller glomerulonefrit terimi MPGN Tip I için kullanılmıştır. Bu tipte global, yaygın artmış mezengial matriks ve sellülarite ile beraber olan endokapiller proliferasyon ve lobuler basitleşme görülür. Artmış mononükleer hücreler ve nadir nötrofiller görülebilir. İdiopatik MPGN’de proliferasyon tipik olarak uniform ve yaygındır. Bazı vakalarda glomerüller daha sıkı/birleşik ve noduler görülebilir. Kapiller duvar kalınlaşmış ve gümüş boya ile çift hat görünümü verir. Bu görünüm subendotelyal birikimlerin varlığından dolayı olur. Sekonder MPGN’de hasar daha düzensizdir. Hilal oluşumu hem idiopatik, hem de sekonder formda görülebilir. Hilal oluşumunun %20’yi geçmesi kötü prognoz ile ilişkilidir. Birikimler glomerüler dışı alanlarda bulunmazlar. Zaman içinde lezyonlar ilerlerken, daha az hücresellik ve daha fazla matriks birikimi görülür. Glomerüler hasarla orantılı
tubulointersitisyel fibrozis ve vasküler sklerozis ilerleyen dönemde görülür. Tubuler atrofi ve intersitisyel fibrozis kötü prognozla ilişkilidir.
İmmunofloresan bulgular Tip I MPGN’de değişkendir. Tipik olarak, IgG, IgM ve C3 varlığı kapiller ve mezenkimde düzensiz ve topak topak dağılım gösterir. IgA birikimi vakaların küçük bir kısmında görülür. Özellikle sekonder MPGN’de C3 boyanması baskın olabileceği gibi, immunoglobulin boyanması yok olmuş olabilir. Periferal loop birikimleri tipik olarak sosis görünümündedir. Dış sınırları glomerüler bazal membranın altında kaldığından dolayı düzgündür.
Tip I MPGN’nin elekton mikroskopisinde subendotelyal ve mezengial bölgelerde çok fazla birikim görülür. Subendotelyal birikimler aslında sıklıkla glomerüler bazal membran içerisinde, tam olarak lamina densa’nın altında bulunur. Bundan dolayı daha doğru olarak intramembranöz tanımlaması yapılabilir. Müphem kurt yemiş görünümü veya mikrotubuler altyapı krioglobulin unsurunun varlığını düşündürür. Mezengial veya mononükleer hücrelerin sitoplazmik çıkıntılarının endotelyal hücre ve bazal membran ile karışmasını ifade eden mezengial karışım bulunmaktadır. Monosit karışımı krioglobulinemi ile ilişkili MPGN lezyonlarında özellikle yaygındır. Yeni oluşan kaidedeki materyalin tekrardan çoğalması hemen şişen endotel hücrelerinin altında gerçekleşir. Bunun üzerindeki visseral epitel hücreleri silinmiştir. Tip III MPGN’deki subendotelyal ve mezengial birikimlere ilaveten çok miktarda subepitelyal birikim de bulunur. Bu Tip I’den ayırıcı bir özelliktir.
B) MPGN Tip II (Yoğun Birikim Hastalığı)
Yoğun birikim hastalığı (YBH) MPGN tip I den farklı bir hastalık durumudur, fakat ışık mikroskobisi görünümleri aynı olduğundan MPGN tip II olarak da isimlendirilir. YBH tip I MPGN den çok daha nadir görülür ve tip I MPGN ve YBH vakalarının toplamının %15-35’ini oluşturur. YBH olan hastalar tipik olarak nefrotik/nefritik sendrom özellikleri, azalmış kompleman düzeyi (özellikle C3), hipertansiyon ve artmış serum kreatininin seviyesi ile tanınırlar. Klasik yolun erken komponentlerinin, C1q ve C4, serum seviyeleri genellikle normaldir. Bazı hastalarda YBH ile ilişkili lipodistrofi bulunur. Hastaların çoğu çocuk veya genç erişkinlerdir. Kadın ve erkekler eşit oranda etkilenir. Hastaların çoğunda yıllar içerisinde gelişen ilerleyici böbrek yetmezliği görülür. Nadir vakalarda spontan iyileşme literatürde bildirilmiştir. Hızlı ilerleme genelde hilal oluşumu ile ilgilidir. Klinik özellikler tek başına ilerleyişi tahmin etmemize yardımcı olmaz.
Işık mikroskobunda polimorf nükleer infiltrasyonunun eşlik ettiği endokapiller proliferasyon görülür. Fokal segmental nekrotizan proliferatif lezyonlarda görülebilir.
Glomerüler bazal membran kalınlaşmış, yüksek derecede refrakter ve eozinofiliktir. Glomerüler bazal membranın etkilenmiş kısımları sosis dizisine benzer. Birikimler PAS pozitiftir ve gümüş boya ile kahverengi boyanırlar. Tioflavin T boyası da, toluidin mavi boyasında olduğu gibi birikimleri gösterir. Kalınlaşma aynı zamanda tubuler bazal membranları ve Bowman kapsülünüde etkiler. Hilal oluşumları görülebilir.
Yoğun birikim hastalığında, immunofloresan kapiller duvar boyunca düz, granüler ve devamlılığı olmayan şekilde düzensiz C3 boyanması gösterir. Berrak granüler mezengial boyanma görülebilir. Genellikle immunoglobulin saptanamaz. Bu bulgu, yoğun birikimlerin klasik antijen antikor immun kompleksleri olmadığını gösterir. Bununla beraber segmental IgM veya daha az olarak IgG ve çok nadir olarak IgA bildirilmiştir.
Elektron mikroskopisinde, YBH’de bazal membranın lamina densası immun kompleks tipi birikimlerin olmadığı çok yoğun transformasyon gösterir. Benzer yoğun materyal çoğunlukla artmış matrikse ilaveten mezengial alanlarda da bulunur. Artmış mezengial hücresellik veya mezengial karışma, tip I MPGN’de olduğundan çok daha azdır. Visseral epitel hücreleri, vakuolizasyon, mikrovillüs dönüşümünden ayaksı çıkıntıların silinmesine kadar olan bir dizi reaktif değişim gösterir. Tubuler bazal membranlar ve Bowman kapsülünde de glomerüler bazal membranda görülen yoğunluk görülebilir.
2.1.2.4 IgA Nefropatisi
IgA nefropatisi (IgAN) renal biyopsilerde karşılaşılan en yaygın glomerulonefrittir. IgAN olan hastalar mikroskopik veya makroskopik hematüri, değişken proteinüri ile tanınırlar. Proteinüri nadiren nefrotik düzeye varır. Hastalık tüm yaş gruplarında görülebilir. Klinik bulgular, hastalığın prognozu hakkında faydalı bilgiler verir. Hipertansiyon, belirgin proteinüri, başlagıçta var olan artmış kreatininin seviyesi ve devamlı mikroskopik hematürisi olan yaşlı erkek hastalarda kötü prognoz görülür. Prognoz, hızlı progresyon gösteren ve uzun süreli takiplerde (yaklaşık 30 yıl) KBY gelişen hastalarda değişkenlik göstermektedir. Transplantasyona giden hastaların %60’ında nüks görülür fakat morfolojik nüks transplant kaybına götürmez.
IgAN’nin ışık mikroskobisindeki görünümü, minimal mezengial genişlemeden, hilal oluşumlu veya yaygın sklerozisli diffuz proliferatif lezyonlara kadar değişebilir. Sıklıkla mezengial hücreler, birikimler ve matriks artışından dolayı mesengial alanlarda artış görülür. Bazı vakalarda, birikimler gümüş boyası ile gümüş negatif alanlar olarak görülebilir. Endokapiller proliferasyon, birikimlerin periferal looplara yayılması ile ilişkili olarak fokal segmental veya diffuz şekilde, tipik olarak görülebilir. Bu birikimler glomerüler bazal
membranın ayrılmasına ve mezengial karışıma neden olur. Ağır vakalarda, segmental nekroz ve hilal oluşumu görülebilir. Kronik vakalarda, çoğunlukla segmental skleroz ile orantılı intersitisyel fibrozis ve tubuler atrofi görülür.
Geniş çaplı bir araştırmada, biyopsilerin %13’ünde sadece minimal mezengial genişleme, %6’sında diffüz mezengial hipersellülarite, %80’inde fokal segmental glomerüloskleroz ve/veya hilal oluşumu gösteren fokal segmental proliferatif lezyonlar, %1’inde ise son evre böbrek hastalığı görülmüştür. IgAN için WHO tarafından sistemik lupus eritamatozus nefriti için kullanılan sınıflamaya paralel ışık mikroskobisine dayalı sınıflandırmalar önerilmiştir.
Henoch-Schönline purpurası IgAN’nin sistemik karşılığı olarak düşünülebilir. İki hastalık böbreklerdeki lezyonları açısından ayrılamazlar. Ayırım, klinik patolojik özelliklere dayanılarak yapılır. Uluslararası Çocuklarda Böbrek Hastalıkları Çalışmasında IgAN sınıflandırması ile birçok benzerlik gösteren sınıflandırma Henoch-Schönline purpurası olan böbrek hastaları için kullanılmıştır.
İmmunofloresan mikroskopi IgA birikimlerinin kesin kartakteristik baskınlığını ortaya koyar. Bu birikimler mezengiumda sınırlı kalabilecekleri gibi, tipik olarak proliferatif lezyonlarla ilişkili olarak periferal kapiller yumağa da yayılabilirler. C3 hemen hemen değişmez olarak görülür, fakat C1q nadiren pozitiftir. IgA’nın immunofloresan pozitifliği ışıkmikroskopide görünüm her ne kadar fokal segmental olsa da diffüz ve globaldir.
Elektron mikroskobisi ile birikimler mezengial alanlarda paramezengial glomerüler bazal membranın altında bulunurlar. Mezengial matriks artmış olmakla beraber, mezengial hücresellikte de artış görülebilir. Subendotelyal birikimler endokapiller proliferasyonu olan vakalarda tipik olarak görülürler ve mezengial alanın dışına uzanırlar. Nadiren subepitelyal veya intramembranöz birikimler görülebilir. Podositlerin ayaksı uzantıları skleroz alanlarının olduğu bölgelerde kaybolmuştur.
2.1.3. SEKONDER NEFROTİK SENDROM NEDENLERİ
2.1.3.1. DİYABETİK NEFROPATİ
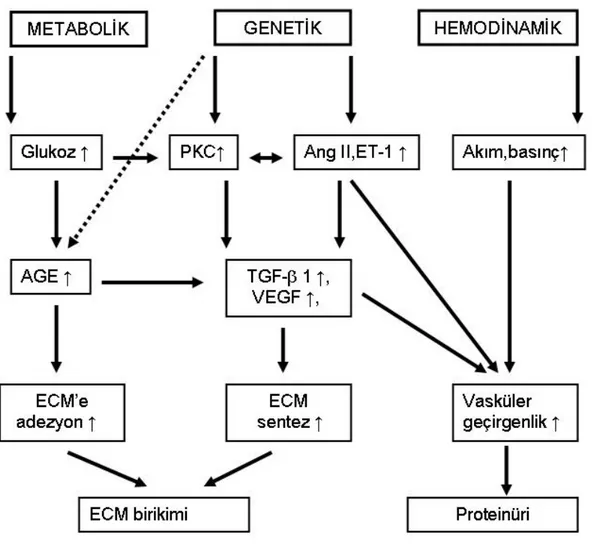
Diyabetik nefropati(DNp) olarak adlandırılan klinik sendrom, süreklilik gösteren mikroalbuminüri, erken kan basıncı yükselmesi, glomeruler filtrasyon hızında(GFR) düşme, yüksek kardiyovasküler morbidite ve mortalite riski ile karakterizedir (19). Tip 1 diyabetes mellitusa(DM) bağlı nefropati gelişen hastalarda %85-99, tip 2 olanlarda %63 oranında diyabetik retinopati de saptanmaktadır (20). Tip 1 diyabetiklerde, diyabet süresiyle ilişkili olarak artan mikroalbuminüri ve proteinürinin, 25-30 yıllık toplam insidansi %35-40 olarak bildirilmiştir (21). Mikroalbuminürik hastaların 1/3’ünde albumin atılımı normal sınırlar içine dönerken, 1/3’ünde aşikar proteinüriye ilerler (22,24). Proteinürik hastaların %10-50’sinde son dönem böbrek yetmezliği(SDBY) gelişirken, %40-50’si kardiyovasküler komplikasyonlarla erken dönemde kaybedilir (21). Tip 2 DM’li beyazlarda, DNp’nin gelişimi tip 1’dekiyle benzer bir seyir izlemektedir (21). Birçok çalışma mikroalbuminüri-proteinüri gelişme insidansının tip 1 ve 2 diyabetiklerde birbirine yakın değerlerde olduğunu ortaya koymuştur (26,27). Gelişmiş ülkelerde, yeni tanı almış SDBY nedenleri içindeki DNp oranı %30-40 civarındadır (28). Ülkemizde de 2005 Türk Nefroloji Derneği verilerine göre SDBY nedenleri arasında %25.3’lük oranla DNp birinci sırayı almaktadır (29). Genetik yatkınlık, ırk, cinsiyet, diyabetin başlama yaşı, hastalığın süresi DNp gelişimini etkileyen risk faktörleridir (29). Glisemik kontrol bozukluğu, hipertansiyon, hiperlipidemi, diyetteki yüksek protein, albuminüri varlığı, sigara kullanımı prognozu kötüleştirmektedir (30). Genetik yatkınlık varlığında, hemodinamik ve metabolik faktörler arasındaki karmaşık etkileşim DNp gelişimini kolaylaştırmaktadır (31). DNp patogenezinde, glukozun direkt toksik etkileri, polyol yolu aktivasyonu, protein-lipid-lipoprotein-aminoasitlerin glikozilasyonu ve ileri glikozilasyon ürünlerinin oluşumu, oksidatif stres, çeşitli büyüme faktörlerinin artmış aktivitesi ve renin anjiotensin aldosteron sistemi rol oynamaktadır (32). DNp gelişimi için hiperglisemi gerekli olsa da yeterli değildir; bazı hastalarda kötü glisemik kontrol olmasına rağmen nefropati gelişmez. Bu durum patogenezde diğer faktörlerin de rolünü ortaya koymaktadır (32). DNp gelişiminde hipertansiyon (HT) da kritik öneme sahiptir. Glomeruler kapillerlere geçen basınç destek hücrelerinde mekanik strese neden olur ve kollajen gibi matriks elemanlarının sentezini uyarır (32). Hem hiperglisemi hem de mekanik stres önemli bir intraselüler medyatör olan protein kinaz C (PKC) aracılığıyla sitokinler ve büyüme faktörlerini [örneğin transforming growth factor-β 1 (TGF-β 1) ve vascular endothelial growth
factor (VEGF)] stimüle ederek hücre içi sinyal yollarını aktive eder (32). Şekil 1’de DNp’nin patogenezi özetlenmektedir. Hipergliseminin ortaya çıkmasıyla başlayan DNp gelişim süreci ilk aşamalarında klinik bulgu vermeyebilir. DNp gelişim süreci 5 evrede incelenmektedir (29):
• Evre I (hiperfiltrasyon): GFR normal değerin %20-40’ı oranında artmıştır. Nefronlarda hipertrofi ve hücre proliferasyonu gelişmiş olup idrarda mikroalbumin saptanmamaktadır. • Evre II (sessiz dönem): GFR, hiperfiltrasyon evresine göre azalmış olmakla birlikte halen normalin üzerinde veya normaldir. Glomeruler bazal membran (GBM) da kalınlaşma ve mezangial matrikste artış vardır.
• Evre III (gizli nefropati): İdrarla albumin atılımı 30-300 mg/gün arasındadır. GFR yılda yaklaşık 1.1 ml/dk azalır. Tip 2 DM hastalarının çoğu tanı konduğunda bu dönemdedir. • Evre IV (aşikar nefropati): Günde 300 mg’ı aşan albuminüri ve 500 mg’ı aşan proteinüri vardır. Bu evrede GFR yılda 10-12 ml/dk azalır. Hastaların çoğu hipertansiftir. HT varlığı prognozu kötüleştirir.
• Evre V (son dönem böbrek yetmezliği): Tip 1 DM hastalarının %50’si, tip 2 DM hastalarının ise %20-30’u, 10 yıl içinde evre IV’ten V’e ilerler. Bu dönemde hastaların renal replasman tedavisine gereksinimi vardır.
Şekil 1: Diyabetik nefropatinin patogenezi (29) 2.1.3.2.RENAL AMİLOİDOZİS
Klinik
Sistemik amiloidozisin zaman zaman ilk göstergesi ve aynı zamanda da en önemli morbidite ve mortalite sebebi olan renal tutulum, AL amiloidoziste sıklıkla, AA amiloidozis ile de hemen her zaman görülmektedir (34). Renal tutulum gösteren diğer sistemik amiloidozis tipleri ApoA1, ApoA2, fibrinojen ve lizozim amiloidojenik proteinleri ile oluşan herediter amiloidozislerdir. ATTR amiloidozis tipik olarak böbreği tutmaz (35,36). Sistemik amiloidoziste tutulan organ spektrumunu dolayısıyla böbrek tutulumunu belirleyen faktörler net olarak bilinmemektedir. Bununla birlikte ailesel ATTR amiloidoziste Val30Met mutasyonu nöropatik tutulum oluştururken Val122Ile mutasyonunda kardiyak tutulum ön plandadır (37). AApoA1’de ise özellikle bazı amino asit sekanslarının renal tutulumu belirlediği bildirilmiştir (38). Renal amiloidozisin insidansı hakkında Chugh ve arkadaşlarının
bir çalışmasında 6431 postmortem biyopside %1.01, 1980 renal biyopside %8.4 oranında bulunmuştur. İtalya ve İspanya’da yapılmış çalışmalarda ise tahmini renal amiloidozis insidansı yılda milyon popülasyonda 2.1 ve 3.3 olarak tespit edilmiştir (39, 40).
Olgular çoğunlukla nefrotik sendroma bağlı ödem, renal disfonksiyon hatta renal yetmezlik bulguları ile gelmektedir (39). Geniş bir seride, AA amiloidozisli hastaların %97 si proteinüri ile %11’i renal yetmezlik ile başvurmuş; %33’ü takip sırasında renal yetmezlik tablosu oluşturmuş; %44’ü de bu nedenle yaşamını yitirmiştir(41). 20 g/gün üzerine çıkan proteinüri görülebilmektedir. Diüretiğe refrakter şiddetli ödem dışında diğer bulgular arasında halsizlik, hepatosplenomegali, kalp yetmezliği, kilo kaybı sayılabilir. AA amiloidozis için 9 ila 87 yaş gibi geniş bir yaş aralığı bulunmakla birlikte, ortanca yaş 50 dir (41, 42, 43). Küçük yaşlarda herediter komponent akılda bulundurulmalıdır (44). Amiloidojenik hastalığın süresi genellikle 5 yılın üzerindedir. Böbrek biyopsisinde amiloid yükünün yaygınlığı ve renal klinik bulguların şiddeti arasındaki ilişki henüz açık bir şekilde gösterilememiştir. GFR deki azalma ve proteinüri miktarı biyopsi bulguları ile net olarak açıklanamamaktadır.
Morfoloji
Otopsi çalışmalarında amiloid ile infiltre olmuş böbrekler normalden büyük ve ağır olarak izlenmektedir; bununla birlikte normal boyutlardaki böbrek amiloid tanısını ekarte ettirmez (45). Kesit yüzleri soluk ve balmumu görünümündedir. İronik olarak böbrek ağırlıkları ve büyüklüleri amiloid yükü ile ters orantılı bulunmuştur ki bu böbrek boyutunun ana belirleyicisinin parenkimal atrofi olduğunun bir göstergesidir (46). Mikroskopik olarak amiloid, amiloid tipinden bağımsız olarak tüm renal kompartmanları ilgilendirir şekilde depolanmaktadır. Amiloid, hematoksilen eozin boyalı preparatlarda amorf, soluk eozinofilik hyalen materyal olarak görülmektedir; gümüş boyanmazken, PAS ile zayıf ve trikrom ile amfofilik özellikte bir boyanma mevcuttur. Depolanma mezangiumdan başlamaktadır; ilerleyen safhalarda periferal kapiller duvara doğru ilerlemekte ve sonunda tüm glomerülü doldurmaktadır (34). Yapılan çalışmalarda glomerüler amiloid depolanma paterni, temelde benzer nitelikte olmakla birlikte 2 farklı şekilde kategorize edilmektedir: 1) Diffüz, nodüler ve mikst tip (46,47); 2) Mezangial, nodüler, mezangiokapiller ve hiler (48,49). Nadir olarak bazal membran rüptürüne bağlı olarak kresent formasyonları (50,51), amiloide karşı gelişen inflamatuar reaksiyon (48) ve dev hücre reaksiyonu (52) görülebilir. Tübülointerstisyal alanda amiloid depolanması değişken şekilde karşımıza çıkmaktadır. Watanabe ve Saniter, olguların %46.7’sinde tübüller ve vaza rekta çevresinde amiloid birikimi saptamıştır (52). Diğer bir çalışmada ise olguların %66.2’sinde peritübüler kapiller ve/veya tübüler bazal
membran depolanması saptanmıştır (48). Bazı nadir amiloidozis tiplerinde (örneğin AApoA1) interstisyal birikimin glomerüler birikimden daha fazla olduğu bildirilmiştir (53, 54). Tübülointerstisyal birikimin ön planda olduğu olgularda proteinüri minimal olup renal yetmezlik daha erken ortaya çıkmaktadır (36). Köpüksü makrofajlar özellikle yüksek proteinüri seviyesi olan hastalarda görülmektedir (52). Renal vasküler sistem, sistemik amiloidozisten yaygın ve şiddetli olarak etkilenen kompartmandır. Öncelikle arterioller olmak üzere arterler, peritübüler kapillerler ve venler sırasıyla etkilenmektedir (52). Renal vasküler depolanma bazı olgularda glomerüler ve interstisyal birikimden daha az olabildiği gibi bazı hastalarda da nadir olarak sadece damarlarda amiloid birikimi saptanabilir (48, 55). Glomerüler depolanmanın masif olduğu durumlarda vasküler depolanma da genellikle ileri derecededir.
Prognostik faktörler
Renal amiloidozun öncelikli prognostik belirteci amiloid tipidir. Amiloid tipi sadece prognozu değil tedavi hedefini ve sürecini de etkilemektedir. AL amiloidozis sistemik amiloidozların en kötü prognozlu olanıdır. 10 yıldan daha uzun yaşayan hastalar da bildirilmesine karşın bu hasta grubu AL amiloidozis in %5’lik bir alt grubunu oluşturmaktadır; AL amiloidoziste ortanca yaşam 13 ay, Melfalan ve steroid tedavisine rağmen 17-18 aydır (51, 56). Prognostik faktörler arasında en önemlisi kardiyak tutulum ve neticesinde gelişen konjestif kalp yetmezliğidir. Amiloid infiltrasyonu nedeniyle kalp yetmezliği oluşan hastalarda aritmi gelişmekte ve çoğu hasta 3 ay içinde kaybedilmektedir. Diğer kötü prognostik faktörler arasında ileri yaş, serum kreatininin seviyesinin 2 mg/dl’den fazla olması, multiple myeloma tanısı, periferik nöropati varlığı sayılabilir (34,56, 57). AL amiloidozis hastalarında izlenen masif proteinüri tedavi ile %10-50 arasında değişen oranlarda gerilemektedir (56, 58). Bununla birlikte hastalar ortalama 13 ayda son dönem böbrek hastalığı nedeniyle diyalize girmekte ve bundan sonra ki ortanca yaşamları ancak 8 ay olmaktadır (59). AA amiloidoziste prognozu belirleyen faktör renal tutulumun boyutudur. Daha eski serilerde AL amiloidozise benzer sağkalım sergileyen AA amiloidoziste, son zamanlarda altta yatan infeksiyöz ya da inflamatuar hastalıkların tedavi edilmesi ile sağkalımın iyileşmesi sağlanmıştır. Hastalığın takibi serum amiloid A seviyesi ya da SAP sintigrafisi ile yapılmaktadır (60). Mortalite, amiloid yükü ve renal prognoz serum amiloid konsantrasyonu ile koreledir; bu nedenle erken tanı kritiktir (41). İleri yaş, düşük serum albumin seviyesi ve renal yetmezlik ile prezantasyon kötü prognoza işaret eder. Yapılan bir araştırmada romatoid artritli hastalarda verilen tedavilere rağmen son dönem böbrek
hastalığının engellenemediği de bildirilmiştir (61). Herediter amiloidozislerin böbrek üzerine olan etkileri değişkenlik göstermektedir. Herediter amiloidozisler arasında en sık görülen AFib amiloidoziste hızlı bir renal kayıp söz konusu iken, AApoA1 ve ALys daha yavaş seyirlidir (53, 62, 63,64).
2.1.3.3.SLE NEFRİTİ:
Böbrekler, sistemik lupus eritematozus (SLE)’da en sık etkilenen organlardır. Böbrek
yetmezliği veya nefrotik sendrom gelişene kadar hastalarda renal tutulum belirti vermez. 1997’de yeniden düzenlenmiş SLE klasifikasyon kriterlerinde 24 saatlik idrarda 0.5 gramın üstünde proteinüri veya eritrosit, granüler, tübüler veya mikst silendirler olması renal hastalık olarak kabul edilmiştir. Enfeksiyon yokluğunda hematüri (>5 eritrosit/hpf) veya piyüri (>5 beyaz küre/hpf) veya ikisinin birlikte olması ve serum kreatinininde yükselme klinik böbrek hastalığının bulgusudur(65). Işık mikroskopisine ek olarak elektron ve immünfloresan mikroskopla yaklaşık tüm lupuslu hastaların böbrek biyopsisinde değişiklikler saptandığı bildirilmiştir(66). Renal yetmezlik, ortalama % 50 hastada mikroskopik hematüri, proteinüri, hipertansiyon, azotemi, trombositopeni, hipokomlemantemi bulguları ile akut nefritik veya
nefrotik sendrom veya rapidly progressif glomerülonefrit şeklinde semptomatik hale gelir. Persistan C3 veya CH50 kompleman düşüklüğü bazı hasta gruplarında böbrek hastalığının
progresyonuyla ilişkili bulunmuştur (67,68).
Rapidly progressif glomerülonefrit gibi klasik klinik bulguları olan vakalarda lupus nefriti tipini belirlemek için renal biyopsi ihtiyacı olmayabilir. Fakat lupus nefritine benzer klinik bulguları olanlarda renal biyopsi tanı ve tedaviye açıklık getirebilir. Anlamlı proteinüri ve idrar sedimenti anormallikleri olmadığı durumlarda ise ranal biyopsi önerilmez(69).
Dünya sağlık örgütü lupus nefritini ışık, immünfloresan ve elektron mikroskobu bulgularındaki değişikliklere göre sınıflandırmıştır(Tablo 2). En sık klas IV diffüz proliferatif glomerülonefrit görülürken, klas II ve klas V benzer sıklıklarda bunu takip etmektedir.
Tablo-2 WHO Lupus Nefriti Sınıflandırması Klas IA Normal veya minimal hastalık
Bütün tekniklerle bulgu yok
Klas IB IM ile normal, EM ve IF ile depozit (+) Klas II Pür mezengiyal değişiklikler
Klas IIIA Fokal segmental glomerülonefrit Klas IIIB Fokal proliferatif glomerülonefrit Klas IV Diffüz proliferatif glomerülonefrit Klas V Diffüz membranöz glomerülonefrit Klas VI İlerlemiş sklerozan glomerülonefrit
Lupus nefriti hastalarında hipertansiyon, renal hastalığın progresyonu ve mortalite ile ilişkilidir(70). Nefrit süresinin veya renal fonksiyonlardaki değişiklik oranının detaylı kaydedilmesi, reversibl ve irreversibl değişikliklerin saptanmasında önemli bir parametredir(71). Birçok çalışmada prognostik faktörler olarak bilinen aktif histolojik bulguların (sellüler kresentler, fibrinoid nekroz, subendotelyal immün depozitler) kronik irreversibl morfolojik belirtilerle (interstisiyel fibrozis, tübüler atrofi ve glomerüler skleroz) kombine olduğu görülmüştür(72).
Austin ve arkadaşlarının yaptığı çalışmada genç yaş, erkek cinsiyet ve artmış serum kreatininin düzeyi, böbrek yetmezliği ile ilişkili bulunmuştur(73). Bu model renal kronisite indeksini de içererek güçlenmiştir. Nossent ve arkadaşları, kronisite indeksinin > 3 olmasını, özellikle genç hastalarda renal sağ kalımın azalmasında en önemli faktör olarak değerlendirmişlerdir(Tablo 3)(74)
SLE ve immün sistem
Sistemik lupus eritematozus(SLE); multifaktöriyel patogeneze sahip,ortaya
çıkmasında çeşitli etkenlerin rol aldığı sebebi bilinmeyen multisistemik bir hastalıktır. Genetik bir predispozisyonun olduğu kabul edilmektedir. Bu temelde çeşitli çevresel faktörlerin etkisi ile sitokin profilinde değişikliklerin olması, normal immün yanıtı otoimmüniteye doğru değiştirir. IL-10’un SLE patogenezinde önemli role sahip olduğu, immün yanıtı hümoral immüniteye doğru yönelttiği ve apoptozisi önlediği ileri sürülmektedir (75). Diğer bir sitokin olan IL-12’nin immün yanıtı Th1’e doğru yönelttiği ve SLE gelişiminde önemli olduğu bildirilmektedir. SLE, B lenfositlerinin poliklonal aktivasyonu ve bunun sonucu olarak çok sayıda otoantikorun sentezi ile karakterize bir hastalıktır. Bu otoantikorlar ve oluşan immün kompleksler doku hasarı ve vaskülit ile sonuçlanabilir. Otoantikor yapımındaki artış, B hücrelerini aktive eden faktörlerin artışına ve/veya baskılayıcı hücre fonksiyonlarının azalmasına bağlı olabilir. IL-6, B lenfositlerinin farklılaşmasını ve antikor sentezleyen hücrelere dönüşümünü sağlayan sitokinlerin en önemlisidir. Otoantikor sentezinde yardımcı olacak Th1 lenfositlerinin de proliferasyon ve stimülasyonunu arttırır. IL-6’nın yanısıra, diğer proinflamatuar sitokinler de SLE’deki sistemik immün yanıttan sorumlu gibi görünmektedir. TNF-α, IL-1 ve bu sitokinlerin aktivitelerini inhibe eden solubl reseptörleri ile hastalık aktivitesi arasında ki ilişkiyi arayan birçok araştırma vardır ve birbirinden çok farklı sonuçlar bildirilmektedir.
En yaygın kullanılan akut faz yanıtı proteinlerinden CRP ölçümlerinin SLE’li hastaların takibindeki değeri tartışmalı bir konudur. Çeşitli çalışmalar, sedimentasyon hızı yüksek ve klinik olarak aktif hastalarda dahi CRP’nin ılımlı yükseldiği yada normal düzeyde kaldığını göstermektedir(76,77). Bununla birlikte, lupuslu hastalarda bakteriyel enfeksiyonlar sırasında CRP düzeylerinin anlamlı yükselmesi, hepatositlerde intrensek bir defekte bağlı olarak akut faz proteinlerinin sentezini indükleyen sitokinlere karşı bir yanıtsızlık olduğu iddialarını ortadan kaldırmaktadır. Bu yükselmeler bazen SLE de enfeksiyonların ayırıcı tanısında yardımcı olmaktadır(78). CRP’nin SLE ‘li hastalardaki yarı ömrü, sağlıklı kişiler kadardır. Yani bu hastalardaki düşük CRP düzeylerinden, CRP klirensinin veya katabolizmasının artışı sorumlu değildir. Diğer akut faz proteinlerinin de hastalığın aktivasyonu ile paralel gitmediği eski çalışmalarda bildirilmektedir (79). SLE’deki akut faz yanıtının hastalıktaki yaygın immün hasardan beklendiği ölçüde yüksek olmaması, sitokin örneğinin diğer bağ dokusu hastalıklardakinden farklı olması olasılığını akla getirir. Diğer bazı araştırmacılar ise,
bakteriyel enfeksiyonların yokluğunda dahi aktif hastalarda CRP düzeylerinin yükseldiğini bildirmektedirler(80).
Tablo 5. SLE düşünülen bir hastada yapılması gereken rutin testler (82)
Tablo 6. SLE tanı kriterleri içinde yer alan klinik ve laboratuvar bulgularının
2.1.4. NEFROTİK SENDROM PATOGENEZİ
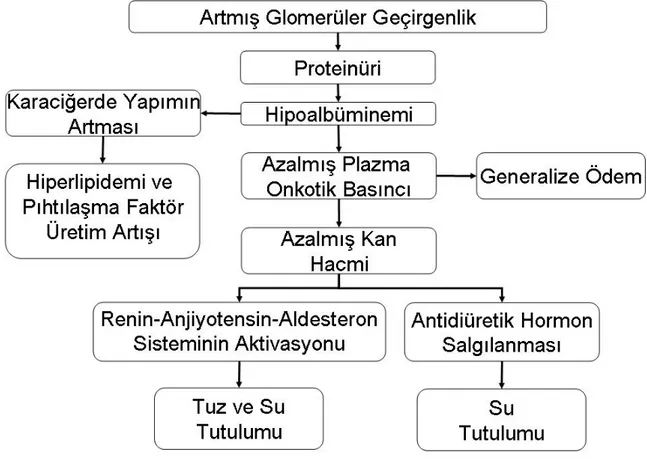
Nefrotik sendromlu vakaların %90’ından yedi hastalık sorumludur. Bunlar MDH (erişkin vakaların %20’si, pediatrik vakaların %80’i), FSGS, MN, MPGN, diabetik nefropati, SLE ve amiloidozdur. Bu hastalıkların her biri, yarıgeçirgen özelliği olan glomerüler duvarın geçirgenliğini arttırırlar. Glomerüler bazal membrandaki ve ayaksı çıkıntılardaki değişimler, proteinlerin glomerüllere ve oradan da idrara atıldığı toplayıcı tübüllere geçmesine neden olur (Şekil 2).
Hipoproteinemi, proteinüriden dolayı olur. Globulinler gibi diğer proteinlerin de idrarla
birlikte kaybedilerek serum seviyelerinin düşmesine rağmen, hipoalbüminemi ana bozukluktur. İdrarla protein kaybı günde 10 gramı aşarak, karaciğerin yeni albumin sentez kapasitesinin (12–14 gram/gün) üzerine çıkabilir.
Ödem, hidrostatik basınç ile onkotik basınç arasındaki denge bozulduğunda oluşur.
Normalde damarsal ağacın arteriol kısmındaki hidrostatik basınç yüksek olduğundan, intravasküler sıvıyı interstisyel sahaya iter ve venlerdeki kolloid onkotik basınçta bu sıvıyı vasküler sahaya çeken artmış bir basınç oluşturur. Serum protein seviyesi düştüğünde, sıvı interstisyel sahada kalır. Ödem hidrostatik basıncın yüksek (sarkık bölgeler), interstisyel basıncın düşük olduğu yerlerde (periorbital bölge) oluşur. Sıvı hareketi interstisyel sahaya doğru olsa da, NS’lu hastaların yaklaşık yarısında normal veya artmış plazma hacmi görülür. Sodyum ve suyun böbreklerde tutulması bu artan hacmin bir kısmını oluşturabilir; ancak diğer faktörler de göz önünde tutulmalıdır. Normal veya artmış plazma hacmine neden olan diğer faktörler şunlardır: 1. Belli bir eşikte aşırı sıvıya direnç gösteren göreceli nonkompliant interstisyum, 2. Sıvının vasküler boşlukta kalmasını sağlayan lenf akımının artması sonucu, interstisyel sahadaki proteinlerin taşınarak, onkotik basıncın vasküler sahadaki onkotik basıncın altına düşürülmesi, 3. Hipoalbüminemide albümine karşı kapiller geçirgenliğin azalması.
Hiperlipidemi, serum albümin konsantrasyonu ile ters orantılıdır. Azalan plazma
albümin seviyesi veya azalan plazma onkotik basıncı nedeni ile karaciğerdeki artmış kolesterol, trigliserit ve lipoprotein yapımı hiperlipidemiye neden olur. Bununla beraber bu maddelerin katabolizmalarında da azalma görülebilir. Lipidüri hiperlipidemiden dolayı oluşur, fakat lipidürinin miktarı idrarla atılan protein miktarı ile daha yakın paralellik gösterir.
Hiperkoagülabilite, pıhtılaşma faktörlerinin değişen seviyelerinden dolayı olabilir.
yapıma bağlı hiperfibrinojenemi, bozulmuş fibrinoliz ve trombositlerin artan agregat oluşturabilirliği; NS’lu hastalarda görülen artmış tromboembolik olaylara neden olur.
Nefrotik sendromlu hastalarda immun sistemin kompetansında azalma bildirilmiştir. Hücre aracılı immunite, hipoalbüminemi, hiperlipidemi veya çinko yetmezliğinden dolayı baskılanmıştır. Genel olarak NS hastaları infeksiyona yatkındırlar.
Nefrotik sendromda, idrarla kaybedilmesinden dolayı triiodotironin ve tiroid bağlayıcı globulin seviyeleri düşmüştür. Eser metaller, demir, bakır ve çinko yetmezliği görülür. Kolekalsiferol (vitamin D prekürsörü) kaybı, vitamin D yetmezliğine ve sekonder hiperparotiroidi, hipokalsemi ve renal osteodistrofiye yol açar. İlaç metabolizması da protein bağımlı olduğundan genellikle NS’lu hastalarda değişmiştir.
2.1.5. KLİNİK VE TANI 2.1.5.1. Klinik tanı kriterleri Nefrotik sendromun tanı kriterleri: 1. Generalize ödem,
2. Globuline oranla orantısız şekilde düşük albuminin görüldüğü hipoproteinemi (<2g/dl veya 20g/L),
3. Proteinüri; > 3.5 gr/1.73 m2/24 saat
4. Hiperkolesterolemi (>200mg/dl veya 5.17 mol/L) dir(15).
Azalmış serum albumin düzeyi, plazma onkotik basıncında belirgin düşmeye neden olur. Sonuç olarak, dolaşım hacmi interstisyel sahaya doğru kaybedilir ve generalize ödem oluşur. Başlangıçta şişme yüzde (özellikle periorbital bölgede) ve pretibial bölgede görülmekle beraber skrotum ve labialarda da belirgin şişmeler oluşur. Düşen onkotik basıncın ilave bir sonucu da, abdominal ağrıya yol açabilen dalak kapiller yatağının azalan perfüzyonudur. Bunun dışında takipne ve göğüs ağrısına yol açan plevral efüzyon ve pulmoner ödem meydana gelebilir(15).
Serum kolesterol, TG ve lipoprotein kolesterol seviyeleri yükselmiştir. Bu durum tam anlaşılamamıştır. Çok düşük yoğunluklu lipoprotein (VLDL) ve LDL kolesterol düzeylerindeki artış karakteristiktir. VLDL’deki artış karaciğerdeki yıkımın azalmasındandır ve neticede dolaşımdaki TG ve kolesterol düzeyleri artar. LDL kolesterol ise suni olarak artmış bir orandan dolayı yükselir(15).
2.1.5.2. Laboratuar bulguları
Nefrotik sendromun ana laboratuar bulgusu 24 saatte 3.5 gr’ı aşan belirgin proteinüridir. Atılan proteinin çoğu albumin olmakla beraber, immunoglobulinler de kaybedilir. Komplike olmamış NS’lu vakaların büyük kısmında mikroskobik hematüri görülmesine rağmen, proteinüri varlığında makroskobik hematüri görmek nadirdir. Gros hematürisi ve proteinürisi olan vakalarda IgA nefropatisi tanısı dikkate alınmalıdır(15). Klinik ödem varlığında, serum protein ölçümü düşük düzeyler gösterir (serum albumin seviyesi yaklaşık 2g/dl dir). 0.5g/dl gibi düşük albumin düzeyleri görülebilir ve albumin/globulin oranı sıklıkla <1’dir. Protein düşüklüğüne bağlı olarakta sıkça total ve iyonize kalsiyum değerlerinde düşüklük olan hipokalsemi görülür, fakat klinik olarak bulgu vermez(15). Nefrotik sendromlu hastalarda hipokalsemiden daha önemli olarak, özellikle yüksek moleküler ağırlıklı pıhtılaşma faktörlerinin konsantrasyonunda artış gözlenir. Trombin
miktarı artarken, dolaşımdaki trombosit adhezyon baskılayıcılarının miktarı ve fibrinolitik aktivite düşer. Bu değişimlerin neticesi olarak ve intravasküler hipovolemininde varlığında, etkilenmiş hastalarda artmış tromboz riski vardır. Kan IgG seviyeleri de düşmüştür. Buna ilave olarak tedavi için eklenen steroidler enfeksiyon riskini arttırır(15).
Azalan intravasküler hacimden dolayı oligürik olan vakalarda hiperkalemi gelişme yatkınlığı vardır. Diüretiklerin kullanımı, elektrolit dengesizliğini arttırabilir ve tedavi esnasında yakın monitorizasyon gerekir.
2.1.6. TEDAVİ
Nefrotik sendrom tedavisi şu noktaları içerir:
1. Altta yatan morfolojik özelliğin ve mümkün olduğu zaman sebep olan hastalığın spesifik tedavisi,
2. İmmunosupresif tedavi ve diğer spesifik tedbirlerle kontrol altına alınamayan proteinüriyi kontrol altına alabilmek için genel önlemler,
3. Nefrotik komplikasyonları önlemek için genel önlemler. (9)
Genel önlemler, immunosupresif tedaviye, özellikli önlemlere yanıt vermeyen ve ilerleyici böbrek yetmezliğine giden veya ağır nefrotik komplikasyonları olan hastalarda proteinüriyi kontrol edebilir. Proteinüriyi azaltacak özellikli olmayan önlemler diette protein kısıtlaması, anjiotensin dönüştürücü enzim inhibitörleri (ACEİ) ve anjiotensin reseptör blokerleri (ARB) ve steroid olmayan antiinflamatuar ilaçlardır (NSAII). Bu tedbirlerin ilk ikisinin amacı proteinüriyi azaltmak, intraglomerüler basıncı azaltarak böbrek yetmezliğine gidişi yavaşlatmak ve hemodinamik nedenlerden oluşan FSGS’nin gelişimini engellemektir. ACEİ ve ARB’lerin insan diabetik nefropatisinde böbrek koruyucu olduğuna ve ACEİ baskılayıcılar ile diyette protein kısıtlamasının deneysel hayvan modellerinde ikincil FSGS gelişimini yavaşlattığına dair kesin bulgular vardır. Ayrıca ARB’lerin tümör büyütücü faktör ß-1 (TGF ß-1) oluşumunu azaltarak böbrekte fibrozis gelişimini engellediği gösterilmiştir. NSAII’lar da NS’lu bazı hastalarda muhtemelen glomerüler hemodinamikleri veya glomerüler bazal membranın (GBM) geçirgenlik özelliklerini değiştirerek proteinüriyi azaltırlar. Bu potansiyel fayda, akut böbrek yetmezliğine yol açma, hiperkalemi, tuz ve su tutulumu ve diğer yan etki risklerine karşı dengelenmelidir(8,9).
Tedaviye ihtiyaç gösteren NS komplikasyonları ödem, hiperlipidemi, tromboembolizm, malnütrisyon ve vitamin D yetmezliğidir. Ödem dikkatli bir şekilde ortalama bir tuz
kısıtlaması (günde 1–2 gram) ve makul diüretik kullanımı ile tedavi edilmelidir. İntravasküler hacmi azaltacak ve prerenal azotemiye yol açacak kadar agresif diürez oluşturarak günde 1 kg’dan fazla ödemi vücuttan atmak akıllıca değildir(8,9).
Hastalara çoğu 24–48 saatte atılan tuzdan fakir albumin verilmesi tavsiye edilmemektedir. Halbuki artmış aterosklerozu, glomerüler filtrasyon oranındaki(GFR) düşüşü yavaşlatan ve nefrotik sendrom da görülen endotel fonksiyonu üzerinde iyileştirici etkisi olan lipid düşürücü ilaçlar ile LDL ve kolesterol seviyelerini düşürmek tavsiye edilmektedir. Antikoagülasyon derin ven trombozlu, arteriel trombozlu ve pulmoner embolizmli hastalar için endikedir. Hastalar antitrombin III yetmezliğinden dolayı heparine dirençli olabilirler. NS’lu hastaların dietleri için genel uzlaşma yoktur. Proteinden yüksek diyetler, kan albumin düzeyine etki etmediğinden ve üriner protein atımından dolayı böbrek hastalığında ilerlemeye neden olduğundan önerilmemektedir. Vitamin D yetmezliği görülen NS’lu hastalarda bu vitaminin verilmesi tavsiye edilir(8,9).
İmmün süpresif ilaçlar: Kortikosteroidler
Sitotoksik ilaçlar(siklofosfamid, klorambusil) Siklosporin Takrolimus Mikofenolat mofetil Rituksimab Eculizumab