T.C.
DİCLE ÜNİVERSİTESİ TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI
KRONİK HEPATİT B ENFEKSİYONUNDA
TENOFOVİR VE ENTEKAVİR TEDAVİ
SONUÇLARININ KARŞILAŞTIRILMASI
Dr. Sezai TUNÇ TIPTA UZMANLIK TEZİ
T.C.
DİCLE ÜNİVERSİTESİ TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI
KRONİK HEPATİT B ENFEKSİYONUNDA
TENOFOVİR VE ENTEKAVİR TEDAVİ
SONUÇLARININ KARŞILAŞTIRILMASI
Dr. Sezai TUNÇ TIPTA UZMANLIK TEZİ
TEZ DANIŞMANI Prof. Dr. Muhsin KAYA
TEŞEKKÜR
Bilimsel düşünme ve çalışmayı bizlere öğreten, engin bilgi ve birikimlerini bizimle paylaşan, bugünlere gelmemizde büyük emeği olan, hekimliği bizlere öğreten değerli hocamız Prof. Dr. Ekrem MÜFTÜOĞLU’na başta olmak üzere, İç Hastalıkları A.B.D. Başkanımız Prof. Dr. M. Emin YILMAZ’a, yetişmemde büyük emekleri olan bütün değerli öğretim üyeleri; Prof. Dr. Muhsin KAYA’ya, Prof. Dr. Kendal YALÇIN’a, Prof. Dr. Ali Kemal KADİROĞLU’na, Prof. Dr. Abdurrahman IŞIKDOĞAN’a, Prof. Dr. Alpaslan Kemal TUZCU’ya, Prof. Dr. Orhan AYYILDIZ’a, Doç. Dr. M. Ali KAPLAN’a, Doç Dr. Mehmet KÜÇÜKÖNER’e, Doç. Dr. Zülfikar YILMAZ’a, Doç. Dr. Mazhar Müslüm TUNA’ya, Yrd. Dr. Abdullah KARAKUŞ’a, Yrd. Doç. Dr. Zuhat URAKÇI’ya, Yrd. Doç. Dr. Yaşar YILDIRIM’a, Yrd. Doç. Dr.Feyzullah UÇMAK’a, Yrd. Doç. Dr. Zafer PEKKOLAY’a, Yrd. Doç. Dr Emre Aydın’a, Uzm. Dr. Nazım Ekin’e, Uzm. Dr. Bahattin Gökdemir’e, Uz. Dr. Elif Tuğba TUNCEL’e, Uz. Dr. Ali Veysel KARA’ya, Uz. Dr. Hüseyin KAÇMAZ’a, Uz. Dr.Zeynep ORUÇ’a, Uz. Dr. Halis YERLİKAYA’ya, Uzm. Dr. Belma Özlem BALSAK’a ve Uzm. Dr. Hikmet SOYLU’ ya teşekkürlerimi sunuyorum.
Tezimin her aşamasında yardımlarını esirgemeyen saygıdeğer hocam Prof. Dr. Muhsin KAYA’ya ve en önemlisi birlikte çalışmaktan her zaman büyük mutluluk ve onur duyduğum tüm asistan arkadaşlarıma ve İç Hastalıkları A.B.D çalışanlarına teşekkür ederim.
Ayrıca tezimin istatistiksel analizinde bana yardımcı olan Doç. Dr. M. Ali KAPLAN’a ve biyoistatistik ABD öğretim üyesi Yrd. Doç. Dr. İsmail YILDIZ’ a teşekkür ederim.
Hayatı paylaştığım, hep yanımda olan ve yardımlarını esirgemeyen sevgili eşim Emine’ye ve hayatımın anlamı biricik oğlum Muhammed Azad’a çok teşekkür ederim.
ÖZET
Hepatit B virüsü (HBV) akut hepatit, kronik hepatit, siroz ve hepatosellüler karsinomun en önemli etkenlerinden birisidir. Hepatit B virüsü (HBV) büyük bir global sağlık sorunu olup yaklaşık olarak 240 milyon insanın kronik enfekte olduğu tahmin edilmektedir (1, 2).
Çalışmamızda KHB enfeksiyonunda kullanılan oral antiviral ajanlardan tenofovir ve entekavirin uzun dönem etkinlikleri değerlendirilmiştir.
Çalışmaya toplamda 400 hasta dahil edilmiş, tenofovir grubunda 234 ve entekavir grubunda 166 hasta değerlendirmeye alınmıştır. 0-3-6-9-12. ayda ve sonrasında 6 ayda bir HBV DNA, ALT, AST değerleri; 0-6-12. ay ve sonrasında 12 ayda bir HBsAg, HBeAg, anti-HBe ve 0-6-12. ayda ALP, GGT, total bilurubin değerleri değerlendirmeye alınmıştır. Her iki grup arasında yaş, cinsiyet, başlangıç ALT, AST, HBV DNA, HBeAg pozitifliği, HAI ve fibroz değerlerine bakıldığında istatistiksel açıdan anlamlı fark saptanmamıştır.
Her iki grubun sonuçlarına bakıldığında, HBV DNA negatifleşmesi açısından entekavir tenofovire göre genel olarak daha etkili görünmesine rağmen, istatistiki açıdan anlamlı fark saptanmadı. İki grup arasında ALT normalleşmesi açısından bakıldığında, entekavirin tenofovire göre daha etkili olduğu görünmesine rağmen, istatiksel olarak sadece 6. ve 60. ayda entekavirin daha etkili olduğu saptandı. HBeAg serokonversiyonu ve HBsAg kayıp oranlarına bakıldığında iki grup arasında fark bulunmadı.
ABSTRACT
Hepatitis B virus (HBV) is one of the most important factors of acute hepatitis, chronic hepatitis, cirrhosis and hepatocellular carcinoma. Hepatitis B virus (HBV) is a major global health problem and it is estimated that approximately 240 million people chronically infected (1, 2).
In our study, the oral antiviral agent tenofovir and entecavir used in CHB infection were evaluated long-term efficacy.
In total 400 patients were included in the study, 234 in the tenofovir group and 166 patients in the entecavir group has been evaluated. 0-3-6-9-12. months and after every six months HBV DNA, ALT, AST levels, 0-6-12. months and after every twelve months HBsAg, HBeAg, anti-HBe levels and 0-6-12. months ALP, GGT, total bilirubin values were evaluated. When we have looked at age, gender, initial ALT, AST, HBV DNA, HBeAg, and HAI fibrosis value and no significant statistical difference between the two groups.
When we look at the results of both groups, although HBV DNA negativity in terms of entecavir compared to tenofovir it appears generally more effective, statistically no significant difference was detected. In terms of ALT normalization between the two groups, although it appears that entecavir is more effective than tenofovir, only 6 and 60 months were found to be statistically entecavir is more effective. Considering the loss of HBsAg and HBeAg seroconversion rates were similar between the two groups.
İÇİNDEKİLER
TEŞEKKÜR ... i
ÖZET ... ii
ABSTRACT... iii
İÇİNDEKİLER ... iv
ŞEKİLLER LİSTESİ ...vi
TABLOLAR LİSTESİ ...vii
KISALTMALAR DİZİNİ ... viii 1. GİRİŞ VE AMAÇ...1 2. GENEL BİLGİLER...3 2.1 Hepatit B Enfeksiyonu...3 2.1.1 Epidemiyoloji...3 2.1.1.1 İnsidans ve Prevalans...3 2.1.2 Viroloji...4 2.1.2.1 Genom Yapısı...5 2.1.3 Patoloji...6
2.1.4 Klinik ve Doğal Seyir...9
2.1.4.1 Tanı ve İlk Değerlendirme...9
2.1.4.2 HBV’nin Antijen ve Antikorları...10
2.1.5 Bulaşma Yolları...15
2.1.6 Kronik HBV Tedavisi...16
2.1.6.1 Siroz Olan Hastalarda Tedavi...17
2.1.6.2 Siroz Olmayan Hastalarda Tedavi...18
2.1.6.3 İnaktif Taşıyıcı Hastalarda Tedavi...18
2.1.6.4 Diğer Hastalarda Tedavi...19
2.1.7 Kronik Hepatit B’de Tedaviye Yanıt Kriterleri...19
2.1.8 Tedavi Sonu Belirteçleri...20
2.1.9 Günümüzde Mevcut Tedaviler...21
2.1.10 Yüzey Antijeni (HBsAg) Düzeyi Takibi...25
2.1.11 Tedaviyi Kesme...26
2.1.11.2 HBeAg Negatif Hastalar...27
2.1.12 Hepatit B Aşısı Nasıl Uygulanmalıdır?...28
3. MATERYAL VE METOT...29
4. BULGULAR...31
5. TARTIŞMA VE SONUÇ...48
ŞEKİLLER LİSTESİ
Şekil 1. HBV virüsünün şematik yapısı...6
Şekil 2. Kronik hepatit B’nin doğal seyri (40)...14
Şekil 3. Tenofovir ve entekavir alan hastaların cinsiyet dağılımı...32
Şekil 4. Tenofovir ve entekavir alan hastaların başlangıç yaş ortalamaları...33
Şekil 5. Başlangıç HAI ve fibroz ortalamaları...33
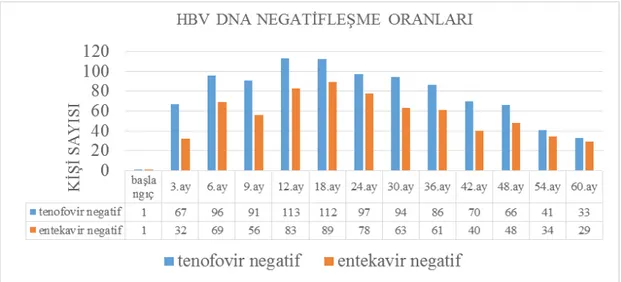
Şekil 6. Tenofovir ve entekavir alan hastaların HBV-DNA negatifleşme oranları...34
Şekil 7. Tenofovir ve entekavir alan hastaların HBV-DNA negatifleşmesi (%)...35
Şekil 8. Tenofovir ve entekavir alan hastaların ALT normalleşme oranları (%)...36
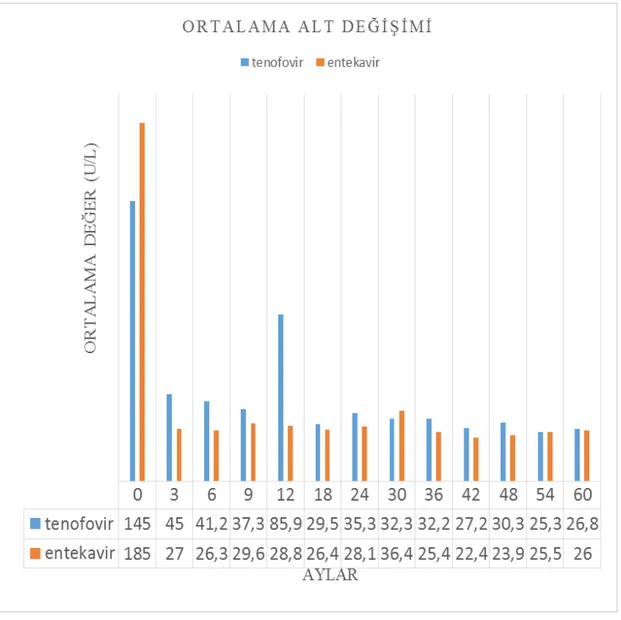
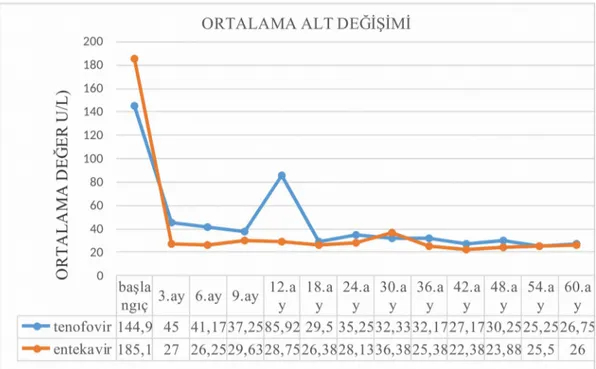
Şekil 9. Tenofovir ve entekavir alan hastaların ortalama ALT değişimi...38
Şekil 10. Tenofovir ve entekavir alan hastaların ortalama ALT değişimi...39
Şekil 11. AST normalleşme oranları...40
Şekil 12. Tenofovir ve entekavir alan hastaların ortalama AST değişimi...40
Şekil 13. Tenofovir ve entekavir alan hastaların ortalama AST değişimi...41
Şekil 14. Tenofovir ve entekavir alan hastaların ortalama HBsAg değişimi...42
Şekil 15. Tenofovir ve entekavir alan hastaların ortalama HBsAg değişimi...42
Şekil 16. HBeAg serokonversiyon oranları (Serolojik yanıt) (%)...43
Şekil 17. HBeAg negatif olan hastaların oranı (%)...44
Şekil 18. Ortalama ALP değişimi...46
Şekil 19. Ortalama GGT değişimi...46
TABLOLAR LİSTESİ
Tablo 1. Modifiye knodell (Ishak) skorlama sistemi (HAI)...8 Tablo 2. Modifiye knodell (Ishak) skorlama sistemi (Fibroz)...9 Tablo 3. Tenofovir ve entekavir alan hastaların başlangıç değerleri...32 Tablo 4. Tenofovir ve entekavir alan hastaların HBeAg durumuna göre HBV DNA
negatifleşme oranları...35 Tablo 5. Tenofovir ve entekavir alan hastaların HBeAg durumuna göre ALT
normalizasyon oranları...37 Tablo 6. Tenofovir ve entekavir alan hastaların 5 yıllık sonuçları...45
KISALTMALAR DİZİNİ
AASLD : Amerikan Karaciğer Hastalıkları Araştırmaları Derneği ABD : Amerika Birleşik Devletleri
AHB : Akut hepatit B
ALP : Alkalen fosfataz ALT : Alanin transaminaz
Anti HBcIgM: Hepatit B çekirdek antikor immunglobulin M Anti HBcIgG : Hepatit B çekirdek antikor immunglobulin G Anti HBe : Hepatit B e antikor
Anti HBs : Hepatit B yüzey antikor
APASL : Asya Pasifik Karaciğer Hastalıkları Araştırmaları Derneği Rehberi AST : Aspartat transaminaz
b- DNA : B tipi DNA
ccc- DNA : Çift sarmallı halkasal DNA Cl Cr : Kreatinin klerensi
DNA : Deoksiribonükleik asit
EASL : Avrupa Karaciğer Hastalıkları Araştırmaları Derneği Rehberi ELISA : Enzyme-Linked ImmunoSorbent Assay
GGT : Gama glutamik asit HAI : Histolojik aktivite indeksi HBcAg : Hepatit B çekirdek antijen HBeAg : Hepatit B e antijen
HBsAg : Hepatit B yüzey antijen HBV : Hepatit B virüsü
HBV DNA : Hepatit B virüs DNA HCC : Hepatosellüler karsinom HCV : Hepatit C virüsü
HDV : Hepatit D virüsü
HIV : İnsan immün yetmezlik virüsü
HT : Hipertansiyon
KC : Karaciğer KHB : Kronik hepatit B KC S : Karaciğer Sirozu
mg : Miligram
mRNA : Mitokondrial RNA
mÜ : Milyon ünite
NÜS : Normalin üst sınırı
OİH : Otoimmün hepatit
ORF : Açık okuma bölgesi
p skoru : İstatistiksel açıdan anlamlı olan değer PCR : Polimeraz zincir reaksiyonu
PEG-INF : Pegile interferon RNA : Ribonükleik asit
SUT : Sağlık Uygulama Tebliği
1. GİRİŞ VE AMAÇ
Hepatit B virüsü (HBV) akut hepatit, kronik hepatit, siroz ve hepatosellüler karsinomun en önemli etkenlerinden birisidir. Hepatit B virüsü (HBV) büyük bir global sağlık sorunu olup yaklaşık olarak 240 milyon insanın kronik enfekte olduğu tahmin edilmektedir (1,2).
Farkındalığın artması, taramaların yaygınlaşması ile tanı konulmamış olgular saptanmış, HBV pozitif olgu sayısı artmıştır. Ancak yapılan metaanalizlere göre KHB prevalansında azalma olduğu belirlenmiştir (3).
HBV infeksiyonunun tanısı serolojik, virolojik, biyokimyasal ve karaciğerin histolojik göstergeleri ile değerlendirilir. Perinatal veya erken çocukluk çağında gelişen infeksiyonların %30-90’ında kronik infeksiyon gelişmekteyken; erişkin dönemde %95’inde doğal bağışıklık, %5’inde kronik infeksiyon gelişir. KHB’lerin bir kısmında da inaktif taşıyıcılık görülebilir (4).
Ülkemizde hepatit sıklığının belirlenmesi amacıyla 2009 yılında başlatılan, 18 yaşın üzerindeki kişilerin değerlendirildiği ulusal hepatit sıklığı çalışmasında, hepatit B taşıyıcılığı (HBsAg +) % 4 saptanmıştır. Kadınlarda HBsAg pozitifliği %3,2, antiHBs pozitifliği % 32,3; erkek populasyonda HBsAg pozitifliği % 4,8, antiHBs pozitifliği % 31,7 bulunmuştur (5).
Kronik HBV infeksiyonunda tedavinin amacı siroz ve/veya hepatoselluler karsinom gibi geriye dönüşümsüz hasarların oluşmasını engellemektir. HBV replikasyonu doğrudan sitopatik etki gostermediği halde, yapılan kohort çalışmalarının sonuçları, viral replikasyonun devamı ile karaciğer hasarının derecesinin ilişkili olduğunu göstermektedir. Dolayısı ile anti-viral tedaviden beklenen uzun vadeli viral supresyondur. Günümüzde bu amaca yönelik olarak ise iki grup ilaç kullanılmaktadır:
1. İmmun modülatorler (alfa interferon ve pegillenmiş formları). 2. Viral polimeraz inhibitorleri (nükleozid ve nükleotid analogları) (6).
Nükleozid analogları, sellüler DNA polimerazlara bağlanmak için doğal substratlar ile yarışan, yeni yapılmakta olan DNA’ya bağlandıklarında ise DNA zincir sentezini durdurup viral replikasyonu susturan bileşiklerdir (DNA polimeraz inhibitorleri). Çoğu nükleozid analogları sitoplazmada bulunan enzimler tarafından
nükleozid 5’-trifosfatlara fosforillenir; ardından virüs-spesifik polimerazlar ile etkileşir. Her bir nükleozid analogu kendine özgü metabolik ve farmakolojik özellikleri ile etki, etkinlik ve toksisite acısından farklılık gosterir (6).
Günümüzde entekavir ve tenofovir isoproksil fumarat kronik hepatit B tedavisinde yaygın olarak kullanılan nükleozid analoglarıdır.
Bu çalışmada; gastroenteroloji polikliniğimizde ve kliniğimizde kronik hepatit B veya KHB’ye bağlı KC sirozu tanıları ile izlenen, entekavir veya tenofovir tedavisi başlanmış olan hastalarda, bu tedavilerin virolojik, serolojik ve biyokimyasal olarak uzun dönem etkinliğinin değerlendirilmesi amaçlanmıştır.
2. GENEL BİLGİLER 2.1 Hepatit B Enfeksiyonu 2.1.1 Epidemiyoloji
Dünya genelinde 240 milyon insan HBV ile enfekte olup her yıl yaklaşık olarak 780 bin insan HBV’ye bağlı komplikasyon nedeniyle ölmektedir. Ayrıca 2010 yılında yapılan çalışmada HBV’ye bağlı gelişen hepatosellüler karsinom mortalitenin yaklaşık % 50 nedeni olarak bulunmuştur (7, 8).
HBV; Hepadnaviridae ailesinin Orthohepadnavirüs genusunda yer alan küçük, 42 nm çapında, yuvarlak, zarflı, replikasyon siklusunu primer olarak karaciğerde gösteren bir DNA virüsüdür (Şekil 1). HBV sadece şempanzeleri ve insanları enfekte eder (9). Hepatit B virüsü, temel olarak parenteral yolla, enfekte kan ve sıvılarla perkütan ve mukozal temas, enfekte kişiyle cinsel temas ve perinatal yolla bulaşır.
Enfeksiyonun edinilme yaşı arttıkça kronikleşme riski azalır. Yenidoğan ve ilk 1 yaşta geçirilen infeksiyon >% 90 kronikleşmekte, bu oran 1–5 yaş arasında % 30’a inmekte, erişkin yaşlar için <% 5 olmaktadır. Kronik HBV infeksiyonu olanların % 4-6'sında HCC, % 30 ‘unda siroz ve % 23 ‘ ünde 5 yıl içerisinde dekompanse siroz gelişir (11).
2.1.1.1. İnsidans ve Prevalans
HBV infeksiyonunun prevelansı ülkemizde % 5 civarındadır. Bölgeler arasında farklılıklar olduğu, güney ve doğu bölgelerinde daha yüksek oranlar olduğu gösterilmiştir (10).
ABD'de 2012 yılından itibaren yapılan sistematik bir incelemede HBV infeksiyonu ile yaklaşık 1,32 milyon kişinin enfekte olduğu bunların % 58’ nin Asya kıtasında doğup göç eden yabancılar olduğu tahmin edilmektedir (12). Dünya’ da prevalansın yüksek oranda olduğu (>%7) bölgeler Güneydoğu Asya, Çin, Afrika, Pasifik Adaları, Orta Doğu ve Amazon havzasını içerir (13). Orta prevalans (%2-7) bölgeleri Güneyorta ve Güneybatı Asya, Doğu ve Güney Avrupa, Rusya, Orta Amerika ve Güney Amerika’dır. Düşük prevalans (<%2) bölgeleri başta ABD olmak üzere Batı Avrupa, Avustralya ve Japonya’dır (2).
1981 yılından beri HBV aşısının kullanıma girmesi, HBV infeksiyonu ve ona bağlı gelişen HCC sıklığında önemli bir azalmaya yol açmıştır (14). Nüfus çalışmalarına göre Tayvan’da HBsAg pozitif olan çocukların prevelansı 1984 yılında % 10’ dan 2009 yılında % 0,9’ a düşmüştür (15). ABD’ de 1984 yılından 2009 yılına kadar olan dönemde HBV ile enfekte olan 6-19 yaşları arası kişilerde prevelans % 1,9 dan % 0,6’ ya (p<0.01) ve 20-49 yaş arası HBV ile enfekte kişilerde % 5,9 dan % 4,6 ‘ya düşmüştür (p<0.01) (16).
2.1.2. Viroloji
İnfekte hücrelerde birden fazla sayıda partikül tipi oluşumuna yol açması nedeniyle diğer hayvan virüslerinden farklı bir yere sahip olan HBV’nin, kısmen saflaştırılmış preparasyonları elektron mikroskobunda incelenecek olur ise; büyüklük, yapı ve miktar gibi değişik özellikleri bakımından birbirine benzemeyen üç tip partiküle rastlanır (17, 18, 19, 20).
1. Yaklaşık 42 nm. (42-47 nm.) çapında, infektif özellikte, tam bir viryon yapısında, küresel şekilli, Dane partikülleri;
2. Yaklaşık 22 nm. (16-25 nm.) çapında, içinde nükleik asit bulunmayan, noninfektif, küresel partiküller;
3. Özellikle replikasyonun söz konusu olduğu kişilerin serumunda bulunan, 22 nm. çapında, 50-500 nm uzunluğunda nükleik asit ihtiva etmeyen, non-infektif, tübüler partiküller.
Her üç form da infekte konak serumunda yüksek miktarda (200-500 mg/ml) saptanabilen ve HBsAg adı verilen ortak yüzey antijenine sahip olup, immünojeniktir. Anti-HBs antikorları ile reaksiyon verirler. Non-infektif formlar daha fazla miktarda üretilir ve kanda dolaşan HBsAg’nin büyük kısmını 22 nm'lik küresel partiküller oluşturur (18, 20, 21).
Karaciğer doku tropizmine sahiptir, hepatositlerde replike olarak hepatit tablosuna neden olur. Uzunluğu 3200 bp olan kısmi çift sarmallı halkasal DNA genomu vardır. Konak hücreden kazanılmış olan lipid zarf üzerinde üç formda viral yüzey antijeni (HBsAg) bulunur; büyük (L), orta (M), küçük (S) yüzey antijenleri. Virüsün kapsidi; 27 nm çapındadır. Kapsid polimeraz enzimi, çekirdek antijeni (HBcAg) ve viral genom içerir. Elektron mikroskobu ile enfekte serumda üç formda
viral partikül gösterilmiştir; Dane partikülü, filamentöz yapılar ve küçük yuvarlak partiküller (9).
2.1.2.1. Genom Yapısı
HBV; kısmen çift sarmallı, genotipe bağlı olarak 3182 ila 3248 nükleotide sahip DNA molekülü taşır (22, 23). Negatif sarmal 3200 nükleotid, pozitif sarmal ise 1700-2800 nükleotid uzunluğundadır. İki sarmal da kovalent bağlı değildir. Negatif sarmal tamamlanmıştır ve 9 nükleotidlik fazlalığı bulunmaktadır. Pozitif sarmal her zaman tamamlanmamıştır ve değişken uzunluktadır, sabit bir 5’ ucu bulunur fakat 3’ uç değişkendir. Her iki sarmalın 5’ ucu arasında kısa (HBV’de 220 baz çifti) bir yapıştırıcı üst üste gelen bölüm bulunur. Her iki sarmalın 5’ucunda, 10-11 nükleotidlik iki direk-tekrar dizisi (DR1 ve DR2) içerirler. 17 bazlık 5’ başlık içeren bir yapı, pozitif sarmalın 5’ ucuna bağlıdır. Bir protein, viral RNA polimeraz, eksi sarmalın 5’ucuna kovalent olarak bağlıdır (24).
Virüsün genomunda, değişik proteinleri kodlayan 4 adet ORF (açık okuma bölgesi) bulunmaktadır. ORF’lar kompakt bir dizayna sahiptirler ve bu nedenle çeşitli genler çakışabilir. Sonuçta aynı DNA kullanılmasına rağmen farklı viral proteinler kodlanabilir (25). ORF’lar dört viral gen kodlamaktadırlar; yüzey (S),çekirdek (C), polimeraz (P) ve X.
HBV’nin dört major geni mevcuttur.
S geni: Pre-S1 (L:geniş), Pre-S2 (M: orta) ve S (S: küçük) bölgelerinden oluşup, virus yüzey veya zarf antijenini (hepatitis B surface antigen – HBsAg) kodlayan gendir.
C geni: Kor veya nükleokapsid genidir. Kor partikülü içinde toplanan “hepatitis B core antigen (HBcAg)’’ini kodlar. HBcAg sadece karaciğer hücresinde tespit edilebilir. Bu antijenin karboksi terminalinin bir bölümünden “hepatitis B e antigen (HBeAg)’’i kodlanarak ekstraselüler bölgeye salınır. Ekstraselüler alanda HBeAg solubl formdadır. HBeAg, replikasyonun ve infeksiyözitenin göstergesidir. HBeAg negatif prekor mutantlarda bu antijen salınmamakta, fakat replikasyon devam etmektedir.
P geni: P proteini = Pol (polimeraz) geni, viral genomun büyük bir kısmını kaplar. En geniş ORF’dir (yaklaşık 800 aminoasit içerir). DNA bağımlı DNA polimeraz ve RNA bağımlı revers transkriptaz aktivitesindeki temel bir polipeptidi kodlar. Polimeraz geni, yüzey geni ile çakışır.
X geni: Viral replikasyon için önemli olan iki transkripsiyon aktivatörünü kodladığı düşünülen küçük bir gendir. X geni, X proteinini kodlar, bu protein yeniden aktivasyonda önemlidir ve hepatik karsinogenezde önemli olabilir (26, 27).
Şekil 1. HBV virüsünün şematik yapısı 2.1.3. Patoloji
HBV, doğrudan sitopatik etkili değildir. Karaciğer hasarı, HBV ile enfekte hepatositler arasındaki etkileşim ve konakçı immun yanıtın sonucu olarak oluşur. Karaciğerin %70'ini oluşturan hepatositler majör hücre türü olduğundan, HBV gibi karaciğere tropizmi olan bir virusun esas hedefinin de bu hücreler olması beklenmektedir. Hepadnavirus ailesinde yer alan üyelerin tümü için doğrulanmış tek replikasyon yeri hepatositlerdir. Safra kanal epitel hücreleri, pankreas, böbrek ve lenfoid sistemdeki bazı hücre grupları da infeksiyonun hedefi olabilir. Ancak bu hücrelerde viral replikasyon ile ilgili veriler yeterli ve güvenilir değildir. Bu nedenle söz konusu dokular üreme ve patogenez tartışmalarında genellikle göz önüne alınmamakta ve ekstrahepatik çoğu semptomun sebebi olarak karaciğer disfonksiyonu değil, antijen-antikor kompleksi birikimi gösterilmektedir.
Hepadnavirus infeksiyonları sırasında homojen bir hücre topluluğu şeklinde görülen hepatositler, bağışıklık sisteminin enfekte hücrelere saldırısı ile aniden değişebilir, eğer tüm hepatositler enfekte ise virusün temizlenmesi ya hepatositlerden
virus eliminasyonu için bir mekanizmanın tetiklenmesini ya da hipotetik olarak enfekte hepatositlerin enfekte olmayan progenitör hücreler tarafından tamamen yerine konmasını gerektirir. HBV infeksiyonunda karaciğer hasarının en önemli nedeni konağın immün yanıtıdır. Konağın infeksiyona karşı verdiği immün yanıt çok sayıda hepatositi yıkarak skarlaşma, kan akımında azalma ve safra akımında obstrüksiyona sebep olur ama infeksiyonu elimine edemez. Hepatositler bütünüyle diferansiye olsalar bile karaciğer hasarına yanıt olarak daha fazla prolifere olabilecek kapasiteye sahip hücrelerdir. Normal koşullarda hepatositlerin yaşam süresi 6 ay ile 12 ay arasında değişir. Hepatosit proliferasyonunu geciktiren akut ve/veya uzun süreli karaciğer hasarı durumlarında (örneğin bazı hepatotoksik ilaçlara bağlı) ise hepatositlerin yerine konma işlemi progenitör hücrelerin proliferasyonu ile gerçekleşebilmektedir (28-30).
1. Portal inflamasyon: Mononükleer hücre infiltrasyonu yoğundur, arada plazma hücreleri de bulunur ama çoğunluğunu CD4+ T hücreleri oluşturur.
2. İnterface hepatit: Parankim ve portal alana ait bağ doku sınırında hepatositlerin ilerleyici hasarı ve beraberinde lenfohistiositik infiltrasyon vardır. Sonuçta hepatositlerde apopitoz gelişir.
3. Lobüler hepatit veya konfluent nekroz: İnflamasyonla santral vene yakın alanda köprüleşme nekrozları gelişir.
4. Fibrozis: Kronik hepatit olgularında skar veya bağ doku artışı öncelikle portal stromanın artışı ile meydana gelmektedir. Bu skar dokusu santral ven ile komşu portal alan arasında veya bir başka santral vene doğru uzanarak devamlı kalabilir (31).
Hepatit B tanısında, patolojik olarak fibrozis ve aktivite derecesini gösteren çeşitli skorlama sistemleri mevcuttur. Bunlar; Knodell skorlama sistemi, Scheuer skorlama sistemi, Metavir skorlama sistemi, Modifiye Knodell (Ishak) skorlama sistemleridir (32). En sık kullanılan sistem günümüzde Modifiye Knodell (Ishak) skorlama sistemidir (Tablo 1 ve 2).
Tablo 1. Modifiye knodell (Ishak) skorlama sistemi (HAI) (32)
A. Periportal veya periseptal interface hepatit (piecemeal nekrozu) Skor
Yok 0
Hafif (fokal, birkaç portal alanda 1
Hafif/orta derecede (fokal, portal alanların çoğunda) 2
Orta derecede (portal traktın veya septanın %50’den azında ve devamlı) 3
Ciddi (portal traktın veya septanın %50’sinin üzerinde ve devamlı) 4
B. Konfluent nekroz Yok 0
Fokal konfluent nekroz 1
Bazı alanlarda zone 3 nekroz 2
Çoğu alanda zone 3 nekroz 3
Zone 3 nekroz ve nadir porto-sentral (P-C) köprüleşme 4
Çok sayıda zone 3 nekroz ve porto-sentral (P-C) köprüleşme 5
Panasiner veya multiasiner nekroz 6
C. Fokal (spotty) litik nekroz, apopitozis ve fokal inflamasyon Yok 0
Bir odak veya her 10x objektif büyütmesinde birden az 1
Her 10x objektif büyütmesinde 2-4 odak 2
Her 10x objektif büyütmesinde 5-10 odak 3
Her 10x objektif büyütmesinde 10’dan fazla odak 4
D. Portal inflamasyon Yok 0
Hafif, portal alanların tümü veya bazıları 1
Orta derecede, portal alanların tümü veya bazıları 2
Orta derecede veya şiddetli, portal alanların tümü 3
Şiddetli, tüm portal alanlar 4
Fibrozis Skor Fibrozis izlenmedi 0 Bazı portal alanlarda fibröz genişleme, kısa fibröz septa ile birlikte veya değil 1 Portal alanların çoğunda fibröz genişleme, kısa fibröz septa ile birlikte veya değil 2 Portal alanların çoğunda fibröz genişleme ve eşlik eden nadir porto-portal (P-P) köprüleşme 3 Portal alanlarda fibröz genişleme ve eşlik eden belirgin porto-portal (P-P) ve aynı zamanda porto-sentral (P-C) köprüleşmeler 4 Belirgin (P-P) ve (P-C) köprüleşmeler ve nadir nodül formasyonu 5 Siroz, açıkça veya büyük olasılıkla 6
2.1.4. Klinik ve Doğal Seyir
2.1.4.1. Tanı ve İlk Değerlendirme
HBV infeksiyonun serolojik belirteçleri hepatit B yüzey antijeni (HBsAg), hepatit B yüzey antijenine karşı gelişen antikor (Anti-HBs), hepatit B e antijeni (HBeAg), hepatit B e antikoru (Anti-HBe), hepatit B çekirdek antikorları Anti-HBc Ig M ve Ig G dir. Serum HBsAg infeksiyonun primer belirtecidir. Genellikle enzim immunoessey (ELISA) yöntemi kullanılarak saptanır. HBV tanısı pozitif HBsAg temelinde konulduktan sonra, tanıyı destekleme amaçlı alanin aminotransferaz (ALT), HBV DNA düzeyi, anti-HBc Ig G, HBeAg durumu ve karaciğer fibrozu değerlendirilmelidir (33-35). HBcAg, infekte hepatositlerde eksprese olan intraselüler bir antijendir; serumda saptanamaz. Kor antikorları ise serumda saptanabilir; anti-HBc IgM, AHB tanısında önemli bir göstergedir. Anti-HBs, HBV infeksiyonuna karşı bağışıklığın göstergesidir. HBeAg prekor proteini tarafından kodlanarak eksprese edilen ve genellikle replikasyonu ve infektiviteyi gösteren bir antijendir (36,37).
2.1.4.2 HBV’nin Antijen ve Antikorları HBsAg
HBsAg HBV’nin yüzeyinde kompleks yapıda bir antijendir. Genellikle kanda saptanan ilk viral göstergedir ve varlığı aktif infeksiyonun kanıtı olarak kabul edilir. En erken HBV ile temastan 1-2 hafta sonra duyarlı yöntemlerle kanda saptanabilirler. HBsAg saptanmasından ortalama 4 hafta (1-7 hafta) sonra ise hepatitin klinik belirtileri ortaya çıkar. Kendini sınırlayan infeksiyonlarda HBsAg pozitifliği ortalama 1-6 hafta en geç 20 hafta devam eder (41).
AntiHBs
HBsAg’ye karşı oluşan antikorlardır. Koruyucu nötralizan özellik gösterirler. Genellikle HBsAg’nin serumdan kaybolmasından bir süre sonra AntiHBs saptanır, bu ara süreye pencere dönemi denir. Bu devre dikkate alınarak anti HBc IgM araştırılmazsa tanı atlanmış olur. B tipi akut viral hepatit geçirenlerin %5-15’inde anti HBs oluşmamaktadır (42). Kandaki antiHBs titresi infeksiyondan sonraki 6-12 ay boyunca yükselişini sürdürür ve daha sonra yıllarca pozitiflik devam eder (41). AntiHBs reinfeksiyondan korunmanın iyi bir işaretidir, ancak bazen kronik hepatit B’li hastaların %10-20’sinde düşük titrede saptanabilirler (40). Aşılama ve Ig transfüzyonu sonrasında serumda tek başına antiHBs pozitifliği saptanır (42).
HBcAg
Dışarıdan HBsAg ve lipid içeren bir zarf ile örtülmüştur. 42 nm çapında intakt virionun kimyasal maddeyle parçalanması sonucunda 27 nm çapındaki nükleokapsid kor partikülü izole edilebilir (41). İnfekte karaciğer dokusunda saptanabilir ancak dolaşımda saptanamaz (42).
AntiHBc
HBcAg’ye karşı oluşmuş antikordur. HbsAg’nin serumda saptanmasından 1-2 hafta sonra anti-HBc IgM serumda pozitifleşir hastalığın akut devresinde tüm hastalarda saptanmaktadır ve pozitifliği 6-24 ay devam edebilir. HBsAg’nin saptanamadığı %5 kadar hastada serumda yüksek titrede anti-HBc IgM antikorları tanıya yardımcıdır (44). Kronik infeksiyon sırasında reinfeksiyon gelişirse tekrar saptanabilir düzeylere çıkabilir. Anti-HBc IgG HBV enfeksiyonu geçiren kişilerde çok uzun süre hatta ömür boyu pozitif kalabilir (41).
HBeAg
Hem akut hem de kronik hepatitlerde infektivite işareti olarak kabul edilmektedir. HBsAg ile beraber veya çok kısa bir süre sonra serumda belirir ve iyileşen olgularda ortalama 10 hafta sonra bir başka deyişle HBsAg’nin kaybolmasından birkaç gün önce negatifleşir (41). HBeAg varlığı ile Dane partikülü yüksek serum yoğunluğu, HBsAg ve HBV DNA polimeraz arasında kuvvetli bir ilişki vardır (48). HBeAg pozitifliği, viral DNA ve aktif replikasyonun varlığını yansıtır (43). HBeAg’nin 10 haftadan daha uzun süren pozitifliği kronikleşme eğilimini yansıtabilir (48).
AntiHBe
HBeAg’ye karşı oluşmış antikordur. Akut infeksiyon sonrasında HBeAg saptanamaz olunca gelişmektedir. Anti HBe saptanan taşıyıcıların infektiviteleri düşüktür. Pozitifliği birkaç ay-yıl devam edebilir (42).
HBV DNA:
PCR ile HBV DNA araştırılması kronik hastaların infektivitesini tayin etmede en etkili metoddur. HBV aktivasyon göstergeleri HBeAg, HBV DNA ve DNA polimerazdır (42).
Başlıca b-DNA ve real time PCR yöntemleri ile tayin edilmektedir. Hastanın inaktif taşıyıcı veya kronik hepatit olup olmadığının ayrımında önemlidir (47).
HBV enfeksiyonlarında saptanan bir başka viral gosterge DNA ve DNA polimeraz içeren virionlardır. Bu partiküller HBsAg’den sonra ortaya çıkar ve varlıkları DNA polimeraz aktivitesi veya viral DNA ile hibridizasyon yapılarak araştırılır. Enkübasyon döneminin son günlerinde yüksek konsantrasyonlara ulaştıktan sonra, hepatit tablosunun gelişmesi ile düşmeye başlarlar ve genellikle hastanın iyileşmesine yakın günlerde serumda saptanamazlar (41).
Akut infeksiyon sonrası, 6 aydan uzun sureli HBsAg pozitifliği kronik hepatit B’nin göstergesidir. Bu durumda viral replikasyon karaciğerde devam eder ve hem karaciğer, hem de kanda titresi değişmekle birlikte viremi devam eder.
KHB’de bazı hastalarda halsizlik, yorgunluk, bulantı, üst abdominal ağrı, kas ve eklem ağrıları, anksiyete, konsantrasyon güçlüğü, uyku bozukluğu, depresyon gibi nonspesifik şikayetlere rastlansa da genellikle asemptomatiktir (38). Ancak hastaların %40-50’inde sarılık hikayesi vardır. Görülebilen diğer semptomlar ise; spider anjiom, splenomegali, asit gibi son evre karaciğer hastalığına ait bulgulardır, ya da karaciğer dışında etkilenen organların eşlik eden hastalıklarına aittir. Kronik hepatit B infeksiyonunda poliarteritis nodosa, vaskülitik raş, glomerülonefrit, ateş ve poliartralji gibi ekstrahepatik hastalıklar görülebilir. Dolaşımda HBsAg ve anti HBs kompleksleri, damar duvarında kriyoproteinler ve HBsAg demonstre edilebilir (39, 45, 46).
Tüm vücut kaslarında atrofik değişiklikler, kas güçsüzlüğü olabilir. Palmar eritem ve tenar/hipotenar bölgelerdeki kas atrofileri sirozlu hastalarda sık görülen bulgulardandır. Çomak parmak ve hipertrofik osteoartropati diğer el bulgularındandır. Ensefalopati gelişen hastalarda ellerde kuşkanadı çırpınmasına benzeyen ve flepping tremor denilen titreme görülebilir. Karaciğer büyüklüğü değişkenlik göstermekle birlikte, genellikle fibroza bağlı olarak küçülmüştür. Portal HT’nun gelişimini takiben splenomegali sık rastalanan bir fizik muayene bulgusudur. Erkek hastalarda jinekomasti, hipogonadizm ve impotans, kadınlarda gonadal yetmezlik ve buna bağlı oligomenore, amenore ve infertilite görülebilir (47).
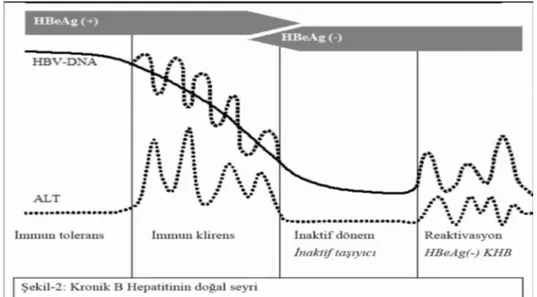
KHB infeksiyonunun doğal seyri virus - konak etkileşimine göre 4 ayrı dönemde incelenebilir (şekil 2) (40).
1. İmmüntolerans Dönemi:
Konak, bu evrede HBV’nin replikasyonuna immüntolerandır, replikasyon sürer. Karaciğer inflamasyonu minimaldir ve siroza progresyon nadirdir. Sağlıklı erişkinlerdeki bu inkübasyon evresi iki-dört hafta sürerken, çocuklarda, özellikle infeksiyonu vertikal yolla almış yenidoğanlarda, bu immüntoleran durum 10 yıllarca sürebilmektedir. Bariz bir belirti ve bulgu olmayan hastanın alanin aminotransferaz (ALT) düzeyleri de normaldir (48).
2. İmmün Klerens Dönem:
İmmunolojik yanıt dönemidir, konağın bağışıklık sistemi olgunlaşır. Hepatositlerde hasar ortaya çıkar ve hepatit tablosu oluşur. Her ne kadar karaciğerde viral replikasyon devam ediyor ve viremi süreklilik gösteriyorsa da enfekte hücrelerin ölümüyle serum HBV DNA düzeyleri düşer (49). Genellikle karaciğer enzimleri yüksektir, HBeAg pozitiftir ve karaciğerde belirgin inflamatuvar aktiviteye rastlanır (50).
HBeAg pozitif hastalarda bir yılda serokonversiyon olasılığı %10-20 olup spontan serokonversiyon HBV infeksiyonunda doğal gidişin önemli bir göstergesidir. HBeAg pozitifliğinin devam etmesi ilerleyici karaciğer hastalığı için risktir. İmmün klerens dönemi çok aktif ve uzun sürerse hastalar siroz olarak karşımıza gelebilirler. Bu hastalarda 5 yıl içinde siroz gelişme olasılığı %12-20’dir (49).
3. İnaktif Taşıyıcılık:
Konak immun yanıtının gelişmesi ile karakterizedir. Bu evrede HBsAg pozitif olmakla birlikte HBeAg negatifleşmiştir. HBV DNA düzeyi düşük (<10.000 kopya/ml) ya da saptanamamaktadır. Sitoplazmada HBsAg varlığı gösterilebilir. Transaminazlar önceki dönemden daha düşüktür. Karaciğer biyopsilerinde nekroenflamatuvar aktivitenin azalmış olduğu dikkati çeker (51). Hastaların çoğu yıllarca bu dönemde kalmaktadır.
4. Reaktivasyon Dönemi (HBeAg negatif KHB):
HBeAg serokonversiyonundan sonra hastaların bir kısmı HBeAg negatif kronik HBV olarak bilinen viral reaktivasyon durumu gelişen hastalığa girebilir. İnaktif taşıyıcılık döneminde olduğu gibi bu durum HBeAg nin kaybolması ile gösterilir. İnaktif taşıyıcıların yaklaşık 1/3’ünde HBeAg reversiyonu olmadan kronik hepatit yineleyebilir (53-55). Bu dönemde HBV DNA düzeyleri genelde önceki iki dönemden (immün tolerans fazı ve immün klirens fazı) daha düşüktür. HBeAg-negatif olmasının temel nedeni HBV genomunda precore bölge mutasyonu olmasıdır ki bu HBeAg üretimini durdurur ancak yüksek seviyede viral replikasyona neden olur(G1896A mutasyonu) (57). HBeAg negatif olan hastalar HBeAg pozitif olan
hastalara göre iki kat siroza ilerleme riskine sahiptir (56). HBeAg negatif KHB olan hastalar tedaviden yarar göreceğinden, HBeAg negatif inaktif taşıyıcı olan hastalardan ayırt edilmeleri önemlidir. Bir başka ikili mutasyon ise basal core promotor mutasyon olarak da bilinen A1762T/G1764A mutasyonları olup, mutasyon olduğunda virüsün precore mRNA üretimi azaldığından HBeAg düzeyleri de düşer (57,58). Bazal core promotor mutasyonuna bağlı HBeAg negatif hastalığı olan kişilerde HBV DNA düzeyine bağlı olarak siroza ve HCC’ye ilerleme riski artmıştır (59-61).
Okült (Gizli) HBV Enfeksiyonu
Okült HBV infeksiyonu HBsAg negatif ancak serum ya da karaciğer dokusunda HBV DNA’nın pozitif olması olarak tanımlanır (62). Serum HBV DNA düzeyleri genellikle 200 IU/mL altındadır. Genellikle hepatit C virüs(HCV) infeksiyonu ile birlikteliğinde görülür. Okült HBV infeksiyonu hastalarda siroza ilerleme, HCC gelişimi açısından büyük bir risk oluşturmasının yanı sıra kısa yaşam süresi ile ilişkilidir (63, 64). Bu hastalar aşikar HBV enfeksiyonu olanlar ile aynı şekilde ele alınmalıdır (65).
Şekil 2. Kronik hepatit B’nin doğal seyri (40) 2.1.5. Bulaşma Yolları
HBV’nin inkübasyon süresi 45-160 gün arasındadır. Bulaş için su ve gıdaların önemi yoktur. Ancak enfekte kanın hasarlanmış oral mukozaya temas etmesiyle oral yolla bulaşabilir (66). Perkütan, horizontal ve perinatal bulaş, cinsel temas başlıca bulaş yollarıdır. Yüksek HBV seviyesi, HBeAg pozitifliği daha yüksek enfektiviteyi gösterir. HBeAg negatif olgularda bulaş %1-6, HBeAg pozitif olgularda % 22-40 oranındadır (67).
ABD gibi düşük endemik bölgelerde, intravenöz ilaç kullanımı ve korunmasız cinsel ilişki ile bulaş daha yaygın iken; Afrika, Alaska ve Akdeniz ülkelerinde sıklıkla bulaş yolu horizantal yolla çocukluk döneminde olmaktadır (68). HBV çevresel yüzeylerde en az yedi gün boyunca stabil ve enfeksiyöz olarak kalabilir. Ailede bulaş kontamine yüzey ve objelerle indirek de olabilmektedir (66).
Cinsel Bulaş
Genital sekresyonlarda kandan daha az miktarda virüs bulunmasına rağmen mukozal giriş kapılarından kolay girmesi sebebiyle cinsel temasla bulaşabilir (69). Hatta mukoza bütünlüğünün bozuk olduğu erkek homoseksüellerde, travmatik ilişkilerde ve başka bir cinsel hastalığın bulunması durumunda bulaş riski artar (70).
Horizontal Bulaş
Özellikle KHB hastalarının aile bireylerinde olan, başka bir bulaşma yolunun saptanamadığı olgularda, ortak ev veya yaşam koşulunun bulaşmaya neden olduğu düşünülmektedir. Enfekte kişilerden ortama yayılan HBV’nin sağlıklı kişilerin mukoza ve açık lezyonuna teması sonucu olduğu hipotezi vardır. Özellikle 7-14 yaş grubunun seroprevalansını arttıran bulaşma şeklidir. Sosyoekonomik düzeyin düşük olması, toplu yaşam ve kötü hijyen şartları bulaşmayı arttırmaktadır (71,72). Ülkemizde en yaygın bulaşma şeklidir. Ailede yaygın öpüşme alışkanlığı; havlu, jilet, makas, manikür-pedikür malzemesi, tırnak makası, cımbız, tarak gibi hijyenik aletlerin ortak kullanılması; çocuklarda oyun sırasındaki temas bu bulaşın sebebi olabilir (73).
Enfekte gebeden bebeğe bulaş, tüm dünyada HBV’nin sık bulaş yollarındandır. Bu bulaş transplasental, perinatal veya postnatal olabilir. Perinatal bulaş en sık doğum sırasında olmaktadır. Uterus içinde de transmisyon %2 oranında olabilir (74).
HBeAg negatif anneden doğan bebeklerde risk düşük olup %5-20 iken HBeAg pozitif anneden bulaş %70-90’dir (75). Doğumdan sonra oluşan cilt ve mukoza sıyrıklarının enfekte maternal sıvılara teması, vajinal kanaldan geçerken anne kanının yutulması, sezaryen sırasında anne kanıyla temas veya plasenta hasarı sonucu maternal dolaşımın fötal dolaşıma karışması gibi nedenlerle bulaş meydana gelebilir. Anne sütünde HBsAg gösterilmiştir, teorik olarak bulaştırıcı olabilir fakat bu durum anne sütünün kesilmesini zorunlu kılmaz (76).
Perkütan Bulaş
Enfekte kan ürünleri, hemodiyaliz ve endoskopi gibi sağlıkla ilgili işlemler, intravenöz ilaç bağımlılarında ortak enjektör kullanımı, hastane personelinde vücuda batan iğne veya keskin malzemeler, dövme ve akupunktur yaptırma, kan bulaşmış günlük malzemeler perkütan yolla virüsün bulaşmasına neden olmaktadır (77).
2.1.6. Kronik HBV Tedavisi
Tedaviye başlama kararı alınırken, HBV DNA düzeyinin supresyonu, ALT normalleşmesi ve HBeAg pozitif hastalarda HBeAg serokonversiyonu amaçlanması yanında, hastalarda siroz varlığı ya da yokluğu ve hepatit B inaktif taşıyıcılık durumu da göz önüne alınmalıdır.
Tedavide iyi tanımlanmış kategoriler, hangi hastaya hangi antiviral tedavi verilmesini öneren güncel rehberler bulunmaktadır.
Rehberler
- Avrupa Karaciğer Hastalıkları Araştırmaları Derneği Rehberi (EASL) 2012 - Asya Pasifik Karaciğer Hastalıkları Araştırmaları Derneği Rehberi (APASL) 2012
- Amerikan Karaciğer Hastalıkları Araştırmaları Derneği(AASLD) 2009 Ülkemizde antiviral tedavi yıllardır Sosyal Güvenlik Kurumu Genel Sağlık Sigortası Genel Müdürlüğü tarafından hazırlanan Sağlık Uygulama Tebliği (SUT) önerilerine uygun olarak planlanmaktadır. KHB’de güncel SUT kriterleri:
1. HBV DNA ≥10.000 kopya/ml, HAI ≥6 veya fibrozis ≥2 tedavi başlama kriterleridir.
2. ALT >2 NÜS (normalin üst sınırı), HBeAg negatif, HBV DNA ≤10^7 kopya/ml veya HBeAg pozitif, HBV DNA ≤10^9 kopya/ml ise INF alfa veya PEG-INF alfa ile en fazla 48 hafta tedavi verilebilir.
3. Oral antiviral tedavisi alan hastalarda negatif olan HBV DNA’nın pozitifleşmesi veya HBV DNA’nın 10 kat yükselmesi ile başka bir oral antiviral ajana geçilebilir veya almakta oldukları tedaviye ikinci bir oral antiviral eklenebilir.
4. Lamivudin veya telbivudin tedavisinin 24. haftasında HBV DNA 50 IU/ml (300 kopya/ml) ve üzerinde ise diğer antivirallere geçilebilir.
5. Tenofovir veya entekavir tedavisinin 48. haftasında halen HBV DNA pozitif olması durumunda bu iki antiviral arasında geçiş yapılabilir veya bu iki antiviral kombine edilebilir.
6. Adefovir tedavisinde koşul aranmaksızın tenofovir veya entekavire geçilebilir.
7. Oral antiviral tedavi, HBsAg negatif ve anti HBs pozitifleştikten sonra en fazla 12 ay daha sürdürülür.
2.1.6.1. Siroz Olan Hastalarda Tedavi
Sirozlu hastalarda klavuzların ortak görüşü dekompanse sirozlu hastaların bir nükleot(z)id analoğu ile HBV DNA ve ALT düzeyi ne olursa olsun tedavi edilmesidir (33-35). Ancak kompanse sirozlu hastaları tedavi etme yaklaşımı farklıdır.
EASL bütün kompanse sirozlu hastalarda ALT konsantrasyonu ve HBV DNA düzeyine bakılmaksızın tedavi verilmesini önermektedir (34). Ancak, AASLD ve APASL klavuzlarının her ikisi de kompanse sirozlu hastalarda HBV DNA viral yükü 2000 IU / ml veya daha fazla olanların tedavi edilmesini önermektedir (33, 35).
HBV DNA düzeyi 2000 IU/ml veya üstünde olan ve aşağıdaki özellikleri gösteren hastalar, kontrendikasyon olmadıkça karaciğer biyopsisi yapılarak tedavi yönünden değerlendirilmelidir:
1. ALT normalin üstünde olan hastalar 2. ALT sürekli normal olan hastalardan a. 35 yaş veya üzerinde olanlar,
b. İleri karaciğer hastalığı kuşkusu uyandıracak belirtileri olan hastalar (trombosit düşüklüğü, AST>ALT olması, globulin yüksekliği, albumin düşüklüğü, protrombin zamanında uzama gibi).
Biyopsisinde Ishak skoruna göre Histolojik Aktivite İndeksi (HAİ; Grade) ≥ 6 veya Fibrozu (stage) ≥ 2 olan hastalara tedavi verilmelidir (78-81). ALT seviyesi normal olan olgularda 3-6 ayda bir ALT kontrolü, 6-12 ayda bir HBeAg kontrolü yapılır (78).
Sirozu olmayanlarda, klavuzlar ve uzmanlardan oluşan bir panel, immün klerens döneminde antivirallere potansiyel direnç ve tedavinin yararını gösteren verilerin eksikliği nedeniyle, gözlem ve 3 ila 6 ayda bir ALT ve HBV DNA değerlerinin takip edilmesi yaklaşımını önermektedir (33, 34, 38, 82). Bununla beraber immün klerens döneminde olan 126 hastada, HBeAg ve normal ALT konsantrasyonu bakılarak yapılan çift kör randomize kontrollü bir çalışmada 4 yıllık nükloz(t)id analoğu tedavisi sonrası HBeAg serokonversiyonun % 5’in altında olduğu gösterilmiştir (83).
2.1.6.3 İnaktif Taşıyıcı Hastalarda Tedavi
Aynı klavuzlar inaktif taşıyıcı hastalarda tedaviden ziyade yakın takibi önermektedir (33-35). Bu fazda olan hastalarda genellikle hastalığın ilerleme riski düşük olmakla beraber, 146 inaktif taşıyıcı hasta üzerinde yapılan bir kohort çalışmasında 23 yılı aşkın takip süresi boyunca, 43 hastada normalin üzerinde ALT düzeylerinde artış olduğu, 1 hastada spontan serokonversiyon (HBeAg negatif) geliştiği ve 2 hastada HCC geliştiği bulunmuştur (84). 20069 inaktif taşıyıcı döneminde olan hasta üzerinde yapılan geniş bir kohort çalışmasında HCC ve
karaciğer ile ilgili yıllık ölüm insidans oranları kontrol grubu ile karşılaştırıldığında (kontrol grubunda % 0.02 ve % 0.02) sırasıyla % 0.06 ve % 0.04 idi. Ayrıca kontrol grubu ile karşılaştırıldığında HCC gelişme riski 4.6 (% 95 güven aralığında 2.5-8.3) ve karaciğer hastalığına bağlı mortalite riski 2.1 (1.1-4.1) idi (85). Bu bulgular inaktif hastalığı olan taşıyıcıların HCC için devamlı gözlemenin önemini vurgulamaktadır. Ayrıca, siroz olmayan kişilerde dahi inaktif taşıyıcı durumu sırasında karaciğer ilişkili komplikasyonların gelişim potansiyeli göz önüne alındığında, tüm sirozlu hastalarda ise HBV DNA düzeyi ne olursa olsun tedavi düşünülmelidir.
2.1.6.4. Diğer Hastalarda Tedavi
Hastaların geri kalanında tedaviye başlama kararı HBeAg durumu, ALT konsantrasyonu, HBV viral yükü, yaş (<40 ya da > 40 yaş) ve karaciğer fibrozis evresi de dahil olmak üzere çeşitli faktörlere dayalı olmalıdır. Bu değişkenler arasında ALT konsantrasyonu, HBV viral yükü ve HBeAg durumu en önemlileridir (86).
2.1.7. Kronik Hepatit B’de Tedaviye Yanıt Kriterleri
Kronik hepatit B’de tedavi yanıtı için kullanılan çeşitli göstergeler; biyokimyasal yanıt, serolojik yanıt, virolojik yanıt, histolojik yanıt ve tam yanıttır (78).
Primer yanıtsızlık: Tedavinin 12. haftasında, HBV DNA duzeyinde < 1 log IU/ml azalma olmasıdır.
Kısmi virolojik yanıt: Nükleoz(t)id tedavisi verilen olgularda ise tedavinin 24. haftasında da HBV DNA düzeyinde > 1 log IU/ml azalma olması fakat real-time PCR ile saptanabilir düzeyde olmasıdır.
Virolojik yanıt: İnterferon tedavisi alan olgularda tedavinin 24. haftasında HBV DNA düzeyinin < 2.000 IU/ml olması, nükleoz(t)id tedavisi verilenlerde ise tedavinin 48. haftada HBV DNA’nın real-time PCR ile saptanmayacak düzeye inmesidir.
Serolojik yanıt: HBeAg pozitif olguda HBeAg serokonversiyonunun olmasıdır.
Biyokimyasal yanıt: Serum ALT seviyesinin normal aralığa gerilemesidir. Histolojik yanıt: Fibroz skorunda kötüleşme olmaksızın nekroinflamatuvar aktivite skorunda en az 2 puan duzelme olmasıdır.
Tam yanıt: Biyokimyasal ve virolojik yanıtla birlikte HBsAg’nin kaybolmasıdır.
Tedavi Sonu Yanıt: Tedavi bitiminde elde edilen yanıttır.
Kalıcı Yanıt: Tedavi kesildikten 6-12 ay sonra elde edilen yanıttır. 2.1.8 Tedavi Sonu Belirteçleri
Kanıtlar tedavinin en önemli sonucunun HBV viral yükün bastırılması olduğunu göstermiştir ki bu parametre siroza ilerleme riski ve HCC gelişimi ile güçlü ilişkilidir (87).
REVEAL-HBV kohort çalışması artan HBV DNA düzeyinin siroza ilerlemenin güçlü bağımsız bir belirleyicisi olduğunu göstermiştir (88). Ek olarak bu kohort çalışması; kontrol grubundaki HBeAg durumu, ALT konsantrasyonu ve siroza göre, 2000 IU/mL’ den büyük HBV DNA düzeyinin HCC için en güçlü risk faktörü olduğunu göstermiştir (89). Ayrıca kontrol grubu ile karşılaştırıldığında başlangıca göre HBV DNA düzeyinin 2000 IU/mL’nin altına düşmesi HCC gelişimi için önemli ölçüde düşük olup risk 2,25 (çalışma grubunda 0,68 ve kontrol grubunda 7.37), HBV DNA düzeyi 2000-20000 IU/ml arasında persiste ettiğinde risk 3.12 (çalışma grubunda 1.09 ve kontrol grubunda 8.89), 20.000-200.000 IU/ml arasında risk 8.85 (çalışma grubunda 3.85 ve kontrol grubunda 20.35) ve 200.000 IU/ml üzerinde risk 16.78 (çalışma grubunda 7.33 ve kontrol grubunda 38.29) bulunmuştur (90).
2.1.9. Günümüzde Mevcut Tedaviler
HBeAg pozitif ve HBeAg negatif hastaların her ikisi için de iki tedavi yaklaşımı mevcuttur: sınırlı tedavi ve uzun süreli baskılama tedavisi. İlk stratejinin amacı HBV’ nin inaktif taşıyıcılık dönemi tamamlandıktan sonra tedavi ile viral replikasyonun baskılanmasının sürdürülmesini sağlamaktır. Bu normal ALT konsantrasyonu, HBV DNA’nın 2000 IU/ml altına düşürülmesi ve özellikle HBeAg pozitif hastalarda HBeAg’ nin anti-HBe’ ye serokonversiyonu olarak belirlenmiştir. Bu tedavi stratejisinde 48 hafta boyunca pegile interferon kullanır. İkinci bir yaklaşım oral nükleoz(t)it analoglarının kullanımı ile hızlı ve uzun süreli viral baskılama elde etmeyi amaçlamaktadır ancak tedavi süresi belirsizdir.
Pegile İnterferon
İnterferonlar; antiviral, antiproliferatif ve immünomodülatör etkili doğal sitokinlerdir. Pegile interferon kullanımının amacı hastaya kısa süreli tedavi verilmesini sağlamaktır. Çünkü pegile interferon yorgunluk, grip benzeri reaksiyon, anemi, pansitopeni ve depresyon (%20-30 hastada) gibi multiple toksisite ile ilişkilidir (91). Tedaviye başlamadan önce ilacın etki edeceği hastaların belirlenmesi önemlidir. Tedaviye olumlu yanıt veren özellikler, düşük HBV DNA düzeyleri, yüksek ALT düzeyleri, HBV genotip A ve B varlığı ve ilerlemiş karaciğer hastalığı olmamasıdır (92,93). Çalışmalar IL28B polimorfizminin tedaviye yanıtı tahmin etmede, daha fazla HBV DNA düşüşü, HBeAg’ nin anti-HBe’ ye daha fazla oranda serokonversiyonu ve HBsAg kaybının CT ve TT polimorfizmine sahip olanlarda CC genotipine sahip olanlara göre daha fazla olduğunu göstermiştir (94).
Standart interferon alfa 9-10 mÜ/haftada 3 gün/4-6 ay, pegile interferon alfa 2a 180 μg/hafta/48 hafta ve pegile interferon alfa 2b 1,5 μg/hafta/48 hafta dozlarında kullanılmaktadır (42, 44).
Pegile interferon etkinliğini değerlendirmek için yapılan büyük çalışmaların birinde, 814 HBeAg pozitif hastaya pegile interferon, lamivudin veya 48 hafta boyunca her ikisinin kombinasyonu verildi ve tedavi kesildikten sonra 24 hafta boyunca hastalar takip edildi. Yalnızca lamivudin alan hastalara kıyasla, HBeAg’nin anti-HBe ‘ye serokonversiyonu interferon monoterapisi (% 32 & % 19, p<0.001)
veya kombinasyon terapisi (%27 & %19, p<0.02) alanlarda anlamlı olarak daha fazla idi (95). Ek olarak interferon verilen 16 hastada HBsAg nin anti-HBs serkonversiyonu gelişirken buna karşın lamivudin verilen hiçbir hastada serokonversiyon gelişmedi (p<0.001). 808 hastanın retrospektif analizinde, HBeAg pozitif HBV genotip A, yüksek ALT konsantrasyonu ve düşük HBV DNA düzeyi olan hastaların HBeAg serokonversiyonu ve HBV DNA 2000 lU / ml’ nin altında olması olarak tanımlanan pegile interferon uzun süreli tedavi yanıtının % 54 tahmini olasılığı vardı (92). İnterferon tedavisi üçte bir hastada başarılı olduğundan, interferon bazlı tedavinin etkinliğini arttırmak için nükleoz(t)id analogları da dahil kombinasyon tedavileri denendi. Ancak, nükleos(t)id analogları veya ribavirin ile kombine interferon içeren rejimlerle HBeAg pozitif ve HBeAg negatif hastalarda tedavi yanıtı düzelmedi (95-97).
Tedavinin süresine bağlı olarak, 544 HBeAg pozitif hasta üzerinde yapılan randomize NEPTUNE çalışması 48 hafta boyunca haftada bir 180 μg pegile interferon verilmesinin (HBeAg serokonversiyonu % 36,2); 24 hafta boyunca 180 veya 90 μg verilmesine göre daha yüksek yanıtla ilgili olduğunu göstermiştir (HBeAg serokonversiyonu sırasıyla %25,8 ve %14,1, p değerleri verilmemiş) (98). Başka bir randomize kontrollü çalışmada, % 94’ ü HBV genotip D’ye sahip toplam 128 HBeAg negatif hastadan, 51 hastaya 48 hafta boyunca 180 μg /hafta pegile interferon; 52 hastaya 48 hafta boyunca 180 μg/hafta ve sonrasında 48 hafta 135 μg/hafta pegile interferon; 25 hastaya 48 hafta 180 μg/hafta pegile interferonla beraber lamivudin ve sonrasında 48 hafta boyunca tek başına pegile interferon 135 μg/hafta verilerek karşılaştırıldı. Bu 48 haftalık tedavi sonrasında, tek başına 96 hafta pegile interferon verilen hastalarda; 48 hafta pegile interferon monoterapisi verilen hastalara göre HBV DNA’nın 2000 IU/mL altına düşüşü çok daha anlamlı bulundu (%28,8 & %11,8; p<0.03). ALT normalizasyon oranı da pegile interferon monoterapisi 96 hafta verilen grupta yüksek bulundu ancak bu istatistiksel olarak anlamlı değildi (%25 & %11,8; p = 0.08) (99). Ancak ilk 48 hafta lamivudin tedavisinin eklenmesi ile tedaviden sonraki 48 hafta boyunca HBV DNA düzeyinin 2000 IU/mL altında sürekli baskılanmasına bakıldığında istatistiksel açıdan anlamlı fark saptanmadı (monoterepi için %28.8 & kombinasyon tedavisi için %20). Pegile
interferon ile ilişkili yan etkiler hastaların %20-30'unda görüldü, ancak bireysel yan etkilerin veri oranları yukarıdaki çalışmalarda nadiren bildirilmiştir.
Nükleoz(t)id analogları
HBV tedavisi için kullanılan lamivudin, adefovir, telbivudin, entekavir ve tenofovir disoproksil fumarat gibi birkaç nükleoz(t)id analoğu mevcuttur. Ancak, uluslararası klavuzlar nükleoz(t)id analoğu olarak naive hastalar için ilk basamak tedavide sadece entekavir ve tenofovir tavsiye eder (33-35). Her iki ilaç da minimal yan etkileri ile genel olarak iyi tolere edilir.
Lamivudin
2’-3’ dideoksi 3’-tiyasitidin’in negatif enatiomeri olan bir sitozin analoğu olup, DNA zincir sentezini bloke ederek HBV replikasyonunu durdurur. Virüsün pregenomik RNA’sı ve mRNA’larının sentezini sağlayan, kapalı, kovalen ve sirküler (ccc)-DNA yapısına etkisi olmamaktadır. Sonuçta, virüs replikasyonu bloke olduğu halde virüs hepatositler içerisinde varlığını devam ettirebilmektedir (38). HBV tedavisinde önerilen doz PO 100 mg/gün’dur. Pediyatrik hastalarda (2-17 yaş) 3mg/kg/gün(maksimum 100mg/gün) tek doz halinde verilir. Aç veya tok karnına alınabilir. Böbrek yetersizliği durumunda doz modifiye edilmelidir.
HBeAg (+) naive hastalarda, 1 yıllık tedavi sonrasında, HBeAg serokonversiyonunun yaklaşık %16-18 civarında olduğu gösterilmiştir (100-102). HBeAg (-) hastalarda, 1 yıllık tedavi sonrası viral DNA süpresyonu; %60-70 arasında gösterilmiştir, ancak tedavi kesimi sonrasında %90 relaps görülmektedir (103-105).
Kompanze ve dekompanze karaciğer sirozlu hastalarda, hastalığın seyrini ve nakile gidişi yavaşlattığı, HCC gelişiminin daha düşük olduğu gösterilmiştir (106,107,137).
Adefovir dipivoxil:
Adenozin monofosfat analoğunun ön ilacı olup nükleotid analoğudur. Aktif formu, hem reverz transkriptazı hem de DNA polimerazı inhibe ederek HBV DNA zincirinin sonlanmasına neden olmaktadır (47, 108). Erişkin dozu 10 mg:/gün’dur.
Alınış şekli aç-tok fark etmez. Karaciğer yetmezliğinde doz ayarlaması gerekmez. Kreatinin klirensi<50ml/dk ise doz ayarlaması gerekir. Böbrek yetersizliğinde doz modifiye edilmelidir.
HBeAg (+) hastalarda, plaseboya göre; histolojik iyileşme, ALT normalizasyonu ve HBV DNA süpresyonunun istatistiksel olarak anlamlı olduğu ve 1 yıllık tedavi sonrasında HBeAg serokonversiyonunun %12 olduğu faz III çalışmaları ile gösterilmiştir (108).
HBeAg (-) hastalarda, 10 mg/gün/48 hafta kullanıldığında, %64 histolojik yanıt, %72 ALT normalizasyonu, %51 DNA negatifleşmesi gösterilmiştir (109).
Telbivudin:
Timidinin L deoksi modifikasyonu olan nükleozid analoğu bir antiviraldir. Fosforilasyon sonrası, aktif formu HBV-DNA polimeraz tarafından sentezlenen DNA zincirine katılabilmek için timidin ile yarışmaktadır (111).
HBeAg (+) hastalarda 600 mg/gün 1 yıllık tedavi sonrasında; HBV DNA negatifleşmesi %60, ALT normalizasyonu %77, HBeAg kaybı %26 olarak saptanmıştır (111, 112).
HBeAg (-) hastalarda 600 mg/gün/1 yıl kullanımı sonucunda; HBV DNA negatifleşmesi %88, ALT normalizasyonu %74 bulunmuştur (111, 112).
Entekavir
2-deoksiguanozin’in karbosiklik analoğu olan nükleozid grubu genetik bariyeri yüksek güçlü bir antiviral ilaçtır. Lamivudin ve adefovirden farklı olarak selektif HBV inhibitörüdür; HIV ve diğer DNA viruslerine etkili değildir. HBV replikasyonunu 3 basamakta inhibe etmektedir; HBV DNA polimeraz, revers transkriptaz üzerinden negatif DNA sarmalının yapımı ve pozitif DNA sarmalının yapımı (110). 0.5 mg ve 1 mg tablet formları vardır. Gıdalar emilimini geciktirir dolayısı ile yemeklerden 2 saat önce veya 2 saat sonra, aç karnına alınmalıdır. Erişkin dozu, daha önceden nükleosid analoğu tedavisi almamış olgularda 0.5 mg/gün; lamivudin-dirençli viremide 1 mg/ gündür. Adolesan 16 yaş olgularda doz, erişkin dozudur. Atılımı idrar yolu ile olduğundan (%60-70’i değiştirilmeden atılır) Clcr<50 ml/dak ise doz ayarlanmalıdır.
HBeAg (+) hastalarda, 48 hafta 0,5 mg entekavir kullanımı sonucunda histolojik yanıt %72, DNA negatifleşmesi % 67 ve biyokimyasal yanıt % 68, HBeAg serokonversiyonu %21 bulunmuştur (113).
HBeAg (-) hastalarda, 48 hafta 0,5 mg entecavir kullanımı sonucunda; histolojik yanıt % 70, virolojik yanıt %90 ve biyokimyasal yanıt % 78 saptanmıştır (114).
Tenofovir Disoproksil Fumarat
Tenofovir, adefovir gibi bir asiklik nükleotit analoğudur. 245 mg tenofovir disoproxil ‘e eşdeğer, 300 mg disoproxil fumarat tabletleri halinde bulunur. Aç veya tok karnına alınabilir. Karaciğer yetmezliğinde doz ayarlaması gerekmez. %70-80’i, değişmeden filtrasyon ve aktif sekresyon ile böbrekler aracılığı ile atılır. Daha az nefrotoksik olması sayesinde günde 300 mg kullanılabilmesi, daha güçlü bir antiviral olarak kullanımına imkan sağlamıştır (115).
HBeAg(+) hastalarda, 300 mg/gün/48 hafta kullanımı sonucunda; HBV DNA negatifleşmesi % 76, ALT normalizasyonu %68, histolojik yanıt %74, HBeAg serokonversiyonu %21 ve HBsAg kaybı %3 saptanmıştır (116).
HBeAg(-) hastalarda, 300 mg/gün/48 hafta kullanımı sonucunda; saptanamaz HBV DNA %93, ALT normalizasyonu % 76, histolojik yanıt % 72 bulunmuştur ve hiçbir hastada HBsAg kaybı gözlenmemiştir (116).
2.1.10. Yüzey Antijeni (HBsAg) Düzeyi Takibi
HBV infeksiyonun tanısı için geleneksel olarak kullanılan HBsAg’nin ticari olarak temin edilebildiği, Architect HBsAg ölçümü (Abbott Diagnostics) (117) ve Elecsys HBsAg II ölçümü (Roche Diagnostics) (118) gibi en son geliştirilmiş iki ölçüm tekniği kullanılmıştır. Son çalışmalar HBsAg titre ölçümlerinin, HBV infeksiyonunun seyrini tahmin etmek ve tedaviye yanıtı değerlendirmek için yararlı olabileceğini düşündürmektedir (119). Çeşitli çalışmalar hastanın klinik seyrini belirlemek için HBsAg ölçümünün yararını göstermiştir. İmmüntoleran aşamasında HBeAg pozitif hastalarda, 25000 IU/mL’den fazla HBsAg değeri hafif karaciğer fibrozis için % 90 pozitif prediktif değere sahiptir (120). Başka bir çalışmada HBeAg
pozitif hastalarda, 38.500 IU/mL veya daha az HBsAg seviyelerinin orta şiddette fibrozis ile ilişkili olduğu gösterilmiştir (121).
HBsAg düzeyleri ayrıca inaktif taşıyıcıları ve HBeAg negatif kronik aktif infeksiyonu olanları ayırt etmede yardımcı olabilir. Çeşitli çalışmalar HBsAg düzeyleri düşük olan inaktif taşıyıcı hastalarda; HBsAg düzeyi 1000 U/mL altında olanların % 87,9 pozitif prediktif değere ve HBV DNA düzeyi 2000 IU/ml altında olanların % 96,7 negatif prediktif değere sahip olduğunu gösterdi (122). REVEAL-HBV çalışma grubu HBsAg 1000 IU/ml altında olmasının daha düşük HCC gelişim riski ile ilişkili olduğunu göstermiştir (91).
HBsAg ve tedaviye yanıt açısından bakıldığında, tedavi öncesi düşük HBsAg değeri ile pegile interferonun daha iyi yanıt ilişkisi belirtilmiş ve HBsAg titrelerinin ilacın devamlı yanıtı için bir tedavi belirteci olarak kullanılabileceği tavsiye edilmiştir (123). Altı aylık tedavi sonrası HBsAg düzeyinin 300 lU/mL altına düşmesi, 12 aylık tedavinin tamamlanmasından sonra uzun süreli tedavi cavabı olarak tanımlanan anti-HBe serokonversiyonu ve HBV DNA düzeyinin 2000 IU/ml’den az olması ile koreledir (124). Ayrıca, 12 hafta boyunca pegile interferon ile tedavi edilen, HBsAg düzeyi düşmeyen hastalarda uzun süreli tedavi cevabı ve HBsAg kaybı ihtimali düşüktür (125).
2.1.11. Tedaviyi Kesme
548 hasta üzerinde yapılan randomize kontrollü bir çalışmadan elde edilen kanıtlara göre pegile interferon; 12.haftada, 24.haftada ve 48 haftalık tedavinin tamamlanması ile HBV DNA düzeyinin 20.000 IU/mL’nin altına ve HBsAg düzeyinin 1500 U/mL altına düşmemesi durumunda tedavi kesilmelidir (33, 134).
Nükeloz(t)id tedavisi, tedaviye başlamadan önce HBeAg pozitif olan hastalarda anti-HBe serokonversiyonu sağlandıktan 6 ila 12 ay sonra ve tedaviye başlarken HBeAg negatif olan hastalarda HBsAg kaybı olduktan sonra kesilebilir. Ancak, tedavi kesildikten sonra relaps oranlarının yüksek olabileceği bildirilmektedir (33, 34, 35).
Nükleoz(t)id analoğu alan HBeAg pozitif 132 hasta üzerinde yapılan tek merkezli bir prospektif kohort çalışması, ortalama 26 ay tedavi alan hastaların 46’sında (%35) HBeAg serokonversiyonu meydana geldiğini göstermiştir. Serokonversiyondan sonra tedaviye devam etmeyen bu hastaların 9'unda ve 6 ay idame tedavisi verilen hastaların sadece 2’sinde uzun süreli tedavi yanıtı alınmıştır (126).
Lamuvidin monoterepisi ile tam yanıt elde edilen (saptanamayan HBV DNA düzeyi, ALT normalleşmesi ve HBeAg kaybı) HBeAg pozitif 178 Koreli hasta üzerinde yapılan retrospektif bir çalışmada, tedavi kesildikten sonraki 5 yıl içinde kümülatif relaps oranı % 30.2 bulundu. Relaps ilk iki yıl içerisinde 40 hastanın 33’ünde meydana geldi (127).
2.1.11.2 HBeAg Negatif Hastalar
HBeAg negatif hastalarda tedaviyi kesme ile ilgili yapılan çalışmalar genellikle küçük örnekler üzerinde yapılmıştır. Dört ya da beş yıl adefovir ile tedavi edilen 33 Yunan hastanın incelendiği bir gözlemsel kohort çalışmasında; tedavi kesildikten 6 yıl sonra 18 hasta 2000 IU / ml altında HBV DNA değerine sahipti ve 13 hastada HBsAg kaybı mevcuttu (128).
2 yıldan uzun süre saptanmayan HBV DNA düzeylerinin olduğu 184 HBeAg negatif hastanın entekavir tedavisi kesildikten sonraki relaps oranlarının değerlendirildiği geniş bir çalışmada; tedavi kesildikten sonraki 24. Haftada % 74,1 ve 48.haftada % 91,4 yüksek relaps oranları bildirildi (129). Ortalama 3 yıl nükleoz(t)id analogları ile tedavi sonrası saptanamaz HBV DNA düzeyi ve Anti-HBV DNA aşısı yapılan hastaların incelendiği randomize kontrollü bir çalışmada; tedaviyi kesmenin %97 HBV reaktivasyonu ile ilişkili olduğu ve nükleoz(t)id analoğu tedavisi kesilmesi sonrası Anti-HBV DNA aşısının relaps oranlarını düşürmediği bildirildi (130). Nükleoz(t)id analoglarının kesilmesinden sonra yüksek nüks oranı göz önüne alındığında, tedavi kesilmesi özellikle HBeAg negatif hastalarda dikkatli yapılmalıdır.
Aşı 0, 1 ve 6.aylarda veya 0, 1, 2 ve 12.aylarda yetişkinlerde deltoid, bebeklerde uyluktan kas içine uygulanır. Herhangi bir aşı ile başlanan aşı programına diğer bir aşı ile devam edilebilir. HBV için bulaş riski olanlarda uygun aşılama ile etkin antikor düzeyi oluşup, oluşmadığı kontrol edilmelidir. Aşı sonrası koruyucu antikor düzeyi saptananlarda (>10 IU/ml) ilave hatırlatma dozlarına gerek yoktur (131).
Çalışmaya Dicle Üniversitesi Tıp Fakültesi Hastanesi İç Hastalıkları Anabilim Dalı Gastroenteroloji Kliniği ve polikliniğinden izlenmiş veya izlenmekte olan tenofovir veya entekavir başlanıp tedaviye devam eden kronik HBV enfeksiyonlu hastalar dahil edildi. Hastaların verileri dosyalar retrospektif olarak taranarak elde edildi. Hastaların bazıları daha önce interferon ve diğer oral nükleoz(t)id analogları almıştı.
Kronik HBV dışında başka bir nedene bağlı kronik karaciğer hastalığı olmayan (HCV, HDV, HIV, OİH, metabolik karaciğer hastalığı, alkol kullanımı) ve kronik HBV’ye bağlı kompanse sirozu olan hastalar çalışmaya dahil edildi.
Karaciğer nakli, immün supresyon tedavisi, kontrol altına alınmamış diyabet, gebelik, dekompanse siroz durumu olan hastalar çalışma dışı bırakıldı.
Hastalardan sadece tenofovir ya da entekavir monoterapi tedavisi alanlar çalışmaya dahil edildi; tenofovir ile beraber entekavir kombine tedavisi alan hastalar çalışma dışında tutuldu.
HBsAg, Anti-HBs, HBeAg, Anti-HBe, HBV-DNA, AST, ALT incelemeleri yapılarak tanısı konulan ve sadece tenofovir ya da entekavir kullanan toplamda 400 hasta çalışmaya dahil edildi.
HBsAg, Anti-HBs, HBeAg, Anti-HBe seviyeleri Dicle Üniversitesi Tıp Fakültesi Moleküler Mikrobiyoloji ABD Seroloji laboratuvarında Cobas E601- E411 cihazı ile Roche kiti kullanılarak ölçülmüştür. HBV DNA değerleri Dicle Üniversitesi Tıp Fakültesi Mikrobiyoloji ABD Seroloji laboratuvarında Cobas Amplipre ile izole edilip, Cobas Taqman cihazı ile PCR olarak Quantitative kiti ile çalışılmıştır. HBV DNA sonucu IU/ml birimiyle belirtilmiştir. Test en az 1 IU/ml, en fazla 1.70x10^8 IU/ml virüsü saptayabilmektedir, ancak bazı hastaların dış merkez sonuçları da çalışmamızda kullanılmıştır.
ALT, AST, ALP, GGT ve total bilurubin gibi biyokimyasal analizler Dicle Üniversitesi Tıp Fakültesi biyokimya laboratuvarında Architec C16000 cihazı ile Abbott kiti kullanılarak ölçülmüştür. Hastaların ALT düzeyinin referans aralığı 0-35 U/L; AST düzeyinin referans aralığı 0-30 U/L; ALP düzeyinin referans aralığı 40-150 U/L; GGT düzeyinin referans aralığı 5-55 U/L ve total bilurubin düzeyinin referans aralığı 0,2-1 mg/dl olarak belirtilmiştir.
Hastaların başlangıç, 3. Ay, 6. ay, 9. ay, 12.ay ve sonrasında 6 aylık aralıklarla HBV DNA, ALT ve AST değerlendirmeye alındı.
Başlangıç, 6. ay, 12.ay ve sonrasında 12 aylık aralıklarla HBsAg, Anti-HBs, HBeAg ve Anti-HBe ayrıca başlangıç, 6. ay ve 12. ay ALP, GGT ve total bilurubin değerlendirmeye alındı.
Hastaların karaciğer biyopsilerinin değerlendirilmesinde Modifiye Knodell skorlaması (İshak) kullanılmış, başlangıç hepatik aktivite indeksi (HAI) (grade) ve fibrozis (stage) skorları kaydedilmiştir.
İstatiksel İnceleme
Hasta verileri dosyalar retrospektif olarak tarandıktan sonra MS Excel programıma kaydedildi. Daha sonra sayısal veriler SPSS 18.0 programına aktarılıp istatistiksel inceleme yapıldı. Kategorik olmayan ve normal dağılım gösteren veriler ortalama ± standart sapma (SD) ile gösterildi. Normal dağılım göstermeyen ve alt-üst sınırı geniş aralıkta olan veriler ortanca ve (alt sınır-üst sınır) olarak gösterildi. Entekavir ve tenofovir kullanan hastaların birbirleriyle karşılaştırılmasında Mann Whitney U analizi yapıldı. Normal dağılım gösteren verilerin karşılaştırılmasında Student’s t testi kullanıldı. Kategorik verilerin karşılaştırılmasında Ki kare testi uygulandı. Sonuçlar: anlamlılık; p < 0.05 düzeyinde değerlendirilmiştir.