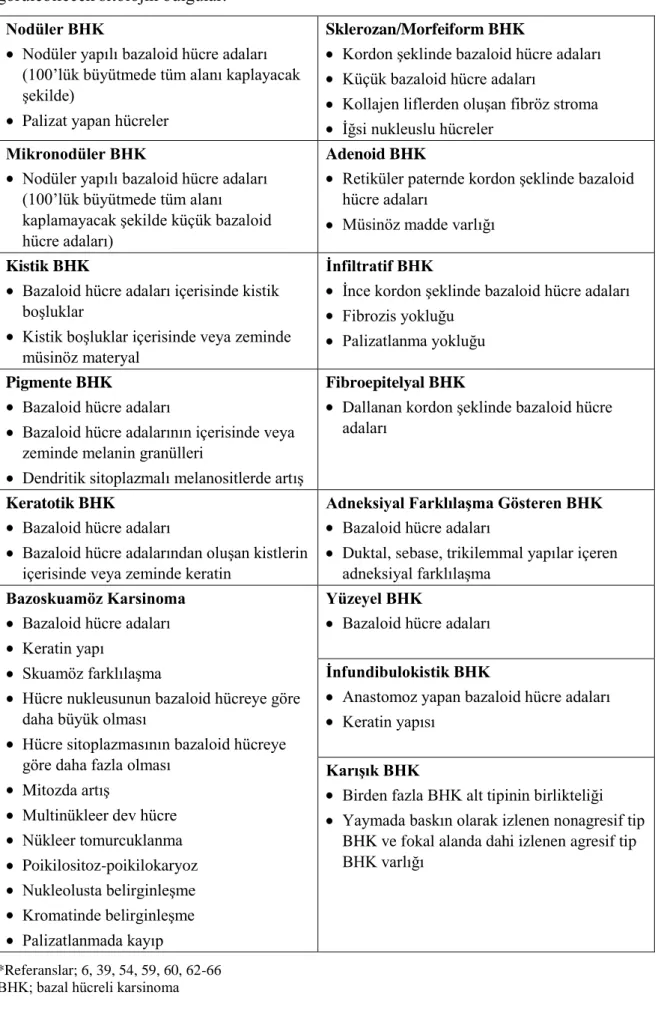
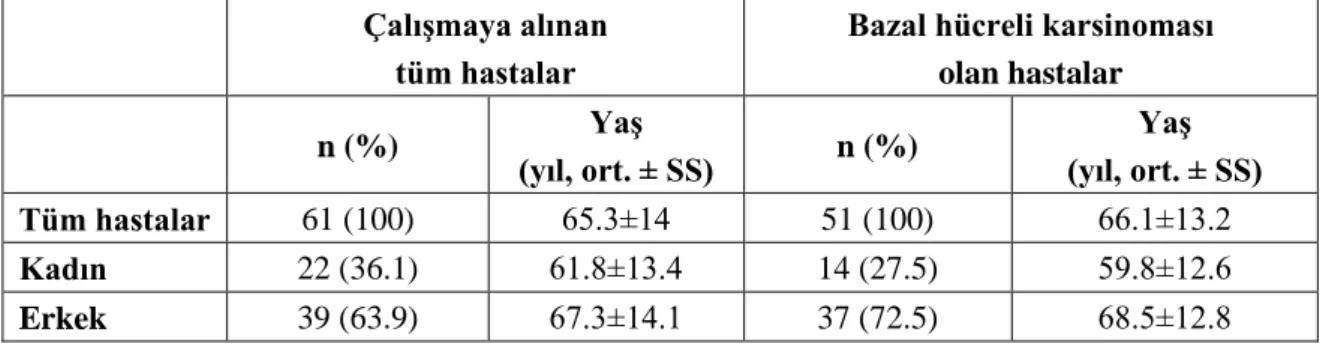
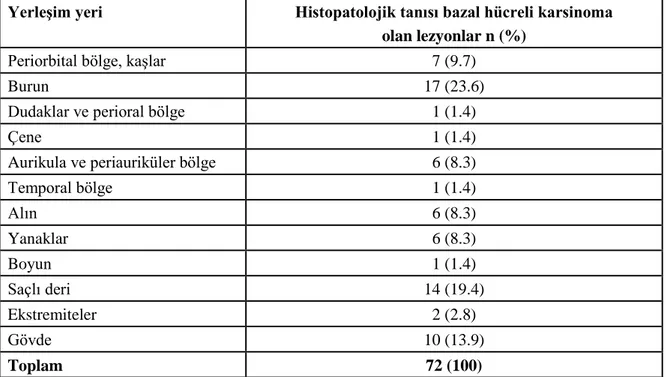
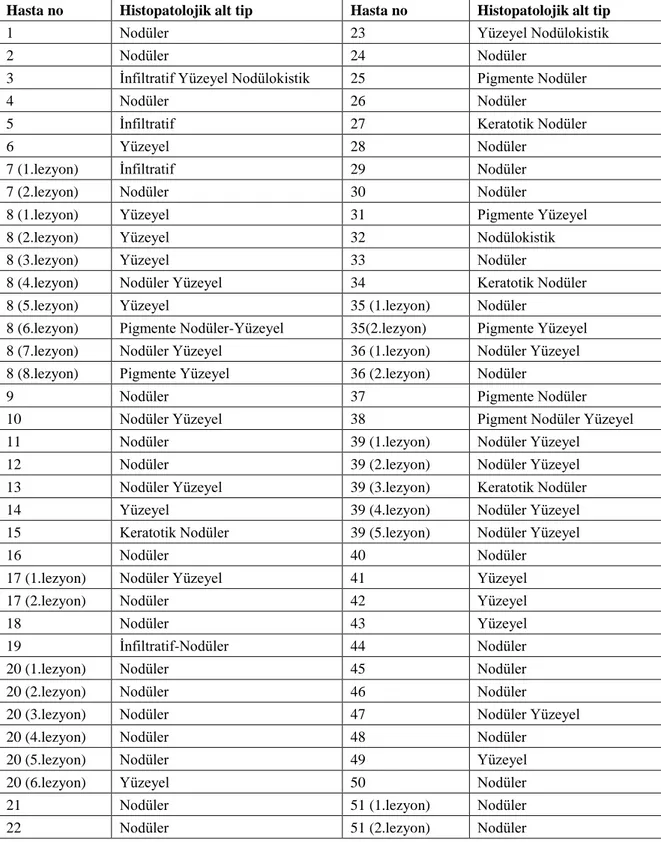
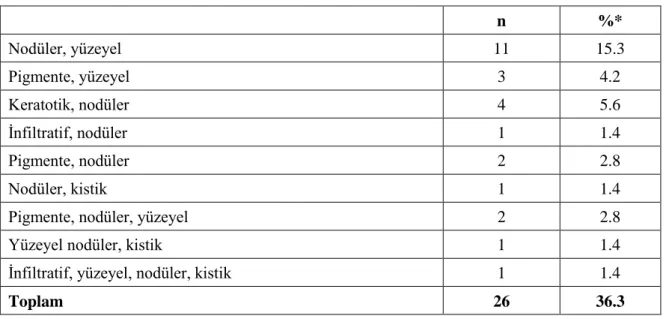
Tzanck yayma testinin bazal hücreli karsinomanın tanısında ve alt tiplerinin belirlenmesindeki yeri
Tam metin
Şekil
Benzer Belgeler
Bazal hücreli adenom, tükrük bezlerinde sıklıkla parotis bezinde nadir rastlanan epitelyal bir tümör olup, monomorfik adenomların bir alt tipidir.. Bazal hücreli adenom
Çalışmamızda yüzde anatomik bölgelerde gözlenen BHK sayısı ile füzyon alan sayısının kıyaslanması ve sonucunda BHK gelişiminde füzyon alanlarının
Clear cell basal cell carcinoma with neuroendocrine differentiation Nöroendokrin diferansiyasyon gösteren berrak hücreli bazal..
Histopatolojik parametreler olarak subtip, hücresel atipi derecesi, peritümöral enflamatuvar infiltrat derecesi (yok; hafif: tümörün <%25’ini çevreleyen infiltrat;
Nevoid bazal hücreli karsinom sendromu (Gorlin sendromu) çok say›da bazal hücreli karsinomlar (BHK), mandibulada kerato- kistler, palmoplantar çukurcuklar ve falks
Sonuç olarak; istatistiksel olarak bak›ld›¤›n- da SHK’da Bax pozitifli¤i orta ve az diferansiye SHK’larda anlaml› olarak yüksek tesbit edilirken, iyi di- feransiye
Klas 2 HLA antijenleri ve BHK aras›ndaki iliflkiyi araflt›rmak için Czarnecki ve arkadafllar›n›n yapt›¤› 74 hastal›k çal›flmaya göre HLA-DR 1 istatistiksel
Bu çalışmada, Aydın ilinde saptanan Blastocystis alt tiplerinin belirlenerek Blastocystis spp.’in laboratuvar tanısında kullanılan direkt mikroskopi, kültür ve