T.C.
D CLE ÜN VERS TES TIP FAKÜLTES
Gö üs Hastal klar ve Tüberküloz Anabilim Dal
SOLUNUMSAL YO UN BAKIM ÜN TES NDE ZOLE ED LEN
M KROORGAN ZMALAR VE ANT B YOT K D RENÇ
DURUMLARI
(UZMANLIK TEZ )
Dr. Hüseyin BEYAZIT
TEZ YÖNET C S
Yard. Doç. Dr. Güngör ATE
Ç NDEK LER SAYFA ÖNSÖZ ... i KISALTMALAR ii TANIMLAR iii G R VE AMAÇ . 1 -2 GENEL B LG LER 3-23 MATERYAL VE METOD 24
STAT ST KSEL ANAL Z .. 25
BULGULAR . 26-35
TARTI MA 36-42
SONUÇ VE ÖNER LER 43
ÖZET 44
SUMMARY . 45
ÖNSÖZ
Uzmanl k e itimim süresince bilgi ve tecrübelerinden yaraland m Anabilim Dal Ba kan m z Prof. Dr. A. Füsun Topçu, ö retim üyelerimiz Prof. Dr. Mehmet Co kunsel, Prof. Dr. M. Recep I k, Prof. Dr. Abdurrahman enyi it, Doç. Dr. Gökhan K rba , Yard. Doç. Dr. Tekin Y ld z, Yard. Doç.Dr. Levent Aky ld z, Yard. Doç. Dr. Güngör Ate , Yard. Doç. Dr. A. Çetin Tanr kulu, Yard. Doç. Dr. Abdurrahman Abakay ve Yard. Doç. Dr. Cengizhan Sezgi ye te ekkür ederim.
Rotasyonlar m süresince bilgi ve deneyimlerinden faydalanma imkân buldu um, ç Hastal klar , Enfeksiyon Hastal klar ve Klinik Mikrobiyoloji, Radyoloji, Kardiyoloji Anabilim Dallar n n de erli ö retim üyeleri ve asistanlar na te ekkür ederim.
Tezimin haz rlanmas a amas nda, de erli görü ve önerileri ile yol gösteren ve ho görüsü ile pozitif enerji veren tez yöneticim Yard. Doç. Dr. Güngör Ate e te ekkür ederim.
Klinikte beraber çal maktan mutluluk duydu um, de erli hocalar m, sevgili doktor, hem ire ve personel arkada lar ma, huzurlu bir çal ma ortam sa lad klar için ayr ca te ekkür ederim.
Asistanl m n en zor günlerinde her zaman deste ini gördü üm sevgili aileme ve e im Remziye ye te ekkür ederim.
Dr. Hüseyin BEYAZIT 2009-Diyarbak r
KISALTMALAR
MIC: Minimal inhibitör konsantrasyon KNS: Koagülaz negatif stafilokoklar YBÜ: Yo un bak m üniteleri
MRSA: Metisilin resistant Staphylococcus aureus (Metisilin dirençli S. aureus) MSSA: Metisilin sensitive Staphylococcus aureus (Metisilin duyarl S. aureus)
GISA: Glikopeptid intermediate sensitive S. aureus (Glikopeptidlere orta düzeyde
duyarl S. aureus)
VRE: Vancomysin resistant enterococcus (Vankomisin dirençli enterokok)
VISA: Vancomysin intermediate sensitive S. aureus (Vankomisine orta düzeyde duyarl
S. aureus)
NNIS: National Nasocomial Infections Surveillance EPIC: European Prevalence of Infection In Intensive Care
GSBL: Geni letilmi spektrumlu beta-laktamazlar (Extended spectrum beta-lactamases,
ESBL)
APACHE: Acute Physiology and Chronic Health Assesment KOAH: Kronik obstrüktif akci er hastal
CD D: Clostridium difficile yle ili kili diare PBP: Penisilin ba layan protein
OMP: Outer membrane protein (d membran proteini) AAC: Asetiltransferazlar
ANT: Nükleotidil transferazlar APH: Fosfotransferazlar
TANIMLAR
Hastane Enfeksiyonu: Hasta hastaneye yatt nda inkübasyon döneminde de ilse veya o enfeksiyonun belirti ve bulgular yoksa hastanede ortaya ç kan enfeksiyonlar nozokomiyal olarak de erlendirilir. Genellikle nozokomiyal enfeksiyonlar hasta hastaneye yatt ktan 48-72 saat sonra ve taburcu olduktan sonra 10 gün içinde geli ir.
Endemi, Endemik: Bir enfeksiyonun bir toplumda belirli ya da al lm s kl kta görülmesini ifade eder. Örne in; kolera Ganj deltas nda, s tma Çukurova bölgesinde endemiktir.
Epidemi, Epidemik: Salg n anlam na gelir. Bir hastal n belirli bir co rafi bölgede ve belirli bir zaman periyodunda her zaman görüldü ünden daha fazla görülmesidir. Epidemi tan m yapabilmek için hastal n o bölgede daha önceki prevalans ve insidans n bilmek gerekir.
Post Antibiyotik Etki: Antibiyotiklerin, mikroorganizmalara etkili minimal inhibitör
konsantrasyon (MIC) de erlerinin alt ndaki kan düzeylerinde de bakterileri öldürme yeteneklerinin sürüyor olmas n ifade eder.
ntrinsik Direnç: Bir mikroorganizman n yap s nedeniyle antibiyotiklere kar dirençli
olu u intrinsik direnç olarak tan mlanmaktad r.
Çapraz Direnç: Bir antimikrobik maddeye kar dirençli hale gelen bir mikroorganizma türünde bu kemoterapötik maddeye yap ca veya etki tarz bak m ndan yak n di er antimikrobiklere kar da direnç geli ebilir, bu duruma çapraz direnç (cross resistance) denir.
Çok laca Direnç: Mikroorganizman n yap s ve etkisi farkl birçok antimikrobik
maddeye kar dirençli hale gelmesi durumuna çok ilaca dirençlilik (multiple-drug resistance) denir.
Geni letilmi Spektrumlu -laktamaz: Geni letilmi spektrumlu beta-laktamaz (GSBL) veya extended spectrum betalactamases (ESBL) olarak tan mlanan bu -laktamazlar n temel özelli i dar ve geni spektrumlu sefalosporinleri, penisilinleri ve monobaktamlar (aztreonam) hidrolize ederek inaktive etmeleri ve sefamisinler (sefoksitin, sefotetan) ile karbapenemleri inaktive etmemeleridir.
De i tirilmi Antibiyoterapi: Hastada mevcut olan enfeksiyonun tedavisi için
kullan lan antibiyoti in, tedavi ba ar s zl veya üreyen kültür sonucuna göre kullan m n n sonland r larak, ba ka bir gruptan antibiyotik ile tedaviye devam edilmesidir.
Geni letilmi Antibiyoterapi: Hastada mevcut olan enfeksiyonun tedavisi için
kullan lan antibiyoti e, tedavi ba ar s zl veya üreyen kültür sonucuna göre, gram pozitif etkinli in sa lanmas veya art r lmas amac yla ba ka bir gruptan antibiyoti in eklenmesidir.
Primer Kan Yoluyla Olu an Enfeksiyon: Kan kültüründe, patojen oldu u bilinen bir
mikroorganizman n izole edilmesi ve bu patojenin ba ka bir yerdeki enfeksiyon ile ili kili olmamas d r.
G R VE AMAÇ
Yo un bak m üniteleri (YBÜ); ciddi hastal klar nedeniyle yak n takip gerektiren ve mortalitesi yüksek hastal klar olan hastalar n izlendi i özel birimlerdir. Bu tür kritik hastalar n bak m önemli düzeyde emek ve özen gerektirmesinin yan nda ciddi düzeyde ekonomik maliyete de yol açmaktad r.
YBÜ ne yatan hastalar, hastaneye yatan tüm hastalar n %5-10 kadar n olu turmas na kar n, hastane enfeksiyonu geli en hastalar n yakla k %25 inden sorumlu tutulmaktad r. Bu ünitelerde yatan hastalarda di er cerrahi ya da medikal servislere göre 5-10 kat daha fazla oranda hastane enfeksiyonu görülmektedir (1-3). Bu enfeksiyonlar n önemli bir bölümünü pnömoniler ve kan dola m na ait enfeksiyonlar olu turmaktad r. Özellikle dirençli mikroorganizmalar n etken oldu u hastane enfeksiyonlar artm morbidite, mortalite ve yüksek maliyete neden olmas nedeniyle önemlidirler (1-6).
YBÜ ne yatan hastalar n primer yat nedeni ne olursa olsun yo un bak mda yat süreleri uzad kça, entübasyon, kateter uygulamalar , tan sal invaziv giri imler, uygun olmayan antibiyotik kullan m , sa l k personeli taraf ndan antibiyotik dirençli bakterinin direk ta n m gibi nedenlerle hastane enfeksiyonu geli me riski artmaktad r. YBÜ ne yatan hastalar n %60 dan fazlas yatt süre içerisinde bir ekilde antibiyotik kullanmaktad r (7). YBÜ nde enfeksiyonlar n tedavisinde kullan lan çe itli antimikrobiyal ajanlara ba l geli en, antibiyotiklere dirençli mikroorganizmalar n yol açt hastane enfeksiyonlar , kaç n lmaz bir gerçektir. Yo un antibiyotik kullan m n n, hem gram pozitif, hem de gram negatif mikroorganizmalarda ciddi boyutlarda direncin olu mas nda önemli katk s vard r. YBÜ nde özellikle artlar optimal olmad nda ve çal anlar n hastalara oran dü ük düzeylerde ise, problemler daha da artmaktad r (7,8).
Özellikle üçüncü ku ak sefalosporinler, florokinolonlar ile karbapenem türevlerinin kullan m , dirençli mikroorganizmalarla olu an hastane enfeksiyonlar n n geli iminde önemli rol oynamaktad r. Antibiyotiklere dirençli etkenlerin neden oldu u enfeksiyonlar, sadece morbidite ve mortaliteyi art rmakla kalmay p, ayn zamanda hastanede yat süresinde uzama, maliyet ve de i ik medikal komplikasyonlarda art a sebep olmaktad r (9-12).
Metisiline dirençli Staphylococcus aureus (MRSA), glikopeptidlere orta düzeyde duyarl S. aureus (GISA), vankomisine dirençli enterokoklar (VRE), geni letilmi spektrumlu beta-laktamaz (GSBL) üreten Escherichia coli, Klebsiella türleri ve di er
Enterobacteriaceae ailesinin üyeleri, Acinetobacter türleri ve Pseudomonas aeruginosa günümüzde yo un bak mlarda antibiyotik kullan m n n neden oldu u hastane enfeksiyonlar ndan sorumlu tutulan belli ba l dirençli mikroorganizmalard r (4,8,13,14).
Yeni kullan ma giren her antibiyotik ba lang çta olumlu klinik sonuçlar verse de, yo un kullan m , yetersiz dozda ve endikasyon d uygun olmayan kullan m gibi nedenlerle, antibiyotik direncine neden olmaktad r. Her kullan ma giren antibiyotik ile bu k s r döngü tekrarlanmaktad r. Bulunan her yeni silaha kar , mikroorganizmalar evrimsel süreci i leterek, antibiyotik dirençli yeni su lar n do mas n sa lamaktad r (15).
Antibiyotiklere kar direnç geli iminde çok say da mekanizma rol oynamaktad r. Kromozomal mutasyonlar, plazmid ya da transpozon transferleri ya da türler aras nda gerçekle en genetik transferler, en s k gözlenen direnç mekanizmalar d r. Özellikle, yo un antibiyotik kullan m sonras nda duyarl su lar n ortadan kald r larak, dirençli olanlar n seçilmesi, direncin geli mesindeki ana mekanizmay olu turmaktad r. Antibiyotik direnci yayg n olarak kullan m süresi ve miktar ile de do ru orant l olarak gerçekle mektedir. Hastanede enfeksiyon hastal klar n n tedavisi için kullan lan birçok antibiyotik mevcuttur: Aminoglikozidler, karbapenemler, sefalosporinler, florokinolonlar, penisilinler ve vankomisin d nda yeni uygulanmaya ba lan lan; linezolid, tigesiklin, daptomisin, kinupristin ve dalfopristin gibi. Bu antibiyotiklerin direnç geli imi üzerindeki etkileri önem ta makta ve bu konu yo un olarak ara t r lmaktad r (12).
Her hastanenin, hatta ayn hastane içindeki farkl yo un bak mlar n kendine özgü bir patojen floras ve antibiyotik direnç paterni mevcuttur (16). Bu farkl l k klinisyenin hastane enfeksiyonlar na bak aç s n etkileyerek uygulanacak ampirik antibiyoterapiye yön verebilmektedir. Sepsiste ve pnömoni de oldu u gibi erken dönemde do ru ve etkili antibiyotik tedavisinin ba lanmas mortalite, morbidite ve tedavi maliyetlerini olumlu yönde etkilemektedir (3,17). Uygun olmayan antibiyoterapi uygulamalar dirençli patojenlerin geli imine de neden olmaktad r (7).
Biz de bu çal mam zda; solunumsal yo un bak m ünitemizde yatan hastalarda enfeksiyonlara neden olan patojenler ve bu patojenlere ait antibiyotik direnç paternlerini tespit ederek, yo un bak m m za ait verileri ortaya ç karmay amaçlad k.
GENEL B LG LER
Hastane enfeksiyonlar (nozokomiyal enfeksiyonlar), hasta hastaneye ba vurdu unda inkübasyon döneminde olmayan, daha sonra geli en veya taburcu olduktan sonra ortaya ç kabilen enfeksiyonlard r. De i ik çal malarda yatan hastalar n %3.1-14.1 inde geli ti i tespit edilmi tir (18,19). Ülkemizde total sürveyans yap lan az say da hastanede %5 civar nda oranlar saptanm t r (20). Amerika Birle ik Devletleri (ABD) nde hastane enfeksiyonlar n n yat süresini ortalama 4 gün uzatt , direkt olarak y lda 60.000 ölüme yol açt ve 10 milyar dolar fazla harcamaya sebep oldu u tespit edilmi tir (21). Ülkemizde yap lan bir çal mada da hasta ba na 1582 dolar fazla harcamaya yol açt saptanm t r (22). Hastane enfeksiyonlar endemik ve epidemik olarak iki ana grupta incelenebilir. Endemik h zlar n ortaya konulabilmesi ve epidemilerin sa l kl olarak tan nabilmesi için hastane enfeksiyonlar n n sürveyans önem ta maktad r.
ABD de süre giden National Nasocomial Infections Surveillance (NNIS) sistemi en s k görülen dört enfeksiyon (üriner, cerrahi yara, pnömoni ve bakteriyemi) ve di er enfeksiyonlar kategorilerinde sürveyans uygulamaktad r. Bu sistem ile 1980 lerin ba ve sonu aras ndaki süreçte hastane enfeksiyonu etkenlerinde dirençli patojenlere do ru bir kayma gözlenmi tir (23). Koagülaz negatif stafilokok ve Candida da belirgin art gözlenmi olup, E. coli ve K. pneumoniae de bir miktar azalma olmu tur. S. aureus, P. aeruginosa, Enterobacter spp. ve enterokoklarda minör art lar olmakla birlikte bu patojenlerde çok önemli antibiyotik direnç geli imi gözlenmi tir. 1996-1999 y llar aras nda NNIS hastanelerindeki yo un bak mlarda nozokomiyal S. aureus izolatlar n n %39.4 ü MRSA, Enterokoklar n ise %16.7 si vankomisin dirençli (VRE) su lard r (24). Ülkemizde y llard r MRSA oran e itim hastanelerimizde %50 nin üzerinde seyretmektedir. VRE ise Avrupa ve ABD nin aksine uzunca bir süre ülkemizde görülmemi , ancak son birkaç y l içinde s n rl say da üniversite hastanesinde küçük epidemilere yol açm t r. NNIS hastanelerinde 3. ku ak sefalosporinlere dirençli K. pneumoniae a yo un bak mlarda bile %6.5 oran nda rastlan rken, ülkemizde yap lan bir çal mada K. pneumoniae yo un bak m ünitelerinde %12 oran nda izole edilmi tir. (25). Ayr ca ülkemizdeki nozokomiyal K. pneumoniae izolatlar %60 ve %62 oranlar nda geni letilmi spektrumlu beta-laktamaz (GSBL/ESBL) üretmektedir (25,26).
Yo un bak mlarda yatan hastalar genellikle kateterize edilmekte ve kateterize hastalar n %10-20 sinde bakteriüri geli mektedir. Bakteriüri için en önemli risk faktörü kateterin vücutta bulunma süresidir. Genellikle 2-4. günler aras ve 3.aydan sonra olmak üzere iki noktada enfeksiyon riski çok fazla yükselmektedir (27). Bakteriürili hastalar n ancak %20-30 unda üriner enfeksiyon semptomlar geli mektedir (28).
Entübe hastada tekrarlanan gram boyama ve kültür sonuçlar klinik durumdaki de i ikliklerle birle tirildi inde, ba lang ç antibiyotik tedavisinin yönlendirilmesinde yararl olabilmektedir. Endotrakeal aspirat kültürleri %89 duyarl l a sahip olmas na ra men özgüllü ü oldukça dü üktür (%14) (29).
Hastane enfeksiyonlar n önlemede en önemli faktör olan sa l k çal anlar n n el y kamaya motive edilmesi yeterince ba ar l olmam t r. Bunun d nda steril olmayan eldivenlerin sürekli kullan m ve hastalar aras de i tirilmesi, alkol içeren el dezenfektanlar n n kullan m gibi yakla mlar yo un olarak ara t r lmaktad r. Antibiyotik dirençli bakterilerin ortaya ç k tüm çabalara ra men önlenememektedir.
SIK GÖRÜLEN M KROORGAN ZMALAR
Geni letilmi Spektrumlu Beta-Laktamaz (GSBL) olu turan mikroorganizmalar:
Beta-laktam antibiyotikleri hidrolize ederek inaktif hale getiren beta-laktamaz enzim üretimi, ba ta Enterobacteriaceae üyeleri olmak üzere birçok bakteri türünün en önemli direnç mekanizmalar ndan birisidir. Bugüne kadar 350 ye yak n beta-laktamaz enzimi tan mlanm t r (30). Bunlar n yakla k 150 si geni letilmi spektrumlu beta-laktamazlar (GSBL, extended-spectrum beta-lactamases, ESBL) olup plazmidik özellikleri nedeniyle bakteriler aras nda transfer edilebilir (30,31). GSBL üreten mikroorganizmalarla enfeksiyon geli iminde önceden antibiyotik kullan m (penisilinler, üçüncü ku ak sefalosporinler, florokinolonlar, aminoglikozidler, karbapenemler vb), yüksek Acute Physiology and Chronic Health Assesment (APACHE) skorlar , mekanik ventilasyon uygulamas , üriner kateterizasyon, arteriyel kateterler, santral venöz kateterler, barsak kolonizasyonu, acil bat n cerrahisi, gastrostomi ya da jejunostomi tüpü, hastanede yat süresi, yo un bak m ünitesinde kal süresi, ya , dü ük do um a rl gibi çok say da risk faktörü mevcuttur. Bu faktörler aras nda en önemlisi önceden antibiyotik kullan m d r (32,33).
Escher ch a Coli ve Klebsiella spp.:
E. coli nin do al ya ama ortam , insan ve hayvanlar n ba rsaklar olup ba rsaklardaki gram negatif aerobik bakterilerin en büyük k sm n olu tururlar. E. coli
hastane ortam nda ya amas zor oldu undan, bu bakteriye ba l hastane enfeksiyonlar n n ço u endojendir ve ba rsak floras ndan köken almaktad r (34-36).
E. coli hastane enfeksiyonlar nda önemli bir etkendir. Üriner sistem enfeksiyonlar nda en s k rastlanan etkendir ve nozokomiyal sepsislerin yakla k %15 inin etkeni E. coli dir (35,36).
Klebsiella türleri do ada, insan ve hayvanlar n ba rsaklar nda oldukça yayg nd r. Klebsiella türleri insan d k s nda %5-38, nazofarenkste ise %1-6 oran nda bulunur. Genellikle bu bölgelerde floran n geçici üyeleri olarak kabul edilirler. K. pneumoniae özellikle alkolizm, diabetes mellitus ve kronik obstrüktif akci er hastal (KOAH) gibi solunum sistemi savunmas n bozan ciddi altta yatan hastal olan hastalarda, nekrotizan lober pnömoniye neden olur (37,38).
Üçüncü ku ak sefalosporinlerin kullan m , GSBL pozitif Klebsiella türlerinin kolonize olmas ve enfeksiyon olu turmas nda çok önemli bir risk faktörüdür. YBÜ nde sa l k personellerinin elleri arac l yla hastadan hastaya geçi i önemli bir bula yoludur. Hastanede kalma süresinin uzamas na ba l olarak kolonizasyon oranlar artmaktad r (38,39).
E. coli ve Klebsiella türlerinin beta-laktam (aminopenisilinler, geni -spektrumlu sefalosporinler, üreidopenisilinler, beta-laktamaz inhibitör kombinasyonlar , monobaktamlar, karbapenemler) ve ba ka gruplarda yer alan antibiyotiklere (kinolonlar, aminoglikozidler, trimetoprim sulfametoksazol) kar in-vitro direnci ciddi boyutlardad r. GSBL üreten E. coli ve Klebsiella türlerinin s kl co rafi alanlara, hastanenin hizmet verdi i etkinliklere, populasyonun ya ve hastalardaki e lik eden hususlara ba l olarak de i mektedir (40).
Enterobacter spp.:
Enterobacter türleri toprakta, suda, bitkilerde, süt ürünlerinde, insan ve hayvanlar n kal n ba rsaklar nda ve d k s nda bulunur. Enterobacter cinsi, toplum kökenli enfeksiyonlarda da etken olarak kar m za ç kmakla birlikte, bu mikroorganizmayla olu an enfeksiyonlar n büyük bir k sm hastane enfeksiyonudur (41-43).
Enterobacter cinsi içerisindeki türler aras nda, insanlardaki enfeksiyonlardan en s k sorumlu tutulanlar Enterobacter aerogenes ve Enterobacter cloacae d r (44,45).
Enterobacter türlerinde tedavi s ras nda direnç geli imi, üzerinde önemle durulmas gereken bir olayd r. Karbapenem grubunda yer alan antibiyotiklere direnç geli imi de giderek artmaktad r (8,40).
GSBL üreten mikroorganizmalar n yol açt enfeksiyonlar n tedavisinde ya anan de i ik sorunlar mortalite oranlar n n artmas na da do rudan etkili olmaktad r. Özellikle tedavinin ba lang c nda uygun olmayan antibiyotik kullan m n n, uygun antibiyotik kullan m na göre önemli ölçüde mortaliteyi art rd bilinmektedir (11).
Acinetobacter türleri
Acinetobacterler, moraksella ve psikobakterlerle birlikte Moraxellaceceae ailesi içinde bulunan k sa, tombul, daha çok kokkoid formda gram negatif çomaklard r. DNA hibridizasyon çal malar na göre Acinetobacter genusu heterojen özellik gösterir. DNA-DNA homolojisine göre imdiye kadar 19 genomik grup saptanm t r. Acinetobacter calcoaceticus, Acinetobacter baumannii, genomik tür 3 ve 13 TU aras nda benzerlik vard r. Bundan dolay birçok ara t r c grubu taraf ndan A. calcoaceticus-A. baumannii kompleks olarak tan mlanm t r. A. baumannii hastane enfeksiyonlar nda en s k kar la lan genomik türdür. Acinetobacter lwoffii ve Acinetobacter johnsonii de A. baumannii den sonra en s k kar la lan türlerdir (46,47).
Acinetobacter türleri toprakta ve suda bulunurlar. Vücudun koltuk alt , kas klar, parmak aralar gibi nemli bölgelerinin floras nda yer al rlar. Sa l kl ki ilerin yakla k %25 i normal floralar nda bu bakterileri ta rlar. Bazen sa l kl ki ilerin oral kavitesinde ve solunum yollar nda da bulunur. Ancak yine de sa l kl ki ilerde ta y c l k hastanede yatanlara göre oldukça azd r (47,48).
Hastane çevresinde kal c özellik gösterirler. Hastane ortam nda birçok farkl materyalden izole edilmi lerdir. Kolonize hasta mevcut de ilken hava yoluyla kontaminasyon nadirdir, ancak kolonize ve/veya enfekte hastalar n çevresindeki respiratuar vb. cihazlar n ve havan n kontamine olabilece i bildirilmi tir. Kolonize ki inin taburcu edilmesinden 13 gün sonra çevre kontaminasyonu gösterilmi tir. Yatak e yalar n n bu bakterinin çevre kontaminasyonu ve kal c l nda önemli rol oynad görülmektedir. Kuru ortamda uzun süre canl l n koruyabilen bir bakteridir (47).
Yo un bak mda yatma, trakeostomi, endotrakeal entübasyon, mekanik ventilasyon, invaziv giri imler ile yak n zamanda antibiyotik kullan lmas (üçüncü ku ak sefalosporinler, kinolonlar, karbapenemler vb) bu etkenlerle enfeksiyon geli mesinde en önemli risk faktörleri aras ndad r. Tedavi s ras nda kolayl kla direnç geli memesi ise bu mikroorganizmalar n önemli ve olumlu bir özelli idir (49,50).
Pseudomonas aeruginosa
P. aeruginosa birçok ciddi enfeksiyona (pnömoni, kan dola m enfeksiyonu vb) neden olabilen invaziv, non-fermentatif gram negatif bir mikroorganizmad r. Özellikle immun yetmezlikli, maligniteli bireyler ve organ transplantasyonu yap lanlarda ya am tehdit eden enfeksiyonlara yol açmaktad r (40).
Do ada ve hastanelerde (özellikle nemli ortamlarda) yayg n olarak bulunur. nsanlar n normal floras nda bazen bulunabilir. Hastane d ndaki sa l kl insanlarda kolonizasyon prevalans dü üktür. Hastaneye yat tan sonra kolonizasyon oranlar nda ciddi bir art olmaktad r. Hastanede yatan hastalarda bu oran ortalama %18 e ve gastrointestinal cerrahi geçiren hastalarda ise %73 e kadar ç kabilir. Bu art özellikle ciddi yan kl hastalar n cildinde, mekanik ventilasyon deste indeki hastalar n alt solunum yollar nda, kanser kemoterapisi alan hastalar n gastrointestinal sisteminde veya antibiyotik alan hastalarda ise yayg n ekilde olmaktad r (51,52).
T bbi cihazlar üzerinde, hastane ortam nda ve dezenfektanlar içinde ya am n devam ettirebilir. Mekanik ventilatörler ve devrelerinin kontaminasyonu nekrotizan pnömoni ile sonuçlanabilir (51).
Çapraz kontaminasyon ile hastadan hastaya geçi bakterinin hastane ortam nda yay lmas nda en önemli etmenlerden biridir (53).
YBÜ nde yatma, invaziv aletlerin kullan lmas yan nda penisilinler, geni -spektrumlu sefalosporinler, florokinolonlar n ve aminoglikozidlerin kullan m çok ilaca dirençli P. aeruginosa enfeksiyonlar n n geli iminde en s k rastlan lan risk faktörleri aras ndad r (54,55).
De i ik olgu-kontrol gruplar n içeren çal malarda;
Piperasilline dirençli P. aeruginosa enfeksiyonlar nda florokinolonlar
mipeneme dirençli P. aeruginosa için imipenem, piperasilin/tazobaktam ve aminoglikozidler
Piperasilin/tazobaktama dirençli P. aeruginosa da imipenem, piperasilin/tazobaktam, aminoglikozidler ile geni spektrumlu sefalosporinler risk faktörü olarak belirlenmi tir (55).
Son y llarda gerçekle tirilen ara t rmalarda özellikle florokinolonlara ve karbapenemlere kar tüm dünyada artan direnç oranlar dikkati çekmektedir. Tedavi s ras nda direnç geli mesi de s kl kla gözlenmektedir. Özellikle uygun olmayan antibiyotikler kullan ld nda mortalitenin de artt bilinmektedir (50,56-58).
Metisilin Dirençli Staphylococcus Aureus (MRSA)
S. aureus özellikle prematüre bireyler, opere edilenler, diyalize girenler ile protez bulunanlarda de i ik enfeksiyonlara (cilt-yumu ak doku enf., kemik-eklem enf., santral kateter enf., endokardit, ant enf., pnömoniler, menenjit, beyin apseleri) yol açan virulans yüksek bakteriyel etkenlerden biridir. YBÜ nde geli en Stafilokoksik enfeksiyonlar tüm dünyada uzun süre yat , artan maliyet ve ölüm oranlar ndan dolay önem ta maktad r (40,59).
Florokinolon grubu antibiyotikler içerisinde yer alan siprofloksasin ve levofloksasin kullan m özellikle hastaneye yat r lanlarda MRSA riskini önemli ölçüde art rmas na kar l k metisilin duyarl Staphylococcus aureus (MSSA) s kl üzerine herhangi bir etkisi bulunmamaktad r (60-62). Kinolonlar yan nda geni spektrumlu sefalosporin ve glikopeptid kullan m da MRSA olu umunda risk faktörleri aras nda dikkati çekmektedir (61).
lk kez 1996 y l nda Japonya da tan mlanan vankomisine orta düzeyde dirençli S. aureus su una (VISA) (M K: 8-16 mg/L) daha sonra ABD de diyaliz hastalar nda rastlanm olup, en önemli risk faktörünün vankomisin kullan m oldu u ortaya konmu tur (8,63).
Vankomisine Dirençli Enterokok (VRE)
Enterokoklar barsak ve kad n alt genital sistemi floras nda en s k gözlenen aerob gram pozitif koklard r. Enterokokal enfeksiyonlar s kl kla immun yetmezlikli, altta yatan hastal bulunan, damar içi kateter ya da üriner kateter uygulanan bireylerde görülmektedir. Bu enfeksiyonlar n yakla k %60 kadar anti-enterokokal aktiviteye sahip olmayan anti-anaerobik etkili ajanlar (metronidazol, klindamisin), sefalosporinler gibi geni spektrumlu antibiyotiklerin s k kullan lmalar ndan dolay özellikle YBÜ nde meydana gelmektedir (64).
Enterococcus faecalis tüm enterokokal enfeksiyonlar n %80-90 kadar ndan sorumludur, Enterococcus faecium ise %10-20 dolay nda etken olarak gözlenmektedir. Özellikle hastane enfeksiyonlar na (kateterle ili kili kan dola m enfeksiyonlar , menenjitler, intraabdominal enfeksiyonlar, menenjitler) neden olan mikroorganizmalar aras nda s kl klar n n artmas nda sefalosporinler, anti-stafilokokal penisilinler, klindamisin ve trimetoprim gibi antibiyotik s n flar na kar artm intrensek direncin en önemli rolü oynad bilinmektedir (64). VRE nin neden oldu u enfeksiyonlarda s kl kla gözlenen risk faktörleri; yüksek APACHE skorlar , yo un antibiyotik kullan m , vankomisin kullan m , hastanede uzun süre yatma ve invaziv giri imlerdir. Özellikle
VRE nin neden oldu u kan dola m enfeksiyonlar sonras nda ise hastanede yat süresi oldukça uzamakta, ek maliyet ve mortalite oranlar önemli ölçüde artmaktad r (65).
VRE kolonizasyonu YBÜ nde yatan hastalarda önem ta yan bir husustur. Bu hastalarda zaman zaman MRSA ta y c l da bildirilmektedir. Kolonizasyon olu umunda geçmi te vankomisin ya da ba ka grup antibiyotiklerin kullan m n n önemli yeri vard r. Piperasilin/tazobaktam gibi antibiyotiklerin verilmesi sonras nda ise kolonizasyon duyarl l n n bu bile i in gastrointestinal konsantrasyonunun azalmas na ba l olarak artmas dikkat çekicidir (64).
SIK KULLANILAN ANT B YOT KLER Aminoglikozidler:
Aminoglikozidler Streptomyces ve Micromonospora cinsi toprak bakterilerinden elde edilen do al ya da semi sentetik antibiyotiklerdir. Aminoglikozidler kimyasal yap lar na göre be aileye ayr l r:
1. Streptomisin ailesi; streptomisin
2. Kanamisin ailesi; kanamisin A, kanamisin B, amikasin, tobramisin, dibekasin
3. Gentamisin ailesi; gentamisin C1, gentamisin C1a, gentamisin C2, sisomisin, netilmisin, isepamisin
4. Neomisin ailesi; neomisin, paromamisin 5. Spektinomisin ailesi; spektinomisin
Aminoglikozidler, duyarl bakteri hücresine h zl bakterisidal etkilidirler. Bu etkilerini hem mRNA daki kodonlar n do ru okunu unu azaltarak ve bozarak hem de tRNA anti-kodonlar ndaki bilginin ribozomlarda yanl okunmas yla proteinlerin yanl kodlanmas na yol açarak yaparlar. Bunun sonucunda protein sentezinin sonlanmas na, dolay s yla bakteri ölümüne neden olurlar (66-70).
Aminoglikozidlere kar direnç geli iminde, plazmid arac l yla enzim inaktivasyonu, effluks sistemleri ve antibiyotik hedefinin modifikasyonuyla hücre içine azalm antibiyotik al n m gibi birkaç mekanizma mevcuttur. Aminoglikozidlerin farkl gruplarda yer alan antibiyotiklere kar direnç geli imi üzerinde etkisine ili kin s n rl veri mevcuttur. Bu grupta yer alan antibiyotiklere kar direnç geli se dahi, bakteri hücre duvar üzerine etkili ajanlarla sinerjistik etkinlik sa lamalar önem ta maktad r (71).
Aminoglikozidlerin yo un kullan m sonucunda zaman zaman dirençli Enterobacter türleri, Acinetobacter baumannii gibi mikroorganizmalarla geli en enfeksiyonlar dikkati çekmektedir.
Karbapenemler:
Karbapenemler, Streptomyces cattleya n n antibakteriyal bir ürünü olan tienamisin ile ilgili ara t rmalar s ras nda bulunan yeni bir beta-laktam grubudur. lk sentetik karbapenem imipenemdir. Daha sonra ise meropenem klinik kullan ma girmi tir. mipenem gram negatif ve pozitif bakterilerin hücre duvar sentezini inhibe ederek bakterisid etki gösterir. Duyarl Enterokoklar a kar , penisilinler de oldu u gibi, bakteriyostatik etkilidir. mipenem ve meropenemin ço u gram negatif bakteriye kar aminoglikozid ve florokinolonlar gibi post-antibiyotik etkisi vard r. Meropenem, gram negatif bakterilere ve özellikle dirençli P. aeruginosa su lar na, penetrasyonu h zl ve mükemmeldir. Pseudomonas enfeksiyonlar na kar imipenemden daha etkilidir (72).
mipenem ve meropenem hastane enfeksiyonunun tedavisinde s kl kla kullan lan geni spektrumlu antibiyotiklerdir. Karbapenem türevleri geni spektrumlu sefalosporinleri ya da penisilinleri hidrolize edebilen birçok beta-laktamaz taraf ndan parçalanmaya kar dayan kl d r. Bu antibiyotiklerin yo un olarak kullan lmas yla özellikle P. aeruginosa ve Acinetobacter türlerinde gözlenen direnç önem ta yan bir konudur. Bu dirençten, düzensiz effluks, d membran proteinlerinin kayb gibi de i ik mekanizmalar sorumlu tutulmaktad r. Özellikle d membran permeabilitesinde azalma sonucu florokinolonlara kar geli en direnç, kullan mda olmasa dahi karbapenemlere kar da direnç geli imine katk da bulunmaktad r. Ayr ca P. aeruginosa ve Acinetobacter türlerinde bulunan karbapenemazlar da dirence önemli katk larda bulunmaktad r (12).
Hastane ortam na yerle ti inde sorun yaratan bir mikroorganizma olan A. baumannii nin karbapenemlere kar direnç geli tirmesinde en önemli predispozan faktörlerden biri de bu grupta yer alan antibiyotiklerin tedavide kullan lmas d r. Bir bölgede böyle dirençli bir su un bulunmas tüm co rafik alanda mikroorganizman n yay lmas na neden olabilmektedir (49).
Enterobacteriaceae ailesinde yer alan ve GSBL üreten mikroorganizmalar n tedavisinde kullan lan karbapenem türevlerine kar bu etkenlerin nadiren direnç geli tirdi i bilinmektedir. Özellikle AmpC ya da TEM, SHV tipi GSBL üretenler yan nda, ABD, Brezilya, Yunanistan, Çin ve Singapur da metallo-betalaktamaz üreten Klebsiella pneumoniae su lar n n ortaya ç kmas endi e verici bir durum olarak
de erlendirilmektedir (11). Özellikle K. pneumoniae lar n üretti i plazmid kökenli karbapenemazlar (KPC-1, KPC-2, KPC-3) sadece karbapenemlere de il, ayr ca piperasilin/tazobaktam, üçüncü ve dördüncü ku ak sefalosporinlere, florokinolonlara ve aminoglikozidlere kar çoklu antibiyotik direnç geli iminden sorumlu tutulmaktad r (11).
Geni -spektrumlu sefalosporinler:
Kimyasal yap lar bak m ndan ve antibakteriyal etki mekanizmalar yönünden penisilinlere benzerler. Sefalosporinlerin ana çekirde ini sefem türevi olan 7-aminosefalosporanik asid olu turur. Üçüncü ve dördüncü ku ak parenteral sefalosporinler, nozokomiyal etkenleri de içeren geni spektrumu, ihmal edilebilir yan etkileri, pozoloji kolayl ve uygun farmakokinetik özellikleri nedeniyle oldukça s k tercih edilirler. Bununla birlikte rasyonel kullan lmad nda belki de en s k suistimale u rayan gruptur. Üçüncü ku ak sefalosporinler gram negatif basillerin beta- laktamazlar na kar dayan kl d r (73,74). Birinci ku a a göre gram pozitif mikroorganizmalara daha az etkilidirler. kinci ku aktan farklar ise ek olarak P. aeruginosa ya etkili olmalar ve enterik gram negatif bakteriler ve Neisseria ya etkinliklerinin daha fazla olmas d r (75). Enterokoklar, Listeria, MRSA ve Acinetobacter e kar ise etkisizdirler (76). Üçüncü ku ak sefalosporinlerin bir üyesi olan seftazidim, s k rastlanan plasmid arac l beta-laktamazlar kar s nda oldukça dayan kl d r. Enterik bakteriler, Neisseria ve H. influenza ya kar yüksek derecede etkilidir. Özellikle P. aeruginosa ya etkisi birçok çal mada defalarca gösterilmi tir. Seftazidimin gram pozitif mikroorganizmalara kar etkisi zay ft r (75,77,78). Dördüncü ku ak sefalosporinlerin iki üyesi sefepim ve sefpiromdur. Klinik kullan mda olan sefepim gram negatif bakterilerin d membran na daha iyi penetre olur. Bir çok plazmid ve kromozomal arac l beta-laktamaza 3. ku ak sefalosporinlere göre daha dayan kl d r (75,77,78). Kromozomal beta-laktamazlar olan Enterobacter, indol pozitif Proteus, Citrobacter ve Serratia gibi gram negatif enterik bakterilere kar daha fazla etkinlik gösterir. Sefepim, P. aeruginosa n n seftazidime duyarl ve dirençli pek çok izolat na kar da etkilidir. Geni -spektrumlu sefalosporinler, klinikte s kl kla kullan lan antibiyotikler aras ndad r.
Bakteri hücre duvar sentezini inhibe eden bu grup antibiyotiklere kar de i ik gram negatif mikroorganizmalar n kromozomlar ve plazmidler yoluyla dirençli enzimlerin sentezlenmesi sonucunda ortaya ç kan direnç önem ta maktad r. Özellikle P. aeruginosa ve Acinetobacter türlerinde ilaç penetrasyonunun azl yan nda effluks
sistemleri ve beta-laktamaz üretimi sefalosporinlerle birlikte karbapenemlere kar dirence de neden olmaktad r (10,12). Sefalosporinlerin yo un kullan m n n bir ba ka sonucu da GSBL üreten Enterobacteriaceae grubunda yer alan mikroorganizmalar n s kl nda art t r. Özellikle hastanelerde ve ba ka sa l k kurulu lar nda bu grupta yer alan antibiyotiklerin k s tlanmas n n gerçekle tirildi i çal malarda GSBL üreten mikroorganizmalar n olu umunun azald görülmektedir (11).
Ayr ca bu grup antibiyotiklerin kullan lmas sonras nda MRSA ve VRE s kl nda art dikkati çekmektedir. Clostridium difficile yle ili kili diarenin (CD D) de özellikle sefalosporin kullan m yla artmas önemlidir (10,12).
Geni spektrumlu penisilinler:
Penisilinler, güçlü bakterisid etkileri yan nda toksisiteleri nispeten dü ük olan ve s k kullan lan do al ve yar sentetik antibiyotiklerdir. lk olarak 1929'da Fleming taraf ndan do al penisilin bulunmu ve ilerleyen zaman içerisinde do al penisilinlerin çe itli sak ncalar n düzelten yar sentetik penisilinler geli tirilmi tir. Yar sentetik penisilinler ya do al penisilinin yap s n n kimyasal manüplasyonlarla de i tirilmesi ya da ço u zaman oldu u gibi penisilin molekülünde ana iskeleti olu turan 6-aminopenisilanik asid'e uygun bir yan zincir eklenmesi ile elde edilirler. Penisilinler, duyarl bakterilerin murain'den olu an hücre duvar n etkileyerek bakterisid etki gösterirler (73).
Penisilinlerin klinik kullan ma girdi i 1940 l y llardan itibaren, özellikle hastane enfeksiyonlar ndan izole edilen S. aureus ile tan mlanmaya ba lanan beta- laktamaz direnci, günümüzde H. influenza, Enterokoklar, Klebsiella pneumoniae ve E. coli ba ta olmak üzere enterik bakteriler aras nda da h zla yay lmaktad r. Metisilin, nafsilin, oksasilin, kloksasilin, flukloksasilin kullan m penisilinaz salg layan stafilokoklarca olu turulan enfeksiyonlar n tedavisinde kullan labilir gibi görünse de gittikçe artan ve mecA geni varl nda farkl bir PBP (PBP 2a) sentezi ile geli en penisilin direnci (metisilin direnci) nedeni ile eski önemini yitirmi lerdir (73).
Karboksipenesilinler (karbenesilin, tikarsilin) ve üreidopenesilinler (piperasilin, mezlosilin, azlosilin) gram negatif bakterilerde etkilidirler. Enterik bakteriler ve P. aeruginosa taraf ndan sentezlenen beta-laktamazlardan etkilenmezler. Stafilokok penisilinazlar nca kolayca hidrolize edilirler. Piperasilin ve azlosilin en güçlü anti-psödomonal penisilinlerdir. A r enfeksiyonlarda aminoglikozidlerle kombine edilerek kullan lmal d rlar (73).
Klavulanik asit, sulbaktam ve tazobaktam üç beta-laktamaz inhibitörüdür. Zay f antibakteriyal etkilidirler. As l etkinlikleri beta-laktamazlar n aktif bölgesine dönü ümsüz olarak ba lanmalar , yani intihar molekülleri olarak beta-laktamaz inhibe etmeleridir (73).
Bakteri hücre duvar sentezini inhibe ederek etkili olabilen penisilin türevlerinin yo un olarak kullan lmas yla ortaya ç kan direnç hem Gram pozitif hem de Gram negatif mikroorganizmalar için önem ta maktad r. Bu direncin olu umunda etkili olan ba l ca mekanizmalar; beta-laktam n y k m ile inaktivasyon, permeabilitede azalma ve effluks mekanizmas yla hücre içerisine al n m n azalmas ve farkl penisilin ba layan- proteinler taraf ndan hedefin de i mesidir. Özellikle GSBL üreten mikroorganizma olu umuna katk s bulunan penisillin kullan m n n k s tlan p yerine sefaosporinlerin verilmesi bu sorunun azalmas na katk da bulunmaktad r. Beta-laktamaz inhibitörü içeren penisilin türevlerinin kullan lmas n n VRE kolonizasyonu ve enfeksiyonlar n azaltmada önemli katk s bulunmaktad r. CD D s kl n n azalt lmas nda da geni spektrumlu sefalosporinlerin yerine beta-laktamaz inhibitörü içeren penisilin gruplar n n (piperasilin/tazobaktam gibi) kullan lmas n n etkili oldu u bilinmektedir (12).
Florokinolonlar:
Florokinolonlar ciddi enfeksiyonlar n tedavisinde s k kullan lan önemli antibiyotik gruplar ndan birini olu turmaktad r. Kinolonlar duyarl bakteride bakterisidal etki gösterirler. Bu etkileri konsantrasyona ba ml d r. Bakterisidal etkilerini DNA sentezini h zl bir ekilde inhibe ederek ve muhtemelen ilave baz mekanizmalarla yaparlar. Kinolonlar n bakteri hücresinde iki hedefi vard r. Her ikisi de tip 2 topoizomerazlardan iki enzim; DNA giraz (topoizomeraz 2) ve topoizomeraz 4 bu hedefleri olu turmaktad r (79,80). Ancak özellikle yo un ve ak lc olmayan kullan m sonucunda önemli direnç sorunu da ortaya ç kmakta ve mikroorganizmalar sadece florokinolonlara de il farkl antibiyotiklere de h zl bir biçimde duyarl l klar n yitirmektedirler.
Effluks pompa sistemlerinin indüksiyonu son y llarda tan mlanm önemli direnç mekanizmalar ndan biridir. Bu mekanizma tüm antibiyotik gruplar na kar geli en dirençte rol oynamaktad r. Özellikle hastanelerde s k olarak kar la lan dirençli P. aeruginosa ve A. baumannii enfeksiyonlar n n geli iminde florokinolonlar n kullan lmas n n çok önemli bir yeri vard r (81). Ciddi enfeksiyonlarda direnç geli imini önlemek için florokinolonlarla birlikte beta-laktam antibiyotiklerin kombine kullan m ndan kaç n lmal d r (82,83).
Kromozomal kökenlilerden daha çok plazmid kökenli direnç mekanizmalar n n Enterobacteriaceae ailesinde yer alan önemli mikroorganizmalarda, kinolonlara ve çoklu ilaç direncinin geli imi ve yay lmas na önemli katk da bulunabilece inden endi e edilmektedir (11).
Florokinolonlar n yo un kullan lmas sonucunda gram negatif mikroorganizmalarda direnç geli imi yan nda MRSA geli imi de artmaktad r (10,11,62). Özellikle siprofloksasin, levofloksasin ve gatifloksasin uyguland nda ise CD D s kl önemli düzeylerde artmaktad r (84).
Vankomisin:
lk kez 1956 y l nda uygulamaya sunulan vankomisin Gram pozitif mikroorganizmalara kar etkili olan bir glikopeptiddir. Bakterisidal etkisini esas olarak ço alan mikroorganizmada hücre duvar sentezini inhibe ederek gösterir (85). Vankomisin kullan m na ba l olarak ortaya ç kan VRE sorunu giderek artmaktad r. Ancak di er antibiyotik gruplar na kar direnç geli imi üzerine herhangi bir etki henüz bildirilmemi tir (12).
Yeni antibiyotik gruplar n n (linezolid, kinupristin-dalfopristin, daptomisin, tigesiklin) yo un kullan m yla ilgili olarak direnç olu umuna katk lar hususunda henüz bilgimiz k s tl d r. Ancak bu gelecekte direncin olu mayaca anlam na gelmemektedir (63).
Linezolid:
Linezolid, oksazolidinon ismi ta yan yeni bir antibiyotik grubunun üyesidir. Linezolid bakteri ribozomu üzerinde 50S alt ünitesinin 23S alt birimine ba lanarak, bakteriyel translasyon i levi için mutlaka gerekli bir komponent olan fonksiyonel 70S ba lang ç kompleksinin olu mas n önler. Linezolid tamamen sentetik bir moleküldür. Aralar nda metisilin dirençli stafilokoklar, penisilin dirençli pnömokoklar, makrolid dirençli streptokoklar ve vankomisin dirençli Enterokoklar n da bulundu u tüm önemli Gram pozitif patojenlere kar iyi aktivite gösterir. Tama yak n biyoyararlan ma sahiptir, bu nedenle ayn dozlar oral veya parenteral verilebilir. At l m yar ömrü günde iki kez al m na izin verir. Renal ve karaci er fonksiyon bozuklu unda doz azalt m na gerek yoktur. Linezolidin cilt ve yumu ak doku enfeksiyonlar , alt solunum yolu enfeksiyonlar ve vankomisin dirençli Enterokok enfeksiyonlar için kullan m onay bulunmaktad r. laç kabul edilebilir bir istenmeyen etki profiline sahiptir, iki haftadan daha uzun ve yüksek doz kullananlarda geriye dönü ebilen kemik ili i bask lanmas gözlenmi tir (86).
Oksazolidinonlar ribozomal protein sentez inhibitörüdür (87). Bu etkilerini ribozom alt ünitelerinin birle erek, 70S ribozom kompleksini olu turmas n engelleyerek yaparlar. Peptid ba olu umunu inhibe etmediklerinden, yak n yerlere ba lanan kloramfenikol ve linkomisin ile çapraz direnç göstermezler. Laboratuar ve klinik kullan mda nadiren Enterococcus faecium ve Staphylococcus aureus ta dirençli mutant geli imi gözlenebilmektedir. Bunlar s kl kla 23S ribozomun V. bölgesinde geli en de i ik mutasyonlara ba lanm t r. u ana dek ilac n inaktivasyonu yolu ile olu an bir direnç mekanizmas saptanmam t r. Linezolid de di er protein sentez inhibitörlerinin ço u gibi bakteriyostatiktir (87).
Antibiyotik direncini en aza indirmek amac yla özellikle antibiyotik kullan m ile direnç aras ndaki ba lant n n iyi anla lmas ve de erlendirilmesi oldukça önemlidir.
laç mikroorganizma ili kisinin do as oldukça de i ken ve çok say da faktörden etkilenebildi inden iyi bir biçimde irdelenmedikçe sorunun çözümü güçle mektedir. Özellikle ba lang çta uygun antibiyotiklerin gerekli, en k sa süreler içerisinde kullan lmas n n önemi her zaman vurgulanmas gereken önemli bir konudur. Uygun antibiyotik tedavisinin gerçekle tirilmesi sadece mortaliteyi azaltmakla kalmay p, YBÜ ve hastanede yat süresini azaltmakta ve maliyeti önemli ölçüde dü ürmektedir (88).
Sonuç olarak hastanelerde genellikle ak lc olmayan ve yo un antibiyotik kullan m n takiben ortaya ç kan direnç sorununun çözümünde, ilgili antibiyotiklerin kullan m n n azalt lmas ve gerekli enfeksiyon kontrol önlemlerinin al nmas yla dirençli mikroorganizmalar n neden oldu u enfeksiyonlar n s kl n önemli ölçüde azaltmak olas d r.
BAKTER LERDE ANT B YOT KLERE KAR I D RENÇ
MEKAN ZMALARI
Bakteriler er ya da geç antibiyotiklere kar direnç kazanmaktad rlar. Antibiyotiklere direnç, hem hasta hem de hekim için baz sorunlar beraberinde getirmektedir. Antibiyoti e dirençli bir bakteri ile enfekte olan ki ilerin tedavi süreleri, dolay s yla hastanede yat süreleri duyarl bir bakteri ile enfekte olan ki ilerin tedavi sürelerinden daha uzun olmaktad r. Dirençli bir bakterinin etken oldu u enfeksiyonlara ba l ölüm oran , duyarl bir bakterinin etken oldu u enfeksiyonlardakinden iki kat fazlad r. Ayr ca antibiyotik direnci, hastalarda daha toksik, daha geni spektrumlu ya da daha pahal olan antibiyotiklerin kullan m na yol açmaktad r (89-91).
Antibiyotik direncinin biyokimyasal mekanizmalar : Bakterilerin, antibiyotik
1. lac n hedefinde de i iklik olu turmas . a. Reseptörün afinitesinde azalma olmas .
b. laçtan etkilenmeyen farkl bir metabolik yol kullanmas . 2. Sentezlenen enzimle ilac n inaktive edilmesi.
3. Hücreye giren ilac n miktar n n azalt lmas . a. Permeabilitenin azalt lmas .
b. Aktif pompalama ile ilac n d ar at lmas .
Bir bakteri, bu mekanizmalardan birkaç n ayn anda kullanarak farkl etki mekanizmalar na sahip antibiyotiklere direnç kazanabilmektedir.
Antibiyotik direncinin genetik mekanizmalar : Bir mikroorganizman n yap s
nedeniyle antibiyotiklere kar dirençli olu u intrinsik direnç olarak tan mlanmaktad r. Örne in, birçok gram negatif bakteri vankomisin ve metisilin, Enterokoklar ise sefalosporinlere, duvar yap lar nedeniyle intrinsik olarak dirençlidir (90).
Aminoglikozidlerin hücre membran ndan transportu oksijene ba ml , enerji gerektiren bir olay oldu undan, oksitadif fosforilasyonun olmad zorunlu anaerop mikroorganizmalarda ilac n hücreye al nmas s ras ndaki enerji gerektiren evreler kullan lamaz ve yeterli miktarda ilaç hücre içine giremez. Bu nedenle aminoglikozid antibiyotikler anaerop mikroorganizmalara kar etki göstermezler (92-95).
Kazan lan direnç ise; ya DNA daki mutasyonlar, ya da yeni bir DNA edinilmesi sonucu ortaya ç kmaktad r. Mutasyonlar genellikle kromomozomal DNA da olu maktad r; örne in streptomisin, rifampin ve florokinolonlara kar geli en direnç bu yolla olmaktad r. Ancak, günümüzde mutasyonlar n plazmid veya transpozonlar üzerindeki genlerle de olu abildi i bilinmektedir (90,96).
a. Kromozomal direnç: Bu tip direnç kromozomda bir spontan mutasyon olu mas sonucu ortaya ç kmaktad r. Bakteri hücresinin metabolik ara ürünleri ve baz çevresel faktörlerle olu abilen spontan mutasyonlar sonucunda hücrelerin ilaca geçirgenli i azalabilir ya da ilac n hedefinde de i iklik olabilir. Ortamda antibiyotik bulundu unda duyarl mikroorganizmalar bask lanaca için ilaca dirençli olanlar yarar na bir seleksiyon olu acakt r. Ancak spontan mutasyon olu ma olas l normal ko ullarda çok dü üktür. Bir bakteri hücresinde tek bir genin kendili inden mutasyona u rama oran , her hücre bölünmesinde 10-5 ile 10-10 civar ndad r ve bu nedenle klinikte bu tip direnç nadirdir (97). Buna kar n baz antibiyotiklerde örne in, rifampin için bu oran daha yüksektir (10-5 10-7). Bu nedenle tedavide tek ba na kullan ld nda rifampine dirençli mutantlar ortaya ç kmakta ve tedavi ba ar s z olmaktad r (98).
b. Plazmidlere ba l direnç: Plazmidler kromozomdan farkl ba ms z olarak replike olan kromozom d genetik elementlerdir. Klinikte görülen direnç daha çok plazmidlere ba l d r. R-plazmidi ad verilen direnç plazmidleri say lar 10 a varabilen farkl antibiyoti e kar direnç genlerini ta maktad r. R-plazmidi içeren bakteriler bu özelliklerini duyarl bakterilere aktararak onlar na dirençli hale gelmesine neden olmaktad rlar (96,97). Bula c tipteki bu direnç daha çok antibiyoti i inaktive eden veya hücrenin geçirgenli ini de i tiren enzimlerle olmaktad r (98). Antibiyotik kullan m direnç genlerini ta yan bakteriler yarar na bir seleksiyona yol açmakta, özeliklle hastaneler gibi antibiyotik kullan m n n yo un oldu u yerlerde dirençli bakterilerde art a yol açmaktad r.
c. Transpozonlara ba l direnç: Transpozonlar, bir DNA molekülünden di erine geçebilen DNA dizileridir. Bunlar n plazmidlerden fark , ba ms z olarak replike olamamalar d r. Bu nedenle, kromozom ya da plazmid içinde bulunmakta bunlar aras nda yer de i tirebilmektedir. Son y llarda baz transpozon veya plazmidlerde integron ad verilen ve yeni genlerin kazan lmas n sa layan genetik yap lar bulundu u gösterilmi tir. Bir bakterinin çok k sa süre içinde birçok antibiyoti e birden
ço ul dirençli duruma geli inde bu elementlerin rolü oldu u anla lm t r (96,97).
BETA-LAKTAM ANT B YOT KLERE KAR I D RENÇ
MEKAN ZMALARI:
Beta-laktam antibiyotikler, bakterilerde hücre duvar n n yap m n engellemektedir. Bu antibiyotiklerin hedefi, hücre duvar sentezinin transpeptidasyon evresini katalize eden penisilin ba layan proteinler (PBP) d r. Beta-laktam antibiyotikler, bu enzimlere ba lan nca enzimin kendi substrat na ba lanmas n engellemekte, böylece duvar sentezi inhibe olmakta ve bakteri lizise u ramaktad r (99,100). Bakterilerde beta-laktam antibiyotiklere kar olu an direnç üç yolla geli ebilmektedir;
1. PBP lerde olu an de i iklikler ile antibiyoti in hedefine ba lanmas n n engellenmesi: PBP lerdeki de i iklikler PBP nin beta-laktam antibiyoti e affinitesinin azalmas , PBP say s nda azalma olmas veya beta-laktam antibiyotiklere dü ük affinite gösteren yeni PBP lerin sentezlenmesi sonucu olu abilmektedir (91,101,102). Bunlar n tümü kromozomal mutasyonlar sonucu ortaya ç kmaktad r. PBP lerdeki de i iklikler ile olu an direnç baz gram-pozitif koklarda ve Pseudomonas ta gözlenmektedir. N. gonorrhoeae, N. meningitidis, H. influenzae ve S.
pneumoniae de gözlenen penisilin direnci bu mekanizma ile olu maktad r (96,103). Metisilin dirençli S. aureus da gözlenen direnç mekanizmas da bu tiptir (104).
2. D membran proteinlerinde (OMP) olu an de i iklikler ile ilac n hücre içine giri inin önlenmesi: Gram negatif bakterilerde beta-laktam moleküleri d membran
OMP (outer membrane protein) ad verilen, porin proteinlerinden olu an porlar yoluyla geçmektedir. Porinlerin özellikleri ve say lar ile antibiyoti in özellikleri (yük, çözünürlük, büyüklük) hücre içine giri h z n belirlemektedir (103). Geçirgenli in azalmas na ba l olarak direnç özellikle enzimatik direnç ile birlikte ise önemli düzeyde bir dirence yol açmaktad r. Klinikte nadir olmakla birlikte son y llarda özellikle imipeneme dirençli olan P. aeruginosa su lar nda karbapenem antibiyotiklerin kullan ld OprD kanal n n eksik oldu u saptanm t r (103,105).
3. Beta-laktamaz enzimleri ile ilac n inaktive edilmesi: Beta-laktam
antibiyotiklere kar klinikte gözlenen direnç, bakterilerin bu antibiyotikleri inaktive eden beta-laktamaz enzimlerini sentezlemesi ile olu maktad r (103,106). Gram pozitif bakteriler içinde beta-laktamaz sentezleyen en önemli patojenler S. aureus tur. S. aureus enzimleri plazmid kontrolündedir ve bakteriyofaj arac l ile duyarl hücrelere geçebilmektedir (103). Gram negatif bakterilerde ise beta-laktamazlar, d membran ile stoplazmik membran aras ndaki periplazmik bo lukta bulunmaktad r. Gram negatif bakterilerde beta-laktamaz enzimleri kromozom yada plazmid kontrolünde sentezlenmektedir.
Kromozomal enzimler: Hemen hemen tüm gram negatif bakterilerde
kromozom kontrolünde sentezlenen beta-laktamazlar bulunmaktad r (103,106,107). Bu enzimler sefalosporinleri penisilinlerden daha h zl hidrolize etmekte, klavulanik asit ve sulbaktam gibi beta-laktamaz inhibitörlerinden etkilenmemektedir. Enzim normalde bir repressör mekanizma ile dü ük düzeyde sentezlenirken ortama bir penisilin ya da sefalosporin eklendi inde enzim sentezinde birkaç yüz kat art olabilmektedir. Ortamdan indükleyici uzakla t r ld nda enzim sentezi normale dönmektedir. Tip1 enzim sentezleyen bakteri toplumlar nda 10-5 10-7 s kl nda stabil olarak dereprese mutantlar ortaya ç kmaktad r. Bu bakterilerde beta-laktamaz enzimlerinin sentezi devaml ve yüksek düzeyde olmaktad r. Beta-laktamaz sentezi dereprese mutantlar, indüklenebilen beta-laktamaz sentezleyen bakteri toplumlar nda geni spektrumlu sefalosporinler, üreidopenisilinler ve karboksipenisilinler gibi bu enzimlere duyarl olup zay f indüksiyon yapan antibiyotiklerin kullan m ile tedavi s ras nda ortaya
ç kmaktad r. Bunun nedeni, bu antibiyotiklerin indüklenebilen hücreleri öldürebilmesi, buna kar n dereprese mutantlar n seleksiyonuna yol açmas d r. Dereprese mutantlar n seçilme riski nedeniyle geni spektrumlu sefalosporinlerin indüklenebilen beta-laktamaz sentezledi i bilinen bakteriler ile geli en enfeksiyonlarda kullan mlar sak ncal d r (103).
Plazmid kontrolündeki beta-laktamazlar: Gram negatif bakterilerde gözlenen beta-laktam antibiyotiklere kar direnç büyük oranda plazmid kontrolündeki beta-laktamazlara ba l d r. Bu enzimlerin say s bu gün elliyi a maktad r. Bush s n fland rmas nda grup 2 b de yer alan geni spektrumlu (broad spectrum) beta-laktamazlar plazmid kontrolündeki enzimlerin en büyük grubunu olu turmaktad r. Bunlar içinde en s k saptanan enzimler TEM-1 ve SHV-1 dir (91,103,108). Ampisilin, karbenesilin, tikarsilin, sefaletin ve sefamandole direnç olu tururken yeni sefalosporinler, monobaktamlar ve sefamisinlere etkisizdirler. Klavulanik asit, sulbaktam ve tazobaktam gibi beta-laktamaz inhibitörlerine duyarl d rlar (91,103). Bush s n fland rmas nda grup 2 b de yer alan geni letilmi spektrumlu (extended broad spectrum) (ESBL) enzimler ise 1980 de ilk kez Fransa ve Almanya da tan mlanm , ülkemizde ise ilk kez 1992 de saptanm olan, Klebsiella ve E. coli su lar nda yayg n olan enzimlerdir (109,110). Bu enzimler sefotaksim, seftazidim, seftriakson ve aztreonam gibi yeni ku ak beta-laktamlara direnç olu turmakta ve ço unlukla TEM veya SHV den köken almaktad r. ESBL ler sefoksitin ve beta-laktamaz inhibitörlerine duyarl d r. Ancak TEM türü beta-laktamazlar a r sentezleyen mikroorganizmalar n ve geçirgenli i azalm mutantlar n beta-laktam/beta-laktamaz inhibitörü kombinasyonlar na direnç gösterebildi i bildirilmektedir. Bunlara ek olarak son y llarda tan mlanm olan ve TEM enzimlerinden köken alm mutantlar nda (IRT) bu kombinasyonlara direnç olu turdu u saptanm t r (111). TEM ve SHV türevleri olan ESBL lardan ba ka son y llarda bunlardan köken almam olan yeni enzimler bildirilmi tir. Bunlardan PER-1 enzimi ilk kez Fransa da bir Türk hastadan izole edilmi , daha sonra Türkiye de P. aeruginosa, Acinetobacter ve Salmonella typhimurium da saptanm t r (112-114). Bu enzim Türkiye de çok yayg n olmas na kar n ülkemiz d nda çok nadir olarak saptanmaktad r. Seftazidime yüksek oranda dirençli olup klavulanik asit ve tazobaktam ile inhibe olmaktad r (103,115).
Gram negatif bakterilerde direnç her üç mekanizma ile olu abilirken, gram pozitif mikroorganizmalarda d membran olmad ndan direnç sadece enzim ve PBP lerdeki de i imlere ba l olabilmektedir (103).
AM NOGL KOZ D GRUBU ANT B YOT KLERE KAR I D RENÇ MEKAN ZMALARI:
Aminoglikozid ler Enterobacteriaceae ve Pseudomonas larda hücre içine hücre duvar ndaki porin kanallar ndan girerek 30s ribozomlar na ba lanmaktad r. Bu antibiyotikler ribozomlara irreversibl olarak ba lanarak translasyonu bozmakta ve mRNA n n genetik kodunun yanl okunmas na yol açmaktad r (92). Gram pozitif ve gram negatif bakterilerde aminoglikozidlere kar direnç ribozomal permeabiliteye ba l veya enzimatik yolla olu abilir (93,94).
Ribozomal Direnç:
Aminoglikozid antibiyotiklere kar geli en ribozomal direnç bu antibiyotiklerin bakteri hücresindeki hedefleri olan ribozomlarda olu an mutasyonlar sonucu ortaya ç kmaktad r. N. gonorrhoeae, Enterokoklar, S. aureus ve Pseudomonas larda bildirilmi olan bu direnç klinikte nadirdir ve di er aminoglikozidlere kar çapraz direnç olu turmamaktad r (94,95).
Permeabiliteye ba l direnç:
Aminoglikozidlere kar kromozomal mutasyonlar sonucu membrandaki geçirgenli in azalmas ile olu an direnç en s k olarak P. aeruginosa su lar nda gözlenmektedir. Bu tip dirençte direnç düzeyinin yüksek olmamas na kar n tüm aminoglikozidlere kar çapraz direnç olu maktad r (93,94).
Enzimatik Direnç:
Günümüzde aminoglikozidlere dirençli bulunan gram pozitif ve gram negatif bakterilerde en s k gözlenen mekanizma plazmid taraf ndan kodlanan enzimlerle antibiyoti in de i tirilmesidir. Bu enzimler kataliz ettikleri reaksiyona göre 3 s n fta toplanmaktad r.
1. Asetiltransferazlar (AAC): Aminoglikozid molekülündeki amino grubunu asetile etmektedir.
2. Nükleotidil transferazlar (ANT): Aminoglikozid molekülündeki hidroksil grubunu adenile etmektedir.
3. Fosfotransferazlar (APH): Aminoglikozid molekülündeki hidroksil grubunu fosforile etmektedir.
Bir aminoglikozid molekülü birden fazla bölgede modifikasyona u rayabilir. Yani birçok farkl enzim için substrat olabilir. Ayr ca bir enzim birçok farkl
aminoglikozidi modifiye edebilir (116). Bu enzimler ile modifiye edilen aminoglikozidler ribozomlara ba lanamamakta ve etki gösterememektedir. Aminoglikozid antibiyotikleri modifiye eden enzimlerin da l m ülkeden ülkeye, hatta hastaneden hastaneye de i mektedir. Bu da antibiyotik kullan m sonucu olu an seleksiyon bask s ile farkl enzimlerin daha yayg n olu una ba lanmaktad r. Örne in, gentamisinin amikasinden daha s k kullan ld ülkelerde en s k gözlenen enzimler ANT(2 ) ve AAC(3) dür. Amikasinin yayg n olarak kullan ld ülkelerde ise amikasini inaktive edebilen AAC(6 ) enzimi s k bulunmaktad r (117). Türkiye de yap lan çok merkezli bir çal mada gram negatif bakterilerde en s k olarak 6 enzim bulundu u bunlar n AAC(3)-1 (gentamisin), AAC(3)-II (gentamisin-tobramisin-netilmisin), AAC(6 )-I (tobramisin-netilmisin-amikasin), AAC(6 )III (tobramisin-netilmisin-amikasin-isepamisin), AAC(6 )IV (gentamisin-tobramisin-netilmisin-amikasin) ve ANT(2 )-I (gentamisin-tobramisin) oldu u saptanm t r. Ülkemizde gentamisin ve tobramisine direnç amikasine k yasla daha yüksektir. Buna kar n amikasin kullan m n n art na paralel olarak bu ilaca kar dirençte de art görülmektedir (118).
GL KOPEPT D ANT B YOT KLERE D RENÇ MEKAN ZMALARI:
Son y llarda özellikle beta-laktam antibiyotiklere dirençli gram pozitif mikroorganizmalar ile olu an enfeksiyonlar n tedavisinde kullan lmakta olan glikopeptid antibiyotikler (vankomisin, ristosetin, avoparsin, teikoplanin) bakterilerde beta-laktam antibiyotikler gibi hücre duvar yap s nda bulunan peptidoglikan sentezini inhibe ederek etki göstermektedir (104). Ancak bu grup antibiyotikler hücre duvar prekürsöründeki D-alanil-D-alanin e non-kovalent olarak ba lanarak hücre duvar sentezini daha erken evrelerde engellemektedir. Ancak, son y llarda Enterococcus türlerinde ve koagülaz negatif stafilokoklarda bu antibiyotiklere kar klinikte direnç gözlenmeye ba lanm t r.(104,119,120)
Günümüzde Enterokoklar da davran ve direnç düzeyi yönünden farkl l k gösteren 4 farkl fenotipte glikopeptid direnci saptanm t r. En son gözlenen VANA tipli dirençte direnç genleri bir transpozondad r. VANB tipi dirençte direnç genleri ço unlukla kromozomdad r. Ancak konjugasyonla geçebilmektedir. VANC direnç genleri ise kromozomdad r ve transfer edilemez (121). Glikopeptidlerde direnç genetik olarak son derece karma k bir olayd r ve bir seri enzim taraf ndan vankomisin ve teikoplanine affinitesi azalm olan modifiye prekürsörlerin sentezlenmesi sonucu ortaya ç kmaktad r (104,120). Birçok ülkede çok yayg n olmas na kar n glikopeptidlere
dirençli Enterokoklar ülkemizde çok nadirdir. imdiye de in sadece E.faecium su unda VANA fenotipinde direnç bildirilmi tir (122).
K NOLON GRUBU ANT B YOT KLERE D RENÇ:
Kinolonlar, bakterilerde DNA replikasyonu için gerekli olan iki tip topoizomeraz; DNA giraz ve topoizomeraz IV ile etkile ime girmekte ve DNA sentezini durdurmaktad r (91,108,123). Bu topoizomerazlar n fizyolojik rolü daha çok E. coli ile yap lan çal malardan ç kart lmakla birlikte, birçok bakteride benzer ekildedir. Florokinolonlar n gram pozitif ve gram negatif bakterilerde enzim hedefleri farkl d r. E. coli de DNA giraz, S. aureus da ise topoizomeraz IV birincil hedeftir (123).
1.Hedef enzimde de i ikli e ba l direnç:
Hedef enzimdeki de i im ile enzim-DNA kompleksinin ilaca affinitesi azalmaktad r. Bugüne de in incelenen gram negatif bakterilerde yüksek düzeyde kinolon direncinin daha çok GyrA daki de i iklilere ba l oldu u saptanm t r. Sadece GyrB deki mutasyonlara ba l direnç dü ük düzeydedir (123). Birçok gram pozitif bakteride ise esas hedef topoizomeraz IV ün ParC alt birimidir; DNA giraz ikincil hedeftir.
2. lac n hücreye giri inin azalmas :
Kinolon lar gram negatif bakterilerde d membrandaki proteinlerden girmektedir. Kromozomal mutasyonlar sonucu d membran porinlerinin azalmas sonucu kinolonlara kar direnç olu maktad r. Buna kar n son y llarda bu tip dirençte porinlerdeki azalma ile birlikte enerji gerektiren pompa sistemlerinin gerekli oldu u anla lm t r (123). Bu sistemlerden en fazla incelenmi olanlar , E. coli nin ço ul antibiyotik dirençli (Mar) mutantlar ve P. aeruginosa daki pompa sistemleridir. Gram-pozitif organizmalarda permeabiliteye ba l direnç ile ilgili bilgi azd r. Ancak son y llarda S. aureus su lar nda 50 Kda a rl nda bir transport protein kodlayan nor A geni tan mlanm t r. NorA mutantlar n n enoksasin , norfloksasin , siprofloksasin ve ofloksasin gibi hidrofilik kinolonlara ve kloramfenikole direnç olu turdu u belirlenmi tir (91,108,123,124).
Sonuç olarak u söylenebilir ki ilaç rezistan enfeksiyonlar n arkas ndaki ana güç tamamen evrimsel süreçtir. Ya am formlar bulunduklar çevrede varl klar n sürdürebilmek için ya tehditlere adapte olacak ya da öleceklerdir. En güçlü ve en uyumlu olanlar ya amlar n sürdürebilecektir. Bu ola anüstü evrimsel süreç çok h zl ve de i ik ekillerde meydana gelmektedir (125). Patojen oldu u zannedilen organizman n eredikasyonu için tedavi dizayn devam etti i sürede dahi hasta vücudundaki bir ilaca
kar rezistans n ba lamas na mikroorganizma izin verir. Subterapotik dozaj, k salt lm ya da kesilmi tedavi süreci ya da antimikrobiyal ajan taraf ndan zay flat lm doku penetrasyonu rezistan mikroorganizman n meydana gelmesini h zland rabilir. Tedavi stratejileri antibiyotik kontrol stratejilerindeki gibi ve daha fazla rezistans organizman n ortaya ç k n minimalize etmek için antibiyotik de i im döngüsünde kabul edilmi metotlara göre yap lmal d r. Rezistans n ortaya ç k n efektif olarak s n rlayan bir stratejiyi gösterecek çok az kan t vard r. Antimikrobiyal seçimi ve kullan m nda klinisyen makul olmaya zorlanmal d r (126). Yo un Bak m Ünitelerindeki antibiyotik direncinin yay lmas n önlemede ve tedavi ba ar s n artt rmada u stratejiler faydal olabilir (127):
I. Antibiyotik stratejileri:
1. Ak lc antibiyotik kullan m için protokoller ve rehberlerin kullan lmas .
2. Antibiyotik tüketimi ve mikrobiyal direnç profilinin hastane verilerine göre daralt l p, s n rland r lmas .
3. Klinik endikasyon yoksa gereksiz antibiyotik kullan m ndan kaç n lmas (ampirik, proflaktik ve tedavinin normal ak nda).
4. Antibiyotik heterojenitesini destekleyen kullan mlar dikkate al (de i im, s ral kulan m, planlanm antibiyotik de i imi).
5. Antibiyotik tedavi seçimine rehberlik etmesi için, yo un bak m ünitesinin antibiyogramlar n n kullan lmas .
6. Etkili antibiyotik kullan lmas (Örne in; en muhtemel bakteriyel patojenler ve onlar n antimikrobiyal duyarl l k paternleri baz al narak uygun antibiyotikler seçilmesi).
II. Antibiyotik d stratejiler:
1. nvaziv i lemler için aseptik teknikler kullan lmas .
2. Enfeksiyon kontrol uygulamalar n n standardizasyonu (El y kama e itimi, alkol bazl el dezenfektanlar n n kullan m , dirençli bakteriler için sürveyans, doktor e itimi). 3. S kl kla kullan lan aletler/cihazlar n dezenfeksiyonu (respiratuar tedavi ekipmanlar ) 4. Klinik olarak önemli antibiyotik dirençli bakterilerle enfekte ya da kolonize hastalar için izolasyon tedbirlerinin al nmas .
MATERYAL VE METOD
Dicle Üniversitesi T p Fakültesi Gö üs Hastal klar Solunumsal Yo un Bak m Ünitesi ne Ocak 2008-Aral k 2008 tarihleri aras nda yatan hastalardan, laboratuara gönderilen örneklerin kültür sonuçlar nda, üreme olanlar çal maya dahil edildi.
Hastaya ait verilere, hasta dosyalar n n ve t bbi kay tlar n n incelenmesi yolu ile ula ld . Ya , cinsiyet, izole edilen mikroorganizman n cinsi, antibiyotik duyarl l klar , enfeksiyon / kolonizasyon oda , yo un bak mda kal süresi, as l tan lar , kullan lan antibiyotik, sonuç (ya ayan, ölen) gibi veriler çal ma için haz rlanan hasta kay t formlar na i lendi.
Laboratuara gönderilen kültür örneklerinden kan kültür örnekleri, hasta ba nda her iki koldan 8-10ml olacak ekilde al nd . Al nan kan BD BACTEC plus + Aerob c/F 30 ml kan kültür tüplerine konarak bekletilmeden laboratuara gönderildi. Gönderilen örnekler BACTEC 9240 ya da BACTEC 9120 cihaz nda üreme oluncaya kadar bekletildi. Bu süre maksimum 7 gündü. Pozitif sinyal veren i eler cihazdan al nd ktan sonra EMB, kanl agar ve Sabouraud dekstroz agar besi yerlerine ekildi. Solunum yolu örnekleri çevreden bula olmayacak ekilde sterilizasyon ko ullar na dikkat edilerek derin trakeal örnek tüplerine, idrar örnekleri hastalar n mevcut foley kateterlerinden sterilizasyon ko ullar na dikkat edilerek, steril tek kullan ml k enjektörlere ve yara sürüntü örnekleri, steril sürüntü örne i çubuklar yla al narak EMB, kanl agar ve Sabouraud dekstroz agar besi yerlerine direkt olarak ekildi. Ekilen tüm besi yerleri etüvde (Bimderz® ya da Heraew®) 35 santigrat derecede 18-24 saat bekletildi. Sonras nda üreyen mikroorganizma kolonileriyle Phoenix 100 cihaz nda antibiyogram çal ld .
Çal mam zda d lanma kriterleri ise öyleydi:
1. Hastan n klinik ve laboratuar bulgular yla uyumlu olmayan kültür sonuçlar çal ma d b rak ld .
2. Ayn zamanda her iki koldan al nan kan kültür örneklerinden her ikisinde üreme varsa duplikasyonu önlemek için sadece biri de erlendirmeye al nd .
3. Farkl iki kültür örneklemesinden üreyen (Örne in; kan ve trakeal aspirat) ayn patojenlerin antibiyogram paternleride ayn ise klinik olarak enfeksiyon oda n hangisi temsil ediyorsa, sadece o sonuç dahil edildi.
4. Kan kültürlerinde her iki koldan al nan örneklerde farkl etkenler üremi se ve klinik ile uyumlu de ilse bu sonuçlar çal ma d b rak ld .
STAT ST KSEL ANAL Z
Sürekli de i kenler ortalama ± standart sapma (SD), kategorik de i kenler ise oran olarak verildi. Kategorik veriler aras ndaki ili ki için Ki-kare testi kullan ld . P de eri 0.05 ise anlaml kabul edildi.
BULGULAR
DÜTF Gö üs Hastal klar Solunumsal Yo un Bak m ünitesinde 2008 y l nda yatan hastalardan al nan 216 örnekte üreme görüldü. Bu örneklerden 12 si klinik olarak anlaml bulunmad ndan; 4 ü primer enfeksiyon oda ndan al nan kültürlerle e zamanl kan kültüründe de üredi inden, bu 4 örne in e zamanl kan kültür sonuçlar çal maya al nmad . Böylece, toplam 16 örnek çal ma d b rak ld . Sonuçta 78 hastaya ait toplam 200 kültür sonucu çal maya dahil edildi.
Yirmi iki hastadan al nan 25 örnek hastaneye yat lar n n ilk 48-72 saatinde al nm t . Bu örnekler incelendi inde 7 hastaya ait 7 kültür örne i, toplum kökenli geli en enfeksiyon etkeni olarak saptand . Di er 15 hastada geli en enfeksiyonlar ise hastane kökenli enfeksiyon kriterlerini ta maktayd (farkl bir klinikte yatarken klini imize sevk edilen hastalar, sa l k bak m yla ili kili enfeksiyonlar, s k acil ba vurusuyla beraber s k antibiyotik kullanan hastalar).
Hastalardaki mevcut enfeksiyonlar n %91 i hastane kökenli, %9 u toplum kökenli olarak tespit edildi.
Çal maya dahil edilen hastalar n 50 si erkek (%64), 28 i kad nd (%36). Hastalar n ya ortalamas 63.9±18.6 d .
En s k görülen enfeksiyon nedenleri s ras yla pnömoni (%63), KOAH akut atak (%19) ve primer kan yoluyla olu an enfeksiyondu (%14).
Gerçekle en mortalite oran %64 (50 hasta) olup, hastalardan %36 s (28 hasta) yo un bak mdan taburcu edildi.
Mortalite-cinsiyet ili kisine bakt m zda; kad nlarda mortalite %82, erkeklerde mortalite %54 olarak saptand (p=0.01).
Ortalama yat süresi tüm hastalarda 22.7 gündü. Ölenlerin yat süresi 19.4±18.8 gün, taburcu olanlar n yat süresi ise 28.6±26.8 gün idi (p=0.08). Ölen hastalar n ya ortalamas 66.0±17.2 y l, taburcu olanlarda ise 60.1±20.7 y l idi (p=0.17).
Üreme olan kültür örneklerinin 133 (%66.5) ü kan, 36 (%18) s derin trakeal aspirat, 23 (%11.5) ü idrar, 4 (%2) ü yara ak nt s , 3 (%1.5) ü balgam ve 1 (%0.5) i CVP kateterinden olu maktayd (Tablo 1).
Tablo 1:Kültür pozitif örneklerin al nd yerlerin da l m .
N %
KAN 133 66,5
DER N TRAKEAL ASP RAT 36 18,0
DRAR 23 11,5
YARA AKINTISI 4 2,0
BALGAM 3 1,5
CVP KATATER 1 0,5
TOPLAM 200 100,0
N: Üreme olan örnek say s ,
Çal mam zda tüm kültür sonuçlar nda üreme olan bakterilerin da l m na bak ld nda; Koagülaz negatif stafilokoklar (KNS) (%29.5), Acinetobacter (%17.5) ve E. coli (%15) en s k saptanan mikroorganizmalard ( Tablo 2).
Tablo 2. Üreme olan kültür sonuçlar n n etkenlere göre da l m .
N % KNS 59 29.5 AC NETOBACTER 35 17.5 ESCHERICHIA COL 30 15 S. AUREUS 17 8.5 ENTEROCOCCUS 16 8 KLEBS ELLA 10 5 STREPTOCOCCUS 10 5 CAND DA 7 3.5 ENTEROBACTER 4 2 D ER 12 6 TOPLAM 200 100
KNS: Koagülaz negatif stafilokok, N: Üreme olan örnek say s ,
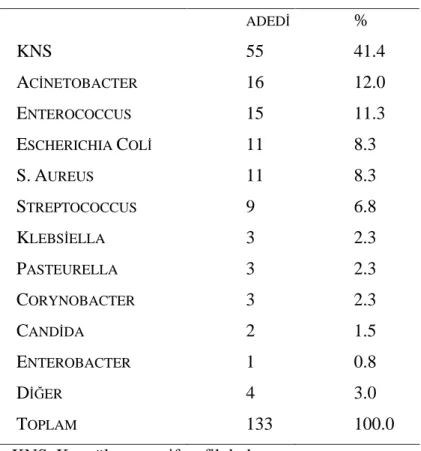
Kanda üreyen patojenlerden en s k saptanan KNS (%41) di. Di er patojenler s ras yla. Acinetobacter (%12), Enterococcus (%11), E. coli (%8) ve S. aureus (%8) olarak saptand (Tablo 3).