T.C.
DİCLE ÜNİVERSİTESİ
TIP FAKÜLTESİ NÖROLOJİ ANABİLİM DALI
AKUT İSKEMİK İNMEDE PLAZMA
MİYELOPEROKSİDAZ SEVİYELERİ VE PROGNOZ
ÜZERİNE ETKİSİ
Dr. ARZU TAY TIPTA UZMANLIK TEZİ
T.C.
DİCLE ÜNİVERSİTESİ
TIP FAKÜLTESİ NÖROLOJİ ANABİLİM DALI
AKUT İSKEMİK İNMEDE PLAZMA
MİYELOPEROKSİDAZ SEVİYELERİ VE PROGNOZ
ÜZERİNE ETKİSİ
Dr. ARZU TAY TIPTA UZMANLIK TEZİ
Doç. Dr. YUSUF TAMAM
İÇİNDEKİLER
Sayfalar
Önsöz……...i
Özet ...…..ii
İngilizce Özet (Abstract) ... iii
Simgeler ve Kısaltmalar Dizini ...iv
Tablolar………vi Şekiller……….vii 1. Giriş ve Amaç ...1 2. Genel Bilgiler ...3 2.1. Serebrovasküler Hastalıklar…...3 2.1.1. Tanım...3 2.1.2. Epidemiyoloji……...3 2.1.3. Risk faktörleri………...3 2.1.4. İnme sınıflaması………8 2.2. Serebral Metabolizma………12
2.2.1. İskemik inmede vasküler otoregülasyon………..12
2.3. Serebral İskeminin Patofizyolojisi……….13
2.3.1. İskemik hücre ölüm mekanizmaları………..16
2.4. Klinik………...17
2.4.1. Karotis sistemi (ön sistem)………....18
2.4.2. Vertebrobaziller sistem (arka sistem)………19
2.5. Tanı………..22
2.6. İnme Komplikasyonları………24
2.7. Prognoz………25
2.8. İskemik İnmede Biyobelirteçlerin Kullanımı………...26
2.9.1.Troponinler………...27 2.9.2.Kreatinin kinaz………...28 2.10. C Reaktif Protein………...……..29 2.11. Miyeloperoksidaz………...…….….30 3. Gereç ve Yöntem ...33 3.1.Çalışma Grubu…………...33
3.2.İnme Tipinin Belirlenmesi...34
3.3.Yapılan İncelemeler………....34
3.3.1. MPO analizi……….38
3.3.2. Kreatinin Kinaz MB (CKMB) izoenzim aktivitesinin ölçümü...39
3.3.3. Troponin T ölçümü………..….39
3.4. İstatiksel Değerlendirme……….40
4. Bulgular ...41
4.1.Klinik ve Demografik Özellikler……….41
4.2.Biyokimyasal Parametreler……….42 4.3.Mortalite………..45 5. Tartışma...55 6. Sonuçlar ...64 7. Kaynaklar ...65
8. Ekler……….82
ÖNSÖZ
Tez konusunun seçiminde ve çalışmaların yürütülmesinde yardımlarını esirgemeyen, tezimin planlanması, yürütülmesi ve sonuçlarının değerlendirilmesi konusunda büyük katkı ve desteğini görmüş olduğum, uzmanlık eğitimim süresince birlikte çalıştığım, örnek kişiliğiyle bizlere her zaman yol gösteren, gerek mesleki gerekse sosyal anlamda her türlü desteğini esirgemeyen tez danışman hocam Sayın Doç. Dr. Yusuf TAMAM’a;
Nöroloji uzmanlık egitim sürem boyunca bilgi ve tecrübelerinden yararlandığım başta anabilim dalı başkanımız Sayın Prof. Dr. Nebahat TAŞDEMİR olmak üzere tüm hocalarıma ve tüm arkadaşlarıma tesekkür ederim.
Laboratuar çalışmalarının yürütülmesinde aktif katkı ve desteğini görmüş olduğum Sayın Doç. Dr. Beran YOKUŞ’a ve sonuçların istatiksel hesaplanmaları ve yorumları konusunda çok değerli katkı ve fikirleri ile beni aydınlatan Sayın Yrd. Doç. Dr. Mehmet ÜSTÜNDAĞ ve Sayın Yrd. Doç. Dr. Murat ORAK’a ayrıca teşekkür ederim.
AKUT İSKEMİK İNMEDE PLAZMA MİYELOPEROKSİDAZ SEVİYELERİ VE PROGNOZ ÜZERİNE ETKİSİ
ÖZET
İskemik inme, beyin dokusunda meydana gelen infarkt nedeni ile ani olarak ortaya çıkan patolojik bir durumdur. Bunlar arasında en fazla üzerinde durulan, inmede inflamasyonun rolüdür. Aterogenez ve akut serebral iskemide inflamatuar süreçlerin rol oynadığına dair deliller giderek artmaktadır. Oksidatif stres ve inflamasyon, aterosklerozun patogenezine katkıda bulunur. Miyeloperoksidaz (MPO) enzimi, oksidatif strese yanıt olarak lökositlerden salgılanan lizozomal bir enzimdir. Lökositelerde bolca bulunan ve reaktif oksidan ürünler oluşturan MPO aterosklerotik reaksiyonlarda bulunur ve katalitik aktivite gösterir.
Biz bu çalışmada akut iskemik inme ile gelen hastaların miyeloperoksidaz plazma düzeylerinin prognoz üzerine etkisini araştırdık. Akut iskemik serebrovasküler hastalık tanısı alan 55 hasta ile kontrol grubu olarak yaş ve cinsiyet dağılımı uyumlu 40 sağlıklı birey prospektif olarak değerlendirmeye alındı. Hastalardan inmeyi takiben ilk 24 saat ve 5. gün kan örnekleri alınırak plazma miyeloperoksidaz düzeylerine bakıldı. Hasta grubunun miyeloperoksidaz düzeyleri kontrol grubuna kıyasen anlamlı derecede yüksekti (p<0.0001). Hasta grubunda sağ kalanların ve ilk 6 ay içinde ölenlerin myeloperoksidaz düzeyleri karşılaştırıldığında, miyeloperoksidaz yükseliği mortalite yönünde anlamlı olarak yüksek bulunmuştur (p<0.000).
Sonuç olarak çalışmamız akut iskemik inmeli hastalarda plazma miyeloperoksidaz düzeyinin arttığını, ve plazma miyeloperoksidaz düzeyinin prognozla ilişkisinin olduğunu göstermektedir. Miyeloperoksidaz düzeyinin aterogenezdeki ve inme sonrası olusan inflamatuar yanıttaki rollerinin daha iyi anlaşılabilmesi için yeni ve kapsamlı çalısmalara ihtiyaç vardır.
ANAHTAR SÖZCÜKLER: Akut iskemik inme, miyeloperoksidaz, inflamasyon, mortalite, ateroskleroz.
THE LEVELS OF MYELOPEROXIDASES IN ACUTE ISCHEMIC STROKE AND ITS EFFECT ON PROGNOSIS
ABSTRACT
Ischemic stroke is a pathological condition with acute onset that is caused by the infarction of brain tissue. The most commonly mentioned etiological factor among those is the role of inflammation in stroke. There is a growing number of evidence suggesting the role of inflammatory process in the etiology of aterogenesis and acute cerebral ischemia. Oxidative stress and inflammation also contribute into pathogenesis of atherosclerosis. Myeloperoxidase enzyme (MPO) is a lyzozomal enzyme secreted from leukocyte as a response to oxidative stress. MPO, as an enzyme present in abundant amount in leucocytes and creating reactive oxidant metabolites, plays an active role in atherosclerotic reactions and presents catalytic activity.
The aim of this study was to evaluate the effect of myeloperoxidase levels on the prognosis of acute ischemic stroke patients. The sample of the study consisted of 55 inpatients who received a diagnosis of acute ischemic cerebrovascular disease and 40 healthy age and sex matched individual as a control group. Plasma MPO levels of the patients have been measured in the first 24 hours after initial stroke and at the 5th day after stroke. MPO levels in the patients were significantly higher than the control group (p<0.0001). Increased levels of MPO was an important indicator for mortality as patients who survived six months had significantly lower levels of MPO than the ones who deceased (p<0.0001).
The results of this study have showed that plasma MPO levels significantly increase in acute ischemic stroke patients and had a significant correlation with prognosis. Larger studies are warranted for better understanding of the role of MPO levels in inflammatory response that appears after aterogenesis and post stroke periods.
KEYWORDS: Acute ischemic stroke, myeloperoxidase, inflammation, mortality , atherosclerosis
SİMGELER VE KISALTMALAR DİZİNİ ACA: Anterior serebral arter
ACS: Akut koroner sendrom AMI: Akut miyokard infarktüsü
AİCA: Anterior inferior serebellar arter AchA: Anterior koroidal arter
BT: Bilgisayarlı tomografi BI: Barthel İndeksi CRP: C-reaktif protein CK: Kreatinin kinaz
CK-MB: Kreatinin Kinaz MB CK-MM: Kreatinin kinaz MM CK-BB: Kreatinin kinaz BB CND: Kanada Strok Skalası DSÖ: Dünya Sağlık Örgütü GİA: Geçici iskemik atak GKS: Glascow Koma Skalası HOCl: Hipoklorik asid hsCRP: high sensitivity CRP
HDL: Yüksek yoğunluklu lipoprotein İMK: İntima media kalınlığı
İCA: İnternal karotid arter LCAI: Laküner infarktlar
LDL: Düşük yoğunluklu lipoprotein MCA: Orta serbral arter
MPO: Miyeloperoksidaz
MRG: Magnetik rezonans görüntüleme
NMDA: N-metil-D-aspartat NO: Nitrik Oksit
NIHSS: National Institute of Health Stroke Skalası OEF: Oksijen ekstraksiyon fraksiyonu
PCA: Posterior serebral arter
PİCA: Posterior inferior serebellar arter PACI: Parsiyel anterior sirkülasyon infarktları POCI: Posterior sirkülasyon infarktları RS: Rankin Skalası
SVH: Serebrovasküler hastalık SKA: Serebral kan akımı SKH: Serebral kan hacmi SCA: Süperior serebellar arter
TACI: Total anterior sirkülasyon infarktları
TOAST: Trial of Org 10172 in Acute Stroke Treatment tPA: Doku plazminojen aktivatörü
TABLOLAR
Tablo 1 İnme risk faktörlerinin sınıflandırılması. 4
Tablo 2 Bamford ve arkadaşlarına göre serebral infarkt alt gruplarının sınıflandırılması.
9 Tablo 3 1993 yılında yapılan TOAST sınıflamasında iskemik infarktlar
etyolojiye göre grublara ayrılmıştır.
10 Tablo 4 TOAST sınıflamasına göre kardioemboli kaynakları. 11
Tablo 5 Akut inmeli hastada tanı incelemeleri. 22
Tablo 6 Strok sonrası gelişebilecek komplikasyonlar 25
Tablo 7 NIHSS - (National institutes of health stroke scale). 35
Tablo 8 Gruplarının yaş ve cinsiyete göre dağılımı. 41
Tablo 9 Hasta ve kontrol grubunun demografik özellikleri tabloda verilmiştir.
42
Tablo 10 Gruplara göre biyokimyasal parametreler. 43
Tablo 11 Takip periyodlarına göre hasta ve kontrol gruplarının MPO düzeyleri.
44 Tablo 12 Sağ kalan ve ölen hastalarımızın klinik ve demografik
özellikleri.
46 Tablo 13 Sağ kalan ve ölen hastalarımızın inme lokalizasyonu, lezyon çapı
ve klinik bulguları arasındaki ilişki.
48 Tablo 14 Sağ kalan ve ölen hastalarımızın biyokimyasal parametreleri ve
diğer sayısal değişkenlerinin karşılaştırılması.
49 Tablo 15 Plazma MPO düzeyleri yüksek ve normal olan hastalarımızda
inme lokalizasyonu, lezyon çapı arasındaki ilişki.
53 Tablo 16 Plazma MPO düzeyleri yüksek ve normal olan hastalarımızda
yaş ve biyokimyasal parametrelerin karşılaştırılması.
54
Şekil 1 Hasta ve kontrol gruplarımızın plazma MPO düzeylerini gösteren boxplot grafik.
44 Şekil 2 Hasta ve kontrol gruplarımızın plazma Troponin T düzeylerini
gösteren boxplot grafik.
45 Şekil 3 Sağ kalan ve ex olan hasta gruplarımızın plazma CKMB
düzeylerini gösteren boxplot grafik.
50 Şekil 4 Sağ kalan ve ex olan hasta gruplarımızın plazma CRP düzeylerini
gösteren boxplot grafik.
51 Şekil 5 Sağ kalan ve ex olan hasta gruplarımızın plazma MPO düzeylerini
gösteren boxplot grafik.
1. GİRİŞ VE AMAÇ
Serebrovasküler hastalıklar (SVH), tüm toplumlarda kalp hastalıkları ve kanserlerden sonra mortalite nedeni olarak üçüncü sırada, özürlülük ve sakatlık yapma açısından birinci sırada yer alan, endüstrileşmiş toplumlarda hastane başvurularında ve sağlık harcamalarında önemli bir yer tutan hastalık grubudur (1,2). Dünya Sağlık Örgütü (DSÖ) inmeyi ‘hızla gelisen ve 24 saat veya daha uzun süren yada ölümle sonuçlanabilen, serebral işlevlerin fokal veya global bozukluğuna bağlı bulgular’ olarak tanımlamaktadır (2, 3).
ABD’de her yıl yaklaşık 700.000 yeni inme vakası eklenmektedir. Bu oran artan yaşlı nüfusla birlikte artma eğilimindedir, ve Amerika Bileşik Devletlerine bu hastaların yıllık maliyeti 30 milyon dolardır (4). Uzun dönem izlemde, inme geçiren hastaların %15’i kişisel hijyeni için başkasına bağımlıyken, %30’u günlük yaşam aktivitelerinde birinin yardımına ihtiyaç duymakta ve %60 kadarı da sosyal aktivitelerde kısıtlılık yaşamaktadır (4).
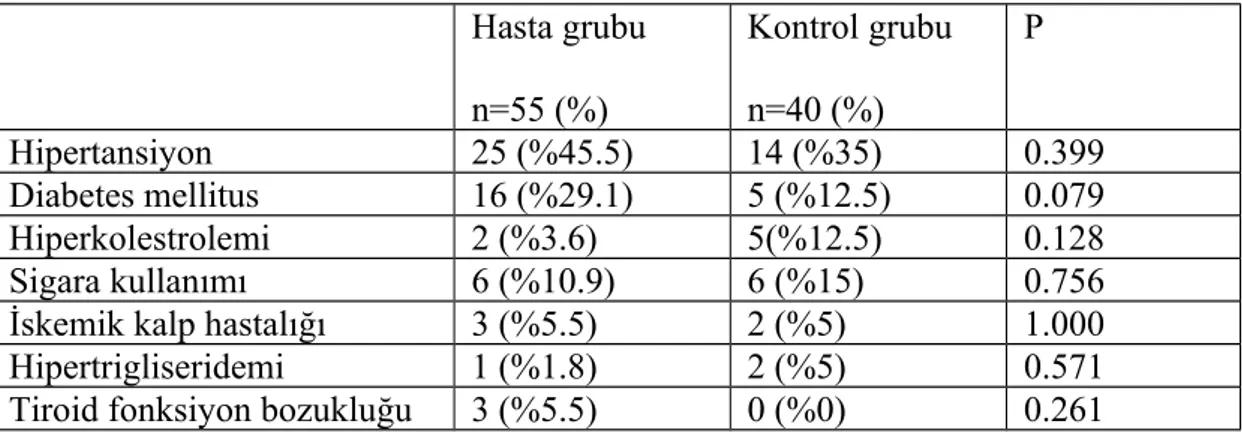
SVH birbirinden bağımsız birçok risk faktöründen etkilenerek gelişmektedir. İskemik inme için bilinen risk faktörleri arasında cinsiyet, yaş, herodofamilyal predispozisyon, hipertansiyon, diabetes mellitus, obesite, hemotokrit, fibrinojen, kan lipidlerinin yüksekliği ve asemptomatik karotis stenozu sayılabilir (5, 6, 7).
Ateroskleroz inflamatuar bir hastalık olup genellikle orta ve büyük damarları tutar. Aterosklerozun komplikasyonlarına sıklıkla kalp ve beyin damarlarında rastlanır. Aterosklerozda görülen aterom plaklarının yapısı farklı olabilmektedir. Hassas plaklar rüptüre olma eğiliminde olup çoğunlukla akut olaylar ile kendini gösterir. Bu nedenle gerek kardiyak iskemik olaylar, gerekse de iskemik inme plak yapısı ile yakından ilişkilidirler.
Aterogenez ve akut serebral iskemide inflamatuar süreçlerin rol oynadığına dair deliller giderek artmaktadır (8, 9). İskemik inmede, serebral kan akımının azalmasına sekonder olarak biyokimyasal ve immünolojik birçok reaksiyon gerçekleşmektedir. İskemi sonrası dinamik bir süreç olup, çeşitli moleküller ve immün hücreler arasında komplike ilişkiler izlenmektedir. Akut iskemik inmenin fizyopatolojisinde iyon değişiklikleri, eksitotoksisite, serbest radikaller ve nitrik oksit hasarı, postiskemik inflamatuar reaksiyonlar rol almaktadır. İskemik inmede,
periferik kandaki lökositlerin 12 saat içinde beyin parankimine göç ettiği deneysel hayvan modellerinde gösterilmiştir (10). Migrasyon, serebral endotel hücreleri ve lökositlerin yüzeylerinde bulunan adezyon molekülleri yardımıyla gerçekleşir. Böylece muhtelif stimuluslarla uyarılarak aktive olan bu hücreler, birçok farklı sitokinler, kemokinler ve diğer inflamatuar mediyatörler salgılarlar (8). Bunların çoğu iskemik inmede hücre hasarından sorumludur.
Oksidatif stres ve inflamasyon koroner aterosklerozda plak destabilizasyonuna yol açarak akut koroner sendromların meydana gelmesinde önemli rol oynarlar. Miyeloperoksidaz LDL ‘nin oksidasyonundan da rol alır. Makrofajlar, matriks metalloproteinazlar ve metal bağımsız miyeloperoksidaz sekresyonu yoluyla aterom plağındaki kollajen tabakasının yıkımı ve fibröz kapsülü zayıflatarak akut koroner olayların meydana gelmesinde rol alır (11, 12).
Kardiyak dışı inflamatuar ve infeksiyöz durumlarından da miyeloperoksidaz düzeyi artabilmektedir. Özetle, Miyeloperoksidaz kardiyak spesifik olmamasına rağmen plak destabilizasyonunun bir belirteci olarak kullanılmaya adaydır (11).
Biz inmeli hastalarda yeni biyobelirteçlerden olan myeloperoksidaz’ın klinik seyir, kısa dönem prognostik etkileri ve risk değerlendirilmesindeki yerini araştırmayı amaçlıyoruz.
2.GENEL BİLGİLER
2.1. Serebrovasküler Hastalıklar 2.1.1. Tanım:
Serebrovasküler hastalık (SVH), santral sinir sisteminde iskemi ya da hemorajinin neden olduğu akut nörolojik bir disfonksiyondur (13,3). Akut iskemik inme, beyin kan damarlarının tıkanmasına bağlı gelişen enfarkt olarak tanımlanır ve hastaneye başvurunun en yaygın nörolojik sebebidir (14). Tüm inmelerin %80 ile %85’ini oluşturur (2,14). İnme, ölüm ve sakatlıkların önemli nedenidir (15). SVH’lar dünyada kalp hastalığı ve kanserden sonra üçüncü en sık ölüm nedeni olup, beynin en sık görülen hastalıklarıdır (1,2).
2.1.2. Epidemiyoloji:
SVH, dünyada 3. sırada ölüm ve 1. sırada özürlülük nedenidir. Amerika Birleşik Devletleri’nde yılda yaklaşık 6.000.000 iskemik, 100.000 hemorajik serebrovasküler olgu görülmekte ve bunlarında 175.000’i ölümle sonuçlanmaktadır (16). Yapılan çalışmalara göre, 55-64 yaşlarda yıllık inme insidansı 1.7- 3.6/1000 kişi, 65-74 yaş arası 4.9-8.9/1000 kişi, 75 yaştan sonra 13.5-17.9/1000 kişidir. Kadınlarda 55-64 yaş arası inme insidansı erkeklere göre 2-3 kat daha azdır. 85 yaşa doğru bu fark azalmaktadır (2).
İnme prevalansı yaşla birlikte artar. Coğrafi özellikler de gösterebilir. Batı ülkelerinde inme prevalansı 8/1000, Japonya’da 20/1000’dir. Ülkemizde ise sağlıklı veriler bulunmamaktadır (2).
Serebrovasküler hastalıklar; serebral iskemi (% 60-80), intraserebral hemoraji (% 10-15), subaraknoid kanama (% 3-10) olmak üzere 3 ana grupta toplanmıştır (2).
2.1.3. Risk faktörleri:
Akut inme tedavisindeki gelişmelere rağmen, inme, ölüm ve sakat bırakmadaki önemini hala korumaktadır. Bunun için risk faktörlerini belirleyip bunlardan
korunmak, toplum sağlığı ve ülke ekonomisi açısından önemlidir. İnmede risk faktörleri şu şekilde sınıflandırılır (Tablo 1).
Tablo 1. İnme risk faktörlerinin sınıflandırılması. I.Değiştirilemeyen risk Faktörleri
a) Yaş b) Cinsiyet c) Irk
d) Aile Öyküsü
II.Değiştirilebilen risk faktörleri a) Kesinleşmiş faktörler 1. Hipertansiyon 2. Diabetes mellitus 3. Kalp hastalıkları 4. Hiperlipidemi 5. Sigara
6. Asemptomatik karotis stenozu 7. Orak hücreli anemi
b) Kesinleşmemiş faktörler 1. Alkol kullanımı 2. Obesite 3. Beslenme alışkanlıkları 4. Fiziksel inaktivite 5. Hiperhomosisteinemi 6. İlaç kullanımı ve bağımlılığı 7. Hormon tedavisi
8. Hiperkoagulabilite 9. Fibrinojen
10. inflamasyon 2.1.3.1. Değiştirilemeyen risk faktörleri:
a)Yaş: İnme ile ilişkili en önemli risk faktörüdür (17). 55 yaştan sonra inme riski, her dekatta iki kat artar (2).
b)Cinsiyet: Erkeklerde inme insidensi kadınlara göre daha fazladır. İnmeye bağlı ölümler ise kadınlarda erkeklerden daha fazladır (18).
c)Irk: Zencilerde, Çinlilerde ve Japonlarda strok insidansı, beyazlara göre daha yüksektir (2).
d)Aile Öyküsü: Anne ve babada, birinci derecede akrabalarda inme öyküsünün bulunması, artmış inme riski ile paralellik gösterir. İnme riskinin tek yumurta ikizlerinde ayrı yumurta ikizlerine göre 5 kat daha fazla olduğu görülmüştür (19,20).
2.1.3.2. Değiştirilebilen risk faktörleri: 2.1.3.2.1. Kesinleşmiş Risk Faktörleri:
a ) Hipertansiyon: Hipertansiyon toplumda prevalansı en yüksek olan, hem serebral infarkt hem de intraserebral hemoraji için en önemli risk faktörüdür. On dört randomize çalışmanın meta-analizine göre diastolik kan basıncında 5.8 mmHg’lık bir düşme, inme riskini %42 oranında azaltmaktadır (21). İnme insidansı; hem sistolik hem diastolik hipertansiyonla artar. Diastolik basınç artışının eşlik etmediği izole sistolik hipertansiyon yaşlılarda önemli inme risklerinden biridir (22).
b ) Diabetes Mellitus: Çeşitli çalışmalarda diabetin, iskemik inme riskini 2-6 kat arttırdığı gösterilmiştir. Büyük damar aterosklerozunu hızlandırdığı, düşük ve yüksek dansiteli lipoprotein kolesterolleri üzerine olumsuz etkide bulunduğu ve hiperinsülinemi yoluyla aterosklerotik plağı büyüttüğü bilinmektedir. İnsülin bağımlı diyabetiklerde, hipertansiyon ve hiperlipidemi gibi diğer aterosklerotik risk faktörleri daha sık bulunur (22).
c ) Kalp Hastalıkları: Kalp hastalıkları inme riskini 2-4 kat artırmaktadır. Gençlerdeki en önemli embolijenik kalp hastalıkları atriyal fibrilasyon ile birlikte veya yalnız olarak görülen mitral stenoz, kapak replasmanı ve bu hastalarda sık görülen infektif endokardit, tek başına ya da interseptal anevrizma ile birlikte olan patent foramen ovale, kardiyak tümörler, mitral regürjitasyon, atriyal fibrilasyon ile birlikte olan mitral kapak prolapsusu, Libman-Sack endokarditi, dilate kardiyomyopatidir. Orta yaş ve üzerinde ise en sık görülen kardiyoemboli sebebi myokard infarktüsüdür. İleri yaşta en önemli kardiyojenik emboli riski nonvalvüler atriyal fibrilasyondur. Yaş arttıkça görülme sıklığı da artar. Nonvalvüler atriyal fibrilasyonda yıllık inme görülme hızı ortalama %3-5 olup, daha önce geçirilen geçici iskemik atak veya inme, hipertansiyon, sol ventrikül fonksiyon bozukluğu, ileri yaş, diyabet ve kadın olmak bu riski arttırmaktadır (2).
d) Dislipidemi: Serum total kolesterol ve düşük yoğunluklu lipoprotein (LDL) fazlalığının aterosklerozla ilişkili olduğu gösterilmiştir. Ayrıca yüksek yoğunluklu
lipoprotein (HDL) kolesterol düşüklüğü de koroner kalp hastalığı ve inmeyle ilişkilidir. Anglo–Scandinavian Cardiac Outcomes Trial–Lipid Lowering Arm (ASCOT–LLA) çalışmasında lipid düsürücü ajanlarla yapılan çalışmada statinlerin, inmede primer korumada etkili olduğunu göstermiştir (23).
‘Multiple risk factor intervention trial’ çalışmasında yüksek kolesterol düzeyi ile inmeye bağlı mortalite arasında direkt ilişki bulunduğu gösterilmiştir. Risk, kolesterol düzeyi 240–279 mg/dl arasında ise 1.8, 280mg/dl’nin üzerinde ise 2.6 kat artmaktadır (24).
e) Sigara: Prevalansı oldukça yüksek olması (ortalama % 25) nedeniyle önemli bir risk faktörü olup, iskemik inme için relatif risk 1.8-6 olarak bulunmuştur. Bu risk sigara bırakıldıktan 5 yıl sonra içmeyenlerin düzeyine inmektedir (25). Sigara dumanına maruz kalanlarda yapılan çalışmalarda iskemik inme riski en az 1.2 olarak bulunmuştur (2).
f) Asemptomatik Karotis Stenozu: % 50’den fazla asemptomatik karotis stenozu, 65 yaş üzeri erkeklerin % 7-10, kadınların % 5-7’sinde görülmektedir. Çeşitli çalışmalarda bu vakalarda yıllık ipsilateral strok riski % 1-2 olarak bulunmuştur. Asemptomatik karotis arter stenozu % 75’in altında yıllık inme riski % 1.3 iken, stenoz % 75’in üzerinde yıllık strok ve geçici iskemik atak (GİA) riski % 10.5’e çıkmaktadır (2, 26, 27).
g) Orak Hücreli Anemi: Bu hastalarda 20 yaşına kadar inme prevalansı %11’dir. Kan transfüzyonlarıyla inme riskinin yılda %10’dan %1’e düştüğü yapılan çalışmalarda gösterilmiştir (2).
2.1.3.2.2. Kesinleşmemiş risk faktörleri:
a)Alkol kullanımı: Alkol tüketimi ile inme arasındaki ilişki oldukça kompleks olup, bu risk profili iskemik inme için ‘’J’’ şeklinde kabul edilmektedir. Günde iki kadehe kadar alkol tüketiminin HDL kolesterol artışı, trombosit agregasyonunda azalma, fibrinojen azalması gibi mekanizmalarla iskemik inme riskinin azalttığı öne sürülmektedir. Fakat daha yüksek miktarlarda alkol, hipertansiyon, hiperkoagülabilite ve kardiyak aritmilerde artışa yol açarak riski arttırmaktadır (2).
Fazla miktarda alkol tüketenlerin ayrıca hemorajik inme geçirme riski, içmeyenlere göre üç kat daha fazladır (22).
b) Obesite: Vücut kitle indeksinin 30 kg/m²’nin üzerinde olması ile karakterize olan ve özellikle erkeklerde sık görülen abdominal obezitenin, diğer risk faktörleri ile birlikte oluşunun dışında, indeksteki artışa paralel olarak inme riskini 1.75-2.37 kat arttırdığı tesbit edilmiştir (2).
c) Beslenme Alışkanllıkları: Diyetteki yağ miktarı, çeşidi ve balık tüketimi ile inme arasındaki ilişki çelişkilidir. Çeşitli çalışmalarda diyete C ve E vitaminlerinin eklenmesinin inme riskini düşürmediği ortaya çıkmıştır (2).
d) Fiziksel İnaktivite: Çeşitli çalışmalarda düzenli fiziksel egzersizin inme riskini azalttığına ilişkin veriler mevcuttur (2).
e) Hiperhomosisteinemi: Artmış kan homosistein düzeyi, ateroskleroz ve tromboz için risk olabilir. Çalışmalarda inmeyle olan ilişkisi gösterilmiştir. Bir meta-analize göre, homosistein düzeyindeki 5 μmol/L düzeyindeki artış, inme riskinin yükselmesine neden olmuştur (28).
f) İlaç kullanımı ve bağımlılığı: Amfetamin, kokain ve eroin gibi bağımlılık yapan maddelerin kullanımı hem hemorajik hem de iskemik inmeye yol açabildiği bilinmekteyse de bu konuda geniş epidemiyolojik çalışma yoktur. Sınırlı çalışmalarda inme riskinin yaklaşık 7 kat arttığı bildirilmektedir (2).
g) Oral kontraseptif kullanımı: Oral kontraseptiflerin inme riski, içerdikleri estradiol miktarı ile ilişkili olup, 50 mikrogram’dan fazla estradiol içeren ilk jenerasyon ilaçlarda bu risk yüksektir. Son zamanlarda kullanılan düşük estradiol ve kombine preparatlarla yapılan çalışmalarda iskemik ve hemorajik inme riskinde hafif bir artış gözlenmiştir (2).
h) Hiperkoagulibite: Hiperkoagülabilteye yol açan trombofililer (Protein C ve S eksikliği, aktive protein C rezistansı, ATIII eksikliği ve protrombin 20210 mutasyonu) öncelikle venöz trombozlara yol açmakla birlikte, iskemik inmelere de neden olabilirler. Fakat diğer risk faktörleri elimine edildiğinde, gerçek risk değerleri kuşkuludur. Bir diğer hiperkoagülabilite nedeni olan antifosfolipid antikor sendromu ile yapılan çalışmalarda farklı antikor izotipleri (IgG, IgM veya IgA) göz önüne alındığından, bu sendromunun da prevalansı ve inme riski tartışmalıdır. Yüksek doku plazminojen aktivatörü (tPA) , fibrin D-dimer, von Willebrand faktör ve faktör
VIIIc’nin inme risk faktörü olduğuna ilişkin bazı çalışmalar bulunmakla birlikte bu konuda daha kapsamlı araştırmalara ihtiyaç bulunmaktadır (2).
ı) Fibrinojen: Yüksek plazma fibrinojen düzeyi serebral infaktın gelişmesinde bağımsız bir risk faktörüdür (26).
i) İnflamasyon: İskemik inmenin en önemli nedeni aterosklerozdur. Aterosklerozun kronik bir inflamatuar hastalık olduğu düşünülmektedir. İnflamasyon süreciyle iskemik olaylar arasında ilişki vardır.
İskemik inme geçirenlerde akut faz reaktanı olan C-reaktif protein (CRP) ve serum amiloid A yüksek olarak bulunmaktadır (2). ‘’CARE’’ çalışmasında aspirin ve ravastatinin CRP’yi düşürerek inme riskine azalttığına ilişkin veriler elde edilmiştir (29).
2.1.4. İnme sınıflaması:
SVH’lar; iskemik (infarkt) ve hemorajik kökenli olmak üzere iki ana kategoriye ayrılabilir (14). İskemik inmeler en sık inme nedenidir. İskemik inmeler tüm SVH’ların %60-80’ini oluşturur. İskemik inmeler gelişmiş ülkelerde ölüme ve iş görmezliğe en sık neden olan erişkin nörolojik hastalığıdır. İskemik inmeler, intrakraniyal veya ekstrakraniyal arterlerden kaynaklanan tromboembolizm (arter-arter embolisi), kalp kaynaklı embolizm, hiperkoagülabilite durumları, beynin küçük penetran arterlerinin tıkanıklıkları, ateroskleroz dışı vaskülopatiler sonucunda oluşur. Hemorajik inme ise primer intraserebral kanama (%10-15) ve subaraknoid kanama (%3-10) olarak ikiye ayrılabilir. SVH’ların %3 kadarı ise sınıflandırılamamaktadır (30, 31, 2).
Hemorajik inmeler: İntraserebral hemorajide genellikle kanamanın kaynağı, beyin parakiminde olup, sıklıkla küçük penetran arterlerin kanamasıyla, bazal ganglion, talamus, pons gibi beynin derin bölgelerinde hematomlar oluşur. Başlıca nedeni hipertansiyona bağlı olarak bu artelerde akkiz olarak gelişen Charcot-Bouchard anevrizması rüptürüdür. Diğer nadir nedenler ise, arteriovenöz malformasyonlar, amiloid anjiopati, kanama diyatezleri, tümör kanamaları, travma, antikoagülasyon, Moyamoya hastalığı ve sempatomimetik ilaç kullanımıdır. Klinik tablo, ani gelişen baş ağrısı, bulantı, kusma, bilinç bozukluğu ve fokal nörolojik
defisitlerle karakterizedir. Ağır klinik bulgulara yol açmayan küçük hematomlar dışında, mortalite oldukça yüksek olup, %70’lere kadar çıkmaktadır (2).
İskemik inmeler: Serebral infarktlarda etyolojiye göre sınıflandırma, iskeminin tedavisi, prognozu ve ikincil önlemler açısından çok önemlidir. Bamford ve arkadaşları 1991 yılında klinik bulgulara göre bir sınıflandırma yapmışlardır (Tablo 2). Ancak bu sınıflandırmada potansiyel etyolojiye yer verilmemiştir (2).
Tablo 2. Bamford ve arkadaşlarına göre serebral infarkt alt gruplarının sınıflandırılması.
1. Total anterior sirkülasyon infarktları (TACI) 2. Parsiyel anterior sirkülasyon infarktları (PACI) 3. Laküner infarktlar (LCAI)
4. Posterior sirkülasyon infarktları (POCI)
Bamford ve arkadaşlarının (32) 1991’de yaptığı bu sınıflamada TACI a. serebri media’nın büyük bir bölümünü kapsayan bir infarkta işaret eder. Bu durum oldukça geniş bir alanda infarkta neden olur ve a. serebri media’nın proksimal oklüzyonu ya da a. karotis interna oklüzyonu sonucu gelişir. PACI’de ise bu düzeyde geniş bir alan etkilenmez ve genellikle a. serebri media dallarından biri, nadiren de anterior serebral arter tıkanması sorumludur. Laküner infarktlar ise kortikal bulgular ve hemianopsinin olmadığı; motor ve/veya duysal bulguların yüz, kol ve bacağın hepsini ya da en azından ikisini içeren durumlardır. Laküner infarktlar penetran arterlerden birinin tıkanmasına bağlı küçük ve derin infarktlardır. Posterior dolaşım infarktlarında ise vertebrobaziler sistemi oluşturan arterlerin oklüzyonuna bağlı olarak oksipital loblar, beyin sapı ve serebellum tutulumu görülür. Klinikte beyin sapı ve serebellar bulgularla hemianopsinin farklı kombinasyonlarının görülmesiyle tanınırlar (33).
1993 yılında yayınlanan TOAST ‘Trial of Org 10172 in Acute Stroke Treatment’ çalışmasında kullanılan sınıflandırma ise, klinik bulguların yanı sıra etyolojiye de yer verdiğinden günümüzde yaygın olarak kullanılmaktadır (Tablo 3). İskemik inmelerde klinik alt grupların belirlenmesi, inme tedavi stratejilerinin seçimi, erken ve geç dönem prognoz hakkında bilgi vermesi açısından önemlidir.
Özellikle tedavinin risk ve yararı arasındaki denge, iskemik inme alt gruplarında ayrı özellikler taşır (34).
Tablo 3. 1993 yılında yapılan TOAST sınıflamasında iskemik infarktlar etyolojiye göre grublara ayrılmıştır.
1.Geniş arter aterosklerozu 2.Kardioembolizm
3.Küçük damar oklüzyonu (laküner infarkt) 4.Diğer belirlenen etyolojiler
5.Neden saptanamayanlar
1.Geniş arter aterosklerozu: Tüm iskemik inmelerin %50’si geniş arter aterosklerozuna bağlıdır. Bu alt grup, özellikle ekstrakraniyal ve daha nadir olmak üzere intrakraniyal damarlarda ve bunların bifurkasyon bölgelerinde, yıllar içerisinde gelişen aterom plaklarının stabilizasyonlarının bozulmasıyla ortaya çıkan trombozlara bağlı olarak gelişir. Klinik tablo, tıkanan artere göre değişir. Kortikal fonksiyon bozuklukları, beyin sapı ve serebellar disfonksiyon bulguları olabilir. Lezyon kortekste, subkortekste, beyin sapında, serebellumda olabilir ve 1.5 cm’den daha büyük olabilir. İnfarkt bölgesini sulayan intrakranial veya ekstrakranial bir arterde saptanacak %50’den fazla (aterosklerotik) darlık bu kategori tanısı için gerekli ve yeterli kanıttır. Tanısal yöntemlerle potansiyel kardiyojenik emboli kaynakları dışlanmalıdır (34). Bu olgularda arterden artere emboli, darlık distalinde hemodinamik yetmezlik veya bu iki mekanizma bir arada rol oynayabilir (35).
2. Kardioembolizm: Tüm iskemik inmelerin %20’sini oluşturan kardiyoembolizmde, arteriyel oklüzyonun nedeni kalpten kaynaklanan embolilerdir. Kardiak emboli kaynakları yüksek ve orta dereceli olmak üzere 2 farklı risk grubuna ayrılmıştır. Kardiyoembolik inme tanısı için en az 1 potansiyel kardiak emboli kaynağı gösterilmelidir (Tablo 4).
Tablo 4. TOAST sınıflamasına göre kardioemboli kaynakları.
Yüksek Riskli Nedenler Orta Riskli Nedenler * Mekanik protez kapak * Mitral valv prolapsusu * Atriyal fibrilasyonlu mitral stenoz * Mitral annulus kalsifikasyonu * Atriyal fibrilasyon * Atriyal fibrilasyonsuz mitral darlık * Sol Atriyum / Atriyal apendikste trombüs * Sol atriyal türbülans
* Hasta sinüs sendromu * Atriyal septal anevrizma * Yeni myokard infarktı (<4 hafta) * Patent foramen ovale * Sol ventrikülde trombüs * Atriyal flatter * Dilate kardiyomyopati * MI (>4 hafta <6ay) * Akinetik sol ventriküler segment * Biyoprotez kalp kapağı * Atriyal miksoma * Nonbakteriel trombüs * Enfektif endokardit * Konjestif kalp yetmezliği * Hipokinetik sol ventrikül
Kardioembolik inmeler kısmen daha genç yaşları ilgilendirir ve sıklıkla hızlı gelişerek saniyeler-dakikalar içinde maksimal defisit açığa çıkarırlar. Multipl damar alanlarında geçici iskemik atak veya infarkt, kortikal dal oklüzyonları, hemorajik infarkt, sistemik embolizasyon, akut inme semptomları yanında başağrısı ve epileptik nöbet gibi özellikler kardioembolik inmelerde daha sıktır. BT (Bilgisayarlı tomografi) /MRG (Magnetik rezonans görüntüleme)’da bir arter alanına uyan geniş kortikal infarkt görüleceği gibi değişik vasküler alanlarda birden fazla lezyon da görülebilir. Kardioembolik infarkt tanısı emboli kaynağının gösterilmesi ve diğer inme nedenlerinin dışlanması ile konur. En sık emboli nedeni olan kalp hastalıkları atrial fibrilasyon, miyokard infarktüsü, kalp kapak hastalıkları ve trombüstür (36, 37, 38).
3. Küçük damar oklüzyonu (laküner infarkt): Tüm strok olgularının %15 ile 30 kadarını oluşturur (39,40). Bu infarktlar tek bir damar alanında tanımlanan küçük iskemik bölgelerde oluşan lezyonlardır. Lakünün patolojik tanımlaması; ortalama 5mm çapta (3-15 mm) ufak serebral infarktlardır. Lakünler talamus, bazal ganglionlar, korona radiata, sentrum semiovale, internal kapsül ve beyin sapında
görülebilir. Temel patoloji damar duvarı yıkımı, damarın fokal ekspansiyonu, trombotik tıkanma, hemorajik ekstravazasyon ve fibrinoid depolanmadır (41).
4. Diğer belirlenen etyolojiler: Bu grupta, santral sinir sisteminin primer ve sekonder vaskülitleri, serebral amiloid anjiopati gibi nadir küçük damar hastalıkları, konjenital damar hastalıkları, mitokondriyal hastalıklar, travma ve disseksiyon ile kan hastalıkları yer alır, ve tüm iskemik inmelerin %5’inden az yer tutarlar.
5. Neden saptanamayanlar: Ayrıntılı tetkiklere rağmen etiyolojisi bulunamayan serebral infarktlarla, yeterli tetkik edilemeyen vakalar yer alır. Ayrıca, yapılan tetkiklerde birden fazla etyolojik neden bulunan vakalar da bu grupta değerlendirilir (34).
2.2. Serebral Metabolizma:
Beynin metabolik ihtiyacı; yeterli glukoz ve oksijen içeren, süreklilik gösteren kan akımı ile sağlanır. Beynin kan akım ihtiyacı kardiyak debinin yaklaşık olarak %15-20’si olan 750-900ml/dk’dır (42). İstirahatte glukoz ve oksijen ihtiyacı tüm beyinde hemen hemen eşit iken hareketle birlikte kortekste artar. Serebral korteksin oksijen ihtiyacı 6 ml/100g/dk’dır. Glukoz ihtiyacı ise 4.5-7 mg/dk’dır.
Serebral kan akımı (SKA) 100 gr beyin dokusu için normalde ortalama 50 ml/dak’dır. SKA, gri cevherde ortalama 70-80 ml/100 gr/dak iken beyaz cevherde 30 ml/100 gr/dak’dır. Beyinde kan akımının bir bölgede yetersiz kalması durumunda, yetersizliğin derecesi ve süresine bağlı olarak dokuda reversibl veya irreversibl iskemik değişiklikler oluşur. İskemik dokuda serebral kan akımının 10-15 ml/100 gr/dak’nın altına düşmesi durumunda ise dokuda nekroz oluşur ve fonksiyon kaybı irreversibl hale gelir (43).
2.2.1.İskemide vasküler otoreülasyon:
Her 100 gram beyin dokusuna dakikada 50 ml kan kan gelir. Ayrıca 100 gram beyin dokusu dakikada 3.3 ml oksijen ve 5.5 mg glukoz tüketir. Gelen kan akımı, belirli sınırlar içindeki kan basıncı değişikliklerinde sabit tutulur. Bu mekanizmaya serebral otoregülasyon denir. Serebral otoregulasyon ortalama arteriyel basınç 70-160 mmHg arasında olduğunda işlevseldir (13). Perfüzyon basıncı degişse bile
otoregülasyon sayesinde serebral kan akımı sabit kalır (perfüzyon basıncı arteriyel kan basıncı ile intrakranial basınç arasındaki farktır). Arterioller artan basınç ile konstrikte olur; basınç düştüğünde ise arteriyel dilatasyon izlenir. Serebral infarkt gelişmekte olan dokudaki arteriyoller, başlangıçta serebral kan akımı (SKA) azalmasına vazodilatasyon ile yanıt verirler. Ancak düşmeye devam eden SKA sonucunda vazoparalizi gelişir ve arterioller haftalar boyunca dilate kalırlar. Bu hastalara anjiografi yapıldığında (eğer oklüzyon açılmıs ise) dilate arteriyoller, kontrastın çabuk yıkanması (erken venöz dönüş) ve kapiller boyanma (lüks perfüzyon) izlenir (44).
Serebral perfüzyon basıncındaki akut bir düşmede beyin dokusu kendisini otoregülasyon ile korumaya çalışır. Başlangıçta bölgesel serebral kan hacmi artırılarak SKA sabit tutulur. Serebral kan hacmi (SKH) vazodilatasyon ile artar. Eğer perfüzyon basıncı düşmeye devam ederse SKH artmasına rağmen bir süre sonra SKA düşer. Maksimal vazodilatasyon varlığında SKA düşmeye devam ederse dokunun metabolik gereksinimlerini karşılamak üzere kandan oksijen ekstraksiyon fraksiyonu (OEF) artar. Perfüzyon basıncı düşüklüğünün devamı halinde metabolik ihtiyaçları karşılanmayan doku ölür. Bu aşamadan sonra OEF’de düşer (44, 45).
2.3.Serebral İskeminin Patofizyolojisi:
Serebral iskemi, hücre ölümü ve doku infarktına yol açan bir dizi hücresel ve moleküler olaylar zincirini tetikler. Beyin kan akımındaki azalmanın en fazla olduğu çekirdek (core) bölgesinde hücreler dakikalar içinde irreversibl olarak zedelenirler. Ancak iskemik bölgenin periferinde kollaterallerce sağlanan kan akımının devam etmesi, nöronların kısa bir süre için morfolojik ve biyokimyasal bütünlüğünü korur. Orta veya hafif derecede iskemik kalmış beyin dokusundaki nöronlar akut dönemde elektriksel olarak sessiz olmakla birlikte yapısal bütünlüklerini sürdürürler. Bu bölgeye penumbra denir. Penumbra, iskeminin şiddetine ve süresine bağlı olarak infarkta doğru ilerlediği dinamik bir süreçtir (46,47). İskemik beyin hasarı rezidüel kan akımının miktarına bağlı olarak dakikalardan saatlere kadar uzanan bir sürede gerçekleşir. SKA’nın 2-3 saat süreyle normalin % 18-20’nin altına düşmesi infarkt oluşumuna neden olmaktadır (48). Penumbra, tıkanmanın erken döneminde trombolitik tedavi ile veya nöroprotektif ajanların kullanılmasıyla potansiyel olarak
kurtarılabilir. Deneysel ve klinik çalışmalarda, tedaviye başlama süresinin 2-3 saat ile sınırlı olduğu saptanmıştır (49,50).
Serebral iskemi fizyopatolojisinde yer alan serbest radikal oluşumu, lipid peroksidasyonu, eksitotoksisite ve aşırı kalsiyum yüklenmesi gibi mekanizmaların aydınlatılması inme tedavisinin hedefleri arasındadır (51, 52). Bu mekanizmalar birbirleriyle karmaşık bir ilişki içindedir ve programlanmış hücre ölümü, nekroz gibi hücre ölüm mekanizmalarını tetiklerler. İskemide nekrotik hücre ölümüne ek olarak apopitotik mekanizmaların da yer aldığı bilinmektedir (53,54). Beyin yüksek oksidatif mekanizma ve yoğun glutamaterjik sinaptik aktivite nedeniyle diğer dokulara göre özellikle eksitotoksisiteye ve serbest radikal hasarına duyarlıdır (51, 52, 55, 56). Kan akımının tekrar sağlanmasından sonra da bu mekanizmalarla hücre hasarı (reperfüzyon hasarı) oluşabilmektedir. Özellikle akut iskemik inmede trombolitik tedavinin sağladığı başarıdan sonra reperfüzyon hasarının önlenmesi ile ilgili ilaç araştırmaları önem kazanmıştır (57).
Glutamat eksitotoksisitesi: Glutamat beyindeki en önemli eksitatör nörotransmitterdir. İskemiye maruz kalan nöronlarda dakikalar içinde ekstrasellüler glutamat konsantrasyonu artar (58). Ekstrasellüler glutamat artışı N-metil-D-aspartat (NMDA) ve non-NMDA reseptörlerinin aktivasyonuna yol açar. Eksitotoksisiteden esas sorumlu olan NMDA reseptör aktivasyonudur. NMDA reseptör kanalı normalde magnezyum ile bloke durumdadır ve iskemik dokuda nöronal membran depolarizasyonu oluşunca voltaja bağımlı bu kanal açılarak nöron içine Na+, Cl ve H2O’nun girmesine neden olur ve hücrede şişme meydana gelir (59). NMDA reseptörlerinin aşırı miktarda glutamata maruz kalması sonucunda ise NMDA reseptörü iyon kanalından nöron içine aşırı Ca++ girerek, Ca++’a bağımlı enzimlerin aktivasyonu ve serbest radikal oluşumu ile gecikmiş hücre ölümüne neden olur (51, 55, 60, 61).
Eksitotoksinlere maruz kalındığında mitokondri aşırı miktarda Ca++ ile yüklenir (62,63). Mitokondrilerin bu Ca++ alımının; enerji yoksunluğu, sitokrom C salınımı ve artmış peroksit oluşumuna neden olarak eksitotoksik nöron ölümünü tetikleyebileceği gösterilmiştir (62).
Ca++ sitotoksisitesi: İskemi sonrasında nöronlarda hücre içi serbest Ca++ düzeyinde hızlı bir artış olurken hücre dışı Ca++ düzeyinde hızlı bir azalma olur
(64). Hücre içine Ca++ girişinin NMDA reseptörünün iyon kanalı ve voltaj-kapılı Ca++ kanalları yoluyla olduğu düşünülmektedir (52, 56). Ca++’un hücre içinde artışını sağlayan asıl faktör ise hücre içi depolarıdır (65). İskemide intrasellüler kompartmanlardan endoplazmik retikulum ve mitokondri kaynaklı Ca++ salınımı artar (66). Hücreler fizyolojik koşullarda hücre içi kalsiyum miktarlarındaki büyük artışları fazla Ca++’u atarak tolere ederler (67). Fakat enerjinin az olduğu durumlarda, pompa ve sekestrasyon mekanizmaları çalışmaz ve hücre içinden atılamayarak biriken Ca++ düzeyindeki ani artışlar lipazları, proteazları, endonükleazları aktif hale getirir ve serbest radikal ve NO’un oluşumunu arttırarak nöronal ölümü tetikleyebilir (68). Serbest radikal oluşumu, kalsiyum atılımını engelleyerek kısır bir döngü oluşturur. Aynı zamanda mitokondride kalsiyum yükünün artmasının, hasarlanmış mitokondriyal membranı daha fazla bozacağı ve enerji eksikliğini arttırıp, serbest radikal oluşumunu arttıracağı öne sürülmektedir (69).
Serbest radikaller: En dış yörüngesinde tek sayılı elektron içeren atom veya moleküllere serbest radikal denir. Bir çok hücresel enzim ve elektron taşıma sistemi ara ürün olarak sınırlı miktarda serbest radikalleri oluşturur. Serbest radikaller hücre sinyal iletiminde, biyolojik olaylarda rol oynarlar. Oluşan serbest radikaller, normal fizyolojik koşullarda biyolojik koruma mekanizmaları ile ortamdan uzaklaştırılırlar, süperoksit dismutaz, glutatyon peroksidaz ve katalaz gibi enzimlerle zararsız hale getirilirler (70). Serbest radikallerin hücre hasarı oluşturabilmesi için aşırı miktarda oluşması ve/veya detoksifikasyon mekanizmalarının yetersiz olması gerekir. Serbest oksijen radikallerinden olan hidroksil radikali ve süperoksit iyonu aşırı reaktiftir ve nükleik asitlere, lipidlere, karbonhidratlara ve proteinlere bağlanarak onları zedelerler. Serbest oksijen radikalleri kan beyin bariyerini yıkarak beyin ödemine, iskemik bölgeye inflamatuar hücrelerin girmesine ve kan akımının bozulmasına neden olurlar (57).
Nitrik Oksit (NO): NO dokularda yaygın olarak bulunan inorganik gaz yapısında bir mediyatördür. L-arjininden nitrik oksit sentaz aracılığıyla sentezlenir. Sentezlendikten sonra depolanmayıp difüzyon yoluyla dağılır ve çevre hücrelerde etki gösterir (71). Fazla nöronal NO üretimi nörotoksik iken, endotelyal NO, bölgesel kan akımını arttırarak ve diğer hemodinamik faktörler üzerine etki ederek beyin
dokusu üzerinde koruyucu rol oynamaktadır. Reperfüzyon sırasında endotelyal NO’in ortaya çıkması ve peroksinitritin oluşumu kan beyin bariyeri hasarına yol açabilir (72).
Kaspazlar: Apopitotik hücre ölümünde önemli rol oynayan proteolitik enzimlerdir. Mitokondriyal yolun aktivasyonu, kaspazların (kaspaz 3,7) aktif formlarına dönüşmesine neden olur ve aktifleşen kaspazlar çeşitli nükleer, sitoplazmik, membranöz proteinlerin parçalanmasına neden olur (73).
Proteazlar (katepsin, kalpain): Katepsin ve kalpain’in sınırlı aktivasyonu apopitozu tetiklerken şiddetli aktivasyonu nekroz gelişimine neden olur (73).
Matriks metalloproteinazlar (MMP): İnme geçiren hastaların kanlarında ve beyinlerinde MMP düzeyleri artar. Damar bazal laminasındaki bağ dokusunu yıkarak kan beyin bariyeri hasarını arttırırlar (73).
İnflamasyon: İnflamasyon otopsi materyallerinde akut inmeden 12-72 saat sonra gösterilmiştir. İnme riski, C-reaktif protein ve çözünebilir hücre içi adezyon molekülü düzeyleri ile ilişkili bulunmuştur. Lökosit infiltrasyonunun geç iskemik hasarın ilerlemesinde rolü olduğu ve nörolojik gelişmeyi olumsuz yönde
etkilediği bildirilmiştir (73). İnflamasyon inme kliniğini ve infarkt doku hacmini olumsuz yönde etkiler (66).
2.3.1.İskemik hücre ölüm mekanizmaları:
Fokal iskemi oluştuğunda bazı hücreler eksitoksik şişme, osmotik parçalanma ve nekroz ile hızla ölürken bazıları apopitotik mekanizmalarla daha yavaş ölmekte, diğerleri ise apopitoz ve nekroz karışımı özellikler göstermektedir (74,75). Nekrozda hücre ölümüne fokal iskeminin başlangıç aşamasında azalan enerji kaynağının yol açtığı membran hasarı ve bunu takip eden iyon değişimleri ile hücrede şişme ve nükleer fragmantasyon neden olur. Apopitoz ise yavaş gelişen, genetik kontrol altında oluşan programlanmış hücre ölümüdür ve hücre kendi ölümünde aktif rol oynayan proteinleri sentez etmektedir. Apopitozun spesifik moleküler belirleyicisi olan kaspaz adı verilen proteolitik enzimler apopitotik hücre ölümünün oluşmasında önemli rol oynarlar (66). İnmede gelişen fizyopatolojik değişiklikleri şöyle sıralayabiliriz:
ATP sentezi ile ilgili iyon pompaları azalır. Hücrede mebran depolarizasyonu oluşur.
Hücre içine Na+ ve Cl- girişinde K+ çıkışında artma olur. ATP/ADP oranı düşer.
Voltaja bağlı Ca++ kanalları açılır.
Eksitatör transmiterlerin salgılanması hızlanır. Anaerobik solunum ve hücre içi laktik asidoz gelişir. NMDA reseptörlerine bağlı Ca++ kanalları açılır. AMPA reseptörleri stimüle olur.
Endotel mediatörlerinin salgılanması artar. Litik enzimlerin aktivitesi artar (76,77). 2.4.Klinik:
Bugün, inmeli hastaya yaklaşım birçok adımdan oluşur. Bunun ilk ve en önemli adımı beynin lezyonuna bağlı olarak gelişen semptom ve bulguların iyi bir şekilde saptanması ve bunların hangi nedene bağlı olduğunun belirlenmesidir (59). Embolik inmeler karakteristik olarak çok ani başlar ve etkileri hızla geçer ya da devam eder. Trombotik inmeler benzer şekilde ani başlangıçlıdır, ama sıklıkla bir miktar daha yavaş (dakikalar, saatler, hatta günler içinde ) gelişir (78). Akut inmeli bir hastanın bilinci, ilk 24 saatte bozulmuşsa, inmeye bağlı konvülziyon, beyin sapına kanama, kalp bloğu veya aritmi, retiküler sistemi tutan bir patoloji düşünülmelidir. Bugün için akut inmeyle başvuran hastaya erken dönemde klinik tanıya en çok yardımcı olan inceleme, BBT yöntemidir. İskemik inmenin lehine olan bulgular özellikle geçici iskemik atak olması, hiperlipidemi, periferik arteriyel hastalık, ve atriyal fibrilasyon bulunmasıdır. Akut iskemik inmede, olayın hangi arteriyel alanda geliştiğinin saptanması önemlidir (59). Bir serebral arterin beslediği alanda, bu arterin tıkanmasıyla oluşan infarkta bağlı fokal nörolojik belirtilerin olduğu tablolara nörovasküler sendromlar denir. Adlandırma ilgili arterin veya beslediği beyin bölgesinin adıyla yapılır (79).
2.4.1.Karotis sistemi (ön sistem)
A)İnternal karotid arter tıkanması (İCA): İnternal karotid arter terminal bir dal olmadığından, tıkanmasında Willis poligonu ve diğer kollateraller iyi çalışıyorsa semptom görülmeyebilir. Ekstrakranial İCA’yı en sık etkileyen neden aterosklerozdur. Ateroskleroz beyaz ırkta İCA’nın en sık ilk 2 cm’lik bölümünde görülür. En sık görülen, bifurkasyonun gerisinde birinci segment tıkanmaları olup çoğu kez asemptomatiktir (80,81).
İCA tıkanmaları sonucunda iki mekanizma ile serebral fonksiyon bozukluğu ortaya çıkabilir. Birincisi, tıkanan yerden kaynaklanan tromboemboli, orta veya anterior serebral arterlerde tıkanmaya yol açabilir. İkincisi, İCA’da oluşan tıkanma sebebiyle distal perfüzyon yetersizliği sonucu retina veya serebral hemisferde iskemi meydana gelebilir (80,81).
İCA tıkanmalarının karakteristik bulguları; kontrlateral hemiparezi ve ipsilateral görme kaybıdır. Ancak, nörolojik tabloya hemihipoestezi, homonim hemianopsi, afazi ve agnoziler eşlik edebilir. Bunun dışında amorozis fugaks, santral retinal arter tıkanması, iskemik optik nöropati de görülebilir. Karotis sistemi darlık ve tıkanmalarında en sık görülen tablo GİA’lardır. Bunlar, kısa süreli 5-15 dak süren hemiparezi ve karşı tarafta geçici görme kaybı’dır (80).
İCA stenozu olan hastalarda boyunda karotis nabzı zayıf palpe edilir, dinlemekle üfürüm duyulabilir (81).
B)Anterior serebral arter tıkanması (ACA): ACA’nın intrensek hastalığı nadirdir. ACA infarktlarının bir bölümü İCA’nın oklüzyonu sonucudur. Bir kısmı da anterior kominikan arter anevrizmasının kanaması sonucu oluşan vazospazma bağlıdır (81). ACA’nın proksimal tıkanmalarında, karşı taraf ACA’dan anterior kominikan arter aracılığıyla kan aldığı için iyi tolere edilir. Distal tıkanmalarında ise parasantral lob tutulmasına bağlı olarak kontralateral, bacak distalinde hakim motor güç kaybı görülür (80).
ACA tıkanmalarında klinik olarak üriner inkontinans, sosyal kişilik değişiklikleri, motivasyon kaybı, abuli veya akinetik mutizm ortaya çıkar. Sol frontal lobta suplementer motor alan etkilenirse konuşma akıcılığının azaldığı, tekrarlamanın korunduğu transkortikal motor afazi ortaya çıkar. Sağ frontal lob etkilenmelerinde, motor ihmal fenomenleri, apraksi ortaya çıkar. Mezial motor lob veya korpus
kallozum hasarlarında “yabancı el sendromu” denilen, elin istemsiz veya yabancı hareketler tarzında bir bozukluğu ortaya çıkar (59).
C)Orta serbral arter tıkanmaları (MCA): MCA, inme sendromlarının en sık tutulan arteridir. MCA internal karotid arterin en geniş dalı olup beyin yüzeyinin konveksitesini sular. Beyin içinde de bazal ganglionları, kapsula eksternayı, klaustrumu, putamen ve globus pallidusu, kaudat nükleusun posterior kısmını, internal kapsülün anterior ve posterior bacaklarının alt kısmını besler (80).
Ana dalın oklüzyonu: Kontrlateral hemiplejiye, baş ve gözlerin lezyon yönüne deviasyonuna, hemianestezi ve hemianopsiye yol açar. Dominant hemisferde global afazi, nondominant hemisferde ise ihmal ve dikkat azalması olur. İnfarkt büyük olursa optik radyasyon tutulumuna bağlı hemianopsi görülür. MCA’nın kök tıkanması sıklıkla herniasyona yol açması nedeniyle bazı yazarlar tarafından malign infarkt olarak tanımlanır (80).
Üst divizyon oklüzyonunda: Kontrlateral hemiparezi, hemihipoestezi, dominant hemisfer tutulduğunda Broca afazisi, nondominant hemisfer tutulduğunda ihmal sendromları görülür. Angüler girus tutulumunda Gerstmann sendromu (agrafi, akalkuli, finger agnozi, sağ-sol dezoryantasyonu) ve aleksi görülür (80).
Alt divizyon oklüzyonunda: Hemiparezi ya çok hafiftir ya da görülmez. İnfarkt dominant hemisferi tuttuğunda Wernicke afazisi görülür. Nondominant hemisfer tutulduğunda konstrüksiyonel apraksi, abuli ve deliryum gibi davranış bozuklukları olur (80).
Küçük penetran arterler tıkandığında: Pür hemiparezi, vizüel, lisan ve/veya davranış bozuklukları olabilir. Geçici veya kalıcı olabilen hemikore, atetoz ve distonileri içeren hareket bozuklukları, kontrlateral vücut yarısında aşırı terleme şeklinde otonomik bozukluklar da görülebilir (80).
2.4.2.Vertebrobaziler sistem (arka sistem)
A)Posterior serebral arter tıkanması (PCA): PCA’lar mezensefalonu, talamusu, oksipital lobu, inferior ve mezial temporal lobu, parietal lobun posterior inferior kısmını besler (81). Orta beyin ve talamusu bilateral olarak etkileyen infarktlarda stupor ve komaya kadar giden şuur bozukluğu, hafıza bozuklukları, hemiplejiler, hemihipoestezi, 3. kranial sinir paralizileri ve internükleer oftalmopleji görülebilir.
PCA’nın unilateral lezyonunda kontrlateral hemipleji, hemisensorial defisit, hemianopsi ve davranış değişiklikleri, Horner sendromu ve kontrlateral hiperhidroz görülür. PCA proksimal lezyonlarında hipoestezi veya anestezi görülür (80).
Talamogenikulat dalın oklüzyonu sonucu Dejerine-Roussy tarafından tanımlanan talamik ağrı sendromu görülür; bu arterin oklüzyonu ile çabuk düzelen koreik hareketler, ataksi, hemiparezi, persistan hipoestezi ve dizestezi ile birlikte ciddi paroksismal ağrılar oluşur. Talamik hiperpati adı verilen bu tabloda taktil stimuluslar ile şiddetli, ağrılı cevaplar ortaya çıkar (80).
Dominant hemisfer infarktı olan olgularda, anomik afazi, agrafisiz aleksi ve vizüel agnozi görülür. Bilateral olarak lingual girus, hipokampal girus ve medial hipokampal strüktürleri tutan lezyonlarda aşırı motor aktivite, ajitasyonlar, hiperfaji, hiperseksüalite, deliryum, ağlama, vizüel, işitsel ve taktil stimuluslara aşırı reaksiyon şeklinde klinik semptomlar (Klüver-Bucy Sendromu) oluşur (80).
Bilateral PCA infarktlarında direkt ve indirekt ışık refleksinin korunduğu kortikal körlük gelişir. Tek taraflı PCA’nın oksipital lobu besleyen dallarının tıkanmasında hemianopsi olur, fakat santral görme liflerinin projekte olduğu polus occipitalis MCA dalları tarafından da beslendiği için santral görme sağlam kalır (80). B) Koroidal arter tıkanması: Anterior koroidal arter (AchA), İCA’nın küçük bir dalıdır. AchA globus pallidus, uncus, capsula interna arka bacağının alt bölümü, anterior hipokampus, mezensefalon rostral bölümü ile serebral pedünkülün kanlanmasını sağlar. Ayrıca optik traktusu izleyerek korpus geniculatum laterale ve radiatio optici arka bölümünü sular (80,81).
AchA infarktlarında hemipleji, hemihipoestezi, hemianopsi, pür motor hemiparezi, pür sensorial inme, ataksik hemiparezi, hemiataksi ve ipsilateral hemisensorial defisit, sol taraf lezyonlarında disfazi, apraksi, amnezi, sağ taraf lezyonlarında hemiihmal, bilateral lezyonda akut pseudobulber mutizm olur (80).
Posterior koroidal arter infarktlarında vizüel alan defekti, üst ve alt kuadranopsi, hafif hemiparezi, hemihipoestezi, konuşma bozuklukları, blefarospazm olur (80).
C) Vertebral arter tıkanması: Ekstrakranial vertebral arter aterom plaklarının sık görüldüğü önemli bir yerleşim yeridir. Vertebral arter orijininde ateroskleroz,
erkeklerde kadınlara oranla daha sıktır ve sıklıkla karotid arter oklusif hastalığı ile birliktedir (80).
Vertebral arterin internal bölümünün oklüzif hastalığı ekstrakranial bölüme göre daha sık olup posterior sirkülasyon yapılarının infarktı ile birliktedir (80).
D)Lateral Medüller İnfarkt (Wallenberg Sendromu): Posterior inferior serebellar arter (PİCA)’in tıkanmasına bağlı oluşur. Wallenberg sendromu bulbusun lateral bölümünde ve inferior oliva arkasında yerleşen bir infarkta bağlı olarak ortaya çıkan, oldukça tipik belirtileri olan ve sık görülen bir klinik tablodur. Wallenberg sendromunda; ipsilateral yüz ve gözde ağrı, Horner sendromu, 9.-10. kranial sinir paralizisi (faringeal ve laringeal paraliziden dolayı ses kısıklığı ve disfaji), ataksi, spinotalamik yolların lezyonuna bağlı ipsilateral yüzde, kontrlateral gövde ve ekstremitelerde ağrı ve ısı duyusunda azalma, vertigo, nistagmus, taşikardi ve kan basıncı değişiklikleri, özellikle uykuda olan solunum güçlükleri, öksürük, hıçkırık, bulantı-kusma, çift görme, oksipital bölgede lokalize baş ağrısı olur (80,81).
E) Anterior inferior serebellar arter (AİCA) tıkanmaları: Klinik olarak AİCA infarktları kaudal pons, serebellum, orta serebellar pedünkül ve flokulusu etkiler, sıklıkla inferolateral pontin alanı tutar. Klasik olarak AİCA tutulumunda; vertigo, kusma, tinnitus, dizartri, ipsilateral fasial paralizi, işitme kaybı, trigeminal duyusal kayıp, Horner sendromu ile birlikte kontrlateral vücutta ağrı ve ısı duyusu kaybı, ipsilateral konjuge bakış paralizisi, komaya kadar giden şuur bozuklukları, izole vertigo, izole serebellar sendrom bulguları görülebilir (80).
F)Süperior serebellar arter (SCA) tıkanması: Serebellar infarktların en sık sebebidir. Tüm serebellar infarktların % 50-65’i bu alanda görülür. SCA serebellumun horizontal sulkusunun altında kalan lobulus sentralis, kulmen, klivus, folium, vermis ve serebellar hemisferlerin lobuslarını besler. SCA oklüzyonunda ipsilateral ekstremite ve yürüyüş ataksisi, Horner sendromu, statik tremor, kontrlateral 4. kranial sinir felci ve spinotalamik duyusal kayıp görülebilir (80).
G)Baziler arter tıkanması: Baziler arterin perforan dalları başlıca bazis pontisi besler. Baziler arter oklüzyonu ponsun bazisinde iki yanlı iskemiye neden olur. İskemi tek veya iki yanlı tegmentumu da etkileyebilir. Baş ağrısı, sersemlik hissi, konfüzyon ve koma gelişir. Pupil anormallikleri, oküler hareket bozuklukları, fasiyal paralizi, hemipleji veya kuadripleji, bilateral ekstansör plantar refleksler görülür.
Klinik olarak internükleer oftalmopleji, konjuge horizontal bakış paralizisi, Fisher’in bir buçuk sendromu, oküler bobbing, pitoz, miyotik pupillalar, nistagmus, skew deviasyon sıklıkla görülür. Palatal myoklonus, koma, Locked-in sendromu, deserebrasyon rijiditesi, solunum anormallikleri görülebilir (80,81).
2.5.Tanı:
İskemik inme acil bir medikal durumdur. Hastanın acile başvurduğunda yapılan tanısal değerlendirmeden elde edilecek bulgular hem hastanın prognozunu belirlemede hem de doğru tedavilerin başlatılmasında önemlidir (Tablo 5). Anamnez ve nörolojik muayene aşamasından sonra en önemli basamak klinik ön tanıyı doğrulamak ve hemorajik inme ile iskemik inme arasında ayırıcı tanıyı yapmaktır. BBT, infarkt ile kanamayı birbirinden ayırmada en güvenilir tetkiktir (82).
Tablo 5. Akut inmeli hastada tanı incelemeleri.
-
Kranial BT - EKG- Akciğer grafisi - Tam kan sayımı - PT/aPTT/INR - Kan şekeri
- BUN/kreatinin/elektrolitler - Sedimentasyon/CRP - Arteryel kan gazları
- Gerekirse CK, CK-MB,Troponin T - Gerekirse BOS incelemesi
BBT aynı zamanda inmeye bağlı gelişebilecek nörolojik komplikasyonlara ait radyolojik değişikliklerin tanınmasını ve inme ile karışabilecek diğer hastalık süreçlerinin dışlanmasını da sağlayacaktır. BBT’de parenkimal değişikliklerin ne kadar erken saptanabileceği; iskeminin süresi, şiddeti, etkilenen alanın genişliği ve lokalizasyonuna göre değişiklik gösterir (82).
Hasta acil olarak değerlendirildikten ve hastaneye yatırıldıktan sonra yapılacak incelemeler inmenin nedenini ortaya koymaya, vasküler risk faktörlerini saptamaya ve böylece de inmeden ikincil koruyucu tedavilerin belirlenmesine yöneliktir. Bu amaçla bazı olgularda beyini daha ayrıntılı olarak görüntüleyebilme özelliği olan kranial MRG ve genel olarak tüm hastalarda da inme etyolojisi araştırmak amacıyla beyin damar ve kardiyak görüntüleme incelemeleri yapılır. Yine seçilmiş olgularda koagülopati taraması bu dönemde yapılacak incelemeler arasındadır (82).
Kranial magnetik rezonans görüntüleme (MRG) incelemesi iskemik lezyonları görüntülemede kranial BT’den daha duyarlı bir yöntemdir. Özellikle arka çukur yapıları, beyin sapındaki iskemik lezyonlar, laküner infarktlar bu inceleme ile daha kolaylıkla görüntülenebilir (83). Difüzyon MRG akut inmenin ilk birkaç saatinde bile, var olan değişiklikleri gösterebilmektedir. Difüzyon ve perfüzyon MRG tekniklerinin kullanılmasi ile, serebral infarkt tanısının daha erken ve kesin konmasının yanısıra, sadece infarktın gelişeceği alan değil tüm iskemik risk altındaki dokuyu belirlemek mümkün olmuştur (83).
MRG spektroskopi (MRGS), beyindeki normal ve anormal metabolitlerin in vivo ölçümünü sağlaması nedeniyle, akut inmenin fizyopatolojisinin anlaşılmasında kullanılabilecek potansiyel bir inceleme yöntemidir. Ancak klinikte inme incelemesinde MRGS kullanımı, göreceli olarak sinyalin düşük olması, inceleme zamanının uzunluğu ve düşük rezolüsyonu nedeniyle son derece sınırlıdır. MRGS’de nöron harabiyetinin bir göstergesi olan N-asetil aspartat (NAA) düşüklüğü ilk birkaç saat içinde tespit edilebilir. Diğer bir majör bulgu ise akut dönemde laktat yüksekliğidir. Kolin ve total kreatin düzeylerinde düşme de bildirilmiştir. Serebral kan akımı, serebral kan volumü, glikoz ve O2’nin serebral metabolik hızlarının değerlendirilmesine imkan veren single photon emission computed tomography (SPECT) ve positron emission tomography (PET) gibi noninvaziv yeni teknik gelişmeler giderek yaygınlaşmaktadır (83).
Boyun renkli doppler ultrasonografi incelemesi ekstrakranial karotis ve vertebral arterleri incelemek amacıyla yaygın kullanılan non invaziv bir incelemedir. Karotis kommunis bifürkasyonu, karotis interna orijini ve vertebral arter orijini düzeyindeki aterosklerotik darlıkları veya tıkanmaları görüntüleyebilir. İntrakranial arterler transkranial doppler, transkranial renkli doppler, magnetik rezonans
anjiografi, bilgisayarlı tomografi anjiografi ve dijital substraksiyon anjiografi incelemeleri ile araştırılır. Dijital substraksiyon anjiografi tanı ve girişimsel nöroradyolojik tedaviler amacıyla yapılan invaziv bir incelemedir. Bu inceleme halen ekstra ve intrakranial damarların en ayrıntılı incelemesine olanak sağlayan yöntemdir ancak invaziv olduğundan dolayı komplikasyon riski olması endikasyonlarını sınırlar (82).
Kalp hastalıkları ve kalp kaynaklı emboli iskemik inmenin önemli bir nedeni olduğundan birçok hastada kardiyak görüntüleme incelemeleri yapılır. Transtorasik veya transösefagial ekokardiyografi bu amaçla en sık başvurulan incelemelerdir (82).
2.6.İnme komplikasyonları:
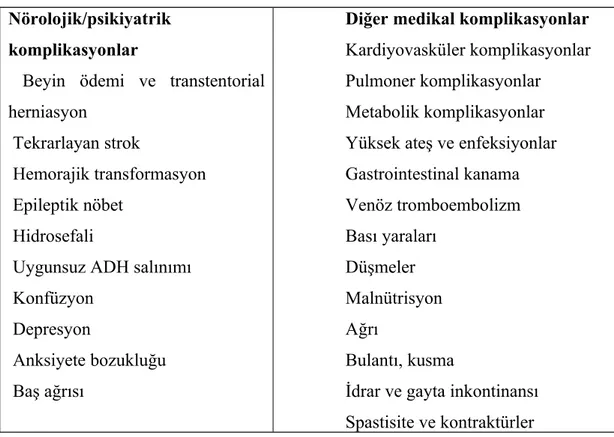
İnme geçiren hastalarda, akut ve kronik dönemde birçok komplikasyon gelişebilir. İnme sonrası komplikasyon gelişimi, farklı çalışmalarda % 40-96 arasında değişen oranlarda bildirilmiştir. Gelişen komplikasyonlar, hem inme mortalitesini arttırır, hem de rehabilitasyonun gecikmesine ve hastaların daha çok özürlü ve bağımlı kalmalarına neden olurlar. İnme sonrası ölümler, beyin hasarı ve inme komplikasyonları sonucu meydana gelir. Bu nedenle inme sonrası gelişebilecek komplikasyonların bilinmesi ve mümkünse önlenmesi, gelişen komplikasyonların ise erken dönemde tanınması ve tedavi edilmesi çok önemlidir (Tablo 6) (82,84).
Tablo 6. İnme sonrası gelişebilecek komplikasyonlar Nörolojik/psikiyatrik
komplikasyonlar
Beyin ödemi ve transtentorial herniasyon
Tekrarlayan strok
Hemorajik transformasyon Epileptik nöbet
Hidrosefali
Uygunsuz ADH salınımı Konfüzyon
Depresyon
Anksiyete bozukluğu Baş ağrısı
Diğer medikal komplikasyonlar Kardiyovasküler komplikasyonlar Pulmoner komplikasyonlar Metabolik komplikasyonlar Yüksek ateş ve enfeksiyonlar Gastrointestinal kanama Venöz tromboembolizm Bası yaraları Düşmeler Malnütrisyon Ağrı Bulantı, kusma
İdrar ve gayta inkontinansı Spastisite ve kontraktürler
2.7.Prognoz:
İnmeli hastaların % 30’u bir yıl içinde ölmektedir. İlk 1 ay içinde ölüm oranı %10-20’dir. İnme geçiren ve hayatta kalan hastaların % 10’u hiçbir sekel olmadan işlerine dönebilirler. % 30’unda hafif disabilite, % 50’sinde ciddi disabilite olur ve % 10’u devamlı kurumsal bakım gerektirir. On yıllık sağ kalma oranı % 35’dir. Hastanın yaşı, lezyonun anatomik büyüklüğü, nörolojik defisitin derecesi, beraberinde medikal hastalığın olması ve altta yatan nedenler sonucu etkiler. Koma skoru ne kadar düşükse prognoz o denli kötüdür. Rekürrens serebral infarkt oranları yılda % 5-15 arasında değişir. Beş yıllık mortalite, erkekler için % 44, kadınlar için % 36’dır (85, 86).
Başlangıçtaki koma, ciddi parezi, bilişsel bozukluklar, konuşma bozukluğu, görme ve yutma bozukluğu, kronik inkontinans, tek taraflı ihmal, ciddi kardiyovasküler hastalık, geniş serebral lezyon, demans, ateş ve birden fazla nörolojik defisit prognozu kötü yönde etkilerler (87).
2.8.İskemik İnmede Biyobelirteçlerin Kullanımı
:
Günümüz koşullarında inme tanısı hastanın fizik muayenesini gerçekleştiren doktorun deneyimine ve birkaç görüntüleme yöntemine dayandırılmaktadır. İskemik inme tedavi kararları doğrultusunda kendi içinde faklı gruplara ayrılabilse de kesin tanı kriterleri netleşmiş değildir. Yaş, risk faktörleri ve klinik bulgular ile birlikte infarktüs alt tipinin (örneğin tromboz ve emboli ayırımı) ayrılmasına çalışılmaktadır. Birçok olgu inme uzmanı nörolog tarafından değerlendirilmeden tanı ve tedavi görmektedir. Öncelikle amannez, fizik muayane, beyin görüntüleme, koagülasyon testleri ve glukoz ile elektrolit düzeyleri istenerek nörolojik bulguların hipoglisemi gibi metabolik veya infeksiyon kaynaklı olmadığının gösterilmesi gerekir (88).
Akut inme şüphesi olan hastalara hızlı ve doğru tanı konmasındaki ısrar ılımlı bulgulara sahip olan hastalarda bile bulguların başlamasından sonraki bir kaç saat içinde başlanacak intravenöz tromboliz veya diğer beyin reperfüzyon tedavilerinin çok başarılı sonuçlar vermesinden kaynaklanmaktadır. Akut tedavi uygulanmadığı zaman ilk iki gün içinde ikinci bir inme geçirme olasılığı %8 olarak hesaplanmıştır (89). Durumun aciliyeti dışında akut dönemde hastalarda sıkça izlenen bilişsel bozukluklar, ajitasyon ve yetersiz kooperasyon nörolojik fonksiyonların değerlendirilmesini çıkmaza sokabilmektedir.
Modern nörogörüntülemenin rutin hizmete girmesinden sonra özellikle invaziv olmayan vasküler görüntüleme, anjiyografi, BT ve MRG kullanımının artması ile iskemik inme tanısı konmasında iyileşme sağlanmışsa da istenilen düzeyde değildir.
Farklı görüntüleme teknikleri ile parankimal hasar ve beyin ödeminin erken bulgularının saptanması prognostik değere sahipse de, iskemi mekanizmasını açıklamada yararlı değildir. Hastaneye başvuranlarda yapılan BT tarama sonuçları normal çıkabilmekte, daha duyarlı olduğu bilinen MRG sonuçlarının %100 duyarlı ve özgül olmadığı görülmektedir. Bunun dışında bazı hastalara ajitasyon nedeni ile MRG çekilmesi bile mümkün olmamaktadır. Ayrıca, her iki radyolojik görüntüleme yönteminin sağlık kurumlarında var olması, 24 saat kesintisiz ulaşılabilmesi ve çalışır durumda tutulabilmesi ile ilgili sorunlar göz önünde bulundurulmalıdır. Son olarak her iki yöntem için radyoloji uzmanı gerekli olduğu için tüm koşullar tanı koymadaki gecikmeleri açıklamak için kullanılmaktadır (90).