T.C.
DİCLE ÜNİVERSİTESİ
Fen Bilimleri Enstitüsü
UV/ VIS SPEKTROMETRESİ İLE
DEVEGEÇİDİ BARAJ SUYUNUN
ANALİZİ
Veysi GÜZEL
YÜKSEK LİSANS TEZİ
(FİZİK ANABİLİM DALI)
DİYARBAKIR
TEŞEKKÜR
Bu çalışmanın her safhasında gerekli desteği ve yardımını esirgemeyen değerli Hocam Prof. Dr. Mahmut AYDINOL’ a en derin saygılarımı sunar; teşekkür etmeyi bir borç bilirim.
Teşvik ve katkılarıyla bana destek olan Fizik Bölümündeki hocalarıma, Tıp Fakültesi Biyokimya Biriminin Değerli Hocası Sayın Prof. Dr. Belkıs AYDINOL’ a, arkadaşlarım M. Sait
İÇİNDEKİLER Amaç...i Özet...ii Summary...iii 1. Giriş...1 2. Teori...3
2.1. Işın Madde Etkileşimi...3
2.1.1. Atomik Absorpsiyon...5
2.1.2. Moleküler Absorpsiyon...5
2.1.3 Manyetik Alanla Oluşan Apsorpsiyon...8
2.2. Suyun Özellikleri ve Etkileşimi...8
2.2.1. Suyun Toprak Tabakalarına Etkisi...9
2.2.1.1. Mekanik Olarak Etkisi...9
2.2.1.2. Doğrudan Doğruya Etkisi...10
2.2.1.3. Karşılıklı Kimyasal Etki ...10
2.2.2. Doğal Suyun Sınıflandırılması ve Orijini...11
2.2.3. Yer altı Suyu ve Kaynak Suları...12
2.2.4. Yeryüzü suları...12
2.2.5. Maden Suları...13
2.2.6. Suyun Fiziksel ve Fizikokimyasal Özellikleri...13
2.2.7.Suyun Kimyasal Özellikleri...14
3. Materyal Metot ve Deney ...16
3.1. Lambda 2 UV/VIS spektrometre (Perkin Elmer) Aletinin Başlıca Kısımları ve Özellikleri...16
3.2. Perkin Elmer Spektrometresinin Teknik Özellikleri...17
3.2.1. İşlem Kontrolleri ve Gösterge...18
3.2.2. Lambda 2 UV/VIS spektrometresinin Aktif Hafızasındaki Analiz Fonksiyonları...19
3.2.3. Lambda 2 UV/VIS spektrometresinin Optik Prensibi...19
3.3.1. Nitrat Tayini...20 4.Tartışma ve Sonuç...27 Kaynaklar...28 Tablo Listesi...29 Şekil Listesi...29 Grafik Listesi...29 Resim Listesi...29 Özgeçmiş...30
AMAÇ
Su analiz metotlarında son yıllarda büyük değişiklikler olmuş; uzun zaman alan klasik metotların yerine daha hassas ve seri sonuçlar veren elektronik aletlerin dayanan analiz metotları almıştır. Bu çalışmanın amacı uzun yıllardan beri geliştirilmiş analiz metotlarının yakın çevrede bulunan Devegeçidi baraj suyu üzerinde uygulanması ve elde edilecek ölçüm sonuçlarıyla biyolojik çevreye etkileri hakkında bir sonuca ulaşılmasıdır.
ÖZET
Bu çalışmada ışın madde etkileşimi, Lamda 2 UV/VIS spektrometresi, Lamda 2 UV/VIS spektrometresi ile yapılabilecek bazı analiz çeşitleri ve analizlerden biri kullanılarak yapılan ölçüm ve sonuçları hakkında bilgi verildi. Bu yapılan ölçüm Devegeçidi baraj suyunun birim hacimdeki nitrat miktarı tayinidir. Ayrıca bu ölçüm sonucu DSİ X. Bölge müdürlüğünce en son yapılan Devegeçidi Baraj suyunun ölçüm sonuçlarıyla karşılaştırıldı.
SUMMARY
In this study, information on interaction between ray and substance, about Lambda 2 UV/VIS spectrometer, on an analysis with Lambda 2 UV/VIS spectrometer and on measurement of nitrat in water which was done by using this instrument were given. Measurements of the nitrat's amount in unit volume in sample waters of the Devegeçidi Dam were carried out. The result of these measurement were compared with the last measurements which were done by X. Regional Directorate of State Hydrolic Works (DSİ X. Bölge Müdürlüğü) as well.
1. GİRİŞ
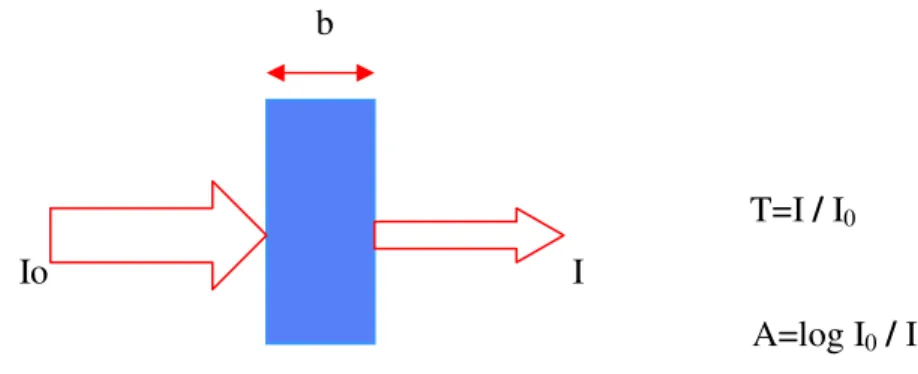
Spektroskopi, çeşitli tipte ışınların madde ile etkileşimini inceleyen bilim dalı için genel bir terimdir. En yaygın şekilde kullanılan spektrometrik yöntemler elektromanyetik ışımaya dayanır; birkaç şekilde bulunan bu enerji tipinin en kolay tanınabilinenleri ışık ve ısı ışımasıdır. İnsan duyuları ile daha zor algılanan enerji tipleri ise gama ışınları, X-ışınları, ultraviyole, mikrodalga ve radyo-frekans ışınlarıdır. Şekil.1-1 de görüldüğü gibi, kantitatif absorpsiyon yöntemleri iki ışın gücü ölçümü gerektirir: ışık demetinin analit içeren ortamdan geçmeden önceki (Io) ve sonraki (I)durumları. Absorpsiyon spektrometrisinde çok kullanılan iki terim,
geçirgenlik(T) ve absorbans(A), Io ve I değerlerinin oranıyla ilgilidir.(6)
b
T=I / I0
Io I
A=log I0 / I
Şekil 1.1. c derişiminde absorpsiyon yapan bir çözelti ile bir ışın demetinde şiddet azalması.
Şekil 1.1. b cm kalınlığında ve absorpsiyon yapan bir türün c derişiminde olduğu bir ortamdan geçirilen bir paralel ışın demetinin geçiş öncesi ve sonrası durumunu vermektedir. Fotonlarla ışın absorplayan atom veya moleküller arasındaki etkileşimin sonucu olarak ışının gücü Io’dan I’ya azalır. Ortam tarafından geçirilen ışının oranına geçirgenlik(T) adı verilir.
T = I/Io (1-1)
Ortamın absorbansı (A)aşağıdaki denklemle verilir:
Işın gücündeki azalma artarken, geçirgenlik değerinin aksine ortamda absorbans artar. Monokromatik ışın için absorbans, ışık yolu b ve absorplayan türün değişimi c ile doğru orantılıdır. Bu bağıntı aşağıda verilmektedir:
A= abc (1-3)
Burada a orantı sabiti olup absorptivite adıyla anılır. a’nın büyüklüğü, b ve c için kullanılan birimlere bağlıdır. Absorplayan türlerin çözeltilerinde b genellikle santimetre, c ise litrede gram olarak verilir. Bu durumda absorptivite, Lg-1cm-1 birimlerinde olacaktır. Eşitlik 1-2’ de derişim litrede mol hücre uzunluğu ise santimetre olarak verildiğinde absorptivite, molar absorptivite adını alır ve özel simgesi ε’dur. Böylece b santimetre, c litrede mol olarak birimleriyle verilirse,
A = εbc (1-4)
bağıntısında ε’nun birimleri Lmol-1cm-1 olur.
Eşitlik 1-3 ve 1-4’deki denklemler, Beer Yasasının bağıntılarıdır ve hem atomik hem de moleküler absorpsiyon ölçümleriyle kantitatif analizin temelini oluşturur. Bu denklemlerdeki (b) numune kabının optik yol kalınlığı olup cm’dir, ε ise moleküler absorpsiyon katsayısıdır. Kullandığımız spektrometre ile A absorpsiyonu doğrudan ölçülebildiğinden,
c = A/ε b (1-5) bağıntısından verilen numunede aradığımız maddeye ait konsantrasyonu hesaplayabiliriz.(6)
2. TEORİ
2.1.Işın Madde Etkileşimi
Işın katı, sıvı veya gaz tabakasından geçtiğinde bazı frekanslar absorpsiyon ile seçici olarak ortamdan alınır; bu süreçte ışın enerjisi numuneyi oluşturan atom, molekül veya iyonlara aktarılır. Absorpsiyon, bu parçacıkları normal oda sıcaklığı hali yani temel halden bir veya daha çok sayıdaki yüksek enerjili uyarılmış hallere çıkarır. Kuantum teorisine göre atom, molekül veya iyonlar yalnız belli değer ve sayıda enerji düzeyinde bulunabilir; ışının absorplanabilmesi için uyarıcı foton enerjisinin, tam olarak absorpsiyon yapan türlerin temel hali ile uyarılmış hallerden biri arsındaki enerji farkına eşit olması gereklidir. Bu enerji farkları ise her tür için özgün olduğundan, absorplanan ışındaki frekansların incelenmesi, numuneyi oluşturan maddenin bileşenlerinin tayini için kullanılabilir. Bu amaçla, deneysel olarak dalga boyu veya frekansa bağlı olarak absorbans değerlerinin bir grafiği hazırlanır. Tipik absorpsiyon spektrumları Şekil 2.1.’de gösterilmektedir. Şekil 2-1’deki dört grafiğin incelenmesi, absorpsiyon spektrumlarının görünüşte büyük farklılıklar gösterebileceğini sergiler; bazıları çok sayıda keskin piklerden, bazıları ise düzgün ve sürekli eğrilerden oluşur. Genel olarak spektrumun nitelikleri, absorpsiyon yapan türlerin karmaşıklığı fiziksel hali ve çevresinden etkilenir. Bununla birlikte, daha temel farklar ise atomların ve moleküllerin absorpsiyon spektrumlarında gözlenir.(7)
2.1.1.Atomik Absorpsiyon
Polikromatik ultraviyole veya görünür bölge ışınının cıva veya sodyum gazı gibi tek atomlu bir ortamdan geçmesi, az sayıda fakat iyi tanımlanmış frekanslar oluşturur. Bu spektrumların oldukça basit niteliği, absorpsiyon yapan parçacıkların muhtemelen az sayıda enerji düzeyine sahip olmasındandır. Uyarılma yalnızca atomda bir veya birden çok elektronun üst enerji düzeylerine yükseltildiği elektronik bir süreçle meydana gelir.
220 260 300 340 Dalga boyu(nm) Grafik 2.1. Tipik ultraviyole absorpsiyon spektrumları(7)
Örneğin sodyum buharı, 3s elektronundan biraz daha üst düzeyde olan iki 3p düzeyine uyarılmasıyla görünür spektrumun sarı bölgesinde olan(589,0 ve 589,6 nm )iki adet birbirine yakın ve keskin absorpsiyon piki gösterir. İzin verilen diğer uyarılma geçişlerine ait diğer birkaç absorpsiyon çizgisi de gözlenir. Örneğin, sodyumda 3s elektronun uyarılmış 5p haline geçişi, 3p’ye uyarılmaya göre daha fazla enerji içerir ve ultraviyole bölgede 285 nm dolaylarında bir sinyal verir(gerçekte 285 nm’deki pik de bir çift sinyaldir; bununla birlikte, iki pik arasındaki enerji farkı o kadar azdır ki çoğu cihazlar bunları ayırt edemez). Ultraviyole ve görünür ışın, yalnızca en dıştaki veya bağ-yapan elektronlarda geçişlere neden olabilecek yeterlikte enerjiye sahiptir. Öte yandan X-ışını frekansları ise, bunlardan birkaç mertebe daha yüksek enerji içerip,
atom çekirdeğine en yakın etkileşim gösterebilirler. En içteki bu elektronların elektronik geçişlerini gösteren absorpsiyon pikleri, bu yüzden X-ışınları bölgesinde yer alır(7).
2.1.2. Moleküler absorpsiyon
Özellikle yoğunlaşmış fazlardaki çok atomlu moleküllerin absorpsiyon spektrumları, atom spektrumlarına göre oldukça karmaşıktır; çünkü bu moleküllerdeki enerji düzeyi sayısı, sadece atomların enerji düzeyleri sayılarına göre genellikle çok daha fazladır. Moleküllerin bantlarına ilişkin enerji (E), üç bileşenden oluşur.
E = E elektronik + E titreşim + E dönme (2-1)
Burada Eelektronik, molekülde bağ-yapan birkaç elektrona ait enerji düzeyinden
kaynaklanan elektronik enerjidir. Sağdaki ikinci terim ise, moleküler türlerde çok sayıda bulunan atomlar arası titreşimlerin toplam enerjisini gösterir. Genel olarak bir moleküldeki kuvantlaşmış titreşim enerji düzeylerinin sayısı, elektronik düzey sayısından çok daha fazladır. Son olarak Edönme ise molekül içindeki çeşitli dönme hareketlerinden oluşan enerjidir; dönme
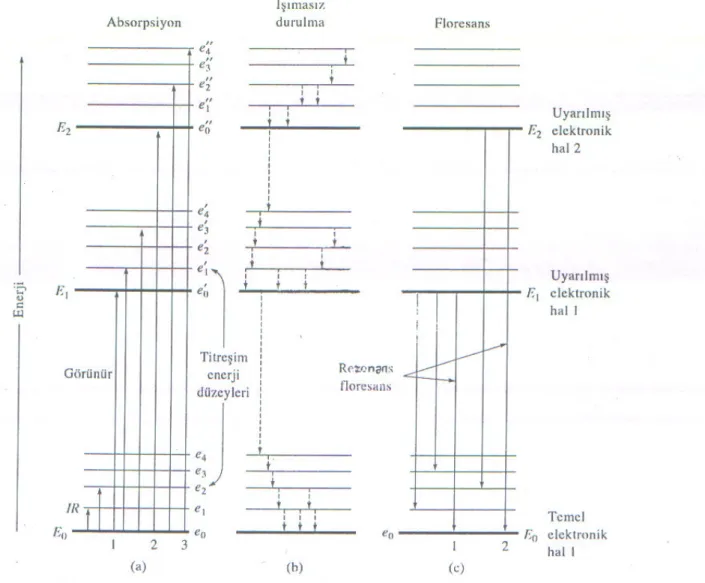
enerji düzeylerinin sayısı da titreşim enerji düzey sayısından çok daha fazladır. Böylece, bir moleküldeki her elektronik enerji hali için doğal olarak mümkün birkaç titreşim hali vardır; ve bu titreşim hallerinin her birisi için de çok sayıda dönme hali bulunmaktadır. Sonuç olarak, bir molekül için olası enerji düzeylerinin sayısı, bir atom için olası enerji düzey sayısına göre çok daha yüksektir. Bir molekülün çok sayıda elektronik ve titreşim hallerinden birkaçı için enerji düzeyleri, Şekil 2.2’de grafik şeklinde gösterilmektedir. Koyu çizgiyle gösterilen E0, molekülün
temel haldeki elektronik enerji düzeyini (en düşük elektronik enerji hali) göstermektedir; E1ve E2
olarak verilen çizgiler ise iki uyarılmış elektronik halin enerjisini simgeler. Her elektronik düzeye ait, çok sayıda titreşim düzeylerinin (e0, e1, ……,en)bazıları şekilde gösterilmektedir.(7)
Grafik 2.2. Bir floresans organik molekül için enerji-düzey diyagramının bir bölümü(7) Şekil 2.2.a’da görüldüğü gibi, temel hal ve uyarılmış elektronik hal arasındaki enerji farkı, bir elektronik hale ait titreşim düzeleri arasındaki farklara göre daha büyüktür(tipik olarak 10-100 kat fark vardır). Şekil 2-2’deki oklar ise, ışının absorplanmasıyla oluşan geçişlerden bazılarını göstermektedir. Görünür ışın, E0’daki bir elektronun E1’le ilgili n titreşim düzeyinden herhangi
birine uyarılmasını sağlar(Şekil 2-2’de n titreşim düzeyinin yalnızca beşi verilmektedir). Olası absorpsiyon frekansları her biri alttaki bağıntıyla verilen n adet denklemle bulunabilir:
νi = (E1 + e’i – E0 )/ h (2-2)
Buna benzer olarak, ikinci elektronik halde m adet titreşim düzeyi varsa (dördü gösterilmektedir), ultraviyole ışının olası absorpsiyon frekansları da aşağıdaki gibi m adet denklemle verilir:
νi = ( E2 + e’’- E0 )/ h (2-3)
i=1,2,3, . . . m.
Son olarak, Şekil 2-2a’da da gösterildiği gibi, enerjisi daha az olan yakın ve orta infrared ışını ise yalnız temel haldeki k adet titreşim düzeyleri arasında geçişler oluşturabilir. Burada, k adet olası absorpsiyon frekansı, aşağıdakine benzer k adet denklemle verilir: i=1,2,3, . . . k. olmak üzere,
νi = (ei + e0 )/h (2-4)
Şekil 2.2.’de gösterilmemekle birlikte, her titreşim düzeyi için birkaç dönme enerji düzeyi vardır. Dönme enerji düzeyleri arasındaki farklar, titreşim düzeyleri arasındaki farklara göre küçüktür. Dönme enerjisi için temel ve uyarılmış hal arası geçişler, 0,01-1 cm arası dalga boyundaki ışın ile oluşabilir; bu enerjiler mikro dalga ve uzun dalga boylu infrared ışın bölgelerini içermektedir. Bir dizi keskin, iyi tanımlanmış çizgiden oluşan atomik absorpsiyon spektrumlardakinin tersine, ultraviyole ve görünür bölgedeki molekül spektrumları, her birisi genellikle önemli bir dalga boyu aralığı içeren absorpsiyon bölgelerinden oluşur(Şekil 2.2. b,c). Moleküler absorpsiyon, elektronik geçişleri de içerir. Bununla birlikte, Eşitlik (2-3) ve (2-4)’te de gösterildiği gibi, çok sayıdaki titreşim halinin varlığından dolayı, her elektronik geçiş için birbirine yakın çok sayıda absorpsiyon çizgileri bulunmaktadır. Bunun ötesinde, daha önce de anıldığı gibi, her dönme hali için de çok sayıda titreşim enerji düzeyi vardır. Sonuç olarak, Şekil 2.1.b’de benzen buharı için gösterildiği gibi, bir absorpsiyon bandı oluşturacak şekilde birbirine yakın çok sayıda absorpsiyon çizgisinden meydana gelmiştir. Yüksek ayırım gücü olan bir cihaz kullanılmadığı sürece, bireysel pikler seçilemez ve spektrumlar Şekil 2-1c’deki gibi geniş ve düzgün pikler halinde görülür. Son olarak, yoğunlaşmış halde ve çözücü moleküllerin varlığında bireysel çizgiler daha da genişleyerek Şekil 2-1d’deki gibi sürekli spektrumlar oluştururlar. Saf
titreşim absorpsiyonu, ışın enerjisinin elektronik geçişleri uyarmaya yetmediği infrared bölgesinde görülür. Bu tür spektrumlar, çeşitli titreşim kuantum düzeyleri arasındaki geçişlerden oluşan dar ve birbirine yakın absorpsiyon pikleri içerir(Şekil 2.2.a’nın altında, IR şeklinde gösterilen geçişler de görebiliriz). Her titreşim düzeyi için dönme düzeyleri bir dizi pik oluşturabilir; ancak sıvı ve katı numunelerde dönme hareketleri o kadar kısıtlanır ki, bu küçük enerji farklarının etkisi gözlenemez. Bununla birlikte, gazlar için saf dönme spektrumları mikrodalga bölgesinde gözlenebilir(7).
2.1.3. Manyetik Alanla Oluşan Absorpsiyon
Bazı elementlerin çekirdekleri ve elektronları güçlü bir manyetik alana maruz kaldığında, bu temel parçacıkların manyetik özelliklerinden dolayı var olanlara ek olarak bazı kuvantlaşmış enerji düzeyleri gözlenebilir. Oluşan bu yeni düzeyler arasındaki enerji farkı çok küçük olup, bu düzeyler arasındaki geçişler, ancak uzun dalga boylu (veya düşük frekanslı ) ışının absorpsiyonuyla üretilebilir. Çekirdek için, 30-500 MHz (λ =1000-60 cm ) arası radyo dalgaları, elektronlar için ise yaklaşık 9500 MHz (λ =3cm) frekansında mikrodalgalar absorplanır. Çekirdek ve elektronların manyetik alanda absorpsiyonu sıra ile nükleer manyetik rezonans (NMR) ve elektron spin rezonans (ESR) teknikleriyle incelenir.(7)
2.2. Suyun Özellikleri ve Etkileşimi
Su yeryüzünün dörtte üçünü kaplar (%71.7). Suyun büyük bir kısmı denizlerde toplanmıştır. Kara kısmında göl, nehir, dere ve yeraltı suları halinde bulunur. Atmosferde ise, buhar ve gözle görülemeyen küçük damlalar halinde su vardır. Su güneş enerjisi etkisi ile deniz, nehir, göl vs. gibi su birikintilerinde devamlı olarak buharlaşır. Hava akımları bu su buharlarını sürükler. Sıcaklık değişimi halinde tekrar yeryüzüne kar ve yağmur halinde düşer. Kısmen geçirgen tabakalardan geçerek yeraltı sularını meydana getirir, kısmen de akarsular halinde göl ve denizlere akar. Bu olayların hepsine birden suyun daimi devri denir. İnsan su ihtiyacını karşılamak için bu devreye müdahale etmek zorundadır.(5)
2.2.1.Suyun Toprak Tabakalarına Etkisi
Yağmur suları saf sular olup, bileşimleri ancak yeryüzü tabakalarına temas ettikten sonra değişir. Yeryüzünün üst tabakaları, hava ile devamlı temas halinde olduklarından boşluklarında hava ihtiva ederler. Yapılan araştırmalar buradaki havanın saf havaya nazaran daha fazla karbondioksitli olduğunu göstermiştir. Bu duruma bileşiminde organik madde bulunan topraklarda daha çok rastlanır. Yeryüzünde ve ona yakın tabakalarda muhtelif cins bozunma olayları olur. Hayvan ve bitki artıkları mikroorganizmaların etkisi ile daha basit parçalara ayrışır. Çürüme olayı oksijenli ortamda kokusuz olur. Burada karbondan karbondioksit, kükürtten sülfürik asit, azottan nitrik ve daha sonra nitrik asit oluşur. Bu olaya genellikle mineralizasyon denir. Bu olay oksijensiz veya az oksijenli ortamda olduğu takdirde fena kokan çürüme olayı meydana gelir. Bunun sonucu olarak diğer bazı maddelerin yanı sıra, karbondioksit, amonyak ve kükürtlü hidrojen teşekkül eder. Bunlar daha sonra oksijenin etkisiyle nitrik ve sülfürik aside dönüşürler. Ara ürün olarak meydana gelen organik maddelerde kısmen organik asitler bulunur. Teşekkül eden gerek organik gerekse anorganik asitler suda çözünerek anorganik maddelerin daha fazla çözünmesini sağlar. Burada en büyük rolü karbondioksit oynar. Yapılan araştırmalarda suyun geçtiği kütlelerin cinsi ve jeolojik menşei olduğu halde, yukarıdaki sebeplerden dolayı iki faklı yerden alınan su numunelerinin bileşimleri farklı bulunmuştur. Demek oluyor ki suyun bileşiminde en üst toprak tabakası da mühim rol oynamaktadır. Bilhassa, karbondioksit bakımından zengin sularda hemen hemen bütün organik maddeler az veya çok çözünür. Hatta güç çözünen silikatlar bile uzun zaman böyle suların etkisinde kalarak çözünürler.
Suyun temas ettiği toprak tabakaları, kalsiyum ve magnezyum karbonatlardan teşekkül etmişse, bikarbonat halinde suda çözünürler.(5)
2.2.1.1. Mekanik Olarak Etkisi
Bunlar genellikle hazırlayıcı sebeplerdir. Örneğin sudaki sıcaklık değişimleri temas ettikleri kütlelerde yarık ve çatlaklar meydana getirir, bunlar gittikçe daha büyür. Özellikle bu etki suyun donmasıyla zaman zaman artar. Bu etkiler nedeniyle aslında dayanıklı olan kütleler ufalanır ve su tarafından sürüklenir. Bunlardan başka akarsular taş, kum vs. yi harekete getirerek bunları mekanik olarak aşındırır ve parçalar.(5)
2.2.1.2. Doğrudan Doğruya Etkisi
Toprakta bulunan klorürler, nitratlar, özellikle alkali ve magnezyum bileşikleri suda kolaylıkla çözünürler. Otasyum tuzları suda hiç bulunmaz, yahut az miktarda bulunur. Bunun sebebi bu bileşiklerin gerekli besleyici madde olmaları nedeniyle bitkiler tarafından alınmış olmalarındandır. Bitki kökündeki potasyum sodyuma nazaran 1/100 oranında fazladır. Doğal su tuzları doymuş hale gelecek kadar çözmese de bu çözünen tuzlar birbirlerinin çözünürlüklerini etkiler. Müşterek iyonlu tuzlar birbirlerinin çözünürlüklerini azaltır, aksi olduğu zaman arttırır. Alkali klorürler, kalsiyum karbonat, fosfat ve sülfatın çözünürlüklerini etkiler. Alkaliler, özellikle sodyum sülfat, kalsiyum ve magnezyum sülfatlar doğrudan doğruya suda çözünür. Bunların çözünürlüklerini klorürler arttırır, sülfatlar ise azaltır. Örneğin sodyum klorür bulunması alçı taşının çözünürlüklerini üç kez arttırır. Alkali bromür iyodür ve stronsiyum ve lityum tuzlarına birçok maden sularında rastlanır. Mineralizasyon neticesinde meydana gelen nitrit ve nitratlar da suda çözünürler.(5)
2.2.1.3. Karşılıklı Kimyasal Etki
Topraktaki demir ve mangan tuzlarının suda çözünmeleri için kimyasal değişikliğe uğramaları gerekir. Çünkü demir hematit ( Fe2O3 ), magnetit ( Fe3O4 ) ve limonit (Fe(OH)3)
halinde çok derin tabakalarda genellikle pirolizit (MnO2) ile birlikte bulunur. Bunlardan başka
pirit ve markazit (FeS2 ) halinde de rastlanır. Bu filizler suda hemen hemen hiç çözünmezler.
Demir ve mangan suda iki değerli bileşikler halinde bulunurlar. O halde yukarda bahsedilen filizlerin suda çözünebilmeleri için bir indirgenme reaksiyonu olmalıdır. Yahut demir sülfürde olduğu gibi asit karakterli bir suyun etkisi olmalıdır. Böyle bir reaksiyonu, çürümeye müsait organik maddeler ve H2S meydana getirir. Çürüme olayında sülfürlerin sudaki serbest CO2 in
etkisiyle açığa çıkar. Bu sırada iki değerli demir ve manganın karbonat ve sülfürleri oluşur. Bunlarda sudaki serbest CO2 etkisiyle bikarbonat haline geçerek suda çözünürler. Sülfürler ise
kuru mevsimlerde alt tabakalara geçebilen hava oksijeni tarafından sülfatlara yükseltgenir ve FeSO4, MnSO4 çözünerek suya geçerler.(5)
2.2.2. Doğal Suyun Sınıflandırılması ve orijini
Tabiatta kimya bakımından saf bir suya rastlanmaz. İçme, sanayi ve başak işlerde kullanılan sularda çözünmüş halde cins ve miktar bakımından çeşitli maddeler vardır. Bu maddelerin cins ve miktarı bir suyun içilebilmesi ve endüstrinin muhtelif kısımlarında kullanılması üzerine tesir eder. Sulardaki anorganik maddeler başlıca, alkali klorürler, sülfatlar, kalsiyum, magnezyum, silis ve silikatlar, bazen demir, alüminyum flor, iyot, fosfat, nitrit ve nitrat bileşenleridir. Organik maddelerde süspansiyon ve çözelti halinde bulunur. Organizmalardan yosunlar, mantarlar, mikroorganizmalar, bakteriler protozoerler bulunabilir. Sular orijinlerine göre: a-Meteor suları, b-Yeraltı ve kaynak suları, c-Yeryüzü suları d-Maden suları olmak üzere dörde ayrılır. Yağmur ve kar suları doğal suların en temizidir. Fakat bununla beraber havada bulunan bütün gazları, bazı anorganik ve organik maddeleri de çözmüştür. Bileşimleri yağdıkları bölgeye göre değişebilir. Aşağıda çeşitli yağmur sularının bileşimi Tablo.1. de gösterilmiştir.
Yağmur sularında bulunan maddeler Endüstri bölgesi pps Orman bölgesi pps Toz ve kömür tozu Anorganik maddeler Potasyum bileşikleri Sodyum bileşikleri Kalsiyum bileşikleri Magnezyum bileşik. Demir oksit Sülfürik asit Fosforik asit Hidroklorik asit Toplam 5.79 13.19 0.53 0.74 0.61 0.21 1.79 1.84 0.23 0.22 25.5 4.17 2.91 0.54 0.85 0.76 0.17 0.37 0.86 0.09 0.17 10.89 Tablo 2.1. Çeşitli yağmur sularının bileşimleri.(5)
2.2.3.Yeraltı Suyu ve Kaynak Suları
Yeryüzüne yağan yağmur suları toprakta temasla daha fazla maddeyi çözerek bünyesine alma imkanı bulur. Yeraltı katmanlarında muhtelif cins ayrışmalar meydana gelir. Örneğin bitkisel ve hayvansal maddeler mikroorganizmaların etkisi ile daha basit maddelere ayrışır. Bu ayrışma olayının oksijenli ve oksijensiz ortamda meydana gelmesine göre muhtelif cins ayrışım maddeleri oluşur. Bu ayrışma, daha doğrusu çürüme olayı, oksijenli ortamda olmuşsa kokusuz çürüme olur. Burada karbondan karbondioksit, kükürtten sülfürik asit, azottan nitrit ve nitrat asitleri teşekkül eder. Çürüme olayı oksijensiz ortamda olduğu takdirde fena kokan çürüme ürünlerinden amonyak, kükürtlü hidrojen oluşur. Organik maddelerin bozulmasından meydana gelen asitler nedeniyle su, daha fazla çözme özelliği kazanır. Burada en büyük rolü miktarca fazla olduğundan karbondioksit oynar. Toprağın bileşimindeki kalsiyum ve magnezyum karbonat bikarbonat haline geçerek suda çözünür. Fazla miktarda silikatlı topraklar daha güç çözünür. Bu nedenle kalkerli tabakalardan geçen sularda killi tabakalardan geçenlere oranla daha fazla çözünmüş madde vardır. Sulardaki asitlerin fazlalığı organik maddelerin ayrışmasından meydana gelir. Organik maddece zengin tabakalardan geçen sularda aynı zamanda amonyak ve demirde fazla bulunur. Genellikle suyun geçtiği yerlerde sırası ile evvela klorürler, alkali sülfatlar, kalsiyum ve magnezyum sülfatlar ve bunların karbonatları demir ve mangan bileşikleri çözünür. Su yeraltına geçerken içerisinde çözünmüş ve çözünebilen maddelerin miktarı artar. Halbuki diğer maddeler yerin süzgeç görevi ile gittikçe azalır. Bu durum özellikle mikroplar için önemlidir. İyi süzgeç vazifesi gören tabakalardan geçen su çok çabuk bakterilerden temizlenir. Çatlakları bulunan yerlerden geçen su iyi süzülmeye uğramadığından bakterilerden ayrılmamıştır.(5)
2.2.4. Yeryüzü Suları
Bunlar çay, dere, göl, baraj ve deniz sularıdır doğal bir süzülmeye uğramadıklarından öncekilere oranla fazla miktarda safsızlıkları vardır. Yeryüzü sularının bileşimi aktıkları veya bulundukları arazinin cinsine, mevsimlere, içine karışan diğer suların bileşimine göre çok farklıdır. İlkbaharda suların bol bulunduğu zamanda toprak süzme işini iyi yapamadığından suda
süspansiyon halinde fazla miktarda maddelere rastlanır. Diğer taraftan bu sular hava ile temasta bulunduklarından sertliklerinin bir kısmını kaybeder. Yukarıda anlatılan sebeplerden dolayı yeryüzü suları sağlık bakımından hiçbir zaman temiz değildir. Bu sularda organik maddeler, nitrit ve nitratların bulunması bunu gösterir. Dağlardan akan dere ve nehir suları en saf sulardır.
Kirletici cisimlerle temas etmeyen yeryüzü suları uzun zaman durmakla kendi kendine temizlenebilir. Bu olay sıcaklık, suyun bileşimi, akma hız, kimyasal ve biyolojik faktörlerin etkisi altında olur. Baraj suları da yeryüzü sularından farklı değildir. Yalnız bunlar özellikle kentsel ve endüstriyel bölgelerde kullanıldıklarından kirletici sularla temasta bulunmamalarına mümkün olduğu kadar dikkat etmelidir.(5)
2.2.5. Maden suları
Doğal sulardaki çözünmüş madde miktarı muayyen sınırı geçecek veya sıcaklığı normalden uzaklaşacak olursa, bu gibi sulara ‘maden suları’ bulunduğu kaynaklara da ‘maden suyu kaynağı’ denir. Bunlar bileşim ve sıcaklıklarına göre muhtelif kısımlara ayrılır.(5)
2.2.6. Suyun Fiziksel ve Fizikokimyasal Özellikleri
Kimyaca saf su hidrojenin oksididir. Bileşimi H2O olup molekül ağırlığı, 18,016 dır.100
kısım su ağırlıkça 11.11 hidrojen ile 88,89 oksijenden meydana gelmiştir. Su molekülü simetrik değildir. Elektrik yükünün heterojen bir şekilde dağılmasından dolayı daracık bir üçgen şeklini alır ve dipol karakteri gösterir. Oksijen atomunun bulunduğu yerde ise pozitif elektrik yükü fazladır. Suyun dielektrik sabitinin büyük oluşu ve çözücülük özelliği bu dipol karakterinden ileri gelir. Suyun donma noktası 760 mm Hg’ da 0 0C kaynama noktası ise aynı şartlarda 100 0C dır.1 kğ su, 0 0Cde sıvı halden katı hale geçerken 76,42 kcal açığa çıkar. Buda gram-mol başına 1,43 kcal eder. Buzu erime noktasından fazla ısıtmak mümkün değildir. Fakat suyu donma noktasından aşağı soğutmak kabildir. Su -4 0C a kadar donmadan sıvı halde kalabilir. Gerek sıvı su gerekse buz çok az sıkışabilir. Donma esnasında hacim büyümesi kapalı yerde olursa yüzlerce atmosferlik basınç meydana gelir. Doğada kayaların parçalanması iyi parçalanmamış ve yaş harcın dökülmesi vs. olaylar bunun bir sonucudur.Buzun özgül ısısı 0 0C de 0.506 kcal/kg dır. Suyun rengi kalın tabaka halinde mavimsidir. Görülen herhangi bir başka renk suda çözünmüş
veya süspansiyon halinde yabancı maddelerden ileri gelir. Çözünmüş demir ve kalsiyum bikarbonat yeşil, organik maddeler, çözünmüş veya süspansiyon halindeki, sarıdan esmere kadar renk verir. Su 100 0C de sıvı halden gaz haline geçerken kilogram başına 539 kcal ısı absorbe eder. Bu gram mol başına 9,72 kcal’dir. Su buharı için diğer gaz kanunları geçerlidir. Ancak buharın ideal bir gaz olmadığını dikkate almak gerekir. Su moleküllerinin büyük bir kısmı assosiye olmuştur. Yani moleküllerin büyük bir kısmı (H2O) halindedir. (n) yani assosiasyon
derecesinin büyüklüğü bilinmemektedir. Saf su elektrik akımını çok az iletir. Bunun sebebi; su moleküllerinin çok az bir kısmının iyonlarına ayrılmış olmasıdır. Suda yabancı maddelerin çözünmesi ile donma ve kaynama noktaları değişir. Saf suya nazaran sulu çözeltilerin buhar basıncı daha düşüktür. Sonuç olarak donma noktası yükselir.1 lt suda 1 mol madde çözüldüğünde molar kaynama noktası düşmesi ise 1,86 0C dir.
2.2.7. Suyun Kimyasal Özellikleri
Su bazı elementler ve birçok bileşiklerle birleşir. Çözünmüş madde molekülleri ile birleşerek hidratları meydana getirir; bu özellik bize suyun elektrolit olmayan maddeleri iyi çözebilmesini açıklar. Su, hidratlarda az veya çok sıkı bağlıdır. Bazen de çözünmüş madde ile beraber ayrılabilir ve mevcut sıcaklık ve konsantrasyon şartlarına göre, aynı maddenin muhtelif hidratları billurlaşabilir. Örneğin, sodyum karbonatın muhtelif hidratları olan dihidrat, hepta hidrat, daka hidrat gibi. Bu hidratların bir kısmı havada kristal suyu kaybedebilir (çamaşır sodasında olduğu gibi ). Bazı maddeler ise havanın nemini hidrat halinde bünyelerine alabilirler Kalsiyum klorür, sülfürik asit ve fosforik asit anhidritinde olduğu gibi. Birçok kimyasal olaylar ancak az miktarda su mevcudiyetinde oluşur. Örneğin, demirin paslanması için eser miktarda suya ihtiyaç vardır. Bazen de suyun katalitik tesiri görülür. Susuz halde hissedilmeyecek derecede yavaş ceryan eden bir reaksiyon, eser miktarda suyun ilavesi ile çok çabuklaşabilir. Suyun katalitik tesiri bazen disosiye ettirme özelliğinden ileri gelir. Bu hal yalnız iyon reaksiyonlarını değil, redoks, yanma ve diğer reaksiyonları da çabuklaştırır veya yavaşlatır. Suyun ait diğer karakteristik bir olayda hidrolizdir. Bu olay çözünmüş maddenin su iyonları ile meydana getirdiği bir reaksiyondur.
Örnek: CH3CHOOH + H2O KOH + CH3COOH
Burada asetik asit zayıf bir asit potasyum hidroksit kuvvetli baz olduğundan suyun pH değeri yükselir. Su buharı halinde de birçok reaksiyonlar verir. Bunların en önemlisi,
3Fe + 4H2O Fe3O4 + 4H2
3. MATERYAL METOT VE DENEY
3.1 Lambda 2 UV/VIS Spektrometre (Perkin Elmer) Aletinin Başlıca Kısımları ve Özellikleri
Resim 3.1.Lambda 2 UV/VIS Spektrometre
Yukarıdaki Resim 3.1 de Lambda 2UV/VIS spektrometresinin dıştan görünüşü verilmiştir. Buna bağlı bir bilgisayar yazıcısı da vardır. Lambda 2 spektrometre aletleri rutin ve otomatik analiz için geliştirilen çok yönlü bir alettir. Aletin yapılışı ve dizayn özellikleri aşağıdaki gibidir. Bu Lambda 2UV/VIS spektrometre aleti çift ışın demetli olup, 190nm-1100nm aralığında ölçüm yapabilme özelliğine sahiptir. Aktif bir hafızaya sahip olan bu alet basit bir kullanım klavyesine sahiptir. Gerekli komutlar ve değiştirmeler bu klavye yardımıyla
3.2 Lambda 2 UV/VIS Spektrometre (Perkin Elmer) Aletinin Teknik Özellikleri
İşlem Prensibi: Çift ışın demetli spektrometre UV-VIS bölge için mini bilgisayar elektronik klavye giriş ve vakumlu flouresans göstergeli.
Monokramatör: Holografik ağ örgülü konkav çizgiler 1053 çizgi/nm
Işın Kaynağı: Döteryum ve Tungusten halojen lambalar otomatik lamba seçim anahtarlı Dalgaboyu genişliği:190nm-1100nm
Sapan ışıma: 2sn zamana karşı ölçülen sapma <0,003%T 220nm <0,02 %T birim
büyüklükte iletilen ışın
Dalgaboyu: ± 0.3 nm Döteryum 656,1 nm de Üretkenlik: ± 0,1 nm
Spektral yarık genişliği: 2 nm
Fotometrik-doğruluk: ± 0,005 A 1A 0
Fotometrik -Üretkenlik: ± 0,002 1A 0
Dayanıklılık-Kararlılık: <0,003 A/n Temel çizgi-Kararlılık: ± 0,001 A
Veri Çıktısı: a) Dijital Kısım: RS-232-L/V24 Epson yazıcı 1402 b)Analog Kısım :
Bağlantısı için, analog çizim kayıt edici, c) Gösterge:40 karakter, parametreler için sayısal flouresans gösterge.
Elektriksel Özellikler:
Güç: 100W 240V arasında her voltaj 50/60Hz frekans alet otomatik olarak voltajı
önceden ayarlar.
Elektrik İşleri: 200-240V için 2,5 amperlik yavaş patlayan sigorta, 100-110v için 4 amperlik yavaş patlayan sigorta.(4)
3.2.1. İşlem Kontrolleri ve Gösterge
Resim 3.2. Lambda 2 UV/VIS spektrometresinin klavye ve göstergesi
Aletin çalışma prensibi kolay anlaşılabilir. Gösterge kullanımda üst basamak aletin durum parametrelerini gösterir. Alt basamak ise herhangi bir girdi için kullanıcının yapması gereken hareketi gösterir. Bütün kullanım girdileri aletin klavyesinde mevcuttur. Aşağıda bunların bir sıralaması ve karakterlerin gördüğü fonksiyonlar listelenmiştir.
Anahtar İşlev
0...9 : Sayısal girdiler için sayısal tuşlar Ce : Silme tuşu
Method :Hafızdaki metotların kullanıcının istediği metotları çağırır ve gerekirse
değiştirir.
Parametreler: Bu anahtar gösterge üzerinde metot parametrelerinin kullanıcı
tarafından değiştirilmesine izin verir.
< > : Bu oklardan biri veya ikisi göstergede görüldüğü takdirde klavyede tuşlanarak
bir önceki basamağa geçilir.
Enter : Değişecek parametre klavyede tuşlandıktan sonra ENTER tuşuna basılıp
yeni değerin metot da sabit olması sağlanır
Goto-Lambda: GOTO’ya basılıp yeni dalga boyu tuşlanır ENTER’e basılıp sabit olması
sağlanır.
Nokta: Sayısal girdiler için ondalıklı noktalama
Help: HELP tuşu göstergedeki duruma ait parametreler veya karakterleri için gerekli özel
bilgileri ekrana getirir.
Stop: STOP tuşuna basılınca alet analizi yapacak başlatma durumuna gelir
Methods: Bu tuş aktif hafızadaki metotları çağırır.(4)
3.2.2. Lambda 2 UV/VIS Spektrometresinin Aktif Hafızasındaki Analiz Fonksiyonları
1)Time-Drive Metodu:Bu metot bir dalga boyunda zamana karşı numunenin
absorpsiyonunu hesaplar
2)Scan Metodu: Bu metot iki dalga boyu arsında numunenin
spektrumunu verir. Maksimum absorpsiyon dalga boyunu saptar.
3) Waveprog Metodu: 20’ye kadar değişik dalga boyunda numunenin absorpsiyonunu
hesaplar
4) Conc-1 Metodu: Örnek standartlar üzerinde kalibrasyon eğrisini çizerek
konsantrasyonu bilinmeyen numunenin konsantrasyonunun saptanmasını sağlar.(4)
3.2.3. Lambda 2 UV/VIS Spektrometresinin Optik Prensibi
Perkin Elmer Lambda 2s aletindeki optik yollar Şekil 3.1. de gösterilmiştir. Alette kullanılan monokromatörün konkav ağ çizgilerinin sıklığı 1053 çizgi/nm’dir. P1 düzlem aynası bir mekanik kol ile pozisyonu değiştirilir.
Monokromator normal durumda iken DL Döteryum lambası kilitlenir, ve Halojen ışık kaynağından çıkan ışınlar (T2) toraidal ayna üzerine yansıtılır. Işık kaynakları P1 aynasının pozisyonundan dolayı özel bir dalga boyunda, monokromatör ile eşzamanlı çalışır. Işınlar T2 aynası tarafından odaklanır.
Döner filtre(FW) içinden geçerek giriş yarığı (ESI) üzerine düşer. Döner filtreler farklı optik özelliklerine sahip filtrelerden oluşmuştur. Bunlar monokromatör ile eş zamanlı çalışırlar. Filtreler monokromatöre ulaşan bir dizi dalga boylarını sınırlar ve bu yüzden sapan ışımaları azaltıcı etki gösterirler.
Işınlar ESI giriş yarığından geçerek monokromatöre ulaşır. Gelen ışınalar monokromatör tarafından spektral olarak dağıtılıp ES2 çıkış yarığı ışınlar, buradan da BS ışın yarıcısı üzerine yansıtılır.
Işın yarıcısı ışınların %50’sinideP4 düzlem aynası %50’sinide P5 düzlem aynası üzerine yansıtır. P4 aynası ışınları içinde numunenin bulunduğu küvete P5 aynası ise referans küveti üzerine odaklar daha sonra bunları geçen ışınlar foto-diyod dedektör üzerine bir basit konveks mercek tarafından odaklanır.(4)
Şekil 3.1. Aletin Optik Şeması (4)
3.3. Kullanılan Metot ve Deney.
3.3.1.Nitrat Tayini
Volkanik kayalarda çok az nitrat bileşiklerine rastlanır. Yüzey sularına nitrat, atmosferik olaylar neticesinde teşekkül eden nitrik asidin yağmur suyu halinde karışmasından geçer. Ayrıca
yeraltı ve yerüstü sularına nitratlı bitkilerin çürümesi neticesinde topraktan da geçebilir. Bundan başka kanalizasyon sularıyla kirlenme halinde nitrat konsantrasyonu yüksektir. Bu gibi hallerde ekseri sularda klorür konsantrasyonu da yüksek olur. Yüzey sularında nitrat genellikle 1 ppm’den azdır. Bazen bu değer 5 ppm olabilir. Yeraltı sularında ise 0-1000 ppm’ e kadar değişik konsantrasyonlarda bulunabilir. Örneğin zemzem suyunda nitrat konsantrasyonu 851 ppm’dir.
Metodun Esası
Bu deneyle suda mevcut nitrat tayini yapılır. Nitrat iyonları burisin sülfatla sarı renk verirler. Bütün yükseltgen ve indirgen maddeler, bakiye klor, demir (II) demir (III), mangan (VI) reaksiyonu bozarlar.
Kullanılan Alet ve Malzemeler
Spektrometre, Propipet, Beher (muhtelif)
Kullanılan Kimyasal Maddeler
Potasyum nitrat (anhidrat), Sodyum arsenit NaAsO2
Brusin sülfat, Sülfanilik asit, Hidroklorik asit ( derişik), Sülfürik asit ( derişik)
Çözeltilerin Hazırlanması
Stok nitrat Çözeltisi
0,7218 gr susuz potasyum nitrat damıtık suda çözülür. Balon jojede litreye tamamlanır. Bu çözeltinin bir litresinde 100 mg azot vardır.
Standart Nitrat Çözeltisi
100 ml stok nitrat çözeltisi alınır. Damıtık su ile balon jojede litreye tamamlanır. Bu çözeltinin 1 ml sinde 0,01 mg azot vardır.
Sodyum Arsenik Çözeltisi
5 mg sodyum arsenik damıtık suda çözülür. Balon jojede litreye tamamlanır.
Sülfürik Asit Çözeltisi
500 ml derişik sülfürik asit dikkatle 75 ml damıtık suya konur.
Brusin Sülfanilik Asit Çözeltisi
1 gr brusin sülfat ve 0,1 gr sülfanilik asit 70 ml sıcak damıtık suda çözülür üzerine 3 ml derişik hidroklorik asit konup soğutulur. Balon jojede 1000ml ye tamamlanır. Bu çözelti birkaç ay bozulmadan kalabilir.
Standart Eğrinin Çizilmesi
Standart nitrat çözeltisinden pipetle, 0 5 15 25 35 50 75 100 ml alınarak 100 ml ye tamamlanır. Böylece; 0,05 0,15 0,25 0,35 0,5 0,75 1,0 mg nitrat azotlu standart seri hazırlanır. Bu çözeltilerin her birinde propipetle 2 şer ml alınarak 50 ml lik beherlere konur.1 ml brusin sülfanilik asit çözeltisi konur. İkinci bir 50 ml’lik behere 10 ml sülfürik asit çözeltisi konur. Üçüncü 50 ml’lik behere de 10 ml damıtık su konur. Sülfürik asitle behere, standart ve brusin sülfanilik asit karışımı konur ve 5-6 defa iki beher birbirine akıtılır. Beherlerin üzerleri kapatılarak karanlıkta 10 dakika bekletilir. Bu müddetin sonunda 3. beherdeki damıtık su konur. Tekrar 2 beher 5-6 kere birbirine aktarıldıktan sonra 20-30 dakika karanlıkta bekletilir. Daha sonra 420 nm ayarlanmış spektrometrede okuma yapılır. Neticenin nitrat konsantrasyonu cinsinden elde edebilmek için ‘nitrat konsantrasyonu = nitrat azotu konsantrasyonu’ formülü
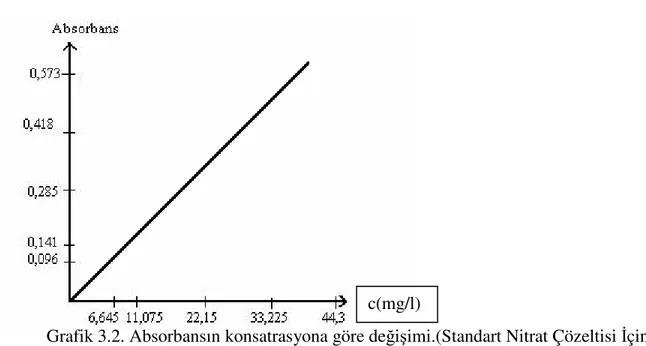
kullanılır. Okunan değerleri ordinat, nitrat konsantrasyonu değerleri apsisde gösterilen standart eğri çizilir.
Grafik 3.2. Absorbansın konsatrasyona göre değişimi.(Standart Nitrat Çözeltisi İçin)
Numunede Nitrat Tayini
Numunede serbest klor varsa önce bunun uzaklaştırılması gerekir.0,1 mg klor için 0,05 ml (yaklaşık bir damla) sodyum arsenik çözeltisi konarak iyice karıştırılır. Aldığımız numunelerde ortalama 9.8 mg/lt oranında klor bulunmaktadır. Bundan dolayı her 1 lt numuneye ortalama 4,9 ml sodyum arsenik çözeltisi koyup karıştırdık.
50 ml’lik bir behere 2 ml (10 mg/l den fazla nitrat azotunu geçmeyecek şekilde) numune konur. Standartlara yapılan işlemler sonra spektrometrede okuma yapılır. Okunan değer standart eğriye uygulanarak nitrat azotu konsantrasyonu hesaplanır. Eğer seyreltme yapılmışsa bulunan değerin bu seyreltme faktörüyle çarpılması gerekir. Biz seyreltme yapmadığımızdan bulduğunuz değeri seyreltme faktörü ile çarpmadık.
hacmi numune ml 1000 miktarı nitrat olarak mg mg/l azotu Nitrat = × c(mg/l)
Eğer mg/l nitrat olarak netice verilmek isteniyorsa ;
Nitrat mg/l = mg/l nitrat azotu x 4,43 formülü kullanılarak hesap yapılır.
Devegeçidi Baraj Suyunun 5 ayrı noktasından birer su örneği aldıktan sonra her bir su örneğine ortalama litre başına 4,9 ml sodyum arsenik çözeltisi koyduk. Daha sonra standartlara uyguladığımız işlemleri numunelere de uyguladık. Daha sonra spektrometrede absorbans değerlerini ölçtük. Önceden standart nitrat çözeltisi kullanarak oluşturduğumuz absorbans-konsantrasyon grafiği ile numunelerden ölçtüğümüz absorbans değerlerini karşılaştırarak numunelerde nitrat konsantrasyonumu belirledik. Baraj Suyundan birer km aralıklarla aldığımız 5 ayrı numunede ölçtüğümüz absorbans değerleri:
1)0,092- 2)0,096- 3)0,093- 4)0,105- 5)0,097. Grafik sonucunda elde ettiğimiz numunelerin konsantrasyonları 1)7,112- 2)7,421- 3)7,190- 4)8,117- 5)7,499 mg/lt olarak ölçüldü.
Tablo 3.1 Numunelerdeki nitrat konsantrasyonları.
1.numune 2.numune 3.numune 4.numune 5.numune ortalama Nitrat mg/lt) 7,112 7,421 7,190 8,117 7,499 7,466
Grafik 3.3. Absorbansın konsatrasyona göre değişimi. (Baraj Suyundan Alınan Numuneler İçin)
Yapılan ölçümlerdeki hatanın %15 den küçük olduğu tahmin edilmektedir.
Dikkat Edilecek Noktalar
Burisin sülfat ve sodyum arsenit çözeltileri zehirli olduğundan çalışılırken çok dikkat edilmesi gerekir. Bütün can malzemelerin kromatlı yıkama asidi veya deterjanla temizlenmesi gerekir.
EK: Numunelerin Baraj Gölünden Alındığı Noktalar ve Baraj Suyunun Kimyasal
Yapısına Etkiyen Faktörler
BÖLÜM.4. TARTIŞMA VE SONUÇ
Analiz edilen numuneler 12 Mayıs 2005 tarihinde Devegeçidi Baraj Suyunun, birer km aralıklarla, 5 ayrı noktasından alındı. Bu numunelerden 1)7.112 mg/lt, 2)7.421 mg/lt, 3)7,190 mg/lt 4)8.117 mg/lt, 5)7.449 mg/lt, ortalama 7.466 mg/lt kadar nitrat konsantrasyonu tespit edildi.
DSİ X. Bölge Müdürlüğü tarafından 1997 yılında Devegeçidi Barajından alınan su numunelerindeki ortalama nitrat konsantrasyonu ise 6.069 mg/lt'dir. Nitrat konsantrasyonlarının 1997 yılına göre artığı görülür. Artışın %18,2 kadar olduğu hesaplandı.
Bu artmanın nedenleri: barajın su toplama havzasında bulunan Ergani ilçesi ve diğer yerleşim alanlarının kanalizasyon sularının arıtılmadan doğrudan derelere deşarj edilmesi, foseptik çukurlarından sızmalar, bilhassa nitratlı yapay gübrelerin, çevredeki tarlalarda, aşırı ve kontrolsüz, yıllara göre artar miktarlarda kullanımı ve hayvan atıkları, yerleşim yerlerinin dere yataklarının yakınından geçmesi sonucu yağışla birlikte akışa geçen çöplerin kirli suları atmosferik olaylar neticesinde teşekkül eden nitrik asidin yağmur suyu halinde karışmasının da sebep olduğu düşünülmektedir.
Kimyasal bir maddenin çevre sularından gereğinden fazla ya da az bulunması canlıların yaşamını olumsuz etkiler. Tespit edilen nitrat konsantrastonu değerleri Dünya Sağlık Örgütü (WHO)'nün suda nitrat için tavsiye ettiği değerin çok altındadır. Dünya Sağlık Örgütünü'nün tavsiyesi: 44 mg/lt'dir. Yüksek nitrat konsantrasyonu balıklarda bağışılık sisteminin zayıflamasına ve büyümenin durmasına neden olabilir. Bu yüzden, özellikle genç balıklar için yüksek nitrat konsantrasyonu büyük tehlike oluşturmaktadır. Balıklar için nitrat konsantrasyonu 25 mg/l’ yi geçmemelidir.
Sonuç olarak, anılan Devegeçidi Baraj suyunun hala nitrat yönünden temiz olduğunu ve UV/VIS spektrometresinin suda birçok kimyasal maddenin konsantrasyon ölçümünde modern, etkin ve güvenilir olarak kullanılabilir olduğunu söyleyebiliriz.
KAYNAKLAR
1. ERDİK, E.,1993. Organik Kİmyada Spekroskopik Yöntemler A.Ü. Fen Fakültesi Yayınları,Ankara.
2. Gündüz.,T.,1990. İnstrumental Analiz Ankara Üniversitesi Fen Fakültesi Yayınları. ANKARA.
3. Kacar B., 1991. Çay ve Çay Topraklarının Kimyasal Analizleri Çaykur Yayını No:14, , Ankara 4. Perkin Elmer, 1992. Lambda 2 UV/VIS Spektrometer Operator’s Manuel Publication, B.2131, 5. Riehl L., 1962. Water Supply and Treatment, Merrill..
6. Schrml E., 1998. Freshwater Coral Fish Chichlids From Lake Malawi. Verlag A.C.S. GmbH; 1 Edition
7. Skoog D. A., Holler F.H., Nieman T. A., 1998. Principles of İnstrumental Analysis, Sounder College Publising,
8. Snell F.D., 1983. Colorimetrik Metots of Analyses,
9. Sondell E.B and Kolthoff I.M., 1963. Text Book of Inorganik Analysis,
10. WHO , 2004. Guidelines for Drinking-Water Quality. 3r ed., World Healt Organization.
TABLO LİSTESİ
1) Tablo 2.1. Çeşitli Yağmur Sularının Bileşimi
2) Tablo 3.1. Beş ayrı numunenin nitrat konsantrasyounu ŞEKİL LİSTESİ
1) Şekil 1.1. c derişiminde absorpsiyon yapan bir çözelti ile bir ışın demetinde şiddet azalması. 2) Aletin optik şeması
GRAFİK LİSTESİ
1. Grafik 2.1. Tipik Ultraviole Absorpsiyon Spektrumları
2. Grafik 2.2. Bir Floresans Organik Molekül İçin Enerji-Düzey Diyagramının Bir Bölümü 3. Grafik 3.2. Absorbansın konsantrasyona göre değişimi (Standart nitrat çözeltisi için)
4. Grafik 3.3. Absorbansın konsantrasyona göre değişimi(Baraj suyundan alınan numuneler için) RESİM LİSTESİ
1. Resim 3.1 Lambda 2 UV/VIS Spektrometre
ÖZGEÇMİŞ
1980 yılında Diyarbakır’da doğdum. İlkokulu Diyarbakır Yahya kemal Beyatlı İlköğretim Okulu’nda, ortaokul ve liseyi Atatürk Lisesi’nde tamamladım.1998 yılında Dicle Üniversitesi Eğitim Fakültesi Fizik Öğretmenliği Bölümü’ne kayıt yaptım; 2003 yılında mezun oldum. Aynı yıl Dicle Üniversitesi’nde yüksek lisans programına kayıt yaptım.