Akneli hastalardaki bel çevresi, bel/kalça oranı ölçümleri ile adipoz doku hormonlarından chemerin, visfatin ve omentin-1 kan düzeylerinin değerlendirilmesi
Tam metin
Şekil
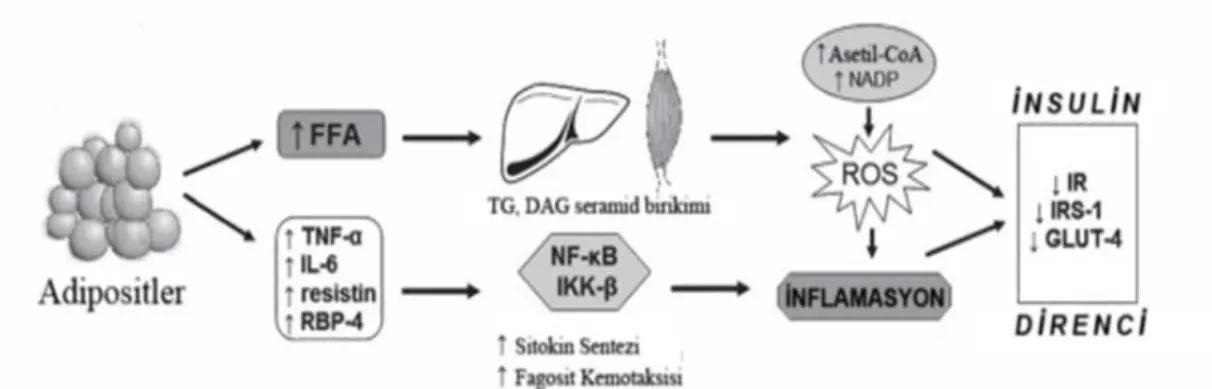
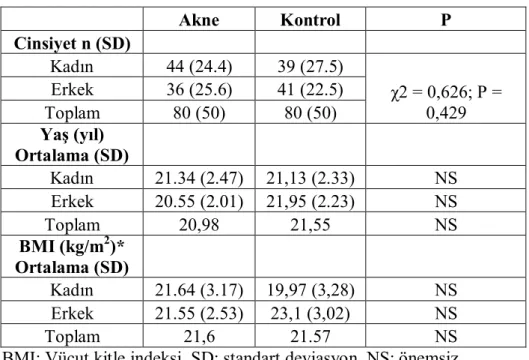
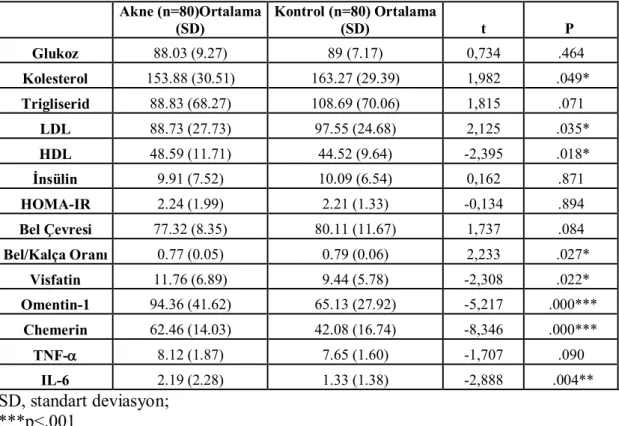
Benzer Belgeler
「 100 年全國大專運動會暨 99 學年度球類運動聯賽」總決賽授旗典禮 本校桌球隊、羽球隊、網球隊,均已報名
傑出校友專訪 赴美深造突破植牙瓶頸 臨床助理教授程國慶(上) (記者吳佳憲專訪) 北醫臨床教授程國慶醫師
C) Türk Tarih Kurumunun açılması D)Hafta tatilinin cuma gününden pazar gününe alınması 13-Atatürk, milliyetçilik ilkesinin gereği olarak; Türk Tarih Kurumu ile Türk
Sonuç olarak, SRT cerrahi uygulanamayan hastalarda primer tedavi, nükslü hastalarda veya subtotal rezeksiyon uygulanan hastalarda güvenli toksisite profiliyle uygulanabilecek
Okul çağı çocuklarının belirli aralıklarla vücut ağırlığı, boy uzunluğu, bel ve boyun çevresi düzenli olarak ölçülmeli, yaş ve cinsiyete uygun.
Bu çalışmanın amacı, dini değerlerin çocuklara öğretilmesinde, davranış haline getirilmesinde son derece önemli konuma sahip, toplumun en küçük ve temel birimi
İlköğretim müfettişlerinin görüşleri incelendiğinde genel olarak, kurs görevlilerinin hizmet-içi eğitim seminerinden geçirilmeleri, kurs görevlilerinin zamana ve