T.C.
SELÇUK ÜNĐVERSĐTESĐ
FEN BĐLĐMLERĐ ENSTĐTÜSÜ
KOK FABRĐKASI ATIKSULARININ ĐLERĐ
OKSĐDASYON YÖNTEMLERĐ ĐLE
ARITILMASI
Nazan ŞĐRĐN
YÜKSEK LĐSANS TEZĐ
Çevre Mühendisliği Anabilim Dalı
Ekim–2010
KONYA
Her Hakkı Saklıdır
iv
ÖZET
YÜKSEK LĐSANS TEZĐ
KOK FABRĐKASI ATIKSULARININ
Đ
LERĐ OKSĐDASYON YÖNTEMLERĐ ĐLE ARITILMASI
Nazan ŞĐRĐN
Selçuk Üniversitesi Fen Bilimleri Enstitüsü
Çevre Mühendisliği Anabilim Dalı
Danışman: Yrd. Doç. Dr. Dünyamın GÜÇLÜ
2010, 59 Sayfa
Jüri
Yrd. Doç. Dr. Dünyamın GÜÇLÜ
Doç. Dr. M. Faik SEVĐMLĐ
Yrd. Doç. Dr. Mustafa ONÜÇYILDIZ
Kok fabrikası atıksuları alıcı ortama deşarj edilmeden önce yüksek konsantrasyonlarda ve toksik bileşikler içermektir. Su kalitesi genellikle, klasik biyolojik arıtma proseslerinden sonra deşarj limitlerini sağlayamamaktadır. Bu çalışmada, kok atıksularının ileri arıtımı için fenton prosesi ile kok atıksularının arıtılabilirliği incelenmiştir. Deney sonuçları, atıksuyun kendi pH’sı olan 7.8 ve 60 dk sürede klasik fenton prosesi ile %86 KOĐ ve %99.5 fenol giderimi sağlandığını göstermiştir. Tüm deneylerde atıksuyun kendi pH’ı kullanılmış, pH ayarlaması yapılmamıştır. Uygun çalışma koşulu 300 mg/L Fe+2 ve 4000 mg/L H2O2 olarak belirlenmiştir. pH’daki ani düşüş, reaksiyon süresi ve maliyeti ileri arıtım için klasik fenton prosesini daha avantajlı ve uygun kılmaktadır.
v
ABSTRACT
MS THESIS
TREATMENT OF COOKĐNG INDUSTRY WASTEWATER USING
ADVANCED OXIDATION PROCESSES
Nazan ŞĐRĐN
THE GRADUATE SCHOOL OF NATURAL AND APPLIED SCIENCE OF
SELÇUK UNIVERSITY
THE DEGREE OF MASTER OF SCIENCE
IN ENVIRONMENTAL ENGINEERING
Advisor: Asst. Prof. Dünyamin Güçlü
2010, 59 Pages
Jury
Asst. Prof. Dünyamin Güçlü
Assoc. Prof. M. Faik Sevimli
Asst. Prof. Mustafa Onucyıldız
Coking wastewater contains high concentration of refractory and toxic compounds to be treated before being discharged into the environment. The water quality usually cannot meet the discharge limits after conventional biological treatment processes. This paper initially investigated the treatability of a coking wastewater with fenton for advanced treatment of coking wastewater. Based on the experimental results, up to 86 % COD and 99,5 % phenol removals were achieved by the conventional fenton process at original pH 7,8 within 60 min. In all trials, pH adjustment was not performed. The optimal operation condition was addition of 300 mg/L of Fe+2 and 4000 and of H2O2, respectively. The sudden drop of original pH, reaction time and cost make conventional fenton process more feasible and advantageous for advanced treatment.
Keywords: Advanced oxidation; coking wastewater; fenton’s oxidation; chemical oxygen demand (COD); phenol.
vi
ÖNSÖZ
Bu çalışmada öncelikle bana üstün tecrübe ve bilgisiyle ışık tutan çalışmalarım
sırasında bilgi ve hoşgörüsü ile yanımda olan, benden her konuda desteğini esirgemeyen
danışmanım Yrd. Doç. Dünyamin GÜÇLÜ’ ye saygılarımı sunarım.
Laboratuar ve literatür çalışmaları sırasında bana her konuda yardımcı olan ve
destek veren Doç. Dr. Mehmet Faik Sevimli ve Arş. Grv. Serkan ŞAHĐNKAYA’ ya ve
özellikle çalışmalarını yaptığım atıksu numunesinin temini konusunda Karabük Demir
Çelik Đşletmesi (KARDEMĐR) yönetici ve personeline teşekkürü bir borç bilirim;
Ayrıca bütün hayatım boyunca maddi ve manevi desteklerini, sevgilerini ve
ilgilerini benden hiç esirgemeyen; bütün öğrenim hayatım boyunca özellikle yüksek
lisans eğitimimde tez yazımım sırasında desteklerini daima hissettiğim sevgili aileme ve
arkadaşlarıma özellikle çok teşekkür ediyorum, iyi ki varsınız.
Nazan ŞĐRĐN
KONYA–2010
vii
Đ
ÇĐNDEKĐLER
ÖZET ... iv
ABSTRACT... v
ÖNSÖZ ... vi
Đ
ÇĐNDEKĐLER ... vii
SĐMGELER VE KISALTMALAR ... ix
1. GĐRĐŞ ... 1
2. KAYNAK ARAŞTIRMASI ... 3
2.1. Kok Kömürü Endüstrisinin Tanımı ... 3
2.2. Kömür Çeşitleri ve Kok Kömürü... 3
2.3. Koklaştırma Prosesi ... 5
2.4. Kok Fabrikaları Atıksuları ... 5
2.5. Kok Üretimi Atık Karakteristikleri... 6
2.5.1. Gaz atıklar... 6
2.5.2. Sıvı atıklar... 6
2.5.3. Katı atıklar ... 7
2.6. Koklaştırma Tesislerinin Atıksularının Arıtımında Uygulanan Yöntemler ... 7
2.7. Fenton Oksidasyonu Đle Arıtım Yönteminin Genel Esasları ... 13
2.7.1. Fenton prosesinde oluşan kimyasal reaksiyonlar... 14
2.7.2. Koagülasyon reaksiyonları ... 15
2.8. Fenton Prosesine Etki Eden Faktörler ... 16
2.8.1. pH etkisi ... 16
2.8.2. Sıcaklık etkisi... 16
2.8.3. Demir sülfat miktarının etkisi ... 16
2.8.4. Hidrojen peroksit miktarının etkisi ... 17
2.8.5. Demir iyonu türünün etkisi ... 18
2.9. Fenton Oksidasyonunun Modifikasyonları... 18
2.9.1. Foto - fenton prosesi ... 18
2.9.2. Elektro-fenton prosesi... 19
2.10. Fenton ile Oksidasyon Đleri Arıtım Yönteminin Avantaj ve Dezavantajları .... 19
2.11. Fenton Oksidasyonu ile KOĐ Giderimi Uygulama Örnekleri ... 19
2.12. Fenol ve Yapısı ... 21
3. MATERYAL VE METOT... 23
3.1. Atıksu ve Özellikleri ... 23
3.2. Fenton Oksidasyon Uygulaması ... 26
3.3. Analitik Metotlar... 27
4. ARAŞTIRMA SONUÇLARI VE TARTIŞMA... 28
viii
4.2. Fenton Prosesi Đçin Uygun FeSO4 Miktarının Belirlenmesi ... 31
4.3. Fenton Prosesi Đçin Uygun H
2O
2Miktarının Belirlenmesi... 35
4.4. Kinetik Çalışmalar ... 38
5. SONUÇLAR VE ÖNERĐLER ... 41
ix
SĐMGELER VE KISALTMALAR
Simgeler
BOĐ
5: Biyolojik Oksijen Đhtiyacı
°C : Santigrat derece
cm : Santimetre
DAS : Demir amonyum sülfat
dk : Dakika
EF : Elektro fenton
Fe
+2: Demir +2 değerlikli
Fe
+3: Demir +3 değerlikli
FeSO
4: Demir sülfat
FSR : Fenton çamuru yeniden işleme
H
2SO
4: Sülfürikasit
H
2O
2: Hidrojen peroksit
K
2Cr
2:
Potasyum dikromat
KOĐ : Kimyasal Oksijen Đhtiyacı
MnO
4: Manganat
NaCl : Sodyum Klorür
NaOH : Sodyum Hidroksit
TKM : Toplam katı madde
PM : Patikül madde
VOC : Uçucu organik bileşikler
PAH : Polinükleer aromatik hidrokarbonlar
TEP : Ton petrol eşdeğeri
WHO : Dünya Sağlık Teşkilatı
x
Ş
EKĐLLER LĐSTESĐ
Şekil 2.1 Kömür çeşitleri ve kaynak durumları……….4
Şekil 2.2 Taşkömürünün sektörler bazında kullanımı……….………..4
Şekil 2.3 Kömürden kimyasal madde üretim, yöntemleri...…...5
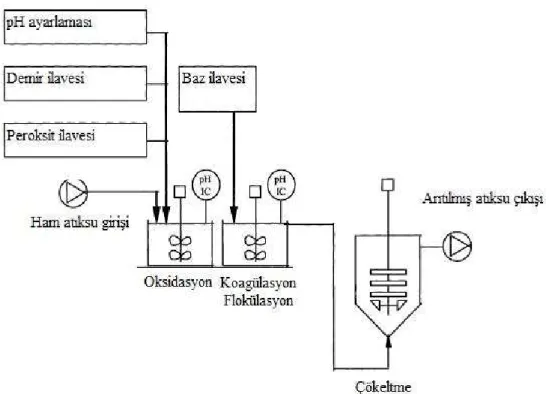
Şekil 2.4 Fenton prosesinin uygulaması……….………..………...15
Şekil 2.5 Fenol halkası...………...……....22
Şekil 3.1 Koklaştırma fabrikaları Đş Akım Şeması………...24
Şekil 3.2 Kardemir kok fabrikası arıtma tesisi proses akım şeması………....25
Şekil 3.3 Deneysel çalışmalarda kullanılan jar test düzeneği………..26
Şekil 4.1 KOĐ, Fenol ve UV
254parametrelerine ait C/C
odeğerleri………...30
Şekil 4.2 KOĐ, Fenol ve UV
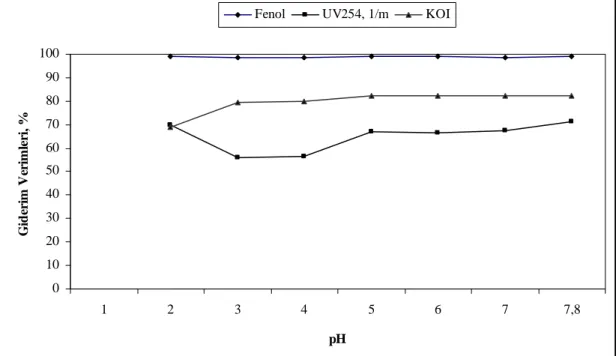
254parametrelerine ait giderim verimleri………30
Şekil 4.3 Zamana bağlı pH ’daki değişim………...31
Şekil 4.4 Fe
+2miktarına bağlı olarak kalan KOĐ ve fenol konsantrasyonları……..…..33
Şekil 4.5 Dozlanan Fe
+2miktarına bağlı olarak C/Co değeri……….…33
Şekil 4.6 Dozlanan Fe
+2miktarına göre KOĐ ve fenol giderim verimleri ………….….34
Şekil 4.7 Dozlanan H
2O
2miktarına göre KOĐ ve fenol giderim verimleri…………...36
Şekil 4.8 Dozlanan H
2O
2miktarına göre KOĐ, fenol, C/Co değerleri ………..…..36
Şekil 4.9 Dozlanan H
2O
2miktarına göre kalan KOĐ ve fenol konsantrasyonları…..…..37
Şekil 4.10. KOĐ ve Fenol için oksidasyon zamanı ve t/(1−C/C
0) arasındaki ilişki …....39
xi
ÇĐZELGELER LĐSTESĐ
Çizelge 2.1 Fenton metodunun avantajları ve dezavantajları………..19
Çizelge 3.1 Biyolojik ünite çıkışı atıksu karakteristiği………23
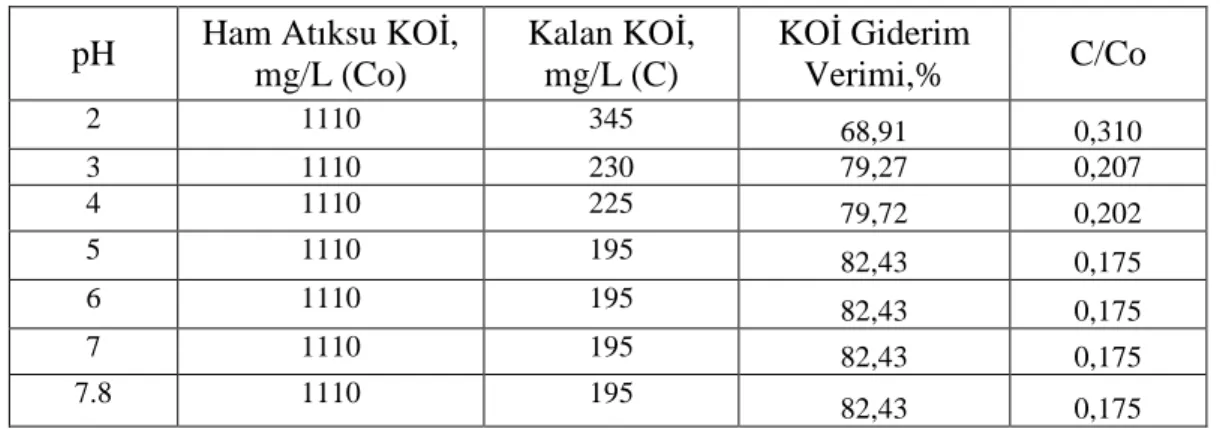
Çizelge 4.1 pH Değerine göre KOĐ giderimi ve giderim verimi……….29
Çizelge 4.2 pH Değerine göre fenol giderimi ve giderim verimi………29
Çizelge 4.3 pH Değerine göre UV
254nm ve giderim verimi………..29
Çizelge 4.4 KOĐ gideriminin Fe
+2konsantrasyonuna bağlı olarak değişimi………...32
Çizelge 4.5 Fenol gideriminin demir tozu konsantrasyonuna bağlı olarak değişimi…..32
Çizelge 4.6 KOĐ gideriminin H
2O
2konsantrasyonuna bağlı olarak değişimi………….35
Çizelge 4.7 Fenol gideriminin H
2O
2konsantrasyonuna bağlı olarak değişimi ………..35
Çizelge 4.8 KOĐ için kinetik çalışmada elde edilen sonuçlar ………38
Çizelge 4.9 Fenol için kinetik çalışmada elde edilen sonuçlar ……….……….38
1. GĐRĐŞ
Günümüzde nüfusun hızla artması, şehirleşme ve endüstrileşme sonucu çeşitli
kirleticiler sulara karışmakta ve su kaynaklarının kalitelerinin bozulmasına, nihayetinde
de kirlenmesine neden olmaktadır. Özellikle endüstriyel atıksularda bulunan ağır
metallerin suda yasayan canlılarda birikmesiyle bu canlılarda kalıcı mutasyonlar ve
ölümler gerçekleşmekte ve çevre dengesi bozulmaktadır. Eser miktarlarda bile toksik
etki yapan bu metaller ile organik kökenli bileşikler arasında en önemli grubu CN
-, Cr,
Ni, Zn, Cu, ve fenol gibi parametreler oluşturmaktadır. Fenol ve türevleri bilinen en
toksik ve tehlikeli organik kirleticilerdendir. Fenol ve türevleri toksik özellikleri
nedeniyle atıksularda bu bileşiklerin miktarlarına sınırlandırmalar getirilmiştir.
Endüstriyel atık akımlarında sıkça fenol ve türevlerine rastlanmaktadır. Özellikle kömür
işletmelerinin kömür destilasyon, petrokimyasallar petrol arıtım ve organik sentezlerin
atık akımları bol miktarda fenol kirliliği içerir. Karbonizasyon prosesi sırasında suya
önemli miktarda fenol karışmaktadır. Demir çelik fabrikaları, kok ve havagazı üretim
tesisleri karbonizasyon prosesi ile isletilmektedir. Aynı zamanda insan sağlığı açısından
da tehlikeli atık sınıfına giren bu parametrelerin atıksulardan uzaklaştırılması, çevreye
verdiği olumsuz etkilerin giderimi amacıyla çeşitli arıtma teknikleri geliştirilmiş ve
geliştirilmektedir.
Ülkemiz açısından önemli sanayi kollarından bir tanesi demir-çelik endüstrisidir.
Entegre demir çelik tesislerinde üretim için gerekli temel hammadde demir cevheri ve
kok kömürüdür. Demir cevherini ergitebilmek için gereken enerji kok kömürü ile
sağlanmaktadır. Genelde entegre tesislerde kok fabrikaları bulunmakla birlikte, son
yıllarda çevre ile ilgili kısıtlamalar paralelinde kok pazarı da gelişmiştir.
Entegre demir çelik tesislerde üretim için temel hammadde demir cevheri ve kok
kömürüdür. Gerekli enerjinin temin edilmesi için tesislerde kömürün koklaştırma
işlemine tabi tutulduğu kok fabrikası atıksuları içerdikleri birçok toksik bileşik
nedeniyle alıcı ortamda olumsuz çevresel etkilere neden olmaktadır. Proseste çok fazla
su kullanımı ise bu etkiyi daha da artırıcı bir etken olarak ön plana çıkmaktadır. Gün
geçtikçe artan sıkı deşarj limitleri, demir -çelik endüstrisi atıksuları için kullanılan
klasik arıtma sistemlerinin modifikasyonunu ve geliştirilmesini zorunlu kılmaktadır.
Kok fabrikaları atık suları genel olarak kimyasal ve biyolojik yollarla
arıtılabilmektedir. Bazı atıksu bileşenleri ve organik maddelerin tümü biyolojik arıtma
sistemleri ile yeteri kadar arıtılamamaktadır. Bu bileşenleri zararsız bir forma
dönüştürme kabiliyetine sahip ileri oksidasyon prosesleri, bu tip atıksuların arıtımında
potansiyel bir metot olarak kullanılmaktadır.
Literatürde, çok farklı endüstriyel atıksuların fenton prosesi ile arıtılabilirliği
uygulama alanı bulunmasına karşın demir-çelik endüstrisi atıksuları için yürütülmüş,
fenton prsosesinin kullanıldığı çok fazla çalışmaya rastlanmamaktadır.
Bu çalışmada; 4 kademeli bir arıtmadan geçmiş kok endüstrisi atıksularında
KOĐ, ve fenol parametrelerinin fenton oksidasyonu ile arıtılabilirliğinin incelenmesi
hedeflenmiştir. Çalışma ile elde edilecek sonuçların mevcut atıksu arıtma tesislerinin
rehabilitasyonunda da önemli veriler ortaya koyması ve bu alanda yapılan çalışmaların
bilgi birikimine katkı sağlaması beklenmektedir.
2. KAYNAK ARAŞTIRMASI
2.1. Kok Kömürü Endüstrisinin Tanımı
Đçinde bulunduğumuz yüzyılda endüstrileşmiş ülkeler içinde metalurjik kok
üretimi için yeterli ve iyi koklaşan kömür kaynakları bir sorun olma özelliğini
korumaktadır. Dünyada koklaşabilir kömür rezervinin sınırlı oluşu nedeniyle,
demir-çelik üretimi gerçekleştiren ülkeler, kok üretiminde kullandıkları kömürün büyük bir
kısmını veya tamamını dışalım yoluyla karşılamaktadır. Bu ülkeler klasik kok
fırınlarında doğrudan şarj ederek kullanılması mümkün olmayan kömürlerin metalurji
sanayinde kullanılabilmesini sağlamak amacıyla araştırmalar yapmaktadır, bunun için
değişik birçok kok prosesi geliştirmektedir.
Kömür; olduğu gibi veya yakıt olarak tam verim elde edebilmek amacıyla,
özelliklerine göre çeşitli proseslerden geçirilmek suretiyle de farklı özelliklerdeki
ürünler halinde de kullanılabilen bir yakıttır. Kömüre uygulanan başlıca prosesler
arasında düşük ve yüksek sıcaklık koklaştırması, gazlaştırma, sıvılaştırma ve briketleme
sayılabilir.
2.2. Kömür Çeşitleri ve Kok Kömürü
Kömür, bataklık alanlarda biriken bitkilerin zamanla ve sıcaklık-basınç altında,
değişim geçirmesi sonucunda oluşmuştur.
Kömür; karbon, hidrojen (%3–13), oksijen ve azottan oluşan, kükürt ve mineral
maddeler içeren, fiziksel ve kimyasal olarak farklı yapıya sahip yanabilen, sedimenter,
organik bir kayaçtır. Şekil 2.1.’de kömür çeşitleri, dünya üzerindeki kaynak durumları
ve kullanım alanları verilmiştir.
Şekil 2.1. Kömür çeşitleri ve kaynak durumları (TKĐ,2010)
Şekil 2.1.’ de görüldüğü gibi metalürjik kömür olarak da bilinen kok kömürü
demir – çelik üretiminde ısıl enerji olarak kullanılır.
Taşkömürü üretiminin %13’ü çelik endüstrisinde kullanılmaktadır.1 ton çelik
üretimi için 0,63 ton kok kömürü gerekmektedir. Kömür, çimento üretiminde ısı
kaynağı olarak kullanılmaktadır. 900 gr çimento üretimi için 450 gr kömür gereklidir.
Şekil 2.2.’de taşkömürünün sektörlere bağlı olarak kullanım oranları verilmiştir.
Şekil 2.2. Taşkömürünün Sektörler Bazında Kullanımı (Ersoy, 2007) 0% 20% 40% 60% 80% 100% 1990 1995 2000 2001 2002 2003 2004 2005 Konut Ulaştırma Sanayi Diğer Kok Fab. Santral
2.3. Koklaştırma Prosesi
Kömürlerin havasız ortamda ısıtılması sonucu, gaz (hava gazı), sıvı (kömür yağı,
kömür likörü ) ve katı (kok) olarak damıtılması işlemine koklaştırma denmektedir.
Ülkemizde demir-çelik endüstrisinde yaklaşık olarak yılda 6,5 milyon ton koklaşabilir
taşkömürü kullanılmaktadır. Koklaşma özelliği olan kömürlerden elde edilen kok,
yüksek fırın için hem gerekli ısıyı sağlayan hem de indirgeme maddesi olan birincil
hammaddedir. Üretilen kokun kalitesi ve yapısı yüksek fırın verimine etki etmektedir.
Şekil 2.3.’ de kömürden kimyasal madde üretim yöntemleri gösterilmektedir.
Şekil 2.3. Kömürden Kimyasal Madde Üretim, Yöntemleri
Kömür koklaştırma işlemi sırasında kokun yanı sıra, kok hane gazı, amonyak,
benzen ve katran gibi değerli yan ürünler ele geçer. Bu ürünlerin miktarları koklaştırılan
kömürün türüne ve koklaştırma sıcaklığına bağımlıdır.
2.4. Kok Fabrikaları Atıksuları
Entegre demir çelik tesislerde üretim için temel hammadde demir cevheri ve kok
kömürüdür. Gerekli enerjinin temin edilmesi için tesislerde kömürün koklaştırma
işlemine tabi tutulduğu kok fabrikası atıksuları içerdikleri birçok toksik bileşik
nedeniyle alıcı ortamda olumsuz çevresel etkilere neden olmaktadır. Proseste çok fazla
su kullanımı ise bu etkiyi daha da artırıcı bir etken olarak ön plana çıkmaktadır. Gün
geçtikçe artan sıkı deşarj limitleri, demir-çelik endüstrisi atıksuları için kullanılan klasik
arıtma sistemlerinin modifikasyonunu ve geliştirilmesini zorunlu kılmaktadır.
Çelik endüstrisi, gerçek anlamda aslında bir “ağır sanayi”dir. Çelik üretimi
çevresel etkileri olan bir süreçtir ve çevresel etkilerin yok edilmesi veya en aza
indirilmesi önemli miktarda yatırım gerektirmektedir. Örneğin bir milyon ton/yıl
kapasiteli bir kok fabrikasının kurulum maliyeti 200 milyon $ ise, çevre etkilerini
gidermek için gereken maliyet de yaklaşık bu kadardır. Bu durum gelişmiş ülkelerdeki
kok üretim kapasitelerinin her geçen yıl azalmasına neden olmaktadır.
Kok gazı da dahil olmak üzere kok kömürü ve yan ürünleri kömürün pirolizi ile
üretilmektedir. Süreç hemde katran, amonyak, fenol, naftalin, hafif yağ ve kükürt
çıkarılması için kok kömürü fırın gazının işleme tabi tutulmasını kapsamaktadır.
2.5. Kok Üretimi Atık Karakteristikleri
2.5.1. Gaz atıklar
Kok fırını kaçak hava emisyonlarının büyük ölçüde kaynağıdır. Koklaştırma
prosesleri, partikül madde (PM), uçucu organik bileşikler (VOC), polisiklik aromatik
hidrokarbonlar (PAH), metan (1 ton kok başına 100 g), amonyak, karbon monoksit,
hidrojen sülfür, hidrojen siyanür ve sülfür oksitleri (SO
x) gibi gaz atıkları oluşmaktadır.
Gaz iyileştirme sistemleri olmadığında her bir ton kok üretiminde, yaklaşık 0.7-7.4 kg
PM, 2.9 kg SO
x, 1.4 kg NO
x, 0.1 kg amonyak, 3 kg VOC (2 kg’ ını benzen
oluşturmaktadır) atmosfere bırakılmaktadır.
Kömür tutma işlemi partikül yükün yaklaşık %10 civarında olabilir. Kömür şarjı,
kok itme ve söndürme toz emisyonlarının önemli kaynaklarıdır.
2.5.2. Sıvı atıklar
Atıksu, kok fırın gazının soğutulmasından ve amonyak, katran, naftalin, fenol
ve hafif yağların işlenmesinden oluşmaktadır. Atıksu 10 mg/L benzen, 4 kg /ton (BOĐ
5),
içerebilmektedir. Bunlara ek olarak bu sular önemli konsantrasyonlarda poliaromatik
hidrokarbon (PAH), amonyak ve siyanür bulundurabilmektedir.
2.5.3. Katı atıklar
Kok üretim tesisleri kok kırıntıları haricinde (1 ton kok üretimi yapıldığında
yaklaşık 1 kg ) benzen ve polisiklik aromatik karbonlara benzer tehlikeli bileşikler
oluşmaktadır.
2.6. Koklaştırma Tesislerinin Atıksularının Arıtımında Uygulanan Yöntemler
Kok fabrikaları atıksuları genel olarak kimyasal ve biyolojik olarak
arıtılabilmektedir. Bazı atıksu bileşenleri ve organik maddelerin tümü biyolojik arıtma
sistemleri ile yeteri kadar arıtılamamaktadır. Bu bileşenleri zararsız bir forma
dönüştürme kabiliyetine sahip ileri oksidasyon prosesleri, bu tip atıksuların arıtımında
potansiyel bir metot olarak kullanılmaktadır (Xu ve ark., 2006). Oksidasyon ve
koagülasyon – flokülasyon basamaklarından oluşan fenton prosesi de bu metotlardan
biridir.
Đleri oksidasyon proseslerinden fenton prosesi diğer oksidasyon prosesleri ile
birlikte uygulanarak da verimi yüksek sonuçlar alınabilir.
Kok fabrikaları atıksularının öne çıkan kirletici parametreleri arasında; fenol,
amonyak, siyanür gibi aynı zamanda tehlikeli atık sınıfına da giren toksik parametreler
öne çıkmaktadır ve çoğu arıtma tesisi özellikle bu 3 parametre dikkate alınarak
tasarlanmaktadır.
Yüksek fenol kirliliği içeren atık sulardan fenolü gidermek için çeşitli ayırma
işlemleri vardır ve çoğu zaman bu metotların uygulanması birbiri içine girmektedir.
Hem fizikokimyasal hem de biyolojik arıtım yöntemleri endüstriyel ölçekli tesislerde
başarıyla uygulanmakta ve oldukça iyi arıtım verimlerinin elde edildiği bildirilmektedir.
Fenollü atıksular için genellikle, biri yıkma-yok etme prosesi prensibine, diğeri geri
kazanım veya rejenerasyona dayanan iki tip arıtım prosesi uygulanmaktadır. Fenolün
giderimi için önerilen bazı metotlar; (Xu ve ark., 2006)
•
Ekstraksiyon,
•
Adsorbsiyon,
•
Membran ayırma,
•
Biyolojik indirgeme,
•
Ozonlama,
•
Termal bozunma ,
olarak sıralanabilir.
Kömür gazlaştırma prosesi çıkış suları yüksek konsantrasyonlarda fenol
içermektedir. Yüksek
fenol konsantrasyonları olan çıkış suları mikroorganizmalar
üzerinde toksik etkiye sahiptir. Bu da klasik biyolojik yöntemlerle arıtımı
imkânsızlaştırmaktadır. Böyle durumlarda, kömür gazlaştırma atıksularındaki gibi
yüksek fenol içeriği olan atıksular ön arıtıma tabi tutulurlar. Bazen de yüksek fenol
çıkışı olan bu proseslerden fenolün hammadde olarak geri kazanılması cazip hale
gelmektedir. Ancak geri kazanım oldukça pahalı bir yöntem olmakla birlikte bu amaçla
en etkili ve en çok kullanılan metot, çözücü extraksiyonudur. Geri kazanım için
performans ve ekonomik açıdan değerli olabilecek değişik çözücü ekstraktların
denendiği pek çok çalışma yapılmaktadır (Li ve ark., 2004; Ferreira ve ark., 2005; Xu
ve ark., 2006; Yang ve ark., 2006).
Kok atıksuyu amonyak yıkama işleminden kaynaklanmaktadır. Kok atıksuyu,
SCN (tiyosiyanat) ve fenoller yanı sıra azot ve amonyum klorür yüksek
konsantrasyonda, CN
-gibi toksik bileşikleri önemli miktarlarda içeren buna rağmen ağır
metaller ve fosforu düşük konsantrasyonlarda olan karmaşık bir endüstriyel atıksudur.
Ayrıca PAH (poliaromatik hidrokarbon) ve kimyasal yapısında karbon dışında
atomlarda bulunan aromatik bileşikleri (heterosiklik) küçük miktarlarda içerir
(V´azquez ve ark., 2007).
Geleneksel, pahalı süreçler kok atıksu arıtması için kostik soda ve buhar sıyırma
eklenmesi ile kullanılmıştır. Son dönemlerde, biyolojik arıtma kirletici yükünü azaltmak
için uygulanmıştır.
Son yıllarda, çeşitli fiziko-kimyasal arıtma teknikleri adsorpsiyon, hava sıyırma,
buhar sıyırma, ıslak oksidasyon, ve biyolojik arıtma gibi teknikler verimli fenol
giderimi, elde etmek için kullanılmaya başlanmıştır (V´azquez ve ark., 2007).
Bazı arıtım metodları ile organik madde ve yüksek renk giderim verimliliği elde
edebilir, örneğin, kimyasal koagülasyon, iyon değişimi, ve aktif karbon adsorpsiyonu,
vs ancak çamur arıtmında ve bertarafında ve yüksek maliyetlidirler (Changa ve ark.,
2008).
Biyolojik arıtmadan sonra kok atıksuyu fenollü bileşikler gibi arıtımı güç olan
maddeleri içerebilmektedir. Koklaştırma biyolojik atıksu arıtma tesisinden gelen
fenoller ve KOĐ giderimini incelemek üzere yapılan çalışmada adsorbans olarak granül
aktif karbon ve reçine (XAD–2, AP–246 ve OC–1074) kullanılmıştır. En iyi sonuçlar
daha yüksek adsorpsiyon kapasiteleri sunan granül aktif karbon da, elde edilmiştir.
Denge deneyleri olarak; adsobsiyon kapasitesi her birinde ayrı olarak granül aktif
karbonda 1.48 mg, AP–246 ve OC–1074 reçineleri için ise sırasıyla 0.07 ve 0.04 mg
olarak bulunmuştur. Farklı adsorbans kullanılan deney kolonlarına ait eğriler
incelenmiştir. Denge ve kinetik deneylerde, granül aktif karbon fenol gideriminde en
iyi kapasiteyi göstermiştir (V´azquez ve ark., 2007).
Güç santralinden oluşan alt kül ile kok ve kağıt yapım atıksularından organik
kirliliğin adsorbsiyonu konusunda yapılan çalışmada KOĐ’nin gideriminde atık kül
partiküllerinin boyut ve miktarının etkisi önemini inceleyen bir çalışma sonuçlarında
kok atıksularında, küçük partikul lerde daha yüksek KOĐ gideriminin gerçekleştiğini
görülmüştür. Kok atıksuları için % 20’den % 30’lara kadar KOĐ giderim veriminin
arttığı görülmüştür. 0.074 mm den küçük ebatlarda olan kül ile KOĐ giderim verimleri
kok ve kağıt endüstrisi atıksular için sırasıyla % 45.0 ve % 40.6 olarak bulunmuştur (
Wei-ling Sun ve ark., 2007).
Magnezyum
cevherleri
ve
manganez
kullanımıyla
kok
atıksuyunun
arıtılabilirliğinin incelendiği çalışmada, mangan cevherleri ve magnezyum kullanılarak
iki aşamada kok atıksularından tipik kirleticilerin giderimi analiz edilmiştir. Asidik
koşullar altında mangan cevheri ile doldurulmuş oksitlenme yeteneği olan bir reaktör
kok atıksuyundan güçlü uçucu fenolleri yok etme, KOĐ, sülfit gideriminde etkili
olmuştur. Mangan cevheri, azot ve fosfat gideriminde çıkış suyuna yardımcı olmaktadır.
Atıksu pH’sı 1.2’ye ayarlandığında, KOĐ, uçucu fenol, ve sülfit için giderim verimleri
sırasıyla 70%, 99% ve 100% olarak bulunmuştur (Chen ve ark., 2009).
Kömür gazlaştırma proseslerinin arıtılmasında yeni tekniklerin incelendiği başka
bir çalışmada ise bu tekniklerin özellikle temiz üretim için önemli ortaya çıkmıştır.
Kömür gazlaştırma atıksu arıtım proseslerinde 3 teknik vardır. Đlk olarak fenol geri
kazanımından önce atıksuyun pH’ ını düşürmek ve fenol giderim performansını
artırmak için amonyak sıyırma yapılır. Đkinci olarak amonyak sıyırıcı ve gaz sıyırıcılar
konulmaktadır. Bu, amonyak sıyırma, karbon dioksit ve hidrojen sülfür giderim
performansını artırmak için yapılır.
Bu metot ile, karbon dioksit, hidrojen sülfür ve atıksu içinde amonyak
konsantrasyonu giderimleri gerçekleşmektedir. Sonuç olarak, atıksuyun pH değeri 9’
dan 7’ ye indirilir böylece fenol giderim performansı önemli ölçüde artırılmaktadır. Bu
yöntem ile karbon dioksit, % 60 oranından % 96 ’a, amonyak için% 96’ dan % 99. 6,
fenol için ise % 80’ dan % 94’ lara çıkan arıtma verimleri saptanmıştır. Buna ek olarak,
atıksuyun biyolojik arıtımı daha kolay olmaktadır. Ekonomik analizler ile, bu prosesin
işletme maliyeti bundan mevcut prosesinden daha ekonomik olacağı da belirtilmiştir
(Gai ve ark., 2007).
Başka bir araştırmacı tarafından ise koagülasyon ve sıfır değerli demir prosesi ile
kok atıksularının ileri arıtımı incelenmiştir. Sonuçlar demir tozunun Kok atıksuyunun
ileri arıtımı için koagülasyondan daha etkili olduğunu göstermiştir (Lai ve ark., 2007).
Yener ve Aksu (1999), aktif karbon ve kurutulmuş aktif çamur üzerine fenol ve
fenol türlerinin adsorpsiyonunda, 500 mg/L fenol konsantrasyonu için sırasıyla %25 ve
% 21 verim elde edebilmişlerdir. 25 mg/L fenol için dahi en yüksek verimi %76 olarak
belirlemişlerdir. Özbelge ve ark. (2002),
kauçuk ve tekstil endüstrisi atıksularından
fenolik bileşiklerin gideriminde, fiziko-kimyasal yöntemler ile fenolün koagülasyonu
için farklı tipte koagülantlar kullanarak, en yüksek 765 mg/L fenolik bileşik içeren
besleme atıksuyunu % 95 verimle uzaklaştırmışlardır.
Sıvı membranla ayırma, katı membranlı ekstraksiyon, elektrokimyasal
oksidasyon ve ozonlama gibi değişik işlemler kullanılmasına rağmen fenolün arıtımı
için en çok kullanılan yöntem biyolojik arıtımdır.
Biyolojik arıtma tesislerine eğilimin artması ile birlikte yüksek verimli
teknolojilerde hızla gelişmektedir. Fenol giderim oranı yük artmasıyla hızla
düşmektedir. Ancak yükleme ayarlandığında aktif çamur tesislerinde fenolü tam olarak
arıtmak mümkündür.
Adsorpsiyon ve çözücü extraksiyonu kirleticinin bir fazdan diğer faza transfer
edildiği, kimyasal oksidasyon ise genellikle dönüşümün yetersiz olduğu yöntemlerdir.
Fenolik bileşikleri arıtmak için biyolojik metotlar, fenolün tam mineralizasyonunun
gerçekleştiği ve çevresel açıdan kabul edilir son ürünlerin oluştuğu, nispeten düşük
maliyetleri ile tercih edilmektedirler.
Foto-fenton prosesinin ön arıtma kademesi olarak kullanımının, diğer
fotokimyasal proseslerden daha etkili olduğu belirlenmiştir. En önemli avantajı ise çok
kısa sürelerde fenolün parçalanmasının ve minerilizasyonunun gerçekleşmesidir. Ayrıca
ileri oksidasyon proseslerinin biyolojik arıtma ünitesinin stabilitesinin arttırılması ve
özellikle toksik endüstriyel atıksuların giderme verimlerinin iyileştirilebilmesinin
mümkün olacağı beklenmektedir (Çatalkaya ve ark., 2004).
Kimyasal olarak arıtma işlemlerinin esası defonolizasyondur. Yüksek
konsantrasyonlarda fenol içeren atıksulardan fenolü gidermek için çeşitli ayırma
işlemleri uygulanmaktadır. Bu işlemler; NaOH ile ekstraksiyon, aktif karbon ile
adsorpsiyon ve kimyasal oksidasyon olarak kısaca özetlenebilir.
Đleri oksidasyon prosesleri fenol gibi toksik ve kalıcı özellikteki organik madde
içeren atıksuların arıtımında oldukça etkili yöntemler olarak önem kazanmaktadır. ĐOP
yöntemleri oldukça etkili hidroksil redikallerin (Mastern ve diğ., 1994) oluşumuna
dayalı bir yöntem olup, toksik ve kalıcı özellikteki organik maddeleri zararsız son
ürünlere dönüştürebilmektedir (Esplugas ve diğ., 1994). Hidroksil redikalleri hemen
hemen hiç organik madde ayrımı yapmadan reaksiyona girmektedir(Buxton ve diğ.,
1988). Hidroksil redikalleri oksidasyon reaksiyonlarının gerçekleşmesine, kirletici
organik maddenin tamamen minerilizasyona uğramasına, CO
2ve H
2O gibi son
ürünlerin oluşmasına neden olmaktadır (Legrini ve ark., 1993).
Fizikokimyasal yöntemler (koagülasyon-floklaştırma, filtrasyon, aktif karbon
adsorpsiyonu, hava ile sıyırma) ise etkili olmalarına rağmen, kirleticinin bir ortamdan
başka bir ortama geçirilmesinden dolayı pek tercih edilmemektedir. Đleri oksidasyon
prosesleri (ĐOP), bu tür kirleticilerin arıtımında oldukça etkili yöntemler olarak son
yıllarda önem kazanmaktadır.
Fenol ve klorofenollerin yoğun şekilde kullanımı, yeraltı ve yüzeysel sularda
değişik konsantrasyonlarda fenol ve klorofenol kirliliğine neden olduğu ortaya çıkınca
UV/H
2O
2prosesi ile fenol arıtımında, H
2O
2/fenol oranının oldukça etkili olduğu, bu
oranın 100–250 aralığında daha verimli olduğu başka bir çalışmada belirtilmiştir. pH
değişiminin ise verime etkisi olmadığı belirtilmiştir. Ayrıca H
2O
2dozundaki artışın hep
verim artışına neden olmadığı, belli bir dozdan sonra inhibe etkisi olduğu gözlenmiştir
(Alnaizy ve Akgerman 2000).
Foto-Fenton yöntemi, fenol gideriminde oldukça etkili olup, fenolün biyolojik
parçalanabilirliğini arttırmakta ve toksisitesini azalttığı sonucuna varılmıştır. Ayrıca,
arıtma esnasında biyolojik arıtma öncesi Fenton/Foto-Fenton prosesinin ön arıtma
olarak kullanılması önerilmektedir (Maletzky ve Bauer 1998).
Montaser (2001) tarafından yılında yapılan çalışmada ise fenolik maddelerin
asidik ortamda fenton prosesi ile kısa sürelere arıtılabildiği belirtilmiştir.
Foto-Fenton yöntemi, fenol gideriminde oldukça etkili olup, fenolün biyolojik
parçalanabilirliğini arttırmakta ve toksisitesini azaltmaktadır. Ayrıca, arıtma esnasında
biyolojik arıtma öncesi Fenton / Foto-Fenton prosesinin ön arıtma olarak kullanılması
önerilmektedir. Fenolik maddelerin asidik ortamda Foto-fenton prosesi ile kısa sürelere
arıtılabildiği belirtilmiştir. Yüksek organik yüke ve kalıcı, biyolojik olarak
parçalanamayan ve toksik özelliklere sahip atık sulardan; organik madde, koku ve renk
giderimi için biyolojik arıtımdan önce veya sonra ileri oksidasyon proseslerine dayanan
kimyasal prosesler kullanılmaktadır. Fenton proses, bir ileri oksidasyon prosesi olup
diğer oksidasyon proseslerine göre basit, ekonomik ve kısa reaksiyon zamanı
gerektirmesi gibi birçok avantaja sahiptir. Fenton proses, sahip olduğu bu avantajlardan
dolayı bir çok alanda uygulanmaktadır (Gürtekin ve Şekerdağ, 2008).
Fenol içerikli atıksuların arıtımında düşük pH, 0,02g/mL katı/sıvı oranı, bir saatlik
süre ve 35°C adsorpsiyon sıcaklığı optimum giderim için uygun olduğu bulunmuştur.
Bu deneysel şartlar sağlandığında, fenolde %59 oranında giderim sağlanırken,
türbiditenin (bulanıklılık) 79,6 mg/L' den 23,5 mg/L' ye düştüğü görülmektedir. Sonuç
olarak, perlit mineralinin düşük maliyetli, herhangi bir çevresel kirlilik oluşturmaması
ve temini kolay malzeme olması gibi özellikler göz önüne alındığında, kâğıt atık
suyunun arıtımı için alternatif adsorbent olabileceği düşünülmektedir (Uğurlu, 2003).
Fenol, 2,4- diklorofenol organik maddelerini içeren sentetik atıksuyun ileri
oksidasyon prosesleri (UV/ H
2O
2, Fenton ve Foto-Fenton) ile arıtılabilirliğinin
incelendiği çalışmada, Fenton prosesinin fenol içeren atıksuların arıtımında oldukça
etkili olduğu ve 120 dakikalık reaksiyon süresinde fenol parçalanmasının tamamen
gerçekleştiği saptanmıştır. Buna karşılık fenolün tamamen parçalanabilmesi için gerekli
olan süre Foto-Fenton prosesi ile 2,5–5 dakikalık reaksiyon süresine düşürülmüştür
(Çokay ve Sengül, 2006).
Fenol ve klorofenollerin yoğun şekilde kullanımı, yeraltı ve yüzeysel sularda
değişik konsantrasyonlarda fenol ve klorofenol kirliliğine neden olmaktadır. Ayrıca
H
2O
2dozundaki artışın hep verim artışına neden olmadığı, belli bir dozdan sonra inhibe
etkisi olduğu gözlenmiştir. Đleri oksidasyon prosesleri ile çeşitli parametrelerin (hidrojen
peroksit ve demir (II) konsantrasyonu ve H
2O
2/fenol molar oranı) atıksularda bulunan
fenol türevlerinin parçalanmasına ve mineralizasyonuna olan etkisi gözlenmiş ve
yorumlanmıştır. Direkt H
2O
2ile oksidasyon yönteminde, fenol türevlerinin
parçalanması yavaş hızla gerçekleşirken, mineralizasyonunda iyi bir verim elde
edilememiştir. UV / H
2O
2prosesinde ise, fenol türevleri tamamen parçalanırken,
duyulmaktadır. 300 dakikalık reaksiyon süresinde, %30 - %55 mineralizasyon giderim
verimi gözlenmiştir (Şengül ve ark., 2006).
2.7. Fenton Oksidasyonu Đle Arıtım Yönteminin Genel Esasları
Fenton metodu, 1894 yılında H.J.H. Fenton tarafından keşfedilmiş bir metottur.
Fe
+2ve hidrojen peroksit (H
2O
2) arasındaki reaksiyonu açıklamıştır. Zincirleme
reaksiyonlar sonucu hidroksil radikallerinin meydana geldiğini belirtmiştir. Oluşan
hidroksil radikalleri oldukça yüksek oksitleme gücüne sahiptirler. Hidrojen
peroksitferro iyonu sistemi “Fenton reaktifi” olarak bilinmektedir (Spetch ve ark.,
1996). Endüstriyel atıksuların arıtımında biyolojik prosesler geniş uygulama imkânı
bulmasına karşın, biyolojik kalıcı organik maddelerin hızlı gideriminin beklendiği
sistemler için ileri oksidasyon prosesleri (ĐOP) daha uygun hale gelmektedir. Fenton
oksidasyonu da biyolojik ve kalıcı organik kirleticilerin gideriminin sağlandığı ĐOP
olarak kullanılabilmektedir (Bidga, 1995; Teel ve.diğ., 2001).
Atıksu arıtma tekniği olarak kullanılan Fenton prosesi, atıksu içerisinde
oksitlenebilir formda bulunan maddelerin gideriminde, giderilen madde türüne bağlı
olarak etkin bir şekilde kullanılmaktadır. Fenton reaksiyonu, atıksu için tanımlanan
KOĐ, toksisite ve renk gibi kolektif parametrelerin gideriminde ve biyolojik olarak
parçalanabilirliğin artırılmasında etkili olabilmektedir. Fenton metoduyla yapılan arıtma
işlemi aşağıdaki sırada gerçekleşmektedir (Kang and Hwang, 2000).
•
Öncelikle asidik koşullar sağlanır. Bunun için uygun pH aralığı 2–5 arasındadır.
•
Önce Fe
2+tuzları, sonra hidrojen peroksit ilave edilerek, hidroksil radikalleri
oluşturulur. Oksidasyonla organik yüksek moleküllü maddeler daha düşük
ağırlıktaki moleküllere dönüşür. Fe
2+bu esnada Fe
3+‘e yükseltgenir.
•
Reaksiyondan sonra, kireç veya sodyum hidroksit ile nötralizasyon yapılarak
ortam pH’ı Fe
3+floklarının en uygun çökelebilme aralığı olan pH 7- 8’e getirilir.
•
Nötralizasyon sonrasında ortamdaki Fe
3+floklarının yeterince çökebilmesinin
temin edildiği bir bekleme süresinin sonunda oluşan duru faz, çamurdan ayrılır.
Aydın ve ark.’ na (2002) göre fenton oksidasyonu, yüksek miktarda kalıcı
organik ve yüksek renk içeriğine sahip biyolojik arıtma görmüş çıkış sularının
arıtımında ve özellikle bu atıksu tipi için çok uygun bir arıtma teknolojisidir.
2.7.1. Fenton prosesinde oluşan kimyasal reaksiyonlar
Fenton reaksiyonu iki prosese ayrılabilir. Đlk proses düşük pH değerinde ( pH
2-5) başlangıç reaksiyonudur. Đkinci proses yüksek pH değerinde (pH 7–8) gerçekleşen
koagülasyondur. Fenton yöntemindeki kimyasal reaksiyonlar aşağıdaki gibidir:
Fenton oksidasyonu reaksiyonunun temeli yüksek oksitleme kapasitesine sahip
OH
-radikallerinin oluşumudur. Fe
2+ve hidrojen peroksidin redoks reaksiyonları asidik
koşullarda daha kararlıdır. Fenton oksidasyonu için en uygun değer olan pH 3–4 değeri
sürekli kontrol edilerek stabil kalması sağlanmalıdır (Kang ve Hwang, 2000; Neyens ve
Baeyens, 2003).
Fe
+2ve hidrojen peroksitin (H
2O
2) redoks reaksiyonları asidik koşullarda daha
kararlıdır. Organik maddelerin ve ferrus iyonlarının var olduğu bir su ortamına hidrojen
peroksit verildiğinde aşağıdaki kompleks reaksiyonlar meydana gelir (Walling ve Kato,
1971).
Fe
+2+ H
2O
2→
Fe
+3+ OH
-+ HOֹ
R-H + HOֹ → Rֹ+ H
2O
Rֹ
+ H
2O
2→
ROH + HO
.Fe
+2+ HOֹ
→ Fe
+3+ OH
-Fenton oksidasyonu, reaksiyon esnasında yüksek oksitleme kapasitesine sahip
hidroksil radikallerinin oluşumunu destekleyen ve aşağıdaki denklemle ifade edilen
kimyasal mekanizmalar içermektedir (Chamarro ve ark., 2001).
Fe
2++H
2O
2→ Fe
3++ OH
-+OHֹ (2.1)
Ortamdaki Fe
2+hidroksil radikallerinin diğer bir reaksiyonuyla Fe
3+’e yükseltgenir.
RH + OH ֹ → Rֹ + H
2O (2.2)
R ֹ + Fe
3+→ R
++Fe
2+(2.3)
Fe
2++OHֹ→ OH
-+ Fe
3+(2.4)
Fe
3+‘ün katalitik etkisiyle aşağıda belirtilen hidroksil ve hidroperoksil radikal
oluşum mekanizmaları ile hidrojen peroksit bozunur.
Fe
3++ H
2O
2→ Fe-OOH
2++H
+(2.5)
Fe-OOH
2+→Fe
2++ HO
2ֹ
(2.6)
Fe
2++ HO
2→ Fe
3++ HO
2-(2.7)
Fe
3++ HO
2→ Fe
2++ H
++ O
2(2.8)
2.7.2. Koagülasyon reaksiyonları
Organik maddelerin parçalanarak ürünlere dönüşmesi renk giderimi açısından da
avantaj sağlamaktadır. Demir iyonları suya verildiği zaman hidroksil iyonları ve ferrik
hidroksi kompleksleri oluşturur ve aşağıdaki koagülasyon reaksiyonları oluşur (Kuo,
1992). Şekil 2.4’de fenton prosesinin uygulanması gösterilmiştir.
[Fe (H
2O)
6]
3++ H
2O → [Fe(H
2O)
5OH]
2++ H
3O
+(2.10)
[Fe(H
2O)
5OH]
2++ H
2O → [Fe (H
2O)
4(OH)
2]4+ + H
3O
+(2.11)
2[Fe(H
2O)
5OH]
2+→ [Fe
2(H
2O)
8(OH)
2]
4++ 2 H
2O (2.12)
[Fe
2(H
2O)
8(OH)
2]
4++ H
2O → [Fe
2(H
2O)
7(OH)
3]
3++ H
3O
+(2.13)
[Fe:(H;O)
7(OH)
3]
3++ [Fe(H
2O)
5OH]
2+→ [Fe
3(H
2O)
5(OH)
4]
5++ 2 H
2O (2.14)
2.8. Fenton Prosesine Etki Eden Faktörler
pH, demir sülfat ve hidrojen peroksit ve sıcaklık miktarlarındaki değişiklikler
fenton prosesinin arıtma verimliliğini etkileyen parametrelerdir.
2.8.1. pH etkisi
Asidik koşullarda redoks sistemi daha iyidir. Bazik bölgede verimin düşmesi;
sulu Fe
2+iyonunun Fe
3+kolloidlerine dönüşerek katalitik etkinliğini kaybetmesi
şeklinde açıklanır. pH değeri 3,5’tan düşük olduğu zaman, hidrojen peroksit ve Fe
2+daha kararlıdır. Fe
2+iyonları pH değeri 4’den yüksek olduğunda kararsızdır ve kolayca
demir hidrokso kompleksleri üretmeye meyilli demir iyonları oluştururlar. Yüksek pH
değerlerinde hidrojen peroksit, oksitleme yeteneği azaldığından kararsızdır (Buxton ve
ark, 1988). Fe
2+iyonları ve hidrojen peroksidin kararsızlığı redoks sistemini
etkilemektedir. FeSO
4ilavesi ile pH değerinde düşme meydana gelir. Bunun sebebi
içerisinde serbest halde H
2SO
4bulundurmasıdır. H
2O
2ilavesi ile pH’da daha büyük bir
düşme meydana gelir. Organik maddelerin organik asitlere parçalanması da pH’nın
düşmesine yol açar (Alnaizy ve ark; 2000). pH’ın değişimi sık sık kontrol edilerek
reaksiyonun istenen düzeyde yürümesi sağlanmalıdır. pH’da düşme meydana
gelmiyorsa H
2O
2’nin reaksiyonu inhibe edici tepkimelere meylettiği ifade edilebilir.
2.8.2. Sıcaklık etkisi
Yüksek sıcaklıkta giderim düşük sıcaklıktakinden daha iyi gerçekleşmektedir.
Sıcaklık hidrojen peroksidin dönüşüm süresinde etkilidir. Reaksiyonda sıcaklık arttıkça
reaksiyon süresi azalır. Reaksiyon ilerleyen safhalarda sıcaklığın yükselmesine neden
olabilir. Fenton uygulaması için uygun sıcaklık aralığı 20–40 °C’dir (Maletzky ve ark;
1998).
2.8.3. Demir sülfat miktarının etkisi
Demir iyonu yokluğunda ortamda hidroksil radikalini üretecek temel faktör
bulunmadığından
fenton
reaksiyonuna
dayalı
etkin
bir
oksidasyon
gerçekleşmemektedir. Demir sülfat dozunun artması veya azalması giderme veriminde
etkilidir. Daha yüksek dozaj, daha iyi etki demektir. Demir sülfat dozunun artması,
redoks reaksiyonunun tamamlanmasına ve koagülasyona sebep olur. Ortamdaki demir
konsantrasyonu arttıkça reaksiyonun hızı artmaktadır. Ancak öyle bir konsantrasyona
ulaşılır ki bundan sonra ilave edilen demir iyonu verimi artırıcı etkide bulunamaz (Bali
ve ark; 2003).
2.8.4. Hidrojen peroksit miktarının etkisi
Hidrojen peroksit fazla miktarda kullanıldığında giderme verimi yüksek, az
miktarda kullanıldığında ise düşüktür. Arıtılmış suda hidrojen peroksit kalması girişim
yaparak KOĐ değerinin artmasına neden olmaktadır. Yüksek miktarda ihtiyaç fazlası
hidrojen peroksidin suda bulunması, yüksek KOĐ’ ye neden olmaktadır (Ancı, 2000).
Hidrojen peroksit fazla miktarda kullanıldığında renk giderme verimi yüksek, az
miktarda kullanıldığında ise düşüktür (Yang ve ark.; 1998).
Ağır kirlilik yüküne sahip
kirli sularda başlangıçtaki demir ve hidrojen peroksit konsantrasyonunu yüksek tutmak
reaksiyon performansı açısından fayda sağlamaktadır. Ancak artan oksidan
konsantrasyonu arıtımı belli bir değere kadar olumlu etkilerken; belli bir
konsantrasyondan sonra aşırı H
2O
2’nin OH. radikalleri ile reaksiyona girerek (denklem
15) oksidasyon verimini önemli derecede düşürdüğü gözlemlenmiştir (Buxton ve ark.,
1988).
H
2O
2+ֹOH →HO
2+ H
2O (2.15)
Yukarıda verilen reaksiyona göre oluşan HO
2ֹserbest radikali de zincir
reaksiyonlarını devam ettirir, ancak OHֹ radikaline göre daha düşük bir oksidan
potansiyeline sahiptir. Bu nedenle arıtım performansını, başka bir deyişle KOĐ giderim
verimini arttırmak için H
2O
2konsantrasyonunun uygun bir değere ayarlanması çok
önemlidir (Tuhkanen, 2005). Ayrıca arıtılmış suda hidrojen peroksit kalması KOĐ
analizlerine pozitif girişim yaparak KOĐ değerinin artmasına neden olmaktadır
(Acarbacan, 2002).
2.8.5. Demir iyonu türünün etkisi
Ortamda reaksiyon için yeteri kadar organik madde ve H
2O
2bulunması
durumunda katalitik dönüşüm zinciri derhal başlar. Düşük hidrojen peroksit
konsantrasyonların da (örneğin 10–25 mg/L H
2O
2değerinden küçük) Fe
2+’nin daha
başarılı olduğu gözlemlenmiştir (Pignatello, 1992).
2.9. Fenton Oksidasyonunun Modifikasyonları
Son yıllarda enton prosesinin verimini artırmak ve maliyeti azaltmak amacıyla
bir takım modifikasyonlar geliştirilmiştir. Bunlar, Foto-Fenton (FF) ve Elektro-Fenton
(EF) ‘ dur.
2.9.1. Foto - fenton prosesi
Fenton oksidasyonunun bu modifikasyonunda katalizör olarak UV ışınları
kullanılmaktadır. Bu sistemde UV ışınları Fenton reaksiyonlarına hız kazandırmakta ve
Fe
+3türlerinin foto indirgenmesi sonucu Fe
+2miktarının artmasına yardımcı olmaktadır
(Brillas ve ark. 2003). Maksimum absorpsiyon dalga boyunun 400 nm’den daha düşük
olması nedeniyle aşağıdaki reaksiyon UV ışınlarının mevcudiyeti halinde
gerçekleşmektedir (Reaksiyon 16) (Xie ve ark. 2000).
Fe
+3+ hv + H
2O → Fe
+2+ OHֹ+ H
+(2.16)
UV ışınlarının fenton uygulamasına olan pozitif etkileri literatürde birçok
çalışma da belirtilmiştir. Bir örnek olarak, farklı ışın yoğunluklarında fenton uygulaması
yapılmış olan bir çalışmada EQ 1023-4Z H.Peschl, civa orta basınç lambası kullanılarak
160 kW/m
3’lük UV ışın yoğunluğunda TOK gideriminde %70’lik bir verim elde
edilmiştir. Aynı deney karanlıkta tekrarlandığında verimin %17 mertebesinde kaldığı
gözlemlenmiştir (Suri ve ark.; 1993). Buradan açıkça UV ışınlı ortamın Fenton
reaksiyonunun verimini artırdığı görülmektedir. Demir katalizör bulunmasa dahi UV
ışınları H
2O
2’den hidroksil radikalleri oluşmasını sağlayabilmektedir (Ruppert ve
2.9.2. Elektro-fenton prosesi
Fenton
prosesinin
ikinci
modifikasyonu
elektro-fenton
(EF)
olarak
adlandırılmaktadır ve üç farklı türü mevcuttur (Chou ve ark., 1999). EF uygulamalarının
en önemli avantajı düşük çamur miktarı ve kimyasal ihtiyacı olmakla birlikte uygun
elektrot seçimi ve enerji ihtiyacı önemli konulardır.
2.10. Fenton ile Oksidasyon Đleri Arıtım Yönteminin Avantaj ve Dezavantajları
Bu yöntem oksidasyon ve koagülasyon proseslerinin avantajlarına sahip olup
sudaki oksijen miktarını da arttırmaktadır. Çizelge 2.2.’da Fenton metodunun
avantajları ve dezavantajları verilmiştir (Flaherty ve Huang, 1992).
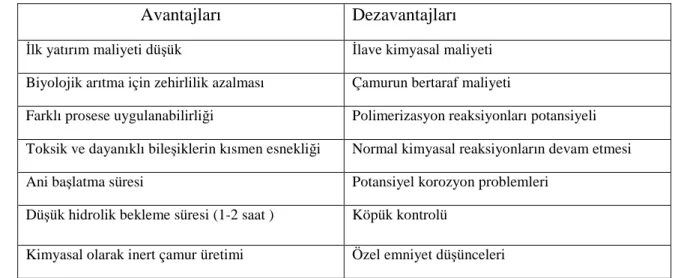
Çizelge 2.1. Fenton metodunun avantajları ve dezavantajları
Avantajları
Dezavantajları
Đlk yatırım maliyeti düşük Đlave kimyasal maliyeti
Biyolojik arıtma için zehirlilik azalması Çamurun bertaraf maliyeti
Farklı prosese uygulanabilirliği Polimerizasyon reaksiyonları potansiyeli Toksik ve dayanıklı bileşiklerin kısmen esnekliği Normal kimyasal reaksiyonların devam etmesi
Ani başlatma süresi Potansiyel korozyon problemleri
Düşük hidrolik bekleme süresi (1-2 saat ) Köpük kontrolü
Kimyasal olarak inert çamur üretimi Özel emniyet düşünceleri
2.11. Fenton Oksidasyonu ile KOĐ Giderimi Uygulama Örnekleri
Literatür incelendiğinde fenton oksidasyonunun pek çok kirletici parametrenin
arıtımı için kullanılmış olduğu görülmektedir.
Meriç, S. ve diğ., (2004), sentetik atıksudan toksisiteye neden olan RB5 (
Reactive Black 5) uzaklaştırmak için Fenton oksidasyonunu kullanmışlardır.
Çalışmaları sırasında belirledikleri optimum koşullar altında %71–88 KOĐ giderimi ve
% 99 renk giderimi sağlamışlardır.
Aydın A.F. ve diğ., (2002), yüksek KOĐ, koyu renk ve biyolojik olarak
parçalanamayan afyon alkoloidleri endüstrisi atıksuları için fenton oksidasyonun
uygulanabilirliğini araştırmışlar ve fenton oksidasyonu ile %90 KOĐ giderimi, %95 renk
giderimi sağlamışlardır.
Tekin H. ve diğ., (2005), ilaç atıksuyunun biyolojik parçalanabilirliğini arttırmak
amaçlı fenton oksidasyonunu ön arıtım olarak kullanmışlardır. Yaptıkları çalışmada
fenton oksidasyonu sonucu % 45- % 65 değerleri arasında KOĐ giderim verimi elde
etmişlerdir
Bae. Kini ve ark., (1997), çöp sızıntı sularının arıtımında, aktif çamur sisteminde
amonyağı nitrifikasyon ve denitrifikasyonla giderdikten sonra, KOĐ giderimi için
Fenton metodunu uygulamışlardır.
Fenton ayıracıyla yapılan ön oksidasyon prosesinde renk giderim hızının KOĐ
giderim hızına göre daha yüksek olduğu renk ile KOĐ gideriminin büyük bir kısmının ön
oksidasyon basamağında gerçekleştiği belirlenmiştir (Kang ve ark.; 1997).
Benatti ve ark., (1984) yaptıkları çalışmalarda Response surface metodunu
kullanarak kimyasal atıksuyun fenton oksidasyonuyla optimizasyon çalışmalarını
yapmışlardır; hidrojen peroksit ve demir varlığında pH= 4 değerinde sürekli kontrol
altında tutularak, [KOĐ]:[ H
2O
2]= 1: 9 ve [H
2O
2] : [Fe
2+]= 4.5:1 oranlarında % 92.3 KOĐ
giderim verimi elde etmişlerdir.
Kank ve ark. (2000) yılında tekstil atıksularında renk giderimi için fenton
metodu denemişlerdir. Optimum pH 3,5 ta Fe
+2dozu 20 mg/L ve H
2O
2dozu 100mg/L
olarak kullanmışlar 30 dk reaksiyon süresi sonunda renk giderimi %96 olmasına rağmen
KOĐ giderim verimi %36 olarak kalmıştır.
Huang ve ark. (1999) yılında petrokimyasal atıksularda fenton ve elektro-fenton
yönteminin uygulanabilirliğini araştırmışlar ve sonuçları mukayese etmişlerdir.
Çalışmalar neticesinde iki fenton uygulamasında da Optimum pH=3,5 Fe
+2dozu =1200
mg/L ve H
2O
2dozu = 600mg/L olarak kullanılmıştır. Klasik fenton uygulamasında KOĐ
giderim verimi %35 elektro-fenton uygulamasında ise KOĐ giderim verimi % 86 olarak
bulunmuştur.
Lau ve ark. (2001) yılında yaptıkları çalışmalarında klasik fenton yöntemiyle
sızıntı sularının arıtılabilirliğini araştırmışlardır. 1g KOI basına 0,28 g Fe
+2ve 0,18 g
H
2O
2kullanılmasını önermişlerdir. Ayrıca optimum Fe
+2dozu =300 mg/L ve H
2O
2dozu = 200 mg/L olarak bulmuşlardır. Bu şartlar altında fenton uygulamasında KOĐ
girişi 15700 mg/L iken KOĐ çıkısı 447 mg/L kadar düşmüştür.
Sheu ve ark. (2001) tarafından yapılan çalışmalarda üretim sırasında kostik
kullanan bir olefin tesisi atıksuyunun arıtımı incelenmiştir. Çalışma sonucunda elde
edilen optimum pH= 1,8–2,4 optimum reaksiyon süresi 50 dk optimum sıcaklık 90 C
optimum Fe
+2dozu =200 mg/L ve H
2O
2/ KOĐ oranı = 1/1 olarak bulunmuştur. Bu
şartlar altında KOĐ giderme verimi % 99,5 elde edilmiştir.
Martinez ve diğ. 2003 yılında yaptıkları çalışmada KOĐ değeri oldukça yüksek
(362000 mg/L) ilaç atıksuyuna ön arıtma olarak fenton prosesini uygulamışlardır.
Đyonları Fe
+2ve H
2O
2konsantrasyonlarının yanında sıcaklık parametresini de optimize
ettiklerinde KOĐ giderimin de % 56,4 verim elde etmişlerdir.
Lau ve ark. (2001) anaerobik olarak arıtılmış sızıntı sularından Fenton
koagülasyon prosesi ile organik madde giderimini araştırmışlardır. Çalışmada sızıntı
suyunun anaerobik arıtımında reaktör olarak yukarı akışlı anaerobik çamur yatağı
kullanılmıştır. Bu şekilde arıtılan atıksuya Fenton prosesi ile ileri arıtım
uygulamışlardır. 200 mg/L H
2O
2ve 300 mg/L FeSO
4ile anaerobik olarak arıtılan
atıksuda kalan KOĐ ’nin % 70’i giderilmiştir. Fenton oksidasyonu ile KOĐ’ nin % 14’ü
giderilirken, koagülasyonla geriye kalan % 56’sının azaldığını tespit etmişlerdir.
Huang ve ark. 2001 yılında yaptıkları çalışmalarda yüksek kirlilik içeren bir
atıksuyun elektro-fentonla arıtımını incelemişler ve çalışmalar sonucunda %98 lik bir
KOĐ giderim verimi elde etmişlerdir.
2.12. Fenol ve Yapısı
Fenol benzen halkasına OH
-molekülünün bağlanmasıyla oluşur. Fenoller,
aromatik halkaya bir ya da daha fazla hidroksil grubunun bağlandığı aromatik
bileşiklerdir. Saf halde, renksiz veya beyazdan hafifçe pembeye çalan renkte kristal katı
şeklindedir. Tatlımsı, buruk bir kokuya sahip fenollerin tespit limiti havada 40 ppb, suda
ise 1–8 ppm’dir. Suya kıyasla çok yavaş buharlaşır, suda orta dereceli bir çözünürlüğe
sahiptir ve oldukça yanıcıdır.
Fenol, karbonik asit veya hidroksil benzen de denilen, çok yönlü organik bir
bileşiktir.
Doğal olarak kömür katranında bulunur ve buradan elde edilir. Klor benzene
sodyum hidroksit etki ettirilerek elde edilir. Katalizör olarak bakır kullanılır. Ayrıca
anilinden de elde edilir.
Fenoller benzenin hidroksi türevleri olarak isimlendirilir. Evsel ve endüstriyel
atıksularda, doğal sularda ve içme suyu temini amacı ile kullanılan sularda
bulunabilirler. Bu tip suların klorlanması kokulu ve hoş olmayan tatta klorofenollerin
oluşmasına neden olur.
Fenol ve bağlı fenoller çevre kirlenmesi açısından önemli yer tutmaktadır. Bu
kimyasallar, plastikler, boyalar, ilaç ve antioksidan üretimi, kağıt ve kağıt hamuru gibi
pek çok endüstriyel sürecin bir bileşeni olarak karsımıza çıkmaktadır. Pek çok fenol
bileşiği biyolojik sistemler üzerinde zehirli ve tehlikeli etkiye sahip olup sular
vasıtasıyla besin zincirine girmektedir. Fenollerin 1 ppb’den düşük seviyeleri bile suyun
tat ve koku özelliklerini değiştirebilmektedir. Endüstriyel atıkların yüzey sularına
karışması ile tabiatta doğal fenol polimerlerinin biyolojik parçalanma dengesi de
olumsuz yönde etkilenmektedir.
Bu anlamda daha çok çiftlik atıkları içerisinde bulunan humik asit, tannin ve
lignin gibi doğal fenol polimeri yapılara ek olarak çeşitli pestisitlerden organofosforlu
insektisitler, klorlu fenoksi asitlerin parçalanma ürünleri olarak klorlu ve nitrolu
bileşikler sulara karışmaktadır. Şekil 2.5.’de fenolün aromatik yapısını da gösteren fenol
halkası gösterilmiştir.
3. MATERYAL VE METOT
3.1. Atıksu ve Özellikleri
Kok endüstrisi atıksularının fenton oksidasyonu ile arıtılabilirliği üzerine
yapılmış olan bu çalışmada Karabük ilinde faaliyet gösteren entegre demir çelik
fabrikasının (KARDEMĐR) koklaştırma birimine ait arıtma tesisinin biyolojik ünite
çıkışından temin edilmiştir. Deneysel çalışmalarda kullanılan atıksu karakteristiği
aşağıda Çizelge 3.1.’de verilmiştir. Atıksuyun deneyler sırasında bozulmasını önlemek
amacıyla 4 °C ve karanlıkta muhafaza edilmiş ve herhangi bir seyreltme olmadan
kullanılmıştır.
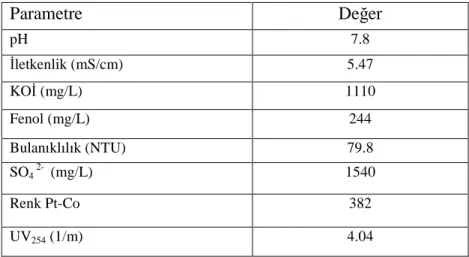
Çizelge 3.1. Biyolojik ünite çıkışı atıksu karakteristiği
Kok fabrikası atıksu kaynağı kömürün doğal nemidir ( %10 – 12 ). Koklaşma
prosesi gereği kapalı ortamda ısıtılan kömürün bünyesindeki nem önce buharlaşıp tekrar
yoğunlaşarak kapalı ortamda katranla beraber dekanter tesisine gider. Dekanter de
katrandan yoğunluk farkıyla ayrılan su amonyaklı su tankına alınır. Katran fabrikaları
benzol fabrikaları amonyum sülfat tesisi ve KG borularından yoğunlaşan kondensat
suları da amonyaklı su tankında toplanır. Şekil 3.1.’de numune alınan kok fabrikasına
ait akım şeması bulunmaktadır.
Parametre
Değer
pH 7.8 Đletkenlik (mS/cm) 5.47 KOĐ (mg/L) 1110 Fenol (mg/L) 244 Bulanıklılık (NTU) 79.8 SO4 2- (mg/L) 1540 Renk Pt-Co 382 UV254 (1/m) 4.04Şekil 3.1. Koklaştırma Fabrikaları Đş Akım Şeması
Kok fabrikaları yan ürünlerin işletilmesinden kaynaklanan atıksular amonyaklı
su tankında depolanıp arıtma tesisinin ilk ünitesi olan ön çöktürme tankları’ na
aktarılmaktadır. Ön çöktürme tanklarında fiziksel olarak katran ve yağı ayrılan atıksu
dengeleme tanklarına alınıp, atıksuyun akış hızı ve derişim gibi parametrelerinde
meydana gelen değişiklikler ayarlandıktan sonra atıksu, uçucu gazların (NH
4, Fenol)
giderimi için stripper tanklarına alınmaktadır. Flotasyon ünitesine gelen atıksuyun ilk
olarak reaksiyon tankına sonra ise flotasyon tankına girmektedir. Bu tanktaki suyun bir
kısmı basınçlandırma tankından geçirilerek tekrar flotasyon tankına alınır ve böylece
basınçlı hava ile yüzdürme işlemi yapılmış olur. Savaklanan su ise Biyolojik Arıtma
için gerekli olan sıcaklık (25 ºC) ve pH (6–9) değerlerinin sağlanması için nötralizasyon
tankına girmektedir. Nötralizasyon tankından pH ayarlaması yapılan atıksu 2 kademeli
biyolojik arıtma sisteminde çalışan nitrifikasyon ve denitrifikasyon havuzlarına
ardından ise birinci ve ikinci kademe çökelme havuzuna gelmektedir. Çökelme
havuzundan savaklanan atıksu ise işlem görmek üzere Kimyasal Arıtma ünitesine
girmektedir. Kimyasal Arıtma Ünitesindeki atıksu akışı sırasıyla 2 adet Koagülasyon, 2
Adet Flokülasyon, Çökeltim ve Temiz Su Havuzu’ndan oluşmaktadır. Koagülasyon
Havuzlarında sisteme FeCl
3ve kireç verilerek hızlı karıştırma
,Flokülasyon’ un ilk
havuzunda ise Polyelektrolit verilerek yavaş karıştırma yapılmaktadır. Böylelikle
Kömür
Hazırlama
Ünitesi
Kok
Fırınları
Kırma
Eleme
Tesisleri
Yüksek
Fırınlar
Kok
Gaz Hattı
FABRĐKA
Kok Gazı
Kirli Gaz
Amonyaklı Su + Katran
Dekanter
NH
3’ lı
su
Ham
Katran
Arıtma Tesisi
Fırınlar
Harmanlanmış
çökemeyen askıda katı maddelerin çökelmesi sağlanmaktadır. Kimyasal Arıtmada
oluşan çamurlar Belt filtrede işlem görmek üzere çamur yoğunlaştırma tankına,
savaklanan su ise cazibe ile direkt deşarj rögarına aktarılmaktadır.
Kardemir kok
fabrikası atıksu arıtma tesisi proses akım şeması Şekil 3.2.’de verilmiştir.
ATIK SU Dekanter Amonyaklı su Ön çökeltme tankı Atık su Katran Dengeleme tankı Stripper (Sıyırıcı) Asidik Gazlar Fenol sıyırılıyor Bazik Gazlar NH3 sıyırılıyor
poli kireç FeCl3
Reaksiyon T. Flotasyon T.
(Yüzdürme işlemi ile katran ve yağ alınıyor.)
Nötralizasyon Tankı
pH=6-9
1.Kademe: FĐZĐKSEL ARITMA
DN /A1
1.Kademe:Biyolojik Arıtma 2.Kademe:Biyolojik Arıtma
Biyolojik Ç. Havuzu 1 Çamur mikser hava DN /B1 Denitrifikasyon H. N /A1 N /B1 Nitrifikasyon Havuzları N A2 2 N B2 DN A 2 DN B Çamur Biyolojik Ç. Havuzu 2
(Bakteri Yardımıyla +Hava NH3 N halinde uzaklaştırılıyor.)2
2.Kademe: BĐYOLOJĐK ARITMA
Kireç FeCI3
Kum Filtre
silis kum kömürparçaları Karbon Filtre çıkış Kimyasal Çökeltim Havuzu Poli.elekt.
3.Kademe:KĐMYASAL ARITMA 4.Kademe:
ĐLERĐ ARITMA
Asit
Buhar Buhar Kostik
1 2