T.C.
DİCLE ÜNİVERSİTESİ
TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI
ENDOKRİNOLOJİ ve METABOLİZMA HASTALIKLARI BİLİM DALI
ADRENAL İNSİDENTALOMALI HASTALARIN
DEMOGRAFİK ÖZELLİKLERİ VE İNSÜLİN
DİRENCİNİN DEĞERLENDİRİLMESİ
Dr. Sezgin BARUTÇU
UZMANLIK TEZİ
TEZ DANIŞMANI
Prof. Dr. Alpaslan Kemal TUZCU
T.C.
DİCLE ÜNİVERSİTESİ
TIP FAKÜLTESİ İÇ HASTALIKLARI ANABİLİM DALI
ENDOKRİNOLOJİ ve METABOLİZMA HASTALIKLARI BİLİM DALI
ADRENAL İNSİDENTALOMALI HASTALARIN
DEMOGRAFİK ÖZELLİKLERİ VE İNSÜLİN
DİRENCİNİN DEĞERLENDİRİLMESİ
Dr. Sezgin BARUTÇU
UZMANLIK TEZİ
TEZ DANIŞMANI
Prof. Dr. Alpaslan Kemal TUZCU
İÇİNDEKİLER
ÖNSÖZ ---iii
ÖZET---iv
ABSTRACT---vi
TABLO LİSTESİ VE ŞEKİL LİSTESİ---viii
KISALTMALAR---ix
1. GİRİŞ ve AMAÇ---1
2. GENEL BİLGİLER---2
2.1. GİRİŞ---2
2.2. TARİHÇE---3
2.3. ADRENAL BEZ ANATOMİSİ---4
2.4. ADRENAL BEZ EMBRİYOLOJİSİ---5
2.5. ADRENAL BEZ HİSTOLOJİSİ---6
2.5.1. Korteks---6
2.5.2. Medulla---7
2.6. ADRENAL BEZ FİZYOLOJİSİ---8
2.7. ADRENAL TÜMÖRLER---11
2.8. ADRENAL KİTLELERE YAKLAŞIM---12
2.8.1. Adrenal Kitlelere Tanısal Yaklaşımlar---13
2.8.1.1. Adrenal Kitlelerde Endokrin Değerlendirme---13
2.8.1.1.1. Kortizol Salgılayan Kitleler---13
2.8.1.1.1.1. Aşikar Cushing Sendromu---13
2.8.1.1.1.2. Subklinik Cushing Sendromu---14
2.8.1.1.2. Feokromasitoma---16
2.8.1.1.4.1. Adenomlar---22
2.8.1.1.4.2. Adrenokortikal karsinom---22
2.8.1.1.5. Hormonal Aktivitesi Olmayan Durumlar---23
2.8.1.1.5.1. Miyelolipom---23
2.8.1.1.5.2. Kistler---23
2.8.1.1.5.3. Metastazlar---24
2.8.1.1.5.4. Diğer Nedenler---24
2.8.1.2. Adrenal Kitlelerin Radyolojik Değerlendirilmesi---24
2.8.1.3. Moleküler Belirteçler---26
2.8.1.4. İğne Aspirasyon Biyopsisi---26
2.8.1.5. Laparaskopik ve Laparatomik Yaklaşım---26
2.8.2. Tedavi---27
2.8.2.1. Tek Taraflı Adrenal Kitleler---27
2.8.2.2. Bilateral Adrenal Kitleler---28
2.8.3. Takip---28
3. MATERYAL ve METOD---29
3.1. Hasta Seçimi---29
3.2. Biyokimyasal Tetkikler ve Diğer Ölçümler---29
3.3. İstatistiksel Analizler---30
4. BULGULAR---31
5. TARTIŞMA---38
6. SONUÇ---44
ÖNSÖZ
Bilimsel düşünme ve çalışmayı bizlere öğreten, engin bilgi ve birikimlerini bizimle
paylaşan, bugünlere gelmemizde büyük emeği olan, hekimliği bizlere öğreten değerli hocamız Prof. Dr. Ekrem MÜFTÜOĞLU’ na başta olmak üzere, İç Hastalıkları A.B.D. Başkanımız Prof. Dr. M. Emin YILMAZ’a yetişmemde büyük emekleri olan bütün değerli öğretim üyeleri; Prof. Dr. Alpaslan Kemal TUZCU, Prof. Dr. Orhan AYYILDIZ, Prof. Dr. Abdurrahman IŞIKDOĞAN, Prof. Dr. Kendal YALÇIN, Prof.Dr. Muhsin KAYA, Prof. Dr. Vedat GÖRAL, Prof. Dr. Ali Kemal KADİROĞLU, Doç. Dr. Ebubekir Şenateş, Yrd. Doç. Dr. M.Ali KAPLAN, Yrd. Doç.Dr. Mehmet KÜÇÜKÖNER, Yrd. Doç.Dr. Zülfikar YILMAZ, Yrd.Doç. Dr. Yaşar YILDIRIM, Uz. Dr. Coşkun BEYAZ, Uz. Dr. Faruk KILINÇ, Uz. Dr.Nazım EKİN, Uz. Dr.Sinan DAL’a teşekkürlerimi sunuyorum.
Tezimin her aşamasında yardımlarını esirgemeyen saygıdeğer hocam Prof. Dr. Alpaslan Kemal TUZCU’ya ve rotasyon eğitimim sırasında bilgilerini benden esirgemeyen Kardiyoloji A.B.D. , Enfeksiyon Hastalıkları ve Mikrobiyoloji A.B.D , Göğüs Hastalıkları ve Tüberküloz A.B.D., Radyoloji A.B.D. başkanlarına ve değerli öğretim üyelerine,birlikte çalışmaktan her zaman büyük mutluluk ve onur duyduğum tüm asistan arkadaşlarıma ve İç Hastalıkları A.B.D. çalışanlarına teşekkür ederim.
Bugünlere gelmemde büyük emeği geçen aileme, her zaman yanımda olan eşime sonsuz saygı ve teşekkürlerimi sunarım.
ÖZET
Adrenal İnsidentalomalı Hastaların Demografik Özellikleri ve İnsülin Direncinin Değerlendirilmesi
Giriş ve amaç: Adrenal insidentalomalar; adrenal bezde herhangi bir hastalık
kuşkusu yokken görüntüleme yöntemleri veya abdominal laparotomide tesadüfen saptanan kitlelerdir. Abdominal ultrasonografinin ve BT’nin kullanımının artması ile adrenal insidentalomaların tespit edilme sıklığıda artmıştır. Bu çalışmamızda Dicle Üniversitesi Endokrinoloji Kliniği’nde takip edilen hastaları retrospektif olarak inceleyip, bu hastalarda diyabet sıklığı ve insülin direncini araştırmayı amaçladık.
Materyal-metod: Bu çalışmaya 2007-2013 yılları arasında Dicle Üniversitesi Tıp
Fakültesi Endokrinoloji Anabilim Dalı’na başvuran 78 hasta ( 53 kadın; 25 erkek) dahil edildi. Hasta dosyalarından hastalara ait fizik muayene, USG, BT sonuçları kaydedildi. Serum kortizolü, idrar metanefrini, idrar normetanefrini, idrar VMA, serum aldosteronu ve serum renin değerleri kaydedildi. Açlık kan şekeri ve insülin değerleri mevcut olan hastaların HOMA-IR formülüne göre insülin direnci hesaplandı, yaş ve BMI farklı olmayan kontrol grubundaki sağlıklı bireylerle karşılaştırıldı.
Bulgular: Hastaların yaş ortalaması 48,6±14,9 idi. Tespit edilen kitlelerin lokalizasyonu açısından anlamlı farklılık saptanmadı. Hastaların vücut kitle indeksi 28,545±5,827 idi. HOMA-IR ortalaması 6,555±11,232 olarak saptandı. 45 hastada (%57,7) non-fonksiyonel adenom, 10 hastada (%12,8) subklinik cushing, 11 hastada (%14,1) feokromasitoma, 3 hastada (%3,8) adrenal karsinom, 2 hastada (%2,6) hiperaldosteronizm, 2 hastada (%2,6) ganglionörom, 1 hastada (%1,3) myelolipom, 1 hastada adrenal adenom, 1 hastada adrenal kist, 1 hastada schwannom ve 1 hastada da küçük yuvarlak hücreli tümör tespit edildi. Adrenal insidentalomalı hastalarda kontrol grubuna göre insülin direnci daha fazla tespit edildi (p=0,004). Adrenal insidentalomalı hastaların 21’inde (%26,9) kontrol grubunda ise 4 hastada (%5,1) diyabet saptanmıştı. Bu karşılaştırmada önceden bilinen diyabeti olan hastalar çalışma dışında bırakıldığında da insülin direnci adrenal insidentalomalı hastalarda daha yüksek bulundu (p=0,000). Non-fonksiyonel adrenal insidentalomalarda da kontrol grubuna göre daha yüksek insülin direnci tespit edildi (p=0,001).
Sonuçlar: Adrenal insidentalomalar arasında non-fonksiyonel adrenal kitleler daha
fazla görülmektedir. Adrenal insidentalomalı hastalarda diyabet sıklığı artmıştır. Diyabetli olan hastaların dahil edildiği ve hariç tutulduğu her iki durumda da insülin direnci varlığını sürdürmüştür.
ABSTRACT
Demographical Characteristics of Patients With Adrenal Incidentaloma and Evaluate İnsulin Resistance
Introduction and Purpose: Adrenal incidentaloma are bulks which are stated
incidentally by imagining methods or in abdominal laparotomy when there is no suspicion of any disease in adrenal gland. With increase in using abdominal ultrasonography and BT, the frequency of determining adrenal incidentaloma also increases. In this study, we aim to examine patients that are followed in Dicle University Clinic of Endocrinology retrospectively and search the diabetes frequency and insulin resistance in those patients.
Material-method: 78 patients, who applied to Dicle University Medical Faculty
Department of Endocrinology between years of 2007-2011 (53 female – 25 male) were included in this study. Results of physical examination, USG and BT were recorded from patients’ files. Values of serum cortisol, urine metanephrine, urine normetanephrine, urine VMA, serum aldosterone and serum renin were recorded. Insulin resistance of patients, of which preprandial blood glucose and insulin values were available, were calculated in accordance with HOMA-IR Formula, and were compared with healthy individuals in control group of which ages and BMI are not different.
Findings: The average of age of patients were 48,6±14,9. There is no significant
difference was stated in terms of localizations of stated bulks. Body Mass Index of patients were 28,545±5,827. Their average of HOMA-IR were stated as 6,555±11,232. There are non-functional adenoma were stated in 45 patients (57,7%), subclinical cushing was stated in 10 patients (12,8%), pheochromocytoma was stated in 11 patients ( 14,1%), adrenal carcinoma was stated in 3 patients (3,8%), hyperaldosteronism was stated in 2 patients (2,6%), ganglioneuroma was stated in 2 patients (2,6%), myelolipoma was stated in 1 patient (1,3%), adrenal adenoma was stated in 1 patient, adrenal cyst was stated in 1 patient schwannoma was stated in 1 patient and neoplasia with small circular cells was stated in 1 patients. Insulin resistance was stated as more in patients with adrenal incidentaloma as to control group (p=0,004). Diabetes Mellitus was stated in 21 (26,9%) patients with adrenal incidentaloma and in 4 patients (5,1%) in control group. In this comparison, when patients who have
stated in patients with adrenal incidentaloma more than control group (p=0,000). Higher insulin resistance was stated in patients with non-functional adrenal incidentaloma as to control group (p=0,001).
Results: Non-functional adrenal bulks are seen more in adrenal incidentalomas.
Frequency of diabetes mellitus increases in patients with adrenal incidentaloma. Insulin resistance subsists in both conditions whether patients with diabetes mellitus are included or not.
TABLO LİSTESİ
Tablo-1: Adrenal insidentaloma nedenleri ve sıklığı
Tablo-2: Feokromasitomada artış gösteren hormon ve metabolitleri Tablo-3: Katekolamin ve metanefrinlerde artışa yol açabilecek ilaçlar Tablo-4: Kitle çapı adenom-ACC ilişkisi
Tablo-5: Adrenal insidentaloma hastalarının bulguları
Tablo-6: Adrenal insidentaloma-kontrol grubu arasındaki insülin direnci ilişkisi Tablo-7: Non-fonksiyonel adrenal insidentaloma-kontrol grubu arasındaki insülin
direnci ilişkisi
Tablo-8: Adrenal insidentaloma-kontrol grubu arasındaki diyabet olmayan hastaların
insülin direnci ilişkileri
ŞEKİL LİSTESİ
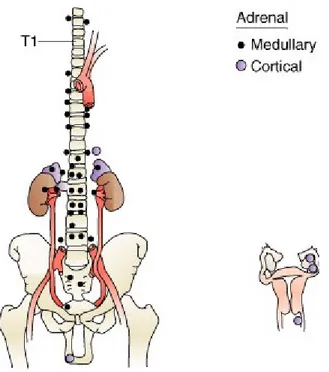
Şekil-1: Adrenal bezlerin anatomik görünümü
Şekil-2: Korteks ve medullanın anormal lokalizasyonları Şekil-3: Adrenal steroidlerin sentezi
Şekil-4: Katekolamin hormon metabolizması Şekil-5: Adrenal kitlelerin sınıflandırılması Şekil-6: Adrenal kitlelerin genel dağılımı
KISALTMALAR
BT : Bilgisayarlı Tomografi
USG : Ultrasonografi VMA : Vanil mandelik asit VKİ : Vücut kitle indeksi
HOMA : Homeostasis model assessment ACTH : Adrenokortikotropik hormon VCI : Vena cava inferior
SER : Sarkoplazmik endoplazmik retikulum DHEA : Dehidroepiandrosteron
CRH : Kortikotropin salgılatıcı hormon MAO : Monoamin oksidaz
COMT : Katekolamin O-metiltransferaz EAS : Ektopik ACTH sendromu LDL : Düşük dansiteli lipoprotein HDL : Yüksek dansiteli lipoprotein PKOS : Polikistik over sendromu DST : Deksametazon süpresyon testi MEN : Multipl endokrin neoplazi NF : Nörofibromatozis
VHL : Von Hipple Lindau
HPLC : High performance liquid chromatography MRG : Manyetik rezonans görüntüleme
PH : Primer hiperaldosteronizm PRA : Plazma renin aktivitesi
ACE : Anjiyotensin converting enzim ARB : Anjiyotensin reseptör blokörü DHEA-S : Dihidroepiandrosteron sülfat ACC : Adrenokortikal karsinom PET : Pozitron Emisyon Tomografisi DNA : Deoksi ribonükleik asit
HU : Hounsfield ünitesi IVP : İntravenöz piyelografi
DDDST : Düşük doz deksametazon süpresyon testi AKBİ : Ayaktan kan basıncı izlemi
IL-6 : İnterlökin-6
TNF-α : Tümör nekrozis faktör alfa HTRP : Hipertansif retinopati PTH : Parathormon
1. GİRİŞ ve AMAÇ
Adrenal insidentaloma; anamnezinde, fizik muayenesinde belirgin adrenal hastalık kuşkusu yok iken, çeşitli sebeplerle yapılan batın görüntüleme yöntemleri veya abdominal laparatomi esnasında tesadüfen saptanan adrenal kitlelere denilir. Görüntüleme yöntemlerindeki teknolojik gelişme ve bu yöntemlerin klinik uygulamada yaygın olarak kullanılması adrenal insidentalomaların günümüzde daha sık karşımıza çıkmasına neden olmaktadır. Bu kitlelerin büyük çoğunluğunu fonksiyon özelliği göstermeyen adenomlar oluşturmasına rağmen, potansiyel letal bir kanser veya fonksiyon gösteren endokrin bir tümör olarak ta karşımıza çıkabilmektedir. Adrenal kitleli bir hasta ile karşılaşıldığında çözülmesi gereken iki temel problem vardır. Bunlar adrenal kitle veya kitlelerin benign-malign ayırımı ile hormonal olarak aktif olup olmadığıdır.
Çalışmamızdaki amaç 2007-2013 yıllar arasında hastanemiz Endokrinoloji polikliniğimize başvuran hastaların demografik özelliklerini incelemek ve adrenal insidentaloma ile insülin direnci arasındaki ilişkiyi araştırmaktır.
2. GENEL BİLGİLER
2.1 GİRİŞ
Sürrenal bezlerle ilişkisi olmayan çeşitli nedenlerle yapılan radyolojik incelemeler sırasında veya laparatomide tesadüfen bulunan; anamnezinde, fizik muayenesinde sürrenal kitle veya sürrenal fonksiyon bozukluğu göstermeyen asemptomatik sürrenal kitlelere insidentaloma adı verilmektedir (1). Adrenal bezler insan vücudunda kitle görülme oranı yüksek olan organlardan birisidir. Adrenal bezde tespit edilen kitleler yüksek malignite riski taşımakla beraber çok farklı klinik, laboratuar ve radyolojik verilerle karşımıza çıkabilmektedir. Görüntüleme yöntemlerindeki teknolojik gelişmeye ve bu yöntemlerin yaygınlaşmasına bağlı olarak insidentalomalar artan oranda karşımıza çıktığından, günümüzde klinik endokrinologların sıklıkla karşılaştığı problemlerden biri olmuştur.
Yapılan farklı çalışmalarda adrenal kitle görülme sıklığı %1,4 ile %8 arasında değişmektedir (2). Uygulanan tekniğin yanı sıra adrenal insidentaloma vakalarında prevalans yaş ile birlikte artmaktadır. Görülme sıklığı 5. ve 7. dekadlarda pik yapar. Genç yaşlarda % 0,2, orta yaşlarda %3, ileri yaşlarda %10 kadardır. İnsidental adrenal kitleler otopsi serilerinde daha fazladır. Otopsi çalışmalarında ise 30 yaşından küçük hastalarda görülme sıklığı %1’in altında iken bu oran 50 yaşından büyük hastalarda %3, 70 yaşından büyük hastalarda ise %7 civarındadır.(3).
Adrenal bezler dışında bir kitle araştırırken adrenal bezlerde fark edilen kitlelere adrenal “insidentaloma” denmektedir. Adrenal bezlerden kaynaklanan bir hastalık düşünülerek yapılan tetkik sonucu tespit edilen kitlelere ise “noninsidentaloma” denmektedir. Adrenal kitlelerde ilk cevaplanması gereken soru kitlenin hormon aktif olup olmadıklarıdır(4). Hormon aktif lezyonlar klinik bulgu verdikleri için araştırma esnasında ortaya çıkabilir. Klinik belirti vermeyen ancak hormonal olarak aktif olan kitleler “subklinik hastalık” kavramını gündeme getirmiştir (7,8). Subklinik hormon yapımı ile seyreden kitlelerin semptomatik düzeye gelinceye kadar tedavi edilmemesi morbiditeyi artırdığı ifade edilmektedir (7).
Sürrenal kitlelerde cerrahi yaklaşım belirlenirken mevcut patolojinin (kanser, kanama, salgı yapan nodül) oluşturduğu anatomik değişiklikler, nodüllerin yol açtığı salgısal değişimler ve kitlenin yerleşimi önemli yer tutar. Hormonal olarak aktif sekretuar kitleler araştırma esnasında ortaya çıkmakla beraber günlük uygulamamızda karşımıza daha az
Conn Sendromu, Cushing Sendromu veya feokromositomaya neden olmaktadır(5).Başlangıçta semptomatik olmayan adrenal insidentalomalar daha sonra semptomatik hale gelebilirler.Klinik olarak belirti vermeyen adrenal insidentalomaların ileride klinik belirti verip vermeyeceği konusunda bugün için net olarak ortaya konmuş bir kriter yoktur (6).
2.2. TARİHÇE
Sürrenal bezler ilk defa 1563 yılında Bartolomeo Eustachia tarafından bahsedilmiştir (9). 1805 yılında ise sürrenal bezler Cuvier tarafından anatomik olarak kortex ve medulla diye adlandırılmıştır (10).
Adrenal bezlerin fonksiyonları ve hayat için ne kadar esansiyel olduğu ancak 1855 yılında Thomas Addison’un destrüksiyon olmuş adrenal bezlerdeki gözlemlerinden sonra bilinmeye başlanmıştır (11,14). Bundan sonra bu organın önemi kavranmış ve tüm dünyada fonksiyonlarının araştırılması gerektiğine dikkat çekilmiştir. Brown-Sequard 1856’da farklı hayvan türlerinde yaptığı adrenalektomi sonrası deneysel çalışmalarında sürrenal bezin hayat için gerekli olduğunu ortaya koymuştur (12).
1895’de George Oliver ve Edward Sharpey-Schafer adlı İngiliz fizyolojistler adrenal medullada adrenalin adını verdikleri, köpeklerde kan basıncını yükselten maddeyi göstermiştir. Bundan 2 yıl sonra ise John Abel maddeyi saflaştırdıktan sonra aktif bölümüne epinefrin adını vermiştir (14).
Feokromasitoma ilk kez 1886’da Frankel tarafından bildirilmiştir (10). Feokromasitoma için yapılan ilk başarılı adrenalektomi ise 1926’da, ABD’de Charles Mayo, İsviçre’de Roux tarafından gerçekleştirilmiştir. Fakat feokromasitoma’nın ilk klinik tanısı 1926 yılında Vaquez ve Donzolet tarafından yapılmıştır (13).
1908-1940 yılları arasındaki araştırmalarda sürrenal korteksin metabolizmada düzenleyici rolü olduğu ve glikokortikoid fonksiyonunun yaşam için gerekli olduğu vurgulanmıştır (12,15). 1943’te adrenokortikotropik hormon (ACTH) tanımlanıp saf olarak elde edilmiştir (12).’’Kortizon’’ terimi ilk defa Kendall tarafından kullanılmıştır (15).
Adrenal tümörün sebep olduğu Cushing sendromu ilk defa 1913’te Turney ve 1926’da Parkes-Weber tarafından bildirilmiştir. Ardından Harvey 1932’de Cushing, bilateral adrenal kortikal hiperplazili hastalarda glikokortikoid fazlalığı sendromunu tanımlamıştır (12).
Deming ve Luetscher tarafından idrarda sodyum iyonu tutan bir faktör olarak tanımlanan ve daha sonra ‘’Aldosteron’’ adını verdikleri faktör, 1952’de Simpson ve arkadaşları tarafından izole edilip gösterilmiştir.1955 yılında Conn, halsizlik ve hipertansiyonu olan bir hastada, kanda potasyum iyonunun düşük ve sodyum iyonunun yüksek olduğunu tespit etmiştir. Bunun üzerine hastada aldosteron salgılayan tümör olduğu düşünülerek ameliyat edilip sağ sürrenal bezde tümör olduğu saptanmıştır. Ameliyat sonrası hastanın kliniği tamamen düzelmiştir. Conn bu sendroma ‘’primer hiperaldosteronizm’’ adını vermiştir (16).
2.3. ADRENAL BEZ ANATOMİSİ
Adrenal bezler, retroperitoneal olarak böbreklerin üst iç yanında bulunurlar (4, 15, 17). Kolumna vertebralisin her iki yanında 11. torasik ve 1. Lomber vertebranın laterallerinde, perirenal faysa ve perirenal yağ dokusu ile çevrilmiş olarak yerleşirler (17,18)
Sağ sürrenal bez sola göre daha yüksekte ve daha dış tarafta lokalize olur. Vena Cava İnferior’a (VCI) yakın yerleşimli olması nedeniyle önem taşır. Şekil olarak üçgene benzer. Sol sürrenal bez ise, sağ sürrenal beze göre biraz daha uzun ve geniştir. Şekil olarak yarım aya benzeyip abdominal aortaya yakınlığı açısından önem taşır. Boyutları yaklaşık 5x3x1 cm kadardır. Her biri yaklaşık olarak 8- 10 gr ağırlığındadır. Adrenal bezler %90’ı korteks ve %10’u medulla olmak üzere iki bölümden oluşur (15, 17, 19).
Adrenal bezler damarsal yapıdan oldukça zengindir. Abdominal aorta, frenik arter ve renal arterlerden dallar alır. Vücudumuzda arteriyel kanlanması her durumda sabit tutulmaya çalışılan üç organ bulunmaktadır. Bunlar kalp, beyin ve adrenal bezlerdir. Damarsal yapıdan çok zengin olmasına karşın bezin her biri 10 ml/dk gibi düşük miktarda kan akımı ile beslenir. Tiroid bezinin gram başına 5 ml/dk’lık akımla kanlandığı göz önüne alınırsa adrenal bezin ne kadar az kan ile beslendiği görülür. Ancak bezin kan akımı strese cevap olarak kısa zamanda artarak 5-6 katına çıkabilir (20).
Şekil-1 Adrenal bezlerin anatomik görünümü (21). 2.4. ADRENAL BEZ EMBRİYOLOJİSİ
Sürrenal korteks gestasyonel hayatın 4- 6, haftalarında çölom epitelinden gelişir. Bu hücreler suprarenal bölgede çoğalırlar. 7. haftada nöral tüpten kaynaklanan ektodermal hücreler (feokromoblastlar) paravertebral, paraaortik ve aortik bifurkasyon hizasında çoğalırlar. Doğumdan sonra fetal korteks hızla dejenere olur ve yetişkin korteks prolifere olmaya başlar. Fetal korteks yaşamın ilk yılında tamamen kaybolurken, adult korteks 12 yılda tamamen değişir. Ektopik adrenokortikal doku adrenal bezlere yakın yerleşimli veya ürogenital çıkıntı ile alakalı olarak yenidoğan infantlarda yaygındır (13).
Sürrenal bezlerin % 90’ını korteks, %10’unu medulla oluşturur. Sürrenal korteks ve medullanın orjini farklıdır. Embriyolojik olarak adrenal korteks mezoderm kökenlidir. Üç bölümden oluşur ve birçok önemli hormonun üretimine kaynaklık eder (17).
Adrenal medulladaki kromaffin hücreler nöroektodermden köken alır. Gestasyonun 2. ayında nöral krest hücreleri fetal kortekse göç ederek istila ederler. Medullayı oluşturacak ektodermal hücrelerin etrafı, korteksi oluşturacak mezodermal hücreler tarafından sarılır (17, 19, 22).
Başlangıçta korteks, genel vücut büyümesiyle orantılı olarak hızla büyür. Bezin büyüklüğü insanda intrauterin dördüncü ayda böbrek büyüklüğüne erişir. Gebeliğin son ayında ise büyümesi yavaşlar (23). Adrenal bezin büyüklüğü, yeni doğmuşlarda böbreğin üçte biri iken, yetişkinlerde yirmi sekizde veya otuzda biridir (24,25). Fötal kortekste gerileme olurken, zona glomerüloza ile fasikülata gelişmeye devam ederler ve bu sırada zona retikülaris belirmeye başlar. Doğumdan sonraki ikinci yaşta fötal korteks, en dış tabakası hariç tamamen ortadan kalkmıştır. Fötal korteksin en dış tabakasından zona retikülaris gelişir. Erişkindeki korteks yapısına ise ancak puberte çağlarında ulaşılır (26,27).
2.5. ADRENAL BEZ HİSTOLOJİSİ
Adrenal bez korteks ve medulla olmak üzere iki kısımdan oluşmaktadır. Korteks ve medulla, anatomik, histolojik, embriyolojik ve fonksiyonel özellikler bakımından birbirinden farklı özelliklere sahiptir. Sürrenal bezin kesitinde, dış tarafta korteks, iç tarafta medulla yer alır. Korteksi fibröz bir kapsül çevreler. Bu kapsülü damarlar delip geçtiği için kapsül bezden ayrılamaz (22).
Kapsulada bol arteriyal ağlar, venler, lenf damarları ve sinir pleksusları bulunur. Kapsulanın iç kısmında yer alan küçük gruplar halindeki indiferansiye hücrelerden, korteks hücrelerinin farklılaştığı ve buranın subkapsüler transformasyon bölgesi olarak adlandırıldığı bildirilmektedir. Transformasyon bölgesine, kapsulanın hemen altında yan yana dizilmiş halde bulunan glomeruloza hücrelerinin de dahil olduğu söylenmektedir (28).
2.5.1. Korteks
Adrenal korteks embriyolojik olarak mezoderm kökenlidir, üç bölümden oluşur ve önemli birçok hormon üretimine kaynaklık eder.
i. Zona glomeruloza: Korteksin yaklaşık %10-15’ini oluşturur. İnsanda
yuvarlağımsı, poligonal veya uzunca hücreler bir araya gelerek ya hücre kümelerini ya da iki uçlarından bükülerek kavisler yapan ve altta zona fasikülata hücreleri ile devam eden hücre kordonlarını oluştururlar. Bu hücrelerin çekirdekleri koyu renkte boyanır ve stoplazmalarında birkaç lipit damlacığı bulunur. Ultrastriktürel olarak en belirgin özelliği ise düz endoplazmik retikulumun ağ şeklindeki yapısıdır (31). Hücre kümelerinin ortasında ekzokrin salgı bezlerindeki gibi lümen yoktur (29, 30).
ii. Zona fasikülata: Korteksin %80’ini oluşturur. Adrenal korteksin en dış
tabakasıdır. Kübik veya poligonal hücreler, medullaya doğru ışınsal olarak birbirine paralel uzanan hücre kordonlarını oluştururlar. Zona glomeruloza’daki hücrelerden biraz daha büyük, merkezi koyu boyanan çekirdeklere ve ince vakuollerle dolu bir stoplazmaya sahip, çok kenarlı hücreler içeren kordonlardan oluşmuştur(31). Zona fasikülatanın üçte iki dış kısmındaki hücrelerde çok sayıda lipit damlası bulunur. Fasikülatanın üçte bir iç kısmındaki hücreler ise lipitten fakirdir ve daha koyu boyanır (28, 29, 32). Ultrastrüktürel olarak zona fasikülata hücrelerinde iyi gelişmiş SER (sarkoplazmik endoplazmik retikulum) bulunur. Mitokondriler oval, uzunca ve sıklıkla düzensiz şekilli olup, tübüler kristalidir. Golgi kompleksi jukstanükleer yerleşimli ve iyi gelişmiştir. Stoplazmada lizozomlar ve mikroperoksizomlar bulunur (30, 33, 34).
iii. Zona retikülaris: Korteksin %5’ini oluştururlar. Zona retikülariste birbirine
paralel kordonlar ve medullaya dayanan yığınlar vardır. Bu hücreler temel olarak fasikülatadaki hücrelere benzerdirler. Asidofiliktir ve hipokrom pigmentini fazlaca içermelerine rağmen stoplazmalarında vakuol yoktur. Bundan dolayı bu hücrelere kompakt veya koyu hücreler denir. Bu hücrelerde düz endoplazmik retikulum sayısı çoktur. Zona fasikülata ve zona retikülaris, glikokortikoid ve seks steroidlerini sentez ederek salgılayan tek fonksiyonel birimdir (31).
2.5.2. Medulla
Santral yerleşimli medulla, bez hacminin yaklaşık yüzde 10’unu kaplar. Medullanın büyük, oval veya poligonal hücreleri bir araya gelerek, kümeler ya da birbiriyle anastomozlaşan kısa kordonlar oluştururlar. Hücre küme ve kordonlarının arasında venüller ve sinüzoid tipte kapiller bulunur (24, 25, 28, 29, 32). Vücudun en büyük epinefrin kaynağıdır. Embriyolojik olarak kromaffin hücreler (feokromasitleri), otonomik ganglion hücreler ve sürrenal dışı paraganglionik hücrelere dönüşebilen primitif nöroektodermal hücrelerden kaynaklanır (31). Kromaffin hücre; kahverengi intrasitoplazmik granüllerle karakterizedir. Bu granüller içinde katekolaminler depo edilmiştir. Başlıca katekolamin epinefrin olmakla beraber norepinefrin de 1/5 veya 1/6 oranında bulunur (17,31). 1894 yılında Oliver ve Schaffer, medulla ekstresini enjekte ettikten sonra kan basıncının yükselmesini tespit ederek sürrenal medulla hormonlarıyla ilgili ilk çalışmayı yapmışlardır. Daha sonra Abel, epinefrin (adrenalin) adını verdiği bileşiği sürrenal bezinden elde etmeyi başarmıştır (37).
Şekil 2. Korteks ve medullanın anormal lokalizasyonları(siyah alanla gösterilen bölgeler anormal yerleşimli korteks ve medullayı simgelemektedir (35).
2.6. ADRENAL BEZ FİZYOLOJİSİ
Sürrenal korteks, salgıladığı hormonlar nedeniyle organizma için çok gerekli ve önemli bir dokudur. Korteksin yokluğunda ölüm doğal bir sonuçtur. Adrenal korteks; plazma kolesterolünden glukokortikoidler, mineralokortikoidler ve seks steroidleri olmak üzere 3 tip steroid hormon sentezler. Z. glomerüloza’dan aldosteron, Z.fasikulata’dan glikokortikoidler, Z. retikularis’ten de androjenik steroidler salgılanır.
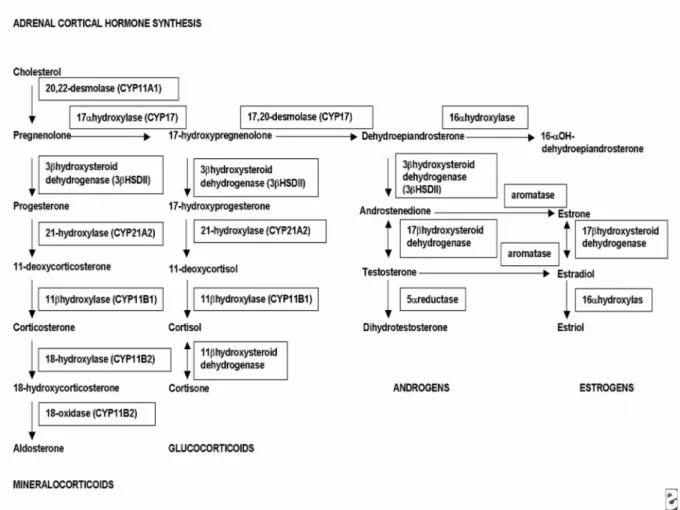
Glukokortikoidlerin karbonhidrat, protein ve yağ metabolizması üzerine geniş etkileri vardır. Mineralokortikoidler sodyum dengesinde ve extrasellüler sıvı hacminin devamlılığında gereklidir. Seks steroidlerinin normal bireylerde sadece küçük etkileri vardır ve steroidogenezisin yan ürünü olarak kabul edilebilir. Glukokortikoidlerden kortizol ve kortikosteron, mineralokortikoidlerden ise aldosteron, androjen ve dehidroepiandrosteron (DHEA) fizyolojik olarak önemli miktarda salgılanan hormonlardır. Steroid sentezi mitokondri ve endoplazmik retikulumda gerçekleşir. Steroid sentezinde ilk basamak kolesterolun pregnenolone dönüşümüdür. Pregnenolon, daha sonra 3 ana yol ile aldosteron, kortizon ve DHEA dönüşür. Kortizon salgılandıktan sonra yüksek afinite ile kortikosteroid bağlayan globuline bağlanır. Aldosteron genellikle serbest form şeklinde salgılanır. Zayıf
androjen DHEA baslıca DHEA-sulfat şeklinde salgılanır ve periferik dokularda testesteron ve östrojenlere dönüşür (Şekil 3) (36).
Glukokortikoid salınımı başlıca hipotalamus, hipofiz ve adrenal bezlerin hormonal etkileşimleri ile düzenlenir. Hipotalamik nöronlardan strese yanıt olarak sinirsel uyaran ile kortikotropin-salgılatıcı hormon (CRH) ve diğer ajanların salınımı gerçekleşir. Salınan CRH, hipofiz bezinden ACTH salınımını uyarır. ACTH adrenal kortekse etki ederek kortikosteroidlerin salınımını artırır. Glukokortikoidler, CRH ve ACTH sentez ve salınımı üzerine negatif feedback etki yapar.
Şekil 3. Adrenal steroidlerin sentezi
Adrenal medulla, direk Santral Sinir Sistemi’nin etkisi altındadır ve katekolaminleri sempatik sinir sistemi boyunca sentezlerler. Sempatoadrenal sistemde katekolaminler tirozinden sentez edilirler. Tirozinin, tirozin hidroksilaz ile 3,4- dihidroksifenilalanine hidroksilasyonu sentez aşamasının hız sınırlayıcı basamağıdır. DOPA daha sonra dopamine, bu da norepinefrine dönüsür. Bu sentez aşamaları sempatoadrenal sistem boyunca gelişir.
Adrenal medulla’da norepinefrin daha sonra feniletanolamin n-metiltransferaz ile epinefrine dönüşür. Bu enzim gloukortikoidler ile indükte olur ki epinefrinin ana kaynağı, glukortikoidlerin yüksek konsantrasyonda bulunduğu kromaffin hücreleridir. Preganglionik sempatik sinirlerden çıkan asetilkolin granüllerden katekolamin salınmasını başlatır. Adrenal medulladan kana verilen katekolaminlerin % 80’i epinefrin, % 20’si norepinefrindir (36,38).
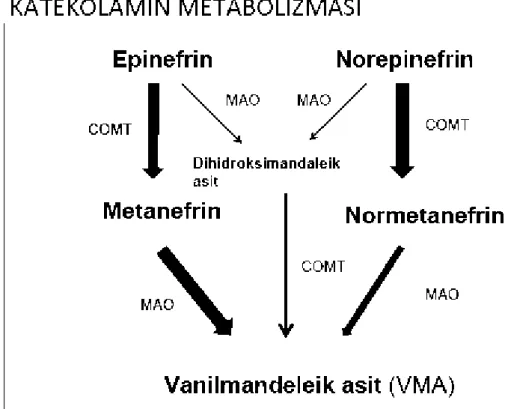
Dolaşımdaki epinefrin ve norepinefrini inaktive eden başlıca enzimler monoaminoksidaz (MAO) ve katekol O-metiltransferaz (COMT) dır. Her iki enzim birçok dokuda bulunmakla beraber en yüksek miktarlar karaciğer ve böbrekte saptanır. Dolaşımdaki epinefrin ve norepinefrinin büyük kısmı COMT tarafından baslangıçta metanefrin ve normetanefrine metillenir. Daha sonra MAO bu maddeleri major atılım ürünü olan 3-metoksi-4-hidroksi-mandelik aside metabolize eder. İnsanlarda idrarda atılan katekolamin metabolitlerinin % 60’nı 3-metoksi-4-hidroksimandelik asit oluşturur (Şekil-4). Sempatoadrenal sistem, birçok değişik fizyolojik uyaran ile etkilenen farklı sistemler ve SSS ile regüle olur. Bazen sempatik sinir sistemi süprese olmuşken, adrenal medulla stimule olabilir. Bu da dolaşımdaki ve lokal salınan katekolaminlerin değişik fonksiyonlar olduğunu göstermektedir. Katekolaminler etkilerini alfa ve beta adrenerjik ve dopaminerjik reseptörler ile gösterir. Başlıca etkileri arasında;
i. Kardiyovasküler (kardiyak output ve vasküler direnci etkiler), ii. visseral (vejetatif etkiler) ve
iii. metabolik etkiler (depolardan enerji rezervlerinin mobilizasyonu, oksijen alımının düzenlenmesi, hücre dışı sıvının devamlılığının sağlanması)sayılabilir (38).
Şekil 4. Katekolamin hormon metabolizması(38) 2.7. ADRENAL TÜMÖRLER
Adrenal tümörler korteks veya medulladan kaynaklanmaktadır. Bu tümörler genel olarak fonksiyonel veya nonfonksiyonel olabildiği gibi benign veya malign de olabilirler. Adrenal tümörlerin çoğunu korteksten çıkan tümörler oluşturur. Bunlar adrenokortikal tümörler adı altında toplanırlar. Adrenal korteksten kaynaklanan fonksiyonel tümörler başta Cushing sendromu olmak üzere birçok klinik hastalığa neden olabilir. Adrenal medulladan kaynaklanan en sık fonksiyonel tümör ise feokromasitomadır (39).
Şekil 5. Adrenal kitlelerin sınıflandırılması 2.8. ADRENAL KİTLELERE YAKLAŞIM
Adrenal bezdeki kitleler başlıca iki şekilde karşımıza çıkmaktadır. Birincisi ve en sık olanı tesadüfen tespit edilen kitlelerdir. Adrenal bezde bir hastalık düşünülmeksizin başka nedenlerle yapılan tetkiklerde tespit edildiği için bu kitlelere adrenal “insidentaloma” denmektedir. İkincisi ve daha az sıklıkta olanı ise adrenal bez hastalıkları araştırılırken tespit edilen, “noninsidentaloma” denilen kitlelerdir (39,40).
Adrenal kitle prevalansı, çalışmaya alınan grubun özelliklerine ve kabul edilen tanı kriterlerine göre değişiklik gösterebilmektedir. Otopsi serilerinde %1 ile 8.7 olarak bildirilmektedir. Klinik çalışmalarda orta yaş grubunda %4 civarında olduğu, yaşlı populasyonda %10’un üzerinde olabileceği tahmin edilmektedir. Bu artışın sebebinin ileri yaşlarda ateroskleroza ve iskemik değişikliklere bağlı lokal büyüme alanları olduğu düşünülmektedir (106).
Benign non fonksiyone adenomların prevalansı onkoloji dışı ve genel hasta populasyonunda %36-94 gibi geniş bir aralıkta bildirilmektedir. 3868 vakalık adrenal insidentalamo serisinde non fonksiyonel kitle oranı %71.2 olarak bulunmuştur. 1004 vakalı İtalyan serisinde kitlelerin %85’i nonfonksiyone, %9.2’i subklinik Cushing, % 4.2’u feokromositoma ve %1.6’i aldosteronoma tespit edilmiştir. Adrenalektomi uygulanan 380 vakanın %52’si kortikal adenom, %12 kortikal karsinom, %11 feokromositoma bulunmuştur (4). Çalışmalar sonucundaki adrenal insidentaloma nedenleri ve sıklığı aşağıda verilen tabloda ki gibidir.(106)
2.8.1. Adrenal Kitlelere Tanısal Yaklaşımlar
2.8.1.1. Adrenal Kitlelerde Endokrin Değerlendirme 2.8.1.1.1. Kortizol Salgılayan Kitleler
2.8.1.1.1.1. Aşikar Cushing Sendromu
Çeşitli sebeplere bağlı olarak gelişen kronik glukokortikoid fazlalığı Cushing Sendromu olarak adlandırlır (41). Cushing Sendromu’nun yıllık insidansı milyonda 2 olarak bildirilmiştir (42). Ancak bu düşük insidans normal popülasyon taramaları sonucu ortaya çıkmıştır. Oysa yüksek riskli (obezite, kötü kontrollü diyabet ve adrenal insidentaloma) populasyonların taranması sonucunda %2 gibi daha yüksek oranlar bulunmuştur (43).
Vücuttaki tüm sistemleri etkileyebilmekle beraber en sık iyatrojenik olarak inflamatuvar hastalıkların tedavisinde yüksek doz kortikosteroid kullanımı sonucu ortaya çıkmaktadır. Egzojen glukokortikoid kullanımı dışlandığında Cushing Sendromu kortikotropin (ACTH) bağımlı veya ACTH bağımsız olarak sınıflandırılır. ACTH bağımlı Cushing Sendrom olguların %60-80’inde neden hipofizer bir mikroadenomdur ve buna
gelişen ektopik ACTH sendromudur (EAS). EAS’a en sık neden olan hastalık küçük hücreli akciğer kanseridir. EAS olgularının hipofizer hastalıkla karışması tanısal bir sorun teşkil eder. ACTH bağımsız Cushing Sendrom’u ise genelde adrenalden kaynaklanır ve adrenal Cushing Sendromu’nun sebepleri ise adrenal adenom, karsinom ve nadiren primer nodüler adrenal hiperplazidir. Bir diğer Cushing Sendromu nedeni ise kronik glukokortikoid kullanımına bağlı gelişen iyatrojenik Cushing Sendromu’dur ve glukokortikoid tedavisi kesilince tablo geriler (107).
Cushing Sendromu’na spesifik bulgu ve semptomlar arasında en önemlisi santral tipte obezitedir. Santral obezite çok sık görülmektedir ve olguları klinik olarak Cushing Sendromu’ndan ayırmak güç olduğundan bu olguların taranması önerilmektedir. Hastalar genellikle halsizlik, kilo artışı ve depresyon gibi spesifik olmayan şikayetlerle başvururlar. Bunun dışında steroidlerin katabolik etkisine bağlı olarak cilt ve cilt altı dokunun incelmesi ve sonucunda gelişen pletorik yüz ve kolay berelenme, aynı mekanizmayla gelişen menekşe-mor strialar da dikkati çekmelidir(107).
Cushing Sendromu metabolik sendromun obezite, hipertansiyon, diyabet ve gonadal bozukluk gibi tüm özellikleriyle karşımıza çıkabilir. Glukokortikoidlerin glukoz kullanımını bozması nedeniyle insülin direnci ortaya çıkar. Cushing Sendromu olgularının %30-60’ında bozulmuş glikoz toleransı görülürken, aşikar diyabet görülme oranı %25-50’dir (44). Özellikle kötü kontrollü diyabet olgularında klinisyen uyanık olmalıdır (43). Cushing Sendromu’nda hipertansiyon genelde hafif derecelidir. Metabolik sendromda olduğu gibi Cushing Sendromu’nda da LDL yüksek, HDL düşüktür ve bunun sonucunda total kolesterol ve trigliserit düzeyleri yüksektir. Cushing Sendromu hastalarında da polikistik over sendromu (PKOS) olgularında olduğu gibi adet düzensizliği ve infertilite görülebilir. Altmış beş yaşın altında, nedeni açıklanamayan osteoporoz olgularında da Cushing Sendromu olasılığı düşünülmelidir. Şiddetli olabilen ajitasyonlu depresyon ya da psikoz tablosu Cushing sendromu olan hastalar için karakteristik olarak değerlendirilmektedir (45).
2.8.1.1.1.2. Subklinik Cushing Sendromu
Cushing sendromunun klinik bulguları olmaksızın hafif hiperkortizoleminin olduğu
bir durumdur. Adrenal insidentalomalarda tespit edilen fonksiyonel anormalliklerin en sık olanıdır (%5–8). Tartışmalara rağmen, subklinik Cushing Sendromu tanısı için hastada aşikar bir Cushing Sendromu kliniği olmamalı ve insidental olarak saptanan bir adenom olmalıdır (46). Çoğu olguda bazal kortizol düzeyi normal olmasına rağmen sirkadiyen ritim
kullanılan en yaygın ve sensitif test düşük doz deksametazon supresyon testidir.Subklinik Cushing Sendrom’lu hastalarda Cushing sendromunun yaygın belirtilerinin çoğunun olmamasına rağmen devamlı endojen kortizol salgılanmasının bazı klinik yansımaları vardır. Subklinik Cushing Sendromlu hastalarda hipertansiyon obezite, dislipidemi, Diyabetes Mellitus, ateroskleroz gibi metabolik durumlar aynı yaş ve cins normal populasyona göre daha fazla görülür (47). Adrenal insidentalamoya bağlı subklinik Cushing Sendromu tespit edilen 28 vakanın, 100 normal hasta ile karşılaştırıldığı bir çalışmada; subklinik Cushing Sendrom’lu hastalarda hipertansiyon, dislipidemi, bozulmuş glikoz toleransı veya Tip 2 Diyabetes Mellitus ve ateroskleroz bulguları daha fazla bulunduğu bildirilmektedir. Hastaların çoğunda hipotalamo-hipofizer-adrenal aks da süprese durumdadır (45).
Asemptomatik adrenal insidentalomalı hastalarda cushing sendromunun tanısında idrar serbest kortizol, gece tükrük kortizolu ve/veya deksametazon supresyon testi (1 mg ve 2 mg) tarama olarak kullanılır. En önemli tarama testi ise deksametazon süpresyon testidir (DST). Bir gecelik deksametazon süpresyon testinde saat 23.00’da 1 mg deksametazon oral olarak verildikten sonra ertesi sabah saat 08.00’da serum kortizolu bakılır. Bazı otorler baskılanmış plazma kortizol seviyesi için limit değerini 5 alırken, hassasiyeti artırmak için diğer bazıları 1,8 μg/dl sınırını tercih etmektedirler. DST sonrası kortizol <1.8 μg/dl gelirse Cushing dışlanabilir. DST sonrası kortizol > 5 μg/dl ise Subklinik Cushing düşünülebilir. Eğer DST sonrası kortisol 1.8-5 μg/dl arasında gelmişse klinik bulgulara göre değerlendirmek gerekir. Subklinik Cushing şüphesi varsa ilave testler yapmak gerekir. Bazı merkezler yanlış pozitifliği azaltmak için daha yüksek doz deksametazon (3 mg) kullanmaktadırlar. Bu durumda kortizol sınırını 3 μg/dl alınması önerilmektedir. Cushing sendromu tanısı için henüz bir görüş birliği yoktur. Eğer test sonucu pozitif cıkmış ise otonomiyi doğrulamak için düşük (2 gün 2 mg) ve yüksek doz (8 mg tek doz) süpresyon testlerinin de yapılması gerekir. Adrenal insidentalomalı geniş bir seride; subklinik cushing sendromlu hastaların hormonal değerlendirmede: %79’unda düşük bazal ACTH sekresyonu, %73’ünde 1 mg deksametazondan sonra kortizolda yetersiz baskılanma, %75’inde subnormal üriner kortizol sekresyonu, % 43’ünde bozulmuş kortizol sirkadiyen ritmi ve %55’ inde CRH’ya körelmiş ACTH cevabı bildirilmektedir (47, 48, 49).
Subklinik Cushingli hastaların unilateral adrenaloktomiye verilip verilmemesi halen tartışma konusudur. Subklinik Cushing Sendrom’lu hastaların ameliyatları konusunda mutlak bir fikir birliği yoktur (47). Hiperkortizoleminin uzun sureli komplikasyonlarından korumak icin hastaların opere edilmeleri düşünülebilir. Ancak hangi hastaların ileride aşikar Cushing
hastalarda ve otonom glukokortikoid sekresyonununa katkıda bulunacak hastalığı (son zamanlarda başlayan hipertansiyon, diyabet, obesite ve düşük kemik kitlesi gibi) olanlar ve gecelik deksametazon süpresyon test ve iki günlük yüksek doz deksametazon süpresyon testinde yetersiz baskılanması olanlarda adreneloktemi düşünülebilir (50).
Sürrenal bezlerin birinde kortizol üreten bir kitlesel lezyon varlığında karşı taraftaki sürrenal bezin baskılanma olasılığı yüksektir. Ameliyat sırasında veya ameliyat sonrasında adrenal yetmezlik gelişebileceği için bu durum cerrahi tedavi açısından önem teşkil etmektedir (51,52). Subklinik Cushing Sendrom’lu hastalar adrenal yetmezlik, hemodinamik krizler ve ölüm riskleri nedeniyle perioperatif glukokortikoid koruması yapılmalı ve hipotalamo-hipofizer adrenal aksı toparlanıncaya kadar izlenmelidir (50).
2.8.1.1.2. Feokromasitoma
Adrenal medullanın kromaffin dokusundan kaynaklanan tümörlerdir. Feokromasitomalar adrenal insidentalomaların %1,5 ile %23’ünü oluşturmaktadır. Hipertansiyonun %0,5’inden sorumlu ve tedavi edilebilir bir sebebidir. Endokrin hastalıklar içerisinde de hayatı en çok tehdit eden hastalık olarak görülmektedir (53). Yıllık insidansı 2-8/1.000.000 (yetişkin) kişidir. Otopsi serilerine göre prevalans %0.1’dir. Hipertansif populasyondaki prevalansı %0.2-0.6’dır. Mayo Klinik'de 1970–1998 yılları arasında yapılan çalışmada 40.078 otopsi vakasında feokromositoma oranı % 0.13 olarak bulunmuş ve bunların % 76'sı yaşamları boyunca hiç fark edilmemiş olduğu bildirilmiştir (54). Erkek ve kadında sıklığı eşittir. Her yaşta görülebilmesine karşılık ortalama tanı yaşı 40’tır (55,57).
Feokromasitomalar sporadik veya herediter sendromun bir parçası olarak ortaya çıkabilir. Bu herediter feokromositomalar; Multipl Endokrin Neoplazi Tip 2 (MEN-2A veya 2B), Nörofibromatozis Tip1 (NF–1), Von Hippel Lindau (VHL) Sendromu, Sturge Weber sendromu ve Von Recklinghausen Hastalığıdır (56). Günümüzde feokromositomaların (% 22) büyük bir oranı genetik sendromlar için tetkikler sırasında veya insidenteloma şeklinde tespit ediliyor (58). Feokromositomalar için bilinen yüzde onlar kuralı (%10 bilateral, %10 ekstra-adrenal, %10 malign) sporadik vakalar için geçerlidir. Ailesel feokromasitomada malignite %26-35’tir. Tümörün daha erken yaşlarda ortaya çıkması, bilateral, ekstra-adrenal, multifokal olma ve rekürrens sıklığı sporadik vakalara göre genellikle (farklı ailesel tiplerine göre değişmekle beraber) artmıştır. Hastalarda feokromasitoma araştırılmasını gerektiren durumlar şöyle özetlenebilir (60);
3- Ailede feokromositoma veya MEN- 2, VHL sendromu, NF 1 öyküsü 4- Adrenal insidentaloma varlığı
5- Anestezi, entübasyon, cerrahi, gebelik, anjiografi sırasında hipertansif atak ve açıklanamayan şok
6- Genç yaşta hipertansiyon (<20 yaş) 7- İdiopatik dilate kardiyomiyopati
Feokromositoma, katekolaminlerin fazla salgılanmasına bağlı klinik belirtilerle kendini gösterir. Klinik tablo hormon salgılanma özelliklerine, salgılanan hormon farklılığına göre ve bireyler arası değişen katekolamin sensitivitesinin bir sonucu olarak çok değişkendir. Bu semptomlar arasında hipertansiyon (% 56- 90), baş ağrısı (% 49-56), terleme (%44-47), çarpıntı (% 34-37), sersemlik (% 15), anksiyete (% 15), konjestif kalp yetmezliği (%12), anestezi sırasında hipertansiyon (% 7) ve bozulmuş glikoz toleransı (% 7) sayılabilir (58,59).
Günümüzde feokromositomaların (% 22) büyük bir oranı genetik sendromlar için yapılan tetkikler sırasında veya insidenteloma şeklinde tespit edilmektedir (58, 22). Genellikle semptomlar paroksismal olabilmekle beraber, hastaların yaklaşık olarak %50 civarında sürekli hipertansiyon mevcuttur (60). Fakat semptomlar atipik olabileceğinden feokromositoma tanısı için en önemli faktör klinik olarak şüphelenmektir.. Labil veya aralıklı hipertansiyonu olanlarda, hipertansiyonu olan gebelerde ve hipertansiyonlu çocuklarda şüphelenilmesi gereken ilk tanıdır.
Adrenal kitlesi olanlarda klinik olarak sessiz feokromositoma olabileceğinden bütün hastalarda mutlaka dışlanması gereklidir. “Subklinik feokromastoma” terimi adrenal bezde kitlesi olup asemptomatik seyreden ve histolojik incelemesinde feokromastoma tespit edilen hastalar için kullanılmıştır (61, 62).
Feokromasitoma tanısı 24 saatlik idrarda serbest katekolaminler (norepinefrin ve epinefrin) veya katekolamin metabolitlerinin (vanilmandelik asit, metanefrin ve normetanefrin) artmış seviyeleri ile gösterilebilir. Sensitivitesinin düşüklüğü ve yanlış pozitif sonuç oranının yüksekliği nedeniyle plazma katekolamin ölçümü önerilmemektedir (63). Görüntüleme yöntemlerinde subklinik feokromositoma şüphesi yüksek, fakat 24 saatlik idrar analizlerinde sonuç normal geliyorsa fraksiyone serbest plazma metanefrinlerinin ölçümü faydalı olabilir. Yüksek plazma fraksiyone metanefrinlerinin feokromositoma için sensivitesinin yüksek olmasına rağmen (%98–100) spesifitesi düşüktür (%85–89). Fraksiyone plazma metanefrin ölçümü sadece yüksek feokromositoma şüphesi olan hastalarda, yanlış pozitif sonucu en aza indirmek amacıyla önerilmektedir (64). Uygun şartlarda yapıldığında
sekresyon özellikleri ve metabolizmaları farklı olan heterojen tümörler olduğundan tanısal doğruluğu yüksek olan multipl testler uygulanmalıdır. Tümörün hormonal aktivitesi fluktuasyonlar gösterir ve bu durum seri katekolamin ölçümlerinde önemli değişikliklere yol açar. Kriz sırasında veya hemen sonrasında yapılan ölçümler daha değerlidir. Farklı testlerin kombinasyonu sensitivite ve spesifiteyi artırır. Fraksiyone katekolaminler (epinefrin, norepinefrin, dopamin) ve fraksiyone metanefrinler (metanefrin, normetanefrin) günümüzde HPLC (high-performance liquid chromatography) veya tandem mass spectroscopy ile oldukça güvenilir şekilde ölçülmektedir. Bu teknikler sayesinde (örneğin ilaçlara bağlı meydana gelebilen) yanlış pozitif ve yanlış negatif sonuç riski azalmıştır. Hangi metotla ölçülürse ölçülsün değerlerde 2- 3 katı yükselme tanı için çok anlamlıdır. Hastalara test öncesi üç gün fenolik asit içeren vanilya, muz, kahve gibi gıda ve içeceklerden yoksun özel bir diyet uygulanmalıdır. Ayrıca beta adrenerjik blokerler ve monoaminoksidaz (MAO) inhibitörleri gibi ilaçların da kullanılmaması gerekmektedir. Tablo 2’de feokromasitoma tanısında kullanılan parametrelerin sensitivite ve spesifite oranları görülmektedir.
Tablo- 2. Feokromasitomada artış gösteren hormon ve metabolitleri
Belirteç Sensitivite(%) Spesifite(%)
Plazma serbest metanefrin 99 82
Plazma katekolaminleri 92 72
İdrar fraksiyone metanefrin 97 45
İdrar katekolaminleri 91 75
Plazma normetanefrin 97 96
Vanil mandelik asit (VMA) 77 86
İdrar testleri sıklıkla başlangıç testi olarak kullanılan testlerdir. Yeterli idrar biriktirildiğinden emin olmak için birlikte idrar kreatinin ölçümü yapılır. Ancak plazma testleri ölçümü daha kolay ve pratiktir. İdrar VMA ölçümü en yüksek yanlış negatif oranına (%14) sahiptir ve tarama testi olarak önerilmez. Bununla birlikte tüm bu testler yükseldiklerinde mükemmel spesifiteye sahiptirler. Yanlış pozitiflik sıklığı yeni ölçüm metotları ile azalmış olmasına rağmen stres (egzersiz, akut miyokard enfarktüsü, hipoglisemi gibi), ilaçlar (levodopa, labetolol, trisiklik antidepressanlar, sempatomimetikler gibi), uygunsuz örnekleme hataları ve diyet faktörleri gibi katekolamin artışı durumlarına dikkat edilmelidir. Antihipertansifler içinde ölçümlerle en az etkileşen selektif α1-bloker (doksazosin) ve kalsiyum kanal blokerleridir. Bu testlerde sınırda yükseklik genellikle yanlış pozitifliği gösterir. Böyle durumlarda test özellikle farklı metotlarla tekrar edilir. İdeal olarak
test sırasında ölçümleri etkileyebilecek ilaçlar kesilir. Tablo 3’te katekolamin ve metanefrinlerde artışa yol açabilecek ilaçlar gösterilmektedir (108).
Tablo- 3. Katekolamin ve metanefrinlerde artışa yol açabilecek ilaçlar
Trisiklik antidepresanlar Levodopa
Adrenerjik reseptör agonisti içeren ilaçlar (dekonjestanlar) Amfetaminler
Buspiron ve psikoaktif ajanların çoğu Proklorperazin
Rezerpin
Klonidin kesilmesi Etanol
Asetaminofen
Normotansif ve asemptomatik bir hastada normal plazma katekolamin düzeyleri feokromositoma tanısını ekarte ettirmez, fakat hipertansif ve semptomatik bir hastada tanıdan büyük ölçüde uzaklaştırır. Diğer bir deyişle, tipik ataklar tanımlayan bir hastada söz konusu atakların sebebi feokromositoma ise o hastada biyokimyasal testlerin normale göre çok (örneğin >10 kat) artmış olması gereklidir. Ayrıca semptomatik bir hastada tümör çapı tipik olarak 4,5 cm’ in üzerindedir. Semptomatik bir hastada tümör lokalize edilemiyorsa tanı tekrar gözden geçirilmeli ve biyokimyasal anormallikler için diğer sebepler araştırılmalıdır. İnsidentalomalı asemptomatik bir hastada (henüz prebiyokimyasal safhada iken) tüm biyokimyasal tester normal olabilir (65).
Biyokimyasal olarak tanı konduktan sonra tümörün lokalizasyonu yapılmalıdır. Öncelikle batın ve adrenaller BT veya MR ile araştırılmalıdır. Tümörlerin çoğu 3 cm’nin üzerinde olduğu için kolaylıkla görülebilir. Ancak MEN-2 sendromundaki tümörler daha küçük olabildiğinden görülemeyebilir. Bu durumda I–131 metaiodobenzil guanidin (MIBG) veya In- 111 pentetiroitide (octreoscan) ile tarama yapılabilir (66).
2.8.1.1.3 Primer Hiperaldosteronizm (Conn Sendromu)
Zona glomeruloza aktivitesinde patolojik artış sonucu meydana gelmektedir. İlk defa
1955 yılında Conn tarafından tanımlanmıştır. 30- 50 yaşları arasında sık görülür. Kadınlarda erkeklere oranla 3 kat daha fazla görülmektedir (67). Genelde 2 cm’ den küçük kitleler olarak karşımıza çıkmaktadır. Primer hiperaldosteronizm (PH) adrenal bezlerde aşırı aldosteron
yüksek aldosteron sekresyonu ile karakterize bir sendromdur (68). Sekonder hiperaldosteronizm ise bir eksternal uyarı sonucunda renin-anjiyotensin-aldosteron sistemindeki kompansatuar reaksiyon sonucu oluşur. PH prevalansının hipertansif hasta populasyonunda oranı %0,05 ile %2,2 arasında olmakla birlikte son zamanlarda bu oranın %15’e kadar yükseldiği belirtilmiştir. Hipertansif hasta populasyonlarında plazma aldosteron/plazma renin aktivitesi oranının bir tarama testi olarak daha sık kullanılmasınında bu artışta payı olduğu ifade edilmektedir (69).
PH ‘nin nedenleri arasında aldosteron salgılayan adenom (%60- 80), bilateral adrenokortikal hiperplazi (idiopatik hiperaldosteronizm, IHA) (%20), aldosteron salgılayan adrenokortikal karsinom (%1), renine cevap veren adrenokortikal adenom (<%1) ve primer adrenokortikal hiperplazi yer alır (<%1) (70).
Spontan olarak hipopotasemi görülmesi primer aldosteronizmin önemli bir bulgusudur. Adrenal insidentaloma vakalarında hasta normotansif ise ve potasyum düzeyi 3,9 mEq/L’nin üzerinde ise hiperaldosteronizm araştırmak gereksizdir. Adrenal kitlesi olan hastalarda hipertansiyon, hipokalemi ve bununla uygun olmayan kaliürezis olması durumunda primer aldosteronizm açısından araştırma yapılması gerekmektedir (71, 72, 73, 74). En fazla görülen klinik semptomlar; hipertansiyon, kas zayıflığı, polidipsi, poliüri, baş ağrısı ve hipokalemik alkalozdur. Sol sürrenal bezde sağ sürrenal beze göre daha sık rastlanır (75).
Plazma aldosteron düzeyi (PAD) /pazma renin aktivitesi (PRA) oranı renin-anjiyotensin-aldosteron aksının bozukluklarını araştırmak için başvurulacak hassas ve özgül bir testtir. Aldosteron ng/dl, PRA ise ng/dl/saat olarak bakılmalıdır. Bu oran 20’nin altında olmalıdır. Plazma aldosteron düzeyinin normal aralıkta fakat üst çeyrekte olması yanında PAD/PRA oranının 20’nin üzerinde olmasıyla primer hiperaldosteronizm (PH) belirleyicilik oranı % 90’nın üzerindedir. Primer hiperaldosteronizm hastalarında plazma renin düzeyi genellikle normalin altındadır. PAD/PRA oranının 40’ın üstünde olması otonom aldosteron salınımını göstermesi açısından %96- 99 duyarlılığa sahiptir. PAD/PRA oranı yüksek olan hastalara 25 mg kaptopril, fludrokortizon veya tuz yükleme testi yapılarak tanı doğrulanmalıdır (73, 74).
PAD ve PRA oranına bakmak için yapılan ilk taramada sabah 8- 10 arası yapılacak örnek alımı yeterlidir. Bu test için postür değişimi önemli değildir. Mineralokortikoid reseptör antagonistleri (spiranolakton ve eplerenon), renin inhibitörleri ve yüksek doz amilorid alımı (5 mg/gün üzerinde) PH tanısı tarama testi değerlendirmesinde önemlidir ve 6 hafta önce kesilmelidir. Yalnız bu orana bakılırken hastaların hipopotasemileri düzeltilmelidir. ACE
yükseltebilirler. Bu ilaçları kullanırken elde edilen PRA daha yüksek olabilir, PAD/PRA bu nedenle daha düşük olabilir. Fakat bu ilaçları alırken PRA’nin düşük olması PH tanısı olasılığını arttırır. PAD/PRA oranı adrenerjik inhibitör kullananlarda yüksek çıkabilir, fakat PAD 15 ng/dl’nin altındadır. PH’li hastaların tamamına yakınında PRA düzeyi 1 ng/ml/saatin altındadır.
Eğer primer aldosteronizm tespit edilmiş ama radyolojide lateralizasyon yapılamıyorsa adrenal venöz örnekleme yapmak gerekir. Adrenal kitlenin görülmüş olması onun mutlaka fonksiyone olduğunu göstermez. Bu durumda önemli olan aldosteronomayı bilateral adrenal hiperplaziden ayırt etmektir (76). Bu iki hastalık arasında ayırım yapmak çok önemlidir. Çünkü aldosteron üreten adenomun(aldosteronoma) cerrahi tedavisi çok iyi sonuç verirken adrenal hiperplazinin cevabı hiçte yüz güldürücü değildir (76). Aldosteron üreten kanserler son derece nadirdir (77).
2.8.1.1.4. Diğer Hormonal Aktif Durumlar
Sex hormonu salgılayan tümörler son derece nadir olmakla birlikte hastaların büyük bir bölümü genellikle erken dönemde semptomatik olur. Virilizasyon veya feminizasyon ile kendini belli ettiğinden genellikle insidental olmazlar. DHEA-S artışı androjenlerin varlığını düşündürür ve adrenal kitlenin büyüklüğü ile orantılı bir seviye göstermektedir. Testesteron ve estradiol ölçümü adrenal insidentaloma vakalarında virilizasyon veya feminizasyon olduğu durumlarda ve kanser şüphesi varsa yapılması uygun görülmektedir. Ayırıcı tanı için serum 17-OH progesteron değeri alınır ve kortikotropin stimülasyon testi yapılır (78).
2.8.1.1.4.1. Adenomlar
Adenomlar normal olarak adrenal hücrelere benzeyen benign bir neoplazi olarak tarif edilir. Mikroskobik olarak adenom zona fasikülata, zona glomeruloza veya daha sıklıkla her ikisinin birlikte bulunduğu bir görünüm gösterebilir (79). Genellikle kendini fonksiyonel otonomi ile gösterir (9). Adenomlar çoğunlukla 2 cm’yi aşmamakla birlikte tektir ve tipik olarak küçük lezyonlardır (80, 81). İnsidentaloma vakalarının büyük çoğunluğunu oluştururlar. Kitle boyutları genellikle küçük olduğundan gerçek adenom, fokal hiperplazi, aksesuar kortikal nodül ayırımı güç olabilir. Çoğu nonsekretuar olmakla birlikte %5 ile %47’si kortizol, %1,6 ile %33’ü mineralokortikoid sekrete ederler (82).
Normal populasyondaki insidansı milyonda 0,6-2 civarındadır. Adrenokortikal karsinomlar, kanserlerden ölümlerin % 0,2’sine sebep olurlar. Her yaşta görülebilmesine rağmen 40 yaşından sonra görülme sıklığı artar. En çok 5. dekadda görülür (83, 84, 85). Adrenokortikal karsinomlar, malignitesi oldukça yüksek, prognozu kötü ve agresif neoplazmlardır (86). Wajchenberg ve arkadaşlarının 920 adrenokortikal karsinomlu hastayı dahil ettikleri çalışmalarında ortalama kanser tanı yaşının 45 olduğunu bildirmişlerdir. Bir meta analizde de 1800’den fazla hastanın dahil edildiği çalışma sonucunda adrenal kanserlerin kadınlarda erkeklerden daha sık görüldüğü ve hastaların %59’unun kadın olduğu belirtilmiştir (87).
Primer adrenal karsinom prevelansı kitle boyutu ile doğrudan ilişkili olmasına rağmen çocukluk çağında görülen kitlelerde malignite oranı daha fazla olduğu için kitle boyutu uygun kriter olarak kabul edilmemektedir (71). Adrenokortikal kitleler sıklıkla büyük boyutlara ulaşırlar. Brigham ve Women’s Hospital’de sürrenal korteks karsinomu tanısı alan 41 vakalık araştırmada tümörün büyüklüğünün 2,5 cm’den 30 cm’ye kadar ulaştığı belirtilmiştir (87). Tablo 4’te kitle çapı ile adrenokortikal karsinom (ACC) ilişkisi belirtilmiştir.
Tablo- 4 Kitle çapı adenom-ACC ilişkisi
Tümör çapı (cm) Adenom ACC*
<4 %65 %2
4,1- 6 %28 %6
>6 %18 %25
*Kitle boyutu dikkate alınmazsa karsinom prevalansı %0,75’tir.
ACC’ların %80’i fonksiyonel kitleler olarak karşımıza çıkabileceği gibi nonfonksiyonel olarak da ortaya çıkabilirler. Erkeklerde nonfonksiyonel tümör prevalansı kadınlara göre daha yüksektir. ACC’ ların yaklaşık % 45’i sadece glukokortikoid, %45’i glukokortikoid ve androjen, %10’u ise sadece androjen salgılarlar. Sadece mineralokortikoid salgılayan tümörler %1’den daha azdır. Androjen salgılayan tümörler çocuklarda sık görülür ve virilizasyona sebep olurlar (88).
ACC’ların tek küratif tedavisi cerrahidir. Genellikle laparoskopik veya lomber girişimler pek uygun olmadığından transabdominal yol tercih edilir. Tümörler genelde büyük boyutlara ulaşabildiklerinden ve çevre dokulara invazyon yaptıklarından çoklu organ rezeksiyonları gerekebilir. Adjuvan terapide en fazla tercih edilen kemoterapötik ilaç
kötü olmakla birlikte ortalama sağ kalım 18 aydır. Sağkalım süresi için hormonal olarak aktif olup olmaması önemli değildir (88).
2.8.1.1.5. Hormonal Aktivitesi Olmayan Durumlar 2.8.1.1.5.1. Miyelolipom
Miyelolipom ilk defa Gierke tarafından tanımlanmıştır (89). Nadir olarak görülür. Miyelolipom, olgun yağ hücreleri ve hematopoetik dokudan meydana gelen, biyokimyasal olarak nonfonksiyonel bir tümördür ve genellikle benigndir (90). Boudreax ve arkadaşları, gerek hematopoetik, gerek sürrenal komponentleri ihtiva eden proliferatif oluşum olarak tarif etmişlerdir. Miyelolipom, normal kemik iliğine benzer; mezenkimal orjinli olduğu düşünülmektedir (91). Myelolipomlar genellikle 5 cm’ den küçüktürler, çok yavaş büyürler, ancak 5 kilograma varan dev kitleler de bildirilmiştir. Büyük olan kitleler ağrılı olabilirler veya retroperitoneal kanama ile kendini gösterebilirler. Genellikle tedavi gerektirmezler.
Ancak semptomatik olan ve hızlı büyüyen kitleler cerrahi olarak çıkarılmalıdır (92).
2.8.1.1.5.2. Kistler
Sürrenal kistler seyrek görülen benign lezyonlardır (93). Genelde nonspesifik abdominal ağrı veya bel ağrısının ultrasonografi (USG), bilgisayarlı tomografi (BT), manyetik rezonans görüntüleme (MRG) veya intravenöz piyelografi (IVP) ile araştırılması esnasında ortaya çıkar (93). Herhangi bir yaşta görülebilmesine rağmen 30- 50 yaşlarında ve kadınlarda erkeklere göre 3 kat daha sık görülmektedir. Her iki sürrenal bezi eşit olarak tutar (93, 94). Küçük sürrenal kistler klinik olarak sessiz olmakla birlikte büyüdükleri zaman semptom verirler. Abdominal kitle, komşu organlara bası nedeniyle bulantı, kusma, epigastrik ağrı gibi gastrointestinal sistem belirtileri ve bel ağrısına neden olabilir (95, 96). Kistler endotelyal, epitelyal, parazitik kistler veya psödo kistler şeklinde karşımıza çıkabilir. Epitelyal kistler; kistik adenomlar, glandüler veya retansiyon kistleri ya da embriyonel artıkların kistik değişimi şeklinde olabilirler. Parazitik kistler ise genellikle Echinococcus granülosus enfeksiyonuna bağlı olarak meydana gelirler (97, 98)
2.8.1.1.5.3. Metastazlar
Akciğer, meme kanserleri, lenfomalar adrenal metastazların çoğunu oluşturur.
Pankreas, kolon ve over kanserleri malign melanomlar adrenal bezlere metastaz yapabilirler. 1000 karsinomlu hastanın otopsi incelemesinde adrenal bezlere %27 oranda metastaz olduğu
bildirilmiştir. Nadiren olarak adrenal kitleler primeri bilinmeyen metastatik bir kanser odağı şeklinde de bulunabilir.
2.8.1.1.5.4. Diğer Nedenler
Hematomlar genellikle antikoagülan ilaç kullanımına, koagülasyon sistemini
etkileyen hastalıklara ve nadiren travmaya bağlı olarak gelişebilir. Ayrıca literatürde 80’e yakın primer adrenal lenfoma bildirilmiştir. Bazı lenfomalarda kür sağlanabildiği için bu nadir durum önemlidir. Histoplazmozis ve özellikle son zamanlarda artış gösteren tuberküloz gibi enfeksiyonlar da adrenal bezlerde kitle ile ortaya çıkabilirler (68, 99).
2.8.1.2 Adrenal Kitlelerin Radyolojik Değerlendirilmesi
Adrenal bezin geleneksel radyolojik tanı yöntemleri genellikle zordur. En çok
kullanılan radyolojik tanı yöntemleri arasında USG, BT, MRG ve PET bulunmaktadır.
USG sensitivite ve spesifite olarak BT ve MR’a göre daha düşüktür. Altmış bir hastadan oluşan bir seride 3 cm’den büyük olan tüm adrenal kitleler USG ile saptanmış, 3 cm’den küçük olanların ise % 65’i saptanabilmiştir. Adrenal kitlenin çap ölçümü USG ve BT’de korelasyon gösterir. Bu nedenle adrenal kitlelerin büyüklüğünün takibinde kullanılabilir. BT adrenal bezi görüntülemede ideal bir yöntemdir. Tomografide kontur düzensizliği, komşu dokulara invazyon, retroperitoneal lenf nodu varlığı adrenal karsinom için önemli ipuçlarıdır.
PET’ te adrenal insidentalomalarda kullanılan diğer bir tanı yöntemidir. Malign tümörlerde deoksiglikoz tutulumunun artması nedeni ile glikolitik metabolizma hızlanmıştır. Adrenal kitlede tutulumun fazla olması testin pozitif olduğu anlamına gelir ve benign-malign ayrımı için faydalı bir testtir. BT ve MRG bulguları ile kara verilemeyen vakalarda değerlidir (101).
Tespit edilen kitlenin yağ oranı tomografik dansiteyi belirler. Yağ oranı arttıkça tomografik dansite düşer (Hounsfield ünitesi, HU). Benign kitlelerde yağ oranı yüksek, malign oluşumlarda ise yağ içeriği oldukça düşük olur (39). Bu gerçekten yola çıkarak yapılan analizlerde, literatürde bugüne kadar 0 HU dansitesinin altında hiç bir adrenal malignensinin rapor edilmediği dikkat çekmiştir. Kitlenin dansitesi ortalama 10 HU’den küçük ise; “adenom” olarak kabul edilir. 10 HU sınır değer; %71 sensitivite, %98 spesifiteye sahiptir. Adenomların %30’u 10 HU’den fazla dansitededir. Bu nedenle; diğer lezyonlardan
%98 oranında benigndir. Yapılan çalışmalarda dansitesi 20 HU’nun üzerinde olan adrenal kitleleri malign kabul etmek gerektiği görüşü savunulmaktadır. Fakat bazı benign adrenal kitlelerde (kanamalar, özellikle akut fazda) tomografik dansitenin oldukça yüksek olabileceği unutulmamalıdır (40). Bugün için net bir görüş birliği olmamakla birlikte radyologlar tomografik dansitesi 4-20 HU arası vakaları şüpheli olarak değerlendirmekte ve MR önermektedirler. MR’ da doku özgüllüğü daha yüksektir. MR ile karaciğer, adrenal-dalak, adrenal- kas kitlesi sinyal intensite oranları hesaplanabilir. Bu oranlar adrenal kitlenin kaynağı hakkında bilgi verebilir. Fakat genelde kitle boyutu 4–6 cm olan vakalarda malign-benign ayırımında görüntüleme yöntemleri hassas değildir. Daha büyük kitleler için ise görüntüleme bulgularından bağımsız olarak cerrahi tavsiye edilmelidir (64).
Adrenal kitlenin maksimum çapı malignensi için belirleyici olabilir. 887 adrenal insidentalomalı hastanın değerlendirildiği bir çalışmada; kitle boyutunun 4 cm’den daha fazla olması adrenokortikal karsinomları %90 sensitivite ile tespit ettiği görülürken daha düşük spesifiteye sahip olduğu bildirilmektedir. Bu nedenle, adrenal kitle boyutu, tedavi kılavuzunda tek parametre olarak kullanılmamalıdır. Özellikle, kitlenin radyolojik özellikleriyle birlikte değerlendirilmelidir. Malign-benign ayırımında görüntüleme yöntemlerinden elde edilen bulgulardan yararlanılmalıdır (100).
Benign adenomlar oval veya yuvarlak, genellikle soliter, unilateral ve homojen
yapıda kitlelerdir. Genellikle düzgün konturlu ve sınırları belirgin olup 4 cm’den küçük kitleler olarak karşımıza çıkarlar. Kontrastsız BT’de lezyon < 10 HU ise lipitten zengin adenom olduğu düşünülür. Kontrastsız BT’de dansite >10 HU ise %10–40 olasılıkla lipitten fakir adenom olabilir veya adenom dışı bir kitledir. Bu durumda ayırıcı tanı için kontrastlı BT gereklidir. İntravenoz kontrast madde sonrası dansite <30–40 HU ve kitle kontrast maddeyi yoğun tutuyor, ancak kontrast madde hızla kayboluyorsa adenomdur. Benign adenomlar MR’da sinyal kaybına uğrarlar (106).
Feokromasitomalar genellikle 4 cm’den büyük, soliter, unilateral, oval veya yuvarlak kitleler olarak karşımıza çıkar. Sınırları düzenli ve heterojen kistik yapıdadır. Hemoraji, kalsifikasyon, kistik nekrotik alanlar içerebilir. Dansitesi; kontrastsız BT’de >20 HU, 30. dakikadaki geç çekimlerde >40 HU’dir. Hipervaskularizasyon nedeni ile kontrastı yoğun olarak tutar. BT’ nin adrenal feokromositoma tayininde sensitivitesi % 93- 100’ dür. MR’ da sinyal kaybına uğramaz. T2’de karaciğere göre hiperintenstir (106)
Adrenokortikal karsinomlar genellikle yoğun, soliter, unilateral, heterojen, düzensiz konturlu, kitleler olarak karşımıza çıkarlar. Genellikle 4 cm’den büyük kitlelerdir. Komşu
BT’de >10 HU, 30. dakikadaki geç çekimlerde >40 HU’ dir. MR’ da T2’ de karaciğere göre hiperintenstir ve MR’ da sinyal kaybına uğramazlar (68).
Metastazlar ise düzensiz ve homojen olmayan yapıya sahip olup sıklıkla 3 cm’den küçük ve bilateraldir. Dansitesi; kontrastsız BT’de >10 HU, 30. dakikadaki geç çekimlerde >40 HU’ dir. MR’da sinyal kaybına uğramazlar. T2’ de karaciğere göre hiperintenstir (106).
2.8.1.3. Moleküler Belirteçler
Adrenokortikal ve medüller kitlelerin diferensiasyonu için immunolojik belirteçler,
DNA ploidi, hücre faz belirteçleri ve onkojenik incelemeler mevcuttur. Bu belirteçler şüpheli durumlarda destekleyici niteliktedir. Tanı koymak için tek başına kullanılamaz (102).
2.8.1.4. İğne Aspirasyon Biyopsisi
Benign adrenal kitlelerle adrenal karsinom ayırımını yapamaz. Adrenal tümör ile
adrenal metastaz ayırımını yapabilmektedir. Tecrübeli sitopatolojilerde bu oran neredeyse %100’e kadar çıkmaktadır (103). İğne aspirasyon biyopsisi adrenale dışarıdan metastaz şüphesi olduğunda veya bilinen bir kanserin evrelendirilmesinin yapılmasında endikasyonu vardır. Maligniteyi göstermedeki sensitivitesi % 81-100’dür (104). En sık komplikasyonu pnömotorakstır. Bakteriyemi, pankreatit, kanama, iğne yolunda tümör ekilmesi gibi komplikayonlar olabilir. İğne aspirasyon biyopsisi yapılmadan önce mutlaka feokromasitoma ekarte edilmelidir. Aksi takdirde hipertansiyon krizine sebep olabilmektedir (22).
2.8.1.5. Laparaskopik ve Laparatomik Yaklaşım
Laparaskopi veya laparatomi patolojik tanı veya cerrahi tedavi için halen
günümüzde kullanılan yöntemlerdir. Sitopatolojik tanı açısından materyal temini içinde başvurulan yöntemler arasında yer almaktadır (105).
2.8.2. Tedavi
Adrenal insidentalomada cerrahi tedavi kararına lezyonun malignite risk faktörleri
ve fonksiyonel durumuna göre karar verilir.
2.8.2.1 Tek Taraflı Adrenal Kitleler
Feokromasitomalı ve primer aldosteronizmli bütün hastalar cerrahiye verilmelidir.
subklinik cushingli hastaların ameliyatları konusunda mutlak bir fikir birliği yoktur. Hiperkortizoleminin uzun süreli komplikasyonlarından korunmak için hastaları opere