T.C.
EGE ÜNİVERSİTESİ TIP FAKÜLTESİ
ÇOCUK SAĞLIĞI VE HASTALIKLARI ANABİLİM DALI Prof. Dr. Savaş KANSOY
FENİLALANİN KISITLI DİYET ALAN FENİLKETONÜRİ TANILI
HASTALARIN NÜTRİSYONEL DURUMLARININ DEĞERLENDİRİLMESİ
UZMANLIK TEZİ
Dr. Hüseyin DERVİŞOĞLU
TEZ DANIŞMANI
Prof. Dr. Mahmut ÇOKER
ÖNSÖZ
Uzmanlık eğitimim boyunca bilgi ve deneyimlerinden faydalandığım, tezimin her aşamasında büyük yardım ve desteğini gördüğüm Sayın Prof. Dr. Mahmut Çoker’e,
Asistanlığım süresince yetişmemde büyük katkıları olan, bilimsel ve klinik deneyimleri ile her zaman yol gösteren başta Çocuk Sağlığı ve Hastalıkları Anabilim Dalı Başkanımız Sayın Prof. Dr. Savaş Kansoy olmak üzere tüm öğretim üyelerimize ve uzmanlarımıza,
4 yıl boyunca birlikte çalıştığım başta Dr. Eser Akkuş, Dr. Caner Turan, Dr. Metin Delebe, Dr. Ahmet Yıldırım olmak üzere tüm asistan arkadaşlarıma ve klinik görevlilerine,
Tez çalışması süresince yardımlarından dolayı EÜTF Çocuk Sağlığı ve Hastalıkları Metabolizma ve Beslenme Bilim Dalı’nda görevli Doç. Dr. Sema Kalkan Uçar, Uzm. Dr. Ebru Canda olmak üzere tüm çalışanlarına, Klinik Biyokimya Anabilim Dalı öğretim üyesi Prof. Dr. Sara Habif’e ve Uzm. Diyetisyen Yasemin Atik Altınok’a,
Klinik Biyokimya laboratuvarı çalışanlarına,
Her zaman yanımda hissettiğim, asistanlık eğitimim boyunca hiçbir fedakarlıktan kaçınmayan anneme ve babama sonsuz teşekkürlerimi sunarım.
Dr. Hüseyin DERVİŞOĞLU
Bu çalışma EÜTF Araştırma Projeleri Alt Komisyonu tarafından desteklenmiştir. Proje No: 2015-TIP-075
İÇİNDEKİLER
KISALTMALAR ... iv
TABLOLAR, ŞEKİLLER VE RESİMLER ... vii
1. GİRİŞ ve AMAÇ ... ...1
2. GENEL BİLGİLER ... 3
2.1. Fenilalanin metabolizması ve bozuklukları ... 3
2.2. Hiperfenilalaninemi ... 4 2.2.1. Fenilketonüri ... 5 2.2.1.1. Fenilketonürinin Sıklığı ... 6 2.2.1.2. Tanı ve Sınıflandırma ... 7 2.2.1.3. Genetik danışma ... 9 2.2.1.4. Tedavi ve Prognoz ... 9
2.2.2. Tetrahidrobiyopterin (BH4) metabolizması bozuklukları ... 16
2.2.2.1. BH4 metabolizması bozuklukları; Klinik ve Tanı ... 16
2.2.2.2. BH4 metabolizması bozuklukları ;Tedavisi ... 19
2.2.3. Maternal Fenilketonüri ... 20
2.3. Nutrisyonel değerlendirme ... 20
2.3.1. Fenilketonüri ve protein metabolizması ... 20
2.3.2.Fenilketonüri ve mineral – vitamin değerlendirmesi ... 21
2.3.3. Fenilketonüri ve kolesterol metabolizması ... 24
2.3.4. Fenilketonüri ve kemik metabolizması ... 25
3. GEREÇ VE YÖNTEM ... 26 3.1. Çalışma Grubu ... 26 3.1.1. Kapsam ... 26 3.1.2. Çalışmanın yürütülmesi ... 26 3.2. Yöntemler ... 28 3.3. İstatistiksel Analiz ... 30 4. BULGULAR... 31 5. TARTIŞMA ... 58 6. SONUÇLAR ... 67 7. KAYNAKLAR ... 70 8. TÜRKÇE ÖZET ... 84 9. İNGİLİZCE ÖZET ... 86 10.EKLER ... 88
KISALTMALAR
% : Yüzde
< : Küçüktür > : Büyüktür
25 OH Vit D : 25 Hidroksi D vitamini 5-HIAA : 5 Hidroksi indol asetik asit 7,8-BPH2 : 7,8 dihidrobiopterin A vit : A vitamini
AADC : Aromatik aminoasit dekarboksilaz ABD : Amerika Birleşik Devletleri
AR : Aldoz redüktaz
arGTPCH : GTP siklohidrolaz eksikliği (otozomal resesif) ATP : Adenozin trifosfat
BH2 : Dihidrobiyopiterin BH4 : Tetrahidrobiopterin C vit : C vitamini Ca+2 : Kalsiyum CoA : Koenzim A CR : Karbonil redüktaz DHFR : Dihidrofolat redüktaz DHPR : Dihidropteridin redüktaz dl : Desilitre
DRD : Dopa duyarlı distoni E vit : E vitamini
ECLIA : Elektrokemilüminesans immünolojik ölçüm yöntemi EEG : Elektroensefalogram
FA : Fenilalanin
FAH : Fenilalanin hidroksilaz
Fe : Demir
Fe +2 : Ferröz Fe +3 : Ferrik
gr : Gram
GMP : Glikomakropeptid GTP : Guanozin trifosfat
GTPCH : Guanozin trifosfat siklohidrolaz
H2O : Su
Hb : Hemoglobin
Hcy : Homosistein
HFA : Hiperfenilalaninemi
HMG CoA : 3-hidroksi 3-metil glutaril Koenzim A HPLC : Yüksek performanslı likid kromatografi HVA : Homovalinik asit
IQ : Intelligence Quotient Kcal : Kilokalori
Kg : Kilogram
L : Litre
LNAA : Büyük nötral aminoasidler m2 : metrekare
max : Maksimum
mg : Miligram
min : Minimum
mL : Mililitre
MMA-CoA : Metilmalonil CoA MR : Manyetik Rezonans
mRNA : Messanger RNA
mTHF : Metil tetrahidrofolat
nmol : Nanomol
OMIM : Online Mendelian Inheritance in Man PAH : Fenilalanin hidroksilaz
PAL : Fenilalanin amonya liyaz
PCD : Pterin-4a-karbinolamin dehidrataz
Pg : Pikogram
PKU : Fenilketonüri
PTP : 6– piruvoil – tetrahidropterin PTPS : Pirüvoyil tetrahidrobiopterin sentaz SDS : Standart deviasyon skoru
SOD : Süperoksit dismutaz
SPSS : Statisitical package for social sciences SR : Sepiapterin redüktaz
Suc-CoA : Süksinil CoA
TDBK : Total demir bağlama kapasitesi TH : Tirozin hidroksilaz THF : Tetrahidrofolat TS : Transferrin satürasyonu Tyr : Tirozin v.b. : ve benzeri VA : Vücut ağırlığı Vit B12 : Vitamin B12 Vitamin D2 : Ergokalsiferol Vitamin D3 : Kolekalsiferol VKİ : Vücut kitle indeksi μmol : Mikromol
TABLOLAR, ŞEKİLLER VE RESİMLER
TABLOLAR
Tablo 1. Hiperfenilalaninemi sınıflandırması
Tablo 2. Primer HFA nedeni olan hastalıklar ve fizyopatolojilerine yönelik terminoloji Tablo 3. FKÜ sıklığı
Tablo 4. Farklı ülkelere göre önerilen hedef kan FA düzeyleri Tablo 5. Günlük FA tüketimi ( yaşa göre )
Tablo 6. Günlük FA tüketimi ( Kan FA düzeylerine göre ) Tablo 7. Anne sütü ve inek sütü FA içerikleri (mg/100 ml) Tablo 8. Hastaların beslenme takip sıklığı
Tablo 9. Hastaların poliklinik izlem sıklığı Tablo 10. Hedef kan FA değerleri
Tablo 12. Bazal beslenme verileri
Tablo 13. Bazal beslenme verilerinin düzeyleri (düşük/normal/yüksek) Tablo 14. Bazal büyüme verileri
Tablo 15. Bazal büyüme verilerinin düzeyleri (düşük/normal/yüksek) Tablo 16. Bazal kan beslenme parametreleri
Tablo 17. Bazal kan beslenme parametrelerinin düzeyleri (düşük/normal/yüksek) Tablo 18. Hastaların geçmiş değerlendirme demografik özellikleri
Tablo 19. Geçmiş beslenme verileri
Tablo 20. Geçmiş beslenme verilerinin düzeyleri (düşük/normal/yüksek) Tablo 21. Geçmiş büyüme verileri
Tablo 22. Geçmiş büyüme verilerinin düzeyleri (düşük/normal/yüksek) Tablo 23. Geçmiş kan beslenme parametreleri
Tablo 24. Geçmiş kan beslenme parametrelerinin düzeyleri (düşük/normal/yüksek) Tablo 25. Her iki grubun demografik özellikleri
Tablo 26. Her iki grubun beslenme verilerinin karşılaştırılması
Tablo 27. Her iki grubun beslenme verilerinin kategorilere (düşük/normal/yüksek) dağılımının karşılaştırılması
Tablo 29. Her iki grubun büyüme verilerinin kategorilere (düşük/normal/yüksek) dağılımının karşılaştırılması
Tablo 30. Her iki grubun kan beslenme parametrelerinin karşılaştırılması
Tablo 31. Her iki grubun kan beslenme parametrelerinin kategorilere (düşük/normal/yüksek) dağılımının karşılaştırılması
Tablo 32. Kan FA ve günlük FA tüketimi ile tüm parametrelerin ilişkisi (Bazal veriler) Tablo 33. Kan FA ve günlük FA tüketimi ile tüm parametrelerin ilişkisi (Geçmiş veriler) Tablo 34. Diyet tüketim listelerindeki FA değerleri ve kan FA değerlerine göre beslenme
faktörleri ile ilişkileri
Tablo 35. Diyet tüketim listelerindeki FA değerleri ve kan FA değerlerine göre büyüme faktörleri ile ilişkileri
Tablo 36. Diyet tüketim listelerindeki FA değerleri ve kan FA değerlerine göre kan nütrisyonel parametreleri ile ilişkileri
ŞEKİLLER
Şekil 1. Fenilalanin Metabolizması
Şekil 2. PAH ve PAL enzimlerinin farklılıkları Şekil 3. Tetrahidrobiopterin metabolizması
Şekil 4. BH4 eksikliği olan hastaların algoritmik yaklaşımı Şekil 5. FKU ve BH4 eksikliği ayırıcı tanısı
Şekil 6. B12 vitaminin biyokimyasal yolağı
Şekil 7. Hastaların bazal değerlendirme yaşları ( ay ) ve tanı yaşları ( gün ) Şekil 8. Olguların bazal değerlendirme yaş aralığı
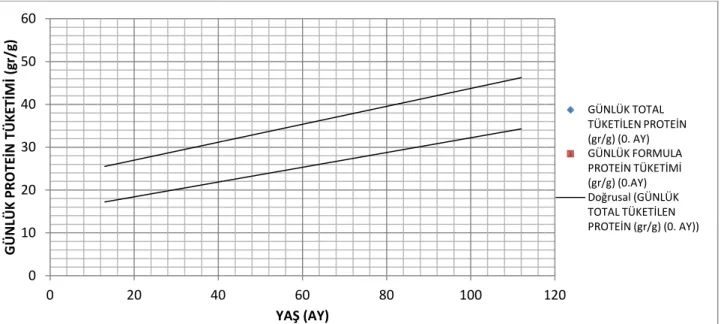
Şekil 9. Yaşa göre günlük protein ve formula protein tüketimi (bazal) Şekil 10. Bazal vücut ağırlığı SDS, boy SDS, VKİ SDS değerleri
Şekil 11. Yaşa göre günlük protein ve formula protein tüketimi (geçmiş) Şekil 12. Geçmiş vücut ağırlığı SDS, boy SDS, VKİ SDS değerleri
RESİMLER
1. GİRİŞ ve AMAÇ
Fenilketonüri sık görülen bir aminoasit metabolizma bozukluğudur. Fenilalanin hidroksilaz gen mutasyonu ile karakterize otozomal resesif geçiş gösteren intoksikasyon tipi metabolik hastalık olarak da tanımlanabilir (1). Karaciğerden salgılandığı bilinen fenilalanin hidroksilaz enziminin, yeteri kadar etki göstermemesi nedeni ile fenilalanin tirozine metabolize olamamaktadır. Bu enzimin kofaktörü olan tetrahidrobiyopterinin ( BH4 ) üretim veya döngüsündeki bozukluklar sonucunda da ortaya çıkabilmektedir. Bu nedenle kanda fenilalanin ( FA ) ve onun toksik ürünleri olan fenil pirüvik asit, fenil laktik asit, fenil asetik asit birikmeye başlar. Fenilalanin ve tirozin; tiroid hormonu, nörotransmiterler ve melanin gibi önemli bileşiklerin öncü aminoasitleri olarak kabul edilirler. Bu nedenle hem biriken yan ürünlerin toksik etkisi, hem de önemli bileşiklerin sentez edilememesine bağlı olarak fenilketonüri ( FKÜ ) hastalığı gelişir. FKÜ hastası bebekler doğumda sağlıklıdır. Genelllikle ilk 4 – 6 ay içerisinde klinik olarak bulgu vermeye başlar. Psikomotor gerilik başlar. Özellikle klasik fenilketonürili olgularda mikrosefali, hipertoni, hiperrefleksi, idrarda fenilasetik asit atılımına bağlı olarak alışılmadık koku ( fare idrarı kokusu ) karakteristiktir. Hastalarda giderek saç, deri ve gözlerde pigmentasyonda azalmaya bağlı olarak sarışın, ince saçlı ve mavi gözlü olurlar. Daha büyük çocuklarda kendine zarar verme hiperaktivite, otistik davranışlar sık görülür. Bazı hastalarda konvülzyon gelişir. Bu durum beraberinde klinik olarak gelişme geriliği ve zeka geriliğini doğurur ve geri dönüşümsüz olması nedeniyle yaş ilerledikçe daha ağır klinik tablo oluşur (1, 2).
FKÜ hastalığı konusunda 1930 yıllarından bu yana tanı ve tedavi konusunda çok büyük gelişmeler olmuştur. Hastalığın genetik temelli olması, otozomal resesif kalıtılması nedeniyle araştırmalar yıllar boyu devam etmiştir. Patogenezi aydınlatmaya yönelik ilgili gen mutasyonları farklı toplumlarda çalışılmış ve pek çok mutasyon bulunmuştur.
FKÜ hastalarına semptomatik dönemde tanı konduğunda, oluşan nörolojik hasar tedavi ile geri döndürülemez. Bu nedenle hasta bebekleri yenidoğan dönemde saptayıp tedavi ederek sağlıklı bireyler olarak yetiştirmeyi hedefleyen “tarama testleri” tüm dünyada kabul edilen bir uygulamadır. Ülkemizde 1987 yılında başlayan program, 25.12.2006 tarihinden bu yana TC Sağlık Bakanlığı’nın denetiminde, her yenidoğana
uygulanmaktadır (3). İlk tarama programlarından elde edilen verilerde Türkiye’de “kalıcı hiperfenilalaninemi” insidensinin 1:4172 olduğu ortaya konmuştur (4).
Olgular, sağlıklı çocuk beslenmesi altında iken bakılan kan fenilalanin düzeyine göre sınıflandırılır. Tanı anındaki kan FA düzeyi > 20 mg/dl ise klasik FKÜ, 10 – 20 mg/dl arasında ise hafif – orta FKÜ ve 2 – 10 mg/dl arasında ise hiperfenilalaninemi ( HFA ) olarak adlandırılır. Hastalar tanı aldıktan sonra diyet ve / veya tıbbi tedavi (sapropterin) açısından değerlendirilir ve izleme alınır. Diyet ile amaçlanan hastanın kan FA düzeyinin normal sınırlarda tutulması, bununla beraber diğer besin öğelerinin eksiksiz karşılanması ve olguların normal gelişimine olanak sağlanmasıdır. Sapropterin ise fenilalanin hidroksilaz enziminin ( FAH ) kofaktörü BH4’ün sentetik analoğudur. FAH enziminin stabilizasyonunu ve regülasyonunu arttırarak FKÜ'de defektif yolakta fenilalanin - tirozin dönüşümünü sağlar, FA toleransını arttırır. Hastaların poliklinik kontrolleri sırasında kan değerleri, beslenmeleri, büyümeleri ve gelişmeleri düzenli olarak ele alınır. Beslenmeleri yeterli olan hastaların tedavi başarılarının yüksek olduğu bilinmektedir.
Bu çalışmada; Ege Üniversitesi Tıp Fakültesi Çocuk Sağlığı ve Hastalıkları Anabilim Dalı, Metabolizma Bilim Dalı’nda FKÜ ve HFA nedeniyle izlenen, FA kısıtlı diyet alan hastalarda, büyüme ve beslenme durumlarının incelenmesi amaçlanmıştır. Buna yönelik olarak hastaların en az altı ay ara ile bakılan fizik muayene ( boy, ağırlık, boya uyan ağırlık, vücut kitle indeksi ölçümleri ) ve kan örneklerindeki beslenme parametreleri ( kolesterol, trigliserid, kalsiyum, çinko, bakır, demir, demir bağlama kapasitesi, ferritin, prealbumin, vitamin A, vitamin E, 25 OH D vitamini, B12 vitamini, folik asit ve hemoglobin düzeyleri ) incelenmiştir. Böylelikle, hastalara uygulanan tedavi etkinliği daha ayrıntılı değerlendirilmiş olacaktır.
2. GENEL BİLGİLER
2.1. Fenilalanin metabolizması ve bozuklukları
Fenilalanin, aromatik yapıda olan esansiyel bir amino asittir. Fenilalanin hidroksilaz enzimi tarafından karaciğerde metabolize edilir. Bu reaksiyon için fenilalanin, fenilalanin hidroksilaz adlı enzim, oksijen ve zorunlu kofaktör olarak tetrahidrobiyopiterin gereklidir. Fenilalanin ile fenilalanin metabolizmasındaki tirozin aminoasitleri; Yroid hormonu, nörotransmiterler ve melanin gibi önemli bileşiklerin öncüleridir (5). Fenilalanin metabolizmasında görevli enzim ve koenzimlerin eksikliği sonucu pek çok doğuştan metabolik hastalık gelişir ( Şekil 1 ). Buna yönelik bilgiler, şekil 1’de gösterilmiştir.
Şekil 1. Fenilalanin Metabolizması (25) [ GTPCH; Guanosine triphosphate siklohidrolaz, PTPS; 6 – piruvoil – tetrahidropterin sentaz, DHPR; Dihidropterinredüktaz, SR; Sepiapterin redüktaz, PAH; Fenilalanin hidroksilaz, PCD; Pterin-4a-karbinolamin dehidrataz ]
2.2. Hiperfenilalaninemiler ( HFA )
Fenilalanin hidroksilaz enziminin yetersizliğine ya da biyopterin metabolizmasında görevli enzimlerin bozukluğuna bağlı gelişen metabolik bozukluktur ( primer HFA ). Bunun sonucunda fenilalanin metabolize edilemez, kanda düzeyleri yükselir ve HFA gelişir (2) ( Tablo 1 ). Ayrıca edinsel olarak yani diğer hastalıklara bağlı oluşan HFA durumları da vardır.
Tablo 1. Hiperfenilalaninemi sınıflandırması (6)
A. Primer ( Kalıtsal ) hiperfenilalaninemiler 1. Fenilalanin hidroksilaz eksikliği
a. Klasik Fenilketonüri b. Hafif – orta FKÜ
c. Hafif hiperfenilalaninemiler
d. Maternal FKÜ veya hiperfenilalaninemiler 2. Tetrahidrobiopterin (BH4) metabolizma bozuklukları
a. Guanozin trifosfat siklohidroksilaz l eksikliği b. 6 – piruvoil – tetrahidropterin sentaz eksikliği c. Dihidropteridin redüktaz eksikliği
d. Pterin – 4a - karbinolamin dehidrataz eksikliği B. Sekonder ( Edinsel ) hiperfenilalaninemiler
1. Tirozinemi
2. Geçici Neonatal hiperfenilalaninemi 3. İlaca bağlı (metotreksat, trimetropim) 4. Ağır enflamatuvar yanıt
5. Renal hastalık 6. Karaciğer hastalığı
Primer HFA nedeni olan hastalıklar ve fizyopatolojilerine yönelik açıklamalar, tablo 2’de verilmiştir. Hiperfenilalaninemi, 2 mg/dl’den ( 120 μmol/L ) daha fazla olan plazma fenilalanin değerini tanımlanmaktadır. Normal olarak kan fenilalanin / tirozin oranı 0,6 - 1 arasında iken, bu değer primer HFA’da 3’ün üstüne çıkar. Olguların bu yüksek değerlerle beraber klinik olarak kalıcı merkezi sinir sistemi etkilenimi oluşmaması amacıyla kan fenilalanin değerleri 120 – 360 μmol/L arasına çekilmelidir (7).
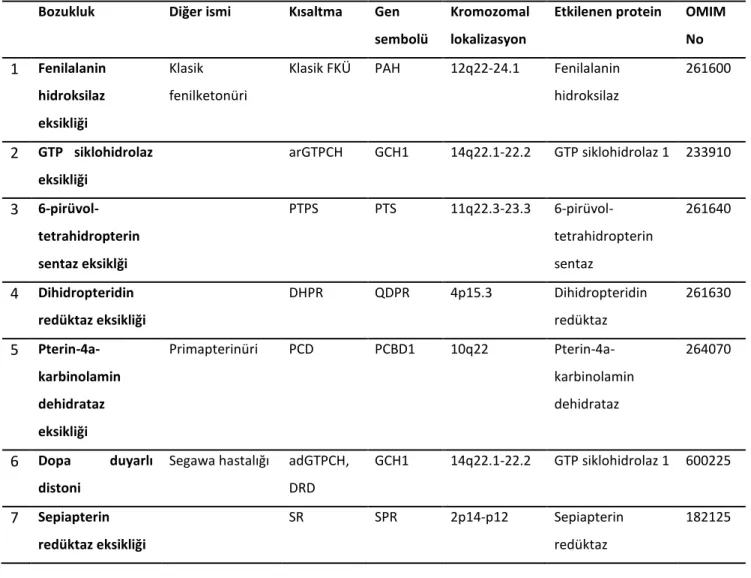
Tablo 2: Primer HFA nedeni olan hastalıklar ve fizyopatolojilerine yönelik terminoloji (8)
Bozukluk Diğer ismi Kısaltma Gen sembolü
Kromozomal lokalizasyon
Etkilenen protein OMIM No 1 Fenilalanin hidroksilaz eksikliği Klasik fenilketonüri
Klasik FKÜ PAH 12q22-24.1 Fenilalanin hidroksilaz 261600 2 GTP siklohidrolaz eksikliği arGTPCH GCH1 14q22.1-22.2 GTP siklohidrolaz 1 233910 3 6-pirüvol-tetrahidropterin sentaz eksiklği PTPS PTS 11q22.3-23.3 6-pirüvol-tetrahidropterin sentaz 261640 4 Dihidropteridin redüktaz eksikliği DHPR QDPR 4p15.3 Dihidropteridin redüktaz 261630 5 Pterin-4a-karbinolamin dehidrataz eksikliği Primapterinüri PCD PCBD1 10q22 Pterin-4a-karbinolamin dehidrataz 264070 6 Dopa duyarlı distoni
Segawa hastalığı adGTPCH, DRD GCH1 14q22.1-22.2 GTP siklohidrolaz 1 600225 7 Sepiapterin redüktaz eksikliği SR SPR 2p14-p12 Sepiapterin redüktaz 182125 2.2.1. Fenilketonüri
Fenilketonüri, otozomal resesif geçiş gösteren intoksikasyon tipi metabolik hastalıktır. FKÜ hastalığı hakkında elde edilen bilgi birikimi çok uzun yıllara dayanmaktadır. 1930’larda Asbjorn Folling’in (9) kanda fenilalanin yüksekliğini saptaması ve Norveçli bir ailenin iki çocuğunda “fenilpürivik oligofreni” adıyla tanımlaması, 1947’de Jervis’in (10) metabolik sorunun; fenilalaninin tirozine okside edilemediğinden kaynaklandığını belirlemesi, 1953’de Jervis’in (10) karaciğerde fenilalanin hidroksilaz eksikliğini hastasında göstermesi, 1950’li yıllarda Horst Bickel (11) tarafından FKÜ hastalarına fenilalanin kısıtlı diyet tedavisinin başlanarak zeka geriliğinin önlenmesi ve son olarak da 1960’larda Robert Guthrie (7) tarafından oluşturulan tanısal testler ile beraber FKÜ hastalarında çok yol
alınmıştır. “Fenilketonüri” terimi ise Lionel Penrose tarafından idrardaki bu bulgu nedeniyle verilmiştir (12). Hastalığın genetik temelini aydınlatan gelişme ise 1984’de fenilalanin hidroksilaz enzimini kodlayan genin 12. kromozomun 12q22-q24.1 bölgesinde yer aldığı tespit edilmesi ile yaşanmıştır (13). Günümüzde FKÜ ile ilgili 700’den fazla mutasyon tariflenmiştir (14).
1950’lerde diyet tedavisi ile hastaların tedavi yöntemine başlanmış, günümüze dek de çok büyük gelişme kaydedilmiştir. Ancak tanı konmayıp tedavisiz kalan olgularda veya yetersiz tedavi uygulandığında hastalarda klasik fenilketonüri bulguları görülür. Fenilketonüri hastalarının doğumda tamamen normal olduğu unutulmamalıdır. Ağır entellektüel bozukluk, spastik refleksler, anormal yürüyüş, egzema ve anormal davranışlar ( aralıksız inilti ve başını ileri geri sallama ) bu hastaların vazgeçilmez bulgularıdır. Hastaların en önemli hatta bazen tek bulgusu zihinsel bozukluktur. Hastaların % 1’inden azında çok düşük IQ görülmesine karşın genellikle IQ seviyesi 50 altındadır (15, 16). Kusma bu olgularda erken belirti olabilir. İrrabilite, egzematoid döküntü ve sıradışı koku ( fenilasetik asit atılımı nedeniyle küflü koku ) erken dönemde FKÜ hastalarda görülebilmektedir. %90 olguda açık saçlar, açık ten rengi ve mavi gözler dikkati çeker (17). Nörolojik bulgular açısından 1/3 olguda serebral felcin hemen tüm bulguları görülür (18). Spastisite ve hipertonisite yanında artmış derin tendon refleksleri göze çarpmaktadır. Sadece %5 olgu ağır derecede etkilenmektedir. Bunun yanında hiperaktivite ve yürüyüş bozuklukları eklenebilir. Nöbet hastaların yaklaşık dörtte birinde kendini göstermektedir, % 80’inde EEG’de anormalliklerle gider (16, 19). Fenilketonürili hastalarda topluma göre daha sık konjenital kalp hastalığı görüldüğü de bildirilmiştir (20).
2.2.1.1 Fenilketonüri Sıklığı
FKÜ görülme sıklığı ülkeden ülkeye farklılık göstermektedir. Türkiye, en sık görülen ülkeler arasında ilk sıralarda yer almaktadır. Akraba evliliği oranının yüksek olması, otozomal resesif kalıtılan FKÜ hastalığının ülkemizde sık rastlanmasına neden olmaktadır. Buna karşılık en az görülen bölgeler olarak Afrika ve Amerika sayılmaktadır, yaklaşık 1:50.000 olarak tespit edilmiştir. Avrupa ülkelerinde prevalansın 1/3.000 ile 1/30.000 arasında değiştiği, bu ülkeler içinde Finlandiya’nın en düşük orana sahip ülke olduğu
( 1:100.000 – 1:200.000 ) bildirilmektedir (21, 22). Bu konudaki sonuçlar tablo 3’de gösterilmiştir.
Tablo 3: FKÜ sıklığı (23)
ÜLKE Canlı doğumda
FAH eksikliği
Taşıyıcılık oranı
Alıntı
Türkiye 1:2,600 1/26 Özalp ve ark. (1986) İrlanda 1:4,500 1/33 DiLelle ve ark. (1986) Kuzey Avrupa orijinli, Doğu Asya 1:10,000 1/50 Scriver & Kaufman (2001) Japonya 1:143,000 1/200 Aoki & Wada (1988) Finlandiya, Aşkenazi Yahudileri 1:200,000 1/225 Scriver & Kaufman (2001)
Afrika 1:100,000 ? Anekdotsal
2.2.1.2 Tanı ve Sınıflandırma
Fenilketonüri tanısı, bir başka anlatımla kanda fenilalanin yüksekliğinin ortaya konması, yenidoğan döneminde, bebek asemptomatik iken, koruyucu hekimlik anlayışının bir uygulaması olan tarama programı ile yapılır. Yenidoğanlarda doğumdan sonraki 3 – 5. günlerde, yeterli beslenmenin ( protein alımı ) ardından alınan topuk kanı ile çalışılır. Bebeğin daha erken taburcu olması durumunda hastaneden ayrılmadan hemen önce kan alınır ve en geç 15 gün içinde tekrarlanır. Bu örneklem yetkili merkezler tarafından çalışılarak FA yüksekliği saptanması durumunda en kısa sürede olgu, pediatrik metabolizma merkezlerine yönlendirilir.
Fenilalanin analizi filtre kağıdına damlatılan birkaç damla topuk kanından çalışılır (Resim 1’de Guthrie kağıdına kan alımı gösterilmiştir). Tarihsel süreçte Guthrie tarafından geliştirilen bakteriyel inhibisyon yöntemine dayanan test bugün gelişen kromatografik analizlerle hızla yapılmaktadır (7).
Resim 1: Guthrie kağıdına kan alımı
Guthrie testinde, filtre kağıdın
içeren agar jel ile muamele edilir. Bu bakterinin büyümesi için fenilalanine ihtiyacı vardır. Ayrıca bu jel beta-2- thienylalanine içerir ki bu madde fenilalanin kullanan bakterilerin büyümelerini inhibe eder. HFA
gösteren çember oluşur, bu durumda test pozitif olarak yorumlanır yani kanda FA değerinin yüksek olduğu anlaşılır.
bilgi vermektedir. Bir başka yöntem olan geliştirilmesi ile birlikte FA değeri,
Bu yöntem sadece FA düzeyini
kullanılmaktadır. Bu metod sayesinde %1 miktarda plazma ile hem kan FA hem Sayılan göstergeler hasta izleminde
micromol/L veya daha yüksek olması FKÜ tanısı koydurur plazma örneğinin, kuru kan örneğine oranla %15 daha yüksek
(27). HFA tanısı konan olgularda BH4 metabolizma bozuklukları araştırılmalıdır. FAH kofaktörü olan BH4 eksikliğine bağlı
Aynı tabloyu oluşturmasına rağmen farklı şekilde tedaviye ihtiyaçları bulunmaktadır. Dolayısıyla kanda ve idrarda
( örneğin DHPR aktivitesi ) çalışılma
FKÜ olguları bilindiği gibi sağl
günlerde topuk kanı alınması önemlidir. Yalancı negatif değerlerin oluşmaması için serbest beslenmenin sağlandığı; beslenmeden
düşünülmektedir. Alınan değerin pozitifliği durumunda Guthrie kağıdına kan alımı
iltre kağıdından kurumuş kanlı bölüm çıkarılıp, Bac
gar jel ile muamele edilir. Bu bakterinin büyümesi için fenilalanine ihtiyacı vardır. thienylalanine içerir ki bu madde fenilalanin kullanan bakterilerin büyümelerini inhibe eder. HFA’lı olgularda bir gün içerisinde bakteriyel çoğalma gösteren çember oluşur, bu durumda test pozitif olarak yorumlanır yani kanda FA değerinin yüksek olduğu anlaşılır. Bakteri kolonisinin çapı FA konsantrasyonu hakkında
Bir başka yöntem olan kütle spektrometrinin ( tandem mass ) ştirilmesi ile birlikte FA değeri, çok daha gerçekçi ve kantitatif olarak
düzeyini değil, diğer amino asitlerin kan düzeyini göstermede de kullanılmaktadır. Bu metod sayesinde %1’in altında yanlış pozitiflik sağlayaca
hem kan FA hem tirozin ( tyr ) hem de FA / Tyr oranını
er hasta izleminde kullanılır (24, 25). Fenilalanin düzeyinin 1200 micromol/L veya daha yüksek olması FKÜ tanısı koydurur (26). FA düzey
plazma örneğinin, kuru kan örneğine oranla %15 daha yüksek sonuç verdiği görülmüş HFA tanısı konan olgularda BH4 metabolizma bozuklukları
AH kofaktörü olan BH4 eksikliğine bağlı benzer hastalık
Aynı tabloyu oluşturmasına rağmen farklı şekilde tedaviye ihtiyaçları bulunmaktadır. Dolayısıyla kanda ve idrarda pterin metabolizmasını ve gerektiğinde ilgili enzimleri
çalışılmalıdır (28).
FKÜ olguları bilindiği gibi sağlıklı doğarlar. Olguların erken tanınması
günlerde topuk kanı alınması önemlidir. Yalancı negatif değerlerin oluşmaması için serbest beslenmeden 72 saat sonra kan örneğinin alınması
değerin pozitifliği durumunda kantitatif ölçüm mutlaka
çıkarılıp, Bacillus subtilis gar jel ile muamele edilir. Bu bakterinin büyümesi için fenilalanine ihtiyacı vardır. thienylalanine içerir ki bu madde fenilalanin kullanan bakterilerin bakteriyel çoğalmayı gösteren çember oluşur, bu durumda test pozitif olarak yorumlanır yani kanda FA Bakteri kolonisinin çapı FA konsantrasyonu hakkında da kütle spektrometrinin ( tandem mass ) gerçekçi ve kantitatif olarak ölçülebilmektedir. değil, diğer amino asitlerin kan düzeyini göstermede de in altında yanlış pozitiflik sağlayacak şekilde, az Tyr oranını saptanabilir. Fenilalanin düzeyinin 1200 FA düzeyi tayininde; sonuç verdiği görülmüştür HFA tanısı konan olgularda BH4 metabolizma bozuklukları da mutlaka hastalık oluşmaktadır. Aynı tabloyu oluşturmasına rağmen farklı şekilde tedaviye ihtiyaçları bulunmaktadır. pterin metabolizmasını ve gerektiğinde ilgili enzimleri
erken tanınması açısından ilk günlerde topuk kanı alınması önemlidir. Yalancı negatif değerlerin oluşmaması için serbest kan örneğinin alınması ideal olarak kantitatif ölçüm mutlaka yeni bir
kan örneğinde tekrar yapılmalıdır (29). Burada önemli olan durum olgularda yanlış negatiflik yaratacak yetersiz beslenme durumlarının olmasını engellemektir (30). Ayrıca prematüre doğum öyküsü olan bazı yenidoğanlarda fenilalanin metabolizmasında görevli enzimlerin tam olgunlaşmaması veya bir başka nedeni karaciğer hastalıklarında ( örneğin enfeksiyon ) da geçici bir FA yüksekliği saptanabilir (31, 32).
Fenilalanin hidroksiksilaz ( FAH ) enzim eksiklikleri, diyette kısıtlılık olmazken yani uygun miktarda proteinli diyet alırken saptanan kan FA düzeylerine göre sınıflandırılır:
• Klasik FKÜ: Kan FA düzeyi ≥ 20 mg/dl ( ≥ 1200 μmol/L ); FAH aktivitesi < %1 • Hafif FKÜ veya HFA: Kan FA düzeyi 10 – 20 mg/dl ( 1200 μmol/L - 600 μmol/L );
FAH aktivitesi % 1 – 5
• Non-FKÜ HFA veya Hafif HFA: Kan FA düzeyi 2 - 10 mg/dl ( 120 - 600 μmol/L ); FAH aktivitesi > % 5
2.2.1.3. Genetik danışma
Prenatal tanı, indeks vakanın mutasyonunun bilinmesi durumunda amniyosentez veya koryonik villus örneklemi sonrası DNA analizi ile FAH geninin incelenmesi olasıdır (1).
2.2.1.4. Tedavi ve Prognoz
Beslenme ( diyet ) tedavisi
FAH eksikliği olan ve tedavi edilmemiş olgularda kalıcı nörolojik hasarın oluştuğu bilinmektedir. Nöropatolojik etkilenmenin önlenmesi amacıyla beslenme tedavisinin mümkün olduğunca erken başlanması, metabolik kontrolün iyi sağlanması ve uzun süreli izlem önem taşımaktadır (33). Yenidoğan döneminde FKÜ tanısı almış olan hastalara muhakkak diyet tedavisi başlanmalıdır. Diyet tedavisi fenilalaninden kısıtlı olmalı ve mümkün olan en kısa zamanda başlanmalıdır. Tedavi başlanmasına işeret eden kan FA düzeyi konusunda fikir birliği olmamasına rağmen genelde kabul edilen görüş; tanı anında kan FA düzeyi 600 μmol/L ( 10 mg/dl ) ve üzerinde olan her bebeğe diyet tedavisi başlamaktır (34, 35). Avrupadaki birçok merkez de FKÜ olgularına 600 μmol/L üzerinde diyet tedavisini önermektedir (36). Tedavide kan FA hedefi çeşitli merkezlerce değişmekle
beraber 120 – 360 μmol/L olarak önerilmektedir ( tablo 4 ). Eğer hastanın kan FA düzeyi < 360 μmol/L ise diyetsiz izleme devam edilmelidir.
Tablo 4. Farklı ülkelere göre önerilen hedef kan FA düzeyleri (22)
YAŞ Hedef kan FA düzeyi ( µmol/L )
Almanya İtalya İngiltere ABD Fransa Hollanda 0-6 yaş 40-240 120-360 120-360 120-360 120-300 120-360 7-9 yaş 40-240 120-360 120-480 120-360 120-300 120-360 10-12 yaş 40-900 120-360 120-700 120-360 < 900 120-360 13-15 yaş 40-900 120-600 120-700 120-600 < 900 120-600 16-18 yaş 40-1200 120-600 120-700 120-600 < 900 120-600 Adolesan ve erişkinler 40-1200 120-600 120-700 120-900 < 1500 120-600
Süt çocukluğu dönemi ile birlikte düşük proteinli ve kısıtlı FA içeren özel ürünler, bazı tahıllar, sebze ve meyvelerden günlük FA ihtiyacı karşılanmalıdır. Bu ürünlerin içerisindeki FA değerini hesaplamak için bir sistem geliştirilmiştir. Bu sistemde 1 gr proteinde 50 mg FA olduğu kabul edilmektedir. Hastalar ve aileleri buna göre beslenme sırasında ne kadar FA aldıklarını hesaplamaktadır. Ayrıca sebze ve mevyeler FA değeri düşük olduğundan ( < 75 mg/100 g besin ) serbest olarak tüketilebilmektedir (37, 38).
Fenilalanin düzeyini istenen düzeye çekebilmek için diyetle alımı azaltmamız gerekmektedir. Ancak esansiyel bir aminoasit olmasından dolayı tamamen kesilmesi mümkün olmamaktadır. Bilindiği üzere diyetle alınan FA’nin birçoğu tirozine dönüşmekte ve tiroid hormonları, dopamin, adrenalin ve noradrenalin gibi nörotransmitterler için öncül madde olmaktadır. FKÜ hastalarının yaşına göre günlük alması gereken protein, FA, tirozin ve enerji gereksinimleri iyice gözden geçirilmelidir. Bunun yanı sıra kontroller sırasında bakılan kan FA düzeylerine göre almakta olduğu diyette değişiklik yapılmasına dikkat etmek gerekir ( Tablo 5 – 6 ).
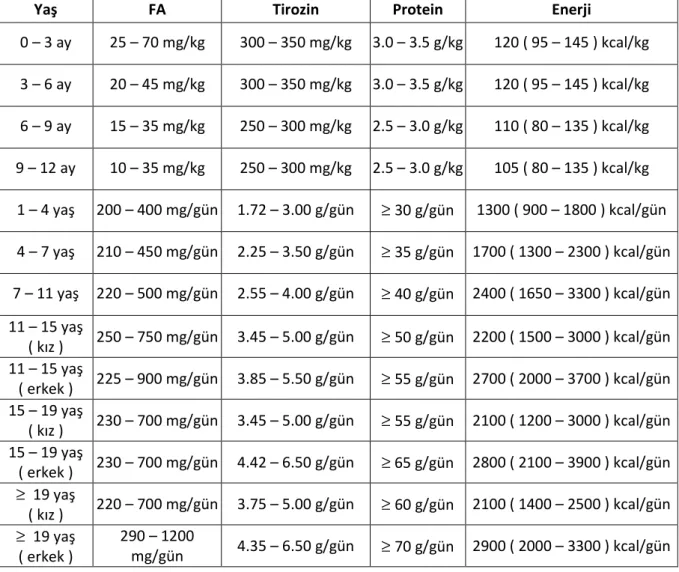
Tablo 5. Günlük FA tüketimi ( yaşa göre ) (39)
Yaş FA Tirozin Protein Enerji
0 – 3 ay 25 – 70 mg/kg 300 – 350 mg/kg 3.0 – 3.5 g/kg 120 ( 95 – 145 ) kcal/kg 3 – 6 ay 20 – 45 mg/kg 300 – 350 mg/kg 3.0 – 3.5 g/kg 120 ( 95 – 145 ) kcal/kg 6 – 9 ay 15 – 35 mg/kg 250 – 300 mg/kg 2.5 – 3.0 g/kg 110 ( 80 – 135 ) kcal/kg 9 – 12 ay 10 – 35 mg/kg 250 – 300 mg/kg 2.5 – 3.0 g/kg 105 ( 80 – 135 ) kcal/kg 1 – 4 yaş 200 – 400 mg/gün 1.72 – 3.00 g/gün ≥ 30 g/gün 1300 ( 900 – 1800 ) kcal/gün 4 – 7 yaş 210 – 450 mg/gün 2.25 – 3.50 g/gün ≥ 35 g/gün 1700 ( 1300 – 2300 ) kcal/gün 7 – 11 yaş 220 – 500 mg/gün 2.55 – 4.00 g/gün ≥ 40 g/gün 2400 ( 1650 – 3300 ) kcal/gün 11 – 15 yaş ( kız ) 250 – 750 mg/gün 3.45 – 5.00 g/gün ≥ 50 g/gün 2200 ( 1500 – 3000 ) kcal/gün 11 – 15 yaş ( erkek ) 225 – 900 mg/gün 3.85 – 5.50 g/gün ≥ 55 g/gün 2700 ( 2000 – 3700 ) kcal/gün 15 – 19 yaş ( kız ) 230 – 700 mg/gün 3.45 – 5.00 g/gün ≥ 55 g/gün 2100 ( 1200 – 3000 ) kcal/gün 15 – 19 yaş ( erkek ) 230 – 700 mg/gün 4.42 – 6.50 g/gün ≥ 65 g/gün 2800 ( 2100 – 3900 ) kcal/gün ≥ 19 yaş ( kız ) 220 – 700 mg/gün 3.75 – 5.00 g/gün ≥ 60 g/gün 2100 ( 1400 – 2500 ) kcal/gün ≥ 19 yaş ( erkek ) 290 – 1200 mg/gün 4.35 – 6.50 g/gün ≥ 70 g/gün 2900 ( 2000 – 3300 ) kcal/gün
Tablo 6. Günlük FA tüketimi ( Kan FA düzeylerine göre ) (39)
Kan FA Düzeyi Günlük FA miktarı
240 – 605 μmol / l 6 – 10 mg/dl 70 mg/kg/gün 605 – 1210 μmol / l 10 – 20 mg/dl 55 mg/kg/gün 1210 – 1815 μmol / l 20 – 30 mg/dl 45 mg/kg/gün 1815 – 2420 μmol / l 30 – 40 mg/dl 35 mg/kg/gün ≥ 2420 μmol / l ≥ 40 mg/dl 25 mg/kg/gün
Özellikle yenidoğan ve süt çocuğu döneminde alınan besinlerin sınırlı olmasından dolayı gereken FA değerine ulaşmak için önem sırasına göre anne sütü, adapte mama ve inek sütü kullanılmalıdır ( Tablo 7 ).
Tablo 7. Anne sütü ve inek sütü FA içerikleri ( mg/100 ml ) (40)
Kolostrum 70
Geçiş sütü 60 – 70
Matür süt 48
İnek sütü 180
Anne sütünü alan bebeklere FA içermeyen amino asit formula verildiğinde uzun dönemde daha iyi kontrol edilebilir kan FA düzeyleri ve sağlıklı büyüme elde edilir (41, 42). Uygulamalarda değişiklik olmakla beraber bazı merkezler ( her beslenmede ) hasta bebekleri anne sütü öncesinde belirlenmiş düzeyde ( miktarda ) FA içermeyen formula ile beslemektedir, daha sonra anne sütü ile beslenmelerine devam edilmektedir. Böylelikle bebekler doygunluğa ulaştığında daha az miktarda FA almış olacaktır (43). Anne sütü alan bebeklerin haftada 2 kez bakılan kan FA düzeyleri ile emzirme süresi ve FA içermeyen formula miktarı ayarlanmaktadır (40).
Tamamlayıcı besinler 4-6 aylıktan itibaren başlanmalıdır. Düşük proteinli besinler olması yanında meyve püreleri, taze sıkılmış mevye suyu, sebze püreleri, çorbaları ile başlanır ( 40 ).
FKÜ hastalarında, tanı anında ya da kontroller sırasında kan FA düzeyinin çok yüksek saptanması olası bir durumdur. Olgulara bu dönemlerde, kan FA değerinin yükseklik derecesine göre 3-7 gün için 0 mg/gün FA içeren “boşaltma diyeti” verilir. Böylelikle kandaki FA düzeylerinde 24 saatte 5 ile 8 mg/dl arasında düşüş sağlanır. Böylece nöropatolojik etkilenimin önlenmesi amaçlanır (44, 45).
Doğal protein alımının (et, balık, yumurta, peynir, kurubaklagiller gibi) yasak olduğu bu olgular için büyüme ve gelişmelerini sağlamaları amacıyla FA içermeyen amino
asit karışımları üretilmiştir. Bu karışımlar tirozin başta olmak üzere vitaminler, minareller ve gerekli yağ asitlerini içinde barındırırlar.
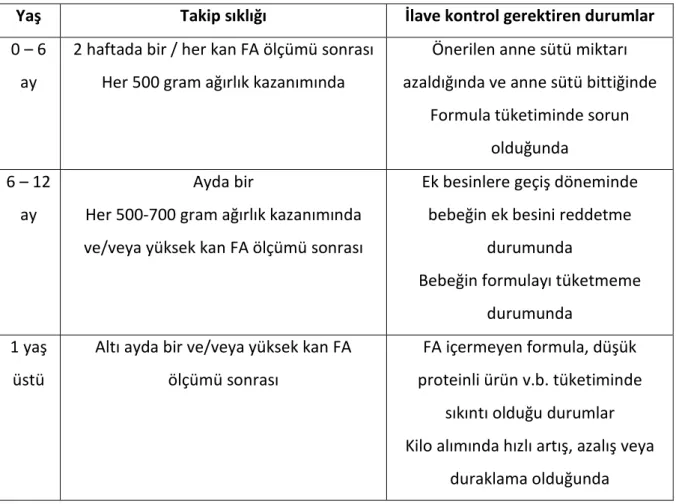
Diyet başlanan hastaların büyümeleri, gelişmeleri, obezite ya da malnütrisyonu düzenli olarak kontrol altına alınmaktadır. Uygun takip yöntemi ile hastaların yaşayabileceği olumsuz durumların önüne geçilmiş olunmaktadır. Bununla ilgili bilgiler tablo 8’de verilmiştir.
Tablo 8. Hastaların beslenme takip sıklığı (39)
Yaş Takip sıklığı İlave kontrol gerektiren durumlar
0 – 6 ay
2 haftada bir / her kan FA ölçümü sonrası Her 500 gram ağırlık kazanımında
Önerilen anne sütü miktarı azaldığında ve anne sütü bittiğinde
Formula tüketiminde sorun olduğunda
6 – 12 ay
Ayda bir
Her 500-700 gram ağırlık kazanımında ve/veya yüksek kan FA ölçümü sonrası
Ek besinlere geçiş döneminde bebeğin ek besini reddetme
durumunda
Bebeğin formulayı tüketmeme durumunda
1 yaş üstü
Altı ayda bir ve/veya yüksek kan FA ölçümü sonrası
FA içermeyen formula, düşük proteinli ürün v.b. tüketiminde
sıkıntı olduğu durumlar Kilo alımında hızlı artış, azalış veya
Hastaların klinik ve laboratuar takip sıklığı hastaya göre değişmekle beraber, uygulamalar arasından bir örnek, tablo 9’da verilmiştir.
Tablo 9. Hastaların poliklinik izlem sıklığı (1)
Kan FA ölçüm sıklığı Fizik bakı sıklığı
Yaş Kan FA Klinik
0 – 3 yaş Haftalık 3 ayda bir
4 – 6 yaş 2 haftada bir 3 – 6 ayda bir
7 – 9 yaş 2 haftada bir 6 ayda bir
10 – 15 yaş Aylık 6 ayda bir
> 16 yaş 2 – 3 ayda bir Yılda bir
Yine hastaların kontrollerde belirli bir seviyede kan FA düzeyi yakalanması gerekmektedir. Hedeflenen kan FA değerleri Tablo 10’da gösterilmiştir.
Tablo 10. Hedef kan FA değerleri (39)
Yaş Kan FA değerleri ( μmol/L )
< 10 yaş 40 – 240
10 – 15 yaş 40 – 600
> 16 yaş 40 – 900
Erişkin 40 – 1200
Hastaların takiplerinde diyetlerindeki uygun olmayan FA alımları sonucu bazen FA eksikliği de görülebilmektedir. Ölümle dahi sonuçlanabilecek bu tür hastalarda megaloblastik anemi, büyüme geriliği, nöbet, protein enerji malnütrisyonu, deri döküntüleri, ishal ve saç dökülmesi görülebilecek belirti ve bulgulardır.
Özellikle adolesan yaş grubunda beslenme yetersizlikleri, lezzet ve FA kısıtlı diyet tedavisinin pahalı oluşu tedavilerinde zorluklara neden olmaktadır. Daha önceleri çocukluk dönemi sonrası diyetlerin açılması uygulaması yapılmış ancak diyete devam edenlerde davranış ve kognitif gelişimin, diyeti sonlandıranlardan daha iyi olduğunun kanıtlanması üzerine FA kısıtlı diyetin ömür boyu sürdürülmesi hedef haline gelmiştir (40).
Diğer tedavi yöntemleri
LNAA Tedavisi
Büyük nötral aminoasidler ( LNAA ) ( histidin, arjinin, lizin, metiyonin, treonin, tirozin, triptofan, lösin, izolösin ve valin ) kan – beyin bariyerinde L – tipi amino asid taşıyıcısı vasıtasıyla FA ile yarışarak beyine geçerler. Böylelikle yüksek FA düzeylerinde, LNAA verilerek beyin FA konsantrasyonu azaltılabilmektedir. Diyete uyumsuz FKÜ hastalarında bu tedavi şekli, FA’nın beyin üzerindeki akut zararlı etkilerinin koruması yanında nöropsikolojik fonksiyonlar üzerine de olumlu etkilenimi göstermektedir ( 46 ). Etkin diyet tedavisini uygulayamayan hastalarda ek bir seçenek olabilir (47).
Fenilalanin ammonia liyaz ( PAL ) Enzim Tedavisi
PAL, FA’yı trans-sinnamik asit ve amonyağa dönüştüren kofaktör ihtiyacı olmayan bir enzimdir. Şekil 2’de fenilalanin hidroksilaz ve fenilalanin ammonia liyaz enzimlerinin faklılıkları gösterilmiştir. Ortaya çıkan trans-sinnamik asit insanlarda hızlıca hippurik asite dönüşür ve idrar ile atılır. Fenilketonürili fare deneylerinde 90 günlük PAL injeksiyonunun kan ve beyin FA değerlerinde düşüş saptandığını göstermiştir (48). Bu enzimin ağız yoluyla alınan formu, barsaklarda preolitik enzimler tarafından etkisini azaltmaktadır. Subkütanöz uygulamalar ile ilgili çalışmalar halen devam etmekle beraber güvenli ve kan FA düzeylerini düşürmede etkili olduğu bildirilmektedir (49).
Şekil 2 : PAH ve PAL enzimlerinin farklılıkları (50). [ Phe: Fenilalanin, Tyr: Tirozin, PAH: Fenilalanin hidroksilaz, PAL: Fenilalanin ammonia liyaz, BH4 : Tetrahidrobiopterin, 4-OH-BH2 : 4 hidroksi dihidrobiopterin, NH3: Amonyak ]
Glikomakropeptid (GMP) Tedavisi
GMP peynirden elde edilen protein derivesi olup FA, tirozin, triptofan, histidin, arjinin ve sistein içermeyen bir protein kaynağıdır. FKÜ’lü bireylerde bu anlamda alternatif doğal protein kaynağı olarak kullanılabilir (51).
Gen Tedavisi
Rekombinan adeno aracılı viral vektör kulanarak yapılan gen tedavisi hayvan modellerinde başarılı olmuştur. İnsanlarda da başarılı olabilmesi için güvenli gen transfer vektör çalışmalarına ihtiyaç vardır (2).
2.2.2. Tetrahidrobiyopterin (BH4) metabolizması bozuklukları
2.2.2.1. Tetrahidrobiyopterin (BH4) metabolizma bozuklukları, Klinik ve Tanı
Fenilalanin hidroksilaz enziminin koenzimi olarak bilinen BH4; dopamin ve serotonin biyosentezinden sorumlu tirozin hidroksilaz ve triptofan hidroksilazlar ile argininden nitrik oksit oluşumunu sağlayan nitrik oksit sentazın da aynı zamanda kofaktörüdür. BH4 eksikliği yenidoğan döneminde saptanan FKÜ hastalarının %2’sinden azını oluşturmaktadır. Bu hastalıkta sentez bozukluğu açısından Guanozin trifosfat siklohidrolaz ( GTP-CH ) eksikliği ve 6 - pirüvoil tetrahidrobiopterin sentaz ( PTPS ) eksikliği sorumlu tutulurken, resiklus bozukluklarında dihidropteridin redüktaz ( DHPR ) eksikliği ve pterin karbinolamin dehidrataz ( PCD ) eksikliği bu durumu yaratmaktadır ( Şekil 3 ).
Şekil 3: Tetrahidrobiopterin metabolizması (9) [ GTPCH; Guanosine triphosphate siklohidrolaz, PTPS; 6 – piruvoil – tetrahidropterin sentaz, DHPR; Dihidropterinredüktaz, SR; Sepiapterin redüktaz, CR; Karbonil redüktaz, DHFR; Dihidrofolat redüktaz, PAH; Fenilalanin hidroksilaz, PCD; Pterin-4a-karbinolamin dehidrataz
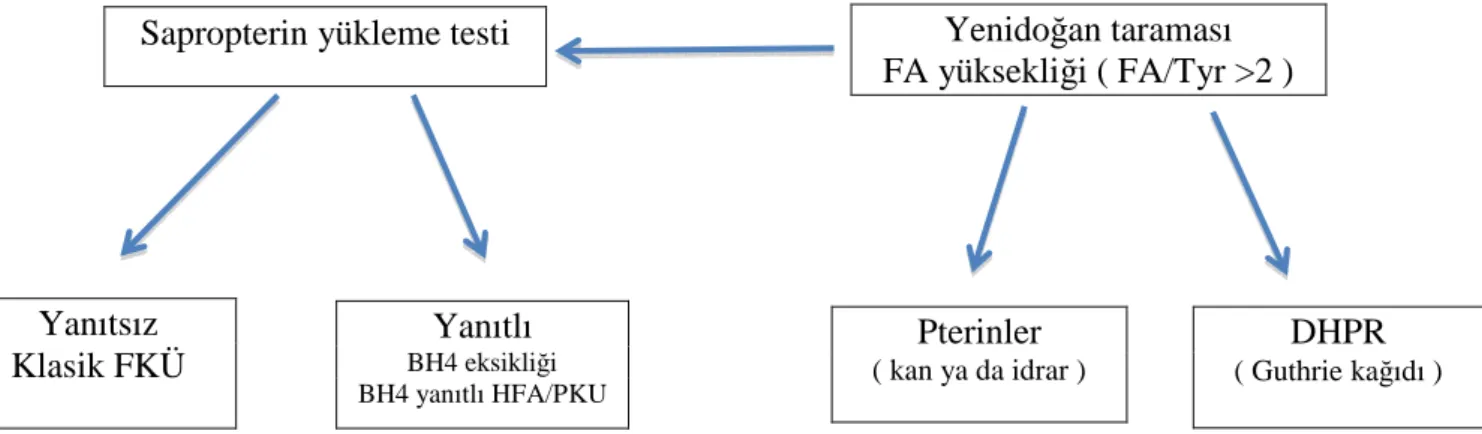
BH4 eksikliği ilk olarak 1960’ların sonunda tanımlanmasına karşın fizyopatolojik mekanizma DHRP eksikliğinin 1975’lerde gösterilmesi ile tam olarak anlaşılmıştır (52, 53). HFA olgularının yaklaşık %1-2 kadarı BH4 eksikliği tanısı almaktadır, özellikle akraba evliliğinin yoğun olduğu Türkiye ve Suudi Arabistan gibi ülkelerde sık görülür (54). BH4 eksikliği olan hastaların tanımlanması algoritma olarak şekil 4’de sergilenmiştir.
Şekil 4 : BH4 eksikliği olan hastaların algoritmik yaklaşımı (26)
Sapropterin yükleme testi Yenidoğan taraması
FA yüksekliği ( FA/Tyr >2 ) Yanıtsız Klasik FKÜ Yanıtlı BH4 eksikliği BH4 yanıtlı HFA/PKU Pterinler ( kan ya da idrar ) DHPR ( Guthrie kağıdı ) Fenilalanin
Bütün hastalardan kan veya idrar pterin analizi ve Guthrie kağıdına alınmış örneklerle DHPR ölçümü yapılarak tanısal işlemlere mümkün olduğunca erkenden başlanmalıdır. Guthrie kağıdı kullanımı pterinlerin ölçümü, DHPR aktivitesi ve amino asit değerlerini göstermesi açısından çok pratik bir yöntemdir. Özellikli olarak otozomal resesif GTPCH eksikliği ve SR eksikliği olan hastalar, yenidoğan döneminde normal kan FA değeri olması nedeniyle atlanabilmektedirler (55). Şekil 5’de gösterildiği gibi olguların değerlerine göre ayırıcı tanı yapılması mümkün olmaktadır.
YENİDOĞAN TARAMASINDA FA YÜKSEKLİĞİ FENİLALANİN VE TİROZİN ( PLAZMA ) FA NORMAL FA (↑) VE TYR (↑)
Amino asitleri tekrarla FA (↑) VE TYR (N-↓)
BH4 yükleme testi ( Kan FA düzeyi )
Diyetin başlangıcından önce ! Pterinler (Guthrie kağıdı/idrar)
DHPR ( Guthrie kağıdı ) Pterinler normal DHPR normal Pterinler anormal DHPR normal FA hidroksilaz eksikliği ( PKÜ ) DHPR eksikliği Neopterin N; Biopterin N - ↑ GTPCH eksikliği Neopterin ↓; Biopterin ↓ YANLIŞ POZİTİF YENİDOĞAN TARAMASI PTPS eksikliği Neopterin ↓; Biopterin ↓ PCD eksikliği Neopterin ↑; Biopterin n-↓; Primapterin ↑ Pterinler ± normal DHPR ↓
Şekil 5. FKU ve BH4 eksikliği ayırıcı tanısı ( 56 ) [ FA; Fenilalanin, Tyr; Tirozin, GTPCH; Guanosine triphosphate siklohidrolaz, PTPS; 6 – piruvoil – tetrahidropterin sentaz, PCD; Pterins- 4akarbinolamin dehidrataz ]
BH4 yükleme testi FKÜ ve BH4 eksikliği olan hastaların ayırımında görev alır (57, 58). Aynı zamanda BH4 yanıtlı FKÜ hastalarının tanınmasında da önemlidir. BH4 yanıtlı hastaların oral olarak aldıkları sapropterin dihidroklorür ( Kuvan R ) tedavisi ile kan FA değerlerinin düştüğü hatta normal düzeye geldiği bilinmektedir (59). Öte taraftan beyinde nörotransmitter sentezini etkilediğinden; katekolaminlerin, nitrik oksitin ve serotoninin metabolitlerinin beyin omurilik sıvısında ölçülmesi, BH4 eksikliğinin ağırlığını ortaya konmasında yardımcı olabilmektedir (60, 61).
Klinik olarak GTPCH ( HFA ile birlikte olan otozomal resesif form ), PTPS, DHPR enzim defektleri olanlarda; konvülzyon, anormal hareketler, salivasyon artışı, yutma güçlüğü, bozulmuş tonus ve postür, egzema, mikrosefali ön plandadır. PCD enzim defektinde ise bulgular beklendiği kadar sık değildir. GTPCH ( HFA ile birlikte olmayan otozomal dominant form ) eksikliğinde ise alt ekstremite, gövde ve kollarda distoni, parkinsonizm, orofasial diskinezi, hiperrefleksi, spastisite görülür (62). Bu hastalar klasik FKÜ ile karşılaştırıldıklarında daha ağır seyirli ve tedavilerinin zor olduğu bilinmektedir. Çünkü burada eksik olan BH4 sadece FAH için kofaktör değil diğer önemli nörotransmitter biyosentezinde de görevlidir. Bu anlamda tedavide BH4 ve fenilalaninden fakir diyet yanında L-dopa, karbidopa ve 5-hidroksitriptofan gibi nörotransmitter öncüllerini uygulamak gerekir (1, 28).
2.2.2.2. Tetrahidrobiyopterin ( BH4; sapropterin ) Tedavisi
Tetrahidrobiyopterin; FA, tirozin ve triptofanın hidroksilasyonu dahil, nitrik oksit sentaz ve alkilgliserol monooksijenazı içeren bir grup enzimin kofaktörüdür. BH4 eksikliğinde aynı zamanda nörotransmitter eksikliği nedeniyle nörolojik bulgulara neden olur (63, 64).
BH4’ün tedavide kullanımı 1999 yılından itibaren başlamıştır (65). Sapropterin dihidroklorid ( Kuvan R ), BH4’ün aktif 6R izomerinin sentetik formulasyonuna sahip olmasıyla HFA ve FKÜ olgularda kullanılmaktadır. BH4 yükleme testi ile kan FA düzeyinde % 30’dan fazla düşüş sağlanması durumunda BH4 yanıtlı HFA/FKÜ olarak kabul edilir. Rezidü enzim aktivitesine sahip olan bu tür olguların diyetlerinde kısıtlamalarına devam edilir ya da diyetleri serbestleştirilir. Avrupa’da 4 yaş üzerinde kullanılırken, ABD’de bütün yaş gruplarında kullanım izni mevcuttur (66). Klasik FKÜ olgularının büyük çoğunluğunun
BH4 tedavisine yanıtsız olduğu, ancak hafif FKÜ’ların 2/3 oranında yanıtlı olduğu bildirilmektedir (67). Sapropterin dihidroklorur tedavisi 10 – 20 mg/kg/gün olacak şekilde uygulanır. Formula ya da su içinde eritilerek uygulanır. Davranışsal ve nörokognitif gelişimleri açısından, kan FA düzeyinin 360 μmol/L değerinin altında tutulması hedeflenmelidir (68).
2.2.3. Maternal Fenilketonüri
Fenilalaninden kısıtlı diyet almayan FKÜ hamilelerin bebeklerinde yüksek risk olduğu bilinmektedir. Bu bebeklerde mikrosefali, mental retardasyon, büyüme geriliği ve konjenital kalp hastalığı açısından artmış risk vardır (69). Özellikle bu durum fenilalanin yüksekliği ile koreledir. Bu gebelerde bu riskler açısından FA düzeyleri 6 mg/dl ( 360 μmol/L ) seviyelerinde tutulmalıdır.
2.3. Nutrisyonel değerlendirme:
FKÜ olgularında beslenmenin yeri tartışılmazdır. Bu olguların FA gibi esansiyel amio asitten kısıtlı beslendiği dikkate alınacak olursa büyüme ve gelişmelerinin sık ve özenle izlenmesi gerekmektedir. Hastalar tanı aldıktan sonra FA kısıtlı diyet , FA’sız amino asit karışımları ve özellikli üretilmiş düşük proteinli gıdalar ile beslenmeye başlanılmalıdır. Hastaların yeterli protein ve kalori alımları 3 günlük diyet listesi ile mutlaka kontroller sırasında değerlendirilmelidir.
2.3.1 Fenilketonüri ve protein metabolizması:
Hastalar, diyetlerindeki fenilalanin kısıtlanması nedeniyle protein dengesi açısından risk altında olabilirler. Takipleri sırasında bakılan diyet listeleri ve laboratuvar değerleri göz önüne alınarak beslenmelerinde düzenlenme yapılır.
Prealbumin, protein durumunu göstermede oldukça yararlı olduğu bilinen bir belirteçtir. Yarılanma ömrü kısadır ( 2 gün ). Protein enerji malnutrisyonunda olduğu gibi düzeyinin düşük saptanması protein sentezindeki azlığı ile açıklanabilir. Prealbumin, protein ve enerjiden kısıtlı beslenmelerde adaptif cevap olarak kendi sentezini azaltmaktadır (70, 71).
2.3.2. Fenilketonüri ve mineral – vitamin değerlendirmesi:
Vitamin E:
E vitamini yağda çözünen bir vitamin olup 8 farklı formda ( alfa, beta, delta ve gama tokoferol, alfa, beta, gama ve delta tokotrienol ) bulunmaktadır ve en aktif formu alfa tokoferoldür. Antioksidan etkinliği olması nedeniyle serbest radikallerin zararlı etkilerinden hücreleri korur (72, 73).
FKÜ olgularında vitamin E ile ilgili olarak oksidatif stresde yer aldığı ve buradaki kullanımı nedeniyle düzeylerinde düşüklük saptandığı belirtilmektedir (74, 75).
Vitamin A:
Çocuklarda vitamin A büyüme ve gelişme için önemlidir. Loş ışıkta görmeyi sağlayan retinal pigmentlerin bir parçası olarak, kemik ve dişlerin gelişimi yanısıra mukozal yüzeylerin yapısının korunmasında, mukus üretiminde ve immun yanıtta önemli rol oynar (76). Eksikliğinde anemi, immun sistemin bozulması ve ishal, kızamık gibi hastalıkların mortalite ve morbiditesinde artış gözlenmektedir (77).
Yapılan çalışmalarda iyi kontrollü FKÜ olgularının vitamin A düzeylerinin kötü kontrollü olgulara göre yüksek olduğu gösterilmiştir (78).
Folik asit:
Diyetle alınan folatın, DNA metilasyonu, tamiri ve replikasyonunda vazgeçilmez önemi vardır. Nükleik asid sentezinde kofaktör rolü olduğu bilinmektedir.
FKÜ olgularında bakılan folik asit değerlerinin yüksek olduğu bildirilmektedir. Bu durumun almakta olduğu diyet tedavisindeki folik asit içeriğinin yüksek olmasından kaynaklanmaktadır (79, 80).
B12 vitamini ( Kobalamin ):
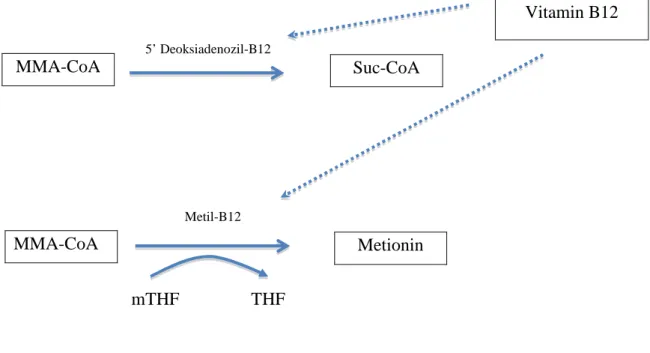
B12 vitamini, başlıca Metilmalonil CoA’nın (MMA-CoA) süksinil CoA’ya (Suc-CoA) dönüşümü ve homosisteinin ( Hcy ) metiyonine dönüşümünde kofaktör rolü oynar (şekil 6). B12 vitamini daha çok balık, yumurta, et, süt ve süt ürünlerinde bulunmaktadır.
Bu gıdaların diyetten çıkarılması, uygulanan diyetin bırakılması veya FA’sız amino asit karışımlarını tüketmemesi B12 vitamin eksikliğine yol açmaktadır. Adölesan ve erişkin hasta popülasyonunda özelikle karşılaşılmaktadır (81). Klinik olarak periferal nöropati, spinal kordun subakut kombine dejenerasyonu, spastik paraparezi, daha ağır formlarında otonomik disfonksiyon, optik atrofi ve psikiyatrik sorunlarla karşılaşılabilir. Bu açıdan hastanın kontrolleri sırasında B12 vitamini düzeyi ölçülmesi gerekli bir parametredir.
Şekil 6 : B12 vitaminin biyokimyasal yolağı (82) ( Metilmalonil CoA’nın (MMA-CoA) süksinil CoA’ya (Suc-CoA) dönüşümü ve homosisteinin ( Hcy ) metiyonine dönüşümünde kofaktör rolü ( mTHF; metil tetrahidrofolat, THF; tetrahidrofolat )
Çinko ve Bakır :
Çinko, beslenmede esansiyel olarak kabul edilen bir eser elementtir. Daha çok et ürünlerinde bulunmaktadır. Çinko birçok enzimin kofaktörü olarak rol oynamaktadır. Bu yüzden hücre yapımı ve fonksiyonları, nükleik asid metabolizması ve immun fonksiyonda önemli rol oynamaktadır (83).
Bakır da birçok enzimin ( seruloplazmin, sitokrom C oksidaz, süperoksit dismutaz, lizil oksidaz, tirozinaz, dopamin beta hidroksilaz gibi ) yapısında yer alır. Eritropoez ve oksidatif olaylardan sorumludur. En çok karaciğerde olmak üzere daha az miktarda beyin, kalp, böbrek, kemik, kas ve endokrin salgı bezlerinde bulunmaktadır. Diyetle alındığında
MMA-CoA 5’ Deoksiadenozil-B12 Suc-CoA MMA-CoA Metionin Metil-B12 Vitamin B12 mTHF THF
büyük bir kısmı duodenumdan emilmektedir.
Çinko için bazı çalışmalar FKU olgularında yeterli düzeyde alım olduğunu söylemesine rağmen bu konuda görüş birliği yoktur. Aslında günlük 20 gr protein eşdeğerinde FA’sız amino asid karışımı alan olgular ihtiyacı ( 4 – 10 mg/gün ) kadar almış kabul edilmektedir (84, 85).
Bakır açısından literatüre bakıldığında FKU olgularında yapılan çalışmalarda çinkodan farklı olarak bakır elementinin eksikliğinin görüldüğü bildirilmiştir (86).
Demir , ferritin, total demir bağlama kapasitesi, hemoglobin:
Demir (Fe); birçok biyolojik süreçte önemli rol alır. Oksidasyon ve redüksiyonda kofaktör olarak hayati yeri vardır. Demir iki şekilde diyette bulunur; hem demiri ( Fe +2 ) ve hem olmayan demir ( Fe +3 ). Diyetteki demirin %10’u Fe +2 şeklindedir. Ette yüksek oranda bulunur. Et tüketimi az olan yerlerde demir eksikliği anemisi sıklıkla bildirilmiştir. Hem olmayan demir ise diyetteki demirin %90’ını oluşturur. Sebze ve tahıllarda bulunur. Demir emilimi duodenumda oluşur. Fizyolojik pH’da diyetle alınan Fe +2, Fe +3’e dönüşür. Duodenum enterosit yüzeyine gelen Fe+3 tekrar ferrik redüktaz ile Fe +2 formuna indirgenir. Böylelikle enterosit içine alınır. Transferrine bağlanarak enterosit içinde bazolateral zara ulaşır. Buradan da dolaşıma geçerek ihtiyacı olan tüm organlara iletilir. Demir, transferrinin yaklaşık 1/3’üne bağlanır. Total demir bağlama kapasitesi ( TDBK ), transferrin üzerindeki demiri bağlayan bölgelerin toplamını gösterir (87).
Transferrin, demir kullanan/depo olarak görev gören organlara demir taşımada kullanılan plazmada bulunan bir proteindir.
Ferritin ise vücuttaki depo demiri gösterir. Eritroid ana hücreler ile makrofaj ve hepatositlerde en yüksek miktarda bulunur (88).
Serum demir düzeyinde azalma, TDBK'de artış ve transferrin satürasyonunda (TS) azalma demir eksikliğini gösterir. “TS = 100 x serum demir konsantrasyonu / total demir bağlama kapasitesi” formülüyle hesaplanır. Demir eksikliği anemisinde TS %16'nin altında bulunur. Serum ferritin düzeyi bahsedildiği üzere vücut demir deposunun en iyi göstergesidir. Yüksekliğinde aynı zamanda akut faz reaktanı olması nedeniyle enfeksiyon
ve inflamasyon ekarte edilmelidir. 10-12 μg/L'den daha düşük olması demir eksikliğinin göstergesidir (87).
Demir eksikliğinin en önemli göstergesi olarak anemi terimi kullanılır. Ancak anemi olmadan da demir eksikliği gelişebilmektedir. Demir eksikliği farklı evrelerde ortaya çıkar. Eğer demir gereksinimde eksiklik varsa, ilk önce demir depolarında azalma beklenir. Bundan sonra hemoglobin düzeyi bir süre normal kalabilmektedir ( anemi olmadan demir eksikliği görülen evre ). Bu dönemde plazma ferritin ve plazma transferin satürasyonu azalır. Demir depoları tüketildikten sonra hemoglobinde azalma kendini gösterir. Bu durum demir eksikliği anemisi olarak tanımlanmıştır (89).
Fe+3 (hem olmayan demir), FA’sız amino asit karışımlarında ferröz sülfat olarak bulunmaktadır. Burada Fe+3 emilimini etkileyen faktörler arasında yüksek oranda kalsiyum alımı, yeşil yapraklı sebzeler ve otlar, baharatlar bulunur. Tam tersi C vitamininden yüksek meyve tüketimi emilimini arttırmaktadır (90). Demir eksikliği anemisi dünya nüfusunun yaklaşık %25’ini etkilemektedir. Tabiki FKÜ olgularında da sıklıkla bu durumdan her yaş grubunda bahsedilmektedir. Topluma göre hemen hemen eşit prevelansa sahiptir. Olgular klinik olarak ( uzun ve ağır demir eksikliğinde ) dikkat, hafıza ve öğrenmenin yanı sıra fiziksel iş performansında olumsuz etkilenimi ön plandadır (91, 92). Unutulmamalıdır ki anemi olmadan da FKÜ olgularında demir eksikliği gözlenebilmektedir (93). Bu açıdan rutin kontrolleri sırasında mutlaka demir parametrelerine bakılması gerekmektedir.
2.3.3. Fenilketonüri ve kolesterol metabolizması değerlendirilmesi:
Günlük kolesterolün %20-25’i karaciğerde sentezlenir. Daha az bir kısmı barsaklar, adrenal bez ve genital organlarda olur. Asetil CoA ve asetoasetil CoA, 3-hidroksi 3-metil glutaril (HMG) ile hidrolize edilerek sentez oluşturulur. HMG CoA redüktaz tarafından mevalenota dönüştürülür. Mevolonat birkaç metabolik yolak sonrası lanostrole, lanosterol ise kolesterole dönüştürülerek sonlanır.
FKU olgularında yapılan çalışmalarda kolesterol düzeyi ile FA düzeyi arasında ters ilişki bulunmuştur (94). Bunun ise diyet tedavisi ile protein alımının azlığına bağlı olabileceği ifade edilmektedir. Bir başka literatürde kolesterol biyosentezinde, sentez basamaklarını inhibe ederek etkileyebileceği belirtilmektedir (95).
2.3.4. Fenilketonüri ve kemik metabolizması değerlendirilmesi:
Kemik gelişimi açısından yeterli miktarda kalsiyum, fosfor ve vitamin D alımı gerekliliği bilinmektedir. D vitamini insanda; vitamin D2 ( ergokalsiferol ) ve vitamin D3 ( kolekalsiferol ) şeklinde bulunur. Kolekalsiferol, güneş ışınları ile karşılaşan deride 7 - dehidrokolesterolden elde edilir. Güneş ışınları ile karşılaşan bitkilerde ergokalsiferol oluşur. Diyetle beraber alınır. Bunlar karaciğerde 25 - hidroksi vitamin D3 ve 25 - hidroksi Vitamin D2’ye çevrilir. Her ikisini tanımlamak için 25 hidroksi D vitamini (kalsitriol) kullanılır (96, 97). 25 hidroksi D vitamini, D vitamini alımını ve sentezini gösteren kan serumunda bakılabilen iyi bir parametredir. Yarılanma ömrü 2-3 hafta olarak bilinmektedir (98).
Kalsiyum kemik sağlığının korunması yanı sıra kas kasılmasında, iyon transportu ve sinir uyarı iletiminde görev alan başlıca minarellerdendir. Besinlerle alınan kalsiyum emilimi için çözünebilir hale getirilmesi gerekir. Mideye geldiğinde çözünürlüğü artar daha sonra duodenumdan kalsiyum bağlayan protein vasıtasıyla ince barsaklardan diffüzyon ile emilir. Kalsiyum emilimini; 1,25 dihidroksi vitamin D, kalsiyum bağlayan protein yapımını uyararak arttırır (99).
FKU hastalarda her yaş grubunda kırık ve azalmış kemik mineral dansitesi bildirilmektedir. Yetersiz mineral, D vitamini ve protein alımı; hastalığın getirdiği süreç ya da prolin gibi (kollajen yapısında bol bulunan) non esansiyel amino asit eksikliği bu durum açısından suçlanmakla beraber net olarak kesinleşmemiştir ( 100, 101 ).
3. GEREÇ VE YÖNTEMLER
3.1. Çalışma Grubu:
Çalışmamız, Temmuz 2015 – Eylül 2015 tarihleri arasında Ege Üniversitesi Tıp Fakültesi Çocuk Sağlığı ve Hastalıkları Anabilim Dalı Metabolizma – Beslenme Bilim Dalı’nda takip edilen 27 FKÜ veya HFA tanılı hasta üzerinde gerçekleştirilmiştir. Çalışmada FKÜ tanılı çocukların, diyet tedavisi ile beraber nütrisyonel durumları üzerindeki etkilerinin belirlenmesi amaçlanmıştır.
3.1.1. Kapsam
Hastalar aşağıdaki özelliklere göre çalışmaya dahil edildi:
• Ege Üniversitesi Tıp Fakültesi Çocuk Sağlığı ve Hastalıkları Anabilim Dalı Metabolizma ve Beslenme Bilim Dalı’nda takip ve tedavi edilen,
• 6 aydan uzun süredir FKÜ veya HFA tanısıyla izlenip feninalaninden kısıtlı diyet alan,
• Tanı anında kan FA düzeyine göre HFA ( kan FA: 120 - 600 μmol/L veya 2 - 10 mg/dl olanlar ), hafif FKÜ ( kan FA: 600 – 1200 μmol/L veya 10 - 20 mg/dl arasında olanlar ), klasik FKÜ ( kan FA: 1200 μmol/L veya 20 mg/dl üzerinde olanlar ) olarak üç gruba ayrılan,
• 6 ay – 12 yaş arasında olan,
• Düzenli poliklinik kontrolleri yapılan olgular. 3.1.2. Çalışmanın yürütülmesi
Çalışma için Ege Üniversitesi Tıp Fakültesi Klinik Araştırmalar Yerel Etik Kurulu tarafından etik kurul onayı ( karar no:15-5.1/45, tarih:25.05.2015 ) alındı. Ege Üniversitesi Tıp Fakültesi Çocuk Sağlığı ve Hastalıkları Anabilim Dalı Metabolizma ve Beslenme Bilim Dalı’na kontrole gelen ve yukarıda belirtilen özelliklere sahip olanlar, ebeveynlerinin onayları alınması şartıyla çalışmaya dahil edildi.
FKÜ/HFA tanısı ile izlenen hastaların poliklinik kontrolleri sırasında aşağıdaki özellikleri dikkate alındı:
1 ) Beslenme anamnezi: 3 günlük besin tüketimi hesaplanarak, günlük FA ve protein tüketimlerinin uygunluğu saptandı.
2 ) Büyümenin değerlendirilmesi: Ağırlık ve boy değerleri; aynı yaş ve cinsiyet persentil değerleri, standart deviasyon skorları ( SDS ), vücut kitle indeks SDS’leri ve rölatif tartıları ile karşılaştırıldı. Burada kullanılan değerlerde, Olcay NEYZİ 2008 Türk çocukları için belirlediği ölçek kullanıldı (102).
Vücut kitle indeksi (VKİ): Ağırlık (kg)/boy uzunluğu (m)2 formülü ile hesaplandı. Boya göre vücut ağırlığı ise boy yaşına uyan 50’inci persentildeki ağırlık değeri olarak tanımlandı.
DSÖ büyüme standartlarına göre yaşa göre boy uzunluğunun -2 z skorunun altında olması kısa boyluluk, yaşa göre ağırlığın -2 z skoru aldnda olması düşük kiloluluk ve yaşa göre VKİ değerinin -2 z skoru aldnda olması ise zayıflık olarak sınıflandırılmışdr. DSÖ çocuk büyüme standartlarında çocukların +1 z skoru üzeri fazla kilolu, +2 z skoru üzeri obezite, +3 z skorunun üzeri ise morbid obezite olarak belirlenmişYr.
Boy, büyümede en yavaş etkilenen değişkendir ve yaşa göre boyun değerlendirilmesi, iskelet sisteminde kemik büyümesini gösteren en temel göstergedir. Buna göre, referans grubun ortanca değerinden eksi iki standart sapma (-2 SD) gösteren çocuklar, yaşlarına göre kısa boylu (bodur-stunded) kabul edilmekte ve bu uzun süreli bir büyüme geriliğinin, kısaca süreğen beslenme sorununun göstergesi sayılmaktadır.
Rölatif tartı: Hastanın tartısı/hastanın boya uyan tartı değeri x 100 formülü ile hesaplandı. Bulunan değer %90-110 arasında olması normal, %80-89’ı arasında olması hafif, %70-79 arasında olması orta, %70’in aldnda olması ise ağır malnütrisyonlu olarak kabul edilmişYr. %110-120 arasında olması fazla kilolu, %120 üzerinde olması ise obezite olarak tanımlanır.
3 ) Hastalığa özgü laboratuvar kontrolü: Kan FA, tirozin değerleri kontrol edildi. Kan FA değeri 2 – 6 mg/dl arası normal kabul edildi. Kan tirozin değeri ise 0,8 – 1,3 mg/dl normal olarak belirlendi.
4 ) Beslenme parametreleri: Kolesterol, trigliserid, kalsiyum, çinko, bakır, hemoglobin, demir, demir bağlama kapasitesi, ferritin, prealbumin, vitamin A, vitamin E, 25 OH D vitamini, B12 vitamini ve folik asit düzeyleri belirlendi. Transferrin saturasyonu ise “100 x serum demir konsantrasyonu / total demir bağlama kapasitesi” formülü ile hesaplandı. Herbir parametre için normal – patolojik ayırımı, literatürden elde edilen değerler kullanılarak yapıldı (103 - 105).
5) Tüm veriler, ortalama ± SD olarak ifade edildi.
6) Hastaların tüm verileri iki aşamalı olarak değerlendirildi.
* Bazal Değerlendirme: Her hastanın, fizik bakı – beslenme durumu ve laboratuvar parametreleri, çalışma sürecinde incelendi.
* Geçmiş Değerlendirme: Hastaların daha önce, geçmişte yapılan fizik bakı – beslenme durumları, laboratuvar parametreleri incelendi. Bu aşamada; bazal değerlendirmeden en az 6 ay veya daha eski zamanda elde edilmiş veriler, dosya kayıtlarından alındı.
7) Aktif veya kronik enfeksiyon belirtileri gösteren ve katabolik süreç içinde olan hastaların yanısıra, ilaç tedavisi ( sapropterin dihidroklorid, vitamin ve mineral ) alan hastalar da çalışmaya dahil edilmedi.
8) Olgular bazal ve geçmiş verilerine göre ayrılarak tüm sonuçları karşılaştırıldı.
3.2. Yöntemler
Hastaların tümünden diyet tedavisine başladıktan en az 6 ay sonra alınan kan örnekleri ve beslenme parametreleri, Ege Üniversitesi Tıp Fakültesi Tıbbi Biyokimya Anabilim Dalı‘nda aşağıda belirtilen yöntem ile çalışıldı.
Hemoglobin düzeyi: Sysmex marka, XN-2000 model tam kan sayım cihazında, amonyum tuzları kullanılarak, siyanit içermeyen kolorimetrik ölçüm yöntemi ile 555 nm dalga boyunda ölçüldü.
Kolesterol düzeyi: Roche marka, Cobas 702 model analizörde, enzimatik kolorimetrik yöntemle ölçüldü.
Trigliserid düzeyi: Roche marka, Cobas 702 model analizörde, enzimatik kolorimetrik yöntemle ölçüldü.
Kalsiyum düzeyi: Roche marka, Cobas 702 model analizörde, Schwarzenbach ile o-cresolphthalein kompleks yöntemi vasıtasıyla ölçüldü.
Vitamin E düzeyi: Shimadzu marka , LC-20 AT model cihazda yüksek performanslı likid kromatografi (HPLC) yöntemi ile ölçüldü.
25 OH D vitamini düzeyi: Shimadzu marka , LC-20 AT model cihazda yüksek performanslı likid kromatografi (HPLC) yöntemi ile ölçüldü.
B12 vitamini düzeyi: Roche marka Cobas 602 model analizörde, immünolojik elektrokemilüminesans ölçüm yöntemi ile ölçüldü. (ECLIA)
Folik asit düzeyi: Roche marka Cobas 602 model analizörde, immünolojik elektrokemilüminesans ölçüm yöntemi ile (ECLIA) ölçüldü.
Çinko düzeyi: Shimadzu marka, AA-7000 model cihazda, atomik absorbsiyon spektrometri (AAS) yöntemi ile ölçüldü.
Bakır düzeyi: Shimadzu marka, AA-7000 model cihazda, atomik absorbsiyon spektrometri (AAS) yöntemi ile ölçüldü.
Demir düzeyi: Roche marka, Cobas 702 model analizörde, kolorimetrik yöntemle ölçüldü.
Ferritin düzeyi: Roche marka Cobas 602 model analizörde, partikül yüzeyi genişletilmiş immunoturbidimetrik yöntem ile ölçüldü.
Total demir bağlama kapasitesi: Roche marka, Cobas 702 model analizörde, demir düzeyi ve ferrozine ile doğrudan ölçüm yöntemi ile saptanan ansatüre demir bağlama kapasitesinin toplamı ile elde edildi.
Prealbumin düzeyi: Roche marka Cobas 602 model analizörde, immunoturbidimetrik yöntem ile ölçüldü.
Vitamin A düzeyi: Shimadzu marka , LC-20 AT model cihazda yüksek performanslı likid kromatografi (HPLC) yöntemi ile ölçüldü.
3.3. İstatistiksel Analiz
Gruplara ayrılan değişkenlerin geçmiş ve bazal arası karşılaştırmalarında Ki-kare testi uygulanmıştır. Numerik değişkenlerin karşılaştırılmasında ise öncelikle Shapiro-Wilk testi ile normallik testi uygulanmış, normal dağılımdan sapma göstermeyen değişkenlerin geçmiş ile bazal arası karşılaştırmasında eşli t-testi (Paired samples t-test) kullanılmıştır. Parametrik olmayan korelasyonlar Spearman’s rho testi ile değerlendirildi. Tanımlayıcı istatistik olarak veriler için ortanca ( min – max ) değerleri verildi. P < 0.05 ise istatistiksel olarak anlamlı kabul edildi.
Bu çalışmadaki tüm istatistik analizleri Statistical Package for Social Sciences (SPSS 20.0) programı yardımı ile gerçekleştirilmiştir.