A. V. Vet. Fak. Derg. 31 (1) : 98-106, 1984
MO:\'OKLO:\'AL A:\'TİKORLAR
Müjgan İzgür*
K.Serdar Diker*
Manadanal Antibadies
Summary:
Monodonal
antibodies
are /lOlIlogeneolıs jJojmlatioııs
of
idenlical antibody molecules. Monodonal antib04y technology is a/orm of geııetic
engineering resulting in the production of specific antibodies by sjJeciali;::,edlissuc
culture lines. The production of these antibodies through cellh)'bridizatiol1 permits
the dissection of complex antiboqy responses into their indiı'idual components.
The tlOo biological components esscntialfor
the creatian of hybrid eells are
antibody-prod/lcing spleen eells .from immunized
miee or rats and t/lmor eell
lines ol (ymphoid origin ealled m)'elomas. Single antibod)'~lormil1g eclls from
immuııized rodents are ji/sed with
m):cloıııa eclis to create /ıybridomas wit/ı
properties of both parent eell types. These /ıybridomas produee the single fype
~r
antibody moleeule tlzat tlzey inlzeı-itedfrom tlze normal antibody-jorming
eell
parent. Hybrid cells derived in tlzis way can produee unlimited
quantitites of
speeifie alZtibody in tissue culture or when grown i"n vivo as aseites tumors. lt
is possible to produee monodonal antibodies to an)' antigen by appropriate
selee-tion teelzniques. Monodonal
antibodies Izave wide applieation in man)' areas
~r
human and veterinary medicine and biologieal seienee.
Özet:
l\lonoklonal
antikorlar Izibrid hücreler tarafindan üretilen
homo-jen alZtikor topluluklarıdır.
Bu antikorlar,
bağışıklanmış fare veya ratlardan
elde edilen dalak Izücreleri ile myeloma adı verilen lenfoid tümör hücrelerinden
geliştirilen melez Izücreler tarafından üretilirler. ller iki tip hücrenin
özellik-lerini taşıyan hibridomalar,
doku kültürlerinde
veya ascites tümörlerinde çok
miktarda
monoklonal antikor oluştururlar.
Alonoklonal
antikorlar,
injeksiyöz
etkenlerin ve hücre yüz~yi
antijenlerinin
teşhisi ve immunoterapi
alanlarında
kullanılmaktadırlar.
Giriş
Organizmaya
antijcnik
bir maddenin
injeksiyonundan
sonra,
B-lcnfositlerinin farklılaşması ilc ortaya çıkan plazma hücreleri,
bu
MONOKLONAL ANTİKORLAR 99
antijene karşı özgül (spesifik) antikorlar üretirler. Antikor i~le\i gören immunoglobulinler, serum proteinlerinin gamma-globu1in fraksiyo-nunda yer alırlar. Bir irnmunoglobulin molekülünün yakla~ık 100 amino asitten ibaret ol<.ın antijen bağlanma ucu, bu amino asitlerin değiljik yerleşim kombinasyonlarına bağlı olarak 106-107 antijeni
tanıma yeteneğine sahiptir (i 7). Antijen molekülünün yapısında bulunan farklı antijenik d(:tcrminantlara karşı olu~an antikorlar, bir-den çok B-lenfüsit kümesinden (klon) köken aldıkları için heterojenik özelliktedirler ve poliklonal antikorlar şeklinde de tanımlanabilirler. Elektrofürez yöntemi ilc incelenen bağışık serumdaki poliklonal anti-karların heterojenik dağılımı Şekil ia 'da gösterilmiştir.
Herhangi bir antijen ilc uyarılan öncü i (prekürsör) bir B-lcnfo-siti seçilerek bu hücrenin üremesi ve antikor oluşturan bir plazma hüc-rcsine değişimi sağlanır ise, bu antijene karşı "monoklonal antikorlar" adı verilen, tek tip antikorların homojen olarak üretimi sağlanır. Yük-sek özgüllükteki bu tip antikorların elde edilmesi, Köhler ve l'vIils-tein'ın (6) somatik hücre melezlemesi (hibridizasyon) ile mycloma hücreleri ve B-lcnfüsitlerini birleştiren çalışmaları ilc gerçekleşmiştir. :\1yeloma; tck bir B-hücresinden kiiken alan ve serumda tck tip bir antikorun çok miktarda bulunması ilc karektcrize neoplastik bir has-talıktır. Monoklonal antikorlar, antijen molekülünün sadece belirli antijenik determinantlarına karşı oluştu kı arı için çok spesifiktirler. Elektrofürez yöntemi ile incelenen mycloma1ı bir serumdaki mono-klonal antikorların homojenik özellikleri şekiII b'de gösterilmiştir (17).
alP
OLiKlCJ.JAl
albumın ""'- p- rglOblJlin b)MONOKlONAl~./"(j)""
ri'iJ
r/,@
\/
albUmın oc- ~- ı-globul;n
Şckil i. Bir antijcnc karşı oluşan, (a) poliklana!, (b) monoklanal antikor1arııı scrumdaki elektroforctik görünümü.
Thc pattcrns obtaincd fram electraphoresis of (a) normal antiserum and (b) scrum with myeloma.
100 M. İZGÜR-K. SERDAR DİKER
Monoklonal Antikor Oretim Tekniği
Monoklanal
antikarlar,
iki tip ana hücreden
geliştirilen
melez
(hibrid)
hücreler
tarafından
üretilirler.
İşlevleri antikor üretimi olan
B-lenfositleri
ile
ncaplastik
myeloma
hücrelerinin
hibridizasyonu
sonucu ortaya çıkan melezIer, her iki ana hücre tipinin özelliklerini
taşırlar.
Hibriclomalar
ana lenfasit hücresinin
sentezlediği
antikorun
aynısını
oluşturabilir
ve ana myeloma
hücresi gibi in "itro
olarak
üreyebilirler.
Monoklanal
antikor üretimini
sağlayan
teknik;
rodent-lerin
immıınizasyonu,
somatik
hücre
melezlemesi
(fusian
işlemi),
hibrid
hücrelerin
antikor
aktivitesinin
belirlenmesi,
antikor
üreten
hücrelerin
kümelendirilmesi
(kıanlama)
ve bu hücrelerin
seri şekilde
üretilmesi gibi aşamaları
içermektedir
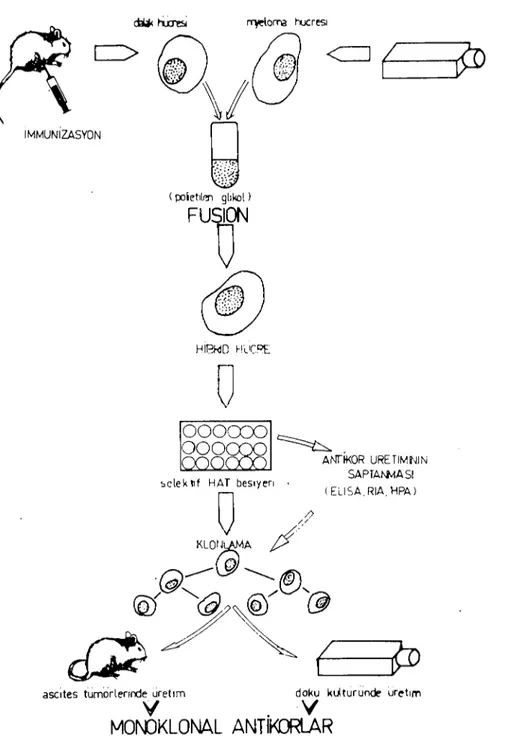
(Şekil 2) (2, 8, 16).
!ıiydoma hücre hatları:
rvIonoklonal antikor
üretimi
fare ve
ratla-rın B-lenfositi myeloma tümörlerinden
elde
edilen
hücre
hatlarının
geliştirilmesi ile mümkün
olmuştur
(6). İn vivo yolla kolaylıkla
oluş-turulabilen
myelomalardan
elde edilen bu hücreler in vitro olarak da
üreyebilmektedirkr.
Bir pürin metabolizması
enzimi olan
hipoksan-tin-guanin
fosforibozil transferaz
enziminden
yoksun olan bu
hücre-ler, hipoksantin,
aminopterin
ve timidin
(HAT)
içeren kültürlerde
üreyemezler.
Ayrıca myeloma hücreleri
kendi
immunoglobulinl,erini
sentezleme
yeteneğini
kaybetmişlerdir.
Monoklanal
antikor
üretimin-de, fare ve rat myeloma
hücreleri
kullanılmaktadır.
Rat
mycloma
hücreleri,
daha büyük olmaları ve daha kolay kaynaşmaları
(fusian)
nedeniyle fare mycloma hücrelerine
tercih edilirler. Ayrıca, fare
mye-lomalan
ile insan
ve diğer
türlerin
B-lenfositlerinclen
elde edilen
melez hücreler,
in vitro kültürlerde
kromozamlarını
ve antikor
sen-tezleme
yeteneklerini
kaybederler.
Fare
myeloma
ve rat
lenfasit
melezIeri, rat-rat
ve fare-fare hibridlcri
kadar dayanıklİdırlar.
Hibri-dizasyon çalışmalarında
en çok Balb je farclerinden
elde edilen X63,
SP2jO
ve ratlardan
elde edilen YB2/30 hücre hatları
kullanılmak-tadır
(3).
Bağışıklama (İmınunizasyon):
Monoklanal
antikor
üretimi
için
gerekli olan immunizasyon
protokolü,
normalde
antiserum
elde
edil-mesinde kullanılan
yol ile aynıdır.
Fakat monoklanal
antikor
üreti-minde bağışıklama
işlemi için saf antijen kullanmak
zorunlu değildir;
saflaştırma
işlemi kontrol
aşamasında
yapılır.
Kuvvetli
antijenler,
melezleme çalışmasından
4 gün önce tek doz şeklinde; zayıf
MONOKLOKAL ANTİKORLAR
ıoı
IMMUNlZASYON cw< ~ rryelOrn1 NJmsıc>
(@)\/~
CJ (~~
~
(ÇXJietll~ glıkol)FUtCX'J
c!)
..
<:i: . .)/}~.
H IPI-<IO H,XO£:O
1:~ffi3I~
000
.
ANrIKOR URETIMNIN
SAPTA~ASI ~CLek ~t HAT
O
besıyerı .,l
(WSA.R(A.HPAIKLOt~A
,tl.,
(91
f~~
~@)~
cd/,
~-====-to
ascites tumorlerırde uretım doku kuturund!.' uretllTl
V
V
MOr-nKlONAl
ANTiKORl.AR
Şekil 2. Monoklonal antikor üretim tekniği. The production of monodonal antihodies.
1()2 M. tZGÜR-K. SERDAR DIKER
şekilde aralıklı birkaç injeksiyon ilc, B-lenfositlerinin eld(~ edileceği deneme hayvanlarına verilir (2).
Ka)'naştmna (FII5ion) iş/fmi: iki ayrı hücrenin birlcştirilme işlemi olan fusion, monoklonal antikor üretiminin en önemli aşamasıdır. Son antijen injeksiyonundan
3-4
gün sonra, bağışık kılınmış fare veya ratın dalağından lenfosit süspansiyonu hazırlanır (G). Bu hücreler, myelo-ma hücreleri ilc polietilen glikol bulunan bir test tüpünde birkaç daki-ka bekletilirler. Standart bir fusion için ortamda i X iO'
lenfosit ve 2 X 107 myeloma hücresinin bulunması geceklidir. Hücrelermikro-titrasyon kapları içindeki kültür vasatında :,;;oCde inkübe edilirler. Bundan sonra, hibridleri selektif olarak üretmek için hipoksantin-aminopterin-timidin (HAT) vasatı kullanılır. Kaynaşmamış parental myeloma hücreleri HAT besiyerinde üreyemezler. Normal lenfositler de, in vitro üreme yeteneklerinin olmaması nedeniyle kısa sürede ölürler. Bu durumda, HAT besiyerinde sadece hibrid hücreler üre-yebilmektedirler. Bu hibrieller, HAT besiyerinde üreyebilme özellik-lerini hipoksantin-guanin fosforibozil transferaz enzimine sahip olan ana lenfasit hücrelerinelen, in vitro üreyebilme özelliklerin ise ana ınyeloma hücrelerinden almışlardır (8).
Antikor
üretiminin
kontrolü:
Standart bir lusian denemesi için, ınikrotitrasyon kabmdaki 400 çukurun herbirine 0.2 ml hücre karışımı konur (I). Her çukur1-5
hibrid hücre içerebilir ve bu hibridler değişik oranlarda ürel'ler. Hızlı üreyen melez hücreler 10 gün içinde gözle görülebilen koloniler oluştururlar. Yavaş ür~yen hücrelerin bu duru-ma gelmelerı ise3-4
haftalık bir zaman alır. Bu üreme dönemi sırasm-da,I-L\
T içeren besiyeri düzenli olarak yenilenındidir.Fusion işleminden sonra oluşan hibridlerin tümünün antikor sentezlcme yeteneğinde olup olmadıkları bilinmemektedir. Bu nedenle, kullanılan antijene karşı hibridomalar tarafindan üretilen antikorlar, hücrelerin ürediği besiyerinin üst sıvısında aranırlar (17). Fusion işlemi rastgele olduğundan, antİkor sentezleyen hibridlerin oranı
% 1-50
arasında değişir. Antikorların üst sıvıdaki varlıklarımn
2-3
gün gibi kısa bir sürede kontrol edilmesi iki yönden önem taşımaktadır. Mikro-titrasyon kabının çukurlannda hızla üreyen melez hücreler metaboliz-ma artıklannın çoğalması nedeniyle ölebilirler. Diğer yönden, antikor üretmeyen hücreler hızla çoğalarak, antikor üretenleri baskılayabilir-ler. Üst sıvıdaki antikorların belirlenmesi amacıyla kullamlan antije-nin özelliğine göre, radyoimmunoassay, ELİsA ve hemolitik plak deneyi gibi duyarlı testlerden yararlamlmaktadır (13).MONOKLONAL ANTİKORLAR 103
Hibridlerin kümelendirilmesi
(kfonlama),
saklanması
1'1!(ada
miktarda
üretilmesi:
Üst sıvısında antikor
bulunan
çukurlardaki
melez
hücrc-ler, monoklonal
antikof üreten hücre hatlarını
elde etmek için
küme-lendirilirler.
Kümelendirme
i~lemi,. mikrotitrasyon
kaplarında
sınırlı
sulandırma
ilc veya yumu~ak agar üzerinde
üreıikrck
yapılır
(8).
Kümelendirilmi~
hibrid hücre hatları,
DMSO
(Dimetil
sülfook-sit) içinde sıvı nitrojenlc dondurulup
saklanırlar
vc gerektiğinde
tekrar
kuııanılabilirler
(2).
Elde edilen hibrid hücre hatları
in vitro olarak,
iml besiyerinde
10-100 mikrogram
monoklonal
antikor oluşturabilirler
(J).
Bu
anti-korlar,
ortamdaki
metabolizma
artıklarından
biyokimyasal
yöntem-lerle ayrılırlar.
Hibrid
hücre hatları,
in vivo olarak, fare ve ratların
karın boşluklarında
ascites tümörleri
oluşturma
özelliğine sahiptirler.
Hibrid hücrelerden
köken alan bu tümörler büyük miktarlarda
mono-klonal antikor sentezleyebilirler.
Böyle bir deneme hayvanından
top-lanan ascites sıvısının
iml'sinde 5-20 mg miktarında
monoklonal
an-tikor bulunabilir
(J 7). Hibrid hücreler ile üretimde kuııanılan
rodent-!erin doku uyu~umu iyi ise bu hücreler
daha kolay üremc ohınağına
sahip olurlar.
:Honokfonal Antikadarın
Kullanun
Alanları
Monoklonal
antikorlar
normal
antiserumların
yararlamldığı
bütün alanlarda
kullanılabilmekteclirler.
Ayrıca, çok yüksek
özgüııük-leri ve fazla miktarda
elde edilcbilmeleri
nedeniyle daha üstün özeııiğe
sahiptirler.
Monoklonal
antikorların
uygulama
alanları,
kuııanılan
antijenlere
göre 3 grupta
toplanabilir.
Bunlar, infeksiyüz hastalık
oluş-turan etkenler,
hücre yüzeyi antijenleri
ile proteinler
vc küçük
molc-küııerdir
(I).
l-
İnfeksi.J!öz etkenler:
Bakteri, virus ve parazitler
gibi infeksiyöz
etkenlere
karşı geliştirilen
monoklonal
antikorlar
bu hastalık
etken-lerinin tqhisinde,
aşı denemelerinde,
a~ı ürctiminde
ve immunoterapi
amacıyla
kuııanılmaktadırlar.
a) Teşhis: Çok geniş özgüııüğü.
tek ürnekliliği ve sınırsız
kuııa-nım alanları
ilc monaklonal
antikorlar,
teşhis amacıyla
kuııaınlmaya
çok uygundurlar.
Veteriner
hekimler,
çok yakın bir gelecekte,
influ-enza ve rhinopneumonitis
gibi atların
solunum
yolu patojenlerinden
ileri gelen infeksiyonları,
ticari kitler lıalindeki monoklonal
antikorları
an-ıoı
M. İZGÜR-K. SERDAR DİKERtijenlcre karşı bile elde edilebilen monoklonal antikorlar, alışılagel-miş scrol~jik testlerle birbirlerinden ayrılamayan çok yakın antijenik yapıya sahip mikroorganizma suşlarını da ayırabilmektedir. (I). Örneğin, köpek parvo virusunu kedi panleukopeni virusundan ayıra~ bilen monoklonal antikarlar üretilmiştir. Monoklonal antikorlar kulla-nılarak influenza virusunun hemaglütinasyon molekülürıün antijenik haritası çıkarılmış ve virusun in vitro mutasyon oranı saptanmıştır (18). Bu çalışma, doğal populasyondaki virusların mutasyon oranları-nı öğrenoranları-nıek bakımından önemlidir. Bu metotla, kuduz virusundaki mutasyon oranının, influenza virusundaki kadar sık olduğu saptan-mıştır. Kuduz virusunun doğal varyantıarının nadir olduğu düşünül-düğü için, bu sonuç araştırmacılar tarafından sürpriz olarak değerlen-dirilmiştir. Moııoklonal antikorlar, ayrıca polio, hepatitis-B, parainf-luenza ve herpes viruslarının teşhisinde kuııanılmaktaclırlar (I, 19). Mikobakterilcr, streptokoklar, stafilokoklar ve neisserialar gibi bakte-rilerin, ekinokoklar gibi parazitlerin ve klamidyaların oluşturdukları infeksiyonlar bu antikorlar ile çok hassas olarak teşhis edilebilmektedir
(5, 7, 9, i I).
b)
Aşı seçimi ve üretimi,'
:Vlonoklonal antikodal', aşı seçinıi aşa-masında, immun yanıtı en çok uyaran antijenIerin belirlenmesi ama-cıyla kullanılmaktadırlar (2). Bu işlem, rekombinant D::\A teknolojisi kullanılarak ölü aşıların hazırlanmasında ilk basamağı oluşturmakta-dır. Aşı seçiminde böyle ayrıntılı bir antijenik analizin yapılması, özellikle paraziter infeksiyonlarda önem taşır. Bu amaçla, tripanazo-malara, plasmodimlara, schistosomalara ve thcilarialara kaqı mono-klonal antikorlar üretilmiştir (I).c)
Pa.>ı!"immunoterapi,'
Ascites sıvısından çok yoğun olarak elde edilebilen monoklonal antikarlar pasif immunoterapi amacıyla da kullanılmaktadırlar (10). Örneğ!n, nakliye işleminden önce monok-Ianal antikorlar ile pasif immunoterapi uygulanan sığırlarda, seyahat hummasından ileri gelen kayıplar önlenebilmektedir (I). ~ormal pasif immunoterapi ile aynı ınekanizmaya sahip olan bu yolun avan-tajı, çok miktarda özgül antikorun sağlanabilmesidir.2- Hücre yüzeyi antijeıılr:ri:
Bu bölümde yer alan normal ve anor-mal hücre yüzeyi antijenleri 3 grup içinde incelenebilirler. Bunlar, polimorfik rnoleküııer, değişim antijenleri ve hücresel reseptörlerdir.a)
Polimo~-rik moleküller,'
Kaıı grubu antijenleri ve doku yuşurn antijenleri polimorfik moleküllerdir. Bu antijenler hakkındaki bilgilerMONOKLONAL ANTİKORLAR 105
sayesinde, klinik organ traı;ı.splantasyonları
ve kan transfüzyonu
C1aha
başarılı hir şekildc yapılabilmektedir
(IS). Ayrıca, kan grubu
antijen-lerine karşı geliştirilen
monoklanal
antikarlar,
sürülerin
genetik
ayrı-mında
kullanılarak,
daha
üstün özelliklr.re sahip sürülerin
gcli~tiril-mcsini sa~layacaklardır
(4). Yine bu antikorlardan,
organ
transplan-tasyonu için verici dokuların seçiminde ve doku uyuşum antijenicrini.ı
yapısının
belirlenmesinde
yararlanılmaktadır.
b) Değişim
antijenleri:
Değişim
antijenleri,
bir
hücreyi,
doku
vcya organı, diğer hücre, doku ve organlardan
ayıran antijenkrclir.
Dcğişim antijenleri
kapsamına
giren tümöre
özgül antijenkrc
karşı
geliştirilen
monoklanal
antikarlar,
immunoterapi
amacıyla
c1irek
ola-rak veya sitotoksik ilaçların taşıyıcısı olaola-rak indirek yolla
kullanılabilir-Icr (12). Tümöre
özgül monokıanal
antikorlar,
normal doku
antijen-Icri
ile
kros-reaksiyon
vermemektcdirler.
c) Hücresel reseptörler: Bu grup antijenkr
içine, hormonlar,
ilaç-lar ve mikroorganizmailaç-lar
için tutunma
ucunu
oluşturan
rescptürlcı
girmektedir.
Gelecekte,
bir hormon reseptörii
için özgül monoklonal
antikorların
injeksiyonu
ile hormon
aktivitesini
artırmaya
yönelik
klinik
uygulamalar
yapılabilecektir
(13).
3- Proteinler
iiediğer küçük molekiiller: Bu tip
antijenkrc
karşı
monoklanal
antikor
uygulaması
klinik
alanda
olmaktadır.
İmmu-noglobulin
sınıf ve alt sınıfları na karşı üretilen monoklonal
antikarial'
ticari kitler halinde satılmaya
başlannuştır
(14). Ayrıca, dokulardaki
ilaç birikimi
ve pcstisidler
ile yarış atlarındaki
yasak
ilaçlar bile bu
yolla rahathkla
belirlenebilir
(I).
Literatür
1-. Antczak, F.D. (I 982): l\1olıodoııal aıııibodies: ler/ıııoloıu aııd Iıoıeıılial ıı-,e. .I.Anı. Vet.
:Vlcd.Ass., 181: 100;). 1010.
2- Davis, W.C., McGuire, T.C. and Perryınan, L.E. (1982): Biomedical aııd biological
alıplicatioıı of monoelonııl mı/ibod)' ı<elmolog)' in deve/olıing coıııılries. l'rioritics in Biotcchno-logy Rcsearch for International Developmcnt. National Academy Press, \VaslıilıglOn,
n.c.
3- GaICre, G. and Milstein, C. (ı 981): Preparalioıı of moııodoııal ilIı/ibodies.' slrnıegies aııd
I"occdures. Mcıh.EnzymoJ., 73: 3-'!7.
4- Gershwin, L.J. (I 98i): H)'bridomas: ılıe prodııclioıı of nWllOdoıwl llIııibodies. California
Vet.,
ıo:
31-33.5- Hewitt, J., Coates, A.R.M., Mitchison, D.A. and Ivanyi, J. (I 982): The use rif
mu-riııe moııoeloııııl IlIllibodies willıoul IJllrificaliolı qf aıııigm iıı ılıe scrodiagııosis of tubereıdosis.
10(, M. lZGC:R-K. SERDAR DiKER
(i- Köhler, G. and Milstein, C. (19i:i): Col/ıillııOIlS cııllıııes ,;f./iIJl'd ce/Is suıeıilig flıııibody of Ii/ede[iııed slıeeijieil)'. :--Jaıure, 2'">0: 4'FI-49i.
i- LaBonardiere, C., Groclaude, j. et Ventura, M. (1983): Deleeıielll des hibrides
Sf(-relCllf.f d'i/ll/llııııoglobiııes ıııoııodoıınler /)(11 ngglıııil/flliıill dr Sınph. aureııs. Aıın. Immuno!.. 134C: 281-291.
8- Milstein, C. (I 980): ,\lol/oC/oıınl flıııibodics. Scienıific American, 243: :'IG.
9- Nowinski, R.C., Tam, M.R., Goldstein, R.C., Strong, L., Kuo, C.C., Corey, L., Stamm, W.E., Handsfield, H.H., Knapp, j.S. and Holmes, K.K. (1983):
f\loııodoıınl 17l1libodir.1 /01 diflgııosis of iııferlioııs disenses iıı hU1IIfllI.l. Scicnee, 2 19: G37,-G44. i 0- Pastoret, P.P. (i 9B2): ,'IIII/cor/ı.! 1IIoııodoııfllll' cl Iıers/ıeclil'e< d'fI/ı/ilimliol/ ciL Illediciııe
ı:elnriıın;,e. Ann.Retlı,\'et., i:{: 21-31.
11- Pavlov, H., Hogarth, M., McKenzie, I.F.C. and Cheers, C. (1982): LLL ı'iw nııd iıı
vilm e/lecls 0/ /Iloııoelıııwl flnıihoı~ı' loI)'ımligmr Dil i/llıııııııil)' lo iıı/eclioıı. Cel!' ımmunol,' 7
ı:
127.138,J2- Peng, W.W., Bressler, j.P., Castiglioni, E.T. and Veııis, j. (1982): Der:elolııııcııı offl moııochillfll nıılihod.)' ngfliJHI fi Iıımoı nssofinlf,d flııligcıı, Scicnce, 21'">:
ı
102-1 104. 13.. Sehröder, j. (I 9HO): Aloııodoıınl fll/ıibodırs: fi IICW {1i01Iii/ rcsearch nı/d i7l1ıı1ııIıodiagııosli(J.ivlcd.Bio!., 'i8: 1.'lf)-148.
14- Srikumaran, S., Guidry, A.j. and Goldsby, R.A. (ı 982): l'IDdllCliolı flııd characleri.
znıiol/ of /Iloııodoıınl nıııibod/i.< lo bOi:i/ıc iııııııııııoglohııliıı (,' , . .'\m ..I.Vet.Re,., 43: 21-2'">. l'i- Thiry, E. et Pastoret, P.P. (1981): !.rs nlılicOl/1S 1IIol/OdOl/nlıx. Anıı.Med.Vet., 12'">:
4Rj.4')3.
i(i- t~stün, T.n.ve AII<an,Ş.Ş. (ı 982): Hiıae ıııelc:;/emesi i'C /IloııohlııTlfl1 1111Ii/:orlar. Doğa,
(j C: 89-98.
17- Yelton, D.A. and Scharff, M.D. (I 980): .HııılodOlwl nıııibodics, :\lller.Sci., G8: 510-~)i(i.
lH- Yewdeıı, j.W., Webster, R.G. and Gerhard, W.U. (197')): Aıııigmic varia/ion iıı
ıhrce dis/il/cl dCIPTmiıımlls of aıı ilı[lııen.:n Iıpc A hamwgglıı/iııalioıı /Ilolrmlc. l\'aıure, 279: 246,248.
19- Weiss, R.A. (191:2\: l{rlııidolıll1S prodııce i'imscs {lS lL'ell as ımıibedies. Immuno!. Taday, 3: 292-294.