T.C.
EGE ÜNİVERSİTESİ TIP FAKÜLTESİ
ÇOCUK SAĞLIĞI VE HASTALIKLARI ANABİLİM DALI
SANTRAL ERKEN PUBERTE TANILI ÇOCUKLARDA
GnRH AGONİST TEDAVİSİNİN VÜCUT KİTLE
İNDEKSİ ÜZERİNE ETKİSİ
UZMANLIK TEZİDr. SEDEF ÖKSÜZ
TEZ DANIŞMANI Prof. Dr. ŞÜKRAN DARCAN
İZMİR 2020
ii ÖNSÖZ
Uzmanlık eğitimim boyunca bilgi ve deneyimleri ile eğitimime katkıda bulunan, kliniğimiz Ana Bilim Dalı Başkanı Sayın Prof. Dr. Kaan KAVAKLI başta olmak üzere tüm Çocuk Sağlığı ve Hastalıkları Öğretim Üyelerine,
Bilgi ve tecrübelerinden faydalandığım, kendisinden hekimlik sanatının inceliklerini öğrenme şansı bulduğum, tez hazırlama sürecim boyunca benden samimiyetini ve ilgisini esirgemeyen çok değerli tez hocam Sayın Prof. Dr. Şükran DARCAN’a,
Enerjisi ve dinamiği hiç bitmeyen, bilgisi ve hekimliği ile bana yol gösteren, tez dönemimde yardımını hiç esirgemeyen Sayın Uzm. Dr. Aysun ATA’ya
Tez çalışmamın istatistiksel analizlerini gerçekleştiren, bilgi ve desteğini sunan biyoistatistik araştırma görevlisi Sayın Gülden HAKVERDİ’ye,
Ekip ruhuyla bütün zor anlarda elinden gelenin en iyisini yapmak için gayret eden tüm Çocuk Sağlığı ve Hastalıkları Ana Bilim Dalı uzman, asistan, hemşire ve personellerine,
Güzel ve zor günlerimizde hep beraber olduğumuz, Ege Pediatri’nin hayatıma kattığı güzelliklerin başlarında gelen değerli insanlara,
Bugüne kadar sevgileriyle, özverileri ve fedakarlıklarıyla beni büyüten ve verdiğim her kararda arkamda duran, şimdiki konumuma gelmemde payları çok büyük olan aileme
Teşekkür ve saygılarımı sunarım.
Dr. Sedef ÖKSÜZ İzmir, Temmuz 2020
iii İÇİNDEKİLER ÖZET ... v ABSTRACT ... vii TABLOLAR LİSTESİ ... ix ŞEKİLLER LİSTESİ ... x KISALTMALAR LİSTESİ ... xi 1 GİRİŞ ... 1 2 GENEL BİLGİLER ... 2 2.1 Pubertenin Tanımı ... 2
2.2 GnRH Nöronal Sistemin Gelişmesi ... 2
2.3 Hipotalamus-Hipofiz-Gonad Aksı ... 2
2.3.1 Gonadotropin Salgılatıcı Hormon (GnRH) ... 2
2.3.2 Hipofizer Gonadotropinler ... 4
2.3.3 Cinsiyet Steroidleri ... 5
2.4 Adrenarş ... 6
2.5 Normal Pubertal Gelişim ... 6
2.5.1 Kızlarda Pubertal Gelişim ... 6
2.5.2 Erkeklerde Pubertal Gelişim ... 9
2.6 Pubertenin Başlangıç Yaşını Etkileyen Faktörler ... 12
2.7 Erken Puberte (Puberte Prekoks) ... 13
2.7.1 Santral (Gerçek) Erken Puberte ... 15
2.7.2 Periferik (Yalancı) Erken Puberte ... 15
2.7.3 Erken Pubertede Öykü ... 16
2.7.4 Erken Puberte Kliniği ... 16
2.7.5 Erken Puberte Tanı ... 17
iv
3 GEREÇ VE YÖNTEM ... 24
4 BULGULAR ... 27
4.1 Demografik Veriler ... 27
4.2 Tanıda Antropometrik Bulgular ve Kemik Yaşı ... 28
4.3 Tanı Laboratuar ve USG Verileri ... 30
4.4 İzlem Yıllarında Antropometrik Bulgularda Değişimler ... 31
4.5 Birinci Yıl İzlem Verileri ... 32
4.6 İkinci Yıl İzlem Verileri ... 33
4.7 Tedavi Sonu Verileri ... 35
4.8 Final Verileri ... 36
4.9 İzlem Yılları ve Final Verilerinin Karşılaştırması ... 39
4.9.1 Normal Kilolu Grup ... 39
4.9.2 Fazla Kilolu ve Obez Grup ... 40
4.9.3 Tüm Grup ... 42
5 TARTIŞMA ... 44
6 SONUÇLAR ... 48
KAYNAKLAR ... 50
v ÖZET
Amaç: Santral erken pubertenin (SEP) tedavisinde uzun yıllardır gonadotropin salgılatıcı hormon (GnRH) agonistleri kullanılmaktadır. Yan etkileri arasında vücut ağırlığında ve vücut kitle indeksinde (VKİ) artış görülmüştür ancak literatür incelendiğinde bununla ilgili yapılan çalışmalarda farklı sonuçlar elde edilmiştir. Biz de çalışmamızda SEP tanısı ile GnRH agonisti kullanmış olgularımızın tedavi süresince ve finalde VKİ standart deviasyon skoru (SDS) değişimlerini değerlendirmeyi amaçladık.
Gereç ve Yöntem: Ege Üniversitesi Çocuk Endokrinoloji ve Diyabet Bilim Dalı’nda Ocak 2004 ile Aralık 2014 tarihleri arasında idiyopatik SEP tanısı alarak GnRH agonist tedavisi kullanan 92 kız hasta çalışmaya dahil edildi. Olguların poliklinik dosyaları retrospektif olarak incelendi. Demografik verileri, izlem süresince belirli aralıkla yapılan antropometrik ölçümleri, tedavi dozları, görüntülemeleri elde edildi.
Bulgular: Çalışmaya alınan 92 kız hastanın 58’i normal kilolu, 31’i fazla kilolu ve 3’ü obezdi. Hastalar normal kilolu grup ile fazla kilolu ve obez grup olarak ikiye ayrıldı. Her iki grubun demografik özellikleri ve tedavi süreleri benzerdi.
Tüm hastaların tedavilerinin 1. yılında VKİ SDS değerinde anlamlı artış (p=0.014) olmasına rağmen tanı ve tedavi sonundaki değerler karşılaştırıldığında anlamlı farklılık saptanmadı (p=0.68).
Normal kilolu grubun tanı ve tedavinin 1. yılı VKİ SDS değeri arasında istatistiksel olarak anlamlı artış olduğu (p=0.004) görüldü ancak tanı ile final VKİ SDS’leri karşılaştırıldığında değerler benzerdi (p=0.15).
Fazla kilolu ve obez grubun VKİ SDS değerinin tedavi süresinde değişimi anlamlı bulunmadı (p=0.46).
Hastaların izlem süresince boy SDS değerlerinde azalma (p<0.01) gözlenirken tahmini erişkin boylarında artış elde edildi (p=0.005).Kemik Yaşı (KY)/Takvim Yaşı(TY) oranının izlem yıllarında istatistiksel anlamlı azaldığı saptandı (p=0.13).
vi Sonuç: Çalışmada SEP tanılı kızlarda GnRH agonist tedavisinin VKİ ve VKİ SDS arttrıcı etkisi görülmedi. Tedavi ile KY ilerlemesinin önüne geçilerek tahmini erişkin boyda artış sağlandı.
vii ABSTRACT
Aim: GnRH agonists have been used for many years in the treatment of central precocious puberty. Although its side effects include increase in body weight and body mass index (BMI), different results have been obtained when studies related in the literature are examined. In our study, we aimed to evaluate the changes of BMI SDS during the treatment and in the final of our patients who used GnRH agonists with the diagnosis of CPB.
Material and Methods: 92 patients who were diagnosed with idiopathic CPB between January 2004 and December 2014 at Ege University, Department of Pediatric Endocrinology and Diabetes were included in the study. The files of the cases were analyzed retrospectively. Demographic data, anthropometric measurements, treatment doses, and imaging performed at certain intervals during the follow-up were obtained.
Results: From the 92 patients included in the study, 58 of them were in normal weight, 31 of them were overweight and 3 were obese. The patients were splitted into two groups as normal weight group and overweight and obese group. The demographic characteristics and duration of treatment of both groups were similar.
Although there was a significant increase in BMI SDS value in the first year of the treatment of all patients (p=0.014), no significant difference was found when the values at diagnosis and the end of treatment (p=0.68).
There was a statistically significant increase between BMI SDS value of the first year of diagnosis and treatment in the normal weight group (p=0.004), but the values were similar when the diagnosis and final BMB SDS values were compared (p=0.15).
The change in BMS SDS value in the treatment period of overweight and obese group was not significant (p=0.46).
During the follow-up period, decrease in height SDS values (p=0.01) was observed, while an increase in estimated adult height was obtained (p = 0.005). CA/BA was found to decrease statistically significantly in the follow-up years (p = 0.13).
viii Conclusion: In the study, BMI and BMI SDS enhancing effects of GnRH agonist treatment were not observed in the girls with CPB. With the treatment, the progression of BA was prevented and increase in estimated adult height was achieved.
ix TABLOLAR LİSTESİ
Tablo 1. GnRH Salınımını Düzenleyen Nörotransmitter ve Nörohormonlar ... 4
Tablo 2. Erken Puberte Etiyolojisi ... 14
Tablo 3. GnRH Agonist Preparatlarının Özellikleri ... 20
Tablo 4. Sık Kullanılan GnRH Agonist Preparatları ... 21
Tablo 5. Grupların Demografik Verileri ... 28
Tablo 6. Tanıda Antropometrik Bulgular ve Kemik Yaşı ... 29
Tablo 7. Yaş Gruplarının Tedavi Başlangıç Hedef boy ve PAH verileri ... 30
Tablo 8. Tedavi Sonu Yaş Gruplarının PAH verileri ... 30
Tablo 9. Tanıda Laboratuvar Verileri ... 31
Tablo 10. Tanıda USG verileri ... 31
Tablo 11. İzlem Yıllarında Olgu Sayıları... 32
Tablo 12. Birinci Yıl İzlem Verileri... 33
Tablo 13. İkinci Yıl İzlem Verileri ... 34
Tablo 14. Tedavisi Tamamlanan Hastaların Tanı ve Tedavi Sonu Verilerinin Karşılaştırması ... 35
Tablo 15. Grupların Tanı ve Tedavi Sonu VKİ SDS Verilerinin Karşılaştırması ... 35
Tablo 16. Final Verileri ... 37
Tablo 17. Final Verilerine Ulaşılan Hastaların Hedef ve Final Boyları ... 38
Tablo 18. Normal Kilolu Grubun İzlem Yılları ve Final Verilerinin Karşılaştırması ... 39
Tablo 19. Fazla Kilolu ve Obez Grubun İzlem Yılları ve Final Verilerinin Karşılaştırması ... 41
x ŞEKİLLER LİSTESİ
Şekil 1. Hipotalamus-Hipofiz-Gonad Aksı ... 3
Şekil 2. Tanner Evrelemesi – Meme gelişimi ... 7
Şekil 3. Tanner Evrelemesi – Pubik kıllanma ... 8
Şekil 4. Kızlarda Pubertenin Maturasyonu ... 9
Şekil 5. Prader Orşidometresi ... 9
Şekil 6. Tanner Evrelemesi – Testis gelişimi... 10
Şekil 7. Tanner Evrelemesi – Pubik kıllanma ... 11
Şekil 8. Erkeklerde Pubertenin Maturasyonu ... 12
Şekil 9. Erken Meme Gelişimi ile Başvuran Kızlarda Klinik ve Laboratuvar Değerlendirme ... 19
Şekil 10. Hastaların VKİ’ye Göre Dağılımı ... 27
Şekil 11. Tedavi öncesi ve tedavi sonrası hasta gruplarının değişimi ... 36
Şekil 12. Normal Kilolu Grubun İzlem Yılları VA SDS, Boy SDS ve VKİ SDS Değişimi ... 40
Şekil 13. Fazla Kilolu ve Obez Grubun İzlem Yılları VA SDS, Boy SDS ve VKİ SDS Değişimi ... 41
Şekil 14. Fazla Kilolu ve Obez Grubun PAH Değişimi ... 42
Şekil 15. Tüm Grubun İzlem Yılları VA SDS, Boy SDS ve VKİ SDS Değişimi ... 43
xi KISALTMALAR LİSTESİ
ACTH : Adrenokortikotropik Hormon BMD : Kemik Mineral Yoğunluğu CAMP : Siklik Adenozin Monofosfat CRH : Kortikotropin Salgılatıcı Hormon
ÇEDD : Çocuk Endokrinoloji ve Diyabet Derneği DHEA : Dehidroepiandrosteron
DHEAS : Dihidroepiandrostenodionsulfat
DLK1 : Delta Benzeri 1 Homolog (Protein Delta Homolog 1) E2 : Östradiol
ECLİA : Elektroemilüminesans İmmunolojik Yöntem EP : Erken Puberte
FSH : Folikül Stimulan Hormon
GnRH : Gonadotropin Salgılatıcı Hormon GPR54 : G-protein coupled receptor 54 GABA : Gama Aminobütirik Asit
GNAS1 : Guanine Nükleotid Bağlayıcı Protein hCG : İnsan Koryonik Gonadotropin
HHG Aksı : Hipotalamus – Hipofiz – Gonad Aksı ICMA : İmmunochemiluminometric Assay KISS1R : Kisspeptin 1 Reseptör
KAH : Konjenital Adrenal Hiperplazi
KY : Kemik Yaşı
LH : Luteinizan Hormon
LHRH : Luteinizan Hormon Salgılatıcı Hormon
xii MRG : Manyetik Rezonans Görüntüleme
PAH : Tahmini Erişkin Boy PEP : Periferik Erken Puberte SDS : Standart Deviasyon Skoru SEP : Santral Erken Puberte SSS : Santral Sinir Sistemi
SHBG : Seks Hormon Bağlayıcı Globülin
TY : Takvim Yaşı
USG : Ultrasonografi
VİP : Vazoaktif İntestinal Peptid VKİ : Vücut Kitle İndeksi
1 1 . GİRİŞ
Puberte, cinsel olgunlaşmanın kazanıldığı gelişim sürecidir (1). Puberte başlangıcının kızlarda 8, erkeklerde ise 9 yaşından önce olması erken puberte olarak değerlendirilir. Erken puberte (EP), gerçek veya santral erken puberte (SEP) ve periferik veya yalancı erken puberte (PEP) olmak üzere ikiye ayrılır (2).
Santral EP’de hipotalamus-hipofiz-gonad aksının aktivasyonu görülür. Artan cinsiyet steroidlerinin etkisi ile kemik yaşında hızlı ilerleme görülür ve erken yaşta epifizler kapanır. Böylece final boy kısa olur (3). Kızlarda SEP, erkeklerden yaklaşık 5 kat daha sıktır ve çoğu idiyopatiktir. Ancak altta yatan organik nedenler (astrositomlar, gliomlar ve germ hücre tümörleri dahil tümörler veya hamartomlar dahil olmak üzere diğer hipotalamik lezyonlar veya kranial manyetik rezonans görüntülemede (MRI) tanımlanabilen araknoid kistler dahil konjenital anormallikler) dışlanmalıdır (2).
Santral erken pubertenin tedavisinde gonadotropin salgılatıcı hormon (GnRH) agonistleri kullanılır. Tedavide amaç, pulsatil gonadotropin salınımının baskılanması, hızlanmış cinsel maturasyonun normal pubertal yaşa dek kontrol altında tutulması, erken epifiz kapanmasının ve final yetişkin boy kaybının önlenmesi, erken menarş ve olgunlaşma ile gelişebilecek psikososyal sorunlardan korunması ve kızların erken yaşlardan itibaren süren yüksek östrojenin oluşturabileceği geç komplikasyonlardan korunmasıdır (2).
GnRH agonistleri hipofizde gonadotropin salgılayan hücreleri sürekli olarak uyarır, bu da reseptörlerde duyarsızlaşmaya böylece folikül stimulan hormon (FSH) ve luteinizan hormon (LH) salınımında azalmaya neden olur. Çeşitli depo formları bulunan GnRH agonistlerinin en çok kullanılanları triptorelin ve leuprolid asetattır. Subkutan, intramusküler, nazal sprey, cilt altı implant şeklinde uygulanabilirler (4).
GnRH agonist tedavisinin vücut kitle indeksini (VKİ) etkileyebileceği ve erken puberte tanılı kızlarda obeziteye yol açabileceğine dair endişeler vardır. Bu alanda yapılan çalışmalarda elde edilen sonuçlar farklılık göstermektedir.
Çalışmamızda SEP tanısı ile GnRH agonist kullanan kızlarda tedavinin VKİ SDS değişimi üzerine etkisini ve bu hastaların final boylarını değerlendirmeyi amaçladık.
2 2 . GENEL BİLGİLER
2.1 Pubertenin Tanımı
Puberte, cinsel olgunlaşmanın kazanıldığı gelişim sürecidir. Hipotalamo-hipofizer sistemin olgunlaşması ile başlayan bu süreç kızlarda 8 yaştan sonra meme gelişimi, pubik ve aksiller bölgede kıllanmanın başlaması, hızlı boy uzaması ve menarş olarak ilerlerken erkeklerde 9 yaştan sonra testis hacminin artması, penis boyunun uzaması, pubik ve aksiller bölgede kıllanmanın başlaması ve hızlı boy uzaması olarak ilerler (1).
2.2 GnRH Nöronal Sistemin Gelişmesi
Gonadotropin salgılatıcı hormon (GnRH) salgılayan nöronlar nazal bölgede primitif olfaktör plaktan köken alır ve daha sonra hipotalamusa göç ederler. Gestasyonel 11. haftadan itibaren GnRH ve buna paralel olarak luteinizan hormon (LH) ve folikül stimülan hormon (FSH) salgılanmaya başlar. 25.-29. gestasyonel haftalarına kadar FSH ve LH düzeyleri giderek artar. Gebeliğin sonlarına doğru negatif geri besleme mekanizmasının gelişmesiyle GnRH seviyesi düşer (5).
Plasental ayrılma ile gonadotropin baskısı sona erer, hipotalamus-hipofiz-gonad aksı aktive olur, bu dönem mini puberte olarak adlandırılır. Aks aktivasyonu yaklaşık postnatal 6-8 haftada pik yapar, cinsiyet steroidlerinin düzeyi bu dönemde erken-orta pubertal düzeylere benzerdir, ancak periferik etkileri oluşmamaktadır. Erken çocukluk döneminde aks baskılanır ve pubertal döneme kadar pulsatil GnRH salınımı olmaz (6).
2.3 Hipotalamus-Hipofiz-Gonad Aksı
2.3.1 Gonadotropin Salgılatıcı Hormon (GnRH)
GnRH, 8. kromozomda kodlanan dekapeptid yapıda bir hormondur. Yarılanma ömrü 2-4 dakikadır. Luteinizan hormon salgılatıcı hormon (LHRH) olarak da adlandırılan GnRH’yı salgılayan nöronlar embriyonik dönemde olfaktör plaktan köken alarak medial bazal hipotalamusa göç ederler.
Hipotalamo-hipofizer portal sisteme pulsatil olarak salgılanan GnRH, hipofizden FSH ve LH salınımını uyarır. GnRH’ya yanıt olarak artan serum LH düzeyleri puberte başlangıcının göstergesidir (7,8). Pubertenin başlaması, devam edebilmesi, cinsel
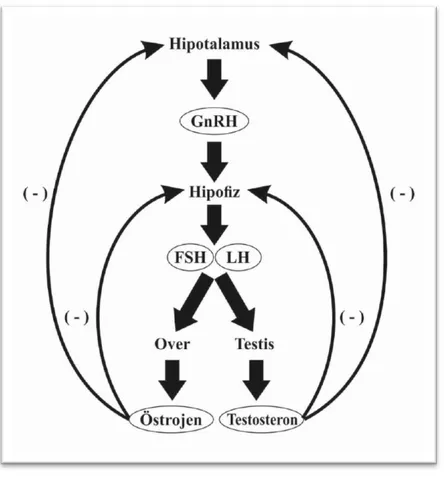
3 olgunlaşmanın sağlanması ve fertilitenin kazanılması hipotalamus-hipofiz-gonad aksının sağlıklı çalışmasına bağlıdır (Şekil 1).
Şekil 1. Hipotalamus-Hipofiz-Gonad Aksı
GnRH= Gonadotropin Salgılatıcı Hormon, FSH= Folikül Stimulan Hormon, LH= Luteinizan Hormon
GnRH salınımının kontrolü karmaşıktır. Baskılayıcı sinyaller temel olarak gama aminobütirik asit (GABA) ve opioidler ile oluşturulurken, uyarıcı sinyaller ise kisspeptin ve glutamat tarafından oluşturulur (Tablo 1) (8). Kisspeptin ve reseptörlerinin olmaması ya da GnRH salınımını inhibe eden maddelerin herhangi bir nedenle artışı puberte gecikmesine neden olurken kisspeptin reseptörlerinin aktive edici mutasyonları ve aktivatör maddelerin artışı erken puberteye yol açabilmektedir (9).
4 Tablo 1. GnRH Salınımını Düzenleyen Nörotransmitter ve Nörohormonlar
UYARANLAR BASKILAYANLAR Glutamat N-metil D-aspartat Noradrenalin Adrenalin Prostaglandin E2 Büyüme faktörleri Kisspeptin GABA Opioidler Dopamin Serotonin Beta-endorfin Melatonin VİP CRH Nöropeptid Y
CRH= Kortikotropin Salgılatıcı Hormon, GABA= Gama Aminobütirik Asit, VİP= Vazoaktif İntestinal Peptid
2.3.2 Hipofizer Gonadotropinler
Ön hipofizden salgılanan folikül uyarıcı hormon (FSH) ile lüteinizan hormon (LH), over ve testis fonksiyonlarını düzenleyen, normal büyüme, cinsel gelişim ve üreme için gerekli olan glikoprotein yapılı hormonlardır. İki peptit zincirinden oluşan heterodimerik proteinlerdir. Alfa zinciri ikisinde de aynıyken beta zinciri hormona spesifiktir, hormonların reseptör özgüllüğünü ve fonksiyonunu belirler (10).
Prepubertal dönemde GnRH salgılanması baskı altındadır, kanda LH ölçülemeyecek kadar düşüktür. Bu dönemde özellikle kızlarda FSH, LH’ya göre daha yüksektir. Hipotalamo-hipofizer aksın aktivasyonu ile GnRH artar ve özellikle geceleri uykuda LH salınımı başlar. Puberte ilerledikçe gece salınım azalır, tüm gün pulsatil salınım şekli kazanır. LH/FSH oranının 1’in altında olması prepubertal, 1’in üzerinde olması ise pubertal olarak değerlendirilir (11). Pubertal dönemin değerlendirmesinde kullanılan bir diğer yöntem GnRH uyarı testinde LH cevabı 30. ve 60. dakikada değerlendirilir. Uyarılmış LH düzeyinin 5 mIU/mL üzerinde olması pubertaldir (11).
Kadınlarda FSH, overlerde granüloza hücrelerini etkileyerek östrojen salgılanmasını ve foliküllerin gelişimini, puberte döneminde uterusun büyüme ve gelişmesini sağlar. LH, ovulasyonu tetikler ve korpus luteum tarafından progesteron salgılanmasını uyarır. Erkeklerde FSH, testislerdeki sertoli hücrelerini etkileyerek spermatogenezi sağlar. FSH aynı zamanda sertoli hücrelerinden inhibin salgılanamasına yol açar. İnhibin ve testosteron negatif geri bildirim ile hem hipotalamus hem hipofizi etkilerek gonadotropin salgılanmasını azaltır.
5 Testosteron ile FSH, normal sperm sayısını ve fonksiyonunu korumak için gereklidir. LH, leydig hücrelerini etkileyerek testosteron salgılatır (12,13).
2.3.3 Cinsiyet Steroidleri
Kadınlarda overlerden salgılanan iki cinsiyet hormonu, östrojenler ve progestinlerdir. Östrojenlerin en önemlisi östradiol (E2) ve progestinlerin en önemlisi progesterondur. Bu hormonlar kolesterolden sentezlenir, kanda taşıyıcı globülinler (SHBG) aracığı ile hedef dokulara taşınır ve karaciğerde metabolize edilirler.
Östrojenler, kadın genital organlarının çocuk görüntüsünden erişkine dönüştürür. Overlerin, fallop tüplerinin, uterus ve vajinanın boyutlarını arttırır. Endometriyal stroma ve bezlerde çoğalmaya, fallop tüplerinde epitel hücrelerin sayısında artışa neden olurlar. Memede stromal doku ve kanal sistemlerinin gelişmesini, memede yağ birikmesini sağlarlar. Kemikte osteoblastik aktivitenin artmasına neden olur böylece kızlarda pubertenin başlaması ile boyda hızlı uzamayı sağlar. Uzun kemiklerin gövdesi ile epifizlerin birleşmesini sağlar. Deri altı dokusunda, kalçalarda ve üst bacaklarda yağ birikimine böylece kadınsı görünümün oluşmasına yol açarlar. Progesteron ise menstruel döngünün ikinci yarısında artarak uterusu ovumun implantasyonuna hazırlar, memede lobül ve alveol gelişimini uyarır.
Erkeklerde testislerden testosteron, androstenedion gibi androjenler salgılanır. Testosteron hedef dokularda dihidrotestosterona dönüşür. Testosteron da östrojen gibi SHBG ile taşınır ve karaciğerde metabolize edilir. İntrauterin dönemde önce genital plaktan ardından testislerden salgılanan testosteron erkek cinsiyet özelliklerinin gelişimini sağlar. Fetal dönemde yüksek östrojen ile gonadotropinler baskılanmaktadır. Doğumdan sonra plasental östrojen devreden çıkınca hipotalamus-hipofiz-gonad aksı aktive olur ve pubertal düzeylere ulaşan hormon profili oluşur. Bu değişime mini puberte adı verilir. Mini puberte ile ileri dönem testis işlevleri, sperm yapımı düzenlenir ve bu dönem beynin maskülinizasyonuna katkıda bulunur (6). Doğumdan sonra giderek kandaki testosteron miktarı azalır ve çocukluk döneminde testosteron az miktarda üretilir. Puberte ile salgılanması kemik büyümesi ve kalsiyum depolanmasını arttırır, protein sentezini ve kas gelişimini arttırır, deri kalınlaşmasını ve deri altı dokusunun güçlenmesini sağlar. (14)
6 2.4 Adrenarş
Hipofizer-gonadal akstan bağımsız olarak adrenal androjenlerin artışına adrenarş denir. Adrenokortikotropik hormon (ACTH) uyarısıyla adrenal korteksin zona retikularisi tarafından artan miktarlarda androjen (DHEA, DHEAS ve androstenedion) üretimi ile karakterizedir. Hipotalamo-hipofizer aksın etkinleşmesinden yaklaşık 2 yıl önce gerçekleşir. Kızlarda ortalama 6-7, erkeklerde ise ortalama 7-8 yaşlarında serumda en önemli adrenokortikal androjen olan dihidroepiandrostenodionsülfat (DHEAS) saptanabilmektedir. Adrenarş ile DHEAS düzeyi 40 mcg/dl’nin üzerine çıkar. Bu artış her iki cinste pubertede izlenen aksiller ve pubik kıllanmadan sorumludur (15).
2.5 Normal Pubertal Gelişim
Puberte, hipotalamo-hipofizer aksın aktivasyonu ve pulsatil GnRH salgılanması ile başlar. Aksın aktivasyonu ikincil cinsiyet özelliklerinin ortaya çıkması, büyüme hızında, kemik mineral kütlesinde ve vücut kitle indeksinde (VKİ) artış olarak kliniğe yansır (2).
2.5.1 Kızlarda Pubertal Gelişim
Kızlarda ikincil cinsiyet karakterlerinin ortaya çıkışı pubertenin ilk belirtisi olan meme dokusu gelişimi (telarş) ile başlayıp pubik kıllanma (pubarş) ve aksiller kıllanma (aksillarş) ve menarş sırasıyla devam etmektedir. Ancak %15’inde ilk bulgu pubik kıllanma (pubarş) olabilir. Meme gelişimi ortalama 10 yaş (8-13 yaş) civarında başlar. Birçok vücut yapısı ve sisteminde meydana gelen boyut, şekil, kompozisyon ve işlev gelişimini içeren bu süreç genellikle 3-4 yılda tamamlanır (8).
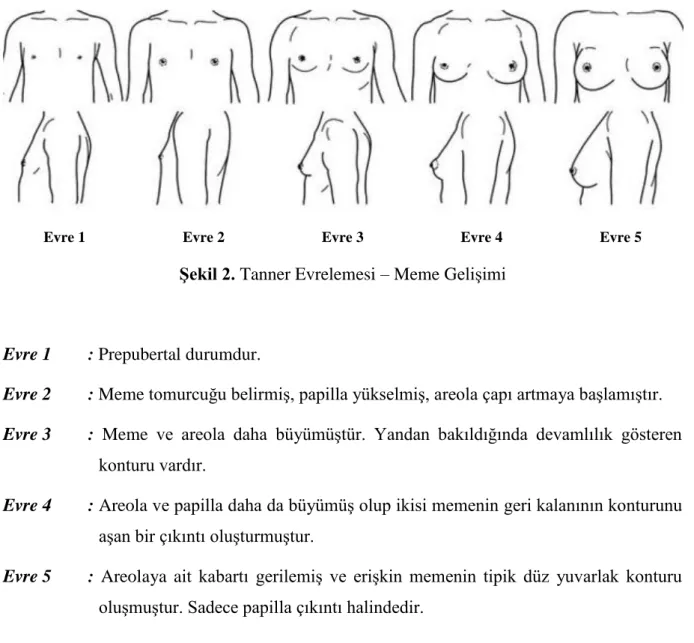
Meme gelişimi bazen tek taraflı başlayabilir ve genellikle 6 ay içinde diğer meme gelişimi eklenir. Meme gelişiminin klinik takibinde Tanner tarafından oluşturulan evreleme kullanılmaktadır (Şekil 2) (16).
7
Evre 1 Evre 2 Evre 3 Evre 4 Evre 5
Şekil 2. Tanner Evrelemesi – Meme Gelişimi
Evre 1 : Prepubertal durumdur.
Evre 2 : Meme tomurcuğu belirmiş, papilla yükselmiş, areola çapı artmaya başlamıştır.
Evre 3 : Meme ve areola daha büyümüştür. Yandan bakıldığında devamlılık gösteren
konturu vardır.
Evre 4 : Areola ve papilla daha da büyümüş olup ikisi memenin geri kalanının konturunu
aşan bir çıkıntı oluşturmuştur.
Evre 5 : Areolaya ait kabartı gerilemiş ve erişkin memenin tipik düz yuvarlak konturu
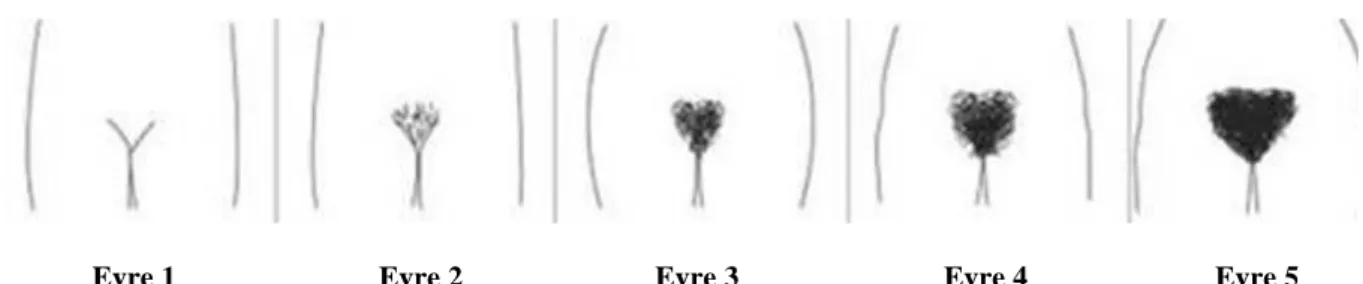
8 Pubik kıllanma da meme gelişimi gibi Tanner tarafından tanımlanan 5 evrede değerlendirilir (Şekil 3).
Şekil 3. Tanner Evrelemesi – Pubik Kıllanma
Evre 1 : Pubik bölgede kıl yoktur.
Evre 2 : Labium majörler üzerinde hafif pigmentli düz kıllar mevcuttur.
Evre 3 : Pigmentli kıllar kıvrıklaşmaya, koyulaşmaya ve mons pubis üzerine yayılmaya başlar.
Evre 4 : Mons pubise kıllar yayılmış ancak üçgeni doldurmamıştır.
Evre 5 : Kıllar pubik üçgeni tamamen doldurmuştur, kasıklara doğru yayılım gösterir (16).
Menarş (ilk menstruel kanamanın başlaması) meme gelişiminden 2 yıl sonra, kızların büyük çoğunluğunda meme gelişiminin 4. evresinde gözlenir. Menarşın 10 yaşından önce olması erken, 16 yaşından sonra olması geç olarak değerlendirilir. İlk iki yıl menstruel döngülerin büyük çoğunluğu anovulatuardır.
Pubertede cinsiyet steroidlerinin ve uyarılan büyüme hormonunun etkisi ile büyüme hızlanır. Bu dönemdeki büyüme atağına zirve büyüme hızı denir. Kızlarda zirve büyüme hızı meme gelişiminin 2.-3. evresinde, menarştan 1-1.5 yıl önce görülür (Şekil 4). Puberte süresince kızlar toplam ortalama 20-25 cm uzarken menarş sonrası uzama 5-8 cm ile sınırlıdır (15).
9 Şekil 4. Kızlarda Pubertenin Maturasyonu (17)
2.5.2 Erkeklerde Pubertal Gelişim
Erkeklerde ikincil cinsiyet özellikleri, testis hacminin artması ile ortaya çıkar. Testis hacminin 3 ml’nin üzerine çıkması pubertenin ilk bulgusudur. Bu artış 9-14 yaş aralığında, ortalama 12 yaşta görülür. Testis hacminin artışıyla beraber dış genital yapı değişiklikleri görülmeye başlar. Testis hacmini artışından sonra penis gergin boyunda artış, pubik ve aksiller kıllanma ardından spermarş izlenir. Bu süreç ortalama 3.5 yıl sürmektedir (15,16,18).
Testis hacminin ölçümü Prader orşidometresi ile yapılır (Şekil 5).
10 Dış genital yapının değişimi ve pubik kıllanmanın izleminde Tanner evrelemesi kullanılır (Şekil 6-7).
Şekil 6. Tanner evrelemesi – Testis Gelişimi
Evre 1 : Testis hacmi <3 ml’dir (puberte öncesi dönem)
Evre 2 : Testis hacmi artmaya başlar, skrotum derisinde koyulaşma vardır.
Evre 3 : Testis hacim artışına penis büyümesi eklenir. Penisin hem boyunda hem de eninde artış vardır.
Evre 4 : Penis ve glans iyice büyür, glans belirginleşir. Testisler daha büyük, skrotal deri koyu renklidir.
11 Şekil 7. Tanner Evrelemesi – Pubik Kıllanma
Evre 1 : Pubik kıl yoktur. Pubis üzerinde birkaç ince tüy olabilir. (puberte öncesi dönem) Evre 2 : Penis kökünde tek tük koyu renkli kıllar belirmeye başlar.
Evre 3 : Kıllar sıklaşır, koyulaşır ve pubis üzerine yayılmaya başlar. Evre 4 : Kıllar sık, koyu renkli, kıvrık ve yaygınlaşmıştır.
Evre 5 : Kıllar erişkin şeklindedir ve tüm pubik bölgeyi kaplar.
Erkeklerde pubertede görülen bir diğer değişiklik ses kalınlaşmasıdır. Ses tellerinin uzaması, krikoid kıkırdak ve larinks kaslarının büyümesi kalınlaşmaya yol açar. Bu dönem pubertenin 3-4. evrelerine denk gelir. Yüz kılları 15 yaştan itibaren üst dudak ve zigomatik çıkıntıdan başlayarak çıkar. Çenede sakal genellikle dış genital yapının gelişimi tamamlandıktan sonra belirir. Spermarş, sperm yapımının başlaması genellikle 13 yaşında gerçekleşir.
Erkeklerde büyüme atağı, pubertenin 3.-4. evresinde, aksiller kıllanmanın başladığı ve ses kalınlaşmasının olduğu dönemde görülür (Şekil 8). Erkeklerde büyüme atağı kızlardan yaklaşık 2 yıl daha geç olur, 25-28 cm boy uzaması gerçekleşir (15,16).
12 Şekil 8. Erkeklerde Pubertenin Maturasyonu (17)
2.6 Pubertenin Başlangıç Yaşını Etkileyen Faktörler
Puberte başlangıç yaşı ırk, etnik özellikler, yaşam koşulları gibi çeşitli faktörlerin etkisi altındadır. Kızlarda pubertenin normal başlama yaşı 8-13 yaş arası, erkeklerde 9-14 yaş arasındadır. Genetik, pubertenin başlama yaşını etkileyen en önemli faktördür. Tek yumurta ikizlerinde, anne-kız ikilisinde pubertenin başlama yaşının benzer olması, siyahlarda beyazlara göre ergenliğin daha erken başlaması genetiğin önemini göstermektedir.
Bir diğer faktör ise kisspeptin ve onun reseptörü G-protein coupled receptor 54 (GPR54)’tür. Hipotalamusta kisspeptin ekpresyonunun artması GPR54 aktivasyonu ile sonuçlanır. KISS-1/GPR54 sisteminin hipotalamus–hipofiz–gonad (HHG) aksını kontrol etmede önemli rolü olduğu, kisspeptinin pulsatil gonadotropin sekresyonu için gerekli faktörlerden biri olduğu bilinmektedir. GPR54’te inhibe edici bir mutasyon otozomal resesif idiopatik hipogonadotropik hipogonadizme neden olurken, aktive edici mutasyon ise santral erken pubertenin bir formuyla ilişkilidir (2). KAL gen mutasyonunun görüldüğü Kallmann Sendromu ise hipogonatropik hipogonadizmin bir diğer genetik nedenidir.
Leptin, enerji depolarının puberteyi sürdürmek, tamamlamak ve hatta muhtemelen başlatmak için yeterli olduğunu bildirmek için metabolik bir barometre görevi gören adiposit
13
türevli hormondur. Kızlarda daha yüksek serum leptin yoğunluğu vücut yağı artışı ve pubertenin daha erken başlamasıyla ilişkilidir. Serumda leptinin 1ng/ml artışı menarşı bir ay, yağ dokusunun 1 kg artışı menarşı 13 gün kadar erkene kaydırmaktadır (1,17). Hastalıklar, araya giren fiziksel ve psikososyal durumlar da pubertenin başlamasını etkileyebilir. Kronik hastalıklar, yetersiz beslenme, anoreksiya nervoza veya yorucu egzersiz nedeniyle pubertenin başlangıcı ileri yaşa kayar. Yaşam koşullarının iyileşmesi ile ergenlik başlama yaşı erkene kaymaktadır (2).
Endokrin sistemin işlevini değiştirerek, hormonal dengeyi bozan, sağlıklı bir organizmada istenmeyen etkilere yol açan doğal ya da yapay maddelere endokrin bozucu kimyasallar denir. Poliklorlu bifeniller, organoklorin pestisitler ve ftalatlar dahil olmak üzere çeşitli çevresel ajanlar ile bitkilerde bulunan fitoöstrojenler endokrin bozucu kimyasallar olarak tanımlanmıştır. Bu kimyasallar östrojen reseptörlerini bağlayarak ve GnRH gen ekspresyonunu değiştirerek üreme sistemlerini etkileyebilir. Genç kızlarda östrojenik aktiviteye sahip kimyasallar içeren kozmetik veya saç bakım ürünlerine maruziyetin erken puberteye yol açtığını bildiren yayınlar vardır (19).
2.7 Erken Puberte (Puberte Prekoks)
Erken puberte (EP), kızlarda 8 yaşından, erkeklerde 9 yaşından önce pubertenin fiziksel belirtilerinin başlaması olarak tanımlanır. Cinsiyet steroidlerinin veya cinsiyet steroid aktivitesi olan bileşiklerin hedef organlar üzerindeki etkisinden kaynaklanır. Kızlarda meme gelişimi ve erkeklerde testis hacminin artması dahil olmak üzere ikincil cinsiyet özelliklerinin ilerleyen gelişimine yol açar, büyüme hızının ve kemik olgunlaşmasının hızlanmasıyla sonuçlanır. Bu da erişkin boydan kayba neden olur.
EP kızlarda erkeklerden daha sık görülür. Vakaların çoğu idiyopatiktir. Erkeklerde daha az görülmesine rağmen organik nedenli olma ihtimali daha fazladır.
Gonadotropin salgılatıcı hormonun (GnRH) pulsatil salgısının erken başlamasından kaynaklananlar (santral/gerçek erken puberte) ve GnRH'den bağımsız artan cinsiyet steroid üretimi ile ilgili olanlar (periferik/yalancı erken puberte) olarak ayrılır. İdiyopatik erken puberte, santral EP’nin en yaygın nedenidir ve kızlarda erkeklerden daha sık görülür. Santral EP, nadiren santral sinir sistemi (SSS) tümörleri, SSS yaralanmaları ve enfeksiyonlarına sekonder görülebilir. Bu nedenlere bağlı SEP daha çok erkeklerde görülmektedir (2,20).
14 Tablo 2. Erken Puberte Etyolojisi
1) Santral erken puberte (GnRH bağımlı, gerçek erken puberte) İdiopatik santral erken puberte Sporadik Ailesel Santral sinir sistemi tümörleri Astrositom Optik gliom Kraniofarengioma Disgerminom Ependimom Nöroblastom Hipofiz adenomu Santral sinir sisteminin konjenital hastalıkları Hidrosefali Araknoid kist Hipotalamik hamartom Septaoptik displazi Suprasellar kist Santral sinir sisteminin edinsel hastalıkları Menenjit Ensefalit Radyoterapi Travma Apse Sendromlar Williams Sendromu Prader-Willi Sendromu Nörofibramotozis Tip 1 Tuberoskleroz Triple X Sendromu Metabolik
durumlar Nonketotik hiperglisinemi Gonad ve adrenal
cinsiyet
steroidlerine uzun süreli maruziyet
Mc Cune Albright sendromu Konjenital adrenal hiperplaziler
2) Santral ve periferik puberte bir arada (Kombine) Mc Cune Albright sendromu
Tedavideki konjenital adrenal hiperplaziler
3) Periferik Erken Puberte (GnRH bağımsız, yalancı)
Er
ke
kler
için
Konjenital adrenal hiperplaziler (21 hidroksilaz eksikliği ve 11 beta hidroksilaz eksikliği)
Mc Cune Albright sendromu
Familyal erken puberte testotoksikozis (LH reseptör aktivasyon mutasyonu) Tümörler (hCG salgılayan tümörler, adrenokortikal tümörler (feminizan veya
cinsiyet uyumlu), Leydig hücre tümörleri, Teratom Glukokortikoid reseptör mutasyonu
Eksojen androjenler
Eksojen östrojenler (cinsiyet uyumsuz)
Kız
lar
için
Tümörler (over tümörleri, adrenokortikal tümör (maskulinizan veya cinsiyet uyumlu), teratomlar)
Otonom over kisti Eksojen östrojen
Mc Cune Albright sendromu Kronik primer hipotiroidi
Konjenital adrenal hiperplazi (maskulinizan) (21 hidroksilaz eksikliği, 11 beta hidroksilaz eksikliği)
Glukokortikoid reseptör defekti (maskulinizan) 4) Normal varyant puberte
15 2.7.1 Santral (Gerçek) Erken Puberte
Santral erken puberte (SEP)’de pulsatil GnRH sekresyonu normal puberteye benzerdir ancak hipotalamus-hipofiz-gonad aksının erken aktivasyon vardır. SEP'de endokrin ve fiziksel gelişim normal olarak zamanlanmış puberte ile aynı kalıpta ve aynı hızda meydana gelir.
Kızlarda SEP, erkeklerden yaklaşık 5 kat daha sıktır ve çoğu idiyopatiktir. Ancak her iki cinsiyette de altta yatan organik bir nedeni dışlama konusunda dikkatli olmak önemlidir. Puberte bulguları ne kadar erken yaşta ortaya çıkarsa, organik bir nedenden kaynaklanma ihtimali o kadar yüksektir. Astrositomlar, gliomlar ve germ hücre tümörleri dahil tümörler veya hamartomlar dahil olmak üzere diğer hipotalamik lezyonlar veya kranial MRI'da tanımlanabilen araknoid kistler dahil konjenital anormallikler SEP nedeni olabilir. Hipotalamus-hipofiz aksına zarar veren tüm durumlar, hipotalamusa veya hipofize radyoterapi uygulanması, hidrosefali, doğum asfiksisi veya nörodejeneratif hastalıklar SEP için bir risk faktörü oluşturur (21). Santral erken puberte bazı dismorfik sendromlarla birliktelik gösterebilmektedir. Silver-Russel Sendromu, Kabuki Make-Up Sendromu, Williams-Beuren Sendromu bu özelliği gösteren sendromlardır (22).
Kızlarda SEP olguların çoğu olarak idiyopatik olarak kabul edilmiştir. Bu konuda en yeni gelişmelerden biri, sporadik ve ailesel SEP olgularının altında yatan 4 genetik mutasyonun tanımlanmasıdır. Aktive edici mutasyonlar kisspeptin reseptör (KISS1R) geninde ve kisspeptin (KISS1) geninde tanımlanırken, baskılanmış makorin halka parmak proteini 3 (MKRN3) genindeki inaktive edici mutasyonların, bazı serilerde SEP olgularının %40'ının temelini oluşturduğu bildirilmiştir. Diğer bir mutasyon birden fazla kuşakta SEP olan bir ailede keşfedilen baskılanmış delta benzeri 1 homolog (DLK1) genindeki delesyonlardır. Moleküler genetik etiyolojilerinin araştırılması devam ederken, idiyopatik SEP yüzdesi giderek azalacaktır (21).
2.7.2 Periferik (Yalancı) Erken Puberte
Periferik erken puberte (PEP), gonadotropinlerden bağımsız olarak gonadal veya adrenal doku tarafından cinsiyet steroidlerinin üretilmesinden kaynaklanır. Gonadal, adrenal veya hCG üreten tümörler (erkeklerde) ve ekzojen cinsiyet steroidlerine veya steroidal aktiviteye sahip bileşiklere maruz kalmak PEP’nin başlıca nedenlerindendir.
PEP nadiren pulsatil GnRH sekresyonunun aktivasyonuna ve hipotalamus-hipofiz-gonad aksının uzun süre kullanılmasından dolayı SEP'ye yol açabilir. PEP'de pubertal gelişim,
16 normal ergenlik veya SEP'den farklı seyredebilir, örneğin menarş meme gelişiminin erken bir aşamasında meydana gelebilir.
Bu nedenlere ek olarak PEP, McCune-Albright Sendromu, aromataz inhibitörü fazlalığı ve konjenital adrenal hiperplazi (KAH) 'de görülebilir. Klasik KAH yenidoğan döneminde daha sık görülürken, klasik olmayan KAH hızlanmış kemik büyümesi ile erken pubik kıllanma ile bulgu verebilir. McCune Albright Sendromu kadınlarda PEP’nin sık görülen nedenlerindendir. Sıklıkla 2-3 yaşlarında görülür. GNAS1 genindeki mutasyon ile adenilat siklazı (CAMP) aktive olur ve birden fazla endokrinopati görülebilir. EP, LH bağlanması olmadan reseptör aktivasyonu ve cinsiyet steroid üretimi ile oluşur (2).
2.7.3 Erken Pubertede Öykü
Erken puberte olgularında puberte belirtilerinden hangilerinin (pubik kıllanma, akne, yağlı saçlar, vücut kokusu, meme ve genital gelişim) olduğu, hangi sırayla fark edildiği, ilk değişikliklerin ne zaman fark edildiği ve ne kadar hızlı ilerlediği, eşlik eden semptomun olup olmadığı, kullanılan ilaçlar sorgulanmalıdır. Ebeveynlerin hangi yaşlarda ergenlik yaşadıkları öğrenilmelidir (20).
2.7.4 Erken Puberte Kliniği
Erken puberte, ikincil cinsiyet özelliklerin (kızlarda meme gelişimi, pubik kıllanma, menarş ve erkeklerde testis hacminin artması, penis büyümesi, kasık kıllarının gelişimi) kazanımı ile birlikte boy uzamasında artış ve kemik maturasyonunda hızlanma olarak ortaya çıkar. Tek puberte bulgusu uzun süre tek bulgu olarak kalabilir ve teşhisi zorlaştırır. Özelikle kızlarda pubik kıllanma veya boy uzamasından aylar önce meme gelişimi olabilir. Bazı çocuklarda, boy uzamasındaki artış, ikincil cinsiyet özelliklerin ortaya çıkmasından önce meydana gelir (2).
Santral erken puberte homojen bir klinik göstermez. Klinik bulgulardaki ilerleme bazı olgularda yavaş gidiş gösterirken (yavaş ilerleyen tip), bir kısmında ise hızlı ilerleme (hızlı ilerleyen tip) olabilmektedir (22).
Pubertal gelişim aşaması Tanner tarafından tarif edildiği gibi sınıflandırılmalıdır. Obez kızlarda meme gelişimini fazla tahmin etmemek için dikkatli bir değerlendirme gerekmektedir.
17 Pubik kıllanmanın gelişimi, santral erken ergenlikte testis veya overler tarafından üretilen androjenlerin etkilerinden kaynaklanır. Kızlarda, meme gelişimi yokluğunda pubik kıllanmanın olması adrenal bozuklukları, erken pubarşı veya androjenlere maruz kalmayı düşündürür.
Erkeklerde testis hacminin ölçülmesi pubertenin nedenini saptamada önemlidir. Santral ve periferik erken pubertede, normal pubertede olduğu gibi testis hacmi artar. Testis hacmi adrenal bozukluklarda, erken pubarşta ve periferik erken pubertenin bazı nedenlerinde prepubertal kalır.
Fizik muayenede, nörofibromatozis veya McCune-Albright Sendromunu düşündüren hiperpigmente cilt lezyonları gibi erken pubertenin spesifik nedenlerinin belirtileri değerlendirilir.
Erken puberte ile büyüme hızı, yaş için normal değerlere göre hızlanır ve çoğu durumda kemik yaşı ilerler. Kemik olgunlaşmasının hızlanması, büyüme plağının erken füzyonuna ve kısa boya yol açabilir. EP'ye bağlı boy kaybının derecesi pubertenin başlangıç yaşı ile ters orantılıdır (3).
Yaşıtlarından hızlı somatik ve cinsel gelişim, ayrıca kızlarda vaginal kanamalar, birçok psikososyal problemi de beraberinde getirmektedir. Bu çocuklar cinsel tacize açık bir duruma gelmektedirler (22).
2.7.5 Erken Puberte Tanı
Erken pubertede tanı klinik ve biyokimyasal verilere dayandırılmalı, idiyopatik ve organik ayırımı santral görüntüleme ile yapılmalıdır.
Kemik yaşını değerlendirmek için sol el bilek grafisi çekilir ve Greulich-Pyle atlası ile değerlendirilir. Cinsiyet steroidlerinin etkisi ile kemik maturasyonu hızlanır ve EP’de kemik yaşının takvim yaşına göre ileri olması beklenir. Kemik yaşı, tahmini erişkin boyun hesaplanmasında ve hedef boya ulaşılıp ulaşılmayacağını değerlendirmek amacıyla kullanılır (23). Yaşıtlarından daha uzun olan bu çocukların final yetişkin boyları epifizler erken kapandığından genetik potansiyellerinin altında kalır.
Cinsiyet steroidleri (östrojen, testesteron) ve gonadotropin düzeylerine bakılmalıdır. Erkeklerde sabah testesteron düzeyleri genellikle 20 ng/dl ve üzerindedir. Kızlarda ise östradiol düzeyleri normal pubertal kızlardaki gibi dalgalanmalar göstermekle beraber 12 pg/mL’nin üstüne çıkan değerler pubertaldir. Bazal LH düzeyi İmmunochemiluminometric
18 Assay (ICMA) ile ≥0.3mIU/ml ise pubertal kabul edilir. Ancak bazal gonadotropin değerleri normal bulunabilir. Bu nedenle gerekli olgularda kesin tanı için LHRH uyarısına LH ve FSH yanıtları belirlenmeli ve uyarılmış gonadotropin düzeyleri ölçülmelidir. Gonadotropin uyarı testinde kısa etkili bir GnRH agonisti olan gonadorelin 2.5 mcg/kg (maksimum 100 mcg) dozunda sabah damardan uygulanıp 60-120 dakika süre ile her 30 dakikada bir kan örnekleri alınır (24). LHRH uyarısına LH predominant yanıt (LH/FSH oranı >0.3) SEP için tanı koydurucudur. Kızlarda uyarılmış LH ICMA ile ≥5 mIU/ml ise pubertal kabul edilir. Erkeklerde uyarılmış LH değerleri ICMA ile >8 mIU/ml ise pubertaldir.(22) Periferik EP’de serum gonadotropin düzeyleri düşük, cinsiyet steroid düzeyleri artmış olarak bulunur. Serum östradiol düzeyi 100 pg/mL’nin üzerinde saptandığında over kisti veya tümörü öncelikli olarak akla gelmelidir. Ayrıca PEP etyolojisini saptanmak için serum hCG düzeyi, 17 hidroksi progesteron, 11 deoksikortizol ve DHEAS düzeyi ölçülmelidir (23).
Erken puberteli kızlarda over ve uterus boyutlarını belirlemek, overlerin folliküler yapısını değerlendirmek, over kist ve tümörlerini ortaya koyabilmek için pelvik ultrasonografi (USG) yararlı bilgiler veren noninvazif bir yöntemdir. Prepubertal kızlarda uterus uzun aksı 35 mm’den kısa olmalı; overlerin uzun çapı 20 mm’yi geçmemelidir. Uterus uzun aksının artması (≥ 35 mm), uterus şeklinin armut benzeri bir görünüm alması ve bilateral overlerin hacminin 2 ml’nin üzerinde olması SEP bulgusudur. Erkeklerde PEP düşünüldüğünde veya asimetrik testis palpe edildiğinde testis tümörleri açısından skrotal USG çekilmelidir.
Santral EP’de hipofizin görüntülenmesi için en uygun yöntem manyetik rezonans görüntüleme (MRI)’ dir. Erkek çocuklarda SEP görülmesi durumunda santral sinir sisteminde (SSS) lezyon olma ihtimali yüksektir, bu nedenle santral görüntüleme yapılmalıdır. Kız çocuklarında SSS’den kaynaklanan patolojiler az görülmekte, özellikle 6 yaş üzerinde sıklık daha da azdır. Bu nedenle 6 yaş üzerinde rutin görüntüleme yapılması tartışmalıdır. Ancak öykü ve fizik muayenede SSS patolojisinin düşündüren bulgu varlığında mutlaka kranial görüntüleme yapılmalıdır (23).
19 Şekil 9. Erken meme gelişimi ile başvuran kızlarda klinik ve laboratuar değerlendirme
GnRH= Gonadotropin Salgılatıcı Hormon, FSH= Folikül Stimulan Hormon, LH= Luteinizan Hormon, KY= kemik yaşı, TY= takvim yaşı, USG= ultrasonografi, LHRH= Luteinizan Hormon Salgılatıcı Hormon, SSS= santral sinir sistemi, tm= tümör, SPP= santral erken puberte
2.7.6 Erken Pubertede Tedavi
SEP’de tedavinin amacı, pulsatil gonadotropin salınımının baskılanması, hızlanmış cinsel maturasyonun normal pubertal yaşa dek kontrol altında tutulması, erken epifiz kapanmasının ve final yetişkin boy kaybının önlenmesi, erken menarş ve olgunlaşma ile gelişebilecek psikososyal sorunlardan korunması ve kızların erken yaşlardan itibaren süren yüksek östrojenin oluşturabileceği geç komplikasyonlardan korunmasıdır.
Tedavi endikasyonunu belirlerken pubertenin başlama yaşı, pubertal evre, bulguların ilerleme hızı, hesaplanan erişkin boyda kayıp, hızlı somatik gelişim dikkate alınmalıdır. Kızlarda bulgular 7 yaşından önce başlamışsa tedavi endikasyonu kesindir, 7-8 yaş arasında ise tartışmalıdır. Erkene kaymış pubertede bulguların ilerleme hızı ve somatik gelişim yakından denetlenmelidir. Yıllık kemik yaşı artışının, takvim yaşı artımına oranı (ΔKY/ΔTY) 1.2’nin üstüne çıkması, iki pubertal evre arasının 3-6 ay kadar kısa olması hızlı progresyona
20 işaret eder. Yavaş ilerleyen idiyopatik SEP’de tedavi önerilmemektedir. Erkeklerde pubertal bulgular 9 yaş öncesinde başlamışsa tedavi edilmelidir (2).
Endikasyonu olan olgularda tedavide GnRH agonistleri kullanılmaktadır. GnRH agonistleri hipofizde gonadotropin salgılayan hücreleri sürekli olarak uyarır, bu da reseptörlerde duyarsızlaşmaya ve LH salımında ve daha az ölçüde FSH salımında azalmaya neden olur. Çeşitli depo formlarında çeşitli GnRH agonistleri mevcuttur (Tablo 3). Triptorelin ve leuprolid tedavide kullanılan başlıca GnRH agonistleridir (Tablo 4). Önerilen doz leuprolid asetat için 150-300 mcg/kg/ay, triptorelin için ise 100-150 mcg/kg/aydır. Subkutan, intramusküler, nazal sprey, cilt altı implant şeklinde uygulanabilirler. Uzun etkili depo formları, subkutan uygulamaya göre daha etkindir ve hasta uyumu nedeni ile daha çok tercih edilmektedir.
Tablo 3. GnRH Agonist Preparatlarının Özellikleri HIZLI
ETKİLİ AYLIK DEPO
3 AYLIK DEPO
12 AYLIK İMPLANT Doz aralığı Günlük 28 günde bir 90 günde bir Yıllık
Pik serum konsantrasyonuna
ulaşma süresi
10-45 dakika 4 saat 4-8 saat 1 ay
Supresif etkinin
başlama süresi 2-4 hafta 1 ay 1 ay 1 ay
Avantajı Hızlı başlama / kesme
Doz ve etkisi en iyi bilinen form
Daha az enjeksiyon ve daha iyi uyum
Enjeksiyon gerektirmemesi
Dezavantajı
Çok sayıda doz gereksinimi ve uyum zorluğu Ağrılı enjeksiyonlar Ağrılı enjeksiyonlar Cerrahi işlem gereksinimi
21 Tablo 4. Sık Kullanılan GnRH Agonist Preparatları
GnRH agonist
preparatları DOZ
Leuprolid asetat
1 aylık depo form
3.75 mg 7.5 mg 11.25 mg
15 mg
3 aylık depo form 11.25 mg
30 mg
Triptorelin pamoat
1 aylık depo form 3.75 mg
11.25 mg
6 aylık depo form 22.5 mg
Histrelin asetat 12 aylık implant 50 mg (65 mcg/gün)
Tedavinin etkinliğini klinik bulgularda gerileme, yıllık kemik yaşı artışının takvim yaşı artışına oranının <1.2 olması, LH düzeyinde baskılanma gösterir. Klinik değerlendirme, fiziksel değişikliklerin stabilitesini değerlendirmek için her 3-6 ayda bir yapılmalıdır. Pubik kıllanma stabilize olabilir veya gerileyebilir, ancak adrenarş oluşmuş olabileceğinden hipotalamus-hipofiz-gonad aks supresyonunun doğru bir göstergesi değildir(4). Klinik pubertal ilerleme, büyüme yavaşlamasının sağlanamaması, aşırı kemik yaşı ilerlemesinin devam etmesi ve LH yüksekliği tedavi başarısızlığı göstergeleridir. Bu göstergeler varlığında tedaviye uyum, zamanlama ve doz kontrol edilmeli, ayrıca GnRH bağımsız erken puberte (PEP) nedenleri gözden geçirilmelidir. SEP tedavisinde etkin olunamıyorsa önce 21 günde bir uygulamaya geçilip yine başarılı olunamazsa doz arttırımı yapılabilir (4,22).
Tedaviye kemik yaşının kızlarda 12, erkeklerde 13 yaştan büyük olması halinde son verilmelidir. Boy uzamasındaki kazanç kemik yaşı ve puberte bulguları ile tedaviye başlanması arasında ne kadar süre olduğu ile yakından ilişkilidir. Çalışmalarda boy kazancı 3-10 cm arasında değişmektedir. 9 yaşından sonra tedaviye başlanan kızlarda boy kazanımına faydası gösterilememiştir.
GnRH agonistlerine karşı tolerans genellikle iyidir. Tedavinin yan etkileri arasında baş ağrısı, döküntü, gastrointestinal şikayetler veya sıcak basması gibi menopoz semptomları sayılabilir. Bu olumsuz etkiler genellikle geçicidir, kendiliğinden veya semptomatik tedavi ile
22 düzelir. Enjeksiyon yerinde steril apse gibi lokal komplikasyonlar görülebilir. Nadir durumlarda anafilaksi görülen hastalar bildirilmiştir.
GnRH agonistinin ilk enjeksiyonundan sonra vajinal kanama özellikle ileri pubertal gelişimi olan kızlarda (Tanner evre 4) ortaya çıkabilir ve bu östrojen konsantrasyonundaki düşüşe bağlanmıştır. Bununla birlikte tedavi sırasında kalıcı vajinal kanama, gonadotropinin salgılanmasının zayıf baskılandığının bir işaretidir.
SEP'li kızlarda GnRH agonist tedavisinin ilk aşamalarında zaman zaman sıcak basması görebilir. Bu, östrojen konsantrasyonlarının azalmasından kaynaklanır, ancak hızlı bir şekilde düzelir.
Bazı çalışmalarda GnRH agonist tedavisi alan hastalarda konvülsiyonlar bildirilmiştir. Bu çalışmalara nöbet öyküsü olan hastalar, epilepsi, serebrovasküler bozukluklar, merkezi sinir sistemi anomalileri veya tümörler ve konvülsiyonlarla ilişkili olan ilaçları olan hastalar dahil edilmiştir. Belirtilen bu durumlardan herhangi birinin yokluğunda da hastalarda konvülsiyonlar bildirilmiş olup literatürdeki veriler sporadik olgularla sınırlıdır (4).
Erişkin hasta gruplarında GnRH agonist kullanımı ile ilişkili uzun QT sendromu bildirilmiştir. Çocuklarda görülmemiş olmasına rağmen hastanın konjenital kalp hastalığı, aritmi veya uzun QT sendromu öyküsü, ailede uzun QT sendromu veya ani kardiyak ölüm öyküsü varsa, uzun QT aralığına neden olduğu bilinen başka ilaçlar kullanıyorsa EKG ile izlem önerilmektedir.
GnRH agonist tedavisi sırasında veya tedavinin kesilmesinden sonra az sayıda hastada femur başı epifiz kayması bildirilmiştir (4). Bunun ergenlikte kritik kemik oluşumu döneminde yeterli cinsiyet hormonuna maruz kalmama ile ilişkili olduğu düşünülmektedir.
SEP’de GnRH agonist tedavisinin uzun dönem etkileri değerlendirildiğinde üreme fonksiyonunu bozduğuna veya fertiliteyi azalttığına dair kanıt yoktur. Çoğu kızda tedavinin kesilmesinden hemen sonra menarş ve düzenli menstrüel sikluslar olarak gonadal fonksiyonlar geri döner.
Erken cinsel olgunlaşması olan hastalarda psikososyal değerlendirme verileri ve GnRH agonistleri ile tedavinin psikolojik sonuçlarına ilişkin çok az veri mevcuttur.
Tedavinin aynı zamanda vücut kitle indeksini (VKİ) etkileyebileceğine dair endişeler vardır. Uzun süreli çalışmalar, tanıdan önce aşırı kilolu ve obez olma prevalansında artış olmasına rağmen, tedaviden önce ve sonra VKİ SD (standart deviasyon) skorlarını karşılaştırdığında tedaviye bağlı kilo alımı kavramını desteklememiştir. Başvuru sırasında ve
23 tedavi sırasında yüksek VKİ SD skorlarına sahip olmak genç erişkinlik döneminde aşırı kilolu veya obez olmakla ilişkili bulunmuştur. GnRH agonist tedavisinin bu çocukların ergenlik veya yetişkinlik döneminde obeziteye doğru uzun süreli ilerlemelerini etkilemediği görülmektedir. Bununla birlikte, erken puberte tanılı kızlarda obezite riski bir endişe kaynağıdır ve VKİ yakından izlenmelidir (2,4)
SEP’li olguların tanı anında sıklıkla kemik mineral yoğunluğunun (BMD) artmış olduğu görülür. GnRH agonist tedavisi kemik mineralizasyonunu yavaşlatır, ancak tedavi kesildikten sonra kemik mineral yoğunluğunu geç ergenlik döneminde yaşıtlarından önemli ölçüde farklı görünmemektedir.
SEP’e hipotalamik bir lezyon (kitle veya malformasyon gibi) neden olduğunda, lezyonun tedavisinin genellikle pubertal gelişim seyri üzerinde etkisi yoktur. Hipotalamik hamartomlara, erken puberteye çözüm olarak cerrahi girişim uygulanmamalı, cerrahi tedavi sadece refrakter epilepsi ve intrakraniyal hipertansiyon gibi nörolojik semptomları olan büyük hamartomlar için düşünülmelidir.
Periferik EP nedeni olan gonadal tümörlerin, cerrahi, kemoterapi ve radyoterapi planı multidisipliner bir ekip tarafından oluşturulmalıdır. Büyük over kistleri (> 20 mL veya 3.4 cm çapında) over torsiyon riski göz önüne alınarak yönetilmelidir. Ekzojen cinsiyet steroidlerinin veya steroidal aktiviteye sahip bileşiklerin PEP’ye yol açtığının saptanması halinde bu maddelere maruziyet ortadan kaldırılmalıdır (2).
24 3 GEREÇ VE YÖNTEM
Bu çalışmada Ege Üniversitesi Tıp Fakültesi Çocuk Endokrinoloji ve Diyabet Bilim Dalı polikliniğinde santral erken puberte tanısı ile GnRH agonist tedavisi almış kız hastaların özellikleri mevcut hasta dosyalarından retrospektif olarak incelendi. Etik kurul onayı Ege Üniversitesi Tıp Fakültesi etik kurul başkanlığından alındı.
Ocak 2004 ile Aralık 2014 yılları arasında polikliniğimize 8 yaşından önce meme gelişimi ve/veya pubik kıllanma, 10 yaşından önce menarş ile başvuran kız çocukları erken ergenlik açısından değerlendirilmeye alındılar. Rutin olarak bu hastalardan ayrıntılı anamnez alındı, şikayetlerin başlangıç yaşı, semptomların ilerleme hızı, hızlı boy uzamasının olup olmadığı, kullanılan ilaçlar ile anne menarş yaşı sorgulandı.
Hastaların vücut ağırlığı Baster marka dijital tartı cihazıyla ayakkabısız şekilde, üzerlerinde ince elbiseleri varken ölçüldü. Boyları nötral pozisyonda dururken Seca marka stadiometre ile yapılan üç ölçümün ortalaması olarak kaydedildi. Vücut ağırlığı, boy, VKİ, hedef boyları, tahmini erişkin boyları ve bunların standart deviasyon skorları (SDS) Çocuk Endokrinoloji ve Diyabet Derneği’nin ÇEDD-ÇÖZÜM programı ile hesaplandı (25).
Genel sistem muayenesi ve pubertal evrelemesi Tanner Marshall evrelemesine göre çocuk endokrinoloji hekimi tarafından yapıldı. Tanner I prepubertal, II-V pubertal kabul edildi. Hastaların kemik yaşları yine çocuk endokrinoloji hekimi tarafından sol el bilek grafilerinden Greulich - Pyle atlası kullanılarak belirlendi.
Meme gelişimi bulunan kızlardan erken puberte ön tanısı sabah alınan kan örneğinde LH, FSH, östradiol ölçümü yapıldı. Laboratuarımızda FSH ve LH Roche Modular e-601 immunoassay cihazında (Roche Diagnostics GmbH, Manheim, Germany) elektroemilüminesans immünolojik yöntemle (ECLİA), sandviç prensibi ile, östradiol ise Roche Modular e-601 immunoassay cihazında (Roche Diagnostics GmbH, Manheim, Germany) elektroemilüminesans immünolojik yöntemle (ECLİA), yarışma prensibi ile çalışıldı. Bazal serum LH düzeyinin ≥ 0.3 mIU/mL olması pubertal olarak kabul edildi. Bazal LH’nın <0.3 mIU/mL olduğu olgulara ise santral erken puberte tanısına yönelik olarak LHRH uyarı testi 100 mcg GnRH (2.5 mcg/kg) (Gonadorelin Acetate, Ferring)’nin intravenöz enjeksiyonu ile yapıldı ve serum LH ve FSH ölçümü için kan örnekleri 0, 30, 60, 90. dakikalarda alındı. Testte pik LH’nın 5 mIU/mL ve üzerinde olması SEP için tanı kriteri olarak kabul edildi.
25 Bazal LH veya LHRH uyarı testindeki pik LH düzeyi ile santral erken puberte tanısı alan olgulara organik nedeni dışlamak için hipofiz bezi MR görüntülemesi yapıldı. Organik lezyon saptanan olgular çalışmaya dahil edilmedi. Çalışmaya alınan idiopatik santral erken puberteli kızlar içerisinde de büyümeyi ve puberteyi etkileyebilecek büyüme hormonu eksikliği, tiroid patolojisi, adrenal ve gonad patolojisi, dismorfik sendromu, iskelet displazisi, kronik hastalık, serebral palsi ve hidrosefali gibi defektleri olan ve kronik ilaç kullanım hikayesi veren olgular da çalışmadan çıkartıldı.
Tanıda olgulara erken puberte tanısını desteklemek ve over patolojilerini dışlamak amacıyla pelvik ultrasonografi yapıldı. Over ve uterus boyutları, endometrial kalınlık ve overde foliküler kist varlığı ve sayısına bakıldı. Uterus uzunluğunun 35 mm’den fazla olması ve over volümlerinin 2 cc’den fazla olması erken puberte için destekleyici bulgu olarak kabul edildi.
Aşağıdaki kriterleri taşıyan hastalara santral erken puberte tanısı aldı:
1. Kızlarda meme gelişimi veya pubik kıllanmanın 8 yaşından önce başlaması 2. Kızlarda menarşın 10 yaşından önce olması
3. Kemik yaşının kronolojik yaştan +2 SD ileri olması
4. Bazal LH’nın pubertal düzeyde olması veya LHRH testinde pik LH’nın 5 mIU/mL’nin üzerinde olması
5. İzlemde hızlı pubertal ilerleme
6. Pelvik USG’de uterus uzun çapının >35 mm ve over hacminin >2 cc olması
7. Erken puberteye yol açabilecek nörolojik-anatomik-organik bir patolojilerin dışlanması (idiyopatik SEP)
GnRH tedavi endikasyonları ;
Santral erken puberte bulguları varlığında tahmin edilen boyun 5 persantil altında kalması Menarş yaşının 10 yaş altında olması
SEP tanısı ile tedavi alan hastalar 6 ay ara ile poliklinikte değerlendirildi. Tedaviye uyumları ve pubertal bulguları dosyalarına kaydedildi. Her poliklinik kontrolünde vücut ağırlığı ve boy yapıldı, vücut kitle indeksi hesaplandı. Takvim yaşına göre boy SDS, vücut ağırlığı SDS, VKİ SDS hesaplandı. Hastaların 6 ay aralar ile hormonal değerlendirmesi
26 yapıldı. Tedavi süresince meme gelişiminin durması veya gerilemesi, prepubertal bazal veya pik LH düzeylerinin sağlanması ile hipotalamus-hipofiz-gonad aksının baskılandığı kabul edildi. Tedavi sırasında kemik yaşı yıllık olarak değerlendirildi. Tedavinin boy üzerine etkinliği tedavi başlangıcında ve izlem yıllarında tahmini erişkin boy ve tahmini erişkin boy SDS hesaplanarak değerlendirildi.
Kemik yaşı, tedavinin seyrindeki büyüme hızı, çocuğun psikolojik durumu ve ailesinin beklentileri göz önüne alınarak her olguda bireysel değerlendirme ile tedavinin kesilmesi planlandı. Tedavisi tamamlanan hastaların retrospektif olarak taranmasında tanı, izlem yılları ve final verilerine ait bilgiler olgu formlarına kaydedildi.
İstatiksel analizlerde IBM SPSS Statistics 25.0 Programı kullanıldı. Nümerik değişkenler ortalama ve standart sapma veya medyan(min-max) olarak verildi. Kategorik değişkenler sayı ve yüzde olarak verildi. Vücut ağırlığı, VKİ, boy, kemik yaşı ölçümleri aynı etkiler için parametrik olmayan yöntem Brunner-Lamger (LD-F1 dizayn) ile, R 3.5.2 yazılımı (R software, version 3.5.2, package: nparLD, R Foundation for Statistical Computing, Vienna, Austria; http://r-project.org) yardımıyla analiz edilmiştir. Tüm hipotezler için anlamlılık düzeyi 0.05 kabul edildi.
27 4 BULGULAR
Çalışmaya Ege Üniversitesi Çocuk Endokrinoloji ve Diyabet Polikliniği’nde santral erken puberte tanısı ile takip edilerek GnRH agonist tedavisi verilen 92 kız hasta dahil edildi. Hastaların 6’sının başvuru yakınması 10 yaşından önce menarş iken diğerlerinin 8 yaşından önce meme gelişimi ya da pubik kıllanmaydı. DSÖ sınıflamasına göre VKİ SDS’si 1 ve altında olan olgular normal kilolu, 1’in üzerinde olanlar fazla kilolu, 2’nin üzerinde olanlar obez olarak kabul edildi. Normal kilolu hasta sayısı 58, fazla kilolu hasta sayısı 31 ve obez hasta sayısı 3 idi. Hastalar 2 gruba ayrıldı. Normal kilolular grup 1’i, fazla kilolu ve obez olanlar grup 2’yi oluşturdu. (Şekil 10)
Şekil 10. Hastaların VKİ’ye göre dağılımı
VKİ= vücut kitle indeksi
4.1 Demografik Veriler
Tanıda normal kilolu grup, fazla kilolu ve obez grup ile tüm olguların demografik veriler Tablo 5’te verildi. Tüm olguların tanı yaşı ortalaması 8.08 ± 1.12 (4.38-10.31) yıl, normal kilolu grubun 8.11 ± 1.09 yıl, fazla kilolu ve obez grubun 8.03 ± 1.19 yıldı. Olguların puberte evreleri evre 1 ile evre 4-5 arasında olup ortalama 2.71 ± 0.64 idi. Tüm grupta anne boy ortalaması 159.3 ± 5.32 cm, baba boy ortalaması 173.6 ± 6.66 cm, hedef boy ortalaması
28 159.9 ± 4.98 cm idi. Hedef boy ortalaması normal kilolu grupta 160.2 ± 4.94 cm, fazla kilolu ve obez grupta 159.4 ± 5.08 cm idi. İki grubun hedef boyları arasında anlamlı farklılık saptanmadı (p=0.46). Tedavi süresi ortalaması tüm grupta 29.5 ± 9.9 ay, normal kilolu grupta 29.7 ± 10.44 ay, fazla kilolu ve obez grupta 29.0 ± 9.12 aydı. Tedavi süreleri karşılaştırıldığında 2 grup arasında farklılık yoktu (p=0.76).
Tablo 5. Grupların Demografik Verileri
Normal kilolu grup Fazla kilolu ve Obez
grup Tüm grup
Tanı Yaşı (yıl) 8.11 ± 1.09 8.03 ± 1.19 8.08 ± 1.12
Tanner Evresi 2.66 ± 0.68 2.83 ± 0.28 2.71 ±0.64
Anne Boyu (cm) 159.7 ± 5.14 158.6 ± 5.62 159.3 ± 5.32 Baba Boyu (cm) 173.7 ± 6.83 173.4 ± 6.43 173.6 ± 6.66 Hedef Boy (cm) 160.2 ± 4.94 159.4 ± 5.08 159.9 ± 4.98 Tedavi Süresi (ay) 29.7 ± 10.44 29.0 ± 9.12 29.5 ± 9.9
4.2 Tanıda Antropometrik Bulgular ve Kemik Yaşı
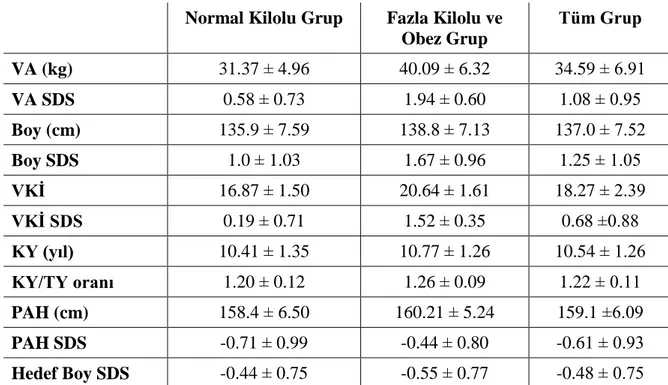
Tanı anında normal kilolu grup, fazla kilolu ve obez grup ile tüm grup antropometrik bulguları Tablo 6’da verildi. Tanıda boy ortalaması tüm grupta 137.0 ± 7.52 cm, normal kilolu grupta 135.9 ± 7.59 cm, fazla kilolu ve obez grupta 138.8 ± 7.13 cm idi. Tanıda boy SDS ortalaması tüm grupta 1.25 ± 1.05, normal kilolu grupta 1.0 ± 1.03, fazla kilolu ve obez grupta 1.67 ± 0.96 SDS idi. Boy SDS değerleri karşılaştırıldığında fazla kilolu ve obez grubun, normal kilolu gruptan daha uzun olduğu görüldü (p=0.003).
Tanıda vücut ağırlığı ortalaması tüm grupta 34.59 ± 6.91 kg, normal kilolu grupta 31.37 ± 4.96 kg, fazla kilolu ve obez grupta 40.09 ± 6.32 kg ’dı. Vücut ağırlığı SDS ortalaması tüm grupta 1.08 ± 0.95, normal kilolu grupta 0.58 ± 0.73, fazla kilolu ve obez grupta 1.94 ± 0.60 idi.
Tanıda VKİ ortalaması tüm grupta 18.27 ± 2.39, normal kilolu grupta 16.87 ± 1.50, fazla kilolu ve obez grupta 20.64 ± 1.61 idi. VKİ SDS ortalaması tüm grupta 0.68 ± 0.88, normal kilolu grupta 0.19 ±0.71, fazla kilolu ve obez grupta 1.52 ± 0.35 idi.
Tanıda kemik yaşı ortalaması tüm grupta 10.54 ± 1.26 yıl, normal kilolu grupta 10.41 ± 1.35 yıl, fazla kilolu ve obez grupta 10.77 ± 1.26 yıldı. Tanıda kemik yaşı / takvim yaşı (KY/TY) oranı ortalaması tüm grupta 1.22 ± 0.11, normal kilolu grupta 1.20 ± 0.12, fazla
29 kilolu ve obez grupta 1.26 ± 0.09 idi. Tanıda grupların KY/TY oranları arasında anlamlı farklılık saptandı (p=0.007).
Tanıda tahmini erişkin boy (PAH) ortalaması tüm grupta 159.1 ± 6.09 cm, normal kilolu grupta 158.4 ± 6.50 cm, fazla kilolu ve obez grupta 160.2 ± 5.24 cm idi. Tanıda PAH SDS ortalaması tüm grupta -0.61 ± 0.93, normal kilolu grupta -0.71 ± 0.99, fazla kilolu ve obez grupta -0.44 ± 0.80 idi. Grupların tanıda PAH SDS değerleri karşılaştırıldığında anlamlı farklılık yoktu (p=0.19).
Hedef boy SDS ortalaması tüm olgularda -0.48 ± 0.75, normal kilolu grupta -0.44 ± 0.75, fazla kilolu ve obez grupta -0.55 ± 0.77 idi. İki grubun hedef boy SDS’leri arasında anlamlı farklılık saptanmadı (p=0.48).
Tablo 6. Tanıda Antropometrik Bulgular ve Kemik Yaşı
Normal Kilolu Grup Fazla Kilolu ve Obez Grup Tüm Grup VA (kg) 31.37 ± 4.96 40.09 ± 6.32 34.59 ± 6.91 VA SDS 0.58 ± 0.73 1.94 ± 0.60 1.08 ± 0.95 Boy (cm) 135.9 ± 7.59 138.8 ± 7.13 137.0 ± 7.52 Boy SDS 1.0 ± 1.03 1.67 ± 0.96 1.25 ± 1.05 VKİ 16.87 ± 1.50 20.64 ± 1.61 18.27 ± 2.39 VKİ SDS 0.19 ± 0.71 1.52 ± 0.35 0.68 ±0.88 KY (yıl) 10.41 ± 1.35 10.77 ± 1.26 10.54 ± 1.26 KY/TY oranı 1.20 ± 0.12 1.26 ± 0.09 1.22 ± 0.11 PAH (cm) 158.4 ± 6.50 160.21 ± 5.24 159.1 ±6.09 PAH SDS -0.71 ± 0.99 -0.44 ± 0.80 -0.61 ± 0.93 Hedef Boy SDS -0.44 ± 0.75 -0.55 ± 0.77 -0.48 ± 0.75
VA= vücut ağırlığı, SDS= standart deviasyon skoru, VKİ= vücut kitle indeksi, KY= kemik yaşı, TY= takvim yaşı, PAH= tahmini erişkin boyu
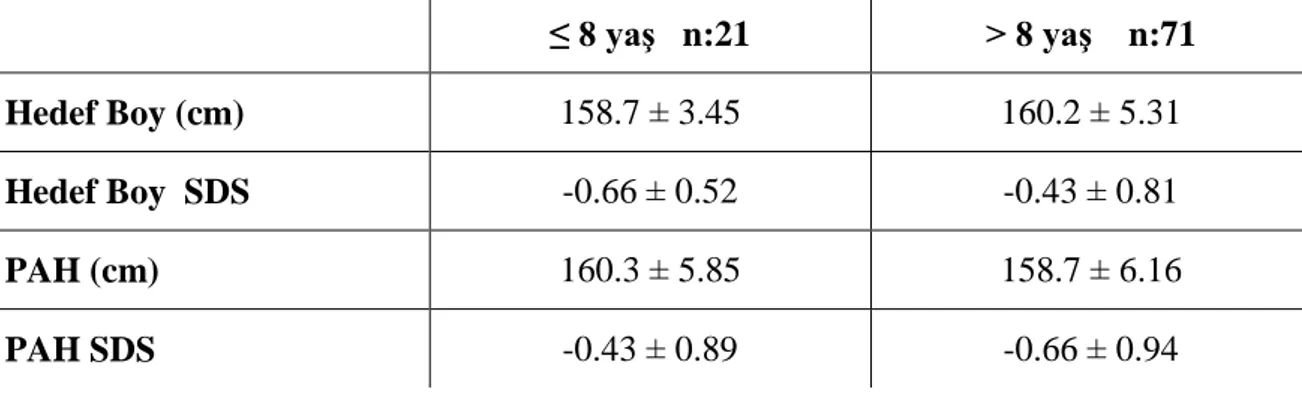
Hastalar tedavi başlama yaşlarına göre 8 yaş ve altı ile 8 yaş üzeri olarak 2 gruba ayrıldığında 8 yaş üzeri hastaların hedef boyları 160.2 ± 5.31 cm, PAH 158.7 ± 6.16 cm ve tedavi sonunda PAH 161.4 ± 5.85 cm saptandı (Tablo 7 ve 8). 8 yaş üzeri hastaların PAH’larının tedavi başlangıcı ve tedavi sonu değerleri karşılaştırıldığında anlamlı artış olduğu görüldü (p<0.01).
30 Tablo 7. Yaş Gruplarının Tedavi Başlangıç Hedef boy ve PAH verileri
≤ 8 yaş n:21 > 8 yaş n:71
Hedef Boy (cm) 158.7 ± 3.45 160.2 ± 5.31
Hedef Boy SDS -0.66 ± 0.52 -0.43 ± 0.81
PAH (cm) 160.3 ± 5.85 158.7 ± 6.16
PAH SDS -0.43 ± 0.89 -0.66 ± 0.94
PAH= tahmini erişkin boyu
Tablo 8. Tedavi Sonu Yaş Gruplarının PAH verileri
≤ 8 yaş n:13 > 8 yaş n:32
PAH (cm) 165.0 ± 6.93 161.4 ± 5.85
PAH SDS 0.28 ± 1.05 -0.25 ± 0.89
4.3 Tanı Laboratuar ve USG Verileri
Tanıda 92 hastanın 86’sının (%93.5) bazal LH değeri mevcuttu. Tüm grupta 50 (%54.3) hastaya LHRH uyarı testi yapılmıştı. Olguların laboratuvar verileri Tablo 9’da görülmektedir. Tanıda bazal LH değerlerinin ortalaması tüm grupta 1.76 ± 1.79 mIU/mL, normal kilolu grupta 1.33 ± 1.25 mIU/mL, fazla kilolu ve obez grupta 2.62 ± 2.33 mIU/mL idi. Tanıda bazal LH düzeyi 0.3 mIU/mL’nin üzerinde olan hasta sayısı 67 idi. Tanıda östradiol düzeyi ortalaması tüm grupta 29.7 ± 21.83 pg/mL, normal kilolu grupta 29.1 ± 21.98 pg/mL, fazla kilolu ve obez grupta 30.98 ± 21.91 pg/mL idi.
Tanıda LHRH uyarı testi yapılan 50 hastanın 34 tanesi normal kilolu grupta, 16 tanesi fazla kilolu ve obez grupta yer almaktaydı. LHRH uyarı testinde pik LH ortalaması tüm grupta 16.0 ± 12.51 mIU/mL, normal kilolu grupta 15.06 ± 12.46 mIU/mL, fazla kilolu ve obez grupta 18.29 ± 12.71 mIU/mL idi.