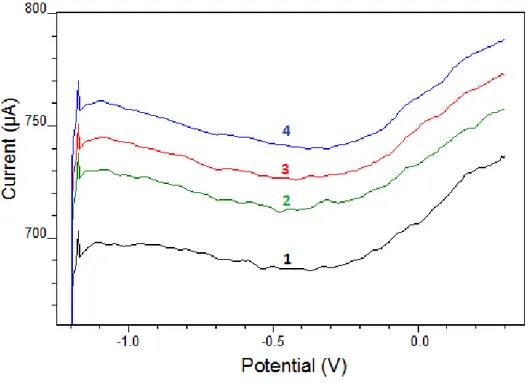
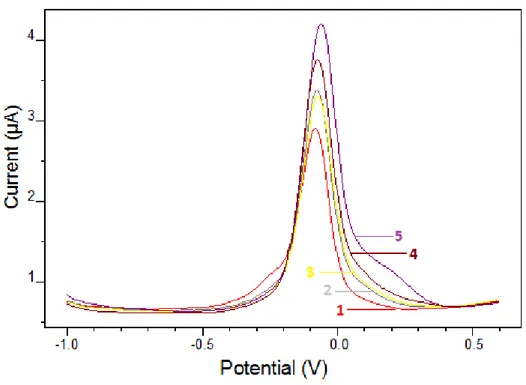
Bizmut film modifiye elektrotlarla voltammetrik tayini
Tam metin
Şekil
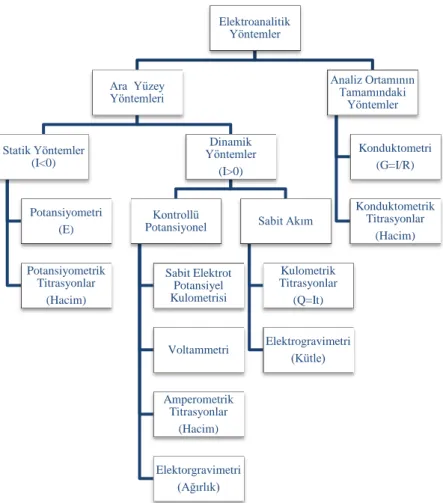
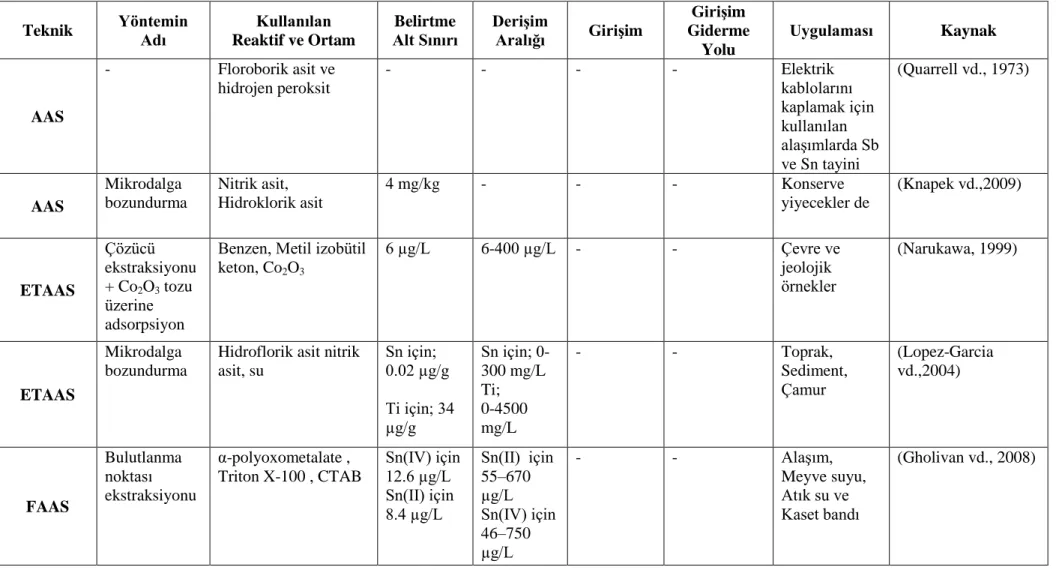

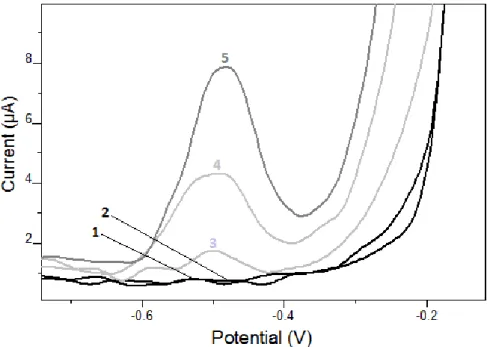
Benzer Belgeler
Araştırmacı tarafından geliştirilen, çoktan seçmeli 20 maddelik “Geometrik Şekiller ve Cisimler Başarı ve Kalıcılık testi” nin geçerliliğini ve
anlamda, tiyatro toplum için bir okul görevi üstlenir. Tiyatro, halka yönelik bir sanattır. Halkın her bireyine yönelmeyi amaçlar. Bireylere yönelik olması, toplumsal
雙和醫院引進乳房手術診斷新技術, 「新型超音波導引真空輔助抽吸技術」可維 持乳房美好曲線
Her ne kadar servet eşitsizliği 1980’lerden bu yana çoğu gelişmiş ülkede artmışsa da ABD’de bu artışın hızı çok daha yüksek olmuş ve özellikle en zengin %1’lik kesim
93 Harbi sonrasında Rumeli‟den Samsun‟a sevk edilen ve buradan Anadolu‟nun iç bölgelerine daimî olarak iskân edilmeleri için gönderilen Çerkes muhacirleri de
Çalışmanın diğer bir amacı da artan düzeyde sulama suyu tuzluluğunun hıyar bitkilerinin meyve özellikleri (meyve çap ve boyu, tek meyve ağırlığı, meyve su
ġekil 3.15 : Kompozit ve izotropik kanatta burulma yükü altında yer değiĢtirme - arka kiriĢ: referans (Bhardwaj, 1997) ve mevcut çalıĢma. Böylece literatürde mevcut olmayan