--- ---
---Ankara Üniv Vct Fak Derg 47,3 i-37, 200{)
ANKARA KEÇİLERİNİN KONJUNKTİV AİLE İLİşKİLİ
LENFOİD DOKUSU (CALT) ÜZERİNDE IŞIK
MİKROSKOBİK ÇALIŞMALAR
Reşat Nuri AŞTı}
Hikmet ALTUNAy2
Nevin KURTDEDE2
Asuman ÖZEN
lLight microscopic studies on the conjUlıctiva-associated
lymphoid tissue (CALT)
of Angora goats
Summary: The purpose
(J{this study was to investiKate the liKht mieroscopic
structure o{conjunctiva-associated
lymphoid tissue (CALT) q/'AnKora goats.
The samples tissue taken from lower and upper eyelids o{lO
healthy, 5-6
month-old Angora goats were used in this study.
The eonjunctiva-associated
lymphoid tissue of Angora goats was formed
by
solilary
and aKgregated
lymphoid folliC!es and follic!e-associated
elJithelium
(FAE) which ('over this follic!es.
Alpha-naphthyl
asetate esterase (ANAE) positive T lymphocytes were seen in
the peripheral region surrounded o{ germinal center, subepithelial area and FA£.
Immunoglobulin
(It;) ('ontaining B lymphocytes were found in the Kerminal center
and subepithelial area. Veryfew T lymphocytes were seen in the B eells reKion and
veryfew B lymphocytes were seen in the T cells regions.
Key words: AnKora goats, CALT. Conjunctiva
Özet: Bu çalı~çma. Ankara
keçilerinin
konjunktiva
ile ili~çkili lenfoid
do-kusunun (CALT) ışık mikroskobik yapısını incelemek amacıyla yapıldı.
Çalışmada
10 adet sağlıklı,
5-6aylık Ankara keçisinin alt ve üst KÖZ
ka-paklarından altnan doku örnekleri materyalolarak
kullanıldı.
Ankara keçilerinin konjunktiva ile ili,,'kili len{oid dokusunun. soliter ya da
aK-reKat lenffollikülleri
ile bu folliküllerin
üzerini örten ./lJllikülle ilişkili epitelden
(FAE) olu",tuğu Közlendi.
Alfa-na/iiI asetat esteraz (ANA E) pozitif T lenfositler Kerminal merkez.i
~'ev-releyen bii/Kede. subepiteliyal alanda ve FAE'de Körüldü. lmmunKlobulin
(Lg)ta-,çıyan B len{ositlere ise Kerminal merkezde ve suhepiteliya! alanda rastlandı. T
len-j(Hit biilgelerinde az sayıda B. B len{osit bÖlKelerinde de az sayıda
T lenj(Hitler
göz.lendi,
Anahtar kelimeler: Ankara keçisi. CA LT, Konjunktiva
iProf. Dr.. AÜ Veteriner Fakültesi Histoloji-Embriyoloji Anabilim Dalı, Ankara 2 Doç. Dr.. AÜ Vcterİner fakültcsi Histoloji-Embriyoloji Anabilim Dalı. Ankara 3 Dr.. AÜ Vetcrincr Fakültesi Histoloji-Embriyoloji Anabilim Dalı. Ankara
32
Giriş
Antijenleri alan ve bunları antikor yapımı
içın sunan hücreleri içeren mukozal lenfoid
doku, mukozal yüzeylerin savunmasında
önem-li roloynar (6). Barsaklarla ilişkili lenfoid doku (GALT) (1 I, 13, 30-32) ve bronşlarla ilişkili
lenfoid doku (BALT) (2, 8, 9, 12, 17)
me-melilcr ilc kanatlılarda incelenmiştir.
Kon-junktiva ile ilişkili lenfoid doku (CALT)
mor-folojik olarak GALT ve BALT'da bildirilen (7,
20) özelliklere benzerlik göstermektedir.
Lo-kalizasyonu, epitel yapısı, hücre kompozisyonu
ve vasküler görünümü ile CAL T mukozal
im-munitede önemli role sahiptir (18). CALT,
an-tijenlerle temas bölgesi oluşturarak bu
an-tijenlcre karşı antikor yapımında roloynar (20). CAL T soliter ya da agregat lenf follikülleri ile hu folliküllerin üzerini örten özellqmiş epi-telden olu~ur. Bu epitel, follikülle ilişkili epitel (FAE) ya da lenfoepitel olarak isimlendirilir (IS-20,36).
F AF, kadeh hücresi içermeyen yassıla~mış
epitelden meydana gelir (1 S-20, 34).
Non-lenfoid konjunktiva epiteli ise kadeh hücreleri içeren (34) çok katlı yassıdır (22, 34).
FAE altında soliter ya da agregat lenf fol-li külleri bulunmaktadır (18-20, 26). Lenf 1'01-liküllerinin germinal merkezinde B lenfositler (26), blast formunda hücreler, mitotik figürler
(I 8, 19) ve az sayıda T lenfosit (37)
bu-lunmaktadır. Germinal merkezin çevresi ise T
lenfositlerce sınırlandırılmıştır (26).
Fol-Iiküllerin çevresindeki bağdoku içinde plazma
hücreleri gözlenmektedir (20, 26, 37).
Bu ara~tırma, Ankara keçilerinin
kon-junktiva ile ilişkili lenfoid dokusunun (CALT)
ı~ık mikroskobik yapısını incelemek amacıyla
yapıldı.
Materyal ve Metot
Çalışmada, Ankara Lalahan Zootekni
Araştırma Enstitüsü'nden sağlanan LO adet
sağ-lıklı 5-6 aylık Ankara keçisinin alt ve üst göz
kapaklarından alınan doku örnekleri materyal
olarak kullanıldı.
R. N. AŞTı' N. KURTDEDE. H. ALTUNA Y. A. ÖZEN
Alınan doku parçalarının bir kısmı genci
görünümü incelemek için % 1O formol'de tespit
edildikten sonra paraplastta bloklandı ve bu
bloklardan alınan 7 mikronluk kesitlere tripk
boya yöntemi uygulandı (14). Alınan doku
par-çalarının diğer kısmı T lenfositlerin
be-lirlenmesi için, önceden soğutulmuş
formol-sukroz soli.isyonunda (pH 6,8) +4°Cde 22 saat
tespit edildikten sonra, +4°Cdeki Holt
so-li.isyonunda 22 saat tutuldu ve kriyostatta alınan 8 mikronluk kesitlere alfa-naftil asetat esteraz
(ANAE) boyama yöntemi (pH 6,4) uygulandı
(27).
Alınan doku parçalarının diğer kısmına ise, IgG içeren hücrelerin belirlenmesi için direkt
immunperoksidaz yöntemi uygulandı (14).
Par-çalar sıvı azotla donduruldu ve bunlardan
kri-yostatta 8 mikronluk kesitler alındı. Bu kesitler
iyice kuruduktan sonra, önceden soğutulımı~
asetonda 10 dakika tespit edildiler. Kesitlere en-dojen peroksidaz aktivitesinin giderilmesi için
metanolde hazırlanmış % 0,5 H2
0
2 20 dakikauygulandı. Daha sonra kesitler fosfat buffer
salin (PBS, pH 7,4) ile yıkandılar ve uygun
oranda sulandırılmı~ anti goat IgG peroksidaı
konjugatı (Sigma, A 5420) ile i saat inhibe
edildiler. Süre sonunda PBS ile iyice yıkanan
kesitlere peroksidaz aktivasyonu için, substrat olarak tris bu ffer salin (pH 7,6) 'de hazırlanan
3, 3' diaminobenzidin (DAB) tetrahidroklorid
(Sigma, D 5905) 20 dakika uygulandı. PBS ilc
iyice yıkanan kesitlerin bazılarına iO saniye
Mayer's hematoksilen (14) ile çekirdek boyası
yapılırken, diğer kesitlere çekirdek boyası uy-gulanmadı.
Alınan doku parçalarının diğer bir kısmı
ise plazma hücrelerinin belirlenmesi için, alkol-formol soli.isyonunda 48 saat tespit edildikten sonra dereceli alkollerden, metilbenzoat ve ben-zollerden geçirilerek paraplastta bloklandılar.
Bu bloklardan alınan 7 mikronluk kesitlere
plazma hücresi boyaması olan
methylgreen-pyronin uygulandı (10).
Bulgular
Hazırlanan preparatlarda konjunktivanın
lenfoid (Şekilla) ve nonlenfoid bölgeler (b)
içerdiği gözlendi. Nonlenfoid bölgenin kadeh
33
••
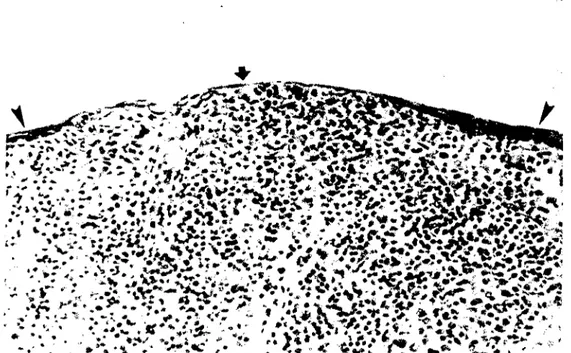
Şekil i. Konjıınktıva'nın lenfoid (a) ve nonlenfoid (b) bölgeleri. ok : lenfoid bölge epiteli. ok ba~ı: nonlenfoid
bölge epiteli. Triple. x i
ın.
Figure i. Lymphoid (a) and nonlymphoid (b) arca of conjıınctiva. arrow : Iymphoid epitheliıım. arrow head ,
nonlymphoid epitheliıım. Triple. x i
ın,
ğişik gelişme aşamalarında olan pironinolilik hücre ile mitoz figürlerine rastlandı. Germinal
merkezin çevresinde ve subepiteliyal bölgede
az sayıda pironinofilik hücre gözlendi.
Fol-liküllerin çevresindeki bağdoku içerisinde tipik plazma hücreleri görüldü.
'b
A/'\Ki\RA KEÇILERININ KONJUNKTIVA ILE ILIŞKILI LENFOlD DOKUSU (CALT) ÜZERI/'\DE ışıK MIKROSKOBIK ÇALIŞMALAR
ı.
2 ok başı) oluştuğu dikkati çekti. Lenfoidbölge ise soliter ya da agregat lenf follikülleri ile bu folliküllerin üzerini örten ve kadeh hüc-resi içermeyen yassılaşmış epitelden (Şekili, 2 oklar) oluştuğu görüldü.
ANAE boyama yöntemi uygulanan kesitler
incelendiğinde
T
lenfositlerin çoğunda bir ikiadet kırmızı granül şeklinde (Şekil 3 oklar, ok-başları), retikulum hücrelerinde ise diffuz re-aksiyon (R) gözlendi. Lenf folliküllerinin
ger-minal merkezinde (G) ANAE negatif, bunu
çevreleyen bölgelerde ise ANAE pozitif
len-rosİtler (oklar) saptandı. Germinal merkezin
pe-rikrinde az sayıda ANAE pozitif hücreye de
rastlandı (ok başları). Ayrıca, ANAE pozitif
lenfositler F AE ve subepiteliyal bölgede de gö-rüldü (Şekil 4oklar).
Methylgreen-pyronin ilc boyanan
pre-paratiarda germinal merkezde çok sayıda ve
de-İmmunperoksidaz boyama yöntemi
uy-gulanan preparatlar incelendiğinde
im-munglobulin (Lg) taşıyan hücreler (Şekil 5
oklar) germinal merkezde (G) çok, gerıTIİnal
merkezin etrafı ve subepiteliyal bölgede (S) az sayıda gözlendi.
Şekıl ~. KOIlJunktıva'nııı lenfoıd (ok) ve nonlenfoıd (ok ba~ı) bölge epıteli. Tnpk. x 285.
34 R. N. AŞTı' N. KURTDEDE, H. ALTUNAY. A ÖZEN
Şekıl 3. Konjunktiva ile ili~kili lenfoid doku. G : germina! merkez, oklar: germinal merkezin çevresındeki bölgede ANAE pOLitif lenfositler, ok ba~ları : germina! merkezin periferindeki ANAE pozitif lenfositler, R : ANAE pozitif retikuluın
hücresi. ANAE. x 350.
Figure 3. Conjunctiva-associated lyınphoid tissue. G : germinal center, arrows : ANAE positive lymphocytes in pcripheral area surrounded of germinal center, arrow heads : ANAE positive lymphocytes inperipheral zone of gerıninal center, R :
ANA E posilive reticulum ceıı. ANAE staining. x 350.
Şekil 4. FI\E ve subepiteliya! hölgede ANI\E pozitif lenfositler (aklar). I\NAE. x 265. Figurc 4. ANAE posilive Iymphocytes (arrows) in FAE and subepithelia1 area. ANAE slaİnİng. x 265
ANKARA KEÇILERININ KONJUNKTIVA ILE ILIŞKILI LENFOlD DOKUSU (CALT) ÜZERINDE IŞIK MIKROSKOBIK ÇALIŞMALAR
35
Şckıl 5. Konjuııktiva ilc i11~kiliIcııfoid doku. G : gcrmiııal merkez. S : subepiteliyal bölge. oklar: 19 pozitif
Icnfositler. Immuııperoksidaz. x 260. Figure 5. Coııjuııctiva-associated Iymphoid lissue. G : genniııal center. S : subepithelial area. arrows : 19 positive
Iynıphoeytes. lınımıııoperoxidase staiııing. x 260.
Tartışma ve Sonuç
CALTın soliter veya agregat lenf
fol-likülleri ile folliküllerin üzel'ini örten özelleşmiş epitelden oluştuğu ve bu epitelin follikülle
iliş-kili epitel ya da lenfoepitel olarak
isim-lendirildiği bildirilmiştir
(18-20,
36). FAE'nin kadeh hücresi içermeyen yassılaşmış epiteldenmeydana geldiği belirtilmektedir
(18-20,
34).Nonlenfoid konjunktiva epitelinin ise aralarında
kadeh hücreleri bulunan (34) çok katlı yassı
epitel (22, 34) karakterinde olduğundan söz
edilmektedir. Çalışmada incelenen
pre-paratlarda korijunktivanın lenfoid ve nonlenfoid hölgeler içerdiği gözlendi. Nonlenfoid bölgenin kadeh hücreleri içeren çok katlı yassı epitelden oluştuğu dikkati çekti. Lenfoid bölge ise soliter ya da agregat lenf follikülleri ile bu failiküllerin
üzel'ini örten ve kadeh hücresi içermeyen
yas-sılaşmış epitelden oluştuğu görüldü.
Ça-lışmadan elde edilen bulgular araştırıcıların bul-guları ile paralellik göstermektedir.
FAE altında solitcr ya da agregat lenf 1'01-liküllerinin ycrleştiği belirtilmektedir (18-20, 26). Lenf folliküllerinin germinal merkezinde B lenfositler (26), blast hücreler, mitotik figürler (18, 19) ve az sayıda
T
.lenfosit (37) bulunduğu bildirilmektedir. Germinal merkezin çevresinin iseT
lenfositlerce sınırlandırıldığından sözedil-mektedir (26). Folliküllerin çevresindeki
bağ-doku içinde plazma hücrelerinin gözlendi
ği
be-lirtilmektedir (20, 26, 37). Çalışmada ANA E
boyama yöntemi uygulanan kesitler
in-celendiğinde lenf folliküllerinin germinal
mer-kezinde ANAE negatif, bunu çevreleyen
böl-gelerde ise ANA E pozitif lenfositler gözlendi.
Germinal merkezin periferinde az sayıda
ANA E pozitif hücreye rastlandı. Ayrıca, ANAE
pozitif lenfositler FAE ve subepiteliyal bölgede
de görüldü. İmmunperoksidaz boyama yöntemi
uygulanan preparatlar incelendiğinde
im-munglobulin taşıyan hücreler germinal
mer-kezde çok, germinal merkezin çevresinde ve
su-bepiteliyal bölgede az sayıda gözlendi.
Methylgreen-pyronin ile boyanan preparatlarda
germinal merkezde çok sayıda ve değişik
ge-lişme aşamalarında olan pironinofilik hücre ile mitoz figürlerine rastlandı. Germinal merkezin
çevresinde ve subepiteliyal bölgede az sayıda
pironinofilik hücre gözlendi. Folliküllerin çev-resindeki bağdoku içinde tipik plazma hücreleri görüldü. Çalışmadan elde edilen bu veriler, yu-karıdaki araştırıcıların bulguları ile uyum içe-risindedir.
Son yıllarda, nonspesifik esterazlardan
olan alfa-naftil asetat esterazın
T
lenfositlerindebulunduğu, B lenfositlerde ise bulunmadığı
çe-şitli araştırıcılar tarafından belirtilmiştir (3, 24,
25, 29). ANAE pozitif reaksiyonun
T
hüc-relerinde 1-2 adet lokalize granüller şeklinde
ol-duğundan, B lenfasitlerin ise ANA E
bo-yanmasına karşı negatif reaksiyon verdiğinden
söz edilmektedir (1, 3, 16, 28). Çalışmada
ANAE boyamasıyla
T
lenfositlerin çoğunda biriki adet kırmızı granül şeklinde, retikulum hüc-relerinde ise diffuz reaksiyon gözlendi. 19
bo-yama yöntemi uygulanan preparatların
in-celenmesinde ise ANAE negatif alanların 19
36
ark. (4) ilc Bianchi ve ark. (S) B lenfasit
böl-gesinde T, T !enfosit bölgesinde ise B
lcn-rositlerin az sayıda bulunduğunu
bil-dirmektedirler. Çalı~mada da, yoğun olarak T
lenfasit içeren bölgelerde B, B lenfasit içeren bölgelerde T hücreleri az sayıda gözlendi.
Ger-minal merkezde T lenfositlere rastlanılması,
sentrum germinativum reaksiyonunun
şe-killenmesi için T lenfasitlerin işbirliğine
ge-reksinim olmasından dolayıdır (21,23). Timusu
çıkarılan veya T hücreleri baskılanan
hay-vanlarda, sentrum germinativum reaksiyonu
şekillenmemektedir (2 I, 33). Bu reaksiyonun
şekillenmesi için germinal merkezde T
len-fositlerin, özellikle de yardımcı T lenfositlerin bulunması gereklidir. Ayrıca, T lenfositlerin
yoğun olarak hulunduğu bölgelerde az sayıda
B lenfosite rastlanılması, T ve B hücrelerinin karşılıklı ilişki kurarak, B hücrelerinin plazma
hücrelerine dönüşümünün bu bölgede
ol-masından ileri geldiği bildirilmektedir (1 S, 35).
Sonuç olarak, Ankara keçilerinin
kon-junktiva ile ilişkili lenfoid dokusunun soliter ya da agregat lenf failikülleri ile bu folliküllerin üzerini örten FAE'den oluştuğu saptandı. Alfa-naftil asetat esteraz pozitif T !enfositler
ger-minal merkezi çevreleyen bölgede,
su-bepiteliyal alanda ve FAE'de göri.ildü.
İm-munglobulin ta~ıyan B lenfasitIere ise germinal
merkezde ve subepiteliyal alanda rastlandı. T
!enfosit bölgelerinde az sayıda B, B lenfasit
bölgelerinde de az sayıda T lenfasitler
göz-!endi.
Kaynaklar
Aleksandersen M, Hcin WR, Landsverk T, Mdure S (1990) DisırihUlion o/ ly111phocyıe suhsels iıı ıhe
/ıırge iıılesıinl/I Iymphoid Fıilicles o/ Iwnhs.
Im-munology. 70. 391-397.
2. Anderson ML, Moore PF, Hyde DM, Dungworth DL (1986) Bmndıus (ıSsocil/led l.vmphoid ıissue iıııhe Iwıgs o/ cal/It': rt'lali(}ıIShip tn age. Res Vet Sci, 41,
211-220.
3 Aştı RN, Kurtdede N, Ergün L (1993) Kwıxal kö-pek/eriniıı perij;'r kaıı T len/osiıleri üzerinde ışık ve
e/ekımn mikmskopik çalı,Hnalar. A Ü Vet Fak Derg.
40, 563-576.
4. Aştı RN, Tanyolaç A, Kurtdcde N, Özen A (1997) T
ve II /enliJsillerin Ankara keçilerinin /enliJid
do-kull/nndakı dafIılı1111.Türk Veı Hay Derg, 21. 99-105.
5. Bianehi ATl, Zwart RJ, .Jeurissen SHM, Moonen-Leusen HWM (\992) Devel0plllt'llt or ıhe B- and
T-cell coıııpl/rımenıs in porcine Iymphoid orııans {i'om
R. N. AŞTı' N. KURTDEDE. H. ALTUNAY. A ÖZEN
hir/h 10 l/dıılı lil;' .(//1 i111mılııohis/fllogıw/ (/iJprol/ch Vet Immtınol Immunopathol. 33. 201-221.
6. Bienenstoek J, Befus AD (1980) MuCIJsoI
im-mwıoloııy Immunology. 41. 249-270.
7. Bicnenstoek J, Befus AD (1984) Cul (//ıd hrlJllchus
associaled Iymphoid ıissut' Am J Anat. 170. 437 -445.
8. Bienenstoek .J, .Johnston N (I 976) A morph%;;ıe
sıudy or rahhiı hmnchial lvmphoid l/Xgrt'gllles (//ıd
Iymphoepiıheliwn. Lab Invesı, 35. 343-348.
9. Bienenstoek .J, .Johnston N, Perey DYE (1973)
Bronchial IY111phoid ıissııe L. Morpholoxic
cha-mclerisıies. Lab Invest. 28, 686-692.
10. Böek P (1989) Romeis Mikmskopische Technik 17. Aufl. Urban und Schwarzenberg. München. s561. i 1. Burns RB (1982) Histoloııy and immwlOlogy or
Peyer's patches in ıhe doıııesıic .1owl (Cailus
do-mesıieus). Res Vel Sci. 32. 359-367.
12. Chamberlain DW, Nopajaroonsri C, Simon GT
(1973) VlırastructLlre olıhe pulmlJl/ar\, l\'llıphoıd
11.1-SUL'. Am Rev Respır Di". ıo8, 621-631.
ı
3. Chu RM, Liu CH (1984) MorphologlUlI andlUlıc-ıional compl/rismıs ol Peyer's palches in difl;'rmı
parls or ıhe swine smail inIl'sıine. Vel Immunol
Im-munopathol. 6. 391-403.
14. Culling eFA, Allison RT, Bar WT (1985) Cpllular
Paıhology Technique. Buııerworth. London. 4. ediıion.
ch 5, Pp: 347-365.
15. Dobashi M, Terashima K, Imai Y (1982) Electron
microscopie sıudy or difjerentiali()/ı ol
(//ıtihod\'-producinK ceil in mouse Iymph nodes atıer
ım-munizaıiOlI wiıh horseradish pemxida.w J Hisıochem
Cytochem, 30. 67-74.
16. Eikelenboom P, Levenbaeh :vıGE, Van den Brink HR, Streefkerk .lG (1979) Developmenı or T and II
cells areas in peripheral Iymphoid organs or ıhe ml
Anal Rec, 194.523-538.
17. Fagerland .lA, Arp LH (1990) A morp/ıo/()gıe SILah
orhrOlıchu.l-associl/ıed Iymphoid lissLle iıı turkeys. Am
J Anal. 189, 24-34.
18. Fix AS, Arp LH (1989) C'JIljwıclivl/-dSSociaıed
l\'mphoid Ti.ısue (CALT) in nonnal and hordelpila
aviUln-inl;'eıed ıurkey.ı. Veı PalhaL, 26. 222-DO.
19. Fix AS, Arp LH (
ı
991) Morphologic ch({rw;ıeriwııon (ır eonjUlıctiva-associaled Iymp/ıoid ıissue ilı e/ıickmsAm J Vet Re". 5,1852-1859.
20. Franklin RM, Remus LE (1984) ConILlncıivcı/-associaled Iymphoid ıissue: evidmce 101' ({mil" in ıhe
secreıory immuııe sysıem. Inv Ophıhalmol Vis Sci. 25.
181-187.
21. Gastkemper NA, Wubbena AS, Bimbrere FJH, De Graff A, Nieuwenhuis P (1981) Cenninul anlers
and ıht' B ceil syslem. V. Presl'nce o/ Kerminl/I cenTer
precursor ails ammıg Iymphocyıes oL ıhp ıhoracic
ducı in the mt. Cell Tissue Re". 219 . 281-289.
22. Goller Th, Weyraueh KD (1993) Ol/s
Kon-jUlıkıivalepiıhel des HUlıdes. Uehı- und
elekı-roııenmikmskopische Unıersuc/ıUlıgeJl. Ann Anat. 175.
A:\IKARA KEÇiLERININ KONJUNKTIVA ILE ILIŞKILI LENFOlD DOKUSU (CALT) ÜZERINDE IŞIK MIKROSKOBIK ÇALIŞMALAR
37
23. Gutman GA, Weissman IL (ı972) Lymphoid tissue
urchiteeture. Experimentul unulysis of the origin und
dıstrihutiıill of T cells und II cells. Immunology, 23,
465-479
24. Higgy KE, Burns Gl', Hayhoe FG (1977)
Disc-riminutwn of 8. T und Null Iymphocytes by esteruse
cywchemistı}'. Scand J Ilaematol, LS, 437-448.
25. Knowles DM, Hoffman '1', Ferrarini M, Kunkel HG
(1978) The demıııısıralion of acid alphu nuphthyl
uce-[(ıle ntemse activitv in humun Iymphocyıes usefulness
us a T cell marka. Cell Immun; 35, i i2-i23.
26. Maslak DM, Reynolds DL (I 995) B cells and
T-Iymphocyte subsets of the head-assoCıuted Iymphoid
ıissues ofthe chiekel1. Avian Dis, 39, 736-742. 27. MueIler J, Brundel Re G, Buerki H, KeIler HU,
Gottier H (1975) Nonspecijic ucid estaase activity : u
eriterionp)r difterentiation of T und B iymphocytes in
mouse iymph nodes. Eur J Immunol, S,270-274,
28. MüIler HK, Heusermann U, Stutte HJ (1974)
Enz-vme histochemicai ohservatio/lS on the iocaiizatimı
and strueture of the T eell and II eell regions in the
humun spleen. Cell TissL1e Res, 154,167-179.
29. MüIler .I, KeIler HU, Hagmann JD, Cornioley RJ, Ruchti C, Gottier H (1981) Nonspesijic estaruse in
human lrmphocytes. int Areh Allergy Appl, 64, 4
ı()-421.
3().Parsons KR, B1and AP, Haıı GA (I 991) Follicle
as-",cialed epıthelium o{ the Mut assocluted Iymphoid tis-sue ofU/ltle. Vet Pathol, 211.22-29.
31. Reynolds JD, Morris B (1983) The evoiwilJll und
in-voiutimı of Peyer's putches in tetal and postnalal
sheep. Eur J Immunol, 13.627-635.
32. Sminia '1', Janse EM, Plcsch BEC. (I 983) OnwMen\"
ofPeyer's patches o/the rat Anat Rec, 207, 3()9-316.
33. Sousa M, Freitas A, Huber B, Cantor H, Boyse EA (I 979) MiKruıory putterns of the iy suhsets o{ T
iymphocytes in the mouse. Adv Exp Med Biol. 114.
51-54.
34. Stock EL, Sobut RA, Roth SI (1987) The upwke o{
horseradish pemxiduse hy the cılııjunctival/:'pitiıe!ıUln
ı~tthe guinea-pi/:. Exp Eye Res. 45.327-337.
35. Weldman JE, Keuning F.I, Molenaar i (1978) Sit/:'
o(iniıiution otpiasma cell reactimı /LL th/:' rahhitiympiı
node Uitrastructural evidence p)r two distinet
(//1-tihody ti)rming celi precursor.\. Wirchows Arch (Cell
Pathol), 28, 187-202.
36. Wolf.l L, Bye WA (1984) The membrwlOUS epithe!ıai
(M) cell und the mucosui immune system. Ann Rev
Med, 35. 95-1 12.
37. Wotherspoon AC, Hardman-Lea S, Isaacson PG
(1994) Mucosu-ussociated Iymphoid tissu/:' (MALT) in the human cOlıjunetiva. J Pathol. 174,33-37.
Yazışma adresi:
Prı~t: Dr. Reşat Nuri AŞTı AÜ Veteriner Fuküitesi
Histoioji-Embriyoioji Anahilim Dulı