T.C.
EGE ÜNİVERSİTESİ TIP FAKÜLTESİ TEMEL TIP BİLİMLERİ BÖLÜMÜ TIBBİ BİYOKİMYA ANABİLİM DALI
KLİNİK REMİSYONDAKİ CROHN HASTALARINDA İNFLAMATUVAR BELİRTEÇLERİN HASTALIK AKTİVİTE VE REKÜRENSİNDEKİ YERİ
TIPTA UZMANLIK TEZİ
Dr. Günel HASANOVA
DANIŞMAN
Doç. Dr. Burcu BARUTÇUOĞLU
İZMİR
Bu çalışma EÜTF Bilimsel Araştırma Projeleri Alt Komisyonu tarafından desteklenmiştir. Proje No: 2016-TIP-083
i
TEŞEKKÜR
Ege Üniversitesi Tıp Fakültesi Tıbbi Biyokimya Anabilim Dalı ve Klinik Biyokimya Bilim Dalı’ndaki uzmanlık eğitimim süresince tecrübe, bilgi ve emeğini hoşgörü ile paylaşan ve bana her konuda destek olan değerli hocam ve tez danışmanım Doç. Dr. Burcu Barutçuoğlu’na,
Bilgi, deneyim ve desteklerini özveriyle aktaran değerli hocalarım Prof. Dr. Dilek Özmen’e, Prof. Dr. Eser Sözmen’e, Prof. Dr. Sara Habif’e, Prof. Dr. Işıl Mutaf’a, Prof. Dr. Ceyda Kabaroğlu’na, Prof. Dr. Ferhan Sağın’a, Prof. Dr. Gülinnaz Ercan’a, Prof. Dr. Yasemin Akçay’a, Prof. Dr. Zuhal Parıldar’a, Doç. Dr. Güneş Başol’a, Doç. Dr. Ali Mert Özgönül’e ve Doç. Dr. Ebru Sezer’e, ayrıca EÜTF İç Hastalıkları Anabilim Dalı, Gastroenteroloji Bilim Dalı’ndan Uz. Dr. Nalan Gülşen ÜNAL 'a,
Uzmanlık eğitimim boyunca beraber çalıştığım uzman, asistan ve teknisyen arkadaşlarıma ve diğer çalışanlara,
En içten sevgi, saygı ve teşekkürlerimi sunarım.
ii
ÖZET
İnflamatuvar barsak hastalıkları, genetik olarak yatkın kişilerde, nedeni ve mekanizması tam olarak bilinmeyen, kronik seyirli, remisyon ve alevlenme dönemleriyle karakterize inflamatuvar bir hastalık grubudur. İnflamatuvar barsak hastalıkları Crohn hastalığı gibi önemli hastalığı da içermektedir. Crohn hastalığı transmural tutulum ile gastrointestinal sistemin herhangi bir bölgesini etkileyebilen, nedeni bilinmeyen immunite temelli inflamatuvar bir hastalıktır. Bu hastalarda; hastalık aktivitesinin değerlendirilmesi, tedavinin şekillendirilmesi için birçok klinik aktivite göstergesi ve girişimsel olmayan belirteçler kullanılmış, fakat hiçbiri inflamatuvar aktivitenin saptanmasında histopatolojik ve endoskopik incelemeler kadar kesin bulgu sağlamamıştır. İnflamatuvar aktiviteye karar vermek, hastalığa yaklaşımda ve tedaviyi şekillendirmede önemlidir. Bu nedenle yapılan çalışmalarda ideal bir hastalık belirteci bulunmaya çalışılmıştır. Crohn hastalığında hastalık aktivitesi klinik olarak hastanın Crohn hastalığı aktivite indeksi (CDAI) puanına göre belirlenir. Buna göre 150 puan altı remisyonda hastalık kabul edilir iken, 450 puan üzeri ciddi fulminan hastalık olarak değerlendirilir. Bu çalışmada, klinik remisyondaki Crohn Hastalarında, hastalık aktivitesini klinik semptomlar başlamadan önce biyokimyasal belirteçler ile öngörebilmeyi ve ideal belirteci bulma amaçlandı. Çalışmaya Ege Üniversitesi Tıp Fakültesi İç Hastalıkları AD, Gastroenteroloji BD polikliniğine başvuran 12 asemptomatik, klinik remisyonda (CDAI <150) olan Crohn Hastası dahil edildi; ve tüm hastalarda polikliniğe başvurduğu gün CDAI puanı hesaplandı, alınan gaita örneklerinde fekal kalprotektin, laktoferrin, ve kan örneklerinde C reaktif protein (CRP), serum amiloid A (SAA), sedimantasyon ve tam kan saymı ölçümü yapıldı. Kolonoskopi sonucuna göre 5 hastanın remisyonda, 7 hastanın ise aktif dönemde olduğu saptandı. Aktif ve remisyondaki CH’ı arasında, fekal kalprotektin, laktoferrin, serum CRP ve SAA’da istatistiksel olarak anlamlı fark saptandı (p<0.050). Kolonoskopi gibi zahmetli ve invazif bir tetkikten önce mukozal inflamasyonu iyi yansıtan fekal kalprotektin ve/veya laktoferrin testlerinin uygulanması, kolonoskopiye gidecek hastaların daha iyi seçilebileceğini göstermektedir. İlgili literatürlerin ışığında daha büyük CH grubunda kapsamlı çalışmalar yapılması bu biyobelirteçlerin tanı ve takipte gücünü arttıracaktır.
iii
ABSTRACT
Inflammatory bowel disease is an inflammatory disease characterized by genetic predisposition, chronic illness, remission and exacerbation periods, whose cause and mechanism are not known precisely. Inflammatory bowel diseases also include important diseases such as Crohn's disease. Crohn's disease is an immunity-based inflammatory disease of unknown etiology that can affect any region of the gastrointestinal tract with transmural involvement. In these patients; many clinical activity indicators and noninvasive markers have been used to assess disease activity, shape the treatment, but none have been as accurate as histopathological and endoscopic examinations in detecting inflammatory activity. Deciding on inflammatory activity is important for approaching the disease and for shaping the treatment. For this reason, an attempt to find an ideal disease suspect has been tried. In Crohn's disease, disease activity is clinically determined by the patient's Crohn's disease activity index (CDAI) score. According to this, while it is accepted as a disease with less than 150 points remission, it is regarded as a serious fulminant disease over 450 points. In this study, in clinical remission of Crohn's disease, disease activity was aimed to be predicted by biochemical markers before the onset of clinical symptoms and to find an ideal locator. Twelve asymptomatic patients with Crohn's disease (CDAI <150) were included in our study, who were referred to Ege University Medical Faculty, the Department of Internal Medicine, Gastroenterology policlinics; and CDAI score was calculated on the day when all patients applied. C reactive protein (CRP), serum amyloid A (SAA), erytrocyte sedimentation rate, and complete blood count were measured in blood samples, and fecal calprotectin, lactoferrin in the gut samples. Colonoscopy revealed that 5 patients were in remission and 7 patients were active. Between active patients and patients in remission; statistically significant difference was found for fecal calprotectin, lactoferrin, serum CRP and SAA (p <0.050 for all). Fecal calprotectin and/or lactoferrin tests which reflect mucosal inflammation well should be performed before a troublesome and invasive test such as colonoscopy. Itis shown that patients who will undergo colonoscopy can be better selected. Comprehensive studies in larger groups of CH in the light of the relevant literature will increase the power of these biomarkers in diagnosis and follow-up.
iv İÇİNDEKİLER Sayfa TEŞEKKÜR ……… İ ÖZET………... ii ABSTRACT ……… iii İÇİNDEKİLER ………... iv KISALTMALAR……… ix ŞEKİLLER ……….. xi TABLOLAR ………... xii 1.GİRİŞ VE AMAÇ ………... 1 2.GENEL BİLGİLER……….... 3
2.1. İnflamatuvar Barsak Hastalıkları………... 3
2.1.1.İnflamatuvar Barsak Hastalıkları Tanımı………... 3
2.1.2. İnflamatuvar Barsak Hastalıkları Epidemiyolojisi………... 4
2.1.3. İnflamatuvar Barsak Hastalıkları Tanısı………... 4
2.1.4.İnflamatuvar Barsak Hastalıklarının Sınıflandırması………... 4
2.1.4.1 Ülseratif Kolit...………... 4
2.1.4.2 Crohn Hastalığı...………... 4
2.2. Ülseratif Kolit………... 5
2.2.1. Ülseratif Kolit Tanımı ve Önemi...………. 5
2.2.2. Ülseratif Kolit Prevelansı.………..………... 5
2.2.3. Ülseratif Kolit Patogenezi………..………... 6
2.3. Crohn Hastalığı…...………... 7
2.3.1. Crohn Hastalığının Tanımı ve Önemi………... 7
v
2.4. Fekal Kalprotektin………….………...………... 11
2.4.1. Fekal Kalprotektin Molekül Yapısı………... 11
2.4.2. Fekal Kalprotektin Etki Mekanizması...……... 11
2.4.3. Fekal Kalprotektin Ölçümü………...………... 13
2.5. Fekal Laktoferrin……… 13
2.5.1. Fekal Laktoferrin Molekül Yapısı………... 13
2.5.2. Fekal Laktoferrin Etki Mekanizması………... 13
2.5.3. Fekal Laktoferrin Ölçümü………... 14
2.6. CRP……… 15
2.6.1. CRP Molekül Yapısı……… 15
2.6.2. CRP Etki Mekanizması……….. 15
2.6.3. CRP Ölçümü……….. 16
2.7. Serum Amilodi A……….. 16
2.7.1. Serum Amilodi A Molekül Yapısı……….. 16
2.7.2. Serum Amilodi A Etki Mekanizması………. 16
2.7.3. Serum Amilodi A Ölçümü……….. 17
2.8. Eritrosit Sedimentasyon Hızı.……… 17
2.9. Tam kan sayımı……….. 18
3. ARAÇ, GEREÇ VE YÖNTEMLER………... 19
3.1. Çalışma Gruplarının Oluşturulması ve Çalışma Düzeni ...………….…………... 19
3.1.1. Çalışmaya Alınma Kriterleri……..……...………... 19
3.1.2. Çalışmadan Dışlanma Kriterleri.……….…… 19
3.1.3. CDAI Puan Hesaplaması.……….……... 20
3.2. Kolonoskopi İle Saptanan CH Aktivite İndeksleri………..…………... 22
3.2.1.Basit Endoskopik Skor(SES) ve Rutgeert Skor İndeksi... 22
vi
3.3.1. Fekal Kalrptektin Feçes Örnek Hazırlığı..…... 23
3.3.2. Fekal Laktoferrin Feçes Örnek Hazırlığı... 24
3.4. Araç ve Gereçler………. 24
3.4.1. Cihazlar ve Sarf Malzemeleri……….. 24
3.4.2. Hazır Kitler……….. 25 3.5. Biyokimyasal Analizler………. 25 3.5.1. Fekal Kalprotektin Ölçümü………. 25 3.5.2. Fekal Laktoferrin Ölçümü………... 26 3.5.3. CRP ölçümü………. 28 3.5.4. SAA Ölçümü……… 28 3.5.5. Eritrosit Sedimentasyon Hızı Ölçümü………. 28
3.5.6. Tam Kan Sayımında Hematokrit ve Lökosit Ölçümü………. 28
3.6. İstatistiksel Analiz………. 28
4. BULGULAR………... 30
4.1. Demografik Veriler……….. 30
4.2.Olguların Ölçülen Biyokimyasal Verileri………. 32
4.3. Dağılım Grafikleri………. 33
4.4. Hastalık Aktivitesi, CDAI ve Biyokimyasal Parametreler Arası İlişki………. 36
4.5. Korelasyon Analizleri……… 37
5.TARTIŞMA ………. 38
KAYNAKLAR……….... 43
EKLER………. 49
EK 1: Olgu Rapor ………... 52
vii
KISALTMALAR
6-MP : 6-merkaptopurin
AZA : Azatioprin
BT : Bilgisayarlı Tomografi
CDAI : Crohn Hastalığı Aktivite İndeksi
CH : Crohn Hastalığı
CRP : C Reaktif Protein
CV : Değişkenlik Katsayısı
Da : Dalton
ELISA : Enzyme Linked Immunosorbent Assay ERCP : Ensokopik Retrogard Kolanjio Pankreatografi ESR : Eritrosit Sedimentasyon Hızı
GİS : Gastro İntestinal Sistem HDL : High Density Lipoprotein
HIV : Human Immunodeficiency Virus
IBSEN : İnflamatuar Barsak Güney Doğu Norveç İBH : İnflamatuar Barsak Hastalığı
MCV : Ortalama Korpuskuler Hacim
MR : Manyetik Rezonans
NSAID : Non Steroidal Anti İnflamatuar İlaç
PA : Fosfatidik Asit
PC : Fosfatidil Kolin
PPİ : Protein Pompa İnhibitörü
PSC : Primer Sklerozan Kolanjit
SAA : Serum Amiloid A
TPN : Total Parental Besleme
viii ŞEKİLLER
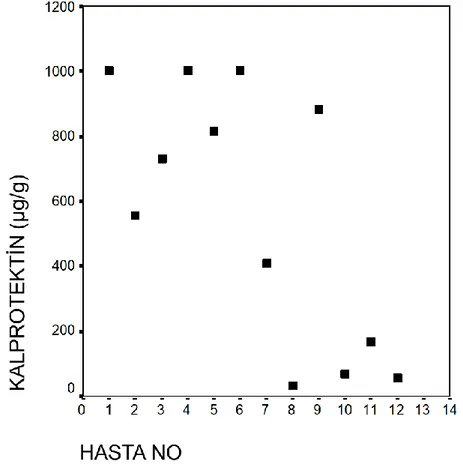
Şekil 1. Fekal kalprotektin hasta dağılımı………33
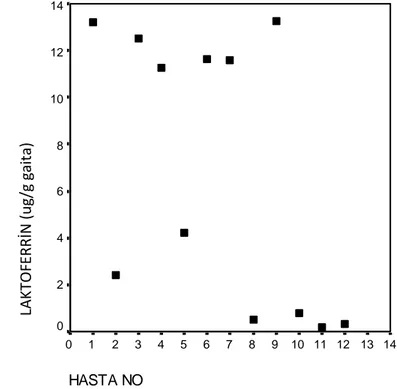
Şekil 2. Fekal laktoferrin hasta dağılımı………...34
Şekil 3: CRP hasta dağılımı……….34
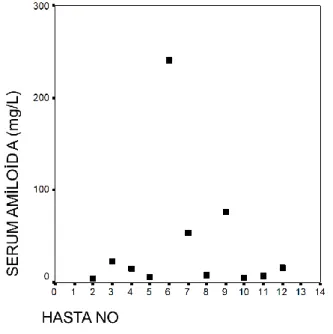
Şekil 4. Serum Amiloid A hasta dağılımı………35
ix TABLOLAR
Tablo 1. Endoskopik olarak doğrulanan aktif inflamatuvar bağırsak hastalığının
inflamatuar belirteçlerin duyarlılığı ve özgüllüğü………. 11
Tablo 2. Basit Endoskopik Skor (SES) indeksi………. 22
Tablo 3. Rutgeerts skor indeksi……… 23
Tablo 4. Standard hazırlığı ve konsantrasyonları……….. 27
Tablo 5. Hastalara ait demografik veriler……….. 30
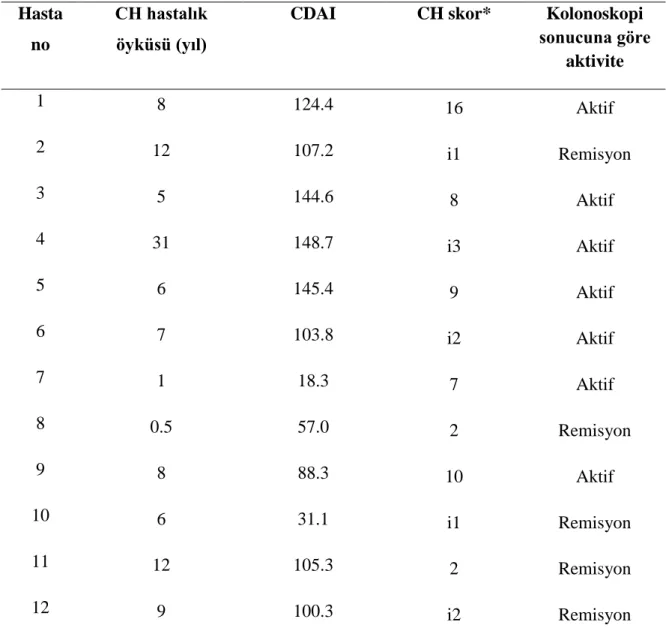
Tablo 6. Olguların hesaplanan CDAI leri, hastalık öyküsü süresi ve kolonoskopi sonuçları………. 31
Tablo 7. Biyokimyasal veriler………... 32
Tablo 8. Hastalık aktivitesi, CDAI ve biyokimyasal parmetreler arası ilişki……… 36
Tablo 9. CDAI, kolonoskopide elde edilen CH aktivite skoru ve biyokimyasal değişkenler arası anlamlı korelasyon gösterenler……….. 37
1
1. GİRİŞ VE AMAÇ
İnflamatuar bağırsak hastalığının iki klinik formu vardır: Ülseratif kolit (UK) ve Crohn hastalığı (CH). Crohn hastalığı karın ağrısı, şiddetli ishal, halsizlik, kilo kaybı ve malnütrisyona yol açabilen gastrointestinal sistemin inflamatuar bağırsak hastalığı (IBH) 'dir. Crohn hastalığında inflamasyonun şiddeti kişiler arası farklılıklar gösterebilir ve gastrointestinal sistemin farklı bölgelerinde lokalize olabilir. Crohn hastalığında bağırsak inflamasyonu, etkilenen bağırsak dokusunun katmanlarına sıklıkla yayılır.
Crohn hastalığı karın ağrısı ve kilo kaybına neden olabilir ve bazen yaşamı tehdit eden komplikasyonlar gelişebilir. Crohn hastalığı için bilinen bir tedavi bulunmamakla birlikte, tedaviler hastalık semptomlarını önemli ölçüde azaltabilir ve hatta uzun süreli remisyona neden olabilir. Crohn hastalığı, ağızdan anüse kadar tüm sindirim kanalını segmenter tarzda ve transmural olarak tutar. Sıklıkla görülen komplikasyonlar, cerrahi müdahale gerektirebilen intestinal darlık ve fistül gelişimidir. Ekstraintestinal tutulumlar sıklıkla görülür. Crohn hastalığı etyolojisi tam olarak anlaşılamamıştır ve medikal tedavi hastalık aktivitesinin kontrol altına alınmasında etkilidir, küratif değildir.
CH klinik tipleri penetran ve obstrüktif-stenozan olmak üzere ikiye ayrılır. Üçüncü grup olarak da CH seyri boyunca her iki klinik tipin de gelişmediği hastalar inflamatuvar tip olarak kabul edilir. İki klinik tip aynı hastada görülebilir. CH’da mukozal fissür, abse, fistüller, perianal hastalık, obstrüksiyon, kolon kanseri başta olmak üzere Hodgkin ve Non-Hodgkin lenfoma, vulva ve anal yassı hücreli karsinom gelişme riski de artmıştır. CH’ da hastalar arasında relaps sayısı açısından belirgin farklılıklar olmakla birlikte bazılarında sürekli bir kronik aktivite de olabilmektedir. CH ‘nın doğal seyrinde hastaların yaklaşık üçte ikisinde komplikasyon gelişmektedir. CH genetik heterojenitenin ve ciddi çevresel risk faktörlerinin patogeneze katkıda bulunduğu multifaktöryel bir hastalıktır.
UK ile CH ayırıcı tanısında endoskopik, radyolojik, histopatolojik incelemeler, laboratuvar testleri, hasta ve aile öyküsüne başvurulur.
Kalprotektin antimikrobiyal ve antiproliferatif özellikleri olan ve esas olarak nötrofillerde bulunan kalsiyum bağlayıcı bir proteindir. İntestinal inflamasyonun klinik tanı ve izleminde kullanılacak ideal yöntemlerin girişimsel olmayan, kolay uygulanabilir, tekrarlanabilir ve ucuz; intestinal hastalık aktivitesini göstermede özgül ve duyarlı bir testtir. İBH’da fekal kalprotektin konsantrasyonunda yükselme olduğu bilinmektedir.
2
Laktoferrin demir bağlayan bir glikoprotein olup örneğin süt, gözyaşı, sinoviyal sıvı ve serum gibi birçok vücut sıvısında bulunabilir. Özellikle polimorfnüveli lökositlerde bulunan sekonder granüllerin temel bileşeni olup birçok mukozal membranlardan salınır. Sekonder granüller özellikle inflamatuvar olaylarda salındığı için laktoferrin doğumsal immünitede bakterisidal olarak önemli rol oynar. İntestinal inflamasyonda polimorfnüveli lökositler barsak duvarını infiltre eder bu nedenle fekal konsantrasyonu inflamatuvar barsak hastalıklarında yükselmesi beklenir.
Bu çalışmanın klinik olarak remisyondaki Crohn hastalarında gaitada kalprotektin, laktoferrin ve serum C reaktif protein (CRP), serum amiloid A(SAA) gibi inflamatuvar belirteçlerin hastalık aktivitesi ve rekürensi öngörmedeki yeri amaçlanmaktadır.
3
2. GENEL BİLGİLER 2.1. İNFLAMATUAR BARSAK HASTALIKLARI
2.1.1.İnflamatuar Barsak Hastalıkları Tanımı
İnflamatuar bağırsak hastalıkları (İBH), bilinen bir tedavisi olmayan gastrointestinal sisteminin (GİS) kronik seyirli, remisyon ve alevlenme dönemleriyle karakterize inflamatuar bir hastalık grubudur. GİS bilindiği gibi, ağızdan anüse kadar gıdaların sindirimi, besin maddelerinin alınması, kullanılamaz hale gelen maddelerin ve atıkların atılmasından sorumludur. GİS boyunca herhangi bir yere yayılmış olan inflamasyon bu normal süreci bozar. İBH genetik olarak yatkın kişilerde farklı şekillerde seyredebilir, çok acı verici ve yıkıcı olabilir ve bazen hayati tehlike oluşturabilir. İBH, Ülseratif kolit(UC) ve Crohn Hastalığı (CH) olarak iki gruba ayrılır. UK ve CH sindirim sisteminin herhangi bir yerinde inflamasyona neden olabilir[1,2,3,4].
2.1.2. İnflamatuar Barsak Hastalıkları Epidemiyolojisi
İBH’na yakalanan kişilerin çoğu çocukluk çağında (yaklaşık 13-18 yaş) olmak üzere, yaklaşık %25'ine yaşamlarının ilk 20 yılında tanı konur. İBH insidansı hayatın ikinci on yılı başılarında artar[2]. Yapılan çeşitli epidemiyolojik araştırmalarda, özellikle puberte döneminde İBH sıklığının artışı gözlenmektedir. Avrupa'da İBH'nın yıllık en yüksek insidansı, her 100.000 kişi içerisinde yılda 0,5 ile 10,6 arasında değişmektedir[3]. Kuzey Avrupa'daki toplam insidans oranları CH için her 100.000 kişide 6.3 ve UK için 11.4, Güney Avrupa’da ise bu oranlar 100.000 kişide 3,6 ve 8,0 olarak görülmektedir[4]. CH ile ilgili yapılan araştırmaların %75'inde ve UK'de yapılan çalışmaların %60'ında bölgeler arasında istatistiksel olarak anlamlı bir fark olduğu göstermiştir[5–9]. Molodecky ve arkadaşları, UK ve CH insidansının ve prevalansının farklı bölgeler ve zaman içinde karşılaştırıldığı sistematik bir inceleme yapmışlardır. Sonuçları IBH sıklığı ve prevalansının batı ülkelerinde, özellikle Kuzey Avrupa ve Kanada'da en yüksek olduğunu göstermiştir[6]. Kanada'da IBH görülme sıklığının en yüksek olduğu şehir olan Nova Scotia'da IBH insidansı ve prevalansı azalmaktadır[10]. IBH'nin azalmış insidansı, çevresel faktörler tarafından açıklanabilir.
4
2.1.3. İnflamatuar Barsak HastalıklarınınTanısı
İBH tanısı tüm belirti ve semptomların etyolojisi dışlandıktan sonra konabilmektedir. İBH tanısı için bir grup test ve prosedürden bir veya daha fazlasının sonuçları gereklidir. Tam kan sayımı veya bazı enfeksiyon testleri anemiyi incelemede ve/veya bakteriyel ve viral hastalıkları dışlamada kullanılabilir. Gaitada gizli kan testinden inflamatuar hastalıkların tanısında yararlanılabilmektedir. Endoskopik işlemler ile de tanı konulabilmektedir. Kolonoskopi, sigmoidoskopi, gastroskopi tanı araçları arasında yer almaktadır. Görüntüleme prosedürleri yine bir başka tanı yöntemidir. X ray, bilgisayarlı tomografi, manyetik rezonans gibi görüntüleme yöntemleri de İBH tanısını sağlayabilmektedir[11– 13].
2.1.4. İnflamatuar Barsak Hastalıklarının Sınıflandırılması
Birçok hastalık İBH şemsiyesi altında olup, en yaygın iki hastalık ülseratif kolit(UK) ve Crohn hastalığıdır(CH)[14]. CH sindirim sisteminin herhangi bir yerinde inflamasyona neden olabilir. UK ise kalın bağırsağın iltihabını içerir[15].
2.1.4.1. Ülseratif Kolit
Ülseratif kolit bir inflamatuar bağırsak hastalığıdır. Ülseratif kolit, kolon, rektum veya her ikisinin tutulduğu durumlarda oluşur. Bu inflamasyon iki nokta üstüste ülserler adlı küçük lezyonlar oluşturur[16, 17]. Genellikle rektumda başlar ve yukarı doğru yayılır. Tüm kolon tutulumu olabilir. İnflamasyon, bağırsağın içeriğinin hızla ve sık sık boşaltmasına neden olur. Bağırsak yüzeyindeki hücreler ölürse, ülserler oluşur. Ülser kanama, mukus ve mide kesesi deşarjına neden olabilir. UK her yaştan insanı etkilemekle birlikte, çoğunlukla 15 - 35 yaşları arasında tanı konur. 50 yaşından sonra genellikle erkeklerde bu hastalığın teşhisinde bir miktar daha artış görülür[15].
2.1.4.2. Crohn Hastalığı
CH, gastrointestinal sistemin ağızdan anüse kadar herhangi bir yerini etkileyebilen, tekrarlayıcı bir hastalıktır. UK'nin tersine, hastalık süreci transmuraldır, fistül, ülserasyon, apse ve darlık oluşumu mümkündür. Crohn cerrahisi, hastanın ömrü boyunca birden fazla defa operasyon geçirme riski öngörülerek dikkatle düşünülmelidir. CH’nın % 70-90'ına yaşamları boyunca mutlaka cerrahi uygulanır[15]. Cerrahi müdahaleye çok dikkatli karar verilmeli ve bağırsak rezeksiyonları hastalık sürecini en aza indirgemelidir. Tekrarlayan rezeksiyonlar hastayı temel beslenme gereksinimlerini karşılamasını engeller ve ince
5
bağırsakların yetersiz dolması sendromu oluşabilir. Bu duruma kısa bağırsak sendromu denir. Hastada ömür boyu parenteral beslenme desteğine bağlayan bir bağırsak yetersizliği oluşur. Crohn cerrahisi, darlık, apse ve fistül gibi hastalığın komplikasyonları için uygulanmalıdır. Hastalık temizleme aracı olarak kullanılmamalıdır. İnce bağırsak rezeksiyonlarının uzunluğu asgari düzeyde tutulmalı ve mikroskobik olarak hastalığın marjinleri dahil rezeksiyonlar rekürrens riski taşımamalıdır[18].
2.2. Ülseratif Kolit
2.2.1 Ülseratif Kolit Tanımı ve Önemi
Yukarıda da belirtildiği gibi UK kalın bağırsağın inflamatuvar hastalığıdır. Genellikle bağırsağın alt kısmı (sigmoid kolon) ve rektumu etkiler. Fakat tüm kolon etkilenebilir. Genel olarak, etkilenen kalın bağırsak ne kadar fazla ise semptomlar o kadar kötü olur. Hastalık, her yaştan insanı etkileyebilir. Ancak nedeni tam olarak bilinmemekle birlikte, çoğu kişide 30 yaşından önce tanı konur. Sindirim sistemindeki normal bakterilere karşı aşırı yanıt veren immun sistemin nedeni olabileceğini düşünülmüştür. Ya da bazı bakteri ve virüsler neden olabilir. UK, diğer aile bireylerinde de görülebilir. Karın ağrısı veya kramplar, diyare, ve rektal kanama hastalığın etkileridir. Bazen ateş, iştahsızlık ve kilo verme de izlenebilir[19]. Ağır vakalarda, günde 10 - 20 kez ishale neden olabilir. UK aynı zamanda eklem ağrısı, göz veya karaciğer hastalıkları gibi başka sorunlara da neden olabilir[20]. Çoğu hastada semptomlar ara ara kendini gösterir. Bazen aylarca ya da yıllarca asemptomatik dönemler geçer. UK’li 100 kişiden yaklaşık 5 - 10'unda ise her zaman belirtiler görülür. Anamnez, fizik muayene ve birtakım testler ile CH, irritabl bağırsak sendromu ve divertikülit gibi benzer belirtilere neden olabilecek diğer sorunlar mutlaka ekarte edilmelidir[21]. Yapılabilecek testler arasında şunlar bulunur: Kolonoskopi, biyopsi, infeksiyon veya inflamasyona yönelik biyokimyasal testler. Kanama, enfeksiyon ve lökosit aramak için gaita testi yapılır.
2.2.2. Ülseratif Kolit Prevelansı
Dünya çapında UK'nin ortaya çıkışı son yıllarda artmıştır. Yayınlar, UK insidansının belirginleştiği veya azaldığı gelişmiş Kuzey Amerika ve Batı Avrupa ülkelerinin aksine, Latin Amerika, Asya ve Doğu Avrupa'daki gibi gelişmekte olan ülkelerde olgu sayısının arttığını gösteriyor. Bu bölgelerde artan insidansa rağmen, UK insidansında ve dünyadaki farklı bölgelerdeki prevalansa ilişkin hâlâ farklılıklar bulunmaktadır. UK görülme oranı, araştırılan nüfusa bağlı olarak, her yıl 100.000 kişi başına 0.5 - 31.5 arasında değişir.
6
Gelişmekte olan ülkelerde prevalans düşüktür. Örneğin, Asya popülasyonlarında, yaygınlık 100.000 kişi başına 5.3 - 63.6 arasında değişirken, Kuzey Amerika'da 100.000 kişi başına 37.5 - 238 arasında değişmektedir[8, 22, 23]. Batı’da ve Asya ülkelerinde UK görülme sıklığı arasındaki farka ek olarak, Avrupa'da, istisnalar olmasına rağmen, IBH sıklığı coğrafi farklar da vardır; İBH kuzeyde daha yüksek olup, güneyde daha düşük sıklıkta görülür. Benzer şekilde, Sonnenberg ve arkadaşları[24], Kuzey Amerika Birleşik Devletleri'nde ülkenin güneyine kıyasla daha yüksek IBH sıklığı saptamıştır. Latin Amerika'da UK prevalansı da değişkenlik göstermektedir. Porto Riko'da yapılan bir araştırma UK prevelansının her 100000 kişide 12.53 olduğunu göstermiştir. Victoria ve ark[25], Brezilya'nın güneydoğu bölgesindeki UK prevalansının son yıllarda arttığını ve 2001'den 2005 yılına kadar olan dönemde prevalansı 100.000 kişi başına 14.81 vakayla sonuçlandığını belirtmişlerdir.Önceki araştırmalara göre, UK'li hastaların mortalitesi, 20. yüzyılın ilk yarısında daha yüksekti. 1950'lerin ortalarından itibaren insidansa devam edilmesine rağmen muhtemelen kortikosteroidler ve sülfasalazinin kullanımı ve cerrahi tekniklerin optimizasyonu nedeniyle ölümlerin sayısında bir düşüş olduğu görülmektedir. Bu ilerlemeye rağmen, 1980'lerde yayınlanan veriler UK'deki mortalitenin genel nüfustan daha yüksek olduğunu göstermiştir. Neyse ki genel olarak UK'li bireylerin mortalite oranı genel popülasyondaki orana benzer veya sadece biraz daha yüksektir[15, 26–28]. Bu sonuç, diğer faktörlerin yanı sıra, son yıllarda immünsüpresif tedavinin kullanımının artmasının bir sonucu olabilir. Bununla birlikte, yalnızca UK nüfusu düşünüldüğünde, bazı alt gruplarda ve özellikle yeni teşhis edilen hastalarda ve geniş kolitli hastalarda mortalitenin daha yüksek olduğu açıktır[29].
2.2.3. Ülseratif Kolit Patogenezi
Ülseratif kolit (UK), inflamatuar bağırsak hastalığının (IBH) idiopatik formlarından biridir ve Crohn hastalığı (CH) ile bu tanımlamayı paylaşmaktadır. Ülseratif kolit, kolonun kronik, tekrarlayıcı bir inflamatuar hastalığıdır ve etkilenen hastalar çekumdan rektuma kadar inflamasyon gösterebilir. Semptomlar, karın ağrısı, yetersiz beslenme ve diyare gibi sıklıkla kanlı olabilir. Ülseratif kolitli hastalarda displazi ve kolon adenokarsinomu riski yüksektir ve yaşam boyu düzenli endoskopik gözlem gerektirirler[14, 26, 28]. Bu durumdaki hastaların yaklaşık% 25-30'unda, ilaçlarla tedavi başarısız olduğunda veya karsinoma için bir öncü lezyon olan displazi bulunursa, hayatlarının bir noktasında kolektomi yapılmasını gerektirecektir. Kolektomi ülseratif kolit için küratif olarak kabul edilir. Ülseratif kolit tedavisinin ayrıntılı bir açıklaması bu tartışmanın kapsamı dışındadır. Kısaca, tedavinin hedefleri semptomları azaltmak ve yaşam kalitesini arttırmaktır.
7
Terapötik müdahaleler, hastalık fişekleri süresince 1 veya daha fazla ilaç, beslenme modifikasyonu ve destekleyici bakım içerebilir. Buna ek olarak, etkilenen birçok hasta (% 25-30) hayatlarının bir noktasında ameliyat yapılmasını gerektirecektir.Kanlı ishal başlangıcının ilk 4 gününde mukozal ödem, akut kriptit, kript ülserleri ve apseler bulunur. Kanlı ishal başlangıcından yaklaşık bir hafta veya 9 gün sonra, klinik görünüm başlar ve histolojik olarak rejeneratif değişiklikler gösterir, mukus tükenmesi ile epitel ve kript epitel hücrelerinde artmış mitotik rakamlar görünebilir. Kriptitin kalıcı odakları da olabilir. Focal active colitis olarak adlandırdığımız bu daha sonraki bulgu, yanan CH ve/veya iskemi ile karıştırılabilir[28]. Kronik inflamatuvar bağırsak hastalığı öyküsü olmayan bir hastada fokal aktif kolit varlığı konservatif olarak yorumlanmalıdır çünkü vakaların büyük çoğunluğu kendine sınırlıdır. Fokal aktif kolit daha olasıdır Pediatrik hastalarda, özellikle genç olanlarda CH'ye sekonder olarak ortaya çıkmaktadır[29]. Fokal aktif kolit, sadece CH'de değil, aynı zamanda nonsteroidal anti-inflamatuar ilaç (NSAID) kullanımı, iskemi, enfeksiyonlar, kısmen tedavi edilen UK ve de neoplaziyi dışlamak için endoskopi yapılan hastalarda izole (tesadüfi) bir bulgu. Ne yazık ki, inflamasyonun miktarı, yeri veya dağılımı gibi, fokal aktif kolitin histolojik parametreleri, sonuçla ilişkili veya enflamatuar bağırsak hastalığı için yüksek riskli olanların seçimine izin veren özel histolojik parametreler bulunmamaktadır. Artmış lenfositler, nötrofiller, eozinofiller ve birkaç plazma hücresi bulunan bir hiper hücreli lamina propriasına sahip olabilir. Bu bulgu, patoloğu kronik kolit teşhisi için kandırmaya neden olabilir; Ancak, yakından incelendiğinde, bazal plazma hücreleri ve crypt bozulması mevcut olmayacaktır.Bazı yüzeyel epitel hasarının ve artmış intraepitelyal lenfositlerin varlığı bazen lenfositik kolit ile karıştırılabilir; Bununla birlikte, klinik bağlam genellikle karışıklığı önleyecek kadar farklıdır[30–32].
2.3. Crohn Hastalığı
2.3.1. Crohn Hastalığının Tanımı ve Önemi
Crohn hastalığı, bağırsak yolunun ağızdan rektuma devam eden inflamasyona neden olan kronik bir inflamatuvar durumdur. Bir başka inflamatuar barsak hastalığı olan ülseratif kolit benzerdir. Ancak ülseratif kolit genellikle kalın bağırsağın ve rektumun en içteki katmanı ile sınırlıdır. Crohn hastalığı bağırsağın herhangi bir yerinde, genellikle sağlıklı dokularla çevrili lekeler oluşabilir ve dokulara daha da yayılabilir. Semptomlar, kronik kanlı veya sulu diyare, karın ağrısı, ateş ve iştah kaybını içerir[33]. Hastalığın aktif hale gelmesi veya kişinin yaşamı boyunca birkaç kez remisyona girmesiyle birlikte belirtiler gelip gidebilir. Crohn hastalığı bağırsak tıkanıklığına, ülserlere (çoğunlukla ince bağırsağın
8
alt bölümünde, kalın bağırsakta veya rektumda), fistüllere (bağırsaklardan bir bölümden oyuk boşluklara) ve anal fissürlere neden olabilir. Buna ek olarak, Crohn hastalığı olan insanlar bağırsak yetersizliği riski altındadır, çünkü bağırsakları diyetlerinden ihtiyaç duydukları tüm besin maddelerini alamaz. Crohn, çoğunlukla 20 ila 40 yaşları arasında gelişir, ancak çocuklar ve yaşlı erişkinler de durumu geliştirebilir. Crohn hastalığının tedavisi yoktur. İlaç ve diyetler durumun kontrol edilmesine yardımcı olabilir ve bazen uzun süreli remisyona neden olabilir. Crohn hastalığı olan bazı insanlar sindirim sisteminin bir bölümünü çıkarmak için ameliyat gerektirebilir. Bununla birlikte, ameliyat hastalığı tedavi etmez[34–36].
2.3.2. Crohn Hastalığı Prevelansı
CHinsidansı incelenen bölgeye göre değişir. İngiltere, Kuzey Amerika ve Avrupa'nın kuzeyi en çok görülen bölgelerdir. 1997 yılındaki Danimarka'da yapılan bir araştırma, 100 000 kişiye yılda ortalama erkekler için insidans hızının 1981-1984'te 3,3 iken 1989-1992'de 4.1'e yükseldiğini bulmuştur. Aynı alandaki ve aynı zaman aralıklarındaki kadınlar için, insidans oranı 4.6'dan 6.2'ye yükselmiştir. 15-29 yaş grubunda erkekler arasında insidans hızı 5.3 ve kadınlarda 9.1 bulundu. 2000 ve 2007 yılları arasında Finlandiya'daki tüm yeni CH vakalarının dahil edildiği yakın tarihli bir araştırmada, 100.000 kişide 9.2'lik bir insidans oranı ortaya çıkmıştır. OlmstedCounty, Minnesota, Birleşik Devletlerde insidans hızı, 1940-1993 yılları arasında 100 000 kişi yılda 5.7 vaka idi. Çalışma süresi boyunca 1940-1943 arasında insidansın belirgin bir şekilde arttığı insidans hızı 1.0 iken, 1984'teki oran -1993, 6,9'du. Geleneksel olarak, Asya ve Afrika'da görülme sıklığı düşüktür. Bu alanlardaki çalışmalar, CH insidansının artmakta olduğunu göstermektedir. Avrupa’da CH prevalansı 100.000 kişide 10'dan 150'ye düşmektedir. 1991'de Amerika Birleşik Devletleri Minnesota'da 100 000'de düzeltilmiş bir prevalans%133 bulundu. Güney Kore'den yapılan bir araştırmada 11,2 prevalansının olduğu belirtilmiştir. Mevcut verilerden yola çıkarak, CH'nininsidans ve prevalans oranlarının son on yılda arttığını düşünebiliriz. Birleşik Krallık'tan CH tanısı konulan hastalar üzerine retrospektif bir çalışmada, hasta popülasyonu 1986-1991, 1992-1997 ve 1998-2003 yıllarında üç gruba ayrılmıştır. CH tanısı alan 341 denekten %62'si kadıntır. Tüm zaman aralıklarında tanıdakı medyan yaş 30 yıldır. Danimarka'dan gelecek prospektif bir çalışmada, 2003-2005 yılları arasında Kopenhag'da UK ve CH tanısı alan tüm hastalar 11,3 ay (medyan) takip edildi; CH hastalarının%54'ü kadın, tanıdaki medyan yaş 31 idi. OlmstedCounty, Minnesota, Birleşik Devletler'denretrospektif bir çalışma, hastaların%54'ünün kadın olduğunu ve tanıdaki medyan yaşın 29,5 yıl olduğunu gösterdi. Norveç'te, prospektif bir çalışmada,
9
İnflamatuvar Bağırsak Güneydoğu Norveç (IBSEN) grubu, 1990'lı yılların başından beri inflamatuvar barsak hastalığı (İBH) olan hastaları izlemiştir. Bu çalışma, kadın / erkek oranı 0.95 olan, CH tanısı alan kadınların hafif bir baskın olduğunu bildirmiştir. Tanıda medyan yaş 30 yıl idi. Finlandiya'da cinsiyetler arasında anlamlı bir fark bulunamadı. Nüfus temelli Kanadalı bir araştırmada kadınların yeniden düzenlenmesi bulundu: hastaların%58'i kadındı. Sigara içimi, CH gelişme riski ile ilişkilidir. Sigara, CH'nin klinik seyrini olumsuz yönde etkiler ve aynı zamanda CH hastalarında cerrahi rezeksiyon sonrası CH'nin klinik rekürrensi ile ilişkilidir. Sigara içmek, özellikle ağır sigara içmek, hastalığın şiddetlenme riskini belirgin biçimde artırmıştır. Bu çalışmalara dayanarak, sonuç, CH tanısı konan kadınlarda hafif bir baskınlık olduğu, teşhis çağındaki yaşın yaklaşık 30 olduğu ve CH'li hastalarda sigara içiminin zararlı olduğu sonucuna varılmıştır[37–40].
2.3.3. Crohn Hastalığı Patolojisi
Crohn hastalığı genellikle gençler ve yirmi yaşlarda başlar; ancak, hastaların altıda biri 15 yaşından önce var. Hastaların %90'dan fazlasının 40 yaşından önce belirtileri var. Hastalar çoğunlukla karın krampları, diyare, gecikmiş büyüme, kilo kaybı, ateş, anemi ile başvuruyor, sağ alt kadran abdominal kitle (ileal bölgede bir komplikasyon gelişirse) veya perianal fistül. Tipik olarak, ileit veya ileokolit bulunan hastalar, sinsi bir başlangıç ve belirli bir tanı almadan önce uzun bir seyir gösterir. Teşhis öncesi semptomların ortalama süresi ve tedavinin başlaması 2-2 ½ yıl sürer, ancak bu gecikme süresi, ultrasonografi ve bilgisayarlı tomografi (BT) gibi daha iyi görüntüleme teknikleriyle ve Crohn hastalığı için daha yüksek bir şüphe endeksi ile kısaltılmıştır. Crohn hastalığı, jejunoileit, ileit, ileokolit ve kolit gibi birkaç örüntü içerebilir. Her alt tipte farklı bir klinik sunum ve tipik bir seyir vardır. Jejunum ve ileumun iltihabı olan hastalar genellikle yemekten sonra kramp şeklinde karın ağrısı yaşarlar ve sonunda ishale neden olurlar. Birçoğu gençler veya genç erişkinler olan bu hastalar, artrit, ateş, cilt lezyonları ve büyümenin gecikmesi gibi göze çarpan ekstraintestinal belirtilere sahip olabilirler. Yemekten 1-2 saat sonra Ileitis rahatsızlığa neden olur. Hastalar rahatsızlığı önlemek için daha az yemek yediğinden kilo verirler. İleumdaki inflamasyon, transmural olarak izler veya fistüller olarak bitişik yapılara kadar uzanabilir veya barsağa komşu apselerin delinmesine neden olabilir. Crohn hastalığının bu formu, fistül oluşturan veya delici olarak bilinir. Tüm formların en kötü prognozuna sahiptir ve genellikle 3-4 yıl sonra cerrahi rezeksiyon gerektirir. İleitli diğer hastalar, kas hipertrofisi ve fibrozis bağırsağın lümenini daralttığından, hastalık başlangıcından 8-10 yıl sonra bağırsak tıkanıklığı gelişir. Crohn hastalığının bu şekli daraltma veya stenozlanma
10
olarak bilinir. Kolonda Crohn hastalığı ishale neden olur ve ülseratif kolitten ayırt etmek zor olabilir. Crohn hastalığının klinik tablosu, bağırsağın bulunduğu alanlara bağlıdır. Ileal tutulumu olan hastalar, yemekten 1-2 saat sonra muğlak kramplayan karın ağrısı ile refah duygularında kademeli bir düşüş fark edebilir. Bağırsak lümeninin kısmi tıkanıklığı ve enflamasyonundan kaynaklanan bu rahatsızlık, periumbilikal bölgeye veya daha yaygın olarak sağ alt kadranda lokalize olabilir. Anoreksiya, mide bulantısı veya abdominal kramp korkusu nedeniyle hastalar daha az yemek yiyor ve kilo vermezler. İnce bağırsak Crohn hastalığı olan hastaların çoğunda bağırsak hareketleri sayısı artarken, nadiren günde beşten fazla olsa da yumuşak ve şekillendirilmemiş dışkılar var. Ileal hastalığı olan hastaların yaklaşık%80'inde ishal vardır. Crohn hastalığı bağırsak hastalığından daha sorunlu olabilen ekstrakstinal bulgularla ilişkilidir. Kolit artriti diz, ayak bilekleri, kalçalar, bilekleri ve Crohn hastalığına eşlik eden dirsekleri etkileyen bir göçmen artrittir (Crohn's ince bağırsağın içindeyken nadirdir). Sıklıkla eklem ağrısı, şişme ve sertlik bağırsak hastalığının seyrine paraleldir. Bağırsak hastalığının başarılı bir şekilde tedavisi artritsemptomlarında düzelme sağlar. Primer sklerozan kolanjit (PSC) ile birlikte görülen perikolangit, enflamatuvar bağırsak hastalığının en sık karaciğer komplikasyonudur. PSC, endoskopik retrograd kolanjio pankreatografi (ERCP) veya hepatik manyetik rezonans görüntüleme (MR) ile gösterilebilir. Perikolangit, portal yolların lenfosit ve eozinofilinfiltratlarla iltihabı ile karakterizedir. Safra kanallarında dejeneratif değişiklikler de karakteristiktir. Böbrek taşları (kalsiyum oksalat taşları) ince bağırsak Crohn hastalığında görülür. Bağırsaktan gelen inflamasyon, üriner sistem komplikasyonlarına neden olabilir. Obstrüksiyon ve hidronefroza yol açan üreterlerin tıkanması, genellikle Crohn hastalarında doğru üretere uygulanır. Fistül, inflamasyonlu bağırsak ve mesane arasındaki enfeksiyona neden olabilir. Crohn hastalığının patogenezini ve karakteristik enflamatuvar paterni açıklayan hiçbir birleştirilmiş hipotez yoktur. Tipik olarak, mukozada fokal inflamatuvar koleksiyonlar ve aflıt ülserler transmural inflamasyona kadar ilerlemektedir. Fistülizasyon hastalığı olan hastaların belirgin bir hastalığa sahip olup olmadıkları veya sitokin cevabının inflamasyon sürecini bağırsak duvarı ile sınırlayamayacakları olup olmadığı bilinmemektedir. İleokolonik rezeksiyon sonrası, neoterminalileumda, ancak luminal akım ve kolonik içerikler ve belki de bakterilerle temas olduğunda hastalık tekrar eder. Aksine, dışkı akışı yönlendirildiğinde veya bağırsak bir element diyeti veya total parenteral beslenme (TPN) ile dinlendiğinde inflamasyon azalır[36, 38, 41, 42].Bağırsaktan gelen enfeksiyöz bir ajanın veya antijenin, belki de bağırsak bakteri florasıyla uyumlu olarak, genetik olarak yatkın bir konakçıya, aşağı regüle edemeyen bir enflamatuar yanıt oluşturması
11
mümkündür. Ayrıca, inflamasyon sürecinin segmental dağılımı, ileumun son kısmı ve sağ kolon için öngörüsü, hastalığa yakalanma ya da rezeke edildikten sonraki yıllar tekrarlama eğilimi ve perianal hastalık sıklığı henüz açıklanamamıştır.
2.4. Fekal Kalprotektin
2.4.1. Fekal Kalprotektin Tanımı
Kalprotektin, özellikle nötrofiller olmak üzere lökositlerde bulunan S100 A8 / A9'un bir heterodimeri olan çinko bağlayıcı proteinlerden S100 ailesinin üyesi bir proteindir. Kalprotektin, kalsiyuma bağlanır ve bağırsaklarda parçalanmaz. Nötrofillerde sitozolün protein içeriğinin ~%60'ına katkıda bulunur[43–45].
2.4.2. Fekal Kalprotektin Etki Mekanizması
İnflamasyona neden olan bağırsak hastalıklarında bağırsaktaki artan nötrofil sayısı fekal kalprotektinde artışa neden olur. Bu nedenle, bağırsakta inflamasyon belirteci olarak kullanılabilir.
Monositlerde ve makrofajlarda nötrofillere kıyasla daha düşük konsantrasyonlarda bulunan kalprotektin antimikrobik özelliklere sahiptir. Bağırsaklarda aktif inflamasyon varlığında, nötrofiller dolaşımdan bağırsak mukozasına göç eder. İnflamatuar süreçten dolayı mukozal yapıda oluşan bozukluk, nötrofillerin ve dolayısıyla da kalprotektinin lümen içine kaçmasına ve bunun ardından dışkıyla atılmasına yol açar. Dışkıdaki kalprotektin konsantrasyonunun "altın standart" olan İndiyum 111 işaretli lökosit sintigrafisi testi ile saptanan bağırsak inflamasyon şiddeti ile iyi korele olduğu gösterilmiştir.
Kalprotektin dışkıda homojen olarak dağılır ve oda sıcaklığında 7 gün boyunca stabildir. Aktif UK'li, toplam 287 dışkı örneği toplanan 18 hastada yapılan bir çalışmada, oda sıcaklığında 3. günde konsantrasyonda azalma başlamış, ancak 7 gün sonra ortalama %28'lik bir azalma ile kalprotektin konsantrasyonunda anlamlı bir değişiklik olmamıştır. Bununla birlikte, bireyler arasındaki dışkıda kalprotektin konsantrasyonlarında günlük değişiklikler olabilir. Kolonoskopide normal bulguları olan, her biri 8 defa dışkı örneği veren 14 kişide yapılan bir çalışmada, değişkenlik katsayısı (CV) %58 bulunmuştur. Remisyonda CH olan 143 hastanın katıldığı bir çalışmada, hastaların sadece %16'sında üç numuneden daha fazla alınan örnekte kalprotektin konsantrasyonu için bireysel değişkenlik saptanmıştır. Dışkıda kalprotektin konsantrasyonları yaşa göre de değişebilir.
12
Yenidoğanlarda fekal kalprotektin konsantrasyonları daha yüksektir ve 5 yaşına kadar azalarak yetişkin değerlerine gerilemektedir[14, 43–46].
Fekal kalprotektin bireylerde günden güne değişebileceği düşünülmüş ve ideal olarak nasıl örnek toplanması gerektiği ile ilgili çalışmalar yapılmştır. Naismith ve ark. CH'li 143 hastadan üç gün üst üste alınan dışkı örneklerinde ve gün içinde alınan örneklerde değişimlerin düşük olduğunu göstererek, klinik kararların tek bir kalprotektin sonucu üzerinden yapılabileceği sonucuna varmışlardır. Özellikle de değişkenlik çoğunlukla yüksek seviyelerde, sınır bölgesi 50-200 mg/L değerlerinde daha az olduğunu göstermişlerdir[47].
Non-steroidal anti-inflamatuar ilaçların (NSAID'ler) alınmasından yanlış pozitiflikler olabilir, ancak hastalardan kalprotektin testinden önce ilaç almayı keserek bu önlenebilir. İBH'lı kişilerde ve genel popülasyonda ilaç kullanımını karşılaştıran Finlandiya’da yapılan araştırmada, İBH olan kişilerde proton pompa inhibitörlerinin (PPİ'ler) kullanımı kalprotektin düzeylerini yaklaşık dört kat arttırmıştır. Bununla birlikte, NSAID'lerin kullanımında kalprotektinde hafif bir artış saptanmıştır. Bununla birlikte, tüm çalışmalar NSAİ'ler ile artış bildirmemiştir. Demir ve ark, sınırda kalprotektin düzeyleri (> 50 ancak <150 g / g) olanlarda yapılan bir çalışmada, NSAID ilaç kullanımı ile anlamlı bir fark bulamamıştır[48]. Tersine, Turvill ve ark, birinci basamaktan bağırsak belirtileri ile başvuran ve kalprotektini ölçülen kişilerin %14'ünde NSAID enteropatininn nihai teşhisi olduğunu bildirmiştir[49].
Akciğer enfeksiyonlarından sonra (yutulan balgamdaki beyaz kan hücreleri nedeniyle) veya bağırsağa kanamalardan sonra yanlış pozitiflikler de olabilir. Fekal kalprotektinin rolü, hafif gastrointestinal semptomları olan kişilerde (ağrı, şişkinlik, diyare, bağırsak alışkanlığındaki değişim) inflamatuvar ve inflamatuvar olmayan hastalıkların ayırımında yardımcı olmaktır.
2.4.3. Fekal Kalprotektin Ölçümü
Dışkıda kalprotektinin seviyesini saptamak veya ölçmek için çeşitli testler yapılmaktadır. Røseth ve ark, 1992 yılında ilk ekstraksiyon ve ELİSA ile ölçüm yöntemini geliştirmişlerdir [50]. 2000 yılında, Tøn ve arkadaşları tarafından daha basitleştirilmiş extraksiyon yöntemi geliştirilmiştir[51]. Sonuç olarak, çeşitli ticari ELİSA kitleri kullanarak yapılan çalışmalar ile saptanan cut off değerlerine bağlı olarak % 80 - 90
13
arasında değişen duyarlılık ve özgüllükler saptanmıştır[52]. Son yıllarda ekstraksiyon aşamasını basitleştirmek için tek kullanımlık ekstraksiyon cihazları geliştirilmiştir, böylece volümetrik bir yöntemle bu örnekler analiz edilebilmiştir.
2.5. Fekal Laktoferrin
2.5.1. Fekal Laktoferrin Molekül Yapısı
Laktoferrin, transferrin protein ailesi içinde yer alan, başta süt olmak üzere birçok sıvıda bulunan, 80 kDa'lık, demir bağlayan bir glikoproteindir. Laktoferrin, nötrofillerin sekonder granüllerinin önemli bir bileşenidir.
Transferrin ailesi içinde yer alan tüm proteinler karbonik anhidraz inhibitörleri olup demir taşınmasında rol oynamaktadırlar. İlk olarak inek sütünden izole edildiği için bu isimle anılan laktoferrin, sadece süte özgü bir protein değildir.
2.5.2. Fekal Laktoferrin Etki Mekanizması
Laktoferrinin antibakteriyal, antifungal, antiviral, antiprotozoal, antioksidan, antikanserojen, sağlıklı kemik yapısı, bağırsakta demir absorpsiyonunu düzenleyici, antienflamatuar, immünomodulatör gibi birçok biyolojik aktiviteye sahip olup; çok fonksiyonlu bir protein olarak değerlendirilmektedir. Bağırsak inflamasyonunda, mukozanın lökosit infiltrasyonu dışkıda laktoferrin konsantrasyonunda artışa neden olur. Nötrofillerin sekonder granülositleri içerisinde bulunur ancak aynı zamanda göz yaşı, sinoviyal sıvı, anne sütü ve tükrük de bulunur. Ayrıca antimikrobiyal etkiye sahiptir, demir içeren mikroorganizmalara bağlanmakta ve bu nedenle aç bırakmaktır. Bakteri, mantar ve virüslere karşı aktiftir. Viral enfeksiyonlarda, virüsün konakçı hücre içine girmesini önlediği düşünülmektedir ve rotavirüs, respiratuvar sinsityal virüsü, herpes virüslerinin yanı sıra sitomegalovirüs ve HIV'e karşı da aktiftir[21, 53, 54].
İki demir bağlama bölgesi içeren laktoferrinin Fe+3’e affinitesi çok yüksek olup laktoferrinin demiri bağlama stabilitesi geniş bir pH aralığına sahiptir. pH=3 gibi kuvvetli asidik durumlarda dahi demiri tutabilmesi nedeniyle mide asitliğinden olumsuz etkilenmemektedir[55].
Kalprotektin gibi laktoferrin de nonspesifiktir. Aktif İBH dışında infektif diyare, kolon kanseri gibi diğer bazı bozukluklarda veya NSAID ilaçların kullanımından sonra artabilir. Laktoferrin daha çok nötrofil kaynaklı olmakla birlikte plazmada düşük miktarlarda
14
bulunmaktadır. Plazma laktoferrin düzeyi yüksek demir alımında, inflamasyonda, infeksiyöz hastalıklarda, tümör gelişiminde ve hamilelikte artmaktadır[55].
2.5.3. Fekal Laktoferrin Ölçümü
Laktoferrin protein yapılı bir molekül olduğundan konvasiyonel ELISA testleri ile belirlenebilmektedir. ELISA testinde Laktoferrin antikorları ile kaplı ELISA plağına uygulanan örnekler bu antikorlara bağlanır. Bu bağlanmadan sonra antikorlara bağlanmış laktoferrin üzerine ikincil bir antikor eklenir. Bu ikincil antikor horse radish peroksidaz veya alkalen fosfataz ile işaretlidir. Bu enzimlere substrat eklendiğinde zamana bağlı oluşan renk ile laktoferrin analizi yaılabilmektedir[51,52].
Laktoferrin antibakteriyel etkiye sahiptir ve dışkıda proteolize dirençlidir. Laktoferrin, ticari bir ELISA geliştirildiğinden ve günümüzde yaygın bir şekilde mevcut olduğundan, dışkıda 4 gün boyunca mükemmel bir kararlılığa sahip olduğu için basit ve ucuz teknikler kullanılarak tespit edilebilir. Negatif bir dışkı laktoferrin testi basitçe önemli nötrofilik bağırsak inflamasyonunun yokluğu anlamına gelir. Laktoferrin, demir bağlayıcı glikoproteinlerin transferin ailesinden biridir[56].
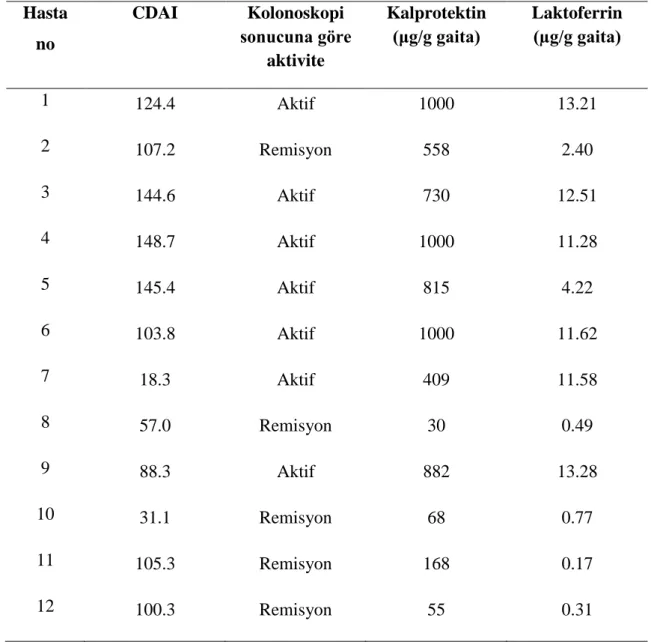
Kalprotektin ve laktoferrinin UK ve CH’daki duyarlılık ve özgüllü tablo 1 de verildi.
Tablo 1. Endoskopik olarak doğrulanan aktif inflamatuvar bağırsak hastalığının
inflamatuar belirteçlerin duyarlılığı ve özgüllüğü[56]
Test Duyarlılık (%95 güven aralığı) Özgüllük (%95 güven aralığı) CRP 49 (34-64) 92 (72-96) Kalprotektin 88 (84-90) 73 (66-79) UK’de Kalprotektin 79 (68-87) CH’da Kalprotektin 67 (58-75) Laktoferrin 82 (73-88 79 (62-89)
15
2.6.CRP
2.6.1 CRP Molekül Yapısı
CRP her biri 206 aminoasitten oluşan, 115 kDa'lık birbirine nonkovalan bağlı, beş adet alt üniteden (protomerden) meydana gelir. Bu şekilde beş alt üniteden oluşan proteinlere pentraksinler denilir. CRP gibi SAA proteini de bu gruba dahildir. CRP'ye ismi, Streptococcus pneumoniae'nın C-polisakkaridini presipite edebildiği için verilmiştir. CRP; infeksiyon, travma, inflamatuvar romatizmal ve malign hastalıklarda inflamasyonu en iyi gösteren testtir[52]. CRP 1930'da keşfedilmiştir ve isimi, Streptococcus pneumoniae'nın C-polisakkaridini presipite edebildiği için verilmiştir. CRP, çok az ya da hiç karbonhidrat içermez ve karaciğerde sentezlenir. CRP sentezi interlökin-6 tarafından kontrol edilir ve birçok bakteri, mantar ve protozoal parazitlerin yanı sıra histonlardaki polisakkaritlere bağlanır[57].
2.6.2. CRP Etki Mekanizması
CRP, inflamatuar proçeste, özellikle enfeksiyona karşı oluşan nonspesifik savunmada önemli bir role sahiptir. İnflamasyon sonrasındaki parçalanmış dokulara bağlanmaktadır. CRP; C1q aktivasyonu ile başlayan klasik kompleman yolunu aktive ederek C3b aracılı reseptörler ile aktive olan fagositozu başlatır. Bir komplement inhibitör faktörü olan ‘CRP bağlayıcı faktör H’ ile kompleks oluşturarak geç kompleman aktivasyon komplekslerinin (C5-C9) azalmasına yol açar ve alternatif kompleman yolağına pozitif feedback sağlar. CRP, bakterilerin artmış opsonizasyonu sonucunda fagasitoza uğraması ile katabolize edilir. Yinede CRP katabolizması tam olarak aydınlatılamamıştır. Benzer tipteki proteinler kalsiyum temelli bağlanma ile C-polisakkaridine bağlanırlar[57].
C-reaktif protein (CRP), inflamasyon sırasında artan ve kısa yarılanma ömrüne (19 saat) sahip akut faz proteini olup, inflamasyonun çözülmesinden sonra hızla düşmektedir. UK sürecinde bir biyobelirteç olarak serum CRP araştırılmış ancak tanısal tarama testi olarak yararlılığı tam olarak değerlendirilmemiştir. Bununla birlikte, CRP, CH'nin iki hastalığın en güçlü CRP tepkisine sahip olduğu IBD'yi saptamak için yetişkin popülasyondaki diğer biyolojik belirteçlere kıyasla en duyarlı tarama biyobelirteçidir. İki hastalık arasındaki bu farkın nedeni bilinmemektedir. Hem CH hastalar hem de UK hastaları, T-yardımcı-1 cevabına ait sitokin düzeylerinde artışa sahiptir[58].
16
2.6.3. CRP Ölçümü
CRP, miyokard enfarktüsü, stres, travma, enfeksiyon, inflamasyon, ameliyat veya neoplastik proliferasyondan sonra 2000 kat artan plazma seviyeleri ile akut faz reaktanlarınIn en hassas göstergelerinden biridir. Düzeyler viral enfeksiyona kıyasla bakteriyelde genel olarak daha yüksektir, ancak komplike olmayan influenza ve enfeksiyöz mononükleozda 100 mg/L'nin üzerindeki seviyeler görülebilir. İnflamasyon ile artış 6-12 saat içinde ortaya çıkar ve yaklaşık 48 saatte doruk noktalara ulaşır. Genellikle doku hasarının derecesi ile orantılıdır. Ancak artış nonspesifik olduğu için, başka klinik bilgiler olmaksızın yorumlanamaz. CRP yüksekliğinin saptanması organik bir hastalığın taranması, romatoid artrit gibi inflamatuar bir hastalığın aktivitesinin değerlendirilmesi, sistemik lupus erthematosus, lösemide veya cerrahiden sonra, böbrek allogreft alıcılarında rejeksiyonun saptanması enfeksiyon, neonatal septisemi ve menenjitte görülür. CRP yanıtının derecesi benzer bazı hastalıklarda farklılık gösterir. Örneğin, klinik olarak akut vekronikinflmatuarhastalıklarda CRP’nin 5-10 mg / L’nin üzerindeki düzeyde ölçülmesi anlamlı olup hastalık tedavisinde inflamasyon süreci izlenebilir.
CRP normal olarak plazmada 5 mg/L'den daha düşük bir konsantrasyonda mevcut olduğundan, ölçülmesi için oldukça hassas immünokimyasal yöntemler gereklidir. Mevcut tahliller, partikül uyarılmış immunoturbidimetri veya nefelometri, immünofloresans ve immünokemilüminesansı içerir. CRP referans aralığı erişkinlerde <5mg/L[57].
2.7. Serum Amiloid A
2.7.1. Serum Amiloid A Molekül Yapısı
İnsan serum amiloid A (SAA), inflamasyon sırasında bol miktarda artan bir akut faz proteini ailesidir. Akut faz yanıtında, SAA ağırlıklı olarak yüksek yoğunluklu lipoproteinler (HDL'ler) ile ilişkilidir. HDL'nin temel protein bileşeni, ters kolesterol taşıma yolunda rol oynayan bir antiaterojenik protein olan apolipoprotein (apo) A-I'dir. SAA'nın apoA-I'i bir dereceye kadar yerinden oynamakla yükümlü olduğu ve böylece kolesterol homeostazını etkilediği varsayılır[59].
2.7.2. Serum Amiloid A Etki Mekanizması
SAA (normalde 104 amino asit uzunluğunda), AA amiloidozlu hastalarda biriktirilen amiloid fibrillerin öncü proteinidir. Bu proteinin sürekli olarak yüksek bir konsantrasyonu
17
gerekli ancak amiloid fibriller oluşturmak için yeterli değildir. AA amiloidoz patogenezinde çeşitli faktörlerin rol aldığı düşünülmektedir. C-terminaliyle kesilmiş SAA (tipik olarak 76 amino asit uzunluğunda) ekstrasellüler matriste bulunduğu için SAA'nın proteolitik bölünmesi ve glikozaminoglikanların varlığının gerekli olduğu düşünülmektedir. Dahası, SAA izoformları (özellikle de SAA1.1, 1.3 ve 1.5 gibi SAA1 izoformlarındaki farklılıklar) AA amiloidoz riskini etkiler. Bununla birlikte, AA amiloidozunun altında yatan ayrıntılı patojenik mekanizmalar açıklanamamıştır. Amiloidojenik polipeptidlerin lipidlerle olan etkileşimlerinin amiloid fibril oluşumu üzerinde önemli etkileri olduğu düşünülmektedir. Özellikle, fosfatidilserin (PS) ve gangliozitler amiloid fibril oluşumunu etkiler. SAA ağırlıklı olarak HDL'ye bağlı plazmada dolaşıma girdiğinden, SAA'nın amiloid fibril oluşumu lipidlerden etkilenmelidir. HDL'nin başlıca fosfolipid bileşeni fosfatidilkolin (PC) olmasına rağmen, sayısız küçük fosfolipid türleri bulunur ve bileşimleri dolaşım sırasında değişir. HDL'de fosfatidik asit (PA) zenginleşmesinin kronik inflamatuar koşullar altında gerçekleştiği ortaya çıkmıştır[59, 60].
2.7.3. Serum Amilod A Ölçümü
Serum amiloid A (SAA), doku hasarı ve inflamasyonu için erken ve duyarlı bir kan biyobelirteçtir ve birçok inflamatuvar hastalıkta endikedir. Kanda dolaşan SAA seviyesinin, doku hasarına veya enflamasyona tepki olarak dramatik bir şekilde arttığı bilinmekte ve akut faz proteini olarak sınıflandırılmaktadır. Dolaşan SAA konsantrasyonları enflamasyon, enfeksiyon, doku hasarı ve hücre nekrozu sonrasında 1000 katına kadar artabilir ve iyileşme sonrasında hızla azalır.SAA örnek alındıktan sonra ELISA veya direkt doku üzerinde immünohistokimyasal ölçümle analiz edilebilmektedir[61, 62].
2.8. Eritrosit Sedimentasyon Hızı
Eritrosit sedimentasyon hızı(ESR), inflamasyonun başka bir nonspesifik markeridir. Orta derecede yükselmiş sonuçlar inflamasyon, anemi, enfeksiyon, gebelik ve yaşlanma ile ilişkilidir. İnflamasyon yokluğunda bile, inflamasyon, vaskülit, ciddi enfeksiyon ve multipl miyelom veya Waldenstrom makroglobulinemi ile ilişkili çok yüksek düzeyler vardır.Artmış ESR semptomatik kişilerde IBH tanısı için ılımlı duyarlılık (% 58-64) ve özgüllük (% 72-94) vardır.5,7 Dolayısıyla IBH semptomları olan bir hastada yüksek bir sonuç tanıyı destekler; Bununla birlikte, normal bir sonuç IBH'yi ekarte etmez[63–65].
18
2.9. Tam kan sayımı
Tam kan sayımı bileşenleri, hastalık aktivitesini ve demir veya vitamin eksikliğini gösterebilir. Aktif IBH hastalarında yüksek lökosit sayımı yaygındır ve mutlaka enfeksiyon anlamına gelmez. Marjinal nötrofillerin uyuşturucu kaynaklı mobilizasyonundan dolayı steroid alan hastalarda yüksek lökosit sayısı da sık görülür. Anemi, ya kronik hastalık anemisi [normal ortalama korpusküler hacim (MCV) ya da demir eksikliği anemisi (düşük MCV)] olarak yaygındır. Yüksek dereceli MCV (makrositoz), azatioprin (AZA) veya 6-merkaptopurin (6-MP) alan hastalarda ortaya çıkar. Trombosit sayısı, aktif inflamasyon veya demir eksikliği nedeniyle sıklıkla yükselmektedir. Hastalık aktivitesini izlemek için trombosit sayısının doğruluğu düşük bulunmuştur. Lökosit diferansiyeliyle tam kan sayımı hemen her zaman bir makrositer veya normositik anemi gösterir; nötropeni ve trombositopeni daha değişkentir. Pansitopeni (yani, anemi, lökopeni ve trombositopeni), teşhis anında hastaların yüzde 50'sine kadar varılmıştır. İzole anemi seyrek olmakla birlikte, hastaların% 5'inden azı izole nötropeni, trombositopeni veya anemi yokluğunda monositoz ile birlikte görülür[65, 66].
19
3. ARAÇ, GEREÇ VE YÖNTEMLER
3.1. Çalışma Gruplarının Oluşturulması ve Çalışma Düzeni
Araştırmanın yapılacağı olgular, Ege Üniversitesi Tıp Fakültesi İç Hastalıkları AD, Gastroenteroloji BD polikliniğine başvuran hastalar arasından seçilerek oluşturuldu. Çalışmaya dahil edilen bireylerin yaş, cinsiyet, boy, vucut ağırlığı, CH başlama süresi, CH nedeniyle geçirilen operasyon, diğer başka sistemik hastalık, gebelik durumu, sigara, alkol kullanımı, son bir yıldır kullanılan ilaçlar ve kullanım süresi, CDAI skor hesaplaması için gerekli bilgiler, hesaplanan CDAI daha önceden hazırlanan olgu rapor formuna (Ek-1) kaydedildi.
3.1.1. Çalışmaya alınma kriterleri:
- Yaş ≥ 19
- En az son 6 ay içinde Crohn hastalığı tanısı almış olmak - Klinik olarak remisyonda olmak: CDAI <150 olmak
3.1.2. Çalışmadan dışlanma kriterleri
- Enfeksiyöz enterokolit
- Otoimmun hastalık (SLE, romatoidartrit, vs) - Akut veya kronik inflamatuar durum
- Kolostomi, poush olması - Karaciğer, böbrek hastalığı - Malignansi öyküsü
- Gebelik
Olgular, Ege Üniversitesi Tıp Fakültesi İç Hastalıkları AD, Gastroenteroloji BD polikliniğine başvuran hastalar arasından seçildi. Araştırmaya dahil olma kriterlerini karşılayan ve dışlama kriterleri özelliklerini göstermeyen 12 olgu çalışmaya dahil edildi. Seçilen olgularda aynı gün içerisinde kan ve gaita örnekleri alındı. Tüm olgularda CRP, SAA, Eritrosit sedimantasyon hızı, tam kan sayımı, fekal kalprotektin ve fekal laktoferrin
20
testleri yapıldı. Ayrıca çalışmaya dahil edilen tüm hastalarda aynı tarihlerde kolonoskopi yapıldı ve hastalık aktivitesi incelendi.
Çalışma öncesinde, Ege Üniversitesi Tıp Fakültesi Araştırma Etik Kurulu’ndan onay alındı. Çalışmaya dahil olan tüm olgulara çalışma hakkında bilgi verildi ve bilgilendirilmiş gönüllü olur formu (Ek-2) imzalatıldı.
3.1.3. CDAI Puan Hesaplaması
CDAI Puan Hesaplamasında aşağıdaki bilgiler kullanıldı: Haftalık (7 gün içinde):
1. Sıvı gaita çıkışı sayısı, 2. Karın ağrısı,
3. Hastanın genel durumu / iyilik hali,
4. Barsak dışı komplikasyonlar (Artrit/artralji, iritis/uveitis, eritema nodosum, piyoderma gangrenosum, aftöz stomatit, anal fissür/fistül/abse, ateş >37.8 °C), 5. Antidiyare ilaç kullanımı,
6. Abdominal kitle varlığı, 7. Hematokrit düzeyi, 8. Hastanın vücut ağırlığı
Sekiz madde sorgulanarak Crohn hastalığı aktivitesi için CDAI aşağıdaki gibi hesaplanır:
1. Son 7 günlük sıvı veya çok yumuşak dışkılama sayısı :
Bir hafta içinde bu şarta uyan günlerin toplam sayısı x 2
2. Son 7 günlük karın ağrısı durumu: (0=yok, 1=hafif, 2=orta, 3=şiddetli)
Son 7 günün ortalaması x 5
3. Son 7 günlük genel iyilik durumu: (0=iyi, 1=ortalamanın biraz altı, 2=kötü, 3=çok
21 Son 7 günün ortalaması x 7
4. CH ile ilgili olduğu varsayılan aşağıdaki hastalık belirti veya semptomlarından
herhangi birisinin varlığı (Hiçbiri=0, Her var olan şık için 20)
a. Eklem problemleri (Artrit veya artralji)
b. Göz problemleri (İris veya üveitis)
c. Cilt veya deri sorunları
d. Anal fissür, fistül veya perirektal abse
e. Bağırsakla ilişkili diğer fistül oluşumu
f. Son 7 gün içinde ateşin 37º C nin üstünde artmış olması
5. Son 7 gün içinde diare için bağırsak motilite düzenleyici veya benzer diare kesici
ilaç alımı (Hayır = 0 Evet = 30)
6. Batında anormal kitle varlığı (0=yok; 0. 4=emin değilim; 10=var)
7. Eğer bir hafta içerisinde tam kan sayımı yapıldı ise hematokrit değeri (normal
ortalama hematokrit değerleri: Erkek = 47, Kadın = 42)
[ (Normal ortalama hematokrit değeri – hastanın ölçülen hematokrit değeri) x 6 ]
8. Sağlıklı yetişkin bir insanın beklenen standard vücut ağırlığı ortalama olarak boyun
santim cinsinden son iki rakamına denk gelen sayı olarak varsayılır.
(Örnek: hasta boyu: 180 cm ise beklenen standard vücut ağırlığı 80 kg dır. Not : beklenen standard vücut ağırlığından daha ağır kişilerde bu soru atlanır.)
[(Beklenen standard sağlıklı bir insanın vücut ağırlığı –hastanın kilosu) / beklenen standard sağlıklı bir insanın vücut ağırlığı] x 100
CDAI sonucu 150 puan altı remisyonda hastalık olarak kabul edilir iken, 450 puan üzeri ciddi fulminan hastalık olarak değerlendirilir.
22
3.2. Kolonoskopi ile saptanan CH aktivite indeksleri
3.2.1. Basit Endoskopik Skor (SES) ve Rutgeert skor indeksi
SES Opere olmamış CH’da kolonoskopik aktivite göstergesidir. SES-CH= Barsağın 5 segmentinde tüm değişkeler değerlendirilir ve toplanır. Her değişkene göre değerlendirilen barsak segmentinin skorları Tablo 2’de verildi.
Tablo 2. Basit Endoskopik Skor (SES) indeksi[67]
Değişkenler Skor 0 1 2 3 Ülser Boyutu(cm) Yok Aftöz Ülser (0,1-0,5 yarıçap) Büyük Ülser (0,5-2 yarıçap) Çok Büyük Ülserler (yarıçap>2) Ülserleşmiş Yüzey Yok <%10 <%10-30 >%30 Etkilenmiş Yüzey Etkilenmemiş segment <%50 %50-70 >%75
Striktür Yok Tek, geçebilir Çoklu, geçebilir Geçemez
SES değerlendirme:
0 -2: remisyon
3 -6: hafif endoskopik aktivite 7-15: orta endoskopik aktivite >15 ciddi endskopik aktivite
23
Rutgeerts skor indeksi opere olmuş CH’da kolonoskopik aktivite göstergesi Tablo 3’de verildi.
Tablo 3. Rutgeerts skor indeksi[68]
Endoskopik Bulgular Skor
Aftöz Ülser Yok 0
Beşten az aftöz ülser 1
Normal mukozada ara ara beşten fazla aftöz lezyon, yayılan alanlarda büyük lezyonlar veya ileokolonik anastomozla sınırlı lezyonlar (ör. 1cm den az)
2
İnflamasyonlu difüz mukozalı difüze aftöz ileitis 3
Difüz inflamasyonlu büyük ülserler, nodüller ve/veya striktür 4
3.3. Örneklerin Alınması, Saklanması, Hazırlanması
Araştırma hakkında bilgilendirilip onayları alınan ve anamnez, klinik bulgularına göre araştırmaya dahil edilmesi uygun görülen olgulardan laboratuar testleri için venöz kan örneği ve gaita örneği alındı.
8-12 saat açlık sonrası venöz kan örnekleri antikoagulan içermeyen jelli tüplere, K3EDTA ve Na2sitratlı (sedimantasyon tüpü) içeren antikoagulanlı tüplere kan örnekleri alındı. Alınan düz kan örnekleri 4000 devir/dk hızda 10 dk süre ile santrifüj edildi. Örneklerden günlük çalışılması gereken serum CRP, SAA, eritrosit sedimantasyon hızı ve tam kan sayımı aynı gün içinde ölçüldü. Fekal kalprotektin ve fekal laktoferrin için gaita örnekleri ön ayırma işlemleri (ekstraksiyon) tamamlandıktan sonra çalışma gününe kadar – 80ºC soğutmalı derin dondurucuda saklandı.
3.3.1. Fekal Kalprotektin feçes örnek hazırlığı
Yaklaşık 1 gr feçes 4 ml ekstraksiyon tamponu ile dilüe edildi ve iyice vortekslendi. Daha sonra dilüe edilmiş örnekler 18-28°C'de en az 5 dakika bekletildi. Bu örnekten 50µL alınarak üzerine 450µL ekstraksiyon solüsyonu eklendi (1:10 dilüsyon), 5 dakika 3000g de
24
santrifüj edilip, sonrasında süpernatant ayrılarak ölçüme kadar -80OC de saklandı. Çalışma günü, süpernatant oda sıcaklığına getirilerek çalışıldı.
3.3.2. Fekal laktoferrin feçes örnek hazırlığı:
Toplanan 55 mg feçes örneğine 2695 μL ekstraksiyon tamponu (BioVendor marka Kat. No: C005821) eklendi. Bu şekilde feçes örneklerine ekstraksiyon sırasında 1:50 dilusyon yapıldı. Numuneler vorteks üzerinde 30 dakika yüksek hızda homojenize edildikten sonra, 3000g'de 5 dakika santrifüj edildi. Süpernatant ayrılarak çalışma yapılacak güne kadar -80OC de saklandı. Feçes içerisindeki bileşenleri açığa çıkarmak için özel dilüsyon tamponu (Cat.No.: C005114) kullanarak 1:3 dilüsyon yapıldı (40 μL feçes süpernatantı + 80 μL Özel Dilüsyon Tamponu).
3.4. Araç ve Gereçler
3.4.1. Cihazlar ve Sarf Malzemeleri
• Otomatik analizör (Roche Cobas 8000, USA)
• Eritrosit Sedimentasyon Hızı cihazı (Greiner Bio-One, Vacuette SRS 100/II) • Bühlmann Quantum Blue® Reader, Bühlmann Laboratories AG (Almanya) • Nefelometre (Siemens-BNII-182579, Almanya)
• Tan Kan Sayım Cihazı (Sysmex XN-2000, USA)
• Mikroplate okuyucu nanometre (Biotek multiskan spektrofotometre) • Mikroplaka karıştırıcı (Eppendorf Thermomixer comfort)
• Santrifüj (HettichRotina 38) • Vortex (HeidolphReax Top)
• Derin dondurucu (Sanyo Ultra low -80°C)
• Otomatik pipetler, çok yollu pipetler (BrandTransferpette S 100-1000 μL, Germany, Eppendorf Research 30-3000 μL, Germany)
• Otomatik Pipet Ucu (5-250 μL, 200-1000μL), filtreli
• Vakumlu Tüp (5-6 ml serum pıhtı aktivatörlü Venosafe 0610039) • Vakumlu Tüp (2 ml mor kapaklı K2EDTA’lı)
25
3.4.2. Hazır kitler
Fekal Kalprotektin: Quantum Blue® fCALextended Quantitative Lateral Flow Assay
Katalog No: LF-CALE25 Bühlmann Laboratorıes, AGBaselstrasse 554124 Schönenbuch, İsviçre.
Fekal Laktoferrin: ELISA yöntemi. BioVendor® Human Lactoferrin ELISA, Katalog
No: RD194334200R, Biotin-labelled antibody – Laboratornimedicina a.s. Karasek 1767/162100, Çek Cumhuriyeti.
C-reaktif protein: C- REAKTİF Protein Gen 3, ROCHE, Katalog No: 05172373190,
Roche Diagnostics, GMBH Sandhofer Str.116 D-68305, Mannheim, Almanya.
Serum amiloid A: N Latex SAA Kiti, Katalog No: OQMP11, Siemens Healthcare
Diagnostics Products Gmbh Emil-Von-Behring Str.76 35041 Marburg, Almanya.
3.5. Biyokimyasal Analizler
3.5.1. Fekal Kalprotektin Ölçümü
Kantitatif lateral flow assay yöntemi ile ölçüldü. Fekal kalprotektin kantitatif lateral flow assay yöntemi, kalprotektin antijeninin sandviç immünoassay ile seçici olarak ölçülmesi için geliştirilmiş bir kartuş testidir.
Sonrasında kartuş Bühlmann Quantum Blue® Reader cihaza takılarak okuma işlemi gerçekleştirildi.
Fekal Kalprotektin çalışma prosedürü
Oda sıcaklığına getirilen süpernatant 5 dakika 3000g de santrifüj edildi. Süpernatantdan 60µL alınarak, lateral flow cip üzerine damlatıldı, 12 dakika örneğin kartuş tarafından emilmesi için beklendi. Bekleme işlemi ile kartuş üzerinde örneğin sağlıklı bir şekilde emilmesi ve doğru bir okuma yapılması sağlandı.
Test membranının üzeri kalprotektin için son derecede spesifik olan bir monoklonal yakalama antikoru (mAb) ile kaplıdır. Altın kolloidlerle konjuge edilmiş ikinci bir monoklonal tespit antikoru, membran ile birlikte bulunan ped üzerinde bulunur. Ekstrakte edilmiş ve seyreltilmiş feçes numunesinin eklenmesinden sonra reaksiyon sistemine salınır. Kalprotektin / anti-kalprotektin altın konjugatı, test membranı (test çizgisi; test bandı)
![Tablo 2. Basit Endoskopik Skor (SES) indeksi[67]](https://thumb-eu.123doks.com/thumbv2/9libnet/3026219.2298/33.892.135.823.353.694/tablo-basit-endoskopik-skor-ses-indeksi.webp)