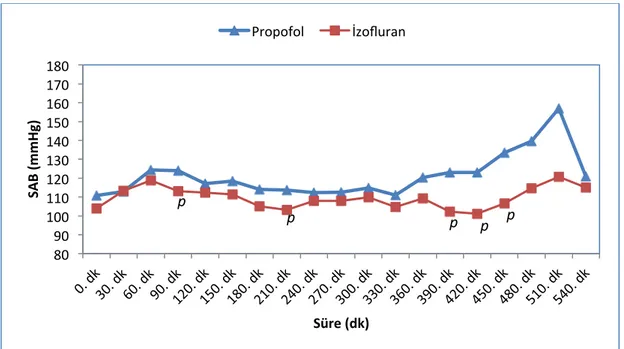
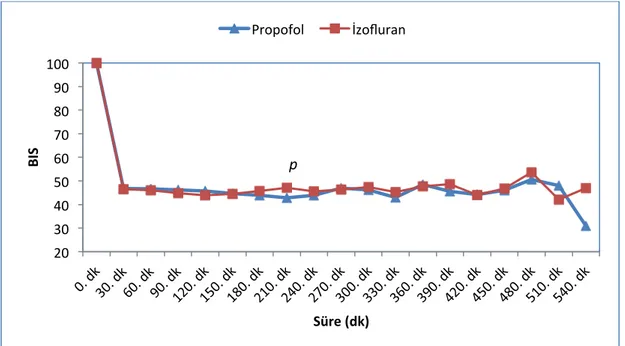
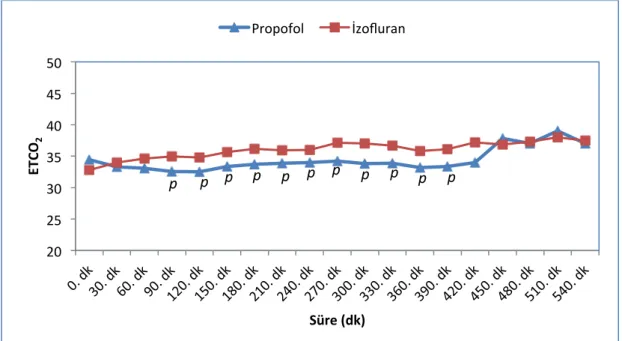
Sağ hepatektomi cerrahisi uygulanan karaciğer nakli vericilerinde propofol ile izofluranın antioksidan etkinliğinin karşılaştırılması
Tam metin
Şekil

Benzer Belgeler
Abdurrahman Yurtaslan Ankara Research and Training Hospital, Ankara/TR, 8 Medical Oncology, Celal Bayar University Hospital, Manisa/ TR, 9 Medical Oncology, Gazi University,
Böyle yüzyıllar boyunca dramatik özellikte, kişileştirmeye dayanan sözlü oyunların gelene ğinin varlığını kısaca belirttikten sonra bu oyunlar ile Karagöz,
Anodization with cathodic pretreatment not only yields a titanium surface with a multi-nanostructure, but also transforms the titanium surface into a nanostructured titania
Bu çalışma, KABG cerrahisi geçiren hastalarda pos- toperatif sedasyon amacıyla deksmedetomidin kulla- nımının propofole dayalı sedasyon rejimlerine göre etkin ve güvenilir
Postoperatif belirleyiciler olan; ekstübasyon zamanı, yoğun bakım süresi, hastanede kalma süresi ile so- lunum sistemi komplikasyonları arasındaki ilişki an- lamlı idi ve
Bu çalışmada elektif karın ve ekstremite cerrahisi planlanan olgularda preoperatif anamnez, fizik muayene, akciğer grafileri, arter kan gazı (AKG) ve solunum fonksiyon
Denemelerde, geleneksel olarak kullanilan tohum ve gübreyi bir arada ayni derinlige birakan kombine ekim makinasi (M 1 ) ile çalisma için tasarlanan, tohum.. ve gübreyi
(Yönetmelikte kriterleri belirtilen bina bilgi düzeylerinde alınması gereken minimum karot numunesi 9’dur ve her kattan minimum 3 tane alınması şart konmuştur. Söz