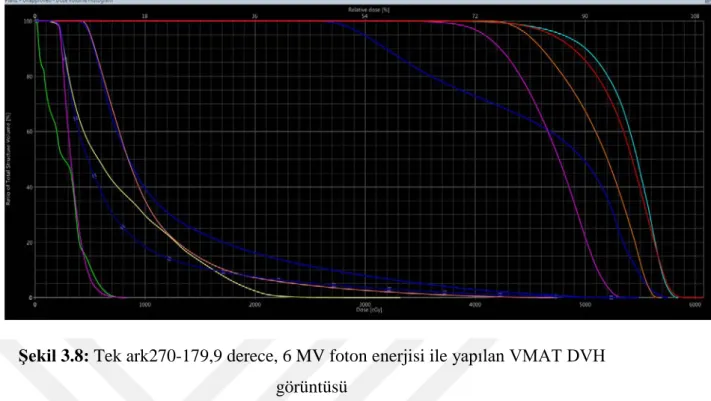
MASTEKTOMİ SONRASI RADYOTERAPİ UYGULANAN SOL MEME KANSERLİ HASTALARDA ALAN İÇİNDE ALAN (FIF), VOLÜMETRİK AYARLI ARK TERAPİ (VMAT) VE YOĞUNLUK AYARLI RADYOTERAPİ (IMRT) YÖNTEMLERİNİN DEĞERLENDİRİLMESİ
Tam metin
Şekil


Benzer Belgeler
Fistula Between Left Internal Mammary Artery Graft and Pulmonary Vasculature After Coronary Bypass Grafting.. Left internal mammary artery (UMA) is very commonly used conduiı
Me: I like bumper cars. It is amazing and thrilling. You? My friend: I disagree, I think it is dull. .... 2) Translate
4 1990 y›l›nda ‹stanbul’da yap›lan bir araflt›rmada hekime bafl- vurmadan reçetesiz ilaç alma oran› düflük sosyo-ekono- mik kültürel konumda olanlarda %56.7,
Monaco TPS sisteminde çeşitli ÇYK parametrelerini kontrol için oluşturulan testlerle Elekta Synergy lineer hızlandırıcı cihazının YART performansı, DÇYK
Her ne kadar mastektomi ile aynı seansta yapılan serbest TRAM flebin, flep beslenm esi açısından pediküllü TRAM flebe oranla daha.üstün olduğu birçok yazar
In our study, we found the pectoral nerve block method which is applied for the treatment of pain after oncologic breast operations is superior to infiltration
In this study, we evaluated the early wound complications and the factors affecting these complications among the patients who diagnosed with breast cancer and
Mastektomi sonrası, meme rekonstrüksiyonu yapılan has- taların rekonstrüksiyonsuz mastektomili hastalara göre beden imajı ve benlik saygılarının daha yüksek olduğu, özgüvene